TEMA 6: Espectroscopía de Resonancia Paramagnética Electrónica. El espín electrónico
|
|
|
- Hugo Carrasco Martin
- hace 5 años
- Vistas:
Transcripción
1 TEMA 6: Espectroscopía de Resonancia Paramagnética Electrónica. El espín electrónico - Evidencia experimental 1. Líneas espectrales del átomo de H poseen estructura fina. 2. Experimento de Stern-Gerlach. 3. Desdoblamiento Zeeman (Zeeman splitting) Resonancia Paramagnética Electrónica RPE en inglés Electron Paramagnetic Resonance EPR o Electron Spin Resonance ESR Técnica espectroscópica que permite obtener información sobre la estructura y dinámica de sistemas con electrones desapareados (i.e. sistemas paramagnéticos).
2 TEMA 6: Espectroscopía de Resonancia Paramagnética Electrónica. Ejemplos de sistemas que se pueden investigar por EPR: Centros paramagnéticos intrinsecos: o Radicales estables en química y biología. o Especies de corta vida, intermedios en reacciones quimicas (t½ ~100 ns). o Pares radicales y estados triplete en fotosíntesis y sistemas relacionados. o Radicales generados por el dano por irradiación (ADN, polimeros). o Iones de metales de transición (Cu, Mn, V, Fe, Cr, Mo, Ti) presentes en catalizadores sintéticos y en metaloproteinas. o Defectos en semiconductores. o Fullerenos Sistemas diamagnéticos con spin introducido artificialmente: o Mn(II) remplazando a Mg(II) en sistemas biológicos. o Co(II) remplazando a Zn(II). o Sondas de spin nitroxido para estudiar: - Estructura y dinamica de proteinas - Orden y dinamica de membranas biologicas - Polimeros - Estructura, dinamica y degradacion de polimeros - Orden y dinamica de cristales liquidos - Sensores de ph - Procesos de autoensamblado - Adsorcion en superficies
3 La espectroscopía de EPR es similar a cualquier otra técnica espectroscópica depende de la absorción de radiación electromagnética Una molécula o átomo tiene estados discretos (o separados) con una energía correspondiente
4 Un electrón aislado, solo en el espacio sin fuerzas externas sin estar orbitando alrededor de un núcleo por ejemplo todavía tiene un momento angular intrínseco llamado espín S. Debido a que el electrón tiene carga, el movimiento angular de espín de esta partícula cargada genera un campo magnético En otras palabras, el electrón debido a su carga y momento angular de espín actúa como una pequeña barra de imán, o sea, un dipolo magnético con un momento magnético,.
5 - De manera simplificada: el electrón, al ser una particula cargada (negativamente) que gira (espín) genera un momento magnético. - Este momento magnetico ( S) generado por el spin electrónico en el seno de un campo magnetico B posee una energía E: - Además se sabe que para el electrón, su momento magnético de spin es: ge = , es el factor g del electrón libre B = J.T -1, magnetón de Bohr. Notar que el signo menos en ecuación 2 indica que vector S y vector S son antiparalelos! Vectores S y B paralelos vectores S y B antiparalelos. Vectores S y B antiparalelos vectores S y B paralelos.
6 La aplicación del campo magnético externo elimina la degeneración de los estados de spin electrónico: Regla de selección: Δm s = ±1 - En B0=0, los estados de spin están degenerados ( juntos en escala de energía). - Cuando el B0 0 estos niveles se separan (esto se conoce como efecto Zeeman). - La separación energética entre estos dos estados de spin viene dada por: Las transiciones entre los diferentes estados de espin son inducidas por radiaciones electromagnéticas a la frecuencia apropiada (microondas) :
7 - Cuando tomamos un electrón que está libre en el espacio, sin fuerzas externas sobre él y lo colocamos en una molécula, su momento angular total cambia - Ahora, además del momento angular de de spin (S), también posee un momento angular orbital (L). e e L I A L ( 1) 2m 2m e L B ( 1) e electrón libre electrón alrededor de un núcleo - Un electrón con momento angular orbital es una corriente circulante, por lo que también hay ahora dos momentos magnéticos. - Estos dos momentos magnéticos S y L interactúan, y la energía de esta interacción spinorbita depende de sus orientaciones relativas. - Si los vectores S y L interactúan, el electrón desapareado responderá no sólo al campo magnético externo aplicado (B 0 ), sino que se verá afectado por el campo magnético generado por el momento magnético angular (L).
8 El campo efectivo Beff experimentado por un electrón es: Donde σ es una constante de apantallamiento similar a la de RMN, y puede tomar valores positivos o negativos. En base a esto, la ecuación 5 se puede escribir como - Debido a que los mecanismos de acoplamiento spin-orbita son bien comprendidos, la magnitud del cambio da información acerca de la naturaleza del orbital atómico (p, d, f ) o molecular (σ, π) que contiene el electrón desapareado. - Si el electrón libre se encuentra en un orbital con número cuántico orbital igual a cero, entonces el acoplamiento spin-orbita será nulo o muy pequeño, y el valor de g ~ g e
9 En sistemas reales los electrones normalmente no están aislados, sino que están asociados con uno o más átomos. Hay varias consecuencias importantes de esto: - Un electrón desapareado puede ganar o perder momento angular, lo cual puede cambiar el valor de su factor g, haciendo que difiera del g e. Esto es especialmente importante para los sistemas químicos con iones de metales de transición. - El momento magnético de un núcleo con un spin nuclear distinto de cero (I 0) afectará a cualquier electrón desapareado cercano a ese átomo. Esto conduce al fenómeno de acoplamiento hiperfino (A), análogo al acoplamiento J en RMN, el cual divide la señal de resonancia de EPR en dobletes, tripletes y así sucesivamente. - Las interacciones de un electrón desapareado con su entorno influyen en la forma de una línea espectral de EPR. Las formas pueden proporcionar información estructural. - El factor g y el A en un átomo o molécula pueden no ser los mismos para todas las orientaciones de un electrón desapareado en un campo magnético externo. Esta anisotropía depende de la estructura electrónica del átomo o molécula (eg. radical libre, metal, etc.) en cuestión, y por lo tanto puede proporcionar información sobre el orbital atómico o molecular que contiene el electrón desapareado.
10 Obtención de un espectro de EPR - En la mayoría de las espectroscopías (UV-Vis, IR, etc.) los niveles de energía (electrónicos, vibracionales, rotacionales) relevantes están "fijos" y presentes en la muestra. - Se realiza un barrido de la longitud de onda / frecuencia de la radiación EM para detectar las absorciones correspondientes a saltos entre los niveles energéticos. En estos espectros se muestran los picos de absorción.
11 - En CW-EPR los niveles de energía responsables de la absorción del fotón de radiación EM están juntos, pero se pueden separar colocando la muestra en el seno de un campo magnético exterior (B0). - En este caso, el E depende de la magnitud del B0 - Se mantiene la frecuencia constante (h constante) y se varía B 0 para detectar absorciones de energía: - El espectro obtenido muestra la primera derivada de los picos de absorción (debido al sistema de detección de EPR es diferente al de las demás espectroscopías por modulación / sensible a fase).
12 Espectrómetro de EPR
13 Formas de los espectros (forma de línea) - La desviación del factor g medido de la del electrón libre surge del acoplamiento spin-órbita entre el estado fundamental y estados excitados. - Debido a que los orbitales están orientados en la molécula, la magnitud de esta mezcla es dependiente de la dirección, o sea, es anisotrópico. - Para cada molécula paramagnética, existe un sistema de ejes único llamado sistema del eje principal. Los factores g medidos a lo largo de estos ejes se llaman los factores g principales y se etiquetan g x, g y y g z. - La mayoría de los espectros de EPR de metales de transición en sistemas biológicos se obtienen en muestras de solución congelada. - Los paramagnetos no están alineados en una dirección única como en un cristal orientado. - Tampoco están girando rápidamente como en una solución. - Las moléculas están en todas las orientaciones posibles muestra congelada = espectro de polvo.
14 Espectros de absorción y primera derivada para tres clases diferentes de anisotropía.
15 Estructura de multipletes en EPR: efecto de un spin nuclear (I) o de otro spin electrónico (S) - En EPR, se pueden detectar tres tipos de interacciones: - Las dos primeras se deben a la interacción entre un electrón desapareado y un nucleo magnetico, o sea, con spin nuclear I 0. - La interacción del electrón no apareado con el momento magnético nuclear se denomina interacción hiperfina nuclear. - Se llama hiperfina si la interacción es con el núcleo (A) en el que está el electrón desapareado y superhiperfina (B) si es con un nucleo vecino. - El tercer tipo es la interacción entre dos electrones desapareados (C) que se encuentran en átomos diferentes, normalmente dentro de una molecula, y se denomina interaccion spin-spin.
16 Interacción hiperfina y superhiperfina: efecto de un spin nuclear (I) E h. g. B.B0 h.a.m
17 Interacción hiperfina y superhiperfina: efecto de un spin nuclear (I) Efecto en una señal isotrópica
18 Interacción hiperfina y superhiperfina: efecto de un spin nuclear (I) Efecto del spin nuclear del Cu en una señal axial de Cu(II) - Cu 2+ generalmente produce un espectro de EPR axiales. - Los dos principales isótopos del Cu, 63 Cu y 65 Cu, tienen espines nucleares de 3/2 la línea Zeeman se dividirá en cuatro líneas (m l = +3/2, +1/2, -1/2, -3/2). - El acoplamiento hiperfino a lo largo de g // para Cu 2+ siempre es mucho mayor que a lo largo de g A // >>> A
19 Interacción hiperfina y superhiperfina: efecto de un spin nuclear (I) Efecto del spin nuclear del V en una señal axial de V 4+
20 Interacción hiperfina y superhiperfina: efecto de varios espines nucleares (I) Efecto del spin nuclear del 1 H (I=1/2) y 14 N (I=1) en una señal nº de líneas = (2nI+1) n: nro. de núcleos iguales
21 Estructura de multipletes en EPR: efecto de otro(s) espin(es) electrónico(s) en el mismo átomo Desdoblamiento a campo cero (zero field splitting, ZFS) El campo cristalino, la interacción dipolar entre espines, el acoplamiento LS pueden remover la degeneración de los niveles de energía del spin e, aún en ausencia de campo magnético externo (zero field) aparición de estructura fina en el espectro. d 5 : Mn(II), Fe(III) high spin, S = 5/2 Idem, pero con un gran ZFS (Fe(III) en hemos)
22 Otros usos prácticos de EPR para estudio de metaloenzimas Cuantificación de espines / cuantificación de centros paramagnéticos Señal de Cu(II) obtenida experimentalmente 1 ra derivada Señal de Cu(II) 1 er integral Señal de Cu(II) 2 do integral J Biol Inorg Chem. DOI /s
23 Otros usos prácticos de EPR para estudio de metaloenzimas Titulaciones potenciométricas
Trabajo Practico nº2
 Trabajo Practico nº2 Espectroscopía de Resonancia Paramagnética Electrónica (RPE). Introducción La Resonancia Paramagnética Electrónica (RPE, en inglés EPR: Electron Paramagnetic Resonance) es una técnica
Trabajo Practico nº2 Espectroscopía de Resonancia Paramagnética Electrónica (RPE). Introducción La Resonancia Paramagnética Electrónica (RPE, en inglés EPR: Electron Paramagnetic Resonance) es una técnica
Trabajo Practico nº3
 Biofisicoquímica de Metaloproteínas Departamento de Física Facultad de Bioquímica y Cs. Biológicas UNIVERSIDAD NACIONAL DEL LITORAL Trabajo Practico nº3 Espectroscopía de Resonancia Paramagnética Electrónica
Biofisicoquímica de Metaloproteínas Departamento de Física Facultad de Bioquímica y Cs. Biológicas UNIVERSIDAD NACIONAL DEL LITORAL Trabajo Practico nº3 Espectroscopía de Resonancia Paramagnética Electrónica
Biofisicoquímica de Metaloproteínas
 Biofisicoquímica de Metaloproteínas Departamento de Física Facultad de Bioquímica y Ciencias Biológicas Universidad Nacional del Litoral - Santa Fe - ARGENTINA Espectroscopía en términos generales: Rama
Biofisicoquímica de Metaloproteínas Departamento de Física Facultad de Bioquímica y Ciencias Biológicas Universidad Nacional del Litoral - Santa Fe - ARGENTINA Espectroscopía en términos generales: Rama
ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR
 ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR La Espectroscopía de Resonancia Magnética Nuclear (RMN) es la herramienta de determinación estructural más potente del químico orgánico. Mediante el RMN podemos
ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR La Espectroscopía de Resonancia Magnética Nuclear (RMN) es la herramienta de determinación estructural más potente del químico orgánico. Mediante el RMN podemos
Modelos Atómicos Históricos.
 Modelos Atómicos Históricos. THOMSON-1910: budín de pasas, radio 10-10 m; máxima deflección de partículas α=10-4 rad. Rutherford-1911: scattering de partículas α Modelo: núcleo central con carga positiva
Modelos Atómicos Históricos. THOMSON-1910: budín de pasas, radio 10-10 m; máxima deflección de partículas α=10-4 rad. Rutherford-1911: scattering de partículas α Modelo: núcleo central con carga positiva
Interacciones intermoleculares: Espectroscopia
 Interacciones intermoleculares: Espectroscopia Presentado por: Wilmer E. Vallejo Narváez 13 de Octubre de 2014 1 Contenido Introducción Espectroscopia Uv vis Espectroscopia IR Espectroscopia RMN 2 Introducción
Interacciones intermoleculares: Espectroscopia Presentado por: Wilmer E. Vallejo Narváez 13 de Octubre de 2014 1 Contenido Introducción Espectroscopia Uv vis Espectroscopia IR Espectroscopia RMN 2 Introducción
ANÁLISIS INSTRUMENTAL_UII_PARTE DOS. Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½
 RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
Tema 14 Mecánica Cuántica
 Tema 14 Mecánica Cuántica 1 14.1 Fundamentos de la mecánica cuántica 14. La ecuación de Schrödinger 14.3 Significado físico de la función de onda 14.4 Soluciones de la ecuación de Schrödinger para el átomo
Tema 14 Mecánica Cuántica 1 14.1 Fundamentos de la mecánica cuántica 14. La ecuación de Schrödinger 14.3 Significado físico de la función de onda 14.4 Soluciones de la ecuación de Schrödinger para el átomo
Tema 14 11/02/2005. Tema 8. Mecánica Cuántica. 8.1 Fundamentos de la mecánica cuántica
 Tema 14 11/0/005 Tema 8 Mecánica Cuántica 8.1 Fundamentos de la mecánica cuántica 8. La ecuación de Schrödinger 8.3 Significado físico de la función de onda 8.4 Soluciones de la ecuación de Schrödinger
Tema 14 11/0/005 Tema 8 Mecánica Cuántica 8.1 Fundamentos de la mecánica cuántica 8. La ecuación de Schrödinger 8.3 Significado físico de la función de onda 8.4 Soluciones de la ecuación de Schrödinger
Movimiento vibracional
 ESPECTROSCOPÍA Movimiento vibracional El oscilador armónico como modelo de la vibración molecular Los sistemas que vibran a nivel molecular incluyen las vibraciones internas de una molécula y las vibraciones
ESPECTROSCOPÍA Movimiento vibracional El oscilador armónico como modelo de la vibración molecular Los sistemas que vibran a nivel molecular incluyen las vibraciones internas de una molécula y las vibraciones
ÍNDICE
 ÍNDICE 1 Radiación térmica y el postulado de Planck... 17 1-1 Introducción... 19 1-2 Radiación térmica... 19 1-3 Teoría clásica de la cavidad radiante... 24 1-4 Teoría de Planck de la cavidad radiante...
ÍNDICE 1 Radiación térmica y el postulado de Planck... 17 1-1 Introducción... 19 1-2 Radiación térmica... 19 1-3 Teoría clásica de la cavidad radiante... 24 1-4 Teoría de Planck de la cavidad radiante...
CAPÍTULO 1. RESONANCIA PARAMAGNÉTICA ELECTRÓNICA (EPR)
 CAPÍTULO 1. RESONANCIA PARAMAGNÉTICA ELECTRÓNICA (EPR) 1.1. Introducción La Resonancia Paramagnética Electrónica EPR puede ser vista como una extensión del experimento de Stern-Gerlach, quienes mostraron
CAPÍTULO 1. RESONANCIA PARAMAGNÉTICA ELECTRÓNICA (EPR) 1.1. Introducción La Resonancia Paramagnética Electrónica EPR puede ser vista como una extensión del experimento de Stern-Gerlach, quienes mostraron
Espectroscopía electrónica molecular
 Espectroscopía electrónica molecular Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Curso 2017/2018 Índice 1. Símbolos de los términos moleculares 2 2. Estructura fina vibracional
Espectroscopía electrónica molecular Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Curso 2017/2018 Índice 1. Símbolos de los términos moleculares 2 2. Estructura fina vibracional
Tema 2: Propiedades magnéticas de las especies químicas. Imán y virutas de hierro.
 Imán y virutas de hierro. Nitrógeno u oxígeno líquido???. Tren de levitación magnética. Aleaciones (NITINOL). A) Importancia del magnetismo en química: Magnetoquímica: Estudio de las propiedades magnéticas
Imán y virutas de hierro. Nitrógeno u oxígeno líquido???. Tren de levitación magnética. Aleaciones (NITINOL). A) Importancia del magnetismo en química: Magnetoquímica: Estudio de las propiedades magnéticas
Espectroscopía. Qué es la espectroscopía? 18/10/2013
 Espectroscopía Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar la frecuencia de
Espectroscopía Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar la frecuencia de
Propiedades del núcleo. Laura C. Damonte 2014
 Propiedades del núcleo Laura C. Damonte 2014 El núcleo Dos problemas principales: Las fuerzas que mantienen unido al núcleo. La descripción de un sistema de muchas partículas. 1. MODELOS Propiedades estáticas:
Propiedades del núcleo Laura C. Damonte 2014 El núcleo Dos problemas principales: Las fuerzas que mantienen unido al núcleo. La descripción de un sistema de muchas partículas. 1. MODELOS Propiedades estáticas:
Espectroscopía Clase integradora
 Espectroscopía Clase integradora Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar
Espectroscopía Clase integradora Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar
TEMARIO DE LOS EXÁMENES DE ADMISIÓN PARA INGRESO AL PROGRAMA DE MAESTRÍA EN CIENCIA DE MATERIALES DE LA UNIVERSIDAD DE SONORA
 TEMARIO DE LOS EXÁMENES DE ADMISIÓN PARA INGRESO AL PROGRAMA DE MAESTRÍA EN CIENCIA DE MATERIALES DE LA UNIVERSIDAD DE SONORA Examen de Química Química Orgánica Orbitales híbridos. Propiedades de los enlaces
TEMARIO DE LOS EXÁMENES DE ADMISIÓN PARA INGRESO AL PROGRAMA DE MAESTRÍA EN CIENCIA DE MATERIALES DE LA UNIVERSIDAD DE SONORA Examen de Química Química Orgánica Orbitales híbridos. Propiedades de los enlaces
MATERIAL 06. TEMA: MÉTODOS ESPECTROSCÓPICOS DE ANÁLISIS
 MATERIAL 06. TEMA: MÉTODOS ESPECTROSCÓPICOS DE ANÁLISIS La espectroscopia es el estudio de las interacciones de las radiaciones electromagnéticas con la materia (átomos y moléculas). Los métodos analíticos
MATERIAL 06. TEMA: MÉTODOS ESPECTROSCÓPICOS DE ANÁLISIS La espectroscopia es el estudio de las interacciones de las radiaciones electromagnéticas con la materia (átomos y moléculas). Los métodos analíticos
Fotones-Propiedades corpusculares de la radiación 45
 &C.A:tQ -~ 2 E. 'S 2ol~ c-t Contenido Radiación térmica y el postulado de Planck l 7 1-1 1-2 1-3 1-4 1-5 1-6 1-7 Introducción 19 Radiación térmica 19 Teoría clásica de la cavidad radiante 24 Teoría de
&C.A:tQ -~ 2 E. 'S 2ol~ c-t Contenido Radiación térmica y el postulado de Planck l 7 1-1 1-2 1-3 1-4 1-5 1-6 1-7 Introducción 19 Radiación térmica 19 Teoría clásica de la cavidad radiante 24 Teoría de
SELECCION DE PREGUNTAS REPRESENTATIVAS SOBRE TEMAS DEL MODULO DE
 SELECCION DE PREGUNTAS REPRESENTATIVAS SOBRE TEMAS DEL MODULO DE ESTRUCTURA Y PROPIEDADES MOLECULARES Temas de Mecánica Cuántica y Estructura atómica 1) Cuál es el operador asociado al observable energía,
SELECCION DE PREGUNTAS REPRESENTATIVAS SOBRE TEMAS DEL MODULO DE ESTRUCTURA Y PROPIEDADES MOLECULARES Temas de Mecánica Cuántica y Estructura atómica 1) Cuál es el operador asociado al observable energía,
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I
 El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
Titulación(es) Titulación Centro Curso Periodo M.U. en Física Médica 12-V.2 FACULTAT DE FÍSICA 1 Primer cuatrimestre
 FICHA IDENTIFICATIVA Datos de la Asignatura Código 43070 Nombre Estructura atómica y nuclear. Radioactividad Ciclo Máster Créditos ECTS 4.0 Curso académico 2015-2016 Titulación(es) Titulación Centro Curso
FICHA IDENTIFICATIVA Datos de la Asignatura Código 43070 Nombre Estructura atómica y nuclear. Radioactividad Ciclo Máster Créditos ECTS 4.0 Curso académico 2015-2016 Titulación(es) Titulación Centro Curso
QUÍMICA PRE_UNIVERSITARIA
 S CUÁNTICOS - CONFIGURACIÓN ELECTRÓNICA En 1926, Erwin Schrödinger propuso una ecuación, ahora conocida como la ecuación de onda de Schrödinger, que involucra los comportamientos tanto ondulatorios como
S CUÁNTICOS - CONFIGURACIÓN ELECTRÓNICA En 1926, Erwin Schrödinger propuso una ecuación, ahora conocida como la ecuación de onda de Schrödinger, que involucra los comportamientos tanto ondulatorios como
Materiales. Eléctricos. Materiales. Magneticos
 Materiales Eléctricos Materiales Magneticos Propiedades Magnéticas de los Materiales Materiales Eléctricos El magnetismo se manifiesta por la fuerza que se ejerce sobre un conductor con corriente eléctrica
Materiales Eléctricos Materiales Magneticos Propiedades Magnéticas de los Materiales Materiales Eléctricos El magnetismo se manifiesta por la fuerza que se ejerce sobre un conductor con corriente eléctrica
Momento angular de espín
 Momento angular de espín 14 Ene 04 Reson 1 Estado de espín de un electrón: Ŝ 2 χ(σ) = s(s + 1) 2 χ(σ) Ŝ z χ(σ) = m s χ(σ) Donde s = 1/2 y hay dos orientaciones: m s = 1/2, 1/2 Estado de espín de un núcleo:
Momento angular de espín 14 Ene 04 Reson 1 Estado de espín de un electrón: Ŝ 2 χ(σ) = s(s + 1) 2 χ(σ) Ŝ z χ(σ) = m s χ(σ) Donde s = 1/2 y hay dos orientaciones: m s = 1/2, 1/2 Estado de espín de un núcleo:
Hoja de Problemas 5. Física Atómica.
 Hoja de Problemas 5. Física Atómica. Fundamentos de Física III. Grado en Física. Curso 25/26. Grupo 56. UAM. 3-3-26 Problema En 896 el astrónomo americano Edward Charles Pickering observó unas misteriosas
Hoja de Problemas 5. Física Atómica. Fundamentos de Física III. Grado en Física. Curso 25/26. Grupo 56. UAM. 3-3-26 Problema En 896 el astrónomo americano Edward Charles Pickering observó unas misteriosas
Estructura de la materia
 Estructura de la materia 6. Aplicar el modelo mecánico-cuántico del átomo para explicar las variaciones periódicas de algunas de sus propiedades. Se trata de comprobar si el alumnado conoce las insuficiencias
Estructura de la materia 6. Aplicar el modelo mecánico-cuántico del átomo para explicar las variaciones periódicas de algunas de sus propiedades. Se trata de comprobar si el alumnado conoce las insuficiencias
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I 2012
 El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I 2012 Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I 2012 Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
Radiación térmica y el postulado de Planck
 Contenido Radiación térmica y el postulado de Planck 17 1-1 1-2 1-3 1.4 1.5 1-6 1-7 Introducción 19 Radiación térmica 19 Teoría clásica de la cavidad radiante 24 Teoría de Planck de 1a cavidad radiante
Contenido Radiación térmica y el postulado de Planck 17 1-1 1-2 1-3 1.4 1.5 1-6 1-7 Introducción 19 Radiación térmica 19 Teoría clásica de la cavidad radiante 24 Teoría de Planck de 1a cavidad radiante
EXTRUCTURA ATOMICA ACTUAL
 ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
Propiedades magnéticas
 Propiedades magnéticas Fuerzas magnéticas Las fuerzas magnéticas se generan mediante el movimiento de partículas cargadas Eléctricamente; existen junto a las fuerzas electrostáticas. Distribuciones del
Propiedades magnéticas Fuerzas magnéticas Las fuerzas magnéticas se generan mediante el movimiento de partículas cargadas Eléctricamente; existen junto a las fuerzas electrostáticas. Distribuciones del
GUIA TEÓRICA NÚMEROS CUÁNTICOS
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSE DE SUCRE VICE RECTORADO PUERTO ORDAZ DEPARTAMENTO DE ESTUDIOS GENERALES SECCIÓN DE QUÍMICA Asignatura: QUÍMICA I GUIA TEÓRICA NÚMEROS CUÁNTICOS
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSE DE SUCRE VICE RECTORADO PUERTO ORDAZ DEPARTAMENTO DE ESTUDIOS GENERALES SECCIÓN DE QUÍMICA Asignatura: QUÍMICA I GUIA TEÓRICA NÚMEROS CUÁNTICOS
Modelo Atómico. Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran embebidos los electrones con carga (-)
 Modelo Atómico 1 Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran embebidos los electrones con carga () Electrón Conceptos:» Neutralidad eléctrica» Carga elemental del
Modelo Atómico 1 Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran embebidos los electrones con carga () Electrón Conceptos:» Neutralidad eléctrica» Carga elemental del
ESPÍN ELECTRÓNICO (4.1)
 TEMA 4 ESPÍN ELECTRÓNICO 1 El momento angular de espín en átomos monoelectrónicos La ecuación de Schrödinger proporciona un valor excelente para la energía de ionización del átomo de hidrógeno; además,
TEMA 4 ESPÍN ELECTRÓNICO 1 El momento angular de espín en átomos monoelectrónicos La ecuación de Schrödinger proporciona un valor excelente para la energía de ionización del átomo de hidrógeno; además,
Moléculas: partícula neutra más pequeña de una sustancia dada que posee sus propiedades químicas y puede existir independientemente
 Especies químicas de interés formadas por átomos: Moléculas: partícula neutra más pequeña de una sustancia dada que posee sus propiedades químicas y puede existir independientemente Iones: Especies cargada
Especies químicas de interés formadas por átomos: Moléculas: partícula neutra más pequeña de una sustancia dada que posee sus propiedades químicas y puede existir independientemente Iones: Especies cargada
RESONANCIA MAGNÉTICA NUCLEAR
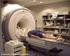 RESONANCIA MAGNÉTICA NUCLEAR SPIN DEL NUCLEO El nucleo de algunos átomos poseen SPIN. Estos núcleos se comportan como si estuvieran girando... no sabemos si realmente giran! Es como la propiedad de un
RESONANCIA MAGNÉTICA NUCLEAR SPIN DEL NUCLEO El nucleo de algunos átomos poseen SPIN. Estos núcleos se comportan como si estuvieran girando... no sabemos si realmente giran! Es como la propiedad de un
U N I V E R S I D A D N A C I O N A L D E L S U R 1/4
 U N I V E R S I D A D N A C I O N A L D E L S U R 1/4 DEPARTAMENTO DE: FISICA PROGRAMA DE: MECANICA CUANTICA II Carreras: Licenciatura en Física CODIGO: 3282 HORAS DE CLASE TEORICAS PRACTICAS Por semana
U N I V E R S I D A D N A C I O N A L D E L S U R 1/4 DEPARTAMENTO DE: FISICA PROGRAMA DE: MECANICA CUANTICA II Carreras: Licenciatura en Física CODIGO: 3282 HORAS DE CLASE TEORICAS PRACTICAS Por semana
Fisicoquímica II-Modulo de Estructura y Propiedades Moleculares.
 Fisicoquímica II-Modulo de Estructura y Propiedades Moleculares. Bolilla 3: Espectroscopía de resonancia magnética nuclear (NMR) y electrónica (EPR/ESR) 3.6 Transiciones de spin nuclear y electrónico.
Fisicoquímica II-Modulo de Estructura y Propiedades Moleculares. Bolilla 3: Espectroscopía de resonancia magnética nuclear (NMR) y electrónica (EPR/ESR) 3.6 Transiciones de spin nuclear y electrónico.
Espectroscopía atómica
 C A P Í T U L O 6 Espectroscopía atómica 6.. ENUNCIADOS Y SOLUCIONES DE LOS PROBLEMAS PROBLEMAS 6. Demuestre la regla de selección angular del átomo hidrogenoide m = 0, ±. Para m m 2π 0 e im Φ e imφ dφ
C A P Í T U L O 6 Espectroscopía atómica 6.. ENUNCIADOS Y SOLUCIONES DE LOS PROBLEMAS PROBLEMAS 6. Demuestre la regla de selección angular del átomo hidrogenoide m = 0, ±. Para m m 2π 0 e im Φ e imφ dφ
UNIVERSIDAD CENTRAL DEL ECUADOR Facultad de Ciencias Químicas. Fundamentos Espectroscópicos. Espectroscopia UV-Visible
 UNIVERSIDAD CENTRAL DEL ECUADOR Facultad de Ciencias Químicas Jhonny Arias Lenin Lombeida 2011-07-05 Fundamentos Espectroscópicos Espectroscopia UV-Visible Orbitales Atómicos Podemos decir que un orbital
UNIVERSIDAD CENTRAL DEL ECUADOR Facultad de Ciencias Químicas Jhonny Arias Lenin Lombeida 2011-07-05 Fundamentos Espectroscópicos Espectroscopia UV-Visible Orbitales Atómicos Podemos decir que un orbital
Espectroscopía de Absorción Molecular
 Espectroscopía de Absorción Molecular La espectroscopía consiste en el estudio cualitativo y cuantitativo de la estructura de los átomos o moléculas o de distintos procesos físicos y químicos mediante
Espectroscopía de Absorción Molecular La espectroscopía consiste en el estudio cualitativo y cuantitativo de la estructura de los átomos o moléculas o de distintos procesos físicos y químicos mediante
UNIVERSIDAD SIMÓN BOLÍVAR Vicerrectorado Académico
 UNIVERSIDAD SIMÓN BOLÍVAR Vicerrectorado Académico 1.Departamento: FÍSICA 2. Asignatura: FISICA MODERNA I 3. Código de la asignatura: FS-3411 No. de unidades-crédito: 4 No. de horas semanales: Teoría 4
UNIVERSIDAD SIMÓN BOLÍVAR Vicerrectorado Académico 1.Departamento: FÍSICA 2. Asignatura: FISICA MODERNA I 3. Código de la asignatura: FS-3411 No. de unidades-crédito: 4 No. de horas semanales: Teoría 4
Estructura electrónica de los átomos
 Estructura electrónica de los átomos Partículas subatómicas Protón (p) 1,673 10-27 Kg + 1,602 10-19 C Goldstein (1886) Electrón (e) 9,109 10-31 Kg - 1,602 10-19 C Thomson (1897) Neutrón (n) 1,673 10-27
Estructura electrónica de los átomos Partículas subatómicas Protón (p) 1,673 10-27 Kg + 1,602 10-19 C Goldstein (1886) Electrón (e) 9,109 10-31 Kg - 1,602 10-19 C Thomson (1897) Neutrón (n) 1,673 10-27
Periferia Atómica. Dra. Lic. Victoria Calzada Prof. Adjunta del Área Radiofarmacia Centro de Investigaciones Nucleares Facultad de Ciencias-UdelaR
 Curso de Química I Periferia Atómica Dra. Lic. Victoria Calzada Prof. Adjunta del Área Radiofarmacia Centro de Investigaciones Nucleares -UdelaR BIBLIOGRAFÍA CAPÍTULO 7 y 8 Teoría Cuántica y estructura
Curso de Química I Periferia Atómica Dra. Lic. Victoria Calzada Prof. Adjunta del Área Radiofarmacia Centro de Investigaciones Nucleares -UdelaR BIBLIOGRAFÍA CAPÍTULO 7 y 8 Teoría Cuántica y estructura
Espectrometría de luminiscencia molecular Cap.15
 Espectrometría de luminiscencia molecular Cap.15 Luz cuyo origen no radica exclusivamente en las altas temperaturas Se da en sustancias que pueden absorber energía, excitándose a niveles mayores y emitirla
Espectrometría de luminiscencia molecular Cap.15 Luz cuyo origen no radica exclusivamente en las altas temperaturas Se da en sustancias que pueden absorber energía, excitándose a niveles mayores y emitirla
Clase N 1. Modelo Atómico II
 Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico II ICAL ATACAMA Módulo Plan Común Síntesis De La Clase Anterior Modelo atómico Átomo Divisible en Protón Neutrón Electrón Carga: +1 Masa:
Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico II ICAL ATACAMA Módulo Plan Común Síntesis De La Clase Anterior Modelo atómico Átomo Divisible en Protón Neutrón Electrón Carga: +1 Masa:
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica
 Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Curso 2015-2016 Problema 1 La línea principal del espectro
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Curso 2015-2016 Problema 1 La línea principal del espectro
Cap. 32: Ecuaciones de Maxwell, Magnetismo en la Materia
 Cap. 32: cuaciones de Maxwell, Magnetismo en la Materia n el caso eléctrico, la estructura básica es una carga aislada. Dos cargas de igual magnitud, pero signos opuestos, separadas por una distancia d,
Cap. 32: cuaciones de Maxwell, Magnetismo en la Materia n el caso eléctrico, la estructura básica es una carga aislada. Dos cargas de igual magnitud, pero signos opuestos, separadas por una distancia d,
Instrumentación en Resonancia Magnética Nuclear: el espectrómetro
 Instrumentación en Resonancia Magnética Nuclear: el espectrómetro Un imán que genere un campo magnético fijo y estable. Generalmente se identifica cada espectrómetro por la frecuencia de resonancia del
Instrumentación en Resonancia Magnética Nuclear: el espectrómetro Un imán que genere un campo magnético fijo y estable. Generalmente se identifica cada espectrómetro por la frecuencia de resonancia del
Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos. Teoría atómica II: Números cuánticos y configuración electrónica
 TEORÍA ATÓMICA Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos Teoría atómica II: Números cuánticos y configuración electrónica Aprendizajes esperados Diferenciar los distintos
TEORÍA ATÓMICA Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos Teoría atómica II: Números cuánticos y configuración electrónica Aprendizajes esperados Diferenciar los distintos
Ejercicios Química PAU Comunidad de Madrid Enunciados Revisado 22 septiembre 2017
 2018-Modelo Pregunta B1.- Considere los cuatro elementos con la siguiente configuración electrónica en los niveles de energía más externos: A : 2s 2 2p 4 ; B: 2s 2 ; C: 3s 2 3p 2 ; D: 3s 2 3p 5. a) Identifique
2018-Modelo Pregunta B1.- Considere los cuatro elementos con la siguiente configuración electrónica en los niveles de energía más externos: A : 2s 2 2p 4 ; B: 2s 2 ; C: 3s 2 3p 2 ; D: 3s 2 3p 5. a) Identifique
Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos
 Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos INTEGRANTES: * Nazate Amuy Ana * Veloz Hidalgo Polet TEMA: Combinación Lineal de Orbitales Atómicos ORBITAL ATÓMICO
Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos INTEGRANTES: * Nazate Amuy Ana * Veloz Hidalgo Polet TEMA: Combinación Lineal de Orbitales Atómicos ORBITAL ATÓMICO
Biofisicoquímica de Metaloproteínas
 Biofisicoquímica de Metaloproteínas Departamento de Física Facultad de Bioquímica y Ciencias Biológicas Universidad Nacional del Litoral - Santa Fe - ARGENTINA Espectroscopía en términos generales: Rama
Biofisicoquímica de Metaloproteínas Departamento de Física Facultad de Bioquímica y Ciencias Biológicas Universidad Nacional del Litoral - Santa Fe - ARGENTINA Espectroscopía en términos generales: Rama
Tema 2: Enlace y propiedades de los materiales
 En la mayoría de moléculas, los enlaces entre los átomos que las constituyen no es mediante la interacción coulombiana que hemos analizado en el caso del enlace iónico. Se necesita tener en cuenta el llamado
En la mayoría de moléculas, los enlaces entre los átomos que las constituyen no es mediante la interacción coulombiana que hemos analizado en el caso del enlace iónico. Se necesita tener en cuenta el llamado
ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS
 ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS Jiménez Bárcenas Nadia Rosalina López Salazar Fátima Mendoza Pérez Bernardo Monzón González César Raúl Equipo 3: Principios de estructura de la materia
ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS Jiménez Bárcenas Nadia Rosalina López Salazar Fátima Mendoza Pérez Bernardo Monzón González César Raúl Equipo 3: Principios de estructura de la materia
de la Espectroscopía Bidimensional
 Teoría y Principios de la Espectroscopía Bidimensional Sebastián Franco Ulloa s.franco1412@uniandes.edu.co Octubre 6, 2016 1 Contenido 1. Espectroscopía 1D 2. Introducción a 2D 3. Experimento pump-probe
Teoría y Principios de la Espectroscopía Bidimensional Sebastián Franco Ulloa s.franco1412@uniandes.edu.co Octubre 6, 2016 1 Contenido 1. Espectroscopía 1D 2. Introducción a 2D 3. Experimento pump-probe
Tema 3 El Átomo. Modelos Atómicos y Configuraciones Electrónicas
 Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 3 Rev 01 El Átomo. Modelos Atómicos y Configuraciones Electrónicas
Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 3 Rev 01 El Átomo. Modelos Atómicos y Configuraciones Electrónicas
SERVICIO DE APOYO A LA INVESTIGACIÓN (SAI) SECCIÓN UNIVERSITARIA DE INSTRUMENTACIÓN CIENTÍFICA (SUIC)
 SERVICIO DE APOYO A LA INVESTIGACIÓN (SAI) SECCIÓN UNIVERSITARIA DE INSTRUMENTACIÓN CIENTÍFICA (SUIC) Murcia, 30 de Octubre de 2013 http://suicsaiumu.wordpress.com/ 1 La RMN es un tipo de Espectroscopía
SERVICIO DE APOYO A LA INVESTIGACIÓN (SAI) SECCIÓN UNIVERSITARIA DE INSTRUMENTACIÓN CIENTÍFICA (SUIC) Murcia, 30 de Octubre de 2013 http://suicsaiumu.wordpress.com/ 1 La RMN es un tipo de Espectroscopía
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León.
 Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Ejercicios Química PAU Comunidad de Madrid Enunciados Revisado 15 septiembre 2016
 2016-Septiembre Pregunta A1.- Los números atómicos de los elementos A, B y C son Z, Z+1 y Z+2, respectivamente. Si B es el gas noble que se encuentra en el tercer periodo, conteste razonadamente a las
2016-Septiembre Pregunta A1.- Los números atómicos de los elementos A, B y C son Z, Z+1 y Z+2, respectivamente. Si B es el gas noble que se encuentra en el tercer periodo, conteste razonadamente a las
ESTRUCTURA DE LA MATERIA
 ESTRUCTURA DE LA MATERIA Cuestiones 1. Conteste breve y razonadamente lo que se plantea en los apartados siguientes: a) Qué son los modelos atómicos y qué utilidad tienen?. b) Cite dos modelos atómicos
ESTRUCTURA DE LA MATERIA Cuestiones 1. Conteste breve y razonadamente lo que se plantea en los apartados siguientes: a) Qué son los modelos atómicos y qué utilidad tienen?. b) Cite dos modelos atómicos
ESTRUCTURA DE LA MATERIA
 ESTRUCTURA DE LA MATERIA 1. Naturaleza de la materia (el átomo). 2. Modelos atómicos clásicos. 3. Modelo mecánico cuántico. 4. Mecánica ondulatoria de Schrödinger. 5. Números cuánticos. 6. Orbitales atómicos.
ESTRUCTURA DE LA MATERIA 1. Naturaleza de la materia (el átomo). 2. Modelos atómicos clásicos. 3. Modelo mecánico cuántico. 4. Mecánica ondulatoria de Schrödinger. 5. Números cuánticos. 6. Orbitales atómicos.
21/03/2017. Modelo Atómico. Donde se ubican en el Átomo E L E C T R O N E S. Modelo Atómico. Que energía tienen. Como interactúan
 Modelo Atómico 1 Modelo Atómico E L E C T R O N E S Donde se ubican en el Átomo Que energía tienen Como interactúan 2 1 Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran
Modelo Atómico 1 Modelo Atómico E L E C T R O N E S Donde se ubican en el Átomo Que energía tienen Como interactúan 2 1 Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran
CIENCIA TECNOLOGÍA Y AMBIENTE FÍSICA - QUÍMICA - BIOLOGÍA - ROBÓTICA
 FÍSICA - QUÍMICA - BIOLOGÍA - ROBÓTICA 1.- PRINCIPIOS DE LA MECÁNICA CUÁNTICA a) PROPIEDADES DUAL DE LA MATERIA: La dualidad onda-corpúsculo, también llamada dualidad onda-partícula, postula que todas
FÍSICA - QUÍMICA - BIOLOGÍA - ROBÓTICA 1.- PRINCIPIOS DE LA MECÁNICA CUÁNTICA a) PROPIEDADES DUAL DE LA MATERIA: La dualidad onda-corpúsculo, también llamada dualidad onda-partícula, postula que todas
Tema 6- Enlace químico en sistemas moleculares
 Tema 6- Enlace químico en sistemas moleculares Diagrama de energía frente a distancia interatómica 2 Enlace en moléculas Intramolecular: El enlace entre átomos en las moléculas es enlace covalente Intermolecular:
Tema 6- Enlace químico en sistemas moleculares Diagrama de energía frente a distancia interatómica 2 Enlace en moléculas Intramolecular: El enlace entre átomos en las moléculas es enlace covalente Intermolecular:
Tema 3.-Espectroscopía de biomoléculas
 Tema 3.-Espectroscopía de biomoléculas Tema 3.-Espectroscopía de biomoléculas 3.1.-El espectro electromagnético 3.2.-Espectros de absorción y de emisión (espontánea y estimulada) 3.2.1.-Momento dipolar
Tema 3.-Espectroscopía de biomoléculas Tema 3.-Espectroscopía de biomoléculas 3.1.-El espectro electromagnético 3.2.-Espectros de absorción y de emisión (espontánea y estimulada) 3.2.1.-Momento dipolar
Tema 2. Los átomos: estructura electrónica.
 Tema 2. Los átomos: estructura electrónica. 1. Introducción. 2. Antecedentes de la mecánica ondulatoria. 3. Mecánica ondulatoria. 4. Orbitales atómicos. 5. Configuraciones electrónicas. 1. Introducción
Tema 2. Los átomos: estructura electrónica. 1. Introducción. 2. Antecedentes de la mecánica ondulatoria. 3. Mecánica ondulatoria. 4. Orbitales atómicos. 5. Configuraciones electrónicas. 1. Introducción
La Teoría de Hückel: Antecedentes
 La Teoría de Hückel: Antecedentes c = Las ecuaciones seculares: s [ H as ESas ] (un conjunto de ecuaciones simultáneas para todos los átomos) s () a, s las etiquetas de los átomos c s los coeficientes
La Teoría de Hückel: Antecedentes c = Las ecuaciones seculares: s [ H as ESas ] (un conjunto de ecuaciones simultáneas para todos los átomos) s () a, s las etiquetas de los átomos c s los coeficientes
DISTORSIONES TETRAGONALES DE LA GEOMETRÍA OCTAÉDRICA
 DISTORSIONES TETRAGONALES DE LA GEOMETRÍA OCTAÉDRICA Si en un complejo octaédrico dos ligantes trans (por ejemplo en el eje z) se acercan o alejan del ion metálico se dice que el complejo resultante está
DISTORSIONES TETRAGONALES DE LA GEOMETRÍA OCTAÉDRICA Si en un complejo octaédrico dos ligantes trans (por ejemplo en el eje z) se acercan o alejan del ion metálico se dice que el complejo resultante está
29/09/2010 TEMA 2. CONTENIDO. Continuación Tema 2. Msc. María Angélica Sánchez P. n= 1, 2, 3, 4, n=2 n=3. n=1. Ecuación de onda de Schrödinger
 Continuación Tema 2 Msc. María Angélica Sánchez P. TEMA 2. CONTENIDO Introducción a la forma y características de la tabla periódica. Introducción a los modelos atómicos. El Método Científico. Introducción
Continuación Tema 2 Msc. María Angélica Sánchez P. TEMA 2. CONTENIDO Introducción a la forma y características de la tabla periódica. Introducción a los modelos atómicos. El Método Científico. Introducción
Física Nuclear Preguntas de Opción Múltiple
 Física Nuclear Preguntas de Opción Múltiple PSI Física Nombre: 1. Un elemento químico desconocido se representa como: Z X. Cuál es el nombre de Z? A. Número de masa atómica B. Número atómico C. Número
Física Nuclear Preguntas de Opción Múltiple PSI Física Nombre: 1. Un elemento químico desconocido se representa como: Z X. Cuál es el nombre de Z? A. Número de masa atómica B. Número atómico C. Número
Acoplamiento de Russell Saunders Términos espectroscópicos Diagramas de Orgel Diagramas de Tanabe Sugano Espectroscopía electrónica de absorción
 Acoplamiento de Russell Saunders Términos espectroscópicos Diagramas de Orgel Diagramas de Tanabe Sugano Espectroscopía electrónica de absorción Números cuánticos n l m l Número cuántico principal gobierna
Acoplamiento de Russell Saunders Términos espectroscópicos Diagramas de Orgel Diagramas de Tanabe Sugano Espectroscopía electrónica de absorción Números cuánticos n l m l Número cuántico principal gobierna
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica
 Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Ultima actualización 3 de febrero de 205 Índice. Aproximación
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Ultima actualización 3 de febrero de 205 Índice. Aproximación
2.2Evolución del modelo atómico:
 Tema 2.1.- El átomo. 2.2Evolución del modelo atómico: 2.2.- Modelo mecánico cuántico ondulatorio 2.2.1.- Números cuánticos 2.3.- Configuración electrónica 2.3.1.- normal, su desarrollo y mención de: spin.
Tema 2.1.- El átomo. 2.2Evolución del modelo atómico: 2.2.- Modelo mecánico cuántico ondulatorio 2.2.1.- Números cuánticos 2.3.- Configuración electrónica 2.3.1.- normal, su desarrollo y mención de: spin.
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS FUNDAMENTOS DE LA ESPECTROSCOPIA
 Integrantes: Ipiales Gabriela Química de Alimentos Olmos Wendy Química Farmacéutica Día: Miércoles 9-11 Fecha: 05/07/2011 DEFINICIÓN DE ORBITALES ATÓMICOS Un orbital atómico representa una región del espacio
Integrantes: Ipiales Gabriela Química de Alimentos Olmos Wendy Química Farmacéutica Día: Miércoles 9-11 Fecha: 05/07/2011 DEFINICIÓN DE ORBITALES ATÓMICOS Un orbital atómico representa una región del espacio
El campo magnético en los medios materiales. Tema 10 Electromagnetismo Grupo C
 El campo magnético en los medios materiales Tema 10 Electromagnetismo Grupo C El campo magnético y la materia El átomo como un dipolo magnético Imanación y corrientes de imanación Teorema de Àmpere para
El campo magnético en los medios materiales Tema 10 Electromagnetismo Grupo C El campo magnético y la materia El átomo como un dipolo magnético Imanación y corrientes de imanación Teorema de Àmpere para
Donde se ubican en el Átomo E L E C T R O N E S. Modelo Atómico. Que energía tienen. Como interactúan
 Modelo Atómico 1 Modelo Atómico E L E C T R O N E S Donde se ubican en el Átomo Que energía tienen Como interactúan 2 Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran
Modelo Atómico 1 Modelo Atómico E L E C T R O N E S Donde se ubican en el Átomo Que energía tienen Como interactúan 2 Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran
 ESTRUCTURA DE LA MATERIA 1.-junio 1996 a) Establezca cuales de las siguientes series de números cuánticos serían posibles y cuáles imposibles para especificar el estado de un electrón en un átomo: serie
ESTRUCTURA DE LA MATERIA 1.-junio 1996 a) Establezca cuales de las siguientes series de números cuánticos serían posibles y cuáles imposibles para especificar el estado de un electrón en un átomo: serie
Métodos Espectrofotométricos. Capítulos 24 y 25 de Fundamentos de Química Analítica Skoog-West-Holler-Crouch (octava Ed.)
 Métodos Espectrofotométricos Capítulos 24 y 25 de Fundamentos de Química Analítica Skoog-West-Holler-Crouch (octava Ed.) 1 Radiación electromagnética Longitud de onda : Frecuencia en s -1 Hertz Numero
Métodos Espectrofotométricos Capítulos 24 y 25 de Fundamentos de Química Analítica Skoog-West-Holler-Crouch (octava Ed.) 1 Radiación electromagnética Longitud de onda : Frecuencia en s -1 Hertz Numero
CONFIGURACION ELECTRONICA
 CONFIGURACION ELECTRONICA Números cuánticos Las soluciones de la ecuación de onda depende de cuatro parámetros, n, l, m l y s. n Número cuántico principal (n = 1, 2, 3, ) l Número cuántico secundario (m
CONFIGURACION ELECTRONICA Números cuánticos Las soluciones de la ecuación de onda depende de cuatro parámetros, n, l, m l y s. n Número cuántico principal (n = 1, 2, 3, ) l Número cuántico secundario (m
Estructura de los átomos: Estructura electrónica
 Estructura de los átomos: Modelos atómicos Después de los modelos iniciales de Thomson y Rutherford, en los que los electrones podían tener cualquier energía, una serie de hechos experimentales llevaron
Estructura de los átomos: Modelos atómicos Después de los modelos iniciales de Thomson y Rutherford, en los que los electrones podían tener cualquier energía, una serie de hechos experimentales llevaron
Práctica 3. Susceptibilidad Magnética
 Laboratorio de Química de Coordinación Práctica 3. Susceptibilidad Magnética Parte II: Las técnicas Tarea previa 1.- Escribir la configuración electrónica de los siguientes iones: Ni 2+ Cu + V 2+ Cr 3+
Laboratorio de Química de Coordinación Práctica 3. Susceptibilidad Magnética Parte II: Las técnicas Tarea previa 1.- Escribir la configuración electrónica de los siguientes iones: Ni 2+ Cu + V 2+ Cr 3+
Efectos del solvente y del entorno local sobre la fluorescencia
 Efectos del solvente y del entorno local sobre la fluorescencia C 6 C 7 Temario Efectos generales del solvente Efectos específicos del solvente Efectos de la temperatura Transferencia interna de carga
Efectos del solvente y del entorno local sobre la fluorescencia C 6 C 7 Temario Efectos generales del solvente Efectos específicos del solvente Efectos de la temperatura Transferencia interna de carga
Información IR EM RMN UV DC
 Técnicas de determinación estructural Información IR EM RMN UV DC Fórmula molecular Grupos funcionales - XXX X - - XXX X XX X - Conectividad X X XXX X - Geometría/ - - XXX - X estereoquímica Quiralidad
Técnicas de determinación estructural Información IR EM RMN UV DC Fórmula molecular Grupos funcionales - XXX X - - XXX X XX X - Conectividad X X XXX X - Geometría/ - - XXX - X estereoquímica Quiralidad
Capítulo 1: Estructura atómica y Sistema periódico
 Capítulo 1: Estructura atómica y Sistema periódico ACTIVIDADES DE RECAPITULACIÓN 1. Qué radiación se propaga con mayor velocidad en el vacío, los rayos X o las ondas de radio? Tanto los rayos X como las
Capítulo 1: Estructura atómica y Sistema periódico ACTIVIDADES DE RECAPITULACIÓN 1. Qué radiación se propaga con mayor velocidad en el vacío, los rayos X o las ondas de radio? Tanto los rayos X como las
QUÍMICA ORGÁNICA. Dr. José Luis Zacur
 QUÍMICA ORGÁNICA 1 Mecánica Cuántica: Desarrolla expresiones matemáticas para describir el movimiento de un electrón en función de su energía. Se conocen como ecuaciones de onda (dualidad onda-partícula).
QUÍMICA ORGÁNICA 1 Mecánica Cuántica: Desarrolla expresiones matemáticas para describir el movimiento de un electrón en función de su energía. Se conocen como ecuaciones de onda (dualidad onda-partícula).
4. Identificar un isótopo radiactivo del carbono e indicar su uso. 5. Cuál es la configuración electrónica del vanadio?
 ESTRUCTURA ATÓMICA 1. Qué afirmación sobre el número de electrones, protones y neutrones del átomo es correcta? A El número de neutrones menos el número de electrones es cero. B. El número de protones
ESTRUCTURA ATÓMICA 1. Qué afirmación sobre el número de electrones, protones y neutrones del átomo es correcta? A El número de neutrones menos el número de electrones es cero. B. El número de protones
QUÍMICA de 2º de BACHILLERATO ESTRUCTURA DE LA MATERIA
 QUÍMICA de 2º de BACHILLERATO ESTRUCTURA DE LA MATERIA EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013)
QUÍMICA de 2º de BACHILLERATO ESTRUCTURA DE LA MATERIA EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013)
Estructura Fina. (Multiplicidad) de las líneas atómicas (serie Balmer, por ejemplo). Exp λ 6563 Å Δλ =5.4 Å. predicción
 Capítulo 8 Espín electrónico Estructura Fina. (Multiplicidad) de las líneas atómicas (serie almer, por ejemplo). predicción Exp. 3 λ 6563 Å Δλ =5.4 Å Efecto Zeeman (896). En un campo magnético el estado
Capítulo 8 Espín electrónico Estructura Fina. (Multiplicidad) de las líneas atómicas (serie almer, por ejemplo). predicción Exp. 3 λ 6563 Å Δλ =5.4 Å Efecto Zeeman (896). En un campo magnético el estado
UNIDAD 1: PRINCIPIOS DE LA QUÍMICA
 UNIDAD 1: PRINCIPIOS DE LA QUÍMICA MODELO ATOMICO DE DALTON RAYOS CATÓDICOS (Thomsom) EL ELECTRÓN MODELO ATÓMICO DE THOMSOM RAYOS CANALES (Goldstein) EL PROTÓN Rutherford MODELO ATÓMICO DE RUTHERFORD Chadwick:
UNIDAD 1: PRINCIPIOS DE LA QUÍMICA MODELO ATOMICO DE DALTON RAYOS CATÓDICOS (Thomsom) EL ELECTRÓN MODELO ATÓMICO DE THOMSOM RAYOS CANALES (Goldstein) EL PROTÓN Rutherford MODELO ATÓMICO DE RUTHERFORD Chadwick:
1- Cuál es el origen del momento magnético permanente de los átomos que lo poseen?
 ASIGNATURA FISICA II AÑO 2012 GUIA NRO. 11 MAGNETISMO EN MEDIOS MATERIALES Bibliografía Obligatoria (mínima) Capítulo 30 Física de Serway Tomo II Apunte de cátedra: capítulo XI PREGUNTAS SOBRE LA TEORIA
ASIGNATURA FISICA II AÑO 2012 GUIA NRO. 11 MAGNETISMO EN MEDIOS MATERIALES Bibliografía Obligatoria (mínima) Capítulo 30 Física de Serway Tomo II Apunte de cátedra: capítulo XI PREGUNTAS SOBRE LA TEORIA
1.1 DEFINICIÓN CLÁSICA DEL MOMENTO ANGU- LAR
 Chapter MOMENTO ANGULAR La teoría del momento angular en mecánica cuántica es de gran importancia tanto por el número como por la variedad de sus consecuencias. A partir de la espectroscopía rotacional,
Chapter MOMENTO ANGULAR La teoría del momento angular en mecánica cuántica es de gran importancia tanto por el número como por la variedad de sus consecuencias. A partir de la espectroscopía rotacional,
ENLACE QUIMICO. Teoría de enlace de valencia Hibridación de orbitales y enlaces múltiples
 ENLACE QUIMICO Teoría de enlace de valencia Hibridación de orbitales y enlaces múltiples Teoría de Enlace de Valencia Teoría de Lewis: El enlace covalente se forma cuando dos átomos comparten pares de
ENLACE QUIMICO Teoría de enlace de valencia Hibridación de orbitales y enlaces múltiples Teoría de Enlace de Valencia Teoría de Lewis: El enlace covalente se forma cuando dos átomos comparten pares de
