CAPÍTULO 1. RESONANCIA PARAMAGNÉTICA ELECTRÓNICA (EPR)
|
|
|
- Pablo Murillo Méndez
- hace 7 años
- Vistas:
Transcripción
1 CAPÍTULO 1. RESONANCIA PARAMAGNÉTICA ELECTRÓNICA (EPR) 1.1. Introducción La Resonancia Paramagnética Electrónica EPR puede ser vista como una extensión del experimento de Stern-Gerlach, quienes mostraron que un átomo con momento magnético neto solo puede tomar orientaciones discretas en un campo magnético. Posteriormente Unhlenbeck y Goudsmith relacionaron el momento magnético electrónico con las propiedades de los radicales. Consecutivo a su descubrimiento, fueron los químicos los encargados de dar a la EPR la importancia que ocupa actualmente en el mundo, pues demostraron que la mayor parte de los compuestos orgánicos e inorgánicos tienen momento magnético no nulo. Desde el descubrimiento de la Resonancia Paramagnética Electrónica por Zavoisky (1944) esta ha sido aplicada a una gran variedad de problemas en física de la materia condensada y química y más recientemente a cuestiones en geología, arqueología y paleoantropología, dosimetría de radiación, bioquímica, biología y ciencias del espacio (Rink, 1997). La técnica EPR es una técnica experimental espectroscópica poderosa, versátil y no destructiva. Un gran número de libros en EPR han sido publicados para físicos, químicos y biólogos tanto en niveles introductorios como avanzados. El espectro EPR es usualmente caracterizado por los parámetros de un Hamiltoniano de spin que son tratados con sumo cuidado en mecánica cuántica. Estos libros contienen los conceptos de mecánica cuántica necesarios para el análisis de los espectros EPR. La técnica EPR es un metodo que permite medir la concentración de centros paramagnéticos y radicales libres en sólidos y líquidos. Su aplicación en dosimetría y datación se basa en el hecho de que la radiación ionizante produce centros paramagnéticos estables en diversos materiales. En este capítulo se muestra los principios teóricos que conforman la técnica EPR, que comprende la interacción Zeeman Electrónica, Interacción fina, Interacción hiperfina, interacción cuadrupolar, e interacción Zeeman nuclear. También se muestra una breve descripción de un equipo de EPR y sus principios de funcionamiento. 1
2 1.2. Resonancia Paramagnética Electrónica (EPR) Las aplicaciones de la EPR son muy numerosas y se extienden a diversos campos de investigación de la física, química, geología, biología medicina. Una lista de la aplicaciones de la EPR incluyen: defectos puntuales paramagnéticos en monocristales (tales como: centros de color, electrones desapareados, huecos, vacancias intersticiales, iones de metales de transición y iones de tierras raras), radicales libres en fases sólidas, líquidas o gaseosas, aceptores o donadores en semiconductores y sistemas con más de un electrón desapareado (como sistemas en estado triplete, birradicales y multirradicales). Actualmente también se aplica en Datación y Dosimetría. El momento magnético es directamente proporcional al momento angular de spin y tenemos, por tanto, el vector momento magnético (Ikeya 1993). g S (1.1) B El signo negativo indica que, para un electrón, el momento magnético es antiparalelo al momentum angular de spin. g, se le denomina factor-g y para el electrón libre su valor es μ B es el Magnetón de Bohr cuyo valor es: x10-24 J T -1. La interpretación de un espectro de EPR debe hacerse en términos del entendimiento mecánico-cuántico de las interacciones de la radiación con la materia y del llamado efecto Zeeman. Clásicamente, la energía de interacción de un dipolo magnético con un campo magnético externo, viene dada por la relación: W B B cos 0 0 (1.2) En donde es el momento dipolar magnético y B 0 es el campo magnético externo. 2
3 Teniendo en cuenta las ecuaciones (1.1) y (1.2) obtenemos el Hamiltoniano para un electrón en presencia de un campo magnético Hˆ g S B 1 (1.3) B 0 Si el campo magnético se aplica en la dirección z, el Hamiltoniano se transforma en: Hˆ g B S B 0 (1.4) z El único operador en el segundo miembro de la ecuación (1.4) es S z y por tanto, los valores propios del Hamiltoniano son simples múltiplos de los valores propios de éste, E gbb0 M S (1.5) Como M s = ± 1/2 hay dos estados degenerados en campo cero y cuya separación entre los llamados niveles Zeeman aumenta linealmente con el campo magnético B = B 0. Figura 1.1. Niveles de energía para un electrón (S=1/2) en un campo magnético B 0. 3
4 Igualando la separación de los dos niveles a un cuanto de radiación a través de la condición de frecuencia de Bohr, obtenemos la condición básica de resonancia para un electrón libre. E h g B (1.6) B 0 La ecuación (1.6) es conocida como la condición básica de resonancia. La absorción de energía causa una transición del nivel energético inferior al nivel energético superior. Las transiciones permitidas para un sistema de spin S se obtienen a partir de la regla de selección: m S 1 La absorción de la radiación (en el rango de las microondas) por el sistema de spin puede ser observada si la frecuencia de la microonda satisface la condición de resonancia (1.6) (ver figura 1.2) Figura 1.2. Curva de absorción de las microondas por una muestra, en función del campo magnético externo. Las diferencias de energía estudiada por espectroscopia EPR son predominantemente debidas a interacción del campo magnético con los electrones desapareados. 4
5 La figura 1.1 muestra el esquema de niveles de energía para una partícula con spin ½ en un campo magnético. En ausencia de campo estático, la partícula se encuentra en cualquiera de los dos estados energéticamente equivalentes (los estados de spin son degenerados). La componente constante de campo magnético aplicado interactúa con el momento dipolar del electrón desapareado, eliminando el degeneramiento de spin y produciendo dos niveles de estados de spin, convencionalmente llamados, spin hacia abajo y spin hacia arriba y denotados por M s = -1/2 y M s = +1/2 respectivamente. Sin embargo, algunas veces los electrones desapareados interactúan con uno o más núcleos cercanos que poseen momento magnético nuclear diferente de cero, lo que resulta en un desdoblamiento de los niveles de energía asociados con el sistema de spin. Esta interacción es conocida como Interacción Hiperfina. Los niveles nucleares de energía están igualmente cuantizados, y se representan por m I. De esta manera, un núcleo con spin I presentará estados nucleares con números cuánticos I, I + 1,..., I. Entonces, para un sistema con spin electrónico S y nuclear I el número de niveles de energía estaría dado por (2S + 1) (2I + 1), y las transiciones permitidas están dadas por las reglas de selección: 1 0 (1.7) m s m I La situación para la interacción de un sistema de spin S = ½ con un I =½, puede ser ilustrada cualitativamente por el diagrama de Stikes, como se muestra en la figura 1.3 Figura 1.3. Diagrama de Stikes 5
6 El espectro EPR está representado por dos líneas de absorción, que corresponde a las dos transiciones que obedecen las reglas de selección (1.7). (Figura 1,4). Para este simple ejemplo la separación entre las líneas es una constante llamada constante acoplamiento Hiperfino A. En muchos problemas prácticos; sin embargo, la interacción Hiperfina es anisotrópica y el tratamiento tensorial es necesario para caracterizar completamente un sistema paramagnético dado. Figura 1.4 Esboce del espectro EPR con interacción hiperfina El Hamiltoniano de espin, teniendo en cuenta la interacción Hiperfina, es: Hˆ g S B1ˆ I A S1ˆ B Donde I es el espin nuclear y A es la constante de acoplamiento Hiperfino. El Hamiltoniano de spin para el electrón, teniendo en cuenta todas las interacciones, es: Hˆ Hˆ Hˆ Hˆ Hˆ Hˆ (1.8) ze hf sf Q zn Dónde: H ze S g B Interacción Zeeman Electrónica B 0 6
7 Hhf I A S Interacción Hiperfina Hsf S D S Interacción de estructura fina HQ I Q I Interacción nuclear cuadrupolar H g I B Interacción Zeeman Nuclear zn N N 0 En estas ecuaciones S representa el espín electrónico, I el espin nuclear, μ B es el Magnetón de Bohr y g, A, D y Q son tensores específicos. Dependiendo del tipo de interacción algunos de los términos en el Hamiltoniano de espin podrían no estar presentes en el problema a resolver. El término Zeeman electrónico describe la interacción entre el espín efectivo S y el campo magnético aplicado. Está compuesto por las contribuciones de las interacciones dipolomagnéticas y espín-órbita (so). Hˆ Hˆ Hˆ (1.10) ze mag so Aquí: H ( ) mag BB0 L gs (1.11) 7
8 Hso L S (1.12) En estas ecuaciones L Representa el momentum angular orbital del electrón y λ es el parámetro de acoplamiento spin-órbita. Sustituyendo las ecuaciones (1.11) y (1.12) en (1.10) obtenemos: ze B 0 H B L gs L S (1.13) H B g S ze B 0 Donde: g g12λ (1.14) Λ y 1 son matrices, Λ se relaciona con la anisotropía o desviación del valor de espín del electrón libre. Una deducción detallada de ecuación (1.14) puede encontrarse en (Weil, 2007). La cantidad g en el caso general forma un tensor simétrico con seis componentes independientes; es decir; g ij g ji g g g g g g g g g g xx xy xz yx yy yz zx zy zz (1.15) 8
9 Para una orientación cualquiera (x,y,z). Si g es diagonal, la interacción Zeeman del electrón puede ser escrita en la siguiente forma: H S g B S g B S g B (1.16) ze B x x x y y y z z z Donde: g x = g xx, g y = g yy, g z = g zz. En los casos de geometría axial el factor g suele ser expresado en función del factor g paralelo (g ǁ ) y el factor g perpendicular (g ) : g ǁ =g zz y g =g yy =g xx (Ikeya, 1993). El término de interacción hiperfina en el Hamiltoniano de espín describe la interacción entre el momento magnético de un electrón desapareado y el momento magnético de un núcleo cercano. En forma general, se describe mediante un tensor A. Este tensor típicamente contiene una parte isotrópica denotada por a y una parte anisotrópica representada por B. A ( a1 B) (1.17) La parte isotrópica a es llamada termino de contacto de Fermi y se relaciona a la densidad de espín desapareada en un sitio nuclear. Para un núcleo que ocupa un sitio r 1, el parámetro de contacto de Fermi es: 8P a gg 2 N en r1 (1.18) 3 Donde μ e y μ N son los momentos magnéticos electrónico y nuclear respectivamente. La parte anisotrópica del tensor A es un resultado de la interacción dipolo-dipolo entre los momentos del electrón y el núcleo y puede ser descrito por un tensor cuyos elementos son ij N e N r r 3x 2 ix j dij 3 ( 5 3 ) (1.19) B gg r d r 9
10 Aquí () r 2 es la función de densidad electrónica. Respecto a los ejes principales del sistema, el Hamiltoniano de interacción hiperfina se hace: Hhf I xax Sx I yays y I zaz Sz (1.20) Donde A x, A y, A z son los elementos de la diagonal de la matriz A. Como el caso de la interacción Zeeman electrónica. Para sistemas con altos valores de espín (S>1/2 ) se puede observar una interacción adicional llamada desdoblamiento de estructura fina. Esta interacción es debida al campo eléctrico cristalino que sienten los electrones desapareados a través del acoplamiento espínórbita y la interacción dipolo-dipolo magnético entre electrones desapareados. Se representa por el tensor de segundo orden, llamado el tensor de estructura fina D. Esta interacción permite un desdoblamiento de las líneas EPR en campo magnético cero. Respecto a sus ejes principales el Hamiltoniano de estructura fina puede ser escrito como: H D S D S D S (1.21) sf x x y y z z Aquí D x, D y, D z son los elementos de la diagonal del tensor D de segundo orden. La traza de D es igual a cero; es decir; D x + D y + D z = 0; por consiguiente hay solo dos términos de los elementos de la diagonal independientes. Usualmente los valores principales del tensor D son expresados en términos de dos parámetros independientes D y E por medio de las siguientes relaciones: D x 1 D E 3 D y 1 D E 3 (1.22) 10
11 2 D z 3 D Reemplazando las ecuaciones (1.22) en la ecuación (1.21) se obtiene equivalente para el Hamiltoniano de estructura fina: otra expresión 2 1 H 2 2 fs D Sz 3 S S 1 E Sx Sy (1.23) Donde D es la parte axialmente simétrica y E el parámetro asimétrico. Existe también una interacción que debe ser tomada en cuenta para sistemas que tienen altos valores de espín nuclear (I > 1/2 ) llamada interacción nuclear cuadrupolar. Esta interacción cuadrupolar se representa por el tensor de acoplamiento cuadrupolar Q, el cual es el producto del momento nuclear cuadrupolar y el gradiente del campo eléctrico en el núcleo debido a todos los electrones que lo rodean. Para una distribución de carga cúbica, el gradiente de campo eléctrico es cero, pero si la simetría de la red o la simetría local del defecto puntual es menor, el gradiente de campo eléctrico podría ser distinto de cero y la magnitud del acoplamiento cuadrupolar es entonces una medida de la distribución relativa de carga alrededor. El termino de interacción cuadrupolar en el Hamiltoniano de espín está dado por: 2 3eQ V 2 1 HQ 2 I z 3 I I 1 4I 2I 1 z (1.24) Donde e es la carga del electrón, Q es el momento cuadripolar nuclear V es el potencial de campo eléctrico cristalino y 2 V 2 z es el gradiente de campo eléctrico. La energía cuadrupolar es usualmente del orden de cm -1. La cual es muy pequeña comparada con la energía de interacción Zeeman. Similarmente al tensor de estructura fina, la traza del tensor 11
12 cuadrupular Q es pequeña; es decir; Q x + Q y + Q z = 0 y solo dos parámetros independientes son necesarios para describir la interacción (Weil, 2007). El último término de la ecuación (1.8) es la interacción Zeeman nuclear. Este término describe la interacción del momento magnético nuclear con el campo magnético externo aplicado. Típicamente los valores de interacción de energía de esta interacción están en el rango de cm Aspectos Experimentales de la Resonancia Paramagnética Electrónica (EPR). La Resonancia Paramagnética Electrónica (EPR) se engloba dentro de las técnicas espectroscópicas modernas utilizadas en el estudio de la estructura y propiedades de la materia (Lezama, 1993). Sus principios teóricos contienen grandes similitudes con otras muchas espectroscopías cuya fuente energética es la radiación electromagnética. La espectroscopía EPR involucra la radiación electromagnética que interacciona con el momento magnético de los electrones de la muestra (interacción dipolar magnética) y para tener señales por EPR es necesaria la aplicación de un campo magnético externo a la muestra. Los procesos inelásticos de interacción radiación - materia, entre los que se encuentra la interacción que da lugar en la EPR, dan información sobre los distintos estados energéticos de la materia. El principal proceso físico que da origen a la separación entre niveles energéticos en la materia es el efecto Zeeman. Otra energía de interacción considerada son las interacciones magnéticas electrón-núcleo y electrón-electrón. En espectroscopía convencional, la frecuencia es variada o barrida desde un valor mínimo hasta un valor máximo y la frecuencia a la cual ocurre la absorción es proporcional a la diferencia de energía de los estados energéticos. En espectroscopia EPR la frecuencia de la radiación electromagnética es mantenida constante y el campo magnético es variado o 12
13 barrido. Para los experimentos EPR la frecuencia de la radiación está en el rango de los Gigahertz (en la zona de las microondas para banda X). La absorción de la microondas por el sistema de espín puede ser observada si la frecuencia de la microonda satisface la condición de resonancia de la ecuación (1.6). Sin embargo, en el sistema de detección empleado en EPR, el espectro observado en el monitor no corresponde al espectro de absorción sino a su primera derivada (figura 1.5). Figura 1.5. Curva de absorción de microondas y su primera derivada que es el espectro obtenido en el equipo de EPR Breve Descripción del Funcionamiento de un Espectrómetro EPR Sin entrar en los múltiples accesorios que forman un equipo comercial, se tratará de explicar brevemente cómo funcionan los espectrómetros de EPR y cuáles son sus componentes principales. La figura 1.6 es un diagrama de bloques de un espectrómetro EPR. La fuente de radiación electromagnética y el detector se hallan en un accesorio que se denomina "puente de microondas, que contiene al Klystron y al detector". Más detalles son dados en la sección La muestra a analizar se coloca en el interior de lo denominado "cavidad". La cavidad se sitúa entre los polos de un electroimán, los cuales proporcionan el campo magnético 13
14 necesario para realizar los ensayos, se logra así tener la diferencia energética entre los niveles energéticos igual a la frecuencia de la radiación incidente. Finalmente, se dispone de un bloque de control que permite coordinar las diferentes unidades y registrar los datos de salida. A continuación se describen de forma simplificada estos componentes y su modo de funcionamiento. Figura 1.6. Principales componentes de un espectrómetro EPR Puente de Microondas Los componentes de un puente microondas comercial son numerosos, pero en la Figura 1.7 se han incluido únicamente aquellos elementos de mayor interés para el usuario del espectrómetro. Figura 1.7. Principales componentes de un puente de microondas. 14
15 La fuente de microondas es generalmente un oscilador electrónico (klystron) que proporciona una alta potencia de microondas. La potencia de salida del klystron no puede variarse fácilmente y para conseguir este efecto se coloca un atenuador variable que permite ajustar con precisión la potencia de microondas que llega a la muestra. La mayoría de los equipos de EPR actuales trabajan con microondas reflejadas, y no con la transmitida. Por este motivo se precisa que al detector sólo llegue la microonda que refleja la cavidad. Para conseguir este efecto se dispone de una válvula de sentido único (circulador) que impide que las microondas lleguen al detector sin pasar por la cavidad y, al mismo tiempo, que las ondas reflejadas por ésta vuelvan hacia el klystron. El detector usa un diodo tipo Shocsky y el Brazo de referencia no es más que un camino de suministro adicional de microondas al detector. Esto garantiza que el diodo detector trabaje su zona lineal de funcionamiento (que es mayor o igual a corrientes de 200µA) La Cavidad La cavidad es en esencia una caja metálica (de forma cilíndrica o rectangular, generalmente) en cuyo interior se va a producir la resonancia. La cavidad almacena la energía de microondas cuando se genera en ella un patrón de ondas estacionarias en la que se procuran obtener máximos de campo magnético y mininos de campo eléctrico en el centro de la cavidad y de esta forma asegurar la interacción del momento magnético de la muestra con el campo magnético externo de las microondas (Figura 1.8). La geometría de la cavidad es en principio arbitraria, pero no sus dimensiones. La obtención de resonancia exige que una de las dimensiones de la cavidad sea exactamente igual a la longitud de onda de la radiación, por tanto cuanto mayor sea la frecuencia de microondas, menores serán las dimensiones de la cavidad. El campo magnético estático externo que provocan los electroimanes debe ser perpendicular al campo magnético de las microondas para que pueda producirse absorción de las microondas por parte de la muestra. Una vez producida esta transición se manifiesta en una absorción de las microondas al interior de la cavidad (figura 1.8). 15
16 Muchas sustancias presentan absorción del campo eléctrico de las microondas y esto se traduce en un incremento de la energía disipada y por consiguiente en una disminución de la sensibilidad de la cavidad. Figura 1.8. Disposición de los campos eléctricos y magnéticos en la cavidad EPR, puede observarse que en el centro de la cavidad se tienen máximos de campo magnético y mínimos de campo eléctrico Detector Sensible a la Fase El registro de las señales de EPR utilizando el sistema anteriormente descrito es prácticamente inviable y la casi totalidad de los equipos utilizan una técnica conocida como "Detección Sensible a la Fase" que permite mejorar la sensibilidad del aparato, eliminando gran parte del ruido de fondo y las inestabilidades de la línea base. La detección de la señal se produce de la siguiente manera: La intensidad de campo magnético que la muestra percibe es una intensidad modulada sinusoidalmente a una determinada frecuencia (habitualmente 100 KHz). Esto se consigue sumando una componente alternante al campo estático B0, de forma que el campo magnético total es: Br = B0 + Bmsen(wt), con Bm denominada amplitud de modulación. Si la amplitud de modulación de campo es pequeña en comparación con la anchura de una línea resonante, la amplitud de la señal detectada será aproximadamente proporcional a la pendiente de la curva de absorción. Como puede observarse en la Figura 1.9, cuando el campo total varía entre los límites B1 y B2, 16
17 la corriente detectada varía sinusoidalmente entre I1 e I2 y la variación sinusoidal de B hace que la intensidad registrada también ocurra a la misma frecuencia (100kHz). Cuando la pendiente de la curva de absorción es cero, la corriente detectada será también nula. En los puntos de inflexión, cuando la pendiente es máxima, la corriente detectada también será máxima. Por consiguiente, la señal registrada será aproximadamente la primera derivada de la curva de absorción. Figura 1.9. Efecto de la modulación de campo sobre la corriente recibida en el detector. Finalmente, el detector amplifica la señal modulada y la compara con una señal de referencia, filtrando todas las componentes que no presenten exactamente la misma frecuencia y fase que la modulación de campo empleada. De esta forma se eliminan gran parte de las interferencias eléctricas y ruido de fondo El Estado Físico De La Muestra El estado físico de la muestra puede ser a priori cualquiera, y de hecho se pueden registrar espectros en disoluciones líquidas o congeladas, en forma de polvo, monocristal e incluso en fase gas. Sin embargo, es preciso tener en cuenta que el espectro registrado y la información que puede obtenerse si depende drásticamente de las condiciones de medida. Cuando la muestra se presenta en forma de polvo, cada pequeño cristal se orienta al azar frente al campo magnético, siendo, en principio, todas las orientaciones igualmente probables. 17
18 Tanto en muestras en polvo como en disoluciones congeladas es preciso evitar la aparición de orientaciones preferenciales. Su presencia se detecta muy fácilmente simplemente registrando una segunda vez el espectro después de haber rotado un poco la muestra. Para eliminarlas en el caso del polvo es preciso proceder a una molienda muy cuidadosa. 18
19 Bibliografía. Barandiarán J.M., Interacción Radiación Materia y Espectroscopias, Espectroscopia de Resonancia Paramagnética Electrónica, Servicio Editorial de la Universidad del País Vasco, primera edición, p , Bilbao. Espitia M, Estudio por Resonancia Paramagnética Electrónica EPR de Monocristales KDP Irradiados con Electrones de Alta Energía. Tesis de Maestría, Universidad Nacional de Colombia, Bogotá. Ikeya, M., New Applications Of Electron Spin Resonance: Dating, Dosimetry and Microscopy. World Scientific Publishing Company, Capítulo 2. Poole Charles, Farach Horacio. Teoria de la Resonancia Magnética, Editorial Reverte S.A, Vidal José, 1993, Aspectos Experimentales de la Resonancia Paramagnética Electrónica, Espectroscopia de Resonancia Paramagnética Electrónica, Servicio Editorial de la Universidad del País Vasco, primera edición, p , Bilbao. Weil Jhon, Bolton James. Electron Paramagnetic Resonance, Elementary Theory and Practical Applications, Second Edition, Wily Interscience a John Wiley & Sons,
Trabajo Practico nº2
 Trabajo Practico nº2 Espectroscopía de Resonancia Paramagnética Electrónica (RPE). Introducción La Resonancia Paramagnética Electrónica (RPE, en inglés EPR: Electron Paramagnetic Resonance) es una técnica
Trabajo Practico nº2 Espectroscopía de Resonancia Paramagnética Electrónica (RPE). Introducción La Resonancia Paramagnética Electrónica (RPE, en inglés EPR: Electron Paramagnetic Resonance) es una técnica
Tema 14 11/02/2005. Tema 8. Mecánica Cuántica. 8.1 Fundamentos de la mecánica cuántica
 Tema 14 11/0/005 Tema 8 Mecánica Cuántica 8.1 Fundamentos de la mecánica cuántica 8. La ecuación de Schrödinger 8.3 Significado físico de la función de onda 8.4 Soluciones de la ecuación de Schrödinger
Tema 14 11/0/005 Tema 8 Mecánica Cuántica 8.1 Fundamentos de la mecánica cuántica 8. La ecuación de Schrödinger 8.3 Significado físico de la función de onda 8.4 Soluciones de la ecuación de Schrödinger
Espectrometría de luminiscencia molecular Cap.15
 Espectrometría de luminiscencia molecular Cap.15 Luz cuyo origen no radica exclusivamente en las altas temperaturas Se da en sustancias que pueden absorber energía, excitándose a niveles mayores y emitirla
Espectrometría de luminiscencia molecular Cap.15 Luz cuyo origen no radica exclusivamente en las altas temperaturas Se da en sustancias que pueden absorber energía, excitándose a niveles mayores y emitirla
ÍNDICE
 ÍNDICE 1 Radiación térmica y el postulado de Planck... 17 1-1 Introducción... 19 1-2 Radiación térmica... 19 1-3 Teoría clásica de la cavidad radiante... 24 1-4 Teoría de Planck de la cavidad radiante...
ÍNDICE 1 Radiación térmica y el postulado de Planck... 17 1-1 Introducción... 19 1-2 Radiación térmica... 19 1-3 Teoría clásica de la cavidad radiante... 24 1-4 Teoría de Planck de la cavidad radiante...
Ejercicios de Ondas Mecánicas y Ondas Electromagnéticas.
 Ejercicios de Ondas Mecánicas y Ondas Electromagnéticas. 1.- Determine la velocidad con que se propagación de una onda a través de una cuerda sometida ala tensión F, como muestra la figura. Para ello considere
Ejercicios de Ondas Mecánicas y Ondas Electromagnéticas. 1.- Determine la velocidad con que se propagación de una onda a través de una cuerda sometida ala tensión F, como muestra la figura. Para ello considere
ESTRUCTURA DE LA MATERIA
 ESTRUCTURA DE LA MATERIA 1. Naturaleza de la materia (el átomo). 2. Modelos atómicos clásicos. 3. Modelo mecánico cuántico. 4. Mecánica ondulatoria de Schrödinger. 5. Números cuánticos. 6. Orbitales atómicos.
ESTRUCTURA DE LA MATERIA 1. Naturaleza de la materia (el átomo). 2. Modelos atómicos clásicos. 3. Modelo mecánico cuántico. 4. Mecánica ondulatoria de Schrödinger. 5. Números cuánticos. 6. Orbitales atómicos.
Espectroscopía Clase integradora
 Espectroscopía Clase integradora Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar
Espectroscopía Clase integradora Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar
C. Trallero-Giner CINVESTAV-DF (2010) IV. - Dispersión Raman. Interpretación macroscópica Dinámica de la luz dispersada Sección eficaz
 Dispersión Raman en Sólidos C. Trallero-Giner CINVESTAV-DF (2010) IV. - Dispersión Raman. Interpretación macroscópica Dinámica de la luz dispersada Sección eficaz Reglas de selección Dinámica de la luz
Dispersión Raman en Sólidos C. Trallero-Giner CINVESTAV-DF (2010) IV. - Dispersión Raman. Interpretación macroscópica Dinámica de la luz dispersada Sección eficaz Reglas de selección Dinámica de la luz
Espectroscopía de Absorción Molecular
 Espectroscopía de Absorción Molecular La espectroscopía consiste en el estudio cualitativo y cuantitativo de la estructura de los átomos o moléculas o de distintos procesos físicos y químicos mediante
Espectroscopía de Absorción Molecular La espectroscopía consiste en el estudio cualitativo y cuantitativo de la estructura de los átomos o moléculas o de distintos procesos físicos y químicos mediante
ANÁLISIS INSTRUMENTAL_UII_PARTE DOS. Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½
 RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
Espectroscopía atómica
 C A P Í T U L O 6 Espectroscopía atómica 6.. ENUNCIADOS Y SOLUCIONES DE LOS PROBLEMAS PROBLEMAS 6. Demuestre la regla de selección angular del átomo hidrogenoide m = 0, ±. Para m m 2π 0 e im Φ e imφ dφ
C A P Í T U L O 6 Espectroscopía atómica 6.. ENUNCIADOS Y SOLUCIONES DE LOS PROBLEMAS PROBLEMAS 6. Demuestre la regla de selección angular del átomo hidrogenoide m = 0, ±. Para m m 2π 0 e im Φ e imφ dφ
ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS
 ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS PRESENTADO POR: ADRIANA LISSETH LUQUE DIAZ JORGE ENRIQUE JURADO TASCO MARCO ANTONIO HUERTA ORTIZ PABLO LABRA VÁZQUEZ MAESTRÍA EN CIENCIAS QUÍMICAS
ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS PRESENTADO POR: ADRIANA LISSETH LUQUE DIAZ JORGE ENRIQUE JURADO TASCO MARCO ANTONIO HUERTA ORTIZ PABLO LABRA VÁZQUEZ MAESTRÍA EN CIENCIAS QUÍMICAS
Experimento 12 LÍNEAS ESPECTRALES. Objetivos. Teoría. Postulados de Bohr. El átomo de hidrógeno, H
 Experimento 12 LÍNEAS ESPECTRALES Objetivos 1. Describir el modelo del átomo de Bohr 2. Observar el espectro del H mediante un espectrómetro de rejilla 3. Medir los largos de onda de las líneas de la serie
Experimento 12 LÍNEAS ESPECTRALES Objetivos 1. Describir el modelo del átomo de Bohr 2. Observar el espectro del H mediante un espectrómetro de rejilla 3. Medir los largos de onda de las líneas de la serie
Movimiento vibracional
 ESPECTROSCOPÍA Movimiento vibracional El oscilador armónico como modelo de la vibración molecular Los sistemas que vibran a nivel molecular incluyen las vibraciones internas de una molécula y las vibraciones
ESPECTROSCOPÍA Movimiento vibracional El oscilador armónico como modelo de la vibración molecular Los sistemas que vibran a nivel molecular incluyen las vibraciones internas de una molécula y las vibraciones
Radiación térmica y el postulado de Planck
 Contenido Radiación térmica y el postulado de Planck 17 1-1 1-2 1-3 1.4 1.5 1-6 1-7 Introducción 19 Radiación térmica 19 Teoría clásica de la cavidad radiante 24 Teoría de Planck de 1a cavidad radiante
Contenido Radiación térmica y el postulado de Planck 17 1-1 1-2 1-3 1.4 1.5 1-6 1-7 Introducción 19 Radiación térmica 19 Teoría clásica de la cavidad radiante 24 Teoría de Planck de 1a cavidad radiante
Bloque I Origen y evolución de los componentes del Universo
 Bloque I Origen y evolución de los componentes del Universo CRITERIOS DE EVALUACIÓN 1. Analizar cronológicamente los modelos atómicos hasta llegar al modelo actual discutiendo sus limitaciones y la necesitad
Bloque I Origen y evolución de los componentes del Universo CRITERIOS DE EVALUACIÓN 1. Analizar cronológicamente los modelos atómicos hasta llegar al modelo actual discutiendo sus limitaciones y la necesitad
QUÍMICA I. TEMA 2: Estructura atómica. Tecnólogo Minero. E s q u e m a d e l a C l a s e
 QUÍMICA I TEMA 2: Estructura atómica Tecnólogo Minero E s q u e m a d e l a C l a s e Tema 2: Estructura atómica El átomo. Partículas atómicas. Número atómico, número másico. Isótopos. Estructura electrónica.
QUÍMICA I TEMA 2: Estructura atómica Tecnólogo Minero E s q u e m a d e l a C l a s e Tema 2: Estructura atómica El átomo. Partículas atómicas. Número atómico, número másico. Isótopos. Estructura electrónica.
EXTRUCTURA ATOMICA ACTUAL
 ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
Desarrollo multipolar del potencial.
 c Rafael R. Boix y Francisco Medina Desarrollo multipolar del potencial. Consideremos un cuerpo cargado que ocupa una región volumétrica. Sea ρ(r ) la densidad volumétrica de carga del cuerpo cargado.
c Rafael R. Boix y Francisco Medina Desarrollo multipolar del potencial. Consideremos un cuerpo cargado que ocupa una región volumétrica. Sea ρ(r ) la densidad volumétrica de carga del cuerpo cargado.
FÍSICA CUÁNTICA 1. Antecedentes y crisis. 2. Modelo atómico de Bohr. 3. Principios de la mecánica cuántica.
 FÍSICA CUÁNTICA 1. Antecedentes y crisis. 2. Modelo atómico de Bohr. 3. Principios de la mecánica cuántica. Física 2º bachillerato Física cuántica 1 0. CONOCIMIENTOS PREVIOS Los conocimientos previos que
FÍSICA CUÁNTICA 1. Antecedentes y crisis. 2. Modelo atómico de Bohr. 3. Principios de la mecánica cuántica. Física 2º bachillerato Física cuántica 1 0. CONOCIMIENTOS PREVIOS Los conocimientos previos que
U N I V E R S I D A D N A C I O N A L D E L S U R 1/4
 U N I V E R S I D A D N A C I O N A L D E L S U R 1/4 DEPARTAMENTO DE: FISICA PROGRAMA DE: MECANICA CUANTICA II Carreras: Licenciatura en Física CODIGO: 3282 HORAS DE CLASE TEORICAS PRACTICAS Por semana
U N I V E R S I D A D N A C I O N A L D E L S U R 1/4 DEPARTAMENTO DE: FISICA PROGRAMA DE: MECANICA CUANTICA II Carreras: Licenciatura en Física CODIGO: 3282 HORAS DE CLASE TEORICAS PRACTICAS Por semana
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León.
 Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Universidad Nacional Autónoma de Honduras Facultad de Ciencias Escuela de Física Practica de FS-321 Espectroscopia
 Universidad Nacional Autónoma de Honduras Facultad de Ciencias Escuela de Física Practica de FS-321 Espectroscopia Elaborada por: Mario Coto y Luis Alcerro I. Objetivos 1. Calibrar correctamente un espectroscopio
Universidad Nacional Autónoma de Honduras Facultad de Ciencias Escuela de Física Practica de FS-321 Espectroscopia Elaborada por: Mario Coto y Luis Alcerro I. Objetivos 1. Calibrar correctamente un espectroscopio
2.2Evolución del modelo atómico:
 Tema 2.1.- El átomo. 2.2Evolución del modelo atómico: 2.2.- Modelo mecánico cuántico ondulatorio 2.2.1.- Números cuánticos 2.3.- Configuración electrónica 2.3.1.- normal, su desarrollo y mención de: spin.
Tema 2.1.- El átomo. 2.2Evolución del modelo atómico: 2.2.- Modelo mecánico cuántico ondulatorio 2.2.1.- Números cuánticos 2.3.- Configuración electrónica 2.3.1.- normal, su desarrollo y mención de: spin.
Tema 2: Enlace y propiedades de los materiales
 En la mayoría de moléculas, los enlaces entre los átomos que las constituyen no es mediante la interacción coulombiana que hemos analizado en el caso del enlace iónico. Se necesita tener en cuenta el llamado
En la mayoría de moléculas, los enlaces entre los átomos que las constituyen no es mediante la interacción coulombiana que hemos analizado en el caso del enlace iónico. Se necesita tener en cuenta el llamado
Piezoelectricidad. CONCEPTOS NECESARIOS PARA LA PRÁCTICA: - Materiales piezoeléctricos - Circuito resonante RLC
 Piezoelectricidad OBJETIVOS: - Observar y analizar la resonancia electromecánica de un cristal piezoeléctrico - Estudiar el modelo eléctrico equivalente, determinado a partir de las frecuencias de resonancia
Piezoelectricidad OBJETIVOS: - Observar y analizar la resonancia electromecánica de un cristal piezoeléctrico - Estudiar el modelo eléctrico equivalente, determinado a partir de las frecuencias de resonancia
Para ser considerada una función aceptable, la función de onda debe ser:
 Cualquier estado de un sistema dinámico de N partículas puede ser descrito por la llamada función de onda de las 3N coordenadas espaciales y del tiempo: (1) Para ser considerada una función aceptable,
Cualquier estado de un sistema dinámico de N partículas puede ser descrito por la llamada función de onda de las 3N coordenadas espaciales y del tiempo: (1) Para ser considerada una función aceptable,
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS FUNDAMENTOS ESPECTROSCOPICOS
 UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS FUNDAMENTOS ESPECTROSCOPICOS Alexis Lema Jueves 10-12 ESPECTROSCOPIA UV-VIS. COMBINACIÓN LINEAL DE ORBITALES ATOMICOS (CLOA). ORBITALES ATOMICOS
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS FUNDAMENTOS ESPECTROSCOPICOS Alexis Lema Jueves 10-12 ESPECTROSCOPIA UV-VIS. COMBINACIÓN LINEAL DE ORBITALES ATOMICOS (CLOA). ORBITALES ATOMICOS
GUIA TEÓRICA NÚMEROS CUÁNTICOS
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSE DE SUCRE VICE RECTORADO PUERTO ORDAZ DEPARTAMENTO DE ESTUDIOS GENERALES SECCIÓN DE QUÍMICA Asignatura: QUÍMICA I GUIA TEÓRICA NÚMEROS CUÁNTICOS
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSE DE SUCRE VICE RECTORADO PUERTO ORDAZ DEPARTAMENTO DE ESTUDIOS GENERALES SECCIÓN DE QUÍMICA Asignatura: QUÍMICA I GUIA TEÓRICA NÚMEROS CUÁNTICOS
Estructura Fina. (Multiplicidad) de las líneas atómicas (serie Balmer, por ejemplo). Exp λ 6563 Å Δλ =5.4 Å. predicción
 Capítulo 8 Espín electrónico Estructura Fina. (Multiplicidad) de las líneas atómicas (serie almer, por ejemplo). predicción Exp. 3 λ 6563 Å Δλ =5.4 Å Efecto Zeeman (896). En un campo magnético el estado
Capítulo 8 Espín electrónico Estructura Fina. (Multiplicidad) de las líneas atómicas (serie almer, por ejemplo). predicción Exp. 3 λ 6563 Å Δλ =5.4 Å Efecto Zeeman (896). En un campo magnético el estado
INDICE. 1. Introducción a los Sistemas de Comunicaciones y sus
 INDICE 1. Introducción a los Sistemas de Comunicaciones y sus 15 Limitaciones 1.1. Objetivos 15 1.2. Cuestionario de autoevaluación 15 1.3. Componentes básicos de un sistema de comunicaciones 16 1.4. Varios
INDICE 1. Introducción a los Sistemas de Comunicaciones y sus 15 Limitaciones 1.1. Objetivos 15 1.2. Cuestionario de autoevaluación 15 1.3. Componentes básicos de un sistema de comunicaciones 16 1.4. Varios
Cap. 32: Ecuaciones de Maxwell, Magnetismo en la Materia
 Cap. 32: cuaciones de Maxwell, Magnetismo en la Materia n el caso eléctrico, la estructura básica es una carga aislada. Dos cargas de igual magnitud, pero signos opuestos, separadas por una distancia d,
Cap. 32: cuaciones de Maxwell, Magnetismo en la Materia n el caso eléctrico, la estructura básica es una carga aislada. Dos cargas de igual magnitud, pero signos opuestos, separadas por una distancia d,
Transferencia de Calor por Radiación
 INSTITUTO TECNOLÓGICO de Durango Transferencia de Calor por Radiación Dr. Carlos Francisco Cruz Fierro Revisión 1 67004.97 12-jun-12 1 INTRODUCCIÓN A LA RADIACIÓN ELECTROMAGNÉTICA 2 Dualidad de la Luz
INSTITUTO TECNOLÓGICO de Durango Transferencia de Calor por Radiación Dr. Carlos Francisco Cruz Fierro Revisión 1 67004.97 12-jun-12 1 INTRODUCCIÓN A LA RADIACIÓN ELECTROMAGNÉTICA 2 Dualidad de la Luz
1.1 DEFINICIÓN CLÁSICA DEL MOMENTO ANGU- LAR
 Chapter MOMENTO ANGULAR La teoría del momento angular en mecánica cuántica es de gran importancia tanto por el número como por la variedad de sus consecuencias. A partir de la espectroscopía rotacional,
Chapter MOMENTO ANGULAR La teoría del momento angular en mecánica cuántica es de gran importancia tanto por el número como por la variedad de sus consecuencias. A partir de la espectroscopía rotacional,
Cálculo de campos eléctricos por medio del principio de superposición.
 Cálculo de campos eléctricos por medio del principio de superposición. En la clase anterior hemos introducido varios conceptos: Carga. Interacción entre cargas (Ley de Coulomb). Campo campo eléctrico.
Cálculo de campos eléctricos por medio del principio de superposición. En la clase anterior hemos introducido varios conceptos: Carga. Interacción entre cargas (Ley de Coulomb). Campo campo eléctrico.
LIGHT SCATTERING MEASUREMENTS FROM SMALL DIELECTRIC PARTICLES
 LIGHT SCATTERING MEASUREMENTS FROM SMALL DIELECTRIC PARTICLES M.Sc. Abner Velazco Dr. Abel Gutarra abnervelazco@yahoo.com Laboratorio de Materiales Nanoestructurados Facultad de ciencias Universidad Nacional
LIGHT SCATTERING MEASUREMENTS FROM SMALL DIELECTRIC PARTICLES M.Sc. Abner Velazco Dr. Abel Gutarra abnervelazco@yahoo.com Laboratorio de Materiales Nanoestructurados Facultad de ciencias Universidad Nacional
1- Cuál es el origen del momento magnético permanente de los átomos que lo poseen?
 ASIGNATURA FISICA II AÑO 2012 GUIA NRO. 11 MAGNETISMO EN MEDIOS MATERIALES Bibliografía Obligatoria (mínima) Capítulo 30 Física de Serway Tomo II Apunte de cátedra: capítulo XI PREGUNTAS SOBRE LA TEORIA
ASIGNATURA FISICA II AÑO 2012 GUIA NRO. 11 MAGNETISMO EN MEDIOS MATERIALES Bibliografía Obligatoria (mínima) Capítulo 30 Física de Serway Tomo II Apunte de cátedra: capítulo XI PREGUNTAS SOBRE LA TEORIA
Capítulo 1. Antecedentes de la Química Cuántica y primeras Teorías Atómicas
 Capítulo 1. Antecedentes de la Química Cuántica y primeras Teorías Atómicas Objetivos: Recordar y actualizar los conocimientos sobre las características de electrones, protones y neutrones Describir la
Capítulo 1. Antecedentes de la Química Cuántica y primeras Teorías Atómicas Objetivos: Recordar y actualizar los conocimientos sobre las características de electrones, protones y neutrones Describir la
Hoja de Problemas 5. Física Atómica.
 Hoja de Problemas 5. Física Atómica. Fundamentos de Física III. Grado en Física. Curso 25/26. Grupo 56. UAM. 3-3-26 Problema En 896 el astrónomo americano Edward Charles Pickering observó unas misteriosas
Hoja de Problemas 5. Física Atómica. Fundamentos de Física III. Grado en Física. Curso 25/26. Grupo 56. UAM. 3-3-26 Problema En 896 el astrónomo americano Edward Charles Pickering observó unas misteriosas
Tema 1: Simetría y teoría de grupos.
 Ejemplos y aplicaciones de la simetría: QUIRALIDAD. La quiralidad no es solo un concepto ligado a la química orgánica donde se asocia a la presencia del carbono asimétrico: QUIRALIDAD. El experimento En
Ejemplos y aplicaciones de la simetría: QUIRALIDAD. La quiralidad no es solo un concepto ligado a la química orgánica donde se asocia a la presencia del carbono asimétrico: QUIRALIDAD. El experimento En
ESPECTROSCOPíA INFRARROJA
 ESPECTROSCOPíA INFRARROJA Química Orgánica 1 Facultad de Farmacia y Bioquímica UBA 2016 Autor: Dra. Isabel Perillo 1 Espectro electromagnético Unidades de l usadas: para UV-visible: nm (mm): 10-9 m para
ESPECTROSCOPíA INFRARROJA Química Orgánica 1 Facultad de Farmacia y Bioquímica UBA 2016 Autor: Dra. Isabel Perillo 1 Espectro electromagnético Unidades de l usadas: para UV-visible: nm (mm): 10-9 m para
ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR
 ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR La Espectroscopía de Resonancia Magnética Nuclear (RMN) es la herramienta de determinación estructural más potente del químico orgánico. Mediante el RMN podemos
ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR La Espectroscopía de Resonancia Magnética Nuclear (RMN) es la herramienta de determinación estructural más potente del químico orgánico. Mediante el RMN podemos
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica
 Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Curso 2015-2016 Problema 1 La línea principal del espectro
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Curso 2015-2016 Problema 1 La línea principal del espectro
ESPECTROSCOPIA DE FLUORESCENCIA, FOSFORESCENCIA Y QUIMIOLUMINISCENCIA MOLECULAR Q.F. ALEX SILVA ARAUJO
 FOSFORESCENCIA Y QUIMIOLUMINISCENCIA Q.F. ALEX SILVA ARAUJO GENERALIDADES Aquí se considerarán tres tipos de métodos ópticos relacionados entre sí: fluorescencia, fosforescencia y quimioluminiscencia.
FOSFORESCENCIA Y QUIMIOLUMINISCENCIA Q.F. ALEX SILVA ARAUJO GENERALIDADES Aquí se considerarán tres tipos de métodos ópticos relacionados entre sí: fluorescencia, fosforescencia y quimioluminiscencia.
JOEL ROCHA BAROCIO CIÉNEGA DE FLORES N.L.
 JOEL ROCHA BAROCIO CIÉNEGA DE FLORES N.L. Alumno: Alan Francisco Hernández Cisneros Grupo: 303 P.S.P. Lic. Miriam de la Rosa Díaz Carrera: Técnico-Bachiller en Informática QUÉ ES LA FÍSICA? Es una ciencia
JOEL ROCHA BAROCIO CIÉNEGA DE FLORES N.L. Alumno: Alan Francisco Hernández Cisneros Grupo: 303 P.S.P. Lic. Miriam de la Rosa Díaz Carrera: Técnico-Bachiller en Informática QUÉ ES LA FÍSICA? Es una ciencia
Tema 3 El Átomo. Modelos Atómicos y Configuraciones Electrónicas
 Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 3 Rev 01 El Átomo. Modelos Atómicos y Configuraciones Electrónicas
Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 3 Rev 01 El Átomo. Modelos Atómicos y Configuraciones Electrónicas
Tema 1: Electrones, energía, átomos y sólidos
 Tema 1: Electrones, energía, átomos y sólidos K. Kano: cap. 1 y cap. El modelo de Bohr Mecánica cuántica. Dualidad onda corpúsculo. Ecuación de Schrödinger en un átomo hidrogenoide. Números cuánticos Formación
Tema 1: Electrones, energía, átomos y sólidos K. Kano: cap. 1 y cap. El modelo de Bohr Mecánica cuántica. Dualidad onda corpúsculo. Ecuación de Schrödinger en un átomo hidrogenoide. Números cuánticos Formación
Efectos del Disolvente modelos implícitos. Esquer Rodríguez Raymundo Química Computacional
 Efectos del Disolvente modelos implícitos Esquer Rodríguez Raymundo Química Computacional 1 S Por qué es Importante? La mayor parte de la química y bioquímica tiene lugar en disolución, y el disolvente
Efectos del Disolvente modelos implícitos Esquer Rodríguez Raymundo Química Computacional 1 S Por qué es Importante? La mayor parte de la química y bioquímica tiene lugar en disolución, y el disolvente
FÍSICA 4 PRIMER CUATRIMESTRE DE 2015 GUÍA 9: POTENCIALES EN 2-D Y 3-D, MOMENTO ANGULAR, ÁTOMO DE HIDRÓGENO, ESPÍN
 FÍSICA 4 PRIMER CUATRIMESTRE DE 2015 GUÍA 9: POTENCIALES EN 2-D Y 3-D, MOMENTO ANGULAR, ÁTOMO DE HIDRÓGENO, ESPÍN 1. Considere el siguiente potencial (pozo infinito): { 0 x a; y b y z c V(x)= sino Escribiendo
FÍSICA 4 PRIMER CUATRIMESTRE DE 2015 GUÍA 9: POTENCIALES EN 2-D Y 3-D, MOMENTO ANGULAR, ÁTOMO DE HIDRÓGENO, ESPÍN 1. Considere el siguiente potencial (pozo infinito): { 0 x a; y b y z c V(x)= sino Escribiendo
Con posterioridad el físico alemán Sommerfeld introdujo en el modelo la posibilidad de órbitas elípticas. Köningsberg, Munich, 1951
 4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
Práctica Nº 4 DIODOS Y APLICACIONES
 Práctica Nº 4 DIODOS Y APLICACIONES 1.- INTRODUCCION El objetivo Los elementos que conforman un circuito se pueden caracterizar por ser o no lineales, según como sea la relación entre voltaje y corriente
Práctica Nº 4 DIODOS Y APLICACIONES 1.- INTRODUCCION El objetivo Los elementos que conforman un circuito se pueden caracterizar por ser o no lineales, según como sea la relación entre voltaje y corriente
La ecuación de Boltzmann
 La ecuación de Boltzmann El movimiento de un portador en un metal o semiconductor está condicionado por un lado por presencia de campos externos (eléctricos, magnéticos), gradientes de temperatura y por
La ecuación de Boltzmann El movimiento de un portador en un metal o semiconductor está condicionado por un lado por presencia de campos externos (eléctricos, magnéticos), gradientes de temperatura y por
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I 2012
 El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I 2012 Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I 2012 Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
Unidad 1 Estructura atómica de la materia. Teoría cuántica
 Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Los pasos que se dan son:
 Hasta ahora hemos admitido que podemos trabajar con la red de cores de nuestro sólido usando una aproximación clásica lo que nos ha permitido determinar los «modos normales de vibración» en el sentido
Hasta ahora hemos admitido que podemos trabajar con la red de cores de nuestro sólido usando una aproximación clásica lo que nos ha permitido determinar los «modos normales de vibración» en el sentido
SELECCION DE PREGUNTAS REPRESENTATIVAS SOBRE TEMAS DEL MODULO DE
 SELECCION DE PREGUNTAS REPRESENTATIVAS SOBRE TEMAS DEL MODULO DE ESTRUCTURA Y PROPIEDADES MOLECULARES Temas de Mecánica Cuántica y Estructura atómica 1) Cuál es el operador asociado al observable energía,
SELECCION DE PREGUNTAS REPRESENTATIVAS SOBRE TEMAS DEL MODULO DE ESTRUCTURA Y PROPIEDADES MOLECULARES Temas de Mecánica Cuántica y Estructura atómica 1) Cuál es el operador asociado al observable energía,
Moléculas: partícula neutra más pequeña de una sustancia dada que posee sus propiedades químicas y puede existir independientemente
 Especies químicas de interés formadas por átomos: Moléculas: partícula neutra más pequeña de una sustancia dada que posee sus propiedades químicas y puede existir independientemente Iones: Especies cargada
Especies químicas de interés formadas por átomos: Moléculas: partícula neutra más pequeña de una sustancia dada que posee sus propiedades químicas y puede existir independientemente Iones: Especies cargada
El campo magnético en los medios materiales. Tema 10 Electromagnetismo Grupo C
 El campo magnético en los medios materiales Tema 10 Electromagnetismo Grupo C El campo magnético y la materia El átomo como un dipolo magnético Imanación y corrientes de imanación Teorema de Àmpere para
El campo magnético en los medios materiales Tema 10 Electromagnetismo Grupo C El campo magnético y la materia El átomo como un dipolo magnético Imanación y corrientes de imanación Teorema de Àmpere para
Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos. Teoría atómica II: Números cuánticos y configuración electrónica
 TEORÍA ATÓMICA Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos Teoría atómica II: Números cuánticos y configuración electrónica Aprendizajes esperados Diferenciar los distintos
TEORÍA ATÓMICA Teoría atómica I: Modelos atómicos, estructura atómica y tipos de átomos Teoría atómica II: Números cuánticos y configuración electrónica Aprendizajes esperados Diferenciar los distintos
Medios materiales y desarrollo multipolar.
 Física Teórica 1 Guia 3 - Medios materiales y multipolos 1 cuat. 2014 Medios materiales y desarrollo multipolar. Medios materiales. 1. Una esfera de radio a está uniformemente magnetizada con densidad
Física Teórica 1 Guia 3 - Medios materiales y multipolos 1 cuat. 2014 Medios materiales y desarrollo multipolar. Medios materiales. 1. Una esfera de radio a está uniformemente magnetizada con densidad
PLANEACIÓN DEL CONTENIDO DE CURSO
 PÁGINA: 1 de 5 FACULTAD DE CIENCIAS BÁSICAS PROGRAMA DE QUÍMICA PLANEACIÓN DEL CONTENIDO DE CURSO 1. IDENTIFICACIÓN DEL CURSO NOMBRE : QUÍMICA CUÁNTICA CÓDIGO : 23415 SEMESTRE : SÉPTIMO NUMERO DE CRÉDITOS
PÁGINA: 1 de 5 FACULTAD DE CIENCIAS BÁSICAS PROGRAMA DE QUÍMICA PLANEACIÓN DEL CONTENIDO DE CURSO 1. IDENTIFICACIÓN DEL CURSO NOMBRE : QUÍMICA CUÁNTICA CÓDIGO : 23415 SEMESTRE : SÉPTIMO NUMERO DE CRÉDITOS
Tema 3.-Espectroscopía de biomoléculas
 Tema 3.-Espectroscopía de biomoléculas Tema 3.-Espectroscopía de biomoléculas 3.1.-El espectro electromagnético 3.2.-Espectros de absorción y de emisión (espontánea y estimulada) 3.2.1.-Momento dipolar
Tema 3.-Espectroscopía de biomoléculas Tema 3.-Espectroscopía de biomoléculas 3.1.-El espectro electromagnético 3.2.-Espectros de absorción y de emisión (espontánea y estimulada) 3.2.1.-Momento dipolar
ESTRUCTURA DE LA MATERIA. Nombre
 ESTRUCTURA DE LA MATERIA Examen primer parcial gen. 2013 Dr. Andoni Garritz Nombre Responde aquí estos cuatro problemas (40%) 1. Según Ira Levine, puede decirse que la fisicoquímica estudia cuatro grandes
ESTRUCTURA DE LA MATERIA Examen primer parcial gen. 2013 Dr. Andoni Garritz Nombre Responde aquí estos cuatro problemas (40%) 1. Según Ira Levine, puede decirse que la fisicoquímica estudia cuatro grandes
Modelo Atómico. Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran embebidos los electrones con carga (-)
 Modelo Atómico 1 Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran embebidos los electrones con carga () Electrón Conceptos:» Neutralidad eléctrica» Carga elemental del
Modelo Atómico 1 Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran embebidos los electrones con carga () Electrón Conceptos:» Neutralidad eléctrica» Carga elemental del
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS FUNDAMENTOS DE LA ESPECTROSCOPIA
 Integrantes: Ipiales Gabriela Química de Alimentos Olmos Wendy Química Farmacéutica Día: Miércoles 9-11 Fecha: 05/07/2011 DEFINICIÓN DE ORBITALES ATÓMICOS Un orbital atómico representa una región del espacio
Integrantes: Ipiales Gabriela Química de Alimentos Olmos Wendy Química Farmacéutica Día: Miércoles 9-11 Fecha: 05/07/2011 DEFINICIÓN DE ORBITALES ATÓMICOS Un orbital atómico representa una región del espacio
EXPERIENCIAS CON MICROONDAS
 EXPERIENCIAS CON MICROONDAS OBJETIVOS 1)Generales 1 1) Comprender en la práctica, algunas de las propiedades generales de las ondas electromagnéticas. 1 2) Estudiar las propiedades y fenómenos relacionados
EXPERIENCIAS CON MICROONDAS OBJETIVOS 1)Generales 1 1) Comprender en la práctica, algunas de las propiedades generales de las ondas electromagnéticas. 1 2) Estudiar las propiedades y fenómenos relacionados
Incidencia de Anestesia General en Operación Cesárea: Registro de Tres Años. Castillo Alvarado, Frencisco Miguel. CAPÍTULO III
 CAPÍTULO III ESTADÍSTICA DE LOS PORTADORES DE CARGA DEL SEMICONDUCTOR 1. Introducción. Cada material suele presentar varias bandas, tanto de conducción (BC) como de valencia (BV), pero las más importantes
CAPÍTULO III ESTADÍSTICA DE LOS PORTADORES DE CARGA DEL SEMICONDUCTOR 1. Introducción. Cada material suele presentar varias bandas, tanto de conducción (BC) como de valencia (BV), pero las más importantes
Programa y planificación de la Física III Ingeniería Industrial Asignatura: FÍSICA III
 2do semestre del curso 2011-2012 Programa y planificación de la Física III Ingeniería Industrial Asignatura: FÍSICA III Objeto de estudio: El cuadro mecánico cuántico Objetivos generales Educativos Contribuir
2do semestre del curso 2011-2012 Programa y planificación de la Física III Ingeniería Industrial Asignatura: FÍSICA III Objeto de estudio: El cuadro mecánico cuántico Objetivos generales Educativos Contribuir
UNIVERSIDAD SIMÓN BOLÍVAR Vicerrectorado Académico
 UNIVERSIDAD SIMÓN BOLÍVAR Vicerrectorado Académico 1.Departamento: FÍSICA 2. Asignatura: FISICA MODERNA I 3. Código de la asignatura: FS-3411 No. de unidades-crédito: 4 No. de horas semanales: Teoría 4
UNIVERSIDAD SIMÓN BOLÍVAR Vicerrectorado Académico 1.Departamento: FÍSICA 2. Asignatura: FISICA MODERNA I 3. Código de la asignatura: FS-3411 No. de unidades-crédito: 4 No. de horas semanales: Teoría 4
EL ESPECTRO ELECTROMAGNÉTICO
 FACULTAD DE CIENCIAS QUÍMICAS Espectrometría Objeto de Estudio Nº 1 LECTURA N 2 EL ESPECTRO ELECTROMAGNÉTICO Bibliografía: http://almaak.tripod.com/temas/espectro.htm Facultad de Ciencias Químicas F.C.Q.
FACULTAD DE CIENCIAS QUÍMICAS Espectrometría Objeto de Estudio Nº 1 LECTURA N 2 EL ESPECTRO ELECTROMAGNÉTICO Bibliografía: http://almaak.tripod.com/temas/espectro.htm Facultad de Ciencias Químicas F.C.Q.
Tema 3.-Espectroscopía de biomoléculas
 Tema 3.Espectroscopía de biomoléculas Tema 3.Espectroscopía de biomoléculas 3..El espectro electromagnético 3.2.Espectros de absorción y de emisión (espontánea y estimulada) 3.2..Momento dipolar de transición:
Tema 3.Espectroscopía de biomoléculas Tema 3.Espectroscopía de biomoléculas 3..El espectro electromagnético 3.2.Espectros de absorción y de emisión (espontánea y estimulada) 3.2..Momento dipolar de transición:
Ecuación de la onda estacionaria Para referirse a la amplitud de la onda electrónica, Schrödinger introdujo el empleo de la letra Ψ.
 Modelo Moderno Bases del modelo Ondas electrónicas La luz (ondas electromagnéticas) tiene no sólo un carácter ondulatorio sino que también corpuscular (ya sabido hacia 1920). Se aplica la ecuación de Plank
Modelo Moderno Bases del modelo Ondas electrónicas La luz (ondas electromagnéticas) tiene no sólo un carácter ondulatorio sino que también corpuscular (ya sabido hacia 1920). Se aplica la ecuación de Plank
Tema 6: Espectroscopia electrónica
 1.- Introducción -El color es uno de los aspectos más llamativos de los compuestos de coordinación. -Desde antiguo se conocen compuestos de coordinación que se usan como colorantes: Azul de prusia Fe 4
1.- Introducción -El color es uno de los aspectos más llamativos de los compuestos de coordinación. -Desde antiguo se conocen compuestos de coordinación que se usan como colorantes: Azul de prusia Fe 4
DIVISIÓN DE CIENCIAS BÁSICAS DEPARTAMENTO DE FÍSICA PROGRAMA DE ASIGNATURA
 CENTRO UNIVERSITARIO DE CIENCIAS EXACTAS E INGENIERÍAS DIVISIÓN DE CIENCIAS BÁSICAS DEPARTAMENTO DE FÍSICA PROGRAMA DE ASIGNATURA NOMBRE DE LA MATERIA FÍSICA MODERNA CLAVE DE MATERIA FS 301 DEPARTAMENTO
CENTRO UNIVERSITARIO DE CIENCIAS EXACTAS E INGENIERÍAS DIVISIÓN DE CIENCIAS BÁSICAS DEPARTAMENTO DE FÍSICA PROGRAMA DE ASIGNATURA NOMBRE DE LA MATERIA FÍSICA MODERNA CLAVE DE MATERIA FS 301 DEPARTAMENTO
OBJETIVO FUNDAMENTACIÓN. Medida de la permitividad dieléctrica compleja del agua y del alcohol.
 Laboratorio_Electromagnetismo Medida de la Permitividad Dieléctrica de Líquidos Polares Francisco Camarena Femenía Miguel Ángel Ballesteros Velasco OBJETIVO Medida de la permitividad dieléctrica compleja
Laboratorio_Electromagnetismo Medida de la Permitividad Dieléctrica de Líquidos Polares Francisco Camarena Femenía Miguel Ángel Ballesteros Velasco OBJETIVO Medida de la permitividad dieléctrica compleja
Teoría de Orbitales Moleculares (OM)
 Teoría de Orbitales Moleculares (OM) El caso de CH4 Ricardo Agusto Valencia Mora. María Magdalena Vázquez Alvarado. Osmaly Villedas Hernández. José Luis Zavala Salgado. Friedrich Hund 1896-1997 Formula
Teoría de Orbitales Moleculares (OM) El caso de CH4 Ricardo Agusto Valencia Mora. María Magdalena Vázquez Alvarado. Osmaly Villedas Hernández. José Luis Zavala Salgado. Friedrich Hund 1896-1997 Formula
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I
 El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
Comportamiento Electrónico de los Materiales. Tema 2. Electrones en Sólidos. Teoría de Bandas de Energía.
 Comportamiento Electrónico de los Materiales Tema. Electrones en Sólidos. Teoría de Bandas de Energía. .1 Teoría de Bandas de Energía..1.1 Partículas en interacción con objetos múltiples. Molécula de Hidrógeno.
Comportamiento Electrónico de los Materiales Tema. Electrones en Sólidos. Teoría de Bandas de Energía. .1 Teoría de Bandas de Energía..1.1 Partículas en interacción con objetos múltiples. Molécula de Hidrógeno.
EXPERIMENTO 19 OPTICA VII : ACTIVIDAD OPTICA
 Física Experimental III 1 1. Objetivo EXPERIMENTO 19 OPTICA VII : ACTIVIDAD OPTICA Comprender el fenómeno de rotación del eje de polarización de la luz que producen algunas substancias y medir dicho efecto
Física Experimental III 1 1. Objetivo EXPERIMENTO 19 OPTICA VII : ACTIVIDAD OPTICA Comprender el fenómeno de rotación del eje de polarización de la luz que producen algunas substancias y medir dicho efecto
Resonancia Magnética Nuclear
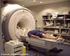 Víctor Moreno de la Cita Jesús J. Fernández Romero 25 de mayo de 2010 1 Base teórica 2 Medicina Química y análisis no destructivo Computación cuántica 3 4 Notación que emplea Kittel: µ = Momento magnético
Víctor Moreno de la Cita Jesús J. Fernández Romero 25 de mayo de 2010 1 Base teórica 2 Medicina Química y análisis no destructivo Computación cuántica 3 4 Notación que emplea Kittel: µ = Momento magnético
GUIA EJERCICIOS PSU TEORIA ATOMICA, NUMEROS CUANTICOS Y CONFIGURACION EDITORIAL SM
 GUIA EJERCICIOS PSU TEORIA ATOMICA, NUMEROS CUANTICOS Y CONFIGURACION EDITORIAL SM 1. Según el modelo mecanocuántico, dónde se pueden encontrar los electrones? A. En una posición definida en un momento
GUIA EJERCICIOS PSU TEORIA ATOMICA, NUMEROS CUANTICOS Y CONFIGURACION EDITORIAL SM 1. Según el modelo mecanocuántico, dónde se pueden encontrar los electrones? A. En una posición definida en un momento
Clase N 1. Modelo Atómico II
 Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico II ICAL ATACAMA Módulo Plan Común Síntesis De La Clase Anterior Modelo atómico Átomo Divisible en Protón Neutrón Electrón Carga: +1 Masa:
Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico II ICAL ATACAMA Módulo Plan Común Síntesis De La Clase Anterior Modelo atómico Átomo Divisible en Protón Neutrón Electrón Carga: +1 Masa:
TEMA 1: Estructura Atómica
 TEMA 1: Estructura Atómica 1. Configuraciones electrónicas. 2. Propiedades periódicas: Energía de activación Afinidad electrónica Electronegatividad Descripción mecánico- cuántica del átomo: Orbitales
TEMA 1: Estructura Atómica 1. Configuraciones electrónicas. 2. Propiedades periódicas: Energía de activación Afinidad electrónica Electronegatividad Descripción mecánico- cuántica del átomo: Orbitales
Física del Estado Sólido I. Tema 2: Enlace y propiedades de los materiales
 Física del Estado Sólido I Tema : Enlace y propiedades de los materiales Tema : Enlace y propiedades de los materiales Introducción Qué interacción es responsable de la cohesión en los cristales? - La
Física del Estado Sólido I Tema : Enlace y propiedades de los materiales Tema : Enlace y propiedades de los materiales Introducción Qué interacción es responsable de la cohesión en los cristales? - La
Física y Química 3º ESO
 1. Física y Química. Ciencias de la medida forman parte de las necesitan Ciencias de la naturaleza medir las propiedades de los cuerpos que se dividen en para lo cual se emplean lo que siempre conlleva
1. Física y Química. Ciencias de la medida forman parte de las necesitan Ciencias de la naturaleza medir las propiedades de los cuerpos que se dividen en para lo cual se emplean lo que siempre conlleva
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO. Lola Castelao
 ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
Gráficas de las partes angulares En la figura presentamos la gráfica de la función s: (1/4π) 1/2
 Gráficas de las partes angulares En la figura presentamos la gráfica de la función s: (1/4π) 1/2 La función s es un círculo porque siempre vale (1/4π) 1/2 independientemente del valor de los ángulos θ
Gráficas de las partes angulares En la figura presentamos la gráfica de la función s: (1/4π) 1/2 La función s es un círculo porque siempre vale (1/4π) 1/2 independientemente del valor de los ángulos θ
ATOMO DE HIDROGENO. o = permitividad al vacío = 8.85 X C 2 N -1 cm -1. = metros. F = Newtons 2. Ó (3)
 ATOMO DE HIDROGENO I. Atomo de hidrógeno A. Descripción del sistema: Dos partículas que interaccionan por atracción de carga eléctrica y culómbica. 1. Ley de coulomb: a. En el sistema cgs en unidades de
ATOMO DE HIDROGENO I. Atomo de hidrógeno A. Descripción del sistema: Dos partículas que interaccionan por atracción de carga eléctrica y culómbica. 1. Ley de coulomb: a. En el sistema cgs en unidades de
Capítulo 1: Estructura atómica y Sistema periódico
 Capítulo 1: Estructura atómica y Sistema periódico ACTIVIDADES DE RECAPITULACIÓN 1. Qué radiación se propaga con mayor velocidad en el vacío, los rayos X o las ondas de radio? Tanto los rayos X como las
Capítulo 1: Estructura atómica y Sistema periódico ACTIVIDADES DE RECAPITULACIÓN 1. Qué radiación se propaga con mayor velocidad en el vacío, los rayos X o las ondas de radio? Tanto los rayos X como las
H. 1/5. Universidad Nacional de La Pampa Facultad de Ingeniería Carrera: Ingeniería Electromecánica. Asignatura: FÍSICA III.
 H. 1/5 Carga Horaria: Objetivos: Teoría Laboratorio Problemas Problemas Proyecto y Tipo/Rutinarios Abiertos Diseño Total 48 18 14 80 Ofrecer un adecuado panorama de formalismos avanzados vinculados con
H. 1/5 Carga Horaria: Objetivos: Teoría Laboratorio Problemas Problemas Proyecto y Tipo/Rutinarios Abiertos Diseño Total 48 18 14 80 Ofrecer un adecuado panorama de formalismos avanzados vinculados con
UNIDAD 1: PRINCIPIOS DE LA QUÍMICA
 UNIDAD 1: PRINCIPIOS DE LA QUÍMICA MODELO ATOMICO DE DALTON RAYOS CATÓDICOS (Thomsom) EL ELECTRÓN MODELO ATÓMICO DE THOMSOM RAYOS CANALES (Goldstein) EL PROTÓN Rutherford MODELO ATÓMICO DE RUTHERFORD Chadwick:
UNIDAD 1: PRINCIPIOS DE LA QUÍMICA MODELO ATOMICO DE DALTON RAYOS CATÓDICOS (Thomsom) EL ELECTRÓN MODELO ATÓMICO DE THOMSOM RAYOS CANALES (Goldstein) EL PROTÓN Rutherford MODELO ATÓMICO DE RUTHERFORD Chadwick:
Principios de estructura de la materia
 Principios de estructura de la materia Equipo 3: Martínez Bourget Diego Martínez Olmedo Esaú Muñoz Gómez Rosa Jenifer Navarro Peñaloza Rubí Posgrado de Ciencias Químicas Luis Vicente Hinestroza Rotor rígido
Principios de estructura de la materia Equipo 3: Martínez Bourget Diego Martínez Olmedo Esaú Muñoz Gómez Rosa Jenifer Navarro Peñaloza Rubí Posgrado de Ciencias Químicas Luis Vicente Hinestroza Rotor rígido
Enlace químico II: geometría molecular e hibridación de orbitales atómicos
 Enlace químico II: geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Teorías de cómo ocurren
Enlace químico II: geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Teorías de cómo ocurren
La espectroscopia de resonanc resonan ia magnética nuclear (RMN) es un fenóme fenóm no
 Resonancia Magnética Nuclear de Sólidos y su aplicación ala caracterización de polímeros Carlos García Aparicio Madrid, 2012 La espectroscopia de resonancia magnética nuclear (RMN) es un fenómeno que ocurre
Resonancia Magnética Nuclear de Sólidos y su aplicación ala caracterización de polímeros Carlos García Aparicio Madrid, 2012 La espectroscopia de resonancia magnética nuclear (RMN) es un fenómeno que ocurre
INTRODUCCION (2) espectroscopía de absorción Espectroscopía de Emisión RMN Espectrometría de Masas espectrometría de fragmentación
 INTRODUCCION (1) Una de las labores más difíciles dentro de la Química Orgánica es la elucidación estructural. En algunos casos es suficiente con algunos datos mínimos. Utilizando algunas propiedades Fisico-Químicas
INTRODUCCION (1) Una de las labores más difíciles dentro de la Química Orgánica es la elucidación estructural. En algunos casos es suficiente con algunos datos mínimos. Utilizando algunas propiedades Fisico-Químicas
CAPÍTULO 3 DISPOSITIVOS ELECTRO-ÓPTICOS
 CAPÍTULO 3 3.1 Sensores optoelectrónicos Una gran ventaja de los dispositivos electro-ópticos es que presentan mayores velocidades de operaciones y menores voltajes ya que la configuración es transversal
CAPÍTULO 3 3.1 Sensores optoelectrónicos Una gran ventaja de los dispositivos electro-ópticos es que presentan mayores velocidades de operaciones y menores voltajes ya que la configuración es transversal
NIVELES DE ENERGÍA EN LOS IONES DE LOS METALES DE TRANSICIÓN
 NIVELES DE ENERGÍA EN LOS IONES DE LOS METALES DE TRANSICIÓN INTRODUCCIÓN CÁLCULO DE LOS TERMINOS ESPECTROSCÓPICOS EN EL ION LIBRE. Acoplamiento de Russell-Saunders 2. Cálculo de los términos espectroscópicos
NIVELES DE ENERGÍA EN LOS IONES DE LOS METALES DE TRANSICIÓN INTRODUCCIÓN CÁLCULO DE LOS TERMINOS ESPECTROSCÓPICOS EN EL ION LIBRE. Acoplamiento de Russell-Saunders 2. Cálculo de los términos espectroscópicos
Efectos de los momentos nucleares y la paridad sobre transiciones nucleares
 Página 1 Las diferencias de momento angular y paridad producen profundos efectos sobre la probabilidad relativa de transiciones nucleares que compiten. Midiendo la probabilidad relativa de varias transiciones
Página 1 Las diferencias de momento angular y paridad producen profundos efectos sobre la probabilidad relativa de transiciones nucleares que compiten. Midiendo la probabilidad relativa de varias transiciones
Histéresis ferromagnética y temperatura de Curie
 Histéresis ferromagnética y temperatura de Curie OBJETIVOS: Observar el comportamiento de histéresis ferromagnética Determinar la temperatura de Curie de la aleación Monel400 Comprender la respuesta en
Histéresis ferromagnética y temperatura de Curie OBJETIVOS: Observar el comportamiento de histéresis ferromagnética Determinar la temperatura de Curie de la aleación Monel400 Comprender la respuesta en
