SISTEMA PAN-EUROPEO DE VERIFICACIÓN DE MEDICAMENTOS EMVO
|
|
|
- Jorge Correa Aguirre
- hace 5 años
- Vistas:
Transcripción
1 SISTEMA PAN-EUROPEO DE VERIFICACIÓN DE MEDICAMENTOS EMVO Jornada Profesional de Farmacia Hospitalaria 8 sept 017, Madrid Sonia Ruiz Morán Vicepresidenta de EMVO
2 ÍNDICE Problema y soluciones Marco regulatorio Trabajos desarrollados por EMVO Estado de avance del NMVS
3 PROBLEMA DE LA FALSIFICACIÓN o Alcance... 50% medicamentos por internet son falsificados Afecta a todo tipo de medicamentos 3
4 PROBLEMA DE LA FALSIFICACIÓN o Sofisticación... Difícil apreciar la diferencia entre envases originales y falsificados Falsificado Auténtico Europa es ahora un mercado de destino: casos notificados in 01, 13 en 013, y 15 en
5 SOLUCIONES A NIVEL EUROPEO o Reforzar la coordinación y cooperación internacionales: Apoyo a la labor de foros internacionales: Consejo de Europa, Europol y ONU o Instrumentos regulatorios: Dispositivos de seguridad en los embalajes - serialización Logo europeo en la venta por internet Normas más estrictas sobre los controles e inspecciones de los productores de APIs; Se refuerzan los requisitos de registro para mayoristas 5
6 DIRECTIVA CONTRA LA FALSIFICACIÓN DE MEDICAMENTOS* o Definición Medicamento falsificado: Presentación falsa de un medicamento en cuanto a: Identidad, Origen e Historial. No comprende: Defectos de calidad involuntarios, ni Infracción de derechos de propiedad intelectual o Dispositivos de seguridad en el embalaje externo: Permitir identificación individual de cada envase y verificación de su autenticidad Permitir verificar que el interior no ha sido manipulado (*) Directiva 011/6/EU que modifica la Directiva 001/83/CE 6
7 REGLAMENTO DELEGADO Objetivos o Características técnicas del Identificador único o Modalidades de Verificación de los dispositivos de seguridad o Establecimiento y Gestión Sistema de Repositorios o Lista de medicamentos exceptuados del ámbito Directiva (Lista Blanca / Lista Negra) o Procedimiento de notificaciones de excepciones por parte de los Estados Miembros (*) Reglamento delegado (UE) 016/161 de la Comisión, de de octubre de 015. Publicado 9//016 7
8 HORIZONTE TEMPORAL DE CUMPLIMIENTO Jul 011 Publicación de la DFM 9 Feb 016 Publicacion del Reglamento Delegado 36 Me. 9 Feb 019 Verificación obligatoria de todos los envases dentro del ambito de aplicación 6/09/017 8
9 CONCEPTOS BÁSICOS DEL SISTEMA Serialización por fabricante Verificación sobre análisis de riesgo por mayoristas Verificación y cancelación en el punto de dispensación Dispositivos de seguridad: Código ( identificador único ) + Dispositivos Anti manipulación Product #: Batch: A1CE3G4I5 Expiry: S/N: 1345AZRQF Gobernanza y gestión por agentes Con supervision de las autoridades competentes Interoperable 9
10 AGENTES INVOLUCRADOS A NIVEL EUROPEO EMVO 6/09/017 10
11 SOBRE EMVO Organización Europea para la Verificación de Medicamentos (EMVO) Asociación belga sin animo de lucro que agentes de la cadena. representa a los Fundada el 13 Febrero 015 Misión: avanzar en la creación del Sistema Europeo de Verificación de Medicamentos(EMVS), para la verificación de medicamentos y la mejora de la seguridad del paciente, conforme a la Directiva de medicamentos falsificados y su Reglamento Delegado. 6/09/017 11
12 ORGANIGRAMA EMVO EMVO Board of Directors President: Hugh Pullen (EFPIA) Vice-President: Sonia Ruiz Morán (PGEU) Treasurer: Richard Freudenberg (EAEPC) Monika Derecque-Pois (GIRP) Adrian van den Hoven (Medicines for Europe) General Management Andreas Walter Commercial & Partner Management Tobias Beer Operations Koen Van Gompel Office Management Marisa Jimenez Sanchez Quality Assurance Stephan Theunissen Fanny Trenteseaux André Geraldes Jannik Jäger (Intern) NN (Legal Counsel) Paul Mills (Consultant) Willem Theunissen (Consultant) 6/09/017 1
13 Interfaz Interf. laboratorio Interf.Distr.Paral. ARQUITECTURA DEL SISTEMA Sistema Laboratorio Nodo Europeo Interfaz Sistema Distribuidor Paralelo Propietario sistema= EMVO Interf.Sist. Nac. Interf.Sist.Blueprint Interfaz Interf.Blueprint. Sistema Nacional específico Sistema nacional basado en standard blueprint Farmacia Distribuidor Interf. Farmacia Interf. Distribución Interfaz Interfaz Interfaz Interfaz Sistema Farmacia Sistema Distribución Sistema Farmacia Sistema Distribución 13
14 GOBERNANZA Y GESTIÓN DEL SISTEMA Gobernanza Consejo EMVO Establecimiento, gestión y operativa del Nodo Europeo Nodo Europeo Nodo Europeo Nodo Europeo Gestión Operación EMVO Proveedor IT Establecimiento estándares para el EMVS Concluir acuerdos con NMVOs/TACs Acuerdos de nivel de servicio Sist. Nacional Nodo Europeo Nodo Europeo Gobernanza Gestión Operación Consejo NMVO NMVO/EMVO Proveedor IT Establecimiento y gestión del Sistema Nacional Concluir acuerdos con EMVO Analisis eventos excepcionales a nivel nacional 14
15 AVANCE IMPLANTACIÓN TÉCNICA A NIVEL EUROPEO 0/015 Fundación EMVO 04/015 Finalizado Nodo Europeo 07/015 Conexión Nodo y securpharm 9 Feb 016 Comienzo implantación desde publicación de Actos Delegados 04/013 Comienzo desarrollo nodo europeo Hasta 013 Diseño Sistema 05/015 Marco contractual con los proveedores tecnológicos Construcción Sistema Europeo Implantación Nodo +Sistemas nacionales Q 017 Versión.0 del Nodo Conexión TACs 15
16 AHORA: IMPLANTACIÓN TECNICA NACIONAL o Proyectos de Conexión al Nodo Europeo Conexión NMVS (3) Conexión Laboratorios (500) o Proyectos de Conexión a los Sistemas Nacionales de Verificación Farmacias Distribuidores Servicios de Farmacia Hospitalaria Otros Puntos de Dispensación Sin consideración proyectos internos de laboratorios, distribuidores, oficinas de farmacias, servicios de farmacia y otros 16
17 CONEXIÓN DE LOS LABORATORIOS AL NODO EUROPEO o Portal para los OBP ya operativo o 17 agentes conectados 17
18 CONEXIÓN DE LOS SISTEMAS NACIONALES Requisitos para los Sistemas Nacionales o El Sistema Nacional debe prever el conjunto necesario de casos de uso (full URS 3.0 y URS Lite 3.0) o Interfaz con la plataforma europea de acuerdo a especificaciones EMVO o Cumplimiento con requisitos de seguridad verificados por EMVO o Acuerdo de términos contractuales entre NMVO y EMVO 18
19 SEGUIMIENTO IMPLANTACIÓN NACIONAL 19/09/017 19
20 CALENDARIO DE REFERENCIA PARA NMVOS, FABRICANTES Y USUARIOS FINALES Year 017 Q Q 3 Q Q Q 3 Q MAH On-boarding 1 Connected to HUB (CH) Products serialized + uploaded (PS) 5% 50% 75% 100% For Pilot 5% 50% 75% 100% NMVO Operation Funding secured (Funding) Team implemented (Team) Initial Tasks completed (Tasks) National Pilot Technical Implementation started (TIS) Prerequisites + Pilot defined (PD) First Products verified (FP) Pilot sucessfully completed (PC) National Ramp Up 1 End User Systems connected + live (SY) End Users connected + live (EC) 6/09/017 For Pilot 5% 50% 75% 100% 5% 50% 75% 100% 0
21 ESTADO DE PREPARACIÓN DE LOS PAÍSES Early Adopter Main Stream Late Follower 16 3 Not started /09/
22 CONEXIÓN TITULARES DE COMERCIALIZACIÓN Above Target Below Target Actual Target 50% /09/
23 CONEXIÓN USUARIOS FINALES Above Target 0 6 Below Target /09/
24 OBSERVACIONES o Estado de avance 14 paises han comenzado la fase de implantación Algunos más están avanzando en esta fase si bien el contrato final con el proveedor aún no ha sido finalizado. o A mejorar La conexión de los TACs va muy retrasada. Aproximadamente parece que el 50% de los paises empezarán demasiado tarde la Fase de Implantación. 6/09/017 4
25 DECISIONES CONSEJO ADMINISTRACIÓN EMVO 19/9/017 o Aprobación de la inclusión del sector de hospitales en el informe de Seguimiento PMMR.0; o Aprobación del establecimiento de la Plataforma de Hospitales de EMVO a fin de elaborar un Plan de Acción para la integración de hospitales (i.e. gobernanza, cómo facilitar la verificación/desactivación a nivel de hospital, cómo integrar a las AC como principales actores, etc) o En la Plataforma participarán todos los miembros de EMVO. HOPE/EAHP liderarán (presidencia, secretaria, contenido, logistica, etc.); o Se ha organizado una primera reunión previa a la constitución de la plataforma el 6/9/ /09/017 5
26 PROXIMOS PASOS o Seguir impulsando la implantación de los sistemas de verificación a nivel nacional. o Conexión masiva de los laboratorios al nodo europeo o Plan de acción para hospitales o Colaboración con las autoridades competentes 6
27 Muchas gracias por su atención. Preguntas? 7
Verificación de Medicamentos. Perspectiva Europea
 Verificación de Medicamentos. Perspectiva Europea 20 Congreso Nacional Farmacéutico 20 Octubre 2016, Madrid Sonia Ruiz Morán Presidenta de EMVO 1 Problema de la falsificación Alcance... 50% medicamentos
Verificación de Medicamentos. Perspectiva Europea 20 Congreso Nacional Farmacéutico 20 Octubre 2016, Madrid Sonia Ruiz Morán Presidenta de EMVO 1 Problema de la falsificación Alcance... 50% medicamentos
Trabajos sobre la verificación de medicamentos en Europa EMVO - Organización Europea para la Verificación de Medicamentos
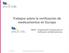 Trabajos sobre la verificación de medicamentos en Europa EMVO - Organización Europea para la Verificación de Medicamentos 1 Países bajo ámbito de aplicación de la Directiva 2011/62/UE 2 Agentes involucrados
Trabajos sobre la verificación de medicamentos en Europa EMVO - Organización Europea para la Verificación de Medicamentos 1 Países bajo ámbito de aplicación de la Directiva 2011/62/UE 2 Agentes involucrados
SERIALIZACIÓN Jornada Profesional de Farmacéuticos de la Distribución Sistema Español de Verificación de Medicamentos
 SERIALIZACIÓN Jornada Profesional de Farmacéuticos de la Distribución Sistema Español de Verificación de Medicamentos 17 de enero de 2018 María Ángeles Figuerola Directora General LEGISLACIÓN DIRECTIVA
SERIALIZACIÓN Jornada Profesional de Farmacéuticos de la Distribución Sistema Español de Verificación de Medicamentos 17 de enero de 2018 María Ángeles Figuerola Directora General LEGISLACIÓN DIRECTIVA
XII Seminario de Periodistas. Medicamentos falsificados: El sistema Europeo de Verificación de Medicamentos (EMVS) y su implementación en España
 Medicamentos falsificados: El sistema Europeo de Verificación de Medicamentos (EMVS) y su implementación en España 1 Objetivo, contenido y plazos Objetivo: Proteger a los pacientes de los medicamentos
Medicamentos falsificados: El sistema Europeo de Verificación de Medicamentos (EMVS) y su implementación en España 1 Objetivo, contenido y plazos Objetivo: Proteger a los pacientes de los medicamentos
Sistema Español de Verificación de Medicamentos
 Sistema Español de Verificación de Medicamentos Visión Global 18 de Mayo de 2016 Índice 1. Contexto Regulatorio 2. Sistema Europeo de Verificación de Medicamentos 3. Principios del Sistema Español de Verificación
Sistema Español de Verificación de Medicamentos Visión Global 18 de Mayo de 2016 Índice 1. Contexto Regulatorio 2. Sistema Europeo de Verificación de Medicamentos 3. Principios del Sistema Español de Verificación
Lucha contra medicamentos falsificados en España: Directiva y Acto Delegado. Iciar Sanz de Madrid. Directora Asuntos Internacionales Farmaindustria.
 Lucha contra medicamentos falsificados en España: Directiva y Acto Delegado Iciar Sanz de Madrid. Directora Asuntos Internacionales Farmaindustria. Interoperatividad de los EMVS europeo y nacionales INTERFACES
Lucha contra medicamentos falsificados en España: Directiva y Acto Delegado Iciar Sanz de Madrid. Directora Asuntos Internacionales Farmaindustria. Interoperatividad de los EMVS europeo y nacionales INTERFACES
SISTEMA ESPAÑOL DE VERIFICACIÓN DE MEDICAMENTOS: REFUERZO EN LA LUCHA CONTRA LA FALSIFICACIÓN
 SISTEMA ESPAÑOL DE VERIFICACIÓN DE MEDICAMENTOS: REFUERZO EN LA LUCHA CONTRA LA FALSIFICACIÓN Belén Crespo Sánchez-Eznarriaga Directora de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS)
SISTEMA ESPAÑOL DE VERIFICACIÓN DE MEDICAMENTOS: REFUERZO EN LA LUCHA CONTRA LA FALSIFICACIÓN Belén Crespo Sánchez-Eznarriaga Directora de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS)
La Directiva 2011/62/UE y el Reglamento Delegado (UE) 2016/161: aspectos generales
 La Directiva 2011/62/UE y el Reglamento Delegado (UE) 2016/161: aspectos generales Belén Escribano Jefe de Departamento de Inspección y Control de Medicamentos 1 Índice Introducción Los dispositivos de
La Directiva 2011/62/UE y el Reglamento Delegado (UE) 2016/161: aspectos generales Belén Escribano Jefe de Departamento de Inspección y Control de Medicamentos 1 Índice Introducción Los dispositivos de
Visión de FEDIFAR. Miguel Valdés Garaizabal Director general de FEDIFAR. Jornada AEMPS - SEVEM 18 MAYO 2016
 DISPOSITIVOS DE SEGURIDAD: ASPECTOS REGULATORIOS Y PUESTA EN MARCHA EN ESPAÑA Visión de FEDIFAR www.fedifar.net @fedifar Miguel Valdés Garaizabal Director general de FEDIFAR 1 Antecedentes Jornada AEMPS
DISPOSITIVOS DE SEGURIDAD: ASPECTOS REGULATORIOS Y PUESTA EN MARCHA EN ESPAÑA Visión de FEDIFAR www.fedifar.net @fedifar Miguel Valdés Garaizabal Director general de FEDIFAR 1 Antecedentes Jornada AEMPS
Verificación de medicamentos Marco regulatorio
 Verificación de medicamentos Marco regulatorio Pilar Fernández del Pozo Bielza Inspectora farmacéutica - DICM AEMPS Sistema dispositivos seguridad Directiva 2011/62/UE medicamentos falsificados, modifica
Verificación de medicamentos Marco regulatorio Pilar Fernández del Pozo Bielza Inspectora farmacéutica - DICM AEMPS Sistema dispositivos seguridad Directiva 2011/62/UE medicamentos falsificados, modifica
Glosario FMD de la UE
 50 términos para entender la Directiva sobre medicamentos falsificados de la UE! Glosario FMD de la UE Un suplemento a Los 144 términos que debe conocer para descifrar la serializacíon Introducción En
50 términos para entender la Directiva sobre medicamentos falsificados de la UE! Glosario FMD de la UE Un suplemento a Los 144 términos que debe conocer para descifrar la serializacíon Introducción En
El repositorio en el Reglamento delegado 2016/161. Manuel Ibarra Lorente Departamento de Inspección y Control de Medicamentos
 El repositorio en el Reglamento delegado 2016/161 Manuel Ibarra Lorente Departamento de Inspección y Control de Medicamentos 1 Estructura y funciones Elemento esencial en la eficacia del sistema de dispositivos
El repositorio en el Reglamento delegado 2016/161 Manuel Ibarra Lorente Departamento de Inspección y Control de Medicamentos 1 Estructura y funciones Elemento esencial en la eficacia del sistema de dispositivos
SERIALIZACIÓN, ASOCIACIONES DE INTEGRACIÓN Y CENTRO DE CONEXIÓN EUROPEO. Sus principales preguntas sobre EMVS y FMD de la UE
 SERIALIZACIÓN, ASOCIACIONES DE INTEGRACIÓN Y CENTRO DE CONEXIÓN EUROPEO Sus principales preguntas sobre EMVS y FMD de la UE INTRODUCCIÓN En 2016, se publicó la Ley delegada sobre características de seguridad,
SERIALIZACIÓN, ASOCIACIONES DE INTEGRACIÓN Y CENTRO DE CONEXIÓN EUROPEO Sus principales preguntas sobre EMVS y FMD de la UE INTRODUCCIÓN En 2016, se publicó la Ley delegada sobre características de seguridad,
Verificación de Medicamentos en Oficina de Farmacia. Nodofarma Verificación
 Verificación de Medicamentos en Oficina de Farmacia Nodofarma Verificación Contexto y normativa europea NORMATIVA DE APLICACIÓN DIRECTIVA 2011/62/UE REGLAMENTO DELEGADO 2016/161 Características técnicas
Verificación de Medicamentos en Oficina de Farmacia Nodofarma Verificación Contexto y normativa europea NORMATIVA DE APLICACIÓN DIRECTIVA 2011/62/UE REGLAMENTO DELEGADO 2016/161 Características técnicas
VERIFICACIÓN DE MEDICAMENTOS EN ESPAÑA Y SU APLICACIÓN EN LA FARMACIA COMUNITARIA
 VERIFICACIÓN DE MEDICAMENTOS EN ESPAÑA Y SU APLICACIÓN EN LA FARMACIA COMUNITARIA Visión de la Farmacia Comunitaria Carmen Recio Jaraba Directora Técnica Consejo General COF La protección de la salud de
VERIFICACIÓN DE MEDICAMENTOS EN ESPAÑA Y SU APLICACIÓN EN LA FARMACIA COMUNITARIA Visión de la Farmacia Comunitaria Carmen Recio Jaraba Directora Técnica Consejo General COF La protección de la salud de
La serialització: el gran canvi en la cadena del medicament Emili Esteve Sala Departamento Técnico Director
 La serialització: el gran canvi en la cadena del medicament. 26.09.2016 Emili Esteve Sala Departamento Técnico Director MINIMIZACION DE FALSIFICACIONES PUESTA EN EL MERCADO (ACTIVACION) VERIFICACION DE
La serialització: el gran canvi en la cadena del medicament. 26.09.2016 Emili Esteve Sala Departamento Técnico Director MINIMIZACION DE FALSIFICACIONES PUESTA EN EL MERCADO (ACTIVACION) VERIFICACION DE
Reglamento delegado de la Comisión 2016/161 DISPOSITIVOS DE SEGURIDAD
 II Encuentro LOS RETOS DEL PACKAGING FARMACÉUTICO MACULART 30 marzo 2017 Reglamento delegado de la Comisión 2016/161 DISPOSITIVOS DE SEGURIDAD Pilar Fernández del Pozo Bielza Inspectora Farmacéutica Departamento
II Encuentro LOS RETOS DEL PACKAGING FARMACÉUTICO MACULART 30 marzo 2017 Reglamento delegado de la Comisión 2016/161 DISPOSITIVOS DE SEGURIDAD Pilar Fernández del Pozo Bielza Inspectora Farmacéutica Departamento
La trazabilidad total a debate: Cómo convertir el sueño en realidad
 La trazabilidad total a debate: Cómo convertir el sueño en realidad 1ª PARTE: La trazabilidad de medicamentos en el hospital Visión del farmacéutico de hospital de la trazabilidad total. Dr. Miguel Ángel.
La trazabilidad total a debate: Cómo convertir el sueño en realidad 1ª PARTE: La trazabilidad de medicamentos en el hospital Visión del farmacéutico de hospital de la trazabilidad total. Dr. Miguel Ángel.
Verificación de Medicamentos en Oficina de Farmacia. Preguntas y respuestas Versión I
 Verificación de Medicamentos en Oficina de Farmacia. Preguntas y respuestas Versión I Índice Sección 1: Introducción. Sistema de autenticación de medicamentos... Sección 2: Aspectos Operativos en la oficina
Verificación de Medicamentos en Oficina de Farmacia. Preguntas y respuestas Versión I Índice Sección 1: Introducción. Sistema de autenticación de medicamentos... Sección 2: Aspectos Operativos en la oficina
El nuevo escenario en materia de serialización:
 El nuevo escenario en materia de serialización: Implantación del sistema de dispositivos de seguridad, perspectiva de las autoridades nacionales competentes. Manuel Ibarra Departamento de Inspección y
El nuevo escenario en materia de serialización: Implantación del sistema de dispositivos de seguridad, perspectiva de las autoridades nacionales competentes. Manuel Ibarra Departamento de Inspección y
Antecedentes de la norma
 CONSULTA PÚBLICA PREVIA PROYECTO DE REAL DECRETO POR EL QUE SE MODIFICA EL REAL DECRETO 824/2010, DE 25 DE JUNIO, POR EL QUE SE REGULAN LOS LABORATORIOS FARMACÉUTICOS, LOS FABRICANTES DE PRINCIPIOS ACTIVOS
CONSULTA PÚBLICA PREVIA PROYECTO DE REAL DECRETO POR EL QUE SE MODIFICA EL REAL DECRETO 824/2010, DE 25 DE JUNIO, POR EL QUE SE REGULAN LOS LABORATORIOS FARMACÉUTICOS, LOS FABRICANTES DE PRINCIPIOS ACTIVOS
VERIFICACIÓN, DISTRIBUCIÓN Y GESTIÓN DE DATOS. Sus preguntas más importantes acerca de la verificación del producto y la FMD de la UE
 Sus preguntas más importantes acerca de la verificación del producto y la FMD de la UE INTRODUCCIÓN En 2016, se publicó la Ley delegada sobre características de seguridad, introduciendo leyes estrictas
Sus preguntas más importantes acerca de la verificación del producto y la FMD de la UE INTRODUCCIÓN En 2016, se publicó la Ley delegada sobre características de seguridad, introduciendo leyes estrictas
IMPACTO DEL SISTEMA DE DISPOSITIVOS DE SEGURIDAD VISIÓN AEMPS
 IMPACTO DEL SISTEMA DE DISPOSITIVOS DE SEGURIDAD VISIÓN AEMPS Pilar Fernández del Pozo Bielza Dpto. Inspección y Control de Medicamentos AEMPS IMPACTO EN LA AEMPS Nuevo desarrollo normativo Gestión de
IMPACTO DEL SISTEMA DE DISPOSITIVOS DE SEGURIDAD VISIÓN AEMPS Pilar Fernández del Pozo Bielza Dpto. Inspección y Control de Medicamentos AEMPS IMPACTO EN LA AEMPS Nuevo desarrollo normativo Gestión de
15 principales preguntas y respuestas Características de verificación y seguridad de la FMD en la UE
 15 principales preguntas y respuestas Características de verificación y seguridad de la FMD en la UE Establecido en los actuales momentos para principios de 2019, el Acto Delegado sobre características
15 principales preguntas y respuestas Características de verificación y seguridad de la FMD en la UE Establecido en los actuales momentos para principios de 2019, el Acto Delegado sobre características
OBLIGACIONES DE LA INDUSTRIA FARMACEUTICA. I PRODUCCION
 El Reglamento Delegado de la Comisión (RDC) desarrolla lo que la Directiva 2001/83/CE exige:.. los dispositivos de seguridad son obligatorios. DCM IU SITUACIONES ESPECIALES. MEDICAMENTOS SIN DISPOSITIVOS
El Reglamento Delegado de la Comisión (RDC) desarrolla lo que la Directiva 2001/83/CE exige:.. los dispositivos de seguridad son obligatorios. DCM IU SITUACIONES ESPECIALES. MEDICAMENTOS SIN DISPOSITIVOS
Nuevos requisitos en la fabricación y distribución de medicamentos y principios activos: la transposición del directiva de medicamentos falsificados
 Nuevos requisitos en la fabricación y distribución de medicamentos y principios activos: la transposición del directiva de medicamentos falsificados Belén Escribano Jefe de Departamento de Inspección y
Nuevos requisitos en la fabricación y distribución de medicamentos y principios activos: la transposición del directiva de medicamentos falsificados Belén Escribano Jefe de Departamento de Inspección y
INFORMES DE CUMPLIMIENTO, REQUISITOS POR PAÍS Y COMERCIO MULTIMERCADO. Sus principales preguntas sobre los requisitos multimercado y FMD de la UE
 INFORMES DE CUMPLIMIENTO, REQUISITOS POR PAÍS Y COMERCIO Sus principales preguntas sobre los requisitos multimercado y FMD de la UE INTRODUCCIÓN Las empresas que venden medicamentos en la UE tienen ya
INFORMES DE CUMPLIMIENTO, REQUISITOS POR PAÍS Y COMERCIO Sus principales preguntas sobre los requisitos multimercado y FMD de la UE INTRODUCCIÓN Las empresas que venden medicamentos en la UE tienen ya
Santiago de Chile, 26 de septiembre de 2012.
 Retos para la Industria Farmacéutica en: Auditorias y estrategias de autentificación de medicamentos utilizadas para prevenir la falsificación y fraudulencia de medicamentos Santiago de Chile, 26 de septiembre
Retos para la Industria Farmacéutica en: Auditorias y estrategias de autentificación de medicamentos utilizadas para prevenir la falsificación y fraudulencia de medicamentos Santiago de Chile, 26 de septiembre
Estrategias para Combatir la Falsificación y el Comercio Ilegal en el Perú
 Estrategias para Combatir la Falsificación y el Comercio Ilegal en el Perú Q.F MARISA PAPEN BERNAOLA Jefe de Unidad Funcional Contra el Comercio Ilegal Dirección de Medicamentos Insumos y Drogas DIGEMID.
Estrategias para Combatir la Falsificación y el Comercio Ilegal en el Perú Q.F MARISA PAPEN BERNAOLA Jefe de Unidad Funcional Contra el Comercio Ilegal Dirección de Medicamentos Insumos y Drogas DIGEMID.
Introducción y evolución de las Buenas Prácticas de Distribución. Requisitos para la intermediación de medicamentos: capítulo 10.
 Introducción y evolución de las Buenas Prácticas de Distribución. Requisitos para la intermediación de medicamentos: capítulo 10. Belén Escribano Jefe de Departamento de Inspección y Control de Medicamentos
Introducción y evolución de las Buenas Prácticas de Distribución. Requisitos para la intermediación de medicamentos: capítulo 10. Belén Escribano Jefe de Departamento de Inspección y Control de Medicamentos
De la Directiva a la realidad de la Farmacia. Hospitalaria. Impacto en las tecnologías de dispensación
 De la Directiva a la realidad de la Farmacia Impacto en las tecnologías de dispensación Hospitalaria Ana Álvarez Díaz Coordinadora Grupo TECNO de la SEFH IMPACTO EN LA TECNOLOGÍA DE DISPENSACIÓN DE MEDICAMENTOS
De la Directiva a la realidad de la Farmacia Impacto en las tecnologías de dispensación Hospitalaria Ana Álvarez Díaz Coordinadora Grupo TECNO de la SEFH IMPACTO EN LA TECNOLOGÍA DE DISPENSACIÓN DE MEDICAMENTOS
Control de Mercado de Medicamentos. Farm. Maria Jose Sanchez Directora Vigilancia de Productos para la Salud ANMAT
 Control de Mercado de Medicamentos Farm. Maria Jose Sanchez Directora Vigilancia de Productos para la Salud ANMAT Antecedentes 1997- falsificación MADOPAR 1997 - Programa Nacional de Pesquisa de Medicamentos
Control de Mercado de Medicamentos Farm. Maria Jose Sanchez Directora Vigilancia de Productos para la Salud ANMAT Antecedentes 1997- falsificación MADOPAR 1997 - Programa Nacional de Pesquisa de Medicamentos
Compromiso de la Organización Farmacéutica Colegial en la Transformación Digital. Mª Rosa López-Torres Hidalgo Tesorera del CGCOF
 Compromiso de la Organización Farmacéutica Colegial en la Transformación Digital Mª Rosa López-Torres Hidalgo Tesorera del CGCOF El uso de las Nuevas Tecnologías en la Sanidad (E-Salud) es imprescindible
Compromiso de la Organización Farmacéutica Colegial en la Transformación Digital Mª Rosa López-Torres Hidalgo Tesorera del CGCOF El uso de las Nuevas Tecnologías en la Sanidad (E-Salud) es imprescindible
VERIFICACIÓN Y AUTENTICACIÓN DE MEDICAMENTOS Documento del Grupo de Trabajo del CGCOF 28 de septiembre de 2017
 VERIFICACIÓN Y AUTENTICACIÓN DE MEDICAMENTOS Documento del Grupo de Trabajo del CGCOF 28 de septiembre de 2017 LEGISLACIÓN Directiva 2011/62/UE del Parlamento Europeo y del Consejo, de 8 de junio de 2011,
VERIFICACIÓN Y AUTENTICACIÓN DE MEDICAMENTOS Documento del Grupo de Trabajo del CGCOF 28 de septiembre de 2017 LEGISLACIÓN Directiva 2011/62/UE del Parlamento Europeo y del Consejo, de 8 de junio de 2011,
Cambios relativos a la fabricación de medicamentos y principios activos incluidos en la disposición final primera del real decreto
 Cambios relativos a la fabricación de medicamentos y principios activos incluidos en la disposición final primera del real decreto Cristina Gómez-Chacón Galán Jefe del Área de Inspección de NCF y BPL Departamento
Cambios relativos a la fabricación de medicamentos y principios activos incluidos en la disposición final primera del real decreto Cristina Gómez-Chacón Galán Jefe del Área de Inspección de NCF y BPL Departamento
En el caso de los medicamentos falsificados
 î NORMATIVA Y LEGISLACIÓN Juan Jorge Poveda Álvarez Director del Gabinete de Dirección del Grupo COFARES Vocal de Distribución del Colegio Oficial de Farmacéuticos de Madrid @jjorgepoveda IMPLANTACIÓN
î NORMATIVA Y LEGISLACIÓN Juan Jorge Poveda Álvarez Director del Gabinete de Dirección del Grupo COFARES Vocal de Distribución del Colegio Oficial de Farmacéuticos de Madrid @jjorgepoveda IMPLANTACIÓN
Modificación de la legislación farmacéutica en la UE. 2
 CONTENIDO: 1 Modificación de la legislación farmacéutica en la UE. 2 1 Se prohíbe la reproducción total o parcial del contenido de este "Boletín Europa al Día" sin citar la fuente o sin haber obtenido
CONTENIDO: 1 Modificación de la legislación farmacéutica en la UE. 2 1 Se prohíbe la reproducción total o parcial del contenido de este "Boletín Europa al Día" sin citar la fuente o sin haber obtenido
Estrategia española frente a medicamentos falsificados Belén Escribano Jefe del Departamento de Inspección y Control de Medicamentos
 Estrategia española frente a medicamentos falsificados 2016-2019 Belén Escribano Jefe del Departamento de Inspección y Control de Medicamentos Ante la amenaza para la salud pública que suponen los medicamentos
Estrategia española frente a medicamentos falsificados 2016-2019 Belén Escribano Jefe del Departamento de Inspección y Control de Medicamentos Ante la amenaza para la salud pública que suponen los medicamentos
MINISTERIO DE SANIDAD, CONSUMO Y BIENESTAR SOCIAL SECRETARIA GENERAL DE SANIDAD Y CONSUMO. 18/01/2019
 MINISTERIO DE SANIDAD, CONSUMO Y BIENESTAR SOCIAL 18/01/2019 SECRETARIA GENERAL DE SANIDAD Y CONSUMO. DIRECCION GENERAL DE CARTERA BASICA DE SERVICIOS DEL S.N.S. Y FARMACIA. Proyecto de Real Decreto xx/xxxx,
MINISTERIO DE SANIDAD, CONSUMO Y BIENESTAR SOCIAL 18/01/2019 SECRETARIA GENERAL DE SANIDAD Y CONSUMO. DIRECCION GENERAL DE CARTERA BASICA DE SERVICIOS DEL S.N.S. Y FARMACIA. Proyecto de Real Decreto xx/xxxx,
Verificación vs Trazabilidad. Trazabilidad clínica: más allá de la verificación. Que los árboles no nos impidan ver el bosque 02/10/2017
 Trazabilidad clínica: más allá de la verificación De la Directiva a la realidad de la Farmacia Hospitalaria: retos y oportunidades Dr. Antonio Idoate García Director Servicio de Farmacia Que los árboles
Trazabilidad clínica: más allá de la verificación De la Directiva a la realidad de la Farmacia Hospitalaria: retos y oportunidades Dr. Antonio Idoate García Director Servicio de Farmacia Que los árboles
Securización en la Farmacia y en Internet
 Mesa Debate: Los farmacéuticos actúan contra los Medicamentos falsificados y el comercio ilegal de Medicamentos Securización en la Farmacia y en Internet Teodomiro Hidalgo Sotelo Vocal Nacional de Oficina
Mesa Debate: Los farmacéuticos actúan contra los Medicamentos falsificados y el comercio ilegal de Medicamentos Securización en la Farmacia y en Internet Teodomiro Hidalgo Sotelo Vocal Nacional de Oficina
Experiencias de lucha contra los medicamentos falsificados en la República Dominicana
 Experiencias de lucha contra los medicamentos falsificados en la República Dominicana Dalia Castillo Sánchez Departamento de Vigilancia Sanitaria, Inspección y Control Marco legal Constitución dominicana
Experiencias de lucha contra los medicamentos falsificados en la República Dominicana Dalia Castillo Sánchez Departamento de Vigilancia Sanitaria, Inspección y Control Marco legal Constitución dominicana
III Día de la Tecnología Sanitaria en Castilla-La Mancha. 1 de Julio de 2016
 III Día de la Tecnología Sanitaria en Castilla-La Mancha. 1 de Julio de 2016 TECNOLOGÍA SANITARIA EN ESPAÑA: FORMACIÓN Y ARMONIZACIÓN EUROPEA M. Carmen Abad Luna. Jefe del Departamento de Productos Sanitarios.
III Día de la Tecnología Sanitaria en Castilla-La Mancha. 1 de Julio de 2016 TECNOLOGÍA SANITARIA EN ESPAÑA: FORMACIÓN Y ARMONIZACIÓN EUROPEA M. Carmen Abad Luna. Jefe del Departamento de Productos Sanitarios.
Nuevo Sistema Web para el intercambio rápido de información y alertas sobre medicamentos falsificados y fraudulentos en Iberoamérica
 Nuevo Sistema Web para el intercambio rápido de información y alertas sobre medicamentos falsificados y fraudulentos en Iberoamérica Carlos David Gea Méndez Jose Mª Martín del Castillo Área de Medicamentos
Nuevo Sistema Web para el intercambio rápido de información y alertas sobre medicamentos falsificados y fraudulentos en Iberoamérica Carlos David Gea Méndez Jose Mª Martín del Castillo Área de Medicamentos
î NORMATIVA /LOGÍSTICA Y DISTRIBUCIÓN
 î NORMATIVA /LOGÍSTICA Y DISTRIBUCIÓN Juan Jorge Poveda Álvarez Director del Gabinete de Dirección del Grupo COFARES Vocal de Distribución del Colegio Oficial de Farmacéuticos de Madrid @jjorgepoveda SISTEMA
î NORMATIVA /LOGÍSTICA Y DISTRIBUCIÓN Juan Jorge Poveda Álvarez Director del Gabinete de Dirección del Grupo COFARES Vocal de Distribución del Colegio Oficial de Farmacéuticos de Madrid @jjorgepoveda SISTEMA
VERIFICACIÓN DE MEDICAMENTOS EN ESPAÑA. IMPACTO EN LAS COMUNIDADES AUTÓNOMAS Y EN LA FARMACIA HOSPITALARIA
 VERIFICACIÓN DE MEDICAMENTOS EN ESPAÑA. IMPACTO EN LAS COMUNIDADES AUTÓNOMAS Y EN LA FARMACIA HOSPITALARIA Fco. Javier ARMESTO GÓMEZ Jefe de Servicio de Farmacia Servicio Aragonés de Salud Verificación
VERIFICACIÓN DE MEDICAMENTOS EN ESPAÑA. IMPACTO EN LAS COMUNIDADES AUTÓNOMAS Y EN LA FARMACIA HOSPITALARIA Fco. Javier ARMESTO GÓMEZ Jefe de Servicio de Farmacia Servicio Aragonés de Salud Verificación
Actualización de Guías de Buenas Practicas de Almacenamiento
 Actualización de Guías de Buenas Practicas de Almacenamiento Dr. Mario Ernesto González Larios Jefe de Unidad de Inspección y Fiscalización Dirección Nacional de Medicamentos BASE LEGAL LEY DE MEDICAMENTOS,
Actualización de Guías de Buenas Practicas de Almacenamiento Dr. Mario Ernesto González Larios Jefe de Unidad de Inspección y Fiscalización Dirección Nacional de Medicamentos BASE LEGAL LEY DE MEDICAMENTOS,
REGLAMENTOS -PRODUCTOS SANITARIOS -PRODUCTOS SANITARIOS PARA DIAGNOSTICO IN VITRO
 Proceso legislativo de los Reglamentos de Productos Sanitarios REGLAMENTOS -PRODUCTOS SANITARIOS -PRODUCTOS SANITARIOS PARA DIAGNOSTICO IN VITRO MSSSI, AEMPS Madrid, 13 Septiembre 2016 Francisco Sevilla
Proceso legislativo de los Reglamentos de Productos Sanitarios REGLAMENTOS -PRODUCTOS SANITARIOS -PRODUCTOS SANITARIOS PARA DIAGNOSTICO IN VITRO MSSSI, AEMPS Madrid, 13 Septiembre 2016 Francisco Sevilla
Sector Salud. Guía GS1 de Implantación de Serialización de Medicamentos
 The Global Language of Business Sector Salud Guía GS1 de Implantación de Serialización de Medicamentos Pasos para la correcta adopción de los estándares GS1 para cumplir con la Directiva 2011/62/EU anti-falsificación
The Global Language of Business Sector Salud Guía GS1 de Implantación de Serialización de Medicamentos Pasos para la correcta adopción de los estándares GS1 para cumplir con la Directiva 2011/62/EU anti-falsificación
Modificaciones que afectan a la inspección n y el control de los medicamentos
 Modificaciones que afectan a la inspección n y el control de los medicamentos Belén n Escribano Romero Jefe de Departamento de Inspección n y Control de Medicamentos 1 Índice Descripción general de los
Modificaciones que afectan a la inspección n y el control de los medicamentos Belén n Escribano Romero Jefe de Departamento de Inspección n y Control de Medicamentos 1 Índice Descripción general de los
FENIN, LA TECNOLOGÍA SANITARIA EN ESPAÑA
 FENIN, LA TECNOLOGÍA SANITARIA EN ESPAÑA Qué es Fenin? La Federación Española de Empresas de Tecnología Sanitaria (Fenin) es una organización de ámbito nacional con más de 500 miembros (empresas individuales,
FENIN, LA TECNOLOGÍA SANITARIA EN ESPAÑA Qué es Fenin? La Federación Española de Empresas de Tecnología Sanitaria (Fenin) es una organización de ámbito nacional con más de 500 miembros (empresas individuales,
DIRECCIÓN NACIONAL DE VIGILANCIA SANITARIA -PARAGUAY-
 DIRECCIÓN NACIONAL DE VIGILANCIA SANITARIA -PARAGUAY- Iturbe N 883 e/ Manuel Domínguez y Fulgencio R. Moreno. Asunción - Paraguay La Dirección Nacional de Vigilancia Sanitaria, es un organismo dependiente
DIRECCIÓN NACIONAL DE VIGILANCIA SANITARIA -PARAGUAY- Iturbe N 883 e/ Manuel Domínguez y Fulgencio R. Moreno. Asunción - Paraguay La Dirección Nacional de Vigilancia Sanitaria, es un organismo dependiente
Q.F. IRENE CHEA WOO DIRECTORA EJECUTIVA DIRECCION DE ESTABLECIMIENTOS FARMACÉUTICOS
 Q.F. IRENE CHEA WOO DIRECTORA EJECUTIVA DIRECCION DE ESTABLECIMIENTOS FARMACÉUTICOS Organigrama Estructural de DIGEMID MINISTERIO DE SALUD DIGEMID DIRECCIÓN Y ACCESO Y USO DE MEDICAMENTOS Y OTRAS TECNOLOGIAS
Q.F. IRENE CHEA WOO DIRECTORA EJECUTIVA DIRECCION DE ESTABLECIMIENTOS FARMACÉUTICOS Organigrama Estructural de DIGEMID MINISTERIO DE SALUD DIGEMID DIRECCIÓN Y ACCESO Y USO DE MEDICAMENTOS Y OTRAS TECNOLOGIAS
VERIFICACIÓN Y AUTENTICACIÓN DE MEDICAMENTOS. Requerimientos de los servicios de farmacia de centros asistenciales
 VERIFICACIÓN Y AUTENTICACIÓN DE MEDICAMENTOS Requerimientos de los servicios de farmacia de centros asistenciales Este documento ha sido elaborado por un Grupo de Trabajo constituido en el Consejo General
VERIFICACIÓN Y AUTENTICACIÓN DE MEDICAMENTOS Requerimientos de los servicios de farmacia de centros asistenciales Este documento ha sido elaborado por un Grupo de Trabajo constituido en el Consejo General
JORNADA TECNOLOGÍA SANITARIA MADRID NUEVO REGLAMENTO DE PRODUCTOS SANITARIOS EQUIPOS Y SOFTWARE
 JORNADA TECNOLOGÍA SANITARIA MADRID NUEVO REGLAMENTO DE PRODUCTOS SANITARIOS EQUIPOS Y SOFTWARE Mª Carmen Abad Luna Jefe del Departamento de Productos Sanitarios 4 Noviembre 2016 1 FECHAS CLAVE Comienzo
JORNADA TECNOLOGÍA SANITARIA MADRID NUEVO REGLAMENTO DE PRODUCTOS SANITARIOS EQUIPOS Y SOFTWARE Mª Carmen Abad Luna Jefe del Departamento de Productos Sanitarios 4 Noviembre 2016 1 FECHAS CLAVE Comienzo
NORMA UNE : GESTIÓN AMBIENTAL DEL PROCESO DE DISEÑO Y DESARROLLO. ECODISEÑO
 NORMA UNE 150301: GESTIÓN AMBIENTAL DEL PROCESO DE DISEÑO Y DESARROLLO. ECODISEÑO JORNADA EINES PER A L'APLICACIÓ DE L'ECODISSENY PER AL RECICLATGE HERRAMIENTAS PARA LA APLICACIÓN DEL DISEÑO PARA EL RECICLAJE
NORMA UNE 150301: GESTIÓN AMBIENTAL DEL PROCESO DE DISEÑO Y DESARROLLO. ECODISEÑO JORNADA EINES PER A L'APLICACIÓ DE L'ECODISSENY PER AL RECICLATGE HERRAMIENTAS PARA LA APLICACIÓN DEL DISEÑO PARA EL RECICLAJE
LEGISLACIÓN, DEONTOLOGÍA Y GESTIÓN FARMACÉUTICA CURSO
 LEGISLACIÓN, DEONTOLOGÍA Y GESTIÓN FARMACÉUTICA CURSO 2014-2015 Departamento de Farmacia y Tecnología Farmacéutica Facultad de Farmacia. Universidad de Granada Profesorado responsable: Sección de Historia
LEGISLACIÓN, DEONTOLOGÍA Y GESTIÓN FARMACÉUTICA CURSO 2014-2015 Departamento de Farmacia y Tecnología Farmacéutica Facultad de Farmacia. Universidad de Granada Profesorado responsable: Sección de Historia
LISTA DE COMPROBACIÓN
 2 018 Un esquema de auditoría reconocida mundialmente para la inocuidad alimentaria por la Iniciativa Global para la Inocuidad Alimentaria (GFSI) LISTA DE COMPROBACIÓN PrimusGFS v.0 MODULO 1 SAIA Requisitos
2 018 Un esquema de auditoría reconocida mundialmente para la inocuidad alimentaria por la Iniciativa Global para la Inocuidad Alimentaria (GFSI) LISTA DE COMPROBACIÓN PrimusGFS v.0 MODULO 1 SAIA Requisitos
Aspectos generales del nuevo real decreto
 Aspectos generales del nuevo real decreto Belén Escribano Romero Subdirectora General de Inspección y Control de Medicamentos Real Decreto 824/2010, de 25 de junio, por el que se regulan los laboratorios
Aspectos generales del nuevo real decreto Belén Escribano Romero Subdirectora General de Inspección y Control de Medicamentos Real Decreto 824/2010, de 25 de junio, por el que se regulan los laboratorios
Abril El Papel de una Sociedad Científica para la implantación de las TIC en Sanidad
 Abril 2005 El Papel de una Sociedad Científica para la implantación de las TIC en Sanidad INDICE AMBITO DE ACTUACION LA SOCIEDAD ESPAÑOLA DE INFORMATICA DE LA SALUD 1 ESCENARIO El entorno sanitario se
Abril 2005 El Papel de una Sociedad Científica para la implantación de las TIC en Sanidad INDICE AMBITO DE ACTUACION LA SOCIEDAD ESPAÑOLA DE INFORMATICA DE LA SALUD 1 ESCENARIO El entorno sanitario se
Notificación de cumplimiento, el European Hub y los sistemas nacionales
 RESPUESTAS A SUS PRINCIPALES Notificación de cumplimiento, el European Hub y los sistemas nacionales 01 Índice 03 I N T R O D UCC IÓ N 04 CUÁ N TO CUESTA R EG IST RA RS E PA RA L A F M D DE L A U E? 06
RESPUESTAS A SUS PRINCIPALES Notificación de cumplimiento, el European Hub y los sistemas nacionales 01 Índice 03 I N T R O D UCC IÓ N 04 CUÁ N TO CUESTA R EG IST RA RS E PA RA L A F M D DE L A U E? 06
Oficina General de Tecnologías de la Información Oficina de Innovación y Desarrollo Tecnológico Ing. Jhon Henry Garcia Ruiz OIDT OGTI
 MINISTERIO DE SALUD Rumbo a una Salud Digital Oficina General de Tecnologías de la Información Oficina de Innovación y Desarrollo Tecnológico Agenda 1.Ordenamiento de los Sistemas de Información 2.Plataforma
MINISTERIO DE SALUD Rumbo a una Salud Digital Oficina General de Tecnologías de la Información Oficina de Innovación y Desarrollo Tecnológico Agenda 1.Ordenamiento de los Sistemas de Información 2.Plataforma
EL ENVASE DEL MEDICAMENTO
 EL ENVASE DEL MEDICAMENTO Una fuente de información para su correcta dispensación y uso Si aparece una línea negra bordeando la parte superior del cupón (cupón precinto diferenciado ), el medicamento requiere
EL ENVASE DEL MEDICAMENTO Una fuente de información para su correcta dispensación y uso Si aparece una línea negra bordeando la parte superior del cupón (cupón precinto diferenciado ), el medicamento requiere
Entidades de distribución Entidades de intermediación
 Entidades de distribución Entidades de intermediación M Luisa Tarno DICM AEMPS 17/12/2013 Índice Requisitos Funciones Obligaciones Marco legal anterior Ley 29/2006,de 26 de julio, de garantías y uso racional
Entidades de distribución Entidades de intermediación M Luisa Tarno DICM AEMPS 17/12/2013 Índice Requisitos Funciones Obligaciones Marco legal anterior Ley 29/2006,de 26 de julio, de garantías y uso racional
PRESENTACION INTRODUCCIÓN AL SISTEMA DE GESTIÓN ALIMENTARIA ISO 22000:2005
 PRESENTACION INTRODUCCIÓN AL SISTEMA DE GESTIÓN ALIMENTARIA ISO 22000:2005 Propósito de un Sistema de Gestión de Seguridad de alimentos ISO 22000 El desarrollo de un sistema de gestión de seguridad de
PRESENTACION INTRODUCCIÓN AL SISTEMA DE GESTIÓN ALIMENTARIA ISO 22000:2005 Propósito de un Sistema de Gestión de Seguridad de alimentos ISO 22000 El desarrollo de un sistema de gestión de seguridad de
Diario Oficial de la Unión Europea L 146/7
 8.6.2007 Diario Oficial de la Unión Europea L 146/7 REGLAMENTO (CE) N o 633/2007 DE LA COMISIÓN de 7 de junio de 2007 por el que se establecen requisitos para la aplicación de un protocolo de transferencia
8.6.2007 Diario Oficial de la Unión Europea L 146/7 REGLAMENTO (CE) N o 633/2007 DE LA COMISIÓN de 7 de junio de 2007 por el que se establecen requisitos para la aplicación de un protocolo de transferencia
Adquisiciones de insumos médicos y farmacéuticos en Instituciones Costarricenses.
 Adquisiciones de insumos médicos y farmacéuticos en Instituciones Costarricenses. Diferencias Principios Fines De esta suma aproximadamente un 25% corresponde a la CCSS y al INS (en conjunto) Fuente: Contraloría
Adquisiciones de insumos médicos y farmacéuticos en Instituciones Costarricenses. Diferencias Principios Fines De esta suma aproximadamente un 25% corresponde a la CCSS y al INS (en conjunto) Fuente: Contraloría
Q.F. KARLA PALOMINO SALAZAR
 Q.F. KARLA PALOMINO SALAZAR ORGANIGRAMA ESTRUCTURAL DE DIGEMID MINISTERIO DE SALUD DIGEMID DIRECCIÓN DE FARMACOVOGI- LANCIA, ACCESO Y USO DIRECCIÓN DE PRODUCTOS FARMACÉUTICOS DIRECCIÓN DE DISPOSITIVOS
Q.F. KARLA PALOMINO SALAZAR ORGANIGRAMA ESTRUCTURAL DE DIGEMID MINISTERIO DE SALUD DIGEMID DIRECCIÓN DE FARMACOVOGI- LANCIA, ACCESO Y USO DIRECCIÓN DE PRODUCTOS FARMACÉUTICOS DIRECCIÓN DE DISPOSITIVOS
BUS DE INTEGRACIÓN. Presentación al mercado Agosto Proyecto Bus de Integración Camino hacia la Excelencia Operacional
 BUS DE INTEGRACIÓN Presentación al mercado Agosto 2007 Objetivos de la sesión Dar a conocer la estrategia y alcance de proyecto de integración que la BVC ha definido. Promover la creación de un comité
BUS DE INTEGRACIÓN Presentación al mercado Agosto 2007 Objetivos de la sesión Dar a conocer la estrategia y alcance de proyecto de integración que la BVC ha definido. Promover la creación de un comité
La FMD de la UE y los Actos Delegados desde dentro. Guía básica de cumplimiento
 La FMD de la UE y los Actos Delegados desde dentro Guía básica de cumplimiento ÍNDICE 01 02 Requisitos de la FMD de la UE y los Actos Delegados Cómo se rige la FMD de la UE? Cuales son las funciones para
La FMD de la UE y los Actos Delegados desde dentro Guía básica de cumplimiento ÍNDICE 01 02 Requisitos de la FMD de la UE y los Actos Delegados Cómo se rige la FMD de la UE? Cuales son las funciones para
4. Cuál es el objetivo de retirar un producto del mercado?
 PREGUNTAS FRECUENTES DE RETIRO DE MERCADO 1. Qué es el retiro de mercado? 1 Es un proceso para remover un producto de la cadena de distribución, a causa de defectos de calidad del producto o reclamos por
PREGUNTAS FRECUENTES DE RETIRO DE MERCADO 1. Qué es el retiro de mercado? 1 Es un proceso para remover un producto de la cadena de distribución, a causa de defectos de calidad del producto o reclamos por
IPN 85/12 PROYECTO DE REAL DECRETO SOBRE DISTRIBUCIÓN DE MEDICAMENTOS DE USO HUMANO
 IPN 85/12 PROYECTO DE REAL DECRETO SOBRE DISTRIBUCIÓN DE MEDICAMENTOS DE USO HUMANO El Consejo de la Comisión Nacional de la Competencia, en su reunión de 19 de diciembre de 2012, ha aprobado el presente
IPN 85/12 PROYECTO DE REAL DECRETO SOBRE DISTRIBUCIÓN DE MEDICAMENTOS DE USO HUMANO El Consejo de la Comisión Nacional de la Competencia, en su reunión de 19 de diciembre de 2012, ha aprobado el presente
ISDE Farmacéuticos y Laboratorios
 ISDE Farmacéuticos y Laboratorios Mini-Talleres Octubre, 2011 Permitida su circulación y reproducción en todo o en parte citando la fuente. Resumen ejecutivo Los segmentos de producción mas importantes
ISDE Farmacéuticos y Laboratorios Mini-Talleres Octubre, 2011 Permitida su circulación y reproducción en todo o en parte citando la fuente. Resumen ejecutivo Los segmentos de producción mas importantes
Farm. MARIA JOSE SANCHEZ Directora Dirección de Vigilancia de Productos para la Salud- A.N.M.A.T- Argentina
 SERIALIZACIÓN COMO ESTRATEGIAS DE COMBATE CONTRA LA FALSIFICACIÓN Farm. MARIA JOSE SANCHEZ Directora Dirección de Vigilancia de Productos para la Salud- A.N.M.A.T- Argentina msanchez@anmat.gov.ar Buenos
SERIALIZACIÓN COMO ESTRATEGIAS DE COMBATE CONTRA LA FALSIFICACIÓN Farm. MARIA JOSE SANCHEZ Directora Dirección de Vigilancia de Productos para la Salud- A.N.M.A.T- Argentina msanchez@anmat.gov.ar Buenos
LEAN MANAGEMENT. Instituto Lean Management. NUEVOS MODELOS, NUEVO MODELO DE GESTIÓN EMPRESARIAL LEAN TRANSFORMATION PROJECT
 , NUEVOS MODELOS, NUEVO MODELO DE GESTIÓN EMPRESARIAL LEAN TRANSFORMATION PROJECT Instituto Lean Management www.institutolean.org INSTITUTO Misión El Instituto Lean Management de España forma parte de
, NUEVOS MODELOS, NUEVO MODELO DE GESTIÓN EMPRESARIAL LEAN TRANSFORMATION PROJECT Instituto Lean Management www.institutolean.org INSTITUTO Misión El Instituto Lean Management de España forma parte de
3.- Cuáles son los requisitos para el permiso de funcionamiento de Farmacias y botiquines?
 NORMATIVA TÉCNICA SANITARIA PARA EL CONTROL Y FUNCIONAMIENTO DE FARMACIAS Y BOTIQUINES 1.- La Resolución ARCSA 008 2017-JCGO a que establecimientos es aplicable? Esta resolución es aplicable a todas las
NORMATIVA TÉCNICA SANITARIA PARA EL CONTROL Y FUNCIONAMIENTO DE FARMACIAS Y BOTIQUINES 1.- La Resolución ARCSA 008 2017-JCGO a que establecimientos es aplicable? Esta resolución es aplicable a todas las
RETOS EN REGULACIÓN Situación actual y sus proyecciones IX EAMI de Septiembre 2012
 RETOS EN REGULACIÓN Situación actual y sus proyecciones IX EAMI 26-28 de Septiembre 2012 QF ELIZABETH ARMSTRONG JEFA ANAMED Agencia Nacional de Medicamentos ANAMED Le corresponde el control de medicamentos,
RETOS EN REGULACIÓN Situación actual y sus proyecciones IX EAMI 26-28 de Septiembre 2012 QF ELIZABETH ARMSTRONG JEFA ANAMED Agencia Nacional de Medicamentos ANAMED Le corresponde el control de medicamentos,
Nota de prensa. El programa Sanidad en Línea contribuye a situar a España en la vanguardia de la aplicación de las TIC en los servicios de salud
 MINISTERIO DE INDUSTRIA, TURISMO Y COMERCIO MINISTERIO DE SANIDAD Y CONSUMO Nota de prensa Conclusiones del informe Las TIC en el Sistema Nacional de Salud El programa Sanidad en Línea contribuye a situar
MINISTERIO DE INDUSTRIA, TURISMO Y COMERCIO MINISTERIO DE SANIDAD Y CONSUMO Nota de prensa Conclusiones del informe Las TIC en el Sistema Nacional de Salud El programa Sanidad en Línea contribuye a situar
DOCUMENTO DE PREGUNTAS Y RESPUESTAS EN RELACIÓN CON LA IMPORTACIÓN DE PRINCIPIOS ACTIVOS UTILIZADOS EN LA FABRICACIÓN DE MEDICAMENTOS DE USO HUMANO
 DEPARTAMENTO DE INSPECCIÓN Y CONTROL DE MEDICAMENTOS DOCUMENTO DE PREGUNTAS Y RESPUESTAS EN RELACIÓN CON LA IMPORTACIÓN DE PRINCIPIOS ACTIVOS UTILIZADOS EN LA FABRICACIÓN DE MEDICAMENTOS DE USO HUMANO
DEPARTAMENTO DE INSPECCIÓN Y CONTROL DE MEDICAMENTOS DOCUMENTO DE PREGUNTAS Y RESPUESTAS EN RELACIÓN CON LA IMPORTACIÓN DE PRINCIPIOS ACTIVOS UTILIZADOS EN LA FABRICACIÓN DE MEDICAMENTOS DE USO HUMANO
CURSO REGULACION SANITARIA DE PRODUCTOS BIOLOGICOS Y BIOTECNOLOGICOS
 CURSO REGULACION SANITARIA DE PRODUCTOS BIOLOGICOS Y BIOTECNOLOGICOS 1.- Introducción Programa General Fase Virtual de Autoaprendizaje y Fase Presencial Edición 2017 Los medicamentos biológicos y biotecnológicos
CURSO REGULACION SANITARIA DE PRODUCTOS BIOLOGICOS Y BIOTECNOLOGICOS 1.- Introducción Programa General Fase Virtual de Autoaprendizaje y Fase Presencial Edición 2017 Los medicamentos biológicos y biotecnológicos
Gestión de riesgos en la fabricación y distribución de medicamentos
 Santiago de Chile Septiembre 2012 Gestión de riesgos en la fabricación y distribución de medicamentos Belén Escribano Romero Departamento de Inspección y Control de Medicamentos 1 Gestión de riesgos por
Santiago de Chile Septiembre 2012 Gestión de riesgos en la fabricación y distribución de medicamentos Belén Escribano Romero Departamento de Inspección y Control de Medicamentos 1 Gestión de riesgos por
Red o cadena de frío. Conjunto de sistemas logísticos diseñados que comprenden personal, infraestructura, equipos y procedimientos, para mantener los
 Red o cadena de frío. Conjunto de sistemas logísticos diseñados que comprenden personal, infraestructura, equipos y procedimientos, para mantener los productos en condiciones especificas de temperatura
Red o cadena de frío. Conjunto de sistemas logísticos diseñados que comprenden personal, infraestructura, equipos y procedimientos, para mantener los productos en condiciones especificas de temperatura
NUEVOS REGLAMENTOS EUROPEOS DE PRODUCTOS SANITARIOS. CAMBIOS MÁS RELEVANTES Y PERIODOS TRANSITORIOS
 NUEVOS REGLAMENTOS EUROPEOS DE PRODUCTOS SANITARIOS. CAMBIOS MÁS RELEVANTES Y PERIODOS TRANSITORIOS XXV CONGRESO NACIONAL MADRID 2018 M. Carmen Abad Luna Jefe del Departamento de Productos Sanitarios AEMPS
NUEVOS REGLAMENTOS EUROPEOS DE PRODUCTOS SANITARIOS. CAMBIOS MÁS RELEVANTES Y PERIODOS TRANSITORIOS XXV CONGRESO NACIONAL MADRID 2018 M. Carmen Abad Luna Jefe del Departamento de Productos Sanitarios AEMPS
Gestión para la Certificación de. Productos de la Madera y el Mueble
 Gestión para la Certificación de Productos de la Madera y el Mueble Ing. Agr. María Cristina Siri AMBIENTE TECNOLOGICAS PARA LA DISCAPACIDAD CARNES CAUCHO CELULOSA Y PAPEL -CEREALES Y OLEAGINOSAS - CONSTRUCCIONES
Gestión para la Certificación de Productos de la Madera y el Mueble Ing. Agr. María Cristina Siri AMBIENTE TECNOLOGICAS PARA LA DISCAPACIDAD CARNES CAUCHO CELULOSA Y PAPEL -CEREALES Y OLEAGINOSAS - CONSTRUCCIONES
INFORME DE LA COMISIÓN AL PARLAMENTO EUROPEO Y AL CONSEJO
 COMISIÓN EUROPEA Bruselas, 30.3.2015 COM(2015) 138 final INFORME DE LA COMISIÓN AL PARLAMENTO EUROPEO Y AL CONSEJO sobre el ejercicio de los poderes delegados en la Comisión de conformidad con la Directiva
COMISIÓN EUROPEA Bruselas, 30.3.2015 COM(2015) 138 final INFORME DE LA COMISIÓN AL PARLAMENTO EUROPEO Y AL CONSEJO sobre el ejercicio de los poderes delegados en la Comisión de conformidad con la Directiva
Trazabilidad de medicamentos en el Sanatorio Güemes Dra. Silvana Panza - 24 de Octubre de 2013
 Trazabilidad de medicamentos en el Sanatorio Güemes Dra. Silvana Panza - 24 de Octubre de 2013 Oportunidades de trazabilidad Etapas de implementación Factores a tener en cuenta para su implementación.
Trazabilidad de medicamentos en el Sanatorio Güemes Dra. Silvana Panza - 24 de Octubre de 2013 Oportunidades de trazabilidad Etapas de implementación Factores a tener en cuenta para su implementación.
Seminario Internacional de Empresas Ambiental y Socialmente Responsables
 Seminario Internacional de Empresas Ambiental y Socialmente Responsables ESTUDIO DE CASO: MANEJO DE CRISIS" Asociación Nacional de la Industria Química, A.C. Noviembre 17, 2003 Quién debe responder a una
Seminario Internacional de Empresas Ambiental y Socialmente Responsables ESTUDIO DE CASO: MANEJO DE CRISIS" Asociación Nacional de la Industria Química, A.C. Noviembre 17, 2003 Quién debe responder a una
Estructuras de apoyo a los ensayos clínicos en Terapias Avanzadas
 Estructuras de apoyo a los ensayos clínicos en Terapias Avanzadas Natividad Cuende MD, MPH, PhD Directora Ejecutiva Iniciativa Andaluza en Terapias Avanzadas MARCO LEGAL: MEDICAMENTO Imagen MARCO LEGAL:
Estructuras de apoyo a los ensayos clínicos en Terapias Avanzadas Natividad Cuende MD, MPH, PhD Directora Ejecutiva Iniciativa Andaluza en Terapias Avanzadas MARCO LEGAL: MEDICAMENTO Imagen MARCO LEGAL:
PRODUCTOS Y SERVICIOS UTILIZADOS EN LA ADMINISTRACIÓN DISPENSADOR NO
 PRODUCTOS Y SERVICIOS UTILIZADOS EN LA ADMINISTRACIÓN DISPENSADOR NO PRODUCTOS Y SERVICIOS UTILIZADOS EN LA ADMINISTRACIÓN REGULADORES DE PRESIÓN PARA TOMA DE GASES REGULADORES DE PRESIÓN PARA CILINDROS
PRODUCTOS Y SERVICIOS UTILIZADOS EN LA ADMINISTRACIÓN DISPENSADOR NO PRODUCTOS Y SERVICIOS UTILIZADOS EN LA ADMINISTRACIÓN REGULADORES DE PRESIÓN PARA TOMA DE GASES REGULADORES DE PRESIÓN PARA CILINDROS
MINISTERIO DE AMBIENTE, VIVIENDA Y DESARROLLO TERRITORIAL PRESIDENCIA DE LA REPÚBLICA
 MINISTERIO DE AMBIENTE, VIVIENDA Y DESARROLLO TERRITORIAL PRESIDENCIA DE LA REPÚBLICA 1 MINISTERIO DE AMBIENTE, VIVIENDA Y DESARROLLO TERRITORIAL DIRECCIÓN DE LICENCIAS, PERMISOS Y TRÁMITES AMBIENTALES
MINISTERIO DE AMBIENTE, VIVIENDA Y DESARROLLO TERRITORIAL PRESIDENCIA DE LA REPÚBLICA 1 MINISTERIO DE AMBIENTE, VIVIENDA Y DESARROLLO TERRITORIAL DIRECCIÓN DE LICENCIAS, PERMISOS Y TRÁMITES AMBIENTALES
Combate a la Falsificación de Medicamentos PROPUESTA DE UNIDAD EJECUTORA
 GRUPO DE Combate a la Falsificación de Medicamentos PROPUESTA DE UNIDAD EJECUTORA Para implementar las acciones de prevención y combate a la falsificación de medicamentos, se propone un modelo de estructura
GRUPO DE Combate a la Falsificación de Medicamentos PROPUESTA DE UNIDAD EJECUTORA Para implementar las acciones de prevención y combate a la falsificación de medicamentos, se propone un modelo de estructura
El flujo del trabajo del proceso Recursos Humanos y Ambiente de Trabajo se muestra en la figura 17.
 Aplicación de la Evaluación de Desempeño en función del Plan Operativo de Recursos Humanos y Ambiente de Trabajo y actualización del Registro de Recursos Humanos. Aplicación de la Encuesta sobre el Ambiente
Aplicación de la Evaluación de Desempeño en función del Plan Operativo de Recursos Humanos y Ambiente de Trabajo y actualización del Registro de Recursos Humanos. Aplicación de la Encuesta sobre el Ambiente
Real Decreto 110/2015, de 20 de febrero, sobre residuos de aparatos eléctricos y
 Real Decreto 110/2015, de 20 de febrero, sobre residuos de aparatos eléctricos y electrónicos (RAEE) CEOE. Comisión de Desarrollo Sostenible y Medio Ambiente Madrid, 16 de marzo de 2015 INDICE 1. FINALIDAD
Real Decreto 110/2015, de 20 de febrero, sobre residuos de aparatos eléctricos y electrónicos (RAEE) CEOE. Comisión de Desarrollo Sostenible y Medio Ambiente Madrid, 16 de marzo de 2015 INDICE 1. FINALIDAD
INGREDIENTES NATURALES PARA COSMÉTICOS: ACEITES ESENCIALES EN FRANCIA. Parte Tres: Negociación
 INGREDIENTES NATURALES PARA COSMÉTICOS: ACEITES ESENCIALES EN FRANCIA Parte Tres: Negociación PROCESO DE COMPRAS Potenciales clientes y canales de distribución: A través de un importador o mayorista A
INGREDIENTES NATURALES PARA COSMÉTICOS: ACEITES ESENCIALES EN FRANCIA Parte Tres: Negociación PROCESO DE COMPRAS Potenciales clientes y canales de distribución: A través de un importador o mayorista A
Octavo. Se incorpora un nuevo capítulo IX sobre dispositivos de seguridad que figuran en el envase de medicamentos de uso humano.
 Real Decreto por el que se modifica el Real Decreto 1345/2007, de 11 de octubre, por el que se regula el procedimiento de autorización, registro y condiciones de dispensación de los medicamentos de uso
Real Decreto por el que se modifica el Real Decreto 1345/2007, de 11 de octubre, por el que se regula el procedimiento de autorización, registro y condiciones de dispensación de los medicamentos de uso
La modernización administrativa y el desarrollo de la Ley de acceso electrónico de los ciudadanos a los servicios públicosp
 La modernización administrativa y el desarrollo de la Ley de acceso electrónico de los ciudadanos a los servicios públicosp La Universidad del siglo XXI Jornadas de Gerencia Universitaria Zaragoza, 6 de
La modernización administrativa y el desarrollo de la Ley de acceso electrónico de los ciudadanos a los servicios públicosp La Universidad del siglo XXI Jornadas de Gerencia Universitaria Zaragoza, 6 de
«LA MEJOR TERAPIA ES DAR INFORMACIÓN AL PACIENTE Y CREAR UNA NUEVA RELACIÓN MÉDICO FARMACÉUTICO - PACIENTE» (O.M.S.1995)
 CONTENIDO 1. Perfil ocupacional del Tecnólogo en Regencia de Farmacia 1.2. Campo del ejercicio profesional 1.3. Requisitos para el ejercicio profesional 2. Competencias del programa Tecnología en Regencia
CONTENIDO 1. Perfil ocupacional del Tecnólogo en Regencia de Farmacia 1.2. Campo del ejercicio profesional 1.3. Requisitos para el ejercicio profesional 2. Competencias del programa Tecnología en Regencia
División Académica de Informática y Sistemas Licenciatura en Sistemas Computacionales
 Programa elaborado por: PROGRAMA DE ESTUDIO Desarrollo de aplicaciones multiplataforma Programa Educativo: Área de Formación : Licenciatura en Sistemas Computacionales Sustantiva profesional Horas teóricas:
Programa elaborado por: PROGRAMA DE ESTUDIO Desarrollo de aplicaciones multiplataforma Programa Educativo: Área de Formación : Licenciatura en Sistemas Computacionales Sustantiva profesional Horas teóricas:
