Ensayos para la evaluación de la biocompatibilidad según ISO 10993
|
|
|
- Ignacio Paz Torregrosa
- hace 7 años
- Vistas:
Transcripción
1 Ensayos para la evaluación de la biocompatibilidad según ISO Claudia Dei Negri - 29 de Enero de
2
3 Biocompatibilidad y ISO Que es la biocompatibilidad? The ability of a material to perform with an appropriate host response in a specific application The Williams dictionary of Biomaterials, D.F. Williams, 1999 Que significa que un material es biocompatible? El primer descubrimiento de un material biocompatible fue durante la segunda guerra mundial cuando se descubrió que los pilotos heridos por fragmentos de PMMA de las cabinas de los aéreos de combate no tenían reacciones por cuerpos extraños como por ejemplo pasaba con el vidrio Como se puede evaluar si un producto sanitario es biocompatible?
4 Biocompatibilidad y ISO Para qué productos se tiene que evaluar la biocompatibilidad? Qué es la ISO y como se compone? Cómo se aplica la ISO para la evaluación de la biocompatibilidad?
5 Biocompatibilidad y requisitos esenciales 7. Propiedades químicas, físicas y biológicas 7.1. Los productos deberán diseñarse y fabricarse de forma que se garanticen las características y prestaciones contempladas en la parte I, «Requisitos generales», con especial atención a: la elección de los materiales utilizados, especialmente en lo que respecta a la toxicidad y, en su caso, la inflamabilidad; la compatibilidad recíproca entre los materiales utilizados y los tejidos biológicos, células y líquidos corporales, teniendo en cuenta la finalidad prevista del producto ; Los productos deberán diseñarse, fabricarse y acondicionarse de forma que. Deberá prestarse especial atención a los tejidos expuestos y a la duración y frecuencia de la exposición 7.5. Los productos deberán diseñarse y fabricarse de forma que se reduzcan al mínimo los riesgos que se deriven de las sustancias desprendidas por el producto. (DIRECTIVA 93/42/EEC)
6 Biocompatibilidad y requisitos esenciales La evaluación de la biocompatibilidad aplica a todos los productos sanitarios que entran en contacto con el paciente de forma directa o indirecta.
7 Biocompatibilidad y ISO Historia de la ISO : primera descripción de un enfoque sistemático para la evaluación de materiales para uso biológico desarrollada en USA por Autian 1965: primera referencia en la USP 1982: publicación de la norma ASTM F : documentos armonizados entre EEUU, Canada y UK 1992: publicación de la primera edición de la norma ISO : CEN crear herramientas prácticas para que se pudieran aplicar a la legislación Europea de productos sanitarios: la evaluación biológica fue asignada al CEN/TC 206 CEN/TC 206 coopera con ISO/TC : CEN publica la series EN 30993
8 Biocompatibilidad y ISO Hoy: ISO es una serie de normas consolidadas internacional, reconocida en todo el mundo, fiable y en continuo desarrollo Norma horizontal se compone, al día de hoy, de 19 partes distintas Están preparadas en colaboración por el Comité Técnico ISO/TC 194 y el comité técnico CEN/TC 206 Son normas en continuo desarrollo: ISO es una norma voluntaria, pero es muy difícil encontrar una razón para no utilizarla
9 ISO 10993
10 ISO 10993
11 Biocompatibilidad y ISO EN ISO : Es el punto de partida para una completa evaluación. Su enfoque ha evolucionado en el tiempo: Primera edición : Guidance on selection of tests Segunda edición 1997: Evaluation and testing Tercera edición 2003: Evaluation and testing Cuarta edición 2009: Evaluation and testing within a risk management process Enfoque: Checklist Enfoque: Risk management
12 Biocompatibilidad y ISO El objetivo primario de la ISO es la protección de los seres humanos en relación con los posibles riesgos debidos al uso de productos sanitarios Este enfoque combina la revisión de los datos existentes con la selección de los ensayos necesarios. Clasifica el producto sanitario en función de la naturaleza y duración del contacto. Es un método para diseñar una evaluación biológica minimizando el uso de animales en los ensayos.
13 Biocompatibilidad y ISO Un protocolo estructurado de evaluación biológica debería ser llevado a cabo y documentado para cada producto sanitario por un técnico competente y debería considerar la evaluación de la literatura existente. Parte del proceso de diseño es el análisis del riesgo (ISO 14971) La selección de los materiales tiene que considerar las ventajas / desventajas y relevancia de: características fisicoquímicas de los varios posibles materiales datos históricos de uso clínico o datos en humanos datos existentes toxicológicos y de seguridad biológica sobre el producto, los materiales, los productos de degradación y los metabolitos procedimientos de ensayo
14 ISO : PRINCIPIOS GENERALES Riesgos Biológicos Efectos a corto plazo - Toxicidad aguda - Irritación de ojos, piel, mucosas - Sensibilización - Hemocompatibilidad Efectos a largo plazo/efectos tóxicos específicos - Efectos de toxicidad subcrónica y crónica - Genotoxicidad - Carcinogenicidad - Efectos sobre la reproducción Todos los potenciales riesgos se tienen que considerar pero no es necesario ni práctico realizar todos los ensayos para estos riesgos 14
15 ISO : PRINCIPIOS GENERALES La evaluación biológica de un producto sanitario debe tener en cuenta: Las condiciones de exposición del producto sanitarios y sus partes - Naturaleza del contacto cuánto invasivo? - Duración del contacto qué tiempo de contacto? - Frecuencia del contacto qué dosis/duración acumulada? La composición química
16 ISO : PRINCIPIOS GENERALES La evaluación biológica de un producto sanitario debe tener en cuenta: las siguientes características y propiedades del material: material(es) de fabricación aditivo(s), contaminantes de proceso y residuos ISO sustancias lixiviables ISO productos de degradación ISO , 13, -14, -15 otros componentes y sus interacciones en el producto final características físicas del producto(forma, superficie, morfología, porosidad, tamaño de partícula etc.) TS/ISO
17 ISO : PRINCIPIOS GENERALES CHECKLIST
18 ISO : PRINCIPIOS GENERALES Superficie de contacto Piel (sólo superficie de piel intacta) ej. Electrodos, prótesis externas, vendas de compresión, etc. Mucosas (contacto con mucosas): ej. Lentillas, catéteres urinarios, dispositivos intravaginales e intraintestinales, prótesis dentarias, profilácticos, etc. Superficies heridas o comprometidas ej. Apósitos para ulceras, quemaduras etc.
19 ISO : PRINCIPIOS GENERALES Dispositivos de comunicación externa Flujo sanguíneo, indirecto (contacto en un punto y que sirve como conducto para la entrada en el sistema vascular) Ej. equipos de administración de soluciones, equipos de transfusión de sangre, etc. Tejidos/hueso/dentina Ej. Laparoscopios, artroscopios, sistemas de drenaje, cementos dentales, material de obturación dental, grapas para piel, etc. Circulación de la sangre Ej. Catéteres intravasculares, electrodos de marcapasos temporales, tubos y accesorios de diálisis, etc.
20 ISO : PRINCIPIOS GENERALES Productos sanitarios implantables Tejido/ hueso dispositivos principalmente a contacto con hueso Ej. Clavos ortopédicos, placas, prótesis óseas, cementos óseos, etc. dispositivo principalmente a contacto con tejidos y fluidos de los tejidos Ej. Marcapasos, dispositivos de suministro de medicamento, sensores neuromusculares, implantes mamarios, dispositivos intrauterinos, etc. Sangre Ej. Electrodos de marcapasos, válvulas cardiacas, injertos vasculares, catéteres de administración de fármacos internos etc.
21 ISO : PRINCIPIOS GENERALES Categorización por duración del contacto con el cuerpo: exposición limitada < 24 horas exposición prolongada más de 24 horas y menos de 30 días contacto permanente > 30 días Categorías múltiples aplicar los ensayos más rigorosos considerar efectos cumulativos
22 ISO : PRINCIPIOS GENERALES Seleccionar los ensayos sobre la base de toda la información disponible sobre el material utilizado, datos de literatura (de publicaciones científicas y médicas reconocidas), datos de ensayos pre-clínicos y clínicos Documentar la selección de los ensayos Los ensayos se deberían realizar en el producto acabado o en muestras representativas del producto acabado. Tener en cuenta una re-evaluación si hay algún cambio: del producto del uso previsto riesgo de efectos adversos
23 ISO : PRINCIPIOS GENERALES Los ensayos elegidos deberían ser: basados en la aplicación final del producto sensibles, precisos y exactos según GLP / bajo acreditación GLP (?) Análisis y screening in vitro antes de realizar ensayos in vivo Considerar las pruebas pertinentes a la categoría de producto, pero evaluar caso por caso para cada producto sanitario
24 ISO : PRINCIPIOS GENERALES Los ensayos adicionales de caracterización de materiales, extractos, lixiviables se tienen que realizar cuando no hay margen de seguridad suficiente. Para evaluar cuando sean necesarios se puedes tener en cuenta el siguiente árbol de decisiones que nos propone la norma.
25 ISO : PRINCIPIOS GENERALES
26 Necesidad de realizar estudios de degradación? Los estudios de degradación se deberían considerar cuando: - El producto sanitario esta diseñado para ser bioabsorbible - El producto sanitario tiene que ser implantado durante > 30 días - Los materiales podrían ceder contaminantes químicos durante el contacto con el cuerpo.
27 Necesidad de realizar los estudios Tóxico cinéticos (TK)? Los estudios TK se tendrían que considerar cuando: El producto sanitario está diseñado para ser bioabsorbible El dispositivo es un implante permanente y la biodegradación o corrosión es conocida o probable y /o hay migración de sustancias lixiviables Una cantidad considerables de productos de degradación potencialmente tóxicos o reactivos es probable o conocido que se liberan del dispositivos durante su uso clínico.
28 Interpretación de los datos y evaluación general seguridad biológica ISO Asesores expertos que tienen el conocimiento y experiencia necesaria deberían determinar y documentar: 1. La estrategia y el contenido del programa para la evaluación biológica del producto sanitario 2. Los criterios para determinar la aceptabilidad del material en función del uso previsto, en línea con el plan de evaluación de riesgo. 3. La idoneidad de la caracterización de materiales 4. El fundamento de la selección y / o exención de pruebas 5. La interpretación de datos existentes y de los resultados de los ensayos 6. La necesidad de eventuales datos adicionales para completar la evaluación biológica 7. Conclusiones generales de seguridad biológica para el dispositivo médico
29 Casos prácticos
30 Casos prácticos Dispositivo de ortopedia producto sanitario Tipo de contacto: piel intacta Duración del contacto: prolongada Efectos biológicos a evaluar?
31 Casos prácticos
32 Casos prácticos Lubricante vaginal producto sanitario Tipo de contacto: mucosa Duración del contacto: - menor de 24 h - repetida Efectos biológicos a evaluar?
33 Casos prácticos
34 Casos prácticos Implante vascular producto sanitario Tipo de contacto: implante sangre Duración del contacto: permanente Efectos biológicos a evaluar?
35 Casos prácticos
36 Casos prácticos Producto para osteointegración producto sanitario Tipo de contacto: implante hueso Duración del contacto: - permanente? - producto reabsorbible? Efectos biológicos a evaluar?
37 Casos prácticos
38 Gracias Claudia Dei Negri Asesora técnica - Eurofins ClaudiaDeiNegri@eurofins.com Tel
IDENTIFICACIÓN Y CLASIFICACIÓN DE PRODUCTOS PELIGROSOS: SISTEMA GLOBALMENTE ARMONIZADO DE CLASIFICACIÓN Y ETIQUETADO DE PRODUCTOS QUÍMICOS
 IDENTIFICACIÓN Y CLASIFICACIÓN DE PRODUCTOS PELIGROSOS: SISTEMA GLOBALMENTE ARMONIZADO DE CLASIFICACIÓN Y ETIQUETADO DE PRODUCTOS QUÍMICOS 1. Concepto Por Aramis Cardoso El GHS es el Sistema Globalmente
IDENTIFICACIÓN Y CLASIFICACIÓN DE PRODUCTOS PELIGROSOS: SISTEMA GLOBALMENTE ARMONIZADO DE CLASIFICACIÓN Y ETIQUETADO DE PRODUCTOS QUÍMICOS 1. Concepto Por Aramis Cardoso El GHS es el Sistema Globalmente
MATERIALES BIOCOMPATIBLES. Ramírez Ornelas Teresa Urzúa Reyes Daniela Norvit Zacarías Cabello Isela
 MATERIALES BIOCOMPATIBLES Ramírez Ornelas Teresa Urzúa Reyes Daniela Norvit Zacarías Cabello Isela Qué son? Un biomaterial, material biocompatible o material bioaplicable es el material que puede ser utilizado
MATERIALES BIOCOMPATIBLES Ramírez Ornelas Teresa Urzúa Reyes Daniela Norvit Zacarías Cabello Isela Qué son? Un biomaterial, material biocompatible o material bioaplicable es el material que puede ser utilizado
NOTA DE SEGURIDAD SOBRE PRÓTESIS MAMARIAS POLY IMPLANT (PIP)
 SUBDIRECCIÓN GENERAL DE PRODUCTOS SANITARIOS NOTA DE SEGURIDAD SOBRE PRÓTESIS MAMARIAS POLY IMPLANT (PIP) Ref.: 005/Marzo 2010 31 de marzo de 2010 Posible aumento de casos de rotura e inflamaciones locales
SUBDIRECCIÓN GENERAL DE PRODUCTOS SANITARIOS NOTA DE SEGURIDAD SOBRE PRÓTESIS MAMARIAS POLY IMPLANT (PIP) Ref.: 005/Marzo 2010 31 de marzo de 2010 Posible aumento de casos de rotura e inflamaciones locales
Madrid Mayo 2011. Regulación de los Productos Sanitarios
 SESIÓN SEC Madrid Mayo 2011 Regulación de los Productos Sanitarios Mª del Carmen Abad Luna. Subdirectora General de Productos Sanitarios. AEMPS. PRODUCTOS INCLUIDOS EN LA REGULACIÓN DE PS Productos sanitarios
SESIÓN SEC Madrid Mayo 2011 Regulación de los Productos Sanitarios Mª del Carmen Abad Luna. Subdirectora General de Productos Sanitarios. AEMPS. PRODUCTOS INCLUIDOS EN LA REGULACIÓN DE PS Productos sanitarios
Quito Ecuador BIOLOGICAL EVALUATION OF MEDICAL DEVICES. PART 4: SELECTION OF TESTS FOR INTERACTIONS WITH BLOOD (ISO 10993-4:2002, IDT)
 Quito Ecuador NORMA TÉCNICA ECUATORIANA NTE INEN-ISO 10993-4 Primera edición 2014-01 EVALUACIÓN BIOLÓGICA DE PRODUCTOS SANITARIOS. PARTE 4: SELECCIÓN DE LOS ENSAYOS PARA LAS INTERACCIONES CON LA SANGRE
Quito Ecuador NORMA TÉCNICA ECUATORIANA NTE INEN-ISO 10993-4 Primera edición 2014-01 EVALUACIÓN BIOLÓGICA DE PRODUCTOS SANITARIOS. PARTE 4: SELECCIÓN DE LOS ENSAYOS PARA LAS INTERACCIONES CON LA SANGRE
La Respuesta Biológica a los Implantes Ortopédicos. Profesor: Dr.Federico Angel Rodriguez Dr. Aldo Vilchez Villalobos
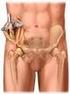 La Respuesta Biológica a los Implantes Ortopédicos Profesor: Dr.Federico Angel Rodriguez Dr. Aldo Vilchez Villalobos Biocompatibilidad Es la capacidad de los materiales para no afectar de manera adversa
La Respuesta Biológica a los Implantes Ortopédicos Profesor: Dr.Federico Angel Rodriguez Dr. Aldo Vilchez Villalobos Biocompatibilidad Es la capacidad de los materiales para no afectar de manera adversa
1. Denominación: 2. Justificación
 BORRADOR DE ORDEN MINISTERIAL POR LA QUE SE ESTABLECEN LOS REQUISITOS PARA LA VERIFICACIÓN DE LOS TÍTULOS QUE HABILITEN PARA EL EJERCICIO DE LA PROFESIÓN DE FARMACÉUTICO. Para la verificación positiva
BORRADOR DE ORDEN MINISTERIAL POR LA QUE SE ESTABLECEN LOS REQUISITOS PARA LA VERIFICACIÓN DE LOS TÍTULOS QUE HABILITEN PARA EL EJERCICIO DE LA PROFESIÓN DE FARMACÉUTICO. Para la verificación positiva
3.- Higiene de manos y Antisepsia cutánea
 Higiene de manos La medida más sencilla y eficaz para reducir la infección asociada a la asistencia sanitaria Transmisión cruzada de microorganismos a través de las manos: Las manos de los profesionales
Higiene de manos La medida más sencilla y eficaz para reducir la infección asociada a la asistencia sanitaria Transmisión cruzada de microorganismos a través de las manos: Las manos de los profesionales
Implicación del farmacéutico en los productos sanitarios. Empezar de cero
 Implicación del farmacéutico en los productos sanitarios Empezar de cero 1 Que es un producto sanitario/producto médico? RD 1591/2009, 1616/2009 Decreto 7/001 Decreto 165/999 Uruguay RD 1591/2009 2 Que
Implicación del farmacéutico en los productos sanitarios Empezar de cero 1 Que es un producto sanitario/producto médico? RD 1591/2009, 1616/2009 Decreto 7/001 Decreto 165/999 Uruguay RD 1591/2009 2 Que
norma española UNE-EN ISO EXTRACTO DEL DOCUMENTO UNE-EN ISO Prótesis de miembros externos y ortesis externas
 norma española UNE-EN ISO 22523 Marzo 2007 TÍTULO Prótesis de miembros externos y ortesis externas Requisitos y métodos de ensayo (ISO 22523:2006) External limb prostheses and external orthoses. Requirements
norma española UNE-EN ISO 22523 Marzo 2007 TÍTULO Prótesis de miembros externos y ortesis externas Requisitos y métodos de ensayo (ISO 22523:2006) External limb prostheses and external orthoses. Requirements
Métodos simplificados de evaluación del riesgo químico: un análisis. Rudolf van der Haar Dpto I+D+i MC MUTUAL
 Métodos simplificados de evaluación del riesgo químico: un análisis Rudolf van der Haar Dpto I+D+i MC MUTUAL rvan@mc-mutual.com Concepto Exposición Posibilidad de contacto Tipo exposición (inhalatoria,
Métodos simplificados de evaluación del riesgo químico: un análisis Rudolf van der Haar Dpto I+D+i MC MUTUAL rvan@mc-mutual.com Concepto Exposición Posibilidad de contacto Tipo exposición (inhalatoria,
ASPECTOS PRÁCTICOS DE LA CLASIFICACIÓN DE LAS MEZCLAS
 ASPECTOS PRÁCTICOS DE LA CLASIFICACIÓN DE LAS MEZCLAS CLP 2105: Hacia un uso seguro de las mezclas 15 de octubre de 2014 Raquel Fernández Sánchez Introducción Obligaciones respecto a las mezclas Principios
ASPECTOS PRÁCTICOS DE LA CLASIFICACIÓN DE LAS MEZCLAS CLP 2105: Hacia un uso seguro de las mezclas 15 de octubre de 2014 Raquel Fernández Sánchez Introducción Obligaciones respecto a las mezclas Principios
MÓDULO 1 CONTENIDO TEÓRICO:
 MÓDULO 1 2-4 de Febrero Diagnóstico y planificación en Odontología Estética: ü Principales parámetros estéticos faciales y dentales. ü La importancia del diagnóstico y planificación en Odontología Estética.
MÓDULO 1 2-4 de Febrero Diagnóstico y planificación en Odontología Estética: ü Principales parámetros estéticos faciales y dentales. ü La importancia del diagnóstico y planificación en Odontología Estética.
NTE INEN-ISO 10993-14 2014-01
 Quito Ecuador NORMA TÉCNICA ECUATORIANA NTE INEN-ISO 10993-14 Primera edición 2014-01 EVALUACIÓN BIOLÓGICA DE PRODUCTOS SANITARIOS. PARTE 14: IDENTIFICACIÓN Y CUANTIFICACIÓN DE LOS PRODUCTOS DE DEGRADACIÓN
Quito Ecuador NORMA TÉCNICA ECUATORIANA NTE INEN-ISO 10993-14 Primera edición 2014-01 EVALUACIÓN BIOLÓGICA DE PRODUCTOS SANITARIOS. PARTE 14: IDENTIFICACIÓN Y CUANTIFICACIÓN DE LOS PRODUCTOS DE DEGRADACIÓN
Quito Ecuador EXTRACTO EVALUACIÓN BIOLÓGICA DE PRODUCTOS SANITARIOS. PARTE 5: ENSAYOS DE CITOTOXICIDAD IN VITRO (ISO 10993-5:2009, IDT)
 Quito Ecuador NORMA TÉCNICA ECUATORIANA NTE INEN-ISO 10993-5 Primera edición 2014-01 EVALUACIÓN BIOLÓGICA DE PRODUCTOS SANITARIOS. PARTE 5: ENSAYOS DE CITOTOXICIDAD IN VITRO (ISO 10993-5:2009, IDT) BIOLOGICAL
Quito Ecuador NORMA TÉCNICA ECUATORIANA NTE INEN-ISO 10993-5 Primera edición 2014-01 EVALUACIÓN BIOLÓGICA DE PRODUCTOS SANITARIOS. PARTE 5: ENSAYOS DE CITOTOXICIDAD IN VITRO (ISO 10993-5:2009, IDT) BIOLOGICAL
INFORMACIÓN VOLUNTARIA DE PRODUCTO basada en el formato de la hoja de seguridad para abrasivos flexibles
 Página 1 de 6 INFORMACIÓN VOLUNTARIA DE PRODUCTO basada en el formato de la hoja de seguridad para abrasivos flexibles 1. Identificación de la sustancia o la mezcla y de la sociedad o la empresa 1.1. Identificaciór
Página 1 de 6 INFORMACIÓN VOLUNTARIA DE PRODUCTO basada en el formato de la hoja de seguridad para abrasivos flexibles 1. Identificación de la sustancia o la mezcla y de la sociedad o la empresa 1.1. Identificaciór
1. Cirugía Bucal: 10 créditos ECTS por asignatura. Tema 5. Anestesia en Cirugía bucal e Implantología.
 TEMARIO POR ASIGNATURA: (CADA TEMA CORRESPONDE A UN MÓDULO) Primer Curso: 1. Cirugía Bucal: 10 créditos ECTS por asignatura. Tema 1. Anatomía bucofacial. Tema 2. Anatomía de los maxilares. Tema 3. Diagnóstico
TEMARIO POR ASIGNATURA: (CADA TEMA CORRESPONDE A UN MÓDULO) Primer Curso: 1. Cirugía Bucal: 10 créditos ECTS por asignatura. Tema 1. Anatomía bucofacial. Tema 2. Anatomía de los maxilares. Tema 3. Diagnóstico
I. INTRODUCCIÓN Y OBJETIVOS.
 I. INTRODUCCIÓN Y OBJETIVOS. 1 I.1. Justificación. Los compósitos son materiales constituidos por más de un componente, los cuales se diferencian en función, forma o composición a escala microscópica,
I. INTRODUCCIÓN Y OBJETIVOS. 1 I.1. Justificación. Los compósitos son materiales constituidos por más de un componente, los cuales se diferencian en función, forma o composición a escala microscópica,
Capítulo 30. Productos farmacéuticos
 Capítulo 30 Productos farmacéuticos Notas. 1. Este Capítulo no comprende: a) los alimentos dietéticos, alimentos enriquecidos, alimentos para diabéticos, complementos alimenticios, bebidas tónicas y el
Capítulo 30 Productos farmacéuticos Notas. 1. Este Capítulo no comprende: a) los alimentos dietéticos, alimentos enriquecidos, alimentos para diabéticos, complementos alimenticios, bebidas tónicas y el
2. Precauciones de Rutina para el Control de Infecciones de Enfermedades Respiratorias
 2. PRECAUCIONES DE RUTINA PARA EL CONTROL DE INFECCIONES DE ENFERMEDADES RESPIRATORIAS 2. Precauciones de Rutina para el Control de Infecciones de Enfermedades Respiratorias Precauciones estándar Las precauciones
2. PRECAUCIONES DE RUTINA PARA EL CONTROL DE INFECCIONES DE ENFERMEDADES RESPIRATORIAS 2. Precauciones de Rutina para el Control de Infecciones de Enfermedades Respiratorias Precauciones estándar Las precauciones
TÉCNICO SUPERIOR UNIVERSITARIO EN TERAPIA FISICA EN COMPETENCIAS PROFESIONALES ASIGNATURA PATOLOGÍA I
 TÉCNICO SUPERIOR UNIVERSITARIO EN TERAPIA FISICA EN COMPETENCIAS PROFESIONALES ASIGNATURA PATOLOGÍA I UNIDADES DE APRENDIZAJE 1. Competencias Integrar el tratamiento terapéutico, a través de la valoración
TÉCNICO SUPERIOR UNIVERSITARIO EN TERAPIA FISICA EN COMPETENCIAS PROFESIONALES ASIGNATURA PATOLOGÍA I UNIDADES DE APRENDIZAJE 1. Competencias Integrar el tratamiento terapéutico, a través de la valoración
Influencia de la evaluación de los efectos de residuos en flora intestinal sobre el IDA de una droga
 Influencia de la evaluación de los efectos de residuos en flora intestinal sobre el IDA de una droga A. Haydée Fernández, DVM, MS, DABT 25 de Septiembre de 2010 Cartagena de Indias, Colombia Como se calcula
Influencia de la evaluación de los efectos de residuos en flora intestinal sobre el IDA de una droga A. Haydée Fernández, DVM, MS, DABT 25 de Septiembre de 2010 Cartagena de Indias, Colombia Como se calcula
EVALUACIÓN DE RIESGOS
 EVALUACIÓN DE RIESGOS Introducción La, la primera de las fases del Análisis de Riesgos, se basa en hechos científicos para, de una forma sistemática, estimar la probabilidad de que ocurra un efecto adverso
EVALUACIÓN DE RIESGOS Introducción La, la primera de las fases del Análisis de Riesgos, se basa en hechos científicos para, de una forma sistemática, estimar la probabilidad de que ocurra un efecto adverso
(Estudios in vivo y estudios in vitro)
 (Estudios in vivo y estudios in vitro) IN VIVO: es la experimentación con un todo, que viven organismos en comparación. Ensayos con animales y ensayos clínicos son dos formas de investigación in vivo.
(Estudios in vivo y estudios in vitro) IN VIVO: es la experimentación con un todo, que viven organismos en comparación. Ensayos con animales y ensayos clínicos son dos formas de investigación in vivo.
Equivalentes terapéuticos
 Versión 1 10 Oct 2006 Equivalentes terapéuticos Por qué surge el concepto de equivalentes terapéuticos? El sistema de autorización de medicamentos por parte de las Agencias Reguladoras provoca que en el
Versión 1 10 Oct 2006 Equivalentes terapéuticos Por qué surge el concepto de equivalentes terapéuticos? El sistema de autorización de medicamentos por parte de las Agencias Reguladoras provoca que en el
Valoración y semiología de patologías del Adulto (1) EU Tania Vásquez S. Enfermería Medico-Quirúrgica
 Valoración y semiología de patologías del Adulto (1) EU Tania Vásquez S. Enfermería Medico-Quirúrgica 1 2016 VALORACIÓN Valoración Es la recogida sistemática y continua, organización, validación y registro
Valoración y semiología de patologías del Adulto (1) EU Tania Vásquez S. Enfermería Medico-Quirúrgica 1 2016 VALORACIÓN Valoración Es la recogida sistemática y continua, organización, validación y registro
PERSPECTIVA DE LA REGULACION DE DISPOSITIVOS MÉDICOS. Héctor Castro Jaramillo Director de Medicamentos y Tecnologías en Salud Noviembre 2016
 PERSPECTIVA DE LA REGULACION DE DISPOSITIVOS MÉDICOS Héctor Castro Jaramillo Director de Medicamentos y Tecnologías en Salud Noviembre 2016 CONTENIDO 2 Los retos ineludibles de nuestro sistema El rol de
PERSPECTIVA DE LA REGULACION DE DISPOSITIVOS MÉDICOS Héctor Castro Jaramillo Director de Medicamentos y Tecnologías en Salud Noviembre 2016 CONTENIDO 2 Los retos ineludibles de nuestro sistema El rol de
240EM132 - Tejidos Vivos y Biointercaras
 Unidad responsable: Unidad que imparte: Curso: Titulación: Créditos ECTS: 2015 240 - ETSEIB - Escuela Técnica Superior de Ingeniería Industrial de Barcelona 702 - CMEM - Departamento de Ciencia de los
Unidad responsable: Unidad que imparte: Curso: Titulación: Créditos ECTS: 2015 240 - ETSEIB - Escuela Técnica Superior de Ingeniería Industrial de Barcelona 702 - CMEM - Departamento de Ciencia de los
Fármaco y Aditivos. Dictaminadores Especializados DIRECCIÓN EJECUTIVA DE AUTORIZACIÓN DE PRODUCTOS Y ESTABLECIMIENTOS
 Fármaco y Aditivos Silvia Reyes Chalico Dictaminadores Especializados Jaime O. Juárez Solís DIRECCIÓN EJECUTIVA DE AUTORIZACIÓN DE PRODUCTOS Y ESTABLECIMIENTOS 1 Toda substancia natural, sintética o biotecnológica
Fármaco y Aditivos Silvia Reyes Chalico Dictaminadores Especializados Jaime O. Juárez Solís DIRECCIÓN EJECUTIVA DE AUTORIZACIÓN DE PRODUCTOS Y ESTABLECIMIENTOS 1 Toda substancia natural, sintética o biotecnológica
Consejo de la Unión Europea Bruselas, 24 de enero de 2017 (OR. en) A: D. Jeppe TRANHOLM-MIKKELSEN, secretario general del Consejo de la Unión Europea
 Consejo de la Unión Europea Bruselas, 24 de enero de 2017 (OR. en) Expediente interinstitucional: 2017/0010 (NLE) 5569/17 ENV 50 COMPET 37 PROPUESTA De: Fecha de recepción: 19 de enero de 2017 secretario
Consejo de la Unión Europea Bruselas, 24 de enero de 2017 (OR. en) Expediente interinstitucional: 2017/0010 (NLE) 5569/17 ENV 50 COMPET 37 PROPUESTA De: Fecha de recepción: 19 de enero de 2017 secretario
Cómo influye la formación específica en el ejercicio de la profesión?
 Bilbao, 16 a 18 de septiembre de 2010 COMPETENCIAS PROFESIONALES DE LOS QUÍMICOS/ INGENIEROS QUÍMICOS XXVIII Jornadas de Ingeniería Química Lejona 16 a 18 de septiembre de 2010 Cómo influye la formación
Bilbao, 16 a 18 de septiembre de 2010 COMPETENCIAS PROFESIONALES DE LOS QUÍMICOS/ INGENIEROS QUÍMICOS XXVIII Jornadas de Ingeniería Química Lejona 16 a 18 de septiembre de 2010 Cómo influye la formación
ANFAH - Comité Técnico
 ANFAH Organización Empresas: Estructura: Presidente Secretario Vicepresidente Comité de Promoción Comité Técnico Comité de Medio Ambiente LA DIRECTIVA EUROPEA DE PRODUCTOS PARA LA CONSTRUCCIÓN (89/106/CEE)
ANFAH Organización Empresas: Estructura: Presidente Secretario Vicepresidente Comité de Promoción Comité Técnico Comité de Medio Ambiente LA DIRECTIVA EUROPEA DE PRODUCTOS PARA LA CONSTRUCCIÓN (89/106/CEE)
Estudios Pre-clínicos y Clínicos
 Estudios Pre-clínicos y Clínicos Rocío Ramírez Herrera Dictaminadoras Especializadas Norma Edith Soto Ruíz DIRECCIÓN EJECUTIVA DE AUTORIZACIÓN DE PRODUCTOS Y ESTABLECIMIENTOS 1 ESTUDIOS PRECLÍNICOS Conjunto
Estudios Pre-clínicos y Clínicos Rocío Ramírez Herrera Dictaminadoras Especializadas Norma Edith Soto Ruíz DIRECCIÓN EJECUTIVA DE AUTORIZACIÓN DE PRODUCTOS Y ESTABLECIMIENTOS 1 ESTUDIOS PRECLÍNICOS Conjunto
La Empresa. PSST Control Operacional de la SST Norma OHSAS 18001:2007
 5.3.7 PSST 4.4.6 01 Control Operacional de la SST La Empresa PSST 4.4.6 01 Control Operacional de la SST Norma OHSAS 18001:2007 REGISTRO DE REVISIONES DE ESTE PROCEDIMIENTO Fecha Revisión Descripción de
5.3.7 PSST 4.4.6 01 Control Operacional de la SST La Empresa PSST 4.4.6 01 Control Operacional de la SST Norma OHSAS 18001:2007 REGISTRO DE REVISIONES DE ESTE PROCEDIMIENTO Fecha Revisión Descripción de
Proceso de Evaluación biológica Ensayos de Biocompatibilidad Dra. Mónica Cameo Directora Biología Aplicada Ciudad Autónoma de Buenos Aires
 Proceso de Evaluación biológica Ensayos de Biocompatibilidad Dra. Mónica Cameo Directora Biología Aplicada Ciudad Autónoma de Buenos Aires PROCESO DE EVALUACIÓN BIOLÓGICA SEGÚN ISO 10993 1.Caracterización
Proceso de Evaluación biológica Ensayos de Biocompatibilidad Dra. Mónica Cameo Directora Biología Aplicada Ciudad Autónoma de Buenos Aires PROCESO DE EVALUACIÓN BIOLÓGICA SEGÚN ISO 10993 1.Caracterización
Norma/Política Precauciones, estándares y uso adecuado de desinfectantes
 01.00 de / Modificación: 01/00 Fecha de Vigencia: 27/12/13 Responsable de Gestión de la norma/política: Dra. Inés Staneloni/ Int. 8165 Mail: maria.staneloni@hospitalitaliano.org.ar Estándar: PCI.9 Referencias:
01.00 de / Modificación: 01/00 Fecha de Vigencia: 27/12/13 Responsable de Gestión de la norma/política: Dra. Inés Staneloni/ Int. 8165 Mail: maria.staneloni@hospitalitaliano.org.ar Estándar: PCI.9 Referencias:
HIGIENE EN EL MEDIO HOSPITALARIO
 HIGIENE EN EL MEDIO HOSPITALARIO Código Nombre Categoría SN_0079 HIGIENE EN EL MEDIO HOSPITALARIO SANIDAD Duración 30 HORAS Modalidad ONLINE Audio SI Vídeo SI Objetivos OFRECER AL PERSONAL DEL CENTRO SANITARIO
HIGIENE EN EL MEDIO HOSPITALARIO Código Nombre Categoría SN_0079 HIGIENE EN EL MEDIO HOSPITALARIO SANIDAD Duración 30 HORAS Modalidad ONLINE Audio SI Vídeo SI Objetivos OFRECER AL PERSONAL DEL CENTRO SANITARIO
Reglamento Sanitario de los Alimentos DS 977/96
 NORMA TÉCNICA- ADMINISTRATIVA SOBRE INCORPORACIÓN A NÓMINA DE EVENTOS BIOTECNOLÓGICOS EN ALIMENTOS DE CONSUMO HUMANO Hugo Schenone C. Depto. Alimentos y Nutrición Reglamento Sanitario de los Alimentos
NORMA TÉCNICA- ADMINISTRATIVA SOBRE INCORPORACIÓN A NÓMINA DE EVENTOS BIOTECNOLÓGICOS EN ALIMENTOS DE CONSUMO HUMANO Hugo Schenone C. Depto. Alimentos y Nutrición Reglamento Sanitario de los Alimentos
Con esta pregunta se desea conocer la cantidad y tipo de residuos peligrosos, que son recolectados en los establecimientos de salud.
 BLOQUE 15 RESIDUOS PELIGROSOS EN ESTABLECIMIENTOS DE SALUD RESIDUOS PELIGROSOS EN ESTABLECIMIENTOS DE SALUD.- Son los residuos generados en establecimientos de salud que tienen propiedades peligrosas y
BLOQUE 15 RESIDUOS PELIGROSOS EN ESTABLECIMIENTOS DE SALUD RESIDUOS PELIGROSOS EN ESTABLECIMIENTOS DE SALUD.- Son los residuos generados en establecimientos de salud que tienen propiedades peligrosas y
MODULO 8. INVESTIGACION EN EL ICTUS
 MODULO 8. INVESTIGACION EN EL ICTUS Dr. Jose Mª Ramírez Moreno Unidad de Ictus. Hospital Universitario Infanta Cristina. Badajoz INDICE: 1. Significado y participación en estudios de investigación en el
MODULO 8. INVESTIGACION EN EL ICTUS Dr. Jose Mª Ramírez Moreno Unidad de Ictus. Hospital Universitario Infanta Cristina. Badajoz INDICE: 1. Significado y participación en estudios de investigación en el
PROCEDIMIENTO PARA LA INSTALACIÓN Y USO DE DESFIBRILADORES PROCEDIMIENTO DE PREVENCIÓN DE RIESGOS LABORALES PROC C12
 Edición: Fecha: Página 1 de 7 PROCEDIMIENTO C12 PROCEDIMIENTO PARA LA INSTALACIÓN Y USO DE DESFIBRILADORES Edición: Fecha: Página 2 de 7 ÍNDICE 1.- Objeto 2.- Alcance 3.- Documentación de referencia 4.-
Edición: Fecha: Página 1 de 7 PROCEDIMIENTO C12 PROCEDIMIENTO PARA LA INSTALACIÓN Y USO DE DESFIBRILADORES Edición: Fecha: Página 2 de 7 ÍNDICE 1.- Objeto 2.- Alcance 3.- Documentación de referencia 4.-
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
Voluntariedad/ Obligatoriedad exámenes de salud
 Voluntariedad/ Obligatoriedad exámenes de salud Maria Jesus Martín Médico de la Unidad de Salud laboral de OSALAN Barakaldo, 10 de junio de 2014 Vitoria, 12 de junio de 2014 Donostia, 17 de junio de 2014
Voluntariedad/ Obligatoriedad exámenes de salud Maria Jesus Martín Médico de la Unidad de Salud laboral de OSALAN Barakaldo, 10 de junio de 2014 Vitoria, 12 de junio de 2014 Donostia, 17 de junio de 2014
LISTADO DE EQUIPOS BIOMÉDICOS DE IMPORTACIÓN YIO ADQUISICIÓN CONTROLADA
 LISTADO DE EQUIPOS BIOMÉDICOS DE IMPORTACIÓN YIO ADQUISICIÓN CONTROLADA Acorde con lo determinado en el artículo DÉCIMO CUARTO de la Resolución N 434 del 2001, a continuación SE detem1ina el listado de
LISTADO DE EQUIPOS BIOMÉDICOS DE IMPORTACIÓN YIO ADQUISICIÓN CONTROLADA Acorde con lo determinado en el artículo DÉCIMO CUARTO de la Resolución N 434 del 2001, a continuación SE detem1ina el listado de
HOSPITAL GENERAL REGIONAL IZTAPALAPA CLÍNICA DE CATÉTERES
 HOSPITAL GENERAL REGIONAL IZTAPALAPA CLÍNICA DE CATÉTERES El Gobierno del Distrito Federal a través de la Secretaria de Salud DF pone en marcha simultáneamente el 21 de Septiembre del 2011, las Clínicas
HOSPITAL GENERAL REGIONAL IZTAPALAPA CLÍNICA DE CATÉTERES El Gobierno del Distrito Federal a través de la Secretaria de Salud DF pone en marcha simultáneamente el 21 de Septiembre del 2011, las Clínicas
Qué significa el Marcado CE en los sistemas de tuberías plásticas?
 Qué significa el Marcado CE en los sistemas de tuberías plásticas? Marzo 2005 Qué significa el Marcado CE INTRODUCCIÓN Este folleto informativo sobre el marcado CE en los sistemas de tuberías plásticas
Qué significa el Marcado CE en los sistemas de tuberías plásticas? Marzo 2005 Qué significa el Marcado CE INTRODUCCIÓN Este folleto informativo sobre el marcado CE en los sistemas de tuberías plásticas
PAVIMENTOS DE EXTERIOR:
 PAVIMENTOS DE EXTERIOR: MARCADO CE Miguel Mateos Área de Construcción División Servicios Tecnológicos Member of XXI Convención de la Federación Española de Pavimentos de Madera 1. RPC-Reglamento (UE) 305/2011
PAVIMENTOS DE EXTERIOR: MARCADO CE Miguel Mateos Área de Construcción División Servicios Tecnológicos Member of XXI Convención de la Federación Española de Pavimentos de Madera 1. RPC-Reglamento (UE) 305/2011
Las Compras Publicas Sostenibles
 Las Compras Publicas Sostenibles 1 Definición de SPP Definición de SPP adoptada por el Grupo de Trabajo: La compra sustentable es el proceso mediante el cual las organizaciones satisfacen sus necesidades
Las Compras Publicas Sostenibles 1 Definición de SPP Definición de SPP adoptada por el Grupo de Trabajo: La compra sustentable es el proceso mediante el cual las organizaciones satisfacen sus necesidades
GUIA TECNICA GUIA PARA LA CARACTERIZACION QUIMICA, FISICO - QUIMICA Y MECANICA DE LOS BIOMATERIALES
 Ministerio de Salud Pública República de Cuba Ciudad de la Habana Centro de Control Estatal Calle 4 #455.Vedado de Equipos Médicos Tel. 32-5072 EMail tx@cceem.sld.cu CCEEM GT 10 1999.12.07 GUIA TECNICA
Ministerio de Salud Pública República de Cuba Ciudad de la Habana Centro de Control Estatal Calle 4 #455.Vedado de Equipos Médicos Tel. 32-5072 EMail tx@cceem.sld.cu CCEEM GT 10 1999.12.07 GUIA TECNICA
SGA. Sistema Globalmente Armonizado para clasificación y etiquetado de productos químicos
 SGA Sistema Globalmente Armonizado para clasificación y etiquetado de productos químicos SGA Sistema Globalmente Armonizado para clasificación y etiquetado de productos químicos SISTEMA GLOBALMENTE ARMONIZADO
SGA Sistema Globalmente Armonizado para clasificación y etiquetado de productos químicos SGA Sistema Globalmente Armonizado para clasificación y etiquetado de productos químicos SISTEMA GLOBALMENTE ARMONIZADO
ANÁLISIS DE RIESGOS EN LA INOCUIDAD DE ALIMENTOS
 ANÁLISIS DE RIESGOS EN LA INOCUIDAD DE ALIMENTOS 1. Presentación La Dirección Ejecutiva de Higiene Alimentaria y Control de Zoonosis DEHAZ Unidad de Evaluación de Riesgos Alimentarios y Rastreabilidad.
ANÁLISIS DE RIESGOS EN LA INOCUIDAD DE ALIMENTOS 1. Presentación La Dirección Ejecutiva de Higiene Alimentaria y Control de Zoonosis DEHAZ Unidad de Evaluación de Riesgos Alimentarios y Rastreabilidad.
Análisis FODA
 Análisis FODA http://www.businessballs.com/swotanalysisfreetemplate.htm El análisis FODA es una herramienta muy útil para comprender todo tipo de situaciones y tomar decisiones en empresas y organizaciones.
Análisis FODA http://www.businessballs.com/swotanalysisfreetemplate.htm El análisis FODA es una herramienta muy útil para comprender todo tipo de situaciones y tomar decisiones en empresas y organizaciones.
TOXICOLOGÍA DE LOS ALIMENTOS GUIA DE ESTUDIO Nº. Tema: PRINCIPIOS DE TOXICOLOGÍA. CURVAS DOSIS - RESPUESTA. ENSAYOS BIOLÓGICOS
 Principios de Toxicología Curvas Dosis-Respuesta-Ensayos Biológicos Año 2015-1 TOXICOLOGÍA DE LOS ALIMENTOS GUIA DE ESTUDIO Nº Tema: PRINCIPIOS DE TOXICOLOGÍA. CURVAS DOSIS - RESPUESTA. ENSAYOS BIOLÓGICOS
Principios de Toxicología Curvas Dosis-Respuesta-Ensayos Biológicos Año 2015-1 TOXICOLOGÍA DE LOS ALIMENTOS GUIA DE ESTUDIO Nº Tema: PRINCIPIOS DE TOXICOLOGÍA. CURVAS DOSIS - RESPUESTA. ENSAYOS BIOLÓGICOS
OBJETIVO ESPECIFICO. Identificar peligros asociados a cada fase o etapa del trabajo y la posterior evaluación de los riesgos.
 ANALISIS DE RIESGO OBJETIVO ESPECIFICO Identificar peligros asociados a cada fase o etapa del trabajo y la posterior evaluación de los riesgos. ADMINISTRACIÓN DEL RIESGO = PREVENCIÓN CONTROL DE ACCIDENTES/
ANALISIS DE RIESGO OBJETIVO ESPECIFICO Identificar peligros asociados a cada fase o etapa del trabajo y la posterior evaluación de los riesgos. ADMINISTRACIÓN DEL RIESGO = PREVENCIÓN CONTROL DE ACCIDENTES/
G2.- Competencia para aplicar los conocimientos adquiridos.
 Competencias generales El egresado del Título de Máster en Técnicas Avanzadas en Química adquirirá al menos las siguientes competencias generales, que desarrollan las competencias básicas previstas en
Competencias generales El egresado del Título de Máster en Técnicas Avanzadas en Química adquirirá al menos las siguientes competencias generales, que desarrollan las competencias básicas previstas en
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. IDENTIFICACIÓN DE LA SUSTANCIA O LA MEZCLA Y DE LA SOCIEDAD O LA EMPRESA
 FICHA DE DATOS DE SEGURIDAD Pagina 1 / 6 1. IDENTIFICACIÓN DE LA SUSTANCIA O LA MEZCLA Y DE LA SOCIEDAD O LA EMPRESA 1.1 Identificador del producto 1.1.1 Nombre comercial del producto 1.2 Usos pertinentes
FICHA DE DATOS DE SEGURIDAD Pagina 1 / 6 1. IDENTIFICACIÓN DE LA SUSTANCIA O LA MEZCLA Y DE LA SOCIEDAD O LA EMPRESA 1.1 Identificador del producto 1.1.1 Nombre comercial del producto 1.2 Usos pertinentes
requisitos en materia de prevención en relación con la compra de productos y equipos
 10 requisitos en materia de prevención en relación con la compra de productos y equipos GUÍA INFORMATIVA Servicio de Prevención Salud Laboral DEFINICIONES Esta guía está dirigida a aquellas personas que
10 requisitos en materia de prevención en relación con la compra de productos y equipos GUÍA INFORMATIVA Servicio de Prevención Salud Laboral DEFINICIONES Esta guía está dirigida a aquellas personas que
Atención Farmacéutica
 Atención Farmacéutica Los farmacéuticos, como parte del Sistema Nacional de Salud, comparten con los pacientes, los médicos, otros profesionales de la salud, y las Autoridades Sanitarias, la misión de
Atención Farmacéutica Los farmacéuticos, como parte del Sistema Nacional de Salud, comparten con los pacientes, los médicos, otros profesionales de la salud, y las Autoridades Sanitarias, la misión de
Sistema de Análisis de Peligros y Puntos de Control Crítico APPCC
 Sistema de Análisis de Peligros y Puntos de Control Crítico APPCC La seguridad de los alimentos se ha convertido en una de las máximas prioridades para el consumidor. El Sistema de Autocontrol es una herramienta
Sistema de Análisis de Peligros y Puntos de Control Crítico APPCC La seguridad de los alimentos se ha convertido en una de las máximas prioridades para el consumidor. El Sistema de Autocontrol es una herramienta
Medicina regenerativa para el tratamiento de
 Medicina regenerativa para el tratamiento de rejuvenecimiento facial TRATAMIENTO CON PLASMA RICO EN FACTORES DE CRECIMIENTO Investigación La medicina regenerativa tiene como objetivo utilizar los propios
Medicina regenerativa para el tratamiento de rejuvenecimiento facial TRATAMIENTO CON PLASMA RICO EN FACTORES DE CRECIMIENTO Investigación La medicina regenerativa tiene como objetivo utilizar los propios
Curso de Curas, Úlceras por Presión y Estomas Manuel Lillo Crespo Supervisor Hospitalización, Clínica Vistahermosa, Alicante
 Curso de Curas, Úlceras por Presión y Estomas Manuel Lillo Crespo Supervisor Hospitalización, Clínica Vistahermosa, Alicante Alicante, 10 y 11 de abril 2015 POR QUÉ UNA UNIDAD DE CURAS Y ESTOMATOTERAPIA?
Curso de Curas, Úlceras por Presión y Estomas Manuel Lillo Crespo Supervisor Hospitalización, Clínica Vistahermosa, Alicante Alicante, 10 y 11 de abril 2015 POR QUÉ UNA UNIDAD DE CURAS Y ESTOMATOTERAPIA?
Nombre de la asignatura: Tratamiento de Aguas Residuales. Créditos: horas teóricas- horas prácticas- total de horas 2-4-6
 Nombre de la asignatura: Tratamiento de Aguas Residuales Créditos: horas teóricas- horas prácticas- total de horas 2-4-6 Aportación al perfil Seleccionar, diseñar, optimizar y operar sistemas de prevención
Nombre de la asignatura: Tratamiento de Aguas Residuales Créditos: horas teóricas- horas prácticas- total de horas 2-4-6 Aportación al perfil Seleccionar, diseñar, optimizar y operar sistemas de prevención
PERFIL PROFESIONAL INGENIERÍA EN TECNOLOGÍA AMBIENTAL. Universidad Politécnica de Durango
 PERFIL PROFESIONAL INGENIERÍA EN TECNOLOGÍA AMBIENTAL Universidad Politécnica de Durango I. Programa Educativo II. Requerimientos del Sector Productivo Ingeniería en Tecnología Ambiental Evaluación de
PERFIL PROFESIONAL INGENIERÍA EN TECNOLOGÍA AMBIENTAL Universidad Politécnica de Durango I. Programa Educativo II. Requerimientos del Sector Productivo Ingeniería en Tecnología Ambiental Evaluación de
DESARROLLO DEL INFORME SOBRE LA SEGURIDAD DE LOS COSMÉTICOS
 DESARROLLO DEL INFORME SOBRE LA SEGURIDAD DE LOS COSMÉTICOS Rosario C. Sánchez S León Productos Cosméticos Departamento de Productos Sanitarios Agencia Española de Medicamentos y Productos Sanitarios 10
DESARROLLO DEL INFORME SOBRE LA SEGURIDAD DE LOS COSMÉTICOS Rosario C. Sánchez S León Productos Cosméticos Departamento de Productos Sanitarios Agencia Española de Medicamentos y Productos Sanitarios 10
GUÍA DIDÁCTICA DEL CURSO
 Escuela de Formación e Investigación en Heridas CURSO REF: X/2015 ULCERAS DE ETIOLOGÍA VENOSA: ABORDAJE Y NUEVOS AVANCES EN EL CUIDADO GUÍA DIDÁCTICA DEL CURSO 1. FUNDAMENTACIÓN Las heridas en las extremidades
Escuela de Formación e Investigación en Heridas CURSO REF: X/2015 ULCERAS DE ETIOLOGÍA VENOSA: ABORDAJE Y NUEVOS AVANCES EN EL CUIDADO GUÍA DIDÁCTICA DEL CURSO 1. FUNDAMENTACIÓN Las heridas en las extremidades
VARIANTES EN EL DISEÑO DE LOS ENSAYOS CLÍNICOS CON ASIGNACIÓN ALEATORIA. Sandra Flores Moreno. AETSA 21 de Diciembre de 2006
 VARIANTES EN EL DISEÑO DE LOS ENSAYOS CLÍNICOS CON ASIGNACIÓN ALEATORIA Sandra Flores Moreno. AETSA 21 de Diciembre de 2006 VARIANTES EN EL DISEÑO DE ENSAYOS CLÍNICOS CON ASIGNACIÓN ALEATORIA *INTRODUCCIÓN
VARIANTES EN EL DISEÑO DE LOS ENSAYOS CLÍNICOS CON ASIGNACIÓN ALEATORIA Sandra Flores Moreno. AETSA 21 de Diciembre de 2006 VARIANTES EN EL DISEÑO DE ENSAYOS CLÍNICOS CON ASIGNACIÓN ALEATORIA *INTRODUCCIÓN
GARANTÍAS EN LAS ADQUISICIONES DE PRODUCTOS SANITARIOS. Dª. Mª Carmen Abad Luna. Subdirectora General de Productos Sanitarios. AEMPS.
 GARANTÍAS EN LAS ADQUISICIONES DE PRODUCTOS SANITARIOS Dª. Mª Carmen Abad Luna. Subdirectora General de Productos Sanitarios. AEMPS. I JORNADA TÉCNICA PRODUCTOS SANITARIOS Y MEDIO AMBIENTE 1 de marzo de
GARANTÍAS EN LAS ADQUISICIONES DE PRODUCTOS SANITARIOS Dª. Mª Carmen Abad Luna. Subdirectora General de Productos Sanitarios. AEMPS. I JORNADA TÉCNICA PRODUCTOS SANITARIOS Y MEDIO AMBIENTE 1 de marzo de
RESIDUOS CITOTOXICOS. Farm. Andrea Imhoff Hospital Dr. O. Alassia
 RESIDUOS CITOTOXICOS Farm. Andrea Imhoff Hospital Dr. O. Alassia RESIDUOS CITOTOXICOS Son aquellos que por sus características y grado de contaminación química o biológica requieren un tratamiento específico
RESIDUOS CITOTOXICOS Farm. Andrea Imhoff Hospital Dr. O. Alassia RESIDUOS CITOTOXICOS Son aquellos que por sus características y grado de contaminación química o biológica requieren un tratamiento específico
Procedimiento RETIRO DE RESIDUOS PELIGROSOS
 Nombre archivo:.doc 1 de 7 Procedimiento RETIRO DE RESIDUOS PELIGROSOS UNIDAD DE PREVENCIÓN DE RIESGOS Diciembre de 2012. Preparado por: Revisado y aprobado por: UPR Mauricio Larco A. 2 de 7 Tabla de contenido
Nombre archivo:.doc 1 de 7 Procedimiento RETIRO DE RESIDUOS PELIGROSOS UNIDAD DE PREVENCIÓN DE RIESGOS Diciembre de 2012. Preparado por: Revisado y aprobado por: UPR Mauricio Larco A. 2 de 7 Tabla de contenido
LA INFECCIÓN RELACIONADA CON LA ATENCIÓN SANITARIA: EXPERIENCIA LEGAL DEL GRUPO ADESLAS
 LA INFECCIÓN RELACIONADA CON LA ATENCIÓN SANITARIA: EXPERIENCIA LEGAL DEL GRUPO ADESLAS Actividad del grupo Adeslas Actividad aseguradora Compañía de Seguros Adeslas, S.A Actividad asistencial Hospital
LA INFECCIÓN RELACIONADA CON LA ATENCIÓN SANITARIA: EXPERIENCIA LEGAL DEL GRUPO ADESLAS Actividad del grupo Adeslas Actividad aseguradora Compañía de Seguros Adeslas, S.A Actividad asistencial Hospital
INDICACIONES PARA LA HIGIENE DE MANOS
 Medicina Preventiva y Salud Pública H.C.U.V. Actualizado 2010 INDICACIONES PARA LA HIGIENE DE MANOS Debe realizarse higiene de las manos por parte del personal sanitario en las siguientes situaciones A.
Medicina Preventiva y Salud Pública H.C.U.V. Actualizado 2010 INDICACIONES PARA LA HIGIENE DE MANOS Debe realizarse higiene de las manos por parte del personal sanitario en las siguientes situaciones A.
(Información) INFORMACIÓN PROCEDENTE DE LAS INSTITUCIONES, ÓRGANOS Y ORGANISMOS DE LA UNIÓN EUROPEA COMISIÓN EUROPEA
 24.1.2013 Diario Oficial de la Unión Europea C 22/1 IV (Información) INFORMACIÓN PROCEDENTE DE LAS INSTITUCIONES, ÓRGANOS Y ORGANISMOS DE LA UNIÓN EUROPEA COMISIÓN EUROPEA Comunicación de la Comisión en
24.1.2013 Diario Oficial de la Unión Europea C 22/1 IV (Información) INFORMACIÓN PROCEDENTE DE LAS INSTITUCIONES, ÓRGANOS Y ORGANISMOS DE LA UNIÓN EUROPEA COMISIÓN EUROPEA Comunicación de la Comisión en
GUÍA FORMATIVA de RESIDENTES Servicio de Farmacología Clínica Hospital Universitario La Princesa
 GUÍA FORMATIVA de RESIDENTES Servicio de Farmacología Clínica Hospital Universitario La Princesa 1. BOE con el programa oficial de la especialidad: BOE con el vigente Programa Oficial de la Especialidad
GUÍA FORMATIVA de RESIDENTES Servicio de Farmacología Clínica Hospital Universitario La Princesa 1. BOE con el programa oficial de la especialidad: BOE con el vigente Programa Oficial de la Especialidad
Manual de uso óptimo de la sangre: análisis del contenido
 Manual de uso óptimo de la sangre: análisis del contenido Dr. Miguel Lozano Molero Servicio de Hemoterapia y Hemostasia Hospital Clínico Universitario Barcelona Organizaciones Europeas Consejo de Europa
Manual de uso óptimo de la sangre: análisis del contenido Dr. Miguel Lozano Molero Servicio de Hemoterapia y Hemostasia Hospital Clínico Universitario Barcelona Organizaciones Europeas Consejo de Europa
Análisis de riesgo y coste-beneficio en las políticas públicas
 Análisis de riesgo y coste-beneficio en las políticas públicas Por qué usar estos métodos Los beneficios de las políticas y los programas públicos tienen un precio: costes impuestos Costes públicos Imposición
Análisis de riesgo y coste-beneficio en las políticas públicas Por qué usar estos métodos Los beneficios de las políticas y los programas públicos tienen un precio: costes impuestos Costes públicos Imposición
INSTRUCTIVO APLICACIÓN DE TERAPIA CON ONDA CORTA
 1. OBJETIVO Establecer la metodología Institucional para la aplicación de Terapia con Onda Corta que permita favorecer en el paciente la regeneración tisular y el alivio del dolor neuromuscular, generando
1. OBJETIVO Establecer la metodología Institucional para la aplicación de Terapia con Onda Corta que permita favorecer en el paciente la regeneración tisular y el alivio del dolor neuromuscular, generando
La Ley de Investigación Biomédica y los CEI.
 Sitges 10-11 Noviembre 2008. La Ley de Investigación Biomédica y los Comités de Etica de la Investigación. (Punto de vista desde un Comité Etico de Investigación Clínica) Cesar Loris. CEICA. Zaragoza.
Sitges 10-11 Noviembre 2008. La Ley de Investigación Biomédica y los Comités de Etica de la Investigación. (Punto de vista desde un Comité Etico de Investigación Clínica) Cesar Loris. CEICA. Zaragoza.
Dirección de Calidad de los Servicios de Salud Programa Nacional de Garantía de Calidad de la Atención Médica
 Estandarización de Procesos Asistenciales - Herramientas- Dra. Nora Castiglia Dra. Victoria Wurcel Lic. Giselle Balaciano Dirección de Calidad de los Servicios de Salud Programa Nacional de Garantía de
Estandarización de Procesos Asistenciales - Herramientas- Dra. Nora Castiglia Dra. Victoria Wurcel Lic. Giselle Balaciano Dirección de Calidad de los Servicios de Salud Programa Nacional de Garantía de
Loop farmacéutico. producen medicamentos destinados al consumo humano con el fin de asegurar la calidad, eficacia y seguridad de los mismos.
 Loop farmacéutico Loop farmacéutico Por: Roxana Cea de Amaya Técnico Sectorial Dirección de Innovación y Calidad En la Industria Farmacéutica Salvadoreña, se deben considerar los requerimientos establecidos
Loop farmacéutico Loop farmacéutico Por: Roxana Cea de Amaya Técnico Sectorial Dirección de Innovación y Calidad En la Industria Farmacéutica Salvadoreña, se deben considerar los requerimientos establecidos
GUÍA PARA LA ADQUISICIÓN DE DISPOSITIVOS MÉDICOS EN LAS INSTITUCIONES DE SALUD Año 2014
 GUÍA PARA LA ADQUISICIÓN DE DISPOSITIVOS MÉDICOS EN LAS INSTITUCIONES DE SALUD Año 2014 CONTENIDO I. INTRODUCCIÓN... 3 II. CONSIDERACIONES GENERALES... 3 III. GLOSARIO... 4 IV. RECOMENDACIONES GENERALES...
GUÍA PARA LA ADQUISICIÓN DE DISPOSITIVOS MÉDICOS EN LAS INSTITUCIONES DE SALUD Año 2014 CONTENIDO I. INTRODUCCIÓN... 3 II. CONSIDERACIONES GENERALES... 3 III. GLOSARIO... 4 IV. RECOMENDACIONES GENERALES...
NTP 137: Etiquetado de sustancias peligrosas
 Página 1 de 8 Documentación NTP 137: Etiquetado de sustancias peligrosas Etiquetage des substances dangereuses Labelling of dangerous substances Redactor: Enrique Gadea Carrera Ldo. en Ciencias Químicas
Página 1 de 8 Documentación NTP 137: Etiquetado de sustancias peligrosas Etiquetage des substances dangereuses Labelling of dangerous substances Redactor: Enrique Gadea Carrera Ldo. en Ciencias Químicas
Curso Complementario C16 EXIGENCIA PARA CONDUCTORES PROFESIONALES DEL TRANSPORTE DE MERCANCIAS Y RESIDUOS PELIGROSOS
 Curso Complementario C16 EXIGENCIA PARA CONDUCTORES PROFESIONALES DEL TRANSPORTE DE MERCANCIAS Y RESIDUOS PELIGROSOS OBJETIVO OBJETIVO DEL CURSO C 16 CONCIENTIZAR Y SENCIBILIZAR AL PERSONAL DE CONDUCTORES
Curso Complementario C16 EXIGENCIA PARA CONDUCTORES PROFESIONALES DEL TRANSPORTE DE MERCANCIAS Y RESIDUOS PELIGROSOS OBJETIVO OBJETIVO DEL CURSO C 16 CONCIENTIZAR Y SENCIBILIZAR AL PERSONAL DE CONDUCTORES
Límites de exposición a agentes químicos. Situación actual
 , Avilés D J é T j d T d D. José Tejedor Traspaderme CNNT Valores Límite ambientales American Conference of Governmental Industrial Higyenists (ACGIH) Publicó en 1938 la primera lista de valores límite
, Avilés D J é T j d T d D. José Tejedor Traspaderme CNNT Valores Límite ambientales American Conference of Governmental Industrial Higyenists (ACGIH) Publicó en 1938 la primera lista de valores límite
PROGRAMA SALUD RENAL UNA GUÍA PARA LOS PACIENTES Y SUS FAMILIAS. Síntomas Insuficiencia Renal // Una Guía para los pacientes y sus familias 1
 PROGRAMA SALUD RENAL UNA GUÍA PARA LOS PACIENTES Y SUS FAMILIAS Síntomas Insuficiencia Renal // Una Guía para los pacientes y sus familias 1 ACERCA DE LA ENFERMEDAD RENAL CRÓNICA Qué son los riñones y
PROGRAMA SALUD RENAL UNA GUÍA PARA LOS PACIENTES Y SUS FAMILIAS Síntomas Insuficiencia Renal // Una Guía para los pacientes y sus familias 1 ACERCA DE LA ENFERMEDAD RENAL CRÓNICA Qué son los riñones y
Normativa que regula la clasificación de los residuos como peligrosos a partir del 1 de junio de 2015
 Normativa que regula la clasificación de los residuos como peligrosos a partir del La normativa comunitaria que regula la clasificación de la peligrosidad de los residuos, ha sido modificada, para adaptarla
Normativa que regula la clasificación de los residuos como peligrosos a partir del La normativa comunitaria que regula la clasificación de la peligrosidad de los residuos, ha sido modificada, para adaptarla
TERMINOLOGÍA ANALÍTICA - PROCESO ANALÍTICO - TÉCNICA ANALÍTICA - MÉTODO ANALÍTICO - PROCEDIMIENTO ANALÍTICO - PROTOCOLO ANALÍTICO
 TERMINOLOGÍA ANALÍTICA - PROCESO ANALÍTICO - TÉCNICA ANALÍTICA - MÉTODO ANALÍTICO - PROCEDIMIENTO ANALÍTICO - PROTOCOLO ANALÍTICO PROCESO ANALÍTICO Conjunto de operaciones analíticas intercaladas que se
TERMINOLOGÍA ANALÍTICA - PROCESO ANALÍTICO - TÉCNICA ANALÍTICA - MÉTODO ANALÍTICO - PROCEDIMIENTO ANALÍTICO - PROTOCOLO ANALÍTICO PROCESO ANALÍTICO Conjunto de operaciones analíticas intercaladas que se
INFORME SECTOR. AIDO ARTES GRÁFICAS. Análisis de ciclo de vida de libros impresos
 2011 INFORME SECTOR www.ecodisseny.net Análisis de ciclo de vida de libros impresos INDICE 1. INTRODUCCIÓN 2. ANÁLISIS DE CICLO DE VIDA 3. ANÁLISIS DE CICLO DE VIDA DEL LIBRO 2 1. INTRODUCCIÓN El cálculo
2011 INFORME SECTOR www.ecodisseny.net Análisis de ciclo de vida de libros impresos INDICE 1. INTRODUCCIÓN 2. ANÁLISIS DE CICLO DE VIDA 3. ANÁLISIS DE CICLO DE VIDA DEL LIBRO 2 1. INTRODUCCIÓN El cálculo
PREPATORIO APLICACIÓN DE PLAGUICIDAS
 PREPATORIO APLICACIÓN DE PLAGUICIDAS 1. Nivel/etapa al que se dirige la actividad: El uso del riego y de la fertilización, así como la lucha contra los enemigos de las plantas, son prácticas agrícolas
PREPATORIO APLICACIÓN DE PLAGUICIDAS 1. Nivel/etapa al que se dirige la actividad: El uso del riego y de la fertilización, así como la lucha contra los enemigos de las plantas, son prácticas agrícolas
EL MARCADO CE APLICADO A LAS VENTANAS. 5 de Mayo de 2009
 EL MARCADO CE APLICADO A LAS VENTANAS 5 de Mayo de 2009 Normativa Técnica Española Unión Europea UE Ley de ordenación de la Edificación. L.O.E. Código Técnico. C.T.E. DPC Marcado CE 2 Marcado CE: Directiva
EL MARCADO CE APLICADO A LAS VENTANAS 5 de Mayo de 2009 Normativa Técnica Española Unión Europea UE Ley de ordenación de la Edificación. L.O.E. Código Técnico. C.T.E. DPC Marcado CE 2 Marcado CE: Directiva
Evaluación y gestión del riesgo ambiental en las sustancias y productos químicos
 Evaluación y gestión del riesgo ambiental en las sustancias y productos químicos Dña. Ana Fresno Coordinadora de Área- S. G. de Calidad del Aire y Medio Ambiente Industrial, MAGRAMA. Buenos días. En primer
Evaluación y gestión del riesgo ambiental en las sustancias y productos químicos Dña. Ana Fresno Coordinadora de Área- S. G. de Calidad del Aire y Medio Ambiente Industrial, MAGRAMA. Buenos días. En primer
D O S S I E R D E P R E N S A D O S S I E R D E P R E N S A D O S S I E R D E P R E N S A
 1 Las instalaciones portuarias concentran hoy en día una gran diversidad de servicios que se desarrollan en el mismo recinto al mismo tiempo. La simultaneidad de estas actividades y las características
1 Las instalaciones portuarias concentran hoy en día una gran diversidad de servicios que se desarrollan en el mismo recinto al mismo tiempo. La simultaneidad de estas actividades y las características
Este documento es un instrumento de documentación y no compromete la responsabilidad de las instituciones
 2009R0041 ES 10.02.2009 000.001 1 Este documento es un instrumento de documentación y no compromete la responsabilidad de las instituciones B REGLAMENTO (CE) N o 41/2009 DE LA COMISIÓN de 20 de enero de
2009R0041 ES 10.02.2009 000.001 1 Este documento es un instrumento de documentación y no compromete la responsabilidad de las instituciones B REGLAMENTO (CE) N o 41/2009 DE LA COMISIÓN de 20 de enero de
"Intercomparaciones y Ensayos de Aptitud"
 "Intercomparaciones y Ensayos de Aptitud" Transferencia del curso llevado a cabo en El Salvador del 24 al 26 de Noviembre 2003. M. Sc. Félix Rodríguez Definición Ensayos de Aptitud Es el uso de comparaciones
"Intercomparaciones y Ensayos de Aptitud" Transferencia del curso llevado a cabo en El Salvador del 24 al 26 de Noviembre 2003. M. Sc. Félix Rodríguez Definición Ensayos de Aptitud Es el uso de comparaciones
Guía del bronceado responsable
 CONSEJOS PARA LOS USUARIOS Guía del bronceado responsable Regulación de los centros de bronceado artificial SI TE BRONCEAS, HAZLO CON GARANTÍAS Establecimiento: SI TE BRONCEAS, HAZLO CON GARANTÍAS INTRODUCCIÓN
CONSEJOS PARA LOS USUARIOS Guía del bronceado responsable Regulación de los centros de bronceado artificial SI TE BRONCEAS, HAZLO CON GARANTÍAS Establecimiento: SI TE BRONCEAS, HAZLO CON GARANTÍAS INTRODUCCIÓN
TÉCNICO SUPERIOR UNIVERSITARIO EN TERAPIA FÍSICA EN COMPETENCIAS PROFESIONALES ASIGNATURA DE PRIMEROS AUXILIOS
 TÉCNICO SUPERIOR UNIVERSITARIO EN TERAPIA FÍSICA EN COMPETENCIAS PROFESIONALES ASIGNATURA DE PRIMEROS AUXILIOS UNIDADES DE APRENDIZAJE 1. Competencias Determinar el tratamiento terapéutico, mediante la
TÉCNICO SUPERIOR UNIVERSITARIO EN TERAPIA FÍSICA EN COMPETENCIAS PROFESIONALES ASIGNATURA DE PRIMEROS AUXILIOS UNIDADES DE APRENDIZAJE 1. Competencias Determinar el tratamiento terapéutico, mediante la
Biomateriales y Biocompatibilidad
 Biomaterial: Material en contacto con el tejido biológico Biocompatibilidad: Cualidad que tiene un biomaterial de no tener efecto tóxico o dañino en un sistema fisiológico. Es una interacción química y
Biomaterial: Material en contacto con el tejido biológico Biocompatibilidad: Cualidad que tiene un biomaterial de no tener efecto tóxico o dañino en un sistema fisiológico. Es una interacción química y
Mejor Curación Mis Células.
 TERAPIA PLAQUETARIA Mejor Curación Mis Células. Totalmente natural, 100% de Ud. Procedimiento holístico simple. Ultima tecnología en curación. Sin químicos, aditivos o sustancias extrañas, sólo las suyas.
TERAPIA PLAQUETARIA Mejor Curación Mis Células. Totalmente natural, 100% de Ud. Procedimiento holístico simple. Ultima tecnología en curación. Sin químicos, aditivos o sustancias extrañas, sólo las suyas.
LA COMISIÓN DE LAS COMUNIDADES EUROPEAS, 0. Visto el Tratado constitutivo de la Comunidad Europea,
 CEE SECCIÓN NÚMERO 1 DISPOSICIONES DE CARÁCTER HORIZONTAL ETIQUETADO Y PUBLICIDAD GENERALES Página 1 REGLAMENTO (CE) Nº 41/2009 DE LA COMISIÓN, DE 20 DE ENERO DE 2009, SOBRE LA COMPOSICIÓN Y ETIQUETADO
CEE SECCIÓN NÚMERO 1 DISPOSICIONES DE CARÁCTER HORIZONTAL ETIQUETADO Y PUBLICIDAD GENERALES Página 1 REGLAMENTO (CE) Nº 41/2009 DE LA COMISIÓN, DE 20 DE ENERO DE 2009, SOBRE LA COMPOSICIÓN Y ETIQUETADO
ANALISIS DE PELIGROS Y PUNTOS CRITICOS DE CONTROL (HACCP)
 ANALISIS DE PELIGROS Y PUNTOS CRITICOS DE CONTROL (HACCP) HACCP (Hazard Analysis Critical Control Point) está enfocado en aquellos aspectos de la preparación de los alimentos que es el área de más importancia
ANALISIS DE PELIGROS Y PUNTOS CRITICOS DE CONTROL (HACCP) HACCP (Hazard Analysis Critical Control Point) está enfocado en aquellos aspectos de la preparación de los alimentos que es el área de más importancia
