2. Recolección, preservación y transporte de las muestras habituales
|
|
|
- Martín Toledo San Segundo
- hace 7 años
- Vistas:
Transcripción
1 RECOLECCION, TRANSPORTE, CONSERVACION Y PROCESAMIENTO DE MUESTRAS PARA ESTUDIOS PARASITOLOGICOS (REFERIRSE A LA GUIA DE TRABAJOS PRACTICOS PARA LOS METODOS DE CONCENTRACION DE MATERIA FECAL) La correcta obtención de muestras es un prerrequisito fundamental para arribar a un diagnóstico adecuado. Para tal fin, deben considerarse los factores que contribuyen al diagnóstico presuntivo de las parasitosis, la preparación física y emocional del paciente para la toma de las muestras, los procedimientos requeridos para su obtención, transporte y preservación y, finalmente, su procesamiento e identificación del agente etiológico. I. ENTEROPARÁSITOS En el caso de la toma de muestra para diagnóstico de enteroparasitosis se deben considerar cuatro abordajes posibles: la obtención de materia fecal, la obtención de muestras perianales, la obtención de biopsias y la obtención de suero o plasma (esto último aplica sólo al diagnóstico serológico de amebosis extraintestinal). Para una mejor orientación con respecto a los posibles agentes etiológicos responsables de la infección intestinal se requiere la elaboración de una ficha tipo. con antecedentes epidemiológicos y clínicos, accesible al laboratorio de diagnóstico parasitológico. Esta ficha debe incluir precisiones sobre los siguientes datos: 1. Nombre y apellido. Edad. Sexo. 2. Lugar de nacimiento. Residencia actual. Residencias anteriores. Viajes. 3. Ocupación laboral. 4. Motivo de la consulta. 5. Sistemas de provisión de agua, de eliminación de excretas y de gestión de residuos en el domicilio. Piso de tierra o material. 6. Hábitos (preparación y consumo de alimentos, geofagia, contacto con el suelo, lavado de manos, etc.). 7. Presencia de animales domésticos y de vectores mecánicos. 8. Familiares/convivientes/contactos con parasitosis actuales o pasadas. 9. Medicación específica administrada actualmente o en forma reciente. 10. Síntomas dominantes (digestivos, prurito, respiratorios, etc.). 11. Evidencias de parasitosis ( antecedente de expulsión de parásitos). 12. Antecedentes de desnutrición e inmunodepresión. 1. Preparación del paciente El paciente debe someterse a una preparación correcta, mínima e indispensable para evitar exámenes falsamente negativos o positivos. Por eso se recomienda evitar, por lo menos tres días antes y durante la recolección de las muestras, la administración oral o rectal de medicamentos que: i. Sean empleados como medio de contraste radiológico (P.ej., compuestos baritados). ii. Alteren el tránsito intestinal (P.ej., carbón vegetal, sales de bismuto, laxantes) iii. Aumenten el contenido lipídico de la materia fecal (P.ej., vaselina líquida) Asimismo, se recomienda suspender, por lo menos tres días antes y durante la recolección de las muestras, la ingestión de alimentos que produzcan abundante residuo no digerible, tales como: i. Fibras vegetales (P.ej., legumbres, frutos de cutícula gruesa) ii. Granos (P.ej., frutas con semillas abundantes y pequeñas, tales como la frutilla u otros frutos del bosque). iii. Polen.
2 2. Recolección, preservación y transporte de las muestras habituales 2.1 Método recomendado por la OMS para estudios coproparasitológicos Recolección Se debe recolectar la materia fecal recién emitida en un frasco con fijador en forma seriada (las muestras únicas tienen una sensibilidad de alrededor del 60%). En casos de que las deposiciones sean formes o blandas se recomienda recolectar 3 muestras en días alternos en un lapso de 7 días, siempre de aquellas zonas más llamativas. En aquellos pacientes con diarrea aguda se recomiendan tomar 3 muestras seriadas, y aquellos con diarrea crónica 6 muestras alternas en un lapso de 12 días. Las materias fecales tienen que ser homogeneizadas por el paciente con una espátula o elemento similar. En todos los casos la cantidad de muestra a recoger será de una cucharita del tamaño de las de té. En caso de emitir heces mucosanguinolentas se recomienda enviarlas en fresco (sin fijador) al laboratorio inmediatamente después de emitidas o conservarlas a 4 ºC y enviarlas dentro de las 24hs. Si se observan estructuras similares a parásitos adultos, se deben recoger en frascos con agua o fijador y remitirlas al laboratorio Preservación Los fijadores habitualmente empleados para la preservación de muestras coproparasitológicas incluyen: formol al 5% en agua o solución fisiológica; alcohol polivinílico, PVA; fenol-alcohol-formol, PAF; acetato de sodio-ácido acético-formol. SAF o; merthiolate-iodo-formol, MIF) en una proporción de 1 parte de heces por cada 3 partes de fijador (aproximadamente el volumen final no debe exceder la mitad del volumen del fijador). No debe estar mezclado con orina u otro líquido Transporte Las muestras fijadas pueden ser transportadas y permanecer utilizables para el diagnóstico por meses a temperatura ambiente o refrigeradas a 4 ºC. Se recomienda dividir la muestra y recogerla por un lado en Formol 5% y por el otro en PVA y/o SAF, debido a que estos fijadores presentan ventajas y desventajas complementarias. El formol preserva mejor morfología de huevos de helmintos y larvas; PVA y SAF son en general más adecuados para realizar coloraciones permanentes de trofozoítos y quistes de protozoarios. El formol, fijador habitual empleado en el diagnóstico coproparasitológico, tiene la ventaja adicional de desodorizar las muestras. 2.2 Examen de heces seriado de 6 muestras con técnica de Deschiens En un frasco de boca ancha con solución de formol al 5% se recolecta una muestra (una cucharadita) de materia fecal por día, de las porciones que llamen más la atención (con moco, pus, sangre, etc.), hasta completar las 6 muestras. No es necesario que sean en días consecutivos. Ventajas del método: i. El formol desodoriza y fija el material. ii. Puede enviarse a distancia. iii. Al ser seriado pone a cubierto las fases negativas de protozoarios (descargas cíclicas de quistes). Desventajas del método: i. El formol no preserva los trofozoítos de protozoarios (en este caso puede reemplazarse por PVA).
3 2.3 Examen de heces frescas: técnica de Neghme Se recolecta una sola muestra de materia fecal en solución fisiológica; debe remitirse rápidamente al laboratorio y procesarse en el día (observación inmediata o fijación para ulterior observación). Ventajas: Se pueden reconocer las formas vegetativas de los protozoarios. Desventajas: No es seriado. 2.4 Métodos especiales de diagnóstico-enterobius vermicularis y Taenia spp Método de Graham-Garaguso para E.vermicularis Preparación del enfermo En todos los casos debe evitarse: i. El aseo de la región anal y perianal antes de la realización de la obtención de la muestra; esto reduce la sensibilidad del método. ii. El uso de talcos, aceites o cremas en la región afectada durante el período que abarque la recolección de las muestras Recolección, preservación y transporte de la muestra. Se entregan 6 portaobjetos con cinta adhesiva de celofán adherido a estos, y 6 espátulas bajalenguas. El método que se describe es adecuado para el diagnóstico de enterobiosis en niños. Se deben tomar 6 muestras seriadas por las mañanas sin previa higiene del margen anal, de la siguiente manera: i. Despegar la cinta adhesiva del portaobjetos y enrollarla en la espátula bajalenguas. La faz adhesiva debe quedar expuesta hacia afuera. El paciente en decúbito ventral, debe separar los glúteos. ii. Se debe aplicar repetidamente la faz adhesiva en la región anal y perianal. iii. Pegar la cinta adhesiva sobre el portaobjetos, a modo de cubreobjetos. En adultos se recomienda reemplazar el procedimiento previo por el que se describe a continuación, para el cual se entregan al paciente 5 gasas dobladas de 5x5 cm, aproximadamente, y un frasco de formol al 5%. Las muestras se toman seriadamente durante 5 días: i. El paciente en decúbito ventral, debe separar los glúteos. ii. Pasar la gasa, previamente humedecida en agua o solución fisiológica, por el ano y la región perianal en forma repetida. iii. Colocar todas las gasas en el mismo frasco de formol. Debe tenerse en cuenta que los huevos de E. vermicularis son altamente infecciosos, por lo que deben extremarse las precauciones de higiene durante y después de la toma de muestra Recolección y preservación de proglótides y adultos de nematodes Ante la sospecha de infección por adultos de nematodes y de proglótides de cestodes intestinales del género Taenia debe proveerse al paciente un frasco con formalina o solución salina. No deben emplearse fijadores como el etanol (frecuentemente empleado en estos casos), ya que opacan la cutícula y dificultan la identificación de la especie. Eventualmente, el paciente puede emplear agua corriente. Si se emplea agua o solución salina la muestra debe ser refrigerada y enviarse sin demora al laboratorio. Debe tenerse en cuenta que el mantenimiento de adultos de nematodes o proglótides en solución fisiológica preserva la viabilidad de los huevos, siendo altamente infecciosos para el humano en el caso de T. solium, H. nana y E. vermicularis.
4 3. Recolección, transporte y procesamiento de muestras para estudios especiales 3.1 Recolección de fluidos y tejidos De acuerdo al cuadro clínico y al diagnóstico presuntivo, las formas evolutivas de los parásitos intestinales pueden ser investigadas en: i. Líquido duodenal. ii. Biopsias de intestino delgado o colon obtenidas mediante endoscopía. iii. Esputo. iv. Filtrado de materia fecal. La obtención de estas muestras, complementarias a los estudios habituales, requiere la intervención del médico especialista, generalmente un gastroenterólogo. Se reservan para situaciones clínicas particulares (P.ej., coproparasitológicos negativos en pacientes con sospecha fundada de giardiosis, amebosis, estrongiloidosis). En el caso de aspirados de líquido duodenal o esputo, estos deben colocarse en un tubo de vidrio o plástico transparente, limpio y seco. La cantidad de la muestra es de 2-5 ml y deberá transportarse de modo inmediato al laboratorio o, en su defecto, refrigerarse a 4 ºC por un tiempo no mayor a las 4 horas. Las biopsias se recogerán en solución fisiológica o paraformaldehído al 4% para su ulterior preparación histológica con fines de microscopía de campo claro, fluorescencia o electrónica. 3.2 Método de la cápsula de Beal o Enterotest Consiste en hacerle tragar al paciente una cápsula con gelatina unida a una cuerda de nylon. La cápsula llega al duodeno y después se la retira y se observa el material mucoso duodenal. Se emplea para identificar trofozoítos de Giardia intestinalis y larvas de Strongyloides stercoralis. 3.3 Recolección de material y detección de antígenos y/o ácidos nucleicos en materia fecal (recomendaciones del CDC) Detección de antígenos de protozoarios en materia fecal: Por regla general deben consultarse las condiciones de recolección y preservación sugeridas por el fabricante del equipo que se empleará para el diagnóstico (materia fecal fresca, fijada o congelada). La detección de coproantígenos parasitarios se realiza tanto mediante ELISA como por inmunocromatografía. Antígenos particulados (p.ej., quistes de protozoarios intestinales) pueden detectarse mediante inmunofluorescencia directa. Se desaconseja el uso de PVA y los métodos de concentración, en el caso de detección de antígenos de Giardia intestinalis mediante ELISA Detección de ácidos nucleicos: Las muestras deben recogerse en ausencia de fijadores y enviarse refrigeradas o congeladas (hielo seco). Como alternativa, las muestras se pueden mezclar en proporción 1:1 con dicromato de potasio o etanol absoluto y enviarse refrigeradas. Para protozoarios intestinales, se recomienda previamente hacer tinciones y examinarlas microscópicamente; en caso de identificar al parásito por morfología, la PCR no se realiza. Es necesario realizar la extracción del ADN de la muestra de materia fecal previo a la realización de la PCR.
5 II. PARÁSITOS DE SANGRE Y TEJIDOS Ficha tipo: Nombre y apellido. Edad. Lugar de nacimiento. Residencia actual y anteriores Tipo de vivienda y características de los alrededores. Viajes recientes. Animales domésticos. Personas parasitadas en la vivienda (si es niño, es de especial interés conocer los antecedentes maternos). Ingesta de carnes mal cocidas. Origen del agua. Reconocimiento de vectores y su presencia en el domicilio o alrededores. Fecha de comienzo de la enfermedad y diagnóstico clínico presuntivo. Preparación del paciente Para la preparación del enfermo que va a ser investigado, ante la sospecha de infección de parásitos de sangre y tejidos. deben cumplirse las normas generales de higiene y antisepsia relativas a la obtención de muestras de sangre y biopsias. Sin embargo, se justifican algunas precisiones: En el caso de muestras de sangre para serología se aplica el requisito de un ayuno mínimo para evitar el exceso de lípidos que pudieran interferir en los métodos de inmunodiagnóstico. Sin embargo, este requisito no es necesario si se obtuviera la muestra de sangre para realizar un diagnóstico directo (P.ej., para tripanosomosis americana, malaria o filariosis). En el caso de biopsias cutáneas o transcuáneas, la piel debe ser adecuadamente lavada con agua y jabón y desinfectada con iodo-povidona o etanol 70 %, antes de realizar el procedimiento quirúrgico (o aspirado en el caso de biopsia de médula ósea o ganglios linfáticos). 1. Recolección, preservación y transporte de las muestras 1.1 Sangre Recolección Punción digital Limpiar del pulpejo del dedo medio (mano izquierda si el paciente es diestro o viceversa), con alcohol 70%, dejar evaporar y punzar el pulpejo con lanceta o aguja estéril (de preferencia en la cara lateral del dedo). En casos pediátricos se puede emplear el mismo procedimiento para punzar el talón Punción venosa Se recogen dos muestras, una sin anticoagulante para estudios serológicos y otra con anticoagulante en condiciones estériles, esta última muestra se empleará para realizar estudios de diagnóstico directo (inocular medios de cultivo o animales), y realizar el examen microscópico en fresco con o sin previa concentración. Las muestras para la determinación directa de un hemoparásito deberán ser remitidas al laboratorio de manera inmediata, a temperatura ambiente (22-25 ºC). Los materiales necesarios incluyen: Agujas y jeringas descartables estériles, algodón, alcohol, capilares heparinizados, tubos de ensayo, heparina, portaobjetos y cubreobjetos, plastilina, centrífuga para microcapilares y/o centrífuga clínica Procesamiento En el caso de investigación de la muestra en fresco, ésta debe ser estudiada de modo inmediato para limitar la pérdida de sensibilidad, debido a la muerte de parásitos. Por el contrario, las muestras fijadas y coloreadas pueden ser enviadas con tiempo al laboratorio de referencia para su evaluación Gota fresca (si se sospecha una tripanosomosis o filariosis) Colocar una gota entre porta y cubre-objeto y revisar microscópicamente el preparado recorriéndolo totalmente en guarda griega. Si la muestra no se observara de
6 manera inmediata, conviene recoger sangre con heparina u otro anticoagulante en un tubo y preparar la gota fresca en el momento de realizar la observación. El reconocimiento de los parásitos se basa en su morfología y movimientos. Los preparados deben ser observados únicamente con objetivos secos (4x-10x-40x). La sensibilidad es baja porque la muestra no está concentrada Extendidos o frotis (para tripanosomosis, filariosis, paludismo y babesiosis) Sobre un extremo de un portaobjeto seco, previamente desengrasado con una mezcla de alcohol-acetona, se coloca una pequeña gota de sangre. La misma se extiende, ayudándose con un segundo portaobjeto que se colocará por delante, pero contactando la gota de sangre en un ángulo de 45 aproximadamente y que servirá para deslizarla formando una fina película. Dejar secar y transportar al laboratorio para su fijación y tinción con colorantes adecuados (May-Grünwald-Giemsa o Wright-Giemsa). Al igual que la gota fresca, esta técnica tiene baja sensibilidad. Sin embargo, permite visualizar detalles morfológicos de los parásitos y ser mantenida como registro permanente Gota gruesa (para tripanosomosis, filariosis y paludismo) Colocar sobre el centro del porta una gota de sangre bastante grande; sobre ella se agregarán 1 a 3 más, según el espesor de las gotas que se extraigan. Con el ángulo de otro portaobjetos efectuar sobre las gotas un movimiento espiral desde el centro hacia la periferia raspando la superficie del portaobjeto. Extender la superficie de las gotas durante uno a dos minutos. De esta manera se desfibrinará la sangre y se extenderá la gota con un diámetro de 2 a 2,5 cm. Dejar secar y enviar al laboratorio para su tinción con Giemsa diluído sin fijación previa. Es una técnica de sensibilidad mayor que las anteriores, pero tiene peor definición de las estructuras parasitarias Microhematocrito Tomar sangre del pulpejo del dedo (o del talón) y cargar varios capilares heparinizados (en general se emplean seis microcapilares por paciente). Sellar un extremo con plastilina o calor y centrifugar a rpm por 5 minutos. Si no se puede proceder a centrifugar inmediatamente, conviene tomar una muestra de sangre heparinizada en tubo y preparar con ella los microhematocritos en el momento de procesarlos. Luego de centrifugado se obtienen 3 fases: plasma, leucocitos y eritrocitos. Los tripomastigotes sedimentan junto con los leucocitos. Se observa microscópicamente la fase leucocitaria entre portaobjetos y cubreobjetos. Es la técnica de elección para el diagnóstico directo de transmisión congénita de enfermedad de Chagas. Tiene una sensibilidad de 90-95% en la infección aguda Xenodiagnóstico (se utiliza para T. cruzi) Se emplean 40 ninfas de T. infestans de tercer estadio, con ayuno previo de 15 días, repartidas en 4 cajas (10 insectos por caja). Las cajas se cubren con una gasa bien fijada y se colocan simultáneamente durante 30 min. en antebrazos y/o muslos del paciente. Se investigará el contenido intestinal de los insectos durante un lapso de días. Este método sólo es usado en casos especiales en los centros de referencia, pues es laborioso y caro, pero su sensibilidad es cercana al 100% en la fase aguda de la infección Detección de antígenos en sangre mediante inmunocromatografía Se emplea para identificar género y especie de Plasmodium (P. vivax y P. falciparum). Sangre obtenida por punción digital es lisada en solución hipotónica, liberando antígenos parasitarios. Los antígenos reaccionan en fase líquida con anticuerpos específicos marcados con oro coloidal. Los complejos inmunes migran en una tira de papel (o dentro de un cassette) y se unen a anticuerpos específicos de
7 captura, unidos covalentemente a la tira de papel. La reacción es positiva si se observan bandas coloreadas, aparte de la correspondiente al control positivo QBC (Quantitative buffy coat o método de naranja de acridina) Es una técnica para detectar infección por Plasmodium y Babesia en muestras de sangre. La sangre se recoge en un tubo capilar con sus paredes internas recubiertas del fluorocromo naranja de acridina. Este fluorocromo se intercala en el ADN. Luego de centrifugar el capilar en una microcentrífuga, se observan los parásitos fluorescentes en los eritrocitos que se concentran debajo de la interfase leucocitaria, empleando un microscopio provisto de luz UV. Esta prueba tiene como ventajas ser más rápida y más sensible que la gota gruesa. 1.2 Tejidos sólidos Recolección Obtención por punción con agujas finas Esta técnica se utiliza habitualmente para el diagnóstico de leishmaniosis visceral, para la cual se obtiene muestras por punción-aspiración generalmente de médula ósea (esternón o cresta ilíaca) y excepcionalmente de bazo, ganglios o hígado Mediante acto quirúrgico a partir de órganos Se pueden obtener muestras de todo tipo de órganos (pulmón, ganglios, hígado, bazo, piel, tejido celular subcutáneo, etc), dependiendo del parásito sospechado Procesamiento Frotis Con los aspirados de médula ósea, ganglio o bazo se pueden realizar extendidos. En estos es posible identificar Leishmania donovani mediante microscopía de campo claro, con los colorantes habituales para hematología, o microscopía de fluorescencia, empleando anticuerpos conjugados con fluorocromos Improntas El material obtenido mediante cirugía (p.ej., ganglios, bazo, hígado) puede emplearse para realizar improntas. Luego de obtener la pieza, se elimina la sangre superficial por aposición sobre papel de filtro. Las improntas se tiñen con colorantes habituales para hematología Cortes histológicos Para microscopia óptica (de campo claro o de fluorescencia) o electrónica. Actualmente, algunos laboratorios también realizan técnicas de biología molecular sobre el material de biopsia (PCR e hibridización in situ), pero su empleo aún no está normatizado.
GUIA DE TRABAJOS PRACTICOS PARASITOLOGIA DEPARTAMENTO DE MICROBIOLOGIA, PARASITOLOGIA E INMUNOLOGIA
 GUIA DE TRABAJOS PRACTICOS PARASITOLOGIA DEPARTAMENTO DE MICROBIOLOGIA, PARASITOLOGIA E INMUNOLOGIA FACULTAD DE MEDICINA UNIVERSIDAD DE BUENOS AIRES 2010 OBJETIVOS Al terminar los Trabajos Prácticos, se
GUIA DE TRABAJOS PRACTICOS PARASITOLOGIA DEPARTAMENTO DE MICROBIOLOGIA, PARASITOLOGIA E INMUNOLOGIA FACULTAD DE MEDICINA UNIVERSIDAD DE BUENOS AIRES 2010 OBJETIVOS Al terminar los Trabajos Prácticos, se
Toma de Muestras Microbiológicas
 Toma de Muestras Microbiológicas MICROBIOLOGÍA CLÍNICA DIAGNÓSTICO DE ENFERMEDADES INFECCIOSAS MUESTRA AISLAMIENTO IDENTIFICACIÓN SENSIBILIDAD A ANTIMICROBIANOS Detección de anticuerpos, antígenos y ácidos
Toma de Muestras Microbiológicas MICROBIOLOGÍA CLÍNICA DIAGNÓSTICO DE ENFERMEDADES INFECCIOSAS MUESTRA AISLAMIENTO IDENTIFICACIÓN SENSIBILIDAD A ANTIMICROBIANOS Detección de anticuerpos, antígenos y ácidos
La muestra idónea es la primera orina de la mañana, ya que permite la multiplicación de bacterias durante la noche.
 INSTRUCCCIONES PARA LA TOMA DE MUESTRA DE ORINAS Y HECES ORINA 1. ORINA PARCIAL Y UROCULTIVO La muestra idónea es la primera orina de la mañana, ya que permite la multiplicación de bacterias durante la
INSTRUCCCIONES PARA LA TOMA DE MUESTRA DE ORINAS Y HECES ORINA 1. ORINA PARCIAL Y UROCULTIVO La muestra idónea es la primera orina de la mañana, ya que permite la multiplicación de bacterias durante la
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS
 PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
TEMA 14. Métodos inmunológicos para la identificación microbiana
 TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
SECCIÓN PARASITOLOGÍA INSTRUCTIVO PARA LA TOMA Y ENVIO DE MUESTRAS. INFECCIÓN POR Plasmodium sp. (Malaria)
 INTRODUCCION SECCIÓN PARASITOLOGÍA INSTRUCTIVO PARA LA TOMA Y ENVIO DE MUESTRAS INFECCIÓN POR Plasmodium sp. (Malaria) La Malaria es una enfermedad parasitaria causada por diferentes especies de Plasmodium
INTRODUCCION SECCIÓN PARASITOLOGÍA INSTRUCTIVO PARA LA TOMA Y ENVIO DE MUESTRAS INFECCIÓN POR Plasmodium sp. (Malaria) La Malaria es una enfermedad parasitaria causada por diferentes especies de Plasmodium
Diagnóstico Parasitológico
 Diagnóstico Parasitológico Dr. Gerardo A. Mirkin Prof. Regular Adjunto Cátedra I de Microbiología y Parasitología UNIVERSIDAD DE BUENOS AIRES FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGÍA, PARASITOLOGÍA
Diagnóstico Parasitológico Dr. Gerardo A. Mirkin Prof. Regular Adjunto Cátedra I de Microbiología y Parasitología UNIVERSIDAD DE BUENOS AIRES FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGÍA, PARASITOLOGÍA
Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención
 Guía de Referencia Rápida Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención Guía de Referencia Rápida
Guía de Referencia Rápida Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención Guía de Referencia Rápida
Universidad de Buenos Aires, Facultad de Medicina. Departamento de Microbiología, Parasitología e Inmunología. Cátedra 1 Microbiología II
 Universidad de Buenos Aires, Facultad de Medicina Departamento de Microbiología, Parasitología e Inmunología Cátedra 1 Microbiología II Teórico 1 Diagnóstico Bacteriológico Cristina Cerquetti ccerquetti@yahoo.com.ar
Universidad de Buenos Aires, Facultad de Medicina Departamento de Microbiología, Parasitología e Inmunología Cátedra 1 Microbiología II Teórico 1 Diagnóstico Bacteriológico Cristina Cerquetti ccerquetti@yahoo.com.ar
EXAMEN EN FRESCO DE HECES Y PRESENCIA DE HUEVOS PRACTICA 3
 EXAMEN EN FRESCO DE HECES Y PRESENCIA DE HUEVOS PRACTICA 3 1. Introducción Examen macroscópico Es importante determinar la consistencia de las heces fecales y clasificarlas en líquidas, blandas o duras,
EXAMEN EN FRESCO DE HECES Y PRESENCIA DE HUEVOS PRACTICA 3 1. Introducción Examen macroscópico Es importante determinar la consistencia de las heces fecales y clasificarlas en líquidas, blandas o duras,
LINEAMIENTOS DE LA UTILIZACION DEL DIAGNÓSTICO Y VIGILANCIA DE LABORATORIO PARA LA ENFERMEDAD DE ZIKA, CHIKUNGUNYA Y DENGUE
 LINEAMIENTOS DE LA UTILIZACION DEL DIAGNÓSTICO Y VIGILANCIA DE LABORATORIO PARA LA ENFERMEDAD DE ZIKA, CHIKUNGUNYA Y DENGUE LABORATORIO NACIONAL DE SALUD Unidad Central de Referencia para la Vigilancia
LINEAMIENTOS DE LA UTILIZACION DEL DIAGNÓSTICO Y VIGILANCIA DE LABORATORIO PARA LA ENFERMEDAD DE ZIKA, CHIKUNGUNYA Y DENGUE LABORATORIO NACIONAL DE SALUD Unidad Central de Referencia para la Vigilancia
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
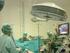 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
Comentario de la encuesta 114: Los resultados fueron sorprendentemente bajos respecto al parásito motivo de la encuesta Dientamoebafragilis.
 Comentario de la encuesta 114: Los resultados fueron sorprendentemente bajos respecto al parásito motivo de la encuesta Dientamoebafragilis. Hemos revisado recientemente el material remitido y del análisis
Comentario de la encuesta 114: Los resultados fueron sorprendentemente bajos respecto al parásito motivo de la encuesta Dientamoebafragilis. Hemos revisado recientemente el material remitido y del análisis
PRÁCTICO N 3. Técnicas para la observación, aislamiento y conservación de microorganismos
 PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
EPIDEMIOLOGÍA y DIAGNÓSTICO DE MALARIA
 EPIDEMIOLOGÍA y DIAGNÓSTICO DE MALARIA Origen de la malaria Origen en África orillas del mediterráneo, India y sudeste asiático Áreas pantanosas de Roma: mal aria, palus, paludis:pantano Hasta 1964: epidemias
EPIDEMIOLOGÍA y DIAGNÓSTICO DE MALARIA Origen de la malaria Origen en África orillas del mediterráneo, India y sudeste asiático Áreas pantanosas de Roma: mal aria, palus, paludis:pantano Hasta 1964: epidemias
PROCESAMIENTO DE MUESTRAS PARA DIAGNÓSTICO DE PARÁSITOS INTESTINALES
 PROCESAMIENTO DE MUESTRAS PARA DIAGNÓSTICO DE Proyecto AECID 2012 Nuevos procedimientos para el diagnóstico de enfermedades olvidadas utilizando tele-microscopía de bajo coste. 1 TABLA DE CONTENIDOS ANTES
PROCESAMIENTO DE MUESTRAS PARA DIAGNÓSTICO DE Proyecto AECID 2012 Nuevos procedimientos para el diagnóstico de enfermedades olvidadas utilizando tele-microscopía de bajo coste. 1 TABLA DE CONTENIDOS ANTES
diferentes sustratos Método de Baermann en embudo y modificación en vaso de precipitado. Rina G. de Kaminsky
 Extracción de larvas de diferentes sustratos Método de Baermann en embudo y modificación en vaso de precipitado. p Rina G. de Kaminsky Método de Baermann Existen algunas variaciones, las dos más utilizadas
Extracción de larvas de diferentes sustratos Método de Baermann en embudo y modificación en vaso de precipitado. p Rina G. de Kaminsky Método de Baermann Existen algunas variaciones, las dos más utilizadas
Enfermedad de Chagas: una realidad en Murcia. Manuel Segovia Hernández 28 de febrero de 2011
 Enfermedad de Chagas: una realidad en Murcia Manuel Segovia Hernández 28 de febrero de 2011 Enfermedades raras Enfermedades raras: Son aquellas enfermedades que tienen una prevalencia (frecuencia) inferior
Enfermedad de Chagas: una realidad en Murcia Manuel Segovia Hernández 28 de febrero de 2011 Enfermedades raras Enfermedades raras: Son aquellas enfermedades que tienen una prevalencia (frecuencia) inferior
Dirección de Redes en Salud Pública
 Dirección de Redes en Salud Pública Recolección de muestras para el estudio de Microcefalias y otras mal formaciones del SNC posiblemente asociadas a infección por virus Zika 22 de Febrero de 2016 Confirmación
Dirección de Redes en Salud Pública Recolección de muestras para el estudio de Microcefalias y otras mal formaciones del SNC posiblemente asociadas a infección por virus Zika 22 de Febrero de 2016 Confirmación
RECOGIDA DE MUESTRAS. Dra. Rocío Martínez Ruiz Microbiología H.U. Puerta de Hierro-Majadahonda
 RECOGIDA DE MUESTRAS Dra. Rocío Martínez Ruiz Microbiología H.U. Puerta de Hierro-Majadahonda RECOGIDA DE MUESTRAS Toda la información diagnóstica que el laboratorio de Microbiología puede proporcionar
RECOGIDA DE MUESTRAS Dra. Rocío Martínez Ruiz Microbiología H.U. Puerta de Hierro-Majadahonda RECOGIDA DE MUESTRAS Toda la información diagnóstica que el laboratorio de Microbiología puede proporcionar
LABORATORIO No. 4 HELMINTOS INTESTINALES
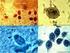 LABORATORIO No. 4 HELMINTOS INTESTINALES PARTE I: NEMÁTODOS (Cont...) Enterobius vermicularis: Gusano de color blanco amarillento, en el extremo anterior se encuentra la boca provista de tres labios y
LABORATORIO No. 4 HELMINTOS INTESTINALES PARTE I: NEMÁTODOS (Cont...) Enterobius vermicularis: Gusano de color blanco amarillento, en el extremo anterior se encuentra la boca provista de tres labios y
TOMA DE MUESTRAS MICROBIOLOGICAS. Dra. Dona Benadof Microbiología Hospital Roberto del Río Comité Vigilancia Infecciones Intrahospitalarias
 TOMA DE MUESTRAS MICROBIOLOGICAS Dra. Dona Benadof Microbiología Hospital Roberto del Río Comité Vigilancia Infecciones Intrahospitalarias INTRODUCCIÓN La confiabilidad de los resultados del estudio microbiológico
TOMA DE MUESTRAS MICROBIOLOGICAS Dra. Dona Benadof Microbiología Hospital Roberto del Río Comité Vigilancia Infecciones Intrahospitalarias INTRODUCCIÓN La confiabilidad de los resultados del estudio microbiológico
PROCESAMIENTO DE MUESTRAS SANGUÍNEAS PARA
 PROCESAMIENTO DE MUESTRAS SANGUÍNEAS PARA DIAGNÓSTICO Proyecto AECID 2012 Nuevos procedimientos para el diagnóstico de enfermedades olvidadas utilizando tele-microscopía de bajo coste. 1 TABLA DE CONTENIDOS
PROCESAMIENTO DE MUESTRAS SANGUÍNEAS PARA DIAGNÓSTICO Proyecto AECID 2012 Nuevos procedimientos para el diagnóstico de enfermedades olvidadas utilizando tele-microscopía de bajo coste. 1 TABLA DE CONTENIDOS
MUESTREO Y DETERMINACIÓN DE LARVAS DE MEJILLÓN CEBRA
 MUESTREO Y DETERMINACIÓN DE LARVAS DE MEJILLÓN CEBRA Octubre 2006 ÍNDICE DE CONTENIDO 1. FUNDAMENTO DEL MÉTODO 2. MATERIAL NECESARIO 3. PREPARACIÓN DE LA MUESTRA 4. PROCEDIMIENTO OPERATIVO 5. IDENTIFICACIÓN
MUESTREO Y DETERMINACIÓN DE LARVAS DE MEJILLÓN CEBRA Octubre 2006 ÍNDICE DE CONTENIDO 1. FUNDAMENTO DEL MÉTODO 2. MATERIAL NECESARIO 3. PREPARACIÓN DE LA MUESTRA 4. PROCEDIMIENTO OPERATIVO 5. IDENTIFICACIÓN
TEMA 9. Métodos ópticos para el diagnóstico de laboratorio de enfermedades infecciosas
 TEMA 9 Métodos ópticos para el diagnóstico de laboratorio de enfermedades infecciosas Tema 9. Métodos ópticos para el diagnóstico de laboratorio de enfermedades infecciosas 1. Examen microscópico del material
TEMA 9 Métodos ópticos para el diagnóstico de laboratorio de enfermedades infecciosas Tema 9. Métodos ópticos para el diagnóstico de laboratorio de enfermedades infecciosas 1. Examen microscópico del material
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt
 Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR
 ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR 1- Prepara un portaobjetos bien limpio con una gota de agua. 2 - Coge una porción pequeña de yogur con un palillo o una aguja enmangada y hacer una extensión
ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR 1- Prepara un portaobjetos bien limpio con una gota de agua. 2 - Coge una porción pequeña de yogur con un palillo o una aguja enmangada y hacer una extensión
ANATOMÍA PATOLÓGICA - HUCA
 HOSPITAL UNIVERSITARIO CENTRAL DE ASTURIAS Celestino Villamil, s/n 33006 Oviedo Teléfono 985108000 106100 Área Sanitaria IV ANATOMÍA PATOLÓGICA - HUCA ESTUDIO BIOPSICO AUTOPSIA CLINICA ESTUDIO CITOLOGICO
HOSPITAL UNIVERSITARIO CENTRAL DE ASTURIAS Celestino Villamil, s/n 33006 Oviedo Teléfono 985108000 106100 Área Sanitaria IV ANATOMÍA PATOLÓGICA - HUCA ESTUDIO BIOPSICO AUTOPSIA CLINICA ESTUDIO CITOLOGICO
URGENCIAS. Servicio de Microbiología
 URGENCIAS Servicio de Microbiología Peticiones urgentes al Servicio de Microbiología 1 I. Consideraciones generales La guardia para las urgencias microbiológicas tiene varios objetivos: 1) Asistencial
URGENCIAS Servicio de Microbiología Peticiones urgentes al Servicio de Microbiología 1 I. Consideraciones generales La guardia para las urgencias microbiológicas tiene varios objetivos: 1) Asistencial
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL
 UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
El Laboratorio en la Vigilancia de Influenza
 El Laboratorio en la Vigilancia de Influenza QBP MANUEL ARROYO ROJAS Laboratorio de Virus Respiratorios del TIPOS DE MUESTRAS Exudado Faríngeo Exudado Nasofaríngeo Aspirado Bronqueoalveolar Suero (pareados)
El Laboratorio en la Vigilancia de Influenza QBP MANUEL ARROYO ROJAS Laboratorio de Virus Respiratorios del TIPOS DE MUESTRAS Exudado Faríngeo Exudado Nasofaríngeo Aspirado Bronqueoalveolar Suero (pareados)
CENTRO NACIONAL DE VIGILANCIA EPIDEMIOLOGICA INSTITUTO DE DIAGNOSTICO Y REFERENCIA EPIDEMIOLOGICOS
 CENTRO NACIONAL DE VIGILANCIA EPIDEMIOLOGICA INSTITUTO DE DIAGNOSTICO Y REFERENCIA EPIDEMIOLOGICOS DIAGNOSTICO POR LABORATORIO DEL VIRUS DEL OESTE DEL NILO Participantes José Carmen Gudiño Rita Flores
CENTRO NACIONAL DE VIGILANCIA EPIDEMIOLOGICA INSTITUTO DE DIAGNOSTICO Y REFERENCIA EPIDEMIOLOGICOS DIAGNOSTICO POR LABORATORIO DEL VIRUS DEL OESTE DEL NILO Participantes José Carmen Gudiño Rita Flores
PRACTICA DE LABORATORIO PROTOZOOS Y HELMINTOS INTESTINALES
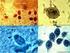 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDACTICA DE MICROBIOLOGÍA AÑO 2015 PRACTICA DE LABORATORIO PROTOZOOS Y HELMINTOS INTESTINALES INTRODUCCIÓN Dra. Sindy Vanessa
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDACTICA DE MICROBIOLOGÍA AÑO 2015 PRACTICA DE LABORATORIO PROTOZOOS Y HELMINTOS INTESTINALES INTRODUCCIÓN Dra. Sindy Vanessa
Trabajo Práctico N 3. Reconocimiento de sustancias ácidas, básicas y neutras. mediante el empleo de indicadores químicos.
 Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
SANGRE ENTERA: Hematología. Parásitos hemáticos
 SANGRE ENTERA: Hematología Parásitos hemáticos Extraer la sangre de la vena evitando la hemólisis y llenar el tubo hasta el límite aconsejado. Agitar el tubo con suavidad invirtiéndolo de 10 a 20 veces
SANGRE ENTERA: Hematología Parásitos hemáticos Extraer la sangre de la vena evitando la hemólisis y llenar el tubo hasta el límite aconsejado. Agitar el tubo con suavidad invirtiéndolo de 10 a 20 veces
TRATAMIENTO Y RECOGIDA DE MUESTRAS EN EL LABORATORIO
 TRATAMIENTO Y RECOGIDA DE MUESTRAS EN EL LABORATORIO GEMA GÓMEZ LAJARA TEL TEL SERVICIO SERVICIO DE DE LABORATORIO LABORATORIO HOSPITAL SANTA BARBARA. PUERTOLLANO. HOSPITAL SANTA BARBARA. PUERTOLLANO.
TRATAMIENTO Y RECOGIDA DE MUESTRAS EN EL LABORATORIO GEMA GÓMEZ LAJARA TEL TEL SERVICIO SERVICIO DE DE LABORATORIO LABORATORIO HOSPITAL SANTA BARBARA. PUERTOLLANO. HOSPITAL SANTA BARBARA. PUERTOLLANO.
COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS BIOLOGÍA I ACTIVIDAD EXPERIMENTAL NUM
 DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS BIOLOGÍA I ACTIVIDAD EXPERIMENTAL NUM. 2 ESTRUCTURA CELULAR (BLOLQUE III) INTRODUCCIÓN La célula es la unidad anatómica y fisiológica de los
DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS BIOLOGÍA I ACTIVIDAD EXPERIMENTAL NUM. 2 ESTRUCTURA CELULAR (BLOLQUE III) INTRODUCCIÓN La célula es la unidad anatómica y fisiológica de los
ENFERMEDADES TRANSMITIDAS POR ALIMENTOS
 ENFERMEDADES TRANSMITIDAS POR ALIMENTOS Melany Aguirre Diana Rivera Christopher Delbrey INTRODUCCIÓN En esta presentación estaremos presentando las siguientes enfermedades transmitidas por alimentos: Salmonelosis,
ENFERMEDADES TRANSMITIDAS POR ALIMENTOS Melany Aguirre Diana Rivera Christopher Delbrey INTRODUCCIÓN En esta presentación estaremos presentando las siguientes enfermedades transmitidas por alimentos: Salmonelosis,
ESTUDIO PARASITOLOGICO DE HECES.
 ESTUDIO PARASITOLOGICO DE HECES. DE MUESTRAS. A:PREPARACIÓN 3 DÍAS ANTES DE LA RECOGIDA DE LAS HECES DEBE SUPRIMIRSE: 1. MEDICAMENTOS QUE CONTENGAN CARBÓN VEGETAL, SALES DE BISMUTO, DE MAGNESIO, CAOLÍN,
ESTUDIO PARASITOLOGICO DE HECES. DE MUESTRAS. A:PREPARACIÓN 3 DÍAS ANTES DE LA RECOGIDA DE LAS HECES DEBE SUPRIMIRSE: 1. MEDICAMENTOS QUE CONTENGAN CARBÓN VEGETAL, SALES DE BISMUTO, DE MAGNESIO, CAOLÍN,
TÉCNICAS DE CONTROL PARASITOLÓGICO DE LOS ALIMENTOS
 TÉCNICAS DE CONTROL PARASITOLÓGICO DE LOS ALIMENTOS Parásitos en Frutas y Vegetales Dr. Jose E. Piñero Barroso Existencia de parásitos intestinales en hortalizas que se comercializan en la ciudad de Corrientes,
TÉCNICAS DE CONTROL PARASITOLÓGICO DE LOS ALIMENTOS Parásitos en Frutas y Vegetales Dr. Jose E. Piñero Barroso Existencia de parásitos intestinales en hortalizas que se comercializan en la ciudad de Corrientes,
6.Prevención de la salud. Giardiasis
 6 6.Prevención de la salud Giardiasis La giardiasis es una enfermedad parasitaria que afecta al intestino y que produce diarrea. Está producida por un parásito microscópico unicelular que vive en el intestino
6 6.Prevención de la salud Giardiasis La giardiasis es una enfermedad parasitaria que afecta al intestino y que produce diarrea. Está producida por un parásito microscópico unicelular que vive en el intestino
FIEBRE HEMORRÁGICA ARGENTINA:
 FIEBRE HEMORRÁGICA ARGENTINA: PROCEDIMIENTO PARA LA VIGILANCIA EPIDEMIOLÓGICA A TRAVÉS DEL SISTEMA NACIONAL DE VIGILANCIA LABORATORIAL SIVILA-SNVS GUIA PARA LA NOTIFICACIÓN, INTERPRETACIÓN DE RESULTADOS,
FIEBRE HEMORRÁGICA ARGENTINA: PROCEDIMIENTO PARA LA VIGILANCIA EPIDEMIOLÓGICA A TRAVÉS DEL SISTEMA NACIONAL DE VIGILANCIA LABORATORIAL SIVILA-SNVS GUIA PARA LA NOTIFICACIÓN, INTERPRETACIÓN DE RESULTADOS,
EJERCICIOS: PREGUNTAS
 ATLAS de H I STOLOGÍA VEGETAL y AN I M AL TÉCNICAS HISTOLÓGICAS EJERCICIOS: PREGUNTAS Manuel Megías, Pilar Molist, Manuel A. Pombal, Manuel Departamento de Biología Funcional y Ciencias de la Salud. Facultad
ATLAS de H I STOLOGÍA VEGETAL y AN I M AL TÉCNICAS HISTOLÓGICAS EJERCICIOS: PREGUNTAS Manuel Megías, Pilar Molist, Manuel A. Pombal, Manuel Departamento de Biología Funcional y Ciencias de la Salud. Facultad
LABORATORIO No. 3 HELMINTOS INTESTINALES
 LABORATORIO No. 3 HELMINTOS INTESTINALES PARTE I: NEMÁTODOS (Cont...) Uncinarias: Se conoce con este nombre principalmente dos parásitos: Necator americanus y Ancylostoma duodenale entre estos adultos
LABORATORIO No. 3 HELMINTOS INTESTINALES PARTE I: NEMÁTODOS (Cont...) Uncinarias: Se conoce con este nombre principalmente dos parásitos: Necator americanus y Ancylostoma duodenale entre estos adultos
LIMPIEZA Y DESINFECCION
 PAGINA: 1 de 7 1. DEFINICION: Es el procedimiento, mediante el cual son eliminados los diferentes desechos generados en los procesos de recolección y procesamiento de muestras; y además se describe el
PAGINA: 1 de 7 1. DEFINICION: Es el procedimiento, mediante el cual son eliminados los diferentes desechos generados en los procesos de recolección y procesamiento de muestras; y además se describe el
Instructivo. Requisitos para el envío de muestras y cultivos fúngicos
 Página 1 de 5 1.- PROPÓSITO: Describir las condiciones para el envío de muestras y cultivos fúngicos al Departamento Micología. 2.- RESPONSABLES: Usuarios del servicio de Diagnóstico Referencial 3.- DESCRIPCIÓN:
Página 1 de 5 1.- PROPÓSITO: Describir las condiciones para el envío de muestras y cultivos fúngicos al Departamento Micología. 2.- RESPONSABLES: Usuarios del servicio de Diagnóstico Referencial 3.- DESCRIPCIÓN:
114. Señala a continuación, sistemas de eliminación de líquidos: a) Pulmones. b) Vómitos. c) Intestino. d) Todos son sistemas de eliminación.
 1 111. En condiciones normales el cuerpo elimina un volumen de líquido que oscila entre: a) 2400 y 2500 ml. b) 2300 y 2500 ml. c) 2300 y 2600 ml. d) 2400 y 2700 ml. 112. Qué es el balance?: a) Es el resultado
1 111. En condiciones normales el cuerpo elimina un volumen de líquido que oscila entre: a) 2400 y 2500 ml. b) 2300 y 2500 ml. c) 2300 y 2600 ml. d) 2400 y 2700 ml. 112. Qué es el balance?: a) Es el resultado
Extracción de Sangre Venosa Periférica
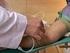 Extracción de Sangre Venosa Periférica Introducción La extracción venosa de sangre es un proceso muy acequiado en el análisis biológico dado que es posible detectar diversas enfermedades o condiciones
Extracción de Sangre Venosa Periférica Introducción La extracción venosa de sangre es un proceso muy acequiado en el análisis biológico dado que es posible detectar diversas enfermedades o condiciones
ABRILLANTADOR SUELOS PIZARRA A-4
 FICHA DE SEGURIDAD Fecha de revisión: 7-02-07. 1. Identificación del preparado y de la empresa Descripción del producto: Abrillantador metalizante suelos pizarra A-4. Uso: Emulsión autobrillante para abrillantar
FICHA DE SEGURIDAD Fecha de revisión: 7-02-07. 1. Identificación del preparado y de la empresa Descripción del producto: Abrillantador metalizante suelos pizarra A-4. Uso: Emulsión autobrillante para abrillantar
EXTRACTOS Y TINTURAS. María Eugenia Ávila M. Q. F. Directora Técnica Y Jefe de Producción LABFARVE
 EXTRACTOS Y TINTURAS María Eugenia Ávila M. Q. F. Directora Técnica Y Jefe de Producción LABFARVE EXTRACCIÓN Es el proceso opuesto a la deshidratación o secado de la planta. Generalmente se utilizan líquidos
EXTRACTOS Y TINTURAS María Eugenia Ávila M. Q. F. Directora Técnica Y Jefe de Producción LABFARVE EXTRACCIÓN Es el proceso opuesto a la deshidratación o secado de la planta. Generalmente se utilizan líquidos
FILTRO DE MESA CON VELAS DE CERÁMICA Y PREFILTRO DE ARENA UNIDAD DE APOYO TÉCNICO PARA EL SANEAMIENTO BÁSICO DEL ÁREA RURAL (UNATSABAR)
 UNIDAD DE APOYO TÉCNICO PARA EL SANEAMIENTO BÁSICO DEL ÁREA RURAL (UNATSABAR) FILTRO DE MESA CON VELAS DE CERÁMICA Y PREFILTRO DE ARENA GUÍA DE CONSTRUCCIÓN, OPERACIÓN Y MANTENIMIENTO Centro Panamericano
UNIDAD DE APOYO TÉCNICO PARA EL SANEAMIENTO BÁSICO DEL ÁREA RURAL (UNATSABAR) FILTRO DE MESA CON VELAS DE CERÁMICA Y PREFILTRO DE ARENA GUÍA DE CONSTRUCCIÓN, OPERACIÓN Y MANTENIMIENTO Centro Panamericano
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
CONTENIDO PROGRAMÁTICO TEÓRICO
 Universidad Central de Venezuela Facultad de Ciencias Escuela de Biología Programa de la asignatura PARASITOLOGIA Tipo de asignatura: Electiva Código: 1620 Unidades de crédito: 5 Requisitos: Horas semana:
Universidad Central de Venezuela Facultad de Ciencias Escuela de Biología Programa de la asignatura PARASITOLOGIA Tipo de asignatura: Electiva Código: 1620 Unidades de crédito: 5 Requisitos: Horas semana:
XX JORNADES SCMIMC LLEIDA 2011
 XX JORNADES logo1 SCMIMC LLEIDA 2011 Infeccions Importades. Cas Clínic. Juan Cabezos Unitat de Malalties Importades i Salut Internacional Drassanes. 1 EOSINOFILIA Se define como una cifra igual o superior
XX JORNADES logo1 SCMIMC LLEIDA 2011 Infeccions Importades. Cas Clínic. Juan Cabezos Unitat de Malalties Importades i Salut Internacional Drassanes. 1 EOSINOFILIA Se define como una cifra igual o superior
Necesidad de eliminación fecal.
 Necesidad de eliminación fecal. Eliminación fecal. Proceso de evacuación del contenido Se produce desde varias veces al día hasta sólo dos o tres veces a la semana. Necesidad de eliminación fecal. 1 Necesidad
Necesidad de eliminación fecal. Eliminación fecal. Proceso de evacuación del contenido Se produce desde varias veces al día hasta sólo dos o tres veces a la semana. Necesidad de eliminación fecal. 1 Necesidad
Protocolo para la toma de muestras de suelo para diagnóstico nematológico
 Protocolo para la toma de muestras de suelo para diagnóstico nematológico Tomador de suelo o auger Laboratori de Sanitat Vegetal Conselleria d Agricultura i Pesca de les illes Balears Toma de muestras
Protocolo para la toma de muestras de suelo para diagnóstico nematológico Tomador de suelo o auger Laboratori de Sanitat Vegetal Conselleria d Agricultura i Pesca de les illes Balears Toma de muestras
CÓMO... Tomar Muestras de Tejido para Histopatología
 para Histopatología Por qué se deben tomar muestras de tejido para histopatología? El tomar muestras de tejido para histopatología es una manera barata y rápida de obtener información adicional importante
para Histopatología Por qué se deben tomar muestras de tejido para histopatología? El tomar muestras de tejido para histopatología es una manera barata y rápida de obtener información adicional importante
V Olimpiada Española de Biología: Fase Nacional
 Código de Identificación 4 últimos dígitos- letra DNI V Olimpiada Española de Biología: Fase Nacional PRÁCTICA 3: IDENTIFICACIÓN DE POLEN Y SUS RELACIONES CON DISTINTOS TIPOS DE POLINIZACIÓN. USO DEL MICROSCOPIO
Código de Identificación 4 últimos dígitos- letra DNI V Olimpiada Española de Biología: Fase Nacional PRÁCTICA 3: IDENTIFICACIÓN DE POLEN Y SUS RELACIONES CON DISTINTOS TIPOS DE POLINIZACIÓN. USO DEL MICROSCOPIO
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
 EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
LABORATORIO CLINICO Y BIOMEDICO
 Curso de TECNICO SUPERIOR EN LABORATORIO CLINICO Y BIOMEDICO TECNICO SUPERIOR EN LABORATORIO CLINICO Y BIOMEDICO Para qué te capacita Los estudios de Técnico Superior en Laboratorio Clínico y Biomédico
Curso de TECNICO SUPERIOR EN LABORATORIO CLINICO Y BIOMEDICO TECNICO SUPERIOR EN LABORATORIO CLINICO Y BIOMEDICO Para qué te capacita Los estudios de Técnico Superior en Laboratorio Clínico y Biomédico
Hematología y Hemostasia
 La División Veterinaria para Pequeñas Especies de Livexlab pone a disposición de su clientela el siguiente portafolio de servicios. Pequeñas Especies Catálogo 2011 precios y servicios vigentes a partir
La División Veterinaria para Pequeñas Especies de Livexlab pone a disposición de su clientela el siguiente portafolio de servicios. Pequeñas Especies Catálogo 2011 precios y servicios vigentes a partir
Comentarios de la Encuesta 100
 Comentarios de la Encuesta 100 La encuesta 100 tenía dos parásitos motivo de la misma, a saber: quistes de Entamoeba coli y quistes de Enteromonas hominis. Un 76,3% de los participantes ha respondido la
Comentarios de la Encuesta 100 La encuesta 100 tenía dos parásitos motivo de la misma, a saber: quistes de Entamoeba coli y quistes de Enteromonas hominis. Un 76,3% de los participantes ha respondido la
ACCESO Y CALIDAD DEL DIAGNOSTICO
 ACCESO Y CALIDAD DEL DIAGNOSTICO Avances en el diagnóstico y capacidades creadas en la Región Secretaria de Salud Programa Nacional de Malaria Laboratorio Nacional de Malaria Dra. Rosa Elena Mejia VISITA:
ACCESO Y CALIDAD DEL DIAGNOSTICO Avances en el diagnóstico y capacidades creadas en la Región Secretaria de Salud Programa Nacional de Malaria Laboratorio Nacional de Malaria Dra. Rosa Elena Mejia VISITA:
FICHA TÉCNICA. Sistema Producto Sistema. Hormigón Alisado. Rev agosto Piso de hormigón alisado con color realizado in situ.
 FICHA TÉCNICA Sistema Producto Sistema Hormigón Alisado Rev agosto 2015 Descripción Ventajas y Posibilidades Características básicas Espesor Usos Superficies a revestir Colores Piso de hormigón alisado
FICHA TÉCNICA Sistema Producto Sistema Hormigón Alisado Rev agosto 2015 Descripción Ventajas y Posibilidades Características básicas Espesor Usos Superficies a revestir Colores Piso de hormigón alisado
Entamoeba coli Entamoeba histolytica Endolimax nana
 Entamoeba coli Entamoeba histolytica Endolimax nana HISTORIA Feder Losch (1875), encontró amebas en las muestras de heces, pero sólo los consideraba responsables de mantener el proceso inflamatorio, no
Entamoeba coli Entamoeba histolytica Endolimax nana HISTORIA Feder Losch (1875), encontró amebas en las muestras de heces, pero sólo los consideraba responsables de mantener el proceso inflamatorio, no
MANUAL DE PROCEDIMIENTOS PUNCION ARTERIAL EN PACIENTES AULA DE SIMULACION USAL
 MANUAL DE PROCEDIMIENTOS PUNCION ARTERIAL EN PACIENTES AULA DE SIMULACION USAL aulasimulacion@usal.edu.ar JUSTIFICACIÓN Los instructores del Laboratorio de Simulación de la USAL hemos elaborado el presente
MANUAL DE PROCEDIMIENTOS PUNCION ARTERIAL EN PACIENTES AULA DE SIMULACION USAL aulasimulacion@usal.edu.ar JUSTIFICACIÓN Los instructores del Laboratorio de Simulación de la USAL hemos elaborado el presente
PROCEDIMIENTO ADMINISTRACIÓN DE MEDICACIÓN POR VÍA SUBCUTÁNEA
 Pág. 1 de 6 REALIZADO por REVISADO por APROBADO por Nombre: Ana Díaz Nombre: Beatriz Bagnasco Nombre: Miriam Gorrasi Cargo:Lic.Enf.Esp. Directora Dpto. Educación Nombre: Silvia de León Nombre: Nancy Fernández
Pág. 1 de 6 REALIZADO por REVISADO por APROBADO por Nombre: Ana Díaz Nombre: Beatriz Bagnasco Nombre: Miriam Gorrasi Cargo:Lic.Enf.Esp. Directora Dpto. Educación Nombre: Silvia de León Nombre: Nancy Fernández
MANUAL DE TOMA DE MUESTRAS
 Página 1 de 9 Nombre Firma Fecha Elaborado por: Nadina Erill Sagalés 29.06.15 Revisado por: Noelia González 29.06.15 Aprobado por: Ana Isabel Marcos 29.06.15 LISTADO DE DISTRIBUCIÓN DEL DOCUMENTO Copia
Página 1 de 9 Nombre Firma Fecha Elaborado por: Nadina Erill Sagalés 29.06.15 Revisado por: Noelia González 29.06.15 Aprobado por: Ana Isabel Marcos 29.06.15 LISTADO DE DISTRIBUCIÓN DEL DOCUMENTO Copia
Toma de muestra, conservación y transporte para estudios microbiológicos Departamento de Microbiología
 , conservación y transporte para estudios microbiológicos Departamento de Microbiología Indice I- INTRODUCCION I 01 II- ORINA A- Urocultivo Instructivo para laboratorio derivante: II 01 Pacientes que controlan
, conservación y transporte para estudios microbiológicos Departamento de Microbiología Indice I- INTRODUCCION I 01 II- ORINA A- Urocultivo Instructivo para laboratorio derivante: II 01 Pacientes que controlan
Patología Médica Facultad de Medicina de Granada. Prof. Juan Jiménez Alonso Curso académico
 TOXOPLASMOSIS Patología Médica Facultad de Medicina de Granada. Prof. Juan Jiménez Alonso Curso académico 2002-2003 TOXOPLASMOSIS * Infección producida por T. Gondii, que es un protozoo intracelular que
TOXOPLASMOSIS Patología Médica Facultad de Medicina de Granada. Prof. Juan Jiménez Alonso Curso académico 2002-2003 TOXOPLASMOSIS * Infección producida por T. Gondii, que es un protozoo intracelular que
Guía para toma de muestras. Cómo elegir los tubos:
 Guía para toma de muestras Cómo elegir los tubos: Para hemograma: tubo con W Tapa color rojo Para determinaciones de bioquímica sérica: eppendorf Es conveniente recolectar 2 tubos para bioquímica (eppendorf)
Guía para toma de muestras Cómo elegir los tubos: Para hemograma: tubo con W Tapa color rojo Para determinaciones de bioquímica sérica: eppendorf Es conveniente recolectar 2 tubos para bioquímica (eppendorf)
Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia
 Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia LABORATORIO NACIONAL DE BACTERIOLOGIA DIAGNOSTICO DE LABORATORIO EN LA VIGILANCIA DE LEPTOSPIROSIS EN LA RED NACIONAL DE LABORATORIOS
Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia LABORATORIO NACIONAL DE BACTERIOLOGIA DIAGNOSTICO DE LABORATORIO EN LA VIGILANCIA DE LEPTOSPIROSIS EN LA RED NACIONAL DE LABORATORIOS
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico.
 FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
Trabajo Práctico de Biología Celular
 Trabajo Práctico de Biología Celular Objetivo General: Reconocimiento de estructuras subcelulares mediante transfección de proteínas fluorescentes e inmunocitoquímica Transfección: proceso por el cual
Trabajo Práctico de Biología Celular Objetivo General: Reconocimiento de estructuras subcelulares mediante transfección de proteínas fluorescentes e inmunocitoquímica Transfección: proceso por el cual
GUIA DE TRABAJOS PRÁCTICOS Microbiología II
 GUIA DE TRABAJOS PRÁCTICOS Microbiología II OBJETIVOS GENERALES Instruir a los estudiantes de medicina en el mecanismo de pensamiento que lleve al diagnóstico microbiológico y prevención de las enfermedades
GUIA DE TRABAJOS PRÁCTICOS Microbiología II OBJETIVOS GENERALES Instruir a los estudiantes de medicina en el mecanismo de pensamiento que lleve al diagnóstico microbiológico y prevención de las enfermedades
RECOMENDACIONES PARA PADRES CON NIÑOS CON TRAQUEOTOMÍA
 RECOMENDACIONES PARA PADRES CON NIÑOS CON TRAQUEOTOMÍA Hospital de Niños R. Gutiérrez Centro Respiratorio Gallo 1330, Ciudad Autónoma de Buenos Aires. TEL. 4963-3224 www.centrorespiratorio.org Qué es una
RECOMENDACIONES PARA PADRES CON NIÑOS CON TRAQUEOTOMÍA Hospital de Niños R. Gutiérrez Centro Respiratorio Gallo 1330, Ciudad Autónoma de Buenos Aires. TEL. 4963-3224 www.centrorespiratorio.org Qué es una
MANEJO DE SOLUCIONES DESINFECTANTES
 PAGINA: 1 de 8 REVISADO: ELABORADO: COORDINADOR DE CALIDAD 1. DEFINICION ENFERMERO JEFE COORDINADOR CIRUGIA Las soluciones desinfectantes son sustancias que actúan sobre los microorganismos inactivándolos
PAGINA: 1 de 8 REVISADO: ELABORADO: COORDINADOR DE CALIDAD 1. DEFINICION ENFERMERO JEFE COORDINADOR CIRUGIA Las soluciones desinfectantes son sustancias que actúan sobre los microorganismos inactivándolos
ADMINISTRACIÓN POR VÍA RECTAL
 Página 1 de 5 ADMINISTRACIÓN POR VÍA RECTAL 1.- OBJETIVO Proporcionar los conocimientos necesarios para administrar por vía rectal la medicación prescrita con fines diagnósticos o terapéuticos. 2.- DEFINICIÓN
Página 1 de 5 ADMINISTRACIÓN POR VÍA RECTAL 1.- OBJETIVO Proporcionar los conocimientos necesarios para administrar por vía rectal la medicación prescrita con fines diagnósticos o terapéuticos. 2.- DEFINICIÓN
 COMPOSICIÓN Plantago ovata (semilla, cutícula) 33 mg, Enterococcus Faecium 2x108UFC/g, Aceite Mineral Refinado 54.5 ml, Dextrosa 45.83 mg. PROPIEDADES Plantago ovata Tienen una gran capacidad de retener
COMPOSICIÓN Plantago ovata (semilla, cutícula) 33 mg, Enterococcus Faecium 2x108UFC/g, Aceite Mineral Refinado 54.5 ml, Dextrosa 45.83 mg. PROPIEDADES Plantago ovata Tienen una gran capacidad de retener
Conservar según el tipo de muestra hasta proceder a su envío al laboratorio.
 Lunes a viernes 9:30 20 h/ Sábado 9:00 13:30 h Tlf: laboratoriosgasset@grupodavsalud.es www.grupodavsalud.es Envío de muestras La hoja de petición del laboratorio debe de cumplimentarse indicando las pruebas
Lunes a viernes 9:30 20 h/ Sábado 9:00 13:30 h Tlf: laboratoriosgasset@grupodavsalud.es www.grupodavsalud.es Envío de muestras La hoja de petición del laboratorio debe de cumplimentarse indicando las pruebas
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Unidad de Endoscopias Servicio de Digestivo RECOMENDACIONES DE ENFERMERÍA DESPUÉS DE LA GASTROSTOMÍA PERCUTÁNEA
 Unidad de Endoscopias Servicio de Digestivo RECOMENDACIONES DE ENFERMERÍA DESPUÉS DE LA GASTROSTOMÍA PERCUTÁNEA La colocación de una sonda por gastrostomía endoscópica percutánea (PEG) está indicada para
Unidad de Endoscopias Servicio de Digestivo RECOMENDACIONES DE ENFERMERÍA DESPUÉS DE LA GASTROSTOMÍA PERCUTÁNEA La colocación de una sonda por gastrostomía endoscópica percutánea (PEG) está indicada para
Sistema Integrado de Gestión RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS PROGRAMAS DE DEPORTE Y FISIOTERAPIA GUIA PRÁCTICA N 6
 Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
3.- Higiene de manos y Antisepsia cutánea
 Higiene de manos La medida más sencilla y eficaz para reducir la infección asociada a la asistencia sanitaria Transmisión cruzada de microorganismos a través de las manos: Las manos de los profesionales
Higiene de manos La medida más sencilla y eficaz para reducir la infección asociada a la asistencia sanitaria Transmisión cruzada de microorganismos a través de las manos: Las manos de los profesionales
MÉTODOS DE ESTUDIO DE LAS ENTEROPARASITOSIS
 MÉTODOS DE ESTUDIO DE LAS ENTEROPARASITOSIS IMPORTANCIA Diagnóstico de enteroparasitosis sintomáticas, asintomáticas. Diagnóstico diferencial de infecciones entéricas. Diagnóstico diferencial con otras
MÉTODOS DE ESTUDIO DE LAS ENTEROPARASITOSIS IMPORTANCIA Diagnóstico de enteroparasitosis sintomáticas, asintomáticas. Diagnóstico diferencial de infecciones entéricas. Diagnóstico diferencial con otras
PANENDOSCOPIA ORAL. -Siempre que se detecte o se sospeche la presencia de un sangrado en la parte alta del tubo digestivo.
 PANENDOSCOPIA ORAL 1. Qué es una panendoscopia oral? Es un procedimiento que permite explorar el esófago, el estómago y el duodeno y obtener multitud de información con un mínimo de molestias para el paciente.
PANENDOSCOPIA ORAL 1. Qué es una panendoscopia oral? Es un procedimiento que permite explorar el esófago, el estómago y el duodeno y obtener multitud de información con un mínimo de molestias para el paciente.
Patología Clínica Forense Bioquímica Citología Hematologia Inmunologia Microbiologia Patología Molecular Microscopia Electrónica
 TOMA DE MUESTRAS EN PATOLOGIA CLINICA FORENSE Alfredo Goytendia Cortez Medico Patologo Clínico Miembro de la Asociación de Patología Forense Miembro de la American Biological Safety Association 18 de Agosto
TOMA DE MUESTRAS EN PATOLOGIA CLINICA FORENSE Alfredo Goytendia Cortez Medico Patologo Clínico Miembro de la Asociación de Patología Forense Miembro de la American Biological Safety Association 18 de Agosto
EDUCACIÓN CONTINUADA. EN EL LABORATORIO CLÍNICO Ed Cont Lab Clín; 16: 82-92 DIAGNÓSTICO DE LABORATORIO DE LA ENFERMEDAD DE CHAGAS.
 EDUCACIÓN CONTINUADA 2012-2013 EN EL LABORATORIO CLÍNICO Ed Cont Lab Clín; 16: 82-92 DIAGNÓSTICO DE LABORATORIO DE LA ENFERMEDAD DE CHAGAS. Cristina Riera. Laboratorio de Parasitología. Facultad de Farmacia,
EDUCACIÓN CONTINUADA 2012-2013 EN EL LABORATORIO CLÍNICO Ed Cont Lab Clín; 16: 82-92 DIAGNÓSTICO DE LABORATORIO DE LA ENFERMEDAD DE CHAGAS. Cristina Riera. Laboratorio de Parasitología. Facultad de Farmacia,
Protocolo de toma de muestra arterial MANUAL DE CALIDAD LABORATORIO CLÍNICO. PRO 08 D Ed 01 Protocolo extracción arterial
 MANUAL DE CALIDAD LABORATORIO CLÍNICO Protocolo de toma de muestra arterial Código Fecha emisión/última revisión Revisado Aprobado PRO 08 D Ed 01 18/11/09 Spsor. Rafael Infantes Viano Dr. Vidal Pérez Valero.
MANUAL DE CALIDAD LABORATORIO CLÍNICO Protocolo de toma de muestra arterial Código Fecha emisión/última revisión Revisado Aprobado PRO 08 D Ed 01 18/11/09 Spsor. Rafael Infantes Viano Dr. Vidal Pérez Valero.
Generalidades de Protozoos
 Generalidades de Protozoos Protozoos: Organismos unicelulares (microscópicos, formados por una sola célula) eucariontes (material genético protegido por una membrana nuclear). Estructura y Metabolismo
Generalidades de Protozoos Protozoos: Organismos unicelulares (microscópicos, formados por una sola célula) eucariontes (material genético protegido por una membrana nuclear). Estructura y Metabolismo
LABORATORIO No. 6 HELMINTOS/PLATELMINTOS
 LABORATORIO No. 6 HELMINTOS/PLATELMINTOS PARTE II: PLATELMINTOS B. CESTODOS O TENIAS: Son gusanos planos de forma acintada, constituídos por escólex, cuello y estróbilo el cual esta constituído por segmentos
LABORATORIO No. 6 HELMINTOS/PLATELMINTOS PARTE II: PLATELMINTOS B. CESTODOS O TENIAS: Son gusanos planos de forma acintada, constituídos por escólex, cuello y estróbilo el cual esta constituído por segmentos
El término de tejido sanguíneo es un tejido conectivo altamente especializado, cuya matriz extracelular es liquida y se denomina plasma
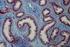 Trabajo Práctico N o 10: Tejido sanguíneo Nombre... Comisión... Objetivos 1. Identificar en microscopio óptico los elementos del tejido sanguíneo 2. Observar cristales de hemoglobina 3. Comprender los
Trabajo Práctico N o 10: Tejido sanguíneo Nombre... Comisión... Objetivos 1. Identificar en microscopio óptico los elementos del tejido sanguíneo 2. Observar cristales de hemoglobina 3. Comprender los
APROXIMACION AL DIAGNOSTICO Y TRATAMIENTO DE LAS ENTEROPARASITOSIS
 5 Congreso Argentino de Pediatría General Ambulatoria Buenos Aires 17 al 20 de Noviembre de 2010 Mesa Redonda ENTEROPARASITOSIS ENFERMEDAD DE LA POBREZA? REALIDAD ACTUAL Y ENFOQUE PRACTICO APROXIMACION
5 Congreso Argentino de Pediatría General Ambulatoria Buenos Aires 17 al 20 de Noviembre de 2010 Mesa Redonda ENTEROPARASITOSIS ENFERMEDAD DE LA POBREZA? REALIDAD ACTUAL Y ENFOQUE PRACTICO APROXIMACION
ENOXPRIM. Solución inyectable. Solución inyectable estéril, libre de pirógenos, contenida en jeringas pre-llenadas listas para usarse.
 ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
Método de flotación con sulfato de zinc de densidad. heces por flotación. Rina G. de Kaminsky
 Método de flotación con sulfato de zinc de densidad 118o120 1.18 1.20. Método de concentración de heces por flotación. Rina G. de Kaminsky Métodos de concentración Cuando el examen directo de heces resulta
Método de flotación con sulfato de zinc de densidad 118o120 1.18 1.20. Método de concentración de heces por flotación. Rina G. de Kaminsky Métodos de concentración Cuando el examen directo de heces resulta
PROTOZOOS INTESTINALES
 PROTOZOOS INTESTINALES Departamento de Parasitología y Micología CEFA CLASIFICACIÓN DE PROTOZOARIOS DE INTERÉS MÉDICO DEL TUBO DIGESTIVO Y VÍAS GÉNITO URINARIAS PATÓGENOS PRIMARIOS E.histolytica G.lamblia
PROTOZOOS INTESTINALES Departamento de Parasitología y Micología CEFA CLASIFICACIÓN DE PROTOZOARIOS DE INTERÉS MÉDICO DEL TUBO DIGESTIVO Y VÍAS GÉNITO URINARIAS PATÓGENOS PRIMARIOS E.histolytica G.lamblia
FUNDAMENTO MATERIAL Y EQUIPOS. Entre otros materiales es necesario disponer de:
 González,E.yAlloza,A.M. Ensayos para determinar las propiedades mecánicas y físicas de los áridos: métodos para la determinación de la resistencia a la fragmentación. Determinación de la resistencia a
González,E.yAlloza,A.M. Ensayos para determinar las propiedades mecánicas y físicas de los áridos: métodos para la determinación de la resistencia a la fragmentación. Determinación de la resistencia a
LA DIGESTIÓN LA NUTRICIÓN
 LA DIGESTIÓN LA NUTRICIÓN Las personas necesitamos energía para desarrollar nuestras actividades y materiales de construcción para crecer o reparar nuestro cuerpo. La función de nutrición comprende todos
LA DIGESTIÓN LA NUTRICIÓN Las personas necesitamos energía para desarrollar nuestras actividades y materiales de construcción para crecer o reparar nuestro cuerpo. La función de nutrición comprende todos
Diagnóstico de Laboratorio de Malaria o Paludismo
 Diagnóstico de Laboratorio de Malaria o Paludismo Dra. Mercedes Subirats S. Microbiología. H. Carlos III Dra. Rocío Martínez S. Microbiología. H. U. Puerta de Hierro-Majadahonda Paludismo 4+1 tipos de
Diagnóstico de Laboratorio de Malaria o Paludismo Dra. Mercedes Subirats S. Microbiología. H. Carlos III Dra. Rocío Martínez S. Microbiología. H. U. Puerta de Hierro-Majadahonda Paludismo 4+1 tipos de
TALLER VIA SUBCUTÁNEA. Equipos de Soporte de Atención Domiciliaria (ESAD) SERVICIO MURCIANO DE SALUD
 TALLER VIA SUBCUTÁNEA Equipos de Soporte de Atención Domiciliaria (ESAD) SERVICIO MURCIANO DE SALUD Elección de la vía de adm: Que permita autonomía al enfermo Fácil utilización Lo menos agresiva posible
TALLER VIA SUBCUTÁNEA Equipos de Soporte de Atención Domiciliaria (ESAD) SERVICIO MURCIANO DE SALUD Elección de la vía de adm: Que permita autonomía al enfermo Fácil utilización Lo menos agresiva posible
