Proteínas y Enzimas. 1ª Parte: Proteínas. Tema 10 de Biología NS Diploma BI Curso
|
|
|
- Nieves María Victoria Ponce Blázquez
- hace 6 años
- Vistas:
Transcripción
1 Proteínas y Enzimas 1ª Parte: Proteínas Tema 10 de Biología NS Diploma BI Curso
2 Proteínas Grupo de moléculas orgánicas más abundantes de los seres vivos (50% del peso celular seco), formadas por C, H, O y N, y en ocasiones aparecen P y S. Concepto: Polímeros denominados polipéptidos, constituidos por la unión de moléculas denominadas aminoácidos (monómeros). Junto con los ácidos nucleicos son portadores de información genética, ya que el ordenamiento de sus monómeros (Aa) no obedece al azar, sino a instrucciones heredadas de nuestros antecesores a lo largo del proceso evolutivo. Las proteínas ejecutan las órdenes dadas por los ácidos nucleicos. Importancia biológica: No radica exclusivamente en su abundancia, sino sobre todo, en su multifuncionalidad, ya que realizan infinidad de funciones, siendo imprescindibles para el mantenimiento de los procesos vitales.
3 Aminoácidos Unidades básicas (monómeros) que forman las proteínas y que se obtienen a partir de su hidrólisis. En la naturaleza existen muchos Aa que no forman parte de las proteínas y que tienen funciones propias. Sólo hay 20 Aa que formen proteínas y se denominan aminoácidos proteicos. Diéz de ellos son esenciales y hay que incluirlos en la dieta al no poder sintetizarlos. Todos los Aa tienen en común un grupo amino (-NH 2 ) y un grupo ácido carboxílico (-COOH), unidos covalentemente a un átomo de carbono (carbono alfa), al cual también se une un átomo de hidrógeno y una cadena lateral (R), que es lo que diferencia a una Aa de otro. Existe una cadena R para cada Aa, que al ser químicamente distintas, les proporcionan propiedades químicas diferentes a los distintos Aa. Web de Johnkyrk
4 Propiedades de los aminoácidos BE Carácter anfótero: Una molécula se denomina así cuando puede comportarse como un ácido o como una base dependiendo del ph del medio en el que se encuentre. Si la disolución es ácida, el grupo NH 2 capta protones y los Aa se comportan como una base. Si la disolución es básica, el grupo COOH cede protones y los Aa se comportan como un ácido. En las condiciones fisiológicas más comunes (ph=7), ambos grupos se encuentran ionizados, apareciendo como iones dipolares o dobles. Algunos Aa poseen en sus cadenas laterales R otros grupos amino o carboxilo que también se pueden ionizar. El punto isoeléctrico es el valor de ph al que un aminoácido presenta una carga neta igual al cero.
5 Propiedades de los aminoácidos BE Estereoisomería: Como el carbono alfa es asimétrico, excepto en el aminoácido glicina donde el grupo R es otro átomo de hidrógeno, los aminoácidos pueden presentar dos configuraciones espaciales distintas o estereoisómeros. Las proteínas se forman con L-aminoácidos, donde el grupo amino se localiza a la izquierda del carbono asimétrico. Web de Johnkyrk Cada uno de los esteroisómeros presenta distinta actividad óptica, desviando la luz polarizada a la derecha (dextrógiros) y se representan con el signo (+), o bien a la izquierda (levógiros), que se representan con el signo (-).
6 Clasificación de los aminoácidos Los distintos Aa proteicos se diferencian en sus cadenas laterales R. En función de la polaridad de dichas cadenas al interaccionar en medio acuoso, los Aa se clasifican en 3 grupos: apolares, polares sin carga y polares con carga (ácidos o bases). Web The Biology Project
7 Clasificación de los aminoácidos Apolares: La cadena R posee grupos hidrofóbicos que interaccionan con otros grupos hidrofóbos mediante fuerzas de Van der Waals. aromático aromático Pueden ser alifáticos cuando R es de dicha naturaleza, o bien aromáticos, cuando R contienen anillos aromáticos.
8 Clasificación de los aminoácidos Polares sin carga: La cadena R posee grupos polares capaces de formar enlaces de hidrógeno con otros grupos polares.
9 Clasificación de los aminoácidos Polares con carga: La cadena R posee grupos polares cargados. Pueden establecer enlaces electrostáticos entre grupos de distinta carga. Pueden ser ácidos, cuando presentan un grupo carboxilo en la cadena R, por lo que tienen carga negativa, o bien básicos, que presentan algún grupo amino en su cadena R, por lo que tienen carga positiva. ácidos básicos Animación1
10 Importancia de los aminoácidos polares y apolares Ambos tipos de aminoácidos, tanto polares como apolares, se usan en la formación de canales proteicos en la membrana plasmática. Las zonas polares permiten que los iones lo atraviesen (moléculas polares o cargadas no pueden normalmente atravesar la bicapa lipidica). Estos canales proteicos permiten la difusión facilitada a través de la membrana plasmática. Las zonas apolares interaccionan con las colas hidrofóbicas de los fosfolípidos.
11 Importancia de los aminoácidos apolares Los aminoácidos apolares ayudan a la unión de las proteínas y glucoproteínas a la membrana plasmática.
12 Importancia de los aminoácidos polares Los aminoácidos polares permiten que las enzimas se unan a sus sustratos para llevar a cabo (catalizar) la reacción. Región polar del sustrato Sitio activo (polar) Atracción Reacción Regiones no polares
13 Enlace peptídico: Formación Enlace que se establece entre el grupo carboxilo (-COOH) de un aminoácido con el grupo amino (-NH 2 ) de otro aminoácido. Web de Johnkyrk Animación2 Su formación es una reacción de condensación donde se pierde una molécula de agua. Mediante la reacción inversa, de hidrólisis, se liberan los Aa.
14 Enlace peptídico: Características BE El enlace se estabiliza porque los átomos de C, O y N comparten electrones, lo que hace que aparezcan formas resonantes. Por tanto, se puede afirmar que el enlace peptídico tiene carácter parcial de doble enlace, lo que impide que la molécula pueda girar alrededor del enlace peptídico, determinado que los átomos de C, N y O se encuentren en el mismo plano. La característica principal de este enlace radica en que no permite el giro de los elementos unidos por él, por lo que es un enlace rígido.
15 Peptidos, polipéptidos y proteínas Existen péptidos de gran interés biológico, como insulina y oxitocina (hormonas), endorfinas (neurotransmisor), gramicidina (antibiótico), etc. La unión sucesiva de varios Aa origina un polipéptido. En los enlaces peptídicos no participan los radicales de los Aa, que quedan colgando del polipéptido. Se suele usar el término péptido cuando la cadena contiene pocos Aa y polipéptido cuando el número es mayor. Por convenio se suele considerar que una proteína es un polipéptido con más de 100 Aa. La mayoría de las proteínas están formadas por más de una cadena polipeptídica.
16 Niveles de organización estructural de las proteínas Cada proteína posee una estructura tridimensional única que le confiere una actividad biológica específica. En esta estructura tridimensional o conformación espacial, se pueden describir cuatro niveles distintos de complejidad creciente, cada uno de los cuales se puede construir a partir del anterior: Estructura primaria o secuencia encadenada de aminoácidos; estructura secundaria, formada por el plegamiento de la estructura primaria; estructura terciaria, cuando se pliega sobre sí misma la secundaria; y estructura cuaternaria, cuando varias cadenas se asocian entre sí. Animación3
17 NH 2 - Estructura primaria Es la disposición lineal de los Aa unidos mediante enlaces peptídicos. Es distinta para cada proteína y se denomina secuencia de Aa: número, tipo y orden en la cadena polipeptídica. Como el Aa de un extremo tiene un grupo amino libre y el Aa del otro extremo un grupo carboxilo libre, por convenio, los Aa se enumeran desde su extremo amino inicial hasta el extremo carboxilo terminal. -COOH En realidad, la estructura 1ª constituye una cadena de placas planas sucesivas, ya que los enlaces peptídicos no pueden girar y los átomos de C, N y O están en un mismo plano.
18 La secuencia de aminoácidos en la cadena polipeptídica está determinada por la información codificada y almacenada en el ADN de los cromosomas en el núcleo, vía ARNm. Cambiar un solo aminoácido en la secuencia de una proteína altera drásticamente sus propiedades. La estructura primaria o secuencia de aminoácidos, es la conexión entre el mensaje genético contenido en el ADN y la configuración tridimensional que perfila la función biológica de la proteína. Animación4 Estructura primaria
19 Estructura secundaria Las cadenas polipeptídicas se pliegan en estado natural a medida que se sintetizan en los ribosomas, hasta adoptar espontáneamente la configuración espacial más estable para el medio en el que se encuentre, adquiriendo la forma tridimensional más cómoda. La sucesión de placas planas de la estructura primaria queda estabilizada cuando adopta tres conformaciones secundarias espaciales posibles: α hélice, lámina β y hélice de colágeno.
20 Estructura secundaria: α hélice Estructura semejante a un cilindro, donde la cadena polipeptídica principal, estrechamente enrollada, forma parte del interior del cilindro, y las cadenas laterales R se colocan hacia el exterior, en disposición helicoidal. La hélice alfa queda estabilizada por enlaces de hidrógeno intracatenarios entre los grupos NH y CO de la cadena principal. El sentido del plegamiento de una hélice puede ser dextrógiro (sentido de giro agujas del reloj) o levógiro (sentido inverso). Las α hélice naturales son dextrógiras. Se encuentra en muchas proteínas como la miosina. Video1
21 Estructura secundaria: Lámina plegada β En contraste con la hélice α, que se construye a partir de una región contínua de la cadena polipeptídica, la hoja β se construye a partir de regiones distintas del polipéptido, que pueden ser paralelas o antiparalelas, según si los enlaces peptídicos de las distintas cadenas avancen en el mismo o en distinto sentido. Las cadenas se estabilizan mediante enlaces de hidrógeno intercatenarios establecidos entre los grupos NH y -CO de los enlaces peptídicos enfrentados. Las cadenas laterales R se colocan por encima o por debajo de los planos en zig-zag de la lámina plegada. Web wiley.com
22 Estructura secundaria: Lámina plegada β La estructura no es plana sino que presenta un ligero plegamiento, donde las cadenas adyacentes pueden ser paralelas o antiparalelas, según si los enlaces peptídicos de las distintas cadenas avanzan en el mismo o en distinto sentido. El resultado es que las distintas regiones de la cadena están plegadas en zig-zag como se observa a la izquierda. Video2
23 Estructura secundaria: Hélice de colágeno Presente en todos los animales pluricelulares, es la proteína más abundante de los vertebrados. Es extracelular y forma fibras insolubles que resisten la tensión (hueso, diente, cartílagos, tendones, ligamentos, piel, vasos sanguíneos). Se considera como otro tipo de estructura secundaria con hélice girando a la izquierda. Web de MSU Cada una de las tres cadenas que forman la superhélice de colageno presenta un plegamiento secundario en forma de hélice, más abierta o extendida que la alfa hélice debido a las elevadas cantidades del Aa prolina en la cadena. Al asociarse tres de estas hélices, los residuos de glicina quedan hacia el interior permitiendo un contacto intimo de las hélices, además de formarse numerosos enlaces de hidrogeno interhélice.
24 Estructura terciaria Es la conformación espacial definitiva que adoptan las diferentes regiones de la cadena polipeptídica (cada una con su correspondiente estructura secundaria) como consecuencia de las interacciones entre las cadenas R. La estructura terciaria confiere a una proteína su actividad biológica. El resultado es diferente según se trate de proteínas globulares, en las cuales la estructura secundaria se pliega sobre sí misma, como un ovillo, hasta formar una proteína esferoidal, compacta y, por lo general, soluble en agua, o de proteínas fibrosas, que son alargadas, muy resistentes e insolubles en agua.
25 Estructura terciaria: Proteínas globulares En una proteína globular los distintos niveles de estructuración (1º, 2º y 3º) se disponen jerárquicamente, de forma que cada nivel contiene a los anteriores y es contenido por los superiores. Lo habitual es que las proteínas globulares contengan ambas conformaciones (α hélice y lámina β), aunque hay excepciones. Como son proteínas solubles, el plegamiento se hace de modo que los Aa con cadenas R apolares se dispongan hacia el interior de la estructura, protegidos del agua, mientras que los Aa con cadenas R polares se localicen en la superficie, formando enlaces con el agua. Las proteínas globulares son funcionales. Ejemplos son la amilasa y la insulina.
26 Estructura terciaria: Proteínas globulares Los enlaces o fuerzas que estabilizan su estructura terciaria son: 1. Puentes disulfuro (enlace covalente S-S) que se establecen entre dos regiones de la cadena peptídica en las que se encuentran dos grupos tiol (-SH) correspondiente al Aa cisteína. 2. Enlaces electrostáticos entre grupos COO - y NH 3 + de Aa ácidos y básicos.
27 Estructura terciaria: Proteínas globulares 3. Enlaces de hidrógeno entre las cadenas laterales R de los Aa polares sin carga. 4. Enlaces hidrofóbicos y fuerzas de Van der Waals entre las cadenas R de los Aa apolares.
28 Estructura terciaria: Proteínas globulares 5. La tendencia de la molécula completa a curvarse en los puntos de inestabilidad, para adoptar una estructura tal que los grupos polares se coloquen hacia fuera (hacia el agua) mientras que los grupos R apolares puedan permanecer en el interior de la macromolécula, en un ambiente sin agua. Si el ambiente es lipídico o apolar, la disposición es al revés.
29 Estructura terciaria: Plegamiento de proteínas Color Número Ejemplo Propiedad Estructura primaria del polipéptido:
30 Estructura terciaria: Plegamiento de proteínas Color Número Ejemplo Propiedad Estructura primaria del polipéptido: Como se plegara el polipéptido al colocarse en agua? 1. Grupos polares en el exterior 2. Grupos apolares en el interior 3. Cargas positivas y negativas próximas 4. Puentes disulfuros
31 Estructura terciaria: Plegamiento de proteínas Estructura 3D alfa-amilasa
32 Estructura terciaria: Proteínas fibrosas La estructura fundamental de las proteínas fibrosas es la estructura secundaria (α hélice, lámina β o hélice de colágeno). En este tipo de proteínas la estructura terciaria es muy simple, ya que las cadenas laterales R apenas influyen, pues suele haber pocos grupos polares. La queratina es una proteína fibrosa cuya estructura terciaria es un nuevo enrollamiento hasta formar una superhélice (hélice que contiene a otra). Las proteínas fibrosas tienen función estructural. Otro ejemplo es el colágeno.
33 Proteínas globulares versus fibrosas Característica Globular Fibrosa Morfología Esférica Filamentosa Solubilidad Solubles Insolubles Variaciones de ph, temperatura, concentración salina, etc. Función Ejemplo Alta sensibilidad Catálisis, transporte, hormonal Insulina, Inmunoglobulina, hemoglobina, amilasa, otros. Baja sensibilidad Estructural Actina, queratina, colágeno, fibrina, otros.
34 Estructura terciaria: Dominios estructurales Para entender mejor el significado de la estructura de las proteínas y su relación con la función que desempeñan, se ha establecido recientemente otro nivel más de organización: dominio proteico. Los dominios están formados por combinaciones de α hélice y lámina β particularmente estables, que hace que se repitan en proteínas diferentes. Video3
35 Estructura cuaternaria Sólo se manifiesta en la proteínas fibrosas o globulares formadas por la asociación de más de una cadena polipeptídica (iguales o diferentes), denominas cada una de ellas subunidades proteicas. Las fuerzas que estabilizan dicha estructura son de la misma índole que las que estabilizan la estructura terciaria (interacciones hidrofóbicas, puentes de hidrógeno, fuerzas de Van der Waals, fuerzas electrostáticas y puentes disulfuro), pero en este caso, se establece entre las cadenas R de los Aa pertenecientes a distintas cadenas o subunidades. Tienen estructura cuaternaria la hemoglobina y los anticuerpos (ambos 4 cadenas).
36 Niveles estructurales de las proteínas Video4
37 Propiedades de las proteínas: 1) Especificidad Sus propiedades físico-químicas dependen casi por completo de los grupos funcionales presentes en las cadenas laterales R de los Aa que quedan expuestos en su superficie tras el plegamiento concreto que adopte la cadena o cadenas. Destacan 3 propiedades, como la especificidad: Los grupos funcionales de las cadenas laterales de los Aa definen en la proteína una superficie activa, capaz de interaccionar con otras moléculas mediante enlaces débiles. Casi todas las actividades de las proteínas se basan en su unión selectiva con otras moléculas (enzima-sustrato, hemoglobina-o 2, antígenoanticuerpo, etc.), cuya geometría es complementaria y que permite adaptarse con precisión a la superficie activa.
38 Propiedades de las proteínas: 1) Especificidad Esta especificidad se basa en el plegamiento particular de cada proteína, que depende de la secuencia de Aa. Por tanto, cualquier cambio en la misma puede originar cambios en las estructuras 2ª, 3ª y 4ª (si la tiene), que pueden alterar la superficie activa, y en consecuencia, la disminución o perdida total de la actividad biológica. Ejemplo: Anemia falciforme. Una mutación en el gen de la hemoglobina provoca que el Aa nº 6 cambie de glutámico a valina, afectando a la zona de contacto entre las cadenas, haciendo que las proteínas de hemoglobina se agregen formando fibras.
39 Propiedades de las proteínas: 1) Especificidad Ejemplo: Encefalopatía espongiforme. Los priones se componen de una proteína denominada PrPSc (isoforma scrapie de la proteína del prión) producida por el plegamiento erríneo de una proteína celular de idéntica secuencia de aminoácidos, presente en prácticamente todos los tejidos del organismo, denominada PrPC (isoforma celular de la proteína del prión).
40 Propiedades de las proteínas: 2) Desnaturalización La desnaturalización consiste en la pérdida de la conformación espacial (estructura 2ª, 3ª y 4ª) característica de una proteína y, como consecuencia de ello, en la anulación de su funcionalidad biológica. Se produce por cambios excesivos de temperatura, ph, salinidad o agentes físicos (presión, electricidad, etc.). Dichas circunstancias pueden provocar una ruptura de los puentes disulfuro, enlaces de H, etc., desestabilizando y rompiendo la estructura tridimensional de la proteína. Animación5 La forma de una proteína depende su secuencia de Aa (estructura primaria) y del medio en el que se encuentra. La desnaturalización puede se reversible o irreversible dependiendo de la intensidad del agente.
41 Propiedades de las proteínas: 3) Solubilidad Las proteínas son macromoléculas solubles en medios acuosos cuando adoptan la conformación globular, ya que se establece una interacción entre las cargas eléctricas, positivas y negativas, de la superficie de la proteína con las moléculas de agua (dipolo) de su entorno, dando lugar a la llamada capa de solvatación. Dicha capa de solvatación impide la unión de moléculas proteicas entre si. El grado de solubilidad en agua de una proteína dependerá directamente de la cantidad de grupos cargados que esta tenga en su superficie.
42 Clasificación de las proteínas según su conformación Cada tipo de molécula proteica posee, en su estado nativo, una forma tridimensional típica que se llama conformación. Según dicha conformación, las proteínas pueden ser: 1) Fibrosas. Son materiales físicamente resistentes, insolubles en agua, formadas por cadenas polipeptídicas ordenadas de modo paralelo a lo largo de un eje, formando fibras o laminas largas. Son proteínas con función estructural, como el colágeno de tendones y huesos, o la queratina del cabello, cuerpo, cuero o unas.
43 Clasificación de las proteínas según su conformación 2) Globulares. En este caso las cadenas polipeptídicas están plegadas estrechamente, de modo que adoptan formas esféricas o globulares. Casi todas son solubles en medio acuoso. Desempeñan una función dinámica en la célula o en los líquidos extracelulares. Ejemplos de dichas proteínas son las enzimas, anticuerpos, algunas hormonas, hemoglobina, etc.
44 Clasificación de las proteínas según su conformación
45 Clasificación de las proteínas según su composición Otra forma de clasificar a las proteínas es según su composición química: A) Holoproteínas o proteínas simples, únicamente formadas por aminoácidos, como la albúmina o las histonas. B) Heteroproteínas o proteínas compuestas, formadas por una parte proteica (grupo proteico) y otra parte con sustancias no proteicas (grupo prostético), como la hemoglobina.
46 Clasificación de las proteínas según su composición Según la naturaleza de dicho grupo prostético, pueden ser: Glucoproteínas (grupo prostético es un glúcido=inmunoglobulinas), Fosfoproteínas (grupos prostético es el fosfórico=caseina de la leche), Cromoproteínas (grupo prostético es un pigmento=hemoglobina) o Lipoproteínas (grupo prostético es un lípido=colesterol).
47 Funciones de las proteínas Las proteínas desempeñan infinidad de funciones dentro de los seres vivos.
48 Funciones de las proteínas 1. Hormonal. Algunas hormonas importantes son de naturaleza proteica, como la insulina, el glucagón o la hormona del crecimiento. 2. Estructural. Las proteínas se consideran los elementos plásticos a partir de los cuales se construyen la mayoría de las estructuras celulares. Destacan el colágeno, queratina y elastina. 3. Catálisis enzimática. Todos los enzimas son proteínas, biocatalizadores de las reacciones químicas que forman el metabolismo celular, como la amilasa o catalasa. 4. Homeostática: tamponante y osmótica. Las proteínas, según los casos, pueden aceptar o desprender H+, por lo que son importantes tampones intracelulares. También intervienen en el mantenimiento del equilibrio osmótico.
49 Funciones de las proteínas 5. Nutrición y reserva. Algunas proteínas como la ovoalbúmina de la clara de huevo o la caseina de la leche constituyen una reserva de aminoácidos dispuestos para ser utilizados durante el desarrollo como elementos nutritivos y como unidades estructurales. 6. Transporte y almacenamiento. Muchas moléculas e iones son transportados por el organismo mediante proteína. La hemoglobina O 2 en la sangre, la seroalbúmina transporta y almacena ácidos grasos, fármacos y tóxicos en la sangre, las lipoproteínas (LHD y LDL) transportan en la sangre el colesterol.
50 Funciones de las proteínas 7. Movimiento y contracción. El movimiento y la locomoción en los organismos uni y pluricelulares depende de proteínas contráctiles, como la actina y la miosina. 8. Defensa. Algunas proteínas desempeñan funciones de protección. Los anticuerpos son proteínas que controlan a los posibles antígenos que pueden penetrar en el organismo. La trombina y el fibrinógeno intervienen en la formación de coágulos durante la hemorragia. 9. Reconocimiento celular. Muchas glucoproteínas situadas en la cara externa de las membranas celulares, sirven de antenas que determinan el lugar de anclaje de otras células, hormonas, bacterias y virus.
51 Funciones de las proteínas 10. Regulación expresión génica. Algunas proteínas intervienen en los procesos de activación e inactivación de la expresión génica, participando en la diferenciación celular. 11. Generación de impulsos nerviosos. Las respuestas de las células nerviosas a los estímulos específicos vienen mediadas por receptores proteicos, como la rodopsina del ojo. Web de la Universidad de Auburn
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS
 UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
Los monómeros de las proteínas
 Las proteínas Los monómeros de las proteínas El carbono α de los aminoácidos es asimétrico y por eso pueden darse dos formas isoméricas que se distinguen como D y L. Los seres vivos sólo construyen a.a.
Las proteínas Los monómeros de las proteínas El carbono α de los aminoácidos es asimétrico y por eso pueden darse dos formas isoméricas que se distinguen como D y L. Los seres vivos sólo construyen a.a.
TEMA 5 BIOMOLÉCULAS ORGÁNICAS (III) PROTEÍNAS. A.- Concepto de prótidos y clasificación B.-Los aminoácidos
 TEMA 5 BIOMOLÉCULAS ORGÁNICAS (III) PROTEÍNAS A.- Concepto de prótidos y clasificación B.-Los aminoácidos Estructura química y funciones Propiedades químicas. El enlace peptídico C.- Estructura tridimensional
TEMA 5 BIOMOLÉCULAS ORGÁNICAS (III) PROTEÍNAS A.- Concepto de prótidos y clasificación B.-Los aminoácidos Estructura química y funciones Propiedades químicas. El enlace peptídico C.- Estructura tridimensional
Existen 20 aminoácidos diferentes y todos ellos tienen una parte común en su molécula que consisten en un grupo amino (NH3) y un grupo ácido, (COOH)
 Existen 20 aminoácidos diferentes y todos ellos tienen una parte común en su molécula que consisten en un grupo amino (NH3) y un grupo ácido, (COOH) como puede verse en el dibujo de los aminoácidos, que
Existen 20 aminoácidos diferentes y todos ellos tienen una parte común en su molécula que consisten en un grupo amino (NH3) y un grupo ácido, (COOH) como puede verse en el dibujo de los aminoácidos, que
Proteínas. Características generales
 Proteínas Características generales Son las macromoléculas más abundantes en las células. Constituyen hasta el 50% del peso. Forman moléculas específicas en cada especie, incluso entre individuos. Además,
Proteínas Características generales Son las macromoléculas más abundantes en las células. Constituyen hasta el 50% del peso. Forman moléculas específicas en cada especie, incluso entre individuos. Además,
TRABAJO SOBRE LAS PROTEÍNAS
 TRABAJO SOBRE LAS PROTEÍNAS INDICE Concepto de Proteína Los Aminoácidos (clasificación y tipos, comportamiento químico) El Enlace Peptídico Estructura de las Proteínas Propiedades de las Proteínas Clasificación
TRABAJO SOBRE LAS PROTEÍNAS INDICE Concepto de Proteína Los Aminoácidos (clasificación y tipos, comportamiento químico) El Enlace Peptídico Estructura de las Proteínas Propiedades de las Proteínas Clasificación
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Biología. Proteínas.
 Proteínas. Los monómeros de las proteínas son veinte aminoácidos, donde 9 de estoss aminoácidos son esenciales, ya que no son producidos por nuestro organismo, por lo tanto deben ser adquiridos a través
Proteínas. Los monómeros de las proteínas son veinte aminoácidos, donde 9 de estoss aminoácidos son esenciales, ya que no son producidos por nuestro organismo, por lo tanto deben ser adquiridos a través
Proteínas y Ácidos Nucleicos
 Proteínas y Ácidos Nucleicos Mapa conceptual Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan carbono en su estructura.
Proteínas y Ácidos Nucleicos Mapa conceptual Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan carbono en su estructura.
CAPÍTULO 4. AMINOÁCIDOS, PÉPTIDOS Y PROTEÍNAS Facultad de Agronomía Curso de Bioquímica
 CAPÍTULO 4. AMINOÁCIDOS, PÉPTIDOS Y PROTEÍNAS Facultad de Agronomía Curso de Bioquímica INTRODUCCIÓN El término proteína fue utilizado por primera vez por el químico Gerardus Mulder en 1838. Vocablo griego
CAPÍTULO 4. AMINOÁCIDOS, PÉPTIDOS Y PROTEÍNAS Facultad de Agronomía Curso de Bioquímica INTRODUCCIÓN El término proteína fue utilizado por primera vez por el químico Gerardus Mulder en 1838. Vocablo griego
PROTEÍNAS. Las proteínas están constituidas por la unión de numerosas moléculas sencillas (monómeros) denominados aminoácidos.
 PROTEÍNAS 1. INTRODUCCIÓN Las proteínas son los constituyentes químicos fundamentales de la materia viva. Constituyen alrededor del 50% en peso seco del cuerpo. Los glúcidos y lípidos se encuentran en
PROTEÍNAS 1. INTRODUCCIÓN Las proteínas son los constituyentes químicos fundamentales de la materia viva. Constituyen alrededor del 50% en peso seco del cuerpo. Los glúcidos y lípidos se encuentran en
EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS
 EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS 1) Qué es un tetrapéptido?. Construye uno, formado por los siguientes aminoácidos: Ala, Cys, Ser y Tyr. 2) Haz corresponder los elementos de las dos columnas: -Cys -Hormona
EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS 1) Qué es un tetrapéptido?. Construye uno, formado por los siguientes aminoácidos: Ala, Cys, Ser y Tyr. 2) Haz corresponder los elementos de las dos columnas: -Cys -Hormona
Estructura y propiedades de las proteínas
 Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
L/O/G/O BIOQUÍMICA II
 L/O/G/O BIOQUÍMICA II Objetivos Contenidos Niveles estructurales de una proteína Relación entre estructura y función 11/10/2011 Ing. Karla Dávila Estructura primaria La estructura primaria, se refiere
L/O/G/O BIOQUÍMICA II Objetivos Contenidos Niveles estructurales de una proteína Relación entre estructura y función 11/10/2011 Ing. Karla Dávila Estructura primaria La estructura primaria, se refiere
Biomoléculas orgánicas: Proteínas y Ácidos nucleicos. Propiedad Intelectual Cpech
 Biología Biomoléculas orgánicas: Proteínas y Ácidos nucleicos Repaso Moléculas orgánicas Carbohidratos Lípidos 1. Monosacáridos: glucosa 2. Disacáridos: maltosa 3. Polisacáridos: glucógeno 1. Ácidos grasos.
Biología Biomoléculas orgánicas: Proteínas y Ácidos nucleicos Repaso Moléculas orgánicas Carbohidratos Lípidos 1. Monosacáridos: glucosa 2. Disacáridos: maltosa 3. Polisacáridos: glucógeno 1. Ácidos grasos.
Introducción al estudio de las proteínas
 Introducción al estudio de las proteínas ESQUEMA - Concepto de Proteína. Características - Clasificación de las proteínas - Funciones de las proteínas - Proteínas conjugadas - Niveles de organización estructural
Introducción al estudio de las proteínas ESQUEMA - Concepto de Proteína. Características - Clasificación de las proteínas - Funciones de las proteínas - Proteínas conjugadas - Niveles de organización estructural
Niveles de organización biológica. La composición de los seres vivos
 Niveles de organización biológica. La composición de los seres vivos Imagen de Fondo bajo licencia Creative Commons, autor: René Ehrtardt. Animación ADN de dominio público, fuente:wikipedia Con este tema
Niveles de organización biológica. La composición de los seres vivos Imagen de Fondo bajo licencia Creative Commons, autor: René Ehrtardt. Animación ADN de dominio público, fuente:wikipedia Con este tema
Material elaborado por F. Agius, O. Borsani, P.Díaz, S. Gonnet, P. Irisarri, F. Milnitsky y J. Monza. Bioquímica. Facultad de Agronomía.
 AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
Aminoácidos. Los aminoácidos se agrupan en la figura según las propiedades de sus cadenas
 Aminoácidos Es esencial tener un conocimiento básico acerca de la química de las proteínas, para entender la nutrición y otros conceptos del metabolismo. Las proteínas se componen de carbono, hidrógeno,
Aminoácidos Es esencial tener un conocimiento básico acerca de la química de las proteínas, para entender la nutrición y otros conceptos del metabolismo. Las proteínas se componen de carbono, hidrógeno,
Clase 5. Los aminoácidos: Precursores de transmisores. Unidades de las proteínas. Las enzimas.
 Clase 5. Los aminoácidos: Precursores de transmisores. Unidades de las proteínas. Las enzimas. Los aminoácidos se clasifican en unas pocas categorías diferenciadas, basadas sobre todo en su solubilidad
Clase 5. Los aminoácidos: Precursores de transmisores. Unidades de las proteínas. Las enzimas. Los aminoácidos se clasifican en unas pocas categorías diferenciadas, basadas sobre todo en su solubilidad
TEMA 2.- PROTEÍNAS. AMINOÁCIDOS
 TEMA 2.- PROTEÍNAS. AMINOÁCIDOS Diversidad estructural y funcional de las proteínas. Aminoácidos: características estructurales y clasificación. Aminoácidos estándares y derivados. Aminoácidos esenciales
TEMA 2.- PROTEÍNAS. AMINOÁCIDOS Diversidad estructural y funcional de las proteínas. Aminoácidos: características estructurales y clasificación. Aminoácidos estándares y derivados. Aminoácidos esenciales
Bloque I: Proteínas y enzimas
 Bloque I: Proteínas y enzimas 1. BASE FÍSICO-QUÍMICA DE LA VIDA PROTEÍNAS Y ENZIMAS CONTENIDOS 1.5. PROTEÍNAS 1.5.1. Concepto e importancia biológica. 1.5.2. Aminoácidos. Enlace peptídico. 1.5.3. Estructura
Bloque I: Proteínas y enzimas 1. BASE FÍSICO-QUÍMICA DE LA VIDA PROTEÍNAS Y ENZIMAS CONTENIDOS 1.5. PROTEÍNAS 1.5.1. Concepto e importancia biológica. 1.5.2. Aminoácidos. Enlace peptídico. 1.5.3. Estructura
Unidad 3: Organización molecular de la célula Proteínas
 Proteínas Las proteínas son las biomoléculas más abundantes de las células, constituyendo el 50% de su peso seco aproximadamente. Estructuralmente, son polímeros de aminoácidos. Existe una enorme variedad
Proteínas Las proteínas son las biomoléculas más abundantes de las células, constituyendo el 50% de su peso seco aproximadamente. Estructuralmente, son polímeros de aminoácidos. Existe una enorme variedad
Proteínas y Enzimas. 1ª Parte: Proteínas. Tema 10 de Biología NS Diploma BI Curso 2011-2013. Proteínas y Enzimas 1/50
 Proteínas y Enzimas 1ª Parte: Proteínas Tema 10 de Biología NS Diploma BI Curso 2011-2013 Proteínas y Enzimas 1/50 Proteínas Grupo de moléculas orgánicas más abundantes de los seres vivos (50% del peso
Proteínas y Enzimas 1ª Parte: Proteínas Tema 10 de Biología NS Diploma BI Curso 2011-2013 Proteínas y Enzimas 1/50 Proteínas Grupo de moléculas orgánicas más abundantes de los seres vivos (50% del peso
REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS.
 REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS. PRESENTACIÓN Los animales incluyendo al hombre, recibimos pocas moléculas sencillas y una gran cantidad de macromoléculas, como almidones, proteínas
REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS. PRESENTACIÓN Los animales incluyendo al hombre, recibimos pocas moléculas sencillas y una gran cantidad de macromoléculas, como almidones, proteínas
Ácidos nucléicos. Los ácidos nucleicos fueron descubiertos por Freidrich Miescher en Mirel Nervenis
 Ácidos nucléicos Los ácidos nucleicos fueron descubiertos por Freidrich Miescher en 1869 La información genética o genoma, está contenida en unas moléculas llamadas ácidos nucleicos. Existen dos tipos
Ácidos nucléicos Los ácidos nucleicos fueron descubiertos por Freidrich Miescher en 1869 La información genética o genoma, está contenida en unas moléculas llamadas ácidos nucleicos. Existen dos tipos
PEPTIDOS Y PROTEINAS ESTRUCTURA Y CARACTERÍSTICAS
 PEPTIDOS Y PROTEINAS ESTRUCTURA Y CARACTERÍSTICAS CARACTERISTICAS En la célula o Estructura celular o Catálisis o ADN proteínas Macromoléculas abundantes La estructura tridimensional es única Funciones
PEPTIDOS Y PROTEINAS ESTRUCTURA Y CARACTERÍSTICAS CARACTERISTICAS En la célula o Estructura celular o Catálisis o ADN proteínas Macromoléculas abundantes La estructura tridimensional es única Funciones
Composición química de la materia viva. Componentes orgánicos. Proteínas
 Composición química de la materia viva. Componentes orgánicos. Proteínas Tema 1 parte 4 PROTEÍNAS: Concepto, clasificación (oligopéptidos, polipéptidos, holoproteínas, heteroproteínas). Aminoácidos: estructura
Composición química de la materia viva. Componentes orgánicos. Proteínas Tema 1 parte 4 PROTEÍNAS: Concepto, clasificación (oligopéptidos, polipéptidos, holoproteínas, heteroproteínas). Aminoácidos: estructura
Estructura tridimensional de las proteínas
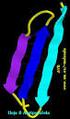 Estructura tridimensional de las proteínas CAPITULO 4 Biochemistry 6th Edition Campbell and Farrell NATURALEZA DE LAS PROTEINAS Proteínas Son polímeros de amino ácidos unidos por un enlace peptídico. El
Estructura tridimensional de las proteínas CAPITULO 4 Biochemistry 6th Edition Campbell and Farrell NATURALEZA DE LAS PROTEINAS Proteínas Son polímeros de amino ácidos unidos por un enlace peptídico. El
inactivación de materiales tóxicos o peligrosos, etc.).
 Proteínas Estructuras 1 Conceptos generales Las proteínas desempeñan papeles cruciales en prácticamente todos los procesos biológicos. El alcance de sus funciones es enorme, por un lado, forman parte de
Proteínas Estructuras 1 Conceptos generales Las proteínas desempeñan papeles cruciales en prácticamente todos los procesos biológicos. El alcance de sus funciones es enorme, por un lado, forman parte de
Clasificación de las proteinas según su conformación
 lasificación de las proteinas según su conformación Proteinas fibrosas (insolubles) olágeno α-queratina elastina tejido conectivo, tendones pelo, uñas tejido conectivo elástico Proteinas globulares (solubles)
lasificación de las proteinas según su conformación Proteinas fibrosas (insolubles) olágeno α-queratina elastina tejido conectivo, tendones pelo, uñas tejido conectivo elástico Proteinas globulares (solubles)
Tema I: Biomoléculas
 República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Ciencias Biológicas 3 Año Tema I: Biomoléculas
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Ciencias Biológicas 3 Año Tema I: Biomoléculas
Biología General y Metodología de las Ciencias 2016 BIOMOLÉCULAS
 BIOMOLÉCULAS Objetivos: Reconocer los distintos niveles de organización de la materia. Diferenciar las propiedades constreñimiento, emergentes y colectivas. Identificar las principales Biomoléculas según
BIOMOLÉCULAS Objetivos: Reconocer los distintos niveles de organización de la materia. Diferenciar las propiedades constreñimiento, emergentes y colectivas. Identificar las principales Biomoléculas según
CLASIFICACION POR LA CADENA LATERAL POR SU REQUERIMIENTO POR SU POLARIDAD. Esenciales No esenciales CADENA LATERAL CON GRUPO
 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2016 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2016 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
Composición química de los seres vivos
 Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Tema 5: aminoácidos y proteínas
 1. Los aminoácidos 2. Propiedades de los aminoácidos 3. El enlace peptídico 4. Estructuras 1 aria y 2 aria de las proteínas 5. Estructuras 3 aria y 4 aria de las proteínas 6. Propiedades de las proteínas
1. Los aminoácidos 2. Propiedades de los aminoácidos 3. El enlace peptídico 4. Estructuras 1 aria y 2 aria de las proteínas 5. Estructuras 3 aria y 4 aria de las proteínas 6. Propiedades de las proteínas
Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de
 Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
Niveles de Organización Conceptos, átomos y enlaces
 Niveles de Organización Conceptos, átomos y enlaces Cómo se organiza la materia viva? NIVELES DE ORGANIZACIÓN ÁTOMO MOLÉCULA (ELEMENTO- COMPUESTO) MACROMOLÉCULA CÉLULA TEJIDO ÓRGANO SISTEMA ORGANISMO MULTICELULAR
Niveles de Organización Conceptos, átomos y enlaces Cómo se organiza la materia viva? NIVELES DE ORGANIZACIÓN ÁTOMO MOLÉCULA (ELEMENTO- COMPUESTO) MACROMOLÉCULA CÉLULA TEJIDO ÓRGANO SISTEMA ORGANISMO MULTICELULAR
TEORIA CELULAR. En el mundo vivo, la unidad fundamental es la célula. DECUBRIMIENTO DE LAS CELULAS
 TEORIA CELULAR En el mundo vivo, la unidad fundamental es la célula. DECUBRIMIENTO DE LAS CELULAS El nombre de célula significa celda, así las llamo Robert Hooke. En 1839 el zoólogo alemán Theodore Schwann
TEORIA CELULAR En el mundo vivo, la unidad fundamental es la célula. DECUBRIMIENTO DE LAS CELULAS El nombre de célula significa celda, así las llamo Robert Hooke. En 1839 el zoólogo alemán Theodore Schwann
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR
 INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - Componentes químicos de la célula - Un poco de química 1 Un poco de química El 99% del peso de una célula corresponde a C, H, N y O. La sustancia más abundante
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - Componentes químicos de la célula - Un poco de química 1 Un poco de química El 99% del peso de una célula corresponde a C, H, N y O. La sustancia más abundante
Plataforma para la monitorización de la Gripe en España
 Plataforma para la monitorización de la Gripe en España La gripe es una de las enfermedades más contagiosas que existen y cada año es responsable de la muerte de cientos de miles de personas en todo el
Plataforma para la monitorización de la Gripe en España La gripe es una de las enfermedades más contagiosas que existen y cada año es responsable de la muerte de cientos de miles de personas en todo el
Tema 4b Estructura tridimensional de las proteínas. Estructura supersecundaria y terciaria.
 Tema 4b Estructura tridimensional de las proteínas. Estructura supersecundaria y terciaria. Estructura supersecundaria Motivos Dominios Estructura terciaria Fuerzas que la estabilizan Plegamiento de proteínas
Tema 4b Estructura tridimensional de las proteínas. Estructura supersecundaria y terciaria. Estructura supersecundaria Motivos Dominios Estructura terciaria Fuerzas que la estabilizan Plegamiento de proteínas
Universidad Nacional de la Patagonia San Juan Bosco Facultad de Ciencias Naturales Química Biológica Introducción
 Química Biológica TP 4 PROTEINAS,. Introducción Las proteínas son biomoléculas formados por 20 L-α-aminoácidos distintos, unidos linealmente entre sí por enlaces peptídicos, en un número que varía entre
Química Biológica TP 4 PROTEINAS,. Introducción Las proteínas son biomoléculas formados por 20 L-α-aminoácidos distintos, unidos linealmente entre sí por enlaces peptídicos, en un número que varía entre
Repaso: Química celular (biomoléculas)
 Repaso: Química celular (biomoléculas) Hay 4 tipos principales de biomoléculas: 1) glúcidos o hidratos de carbono, 2) lípidos o grasas, 3) proteínas y 4) ácidos nucleicos. Las biomoléculas más grandes,
Repaso: Química celular (biomoléculas) Hay 4 tipos principales de biomoléculas: 1) glúcidos o hidratos de carbono, 2) lípidos o grasas, 3) proteínas y 4) ácidos nucleicos. Las biomoléculas más grandes,
TEMA 7: LA MEMBRANA PLASMÁTICA.
 TEMA 7: LA MEMBRANA PLASMÁTICA. 1.-La membrana plasmática como unidad estructural. 2.- Características de la membrana plasmática. 2.1. Estructura y composición. 2.2. Propiedades de la membrana plasmática.
TEMA 7: LA MEMBRANA PLASMÁTICA. 1.-La membrana plasmática como unidad estructural. 2.- Características de la membrana plasmática. 2.1. Estructura y composición. 2.2. Propiedades de la membrana plasmática.
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
BIOMOLÉCULAS. Son moléculas fundamentales para la constitución y funcionamiento de todo ser vivo. Se clasifican en dos grupos:
 FICHA N 2 UNIDAD III: CÉLULAS A ORGANISMOS Profesora Verónica Abasto Córdova Ciencias Naturales 8 Básico Nombre : Curso : Fecha : Revisión BIOMOLÉCULAS Son moléculas fundamentales para la constitución
FICHA N 2 UNIDAD III: CÉLULAS A ORGANISMOS Profesora Verónica Abasto Córdova Ciencias Naturales 8 Básico Nombre : Curso : Fecha : Revisión BIOMOLÉCULAS Son moléculas fundamentales para la constitución
Polímero corto Monómero. síntesis. degradación
 Polímero corto Monómero síntesis degradación Hidratos de carbono. Glúcidos o azúcares. Monómeros Glúcidos. Dímeros. Glu+Glu= Maltosa (azúcar presente en la malta, un grano) Glu+Frc= Sacarosa (azúcar de
Polímero corto Monómero síntesis degradación Hidratos de carbono. Glúcidos o azúcares. Monómeros Glúcidos. Dímeros. Glu+Glu= Maltosa (azúcar presente en la malta, un grano) Glu+Frc= Sacarosa (azúcar de
Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno
 Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno Tema 3 Proteínas Fibrosas y Proteínas Globulares Fibrosas Globulares Forma alargada Unidades repetidas de un solo tipo de estructura secundaria
Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno Tema 3 Proteínas Fibrosas y Proteínas Globulares Fibrosas Globulares Forma alargada Unidades repetidas de un solo tipo de estructura secundaria
Aminoácidos y Proteínas
 Aminoácidos y Proteínas Un aminoácido es una pequeña molécula orgánica que contiene, al menos, un grupo amino (-NH 2), de naturaleza básica, y un grupo carboxilo (-COOH), de carácter ácido. Aunque los
Aminoácidos y Proteínas Un aminoácido es una pequeña molécula orgánica que contiene, al menos, un grupo amino (-NH 2), de naturaleza básica, y un grupo carboxilo (-COOH), de carácter ácido. Aunque los
Tema 4c Estructura tridimensional de las proteínas. Proteínas fibrosas. Proteínas globulares.
 Tema 4c Estructura tridimensional de las proteínas. Proteínas fibrosas. Proteínas globulares. Proteínas fibrosas Estructura y función de las queratinas Estructura y función del colágeno Triple hélice de
Tema 4c Estructura tridimensional de las proteínas. Proteínas fibrosas. Proteínas globulares. Proteínas fibrosas Estructura y función de las queratinas Estructura y función del colágeno Triple hélice de
Holoproteínas (sólo contienen aa)
 TEMA 4: P ROTEÍNAS 1. Concepto y clasificación Las proteínas son biomoléculas orgánicas formadas por C, H, O, N y en menor medida P y S y otros elementos (Fe,Cu, Mg, ). Son polímeros no ramificados de
TEMA 4: P ROTEÍNAS 1. Concepto y clasificación Las proteínas son biomoléculas orgánicas formadas por C, H, O, N y en menor medida P y S y otros elementos (Fe,Cu, Mg, ). Son polímeros no ramificados de
Proteínas. Cual es la gracia? KEVLAR. polímeros biológicos es su versatilidad para formar una gran variedad estructuras con funciones especializadas.
 Estructura de Proteínas KEVLAR Dr. Mauricio Baez mauricio.baez@ciq.uchile.cl uchile cl Laboratorio de Bioquímica Facultad de Ciencias Químicas y Farmacéuticas Universidad de Chile Proteínas. Co-polímeros
Estructura de Proteínas KEVLAR Dr. Mauricio Baez mauricio.baez@ciq.uchile.cl uchile cl Laboratorio de Bioquímica Facultad de Ciencias Químicas y Farmacéuticas Universidad de Chile Proteínas. Co-polímeros
CAPÍTULO 2 FLUJO DE LA INFORMACIÓN BIOLÓGICA FACULTAD DE AGRONOMÍA CURSO DE BIOQUÍMICA
 CAPÍTULO 2 FLUJO DE LA INFORMACIÓN BIOLÓGICA FACULTAD DE AGRONOMÍA CURSO DE BIOQUÍMICA Contenido 2.1 Información biológica e interacciones no covalentes. 2.2 Almacenamiento de la información biológica
CAPÍTULO 2 FLUJO DE LA INFORMACIÓN BIOLÓGICA FACULTAD DE AGRONOMÍA CURSO DE BIOQUÍMICA Contenido 2.1 Información biológica e interacciones no covalentes. 2.2 Almacenamiento de la información biológica
Guía de Biología I Medio Departamento de Ciencias Profesora NATALIA URQUIETA M.
 COLEGIO SAN CRISTOBAL Av. Diego Portales N 1.520. La Florida Guía de Biología I Medio Departamento de Ciencias Profesora NATALIA URQUIETA M. MOLÉCULAS ORGANICAS. Los componentes orgánicos de la materia
COLEGIO SAN CRISTOBAL Av. Diego Portales N 1.520. La Florida Guía de Biología I Medio Departamento de Ciencias Profesora NATALIA URQUIETA M. MOLÉCULAS ORGANICAS. Los componentes orgánicos de la materia
I) Biomoléculas 5) Proteínas I-5 PROTEÍNAS
 I-5 PROTEÍNAS CONCEPTO Y CARACTERÍSTICAS Concepto: Se pueden definir como polímeros formados por la unión, mediante enlaces peptídicos, de unidades de menor masa molecular llamadas aminoácidos. Son moléculas
I-5 PROTEÍNAS CONCEPTO Y CARACTERÍSTICAS Concepto: Se pueden definir como polímeros formados por la unión, mediante enlaces peptídicos, de unidades de menor masa molecular llamadas aminoácidos. Son moléculas
EL CONTROL DE LAS ACTIVIDADES CELULARES
 EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
Organización básica del cuerpo humano
 Organización básica del cuerpo humano I. Niveles de organización del cuerpo humano El ser humano es un organismo extremadamente complejo. Existen diferentes niveles de complejidad o de organización en
Organización básica del cuerpo humano I. Niveles de organización del cuerpo humano El ser humano es un organismo extremadamente complejo. Existen diferentes niveles de complejidad o de organización en
Aminoácidos y péptidos
 Aminoácidos y péptidos AMINOÁCIDOS: Moléculas orgánicas con un grupo amino (NH 2) y un grupo carboxilo (COOH). Los aminoácidos proteicos son α aminoácidos, que portan las dos funciones sobre el carbono
Aminoácidos y péptidos AMINOÁCIDOS: Moléculas orgánicas con un grupo amino (NH 2) y un grupo carboxilo (COOH). Los aminoácidos proteicos son α aminoácidos, que portan las dos funciones sobre el carbono
Componentes químicos de
 Componentes químicos de las célulasc Componentes químicos Las células están compuestas por una enorme cantidad y variedad de moléculas que pueden clasificarse en: Componentes inorgánicos Componentes orgánicos
Componentes químicos de las célulasc Componentes químicos Las células están compuestas por una enorme cantidad y variedad de moléculas que pueden clasificarse en: Componentes inorgánicos Componentes orgánicos
SUMARIO Ácidos nucleicos. Estructura general. Tipos principales: ADN y ARN. ADN. Estructura primaria. Estructura secundaria o modelo de Watson y Crick
 COFERENCIA 5 TÍTULO: COMPONENTES MOLECULARES: MACROMOLÉCULAS. ÁCIDOS NUCLEICOS Autor: Dr. Daniel Sánchez Serrano SUMARIO Ácidos nucleicos. Estructura general. Tipos principales: ADN y ARN. ADN. Estructura
COFERENCIA 5 TÍTULO: COMPONENTES MOLECULARES: MACROMOLÉCULAS. ÁCIDOS NUCLEICOS Autor: Dr. Daniel Sánchez Serrano SUMARIO Ácidos nucleicos. Estructura general. Tipos principales: ADN y ARN. ADN. Estructura
Biomoléculas orgánicas: Carbohidratos y Lípidos. Propiedad Intelectual Cpech
 Biología Biomoléculas orgánicas: Carbohidratos y Lípidos Repaso Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan
Biología Biomoléculas orgánicas: Carbohidratos y Lípidos Repaso Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan
Agua, carbohidratos y Lípidos
 Agua, carbohidratos y Lípidos Biomoléculas Inorgánicas Características del agua El agua es el principal e imprescindible componente del cuerpo humano. Aproximadamente el 60 % de este agua se encuentra
Agua, carbohidratos y Lípidos Biomoléculas Inorgánicas Características del agua El agua es el principal e imprescindible componente del cuerpo humano. Aproximadamente el 60 % de este agua se encuentra
BIOLOGIA GENERAL Y METODOLOGIA DE LAS CIENCIAS Trabajo Práctico Nº 1:
 BIOLOGIA GENERAL Y METODOLOGIA DE LAS CIENCIAS Trabajo Práctico Nº 1: - 1 - NIVELES DE ORGANIZACIÓN Y BIOMOLÉCULAS Objetivos: Comprender como la materia se va organizando en diferentes niveles. Diferenciar
BIOLOGIA GENERAL Y METODOLOGIA DE LAS CIENCIAS Trabajo Práctico Nº 1: - 1 - NIVELES DE ORGANIZACIÓN Y BIOMOLÉCULAS Objetivos: Comprender como la materia se va organizando en diferentes niveles. Diferenciar
Tema 1: Los seres vivos: composición y función
 Tema 1: Los seres vivos: composición y función https://www.youtube.com/watch?v=-s28cydwauo El nivel atómico El nivel atómico Bioelementos: elementos que constituyen la materia viva Fundamentales: C, H,
Tema 1: Los seres vivos: composición y función https://www.youtube.com/watch?v=-s28cydwauo El nivel atómico El nivel atómico Bioelementos: elementos que constituyen la materia viva Fundamentales: C, H,
OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo.
 1 OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo. 2 3 4 Son las moléculas que forman a los organismos o participan de su metabolismo. Orgánicas
1 OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo. 2 3 4 Son las moléculas que forman a los organismos o participan de su metabolismo. Orgánicas
MEMBRANA PLASMÁTICA. Guía de Actividades N 10
 Guía de Actividades N 10 MEMBRANA PLASMÁTICA SECTOR EJE 1 UNIDAD 1 : CIENCIAS NATURALES - BIOLOGÍA : ESTRUCTURA Y FUNCIÓN DE LOS SERES VIVOS : ESTRUCTURA Y FUNCIÓN DE LA CÉLULA ESTUDIANTE : PROFESOR :
Guía de Actividades N 10 MEMBRANA PLASMÁTICA SECTOR EJE 1 UNIDAD 1 : CIENCIAS NATURALES - BIOLOGÍA : ESTRUCTURA Y FUNCIÓN DE LOS SERES VIVOS : ESTRUCTURA Y FUNCIÓN DE LA CÉLULA ESTUDIANTE : PROFESOR :
CAPÍTULO 10 Y 11 ESTRUCTURA, FUNCIÓN Y REPLICACIÓN DE AND FACULTAD DE AGRONOMÍA CURSO DE BIOQUÍMICA
 CAPÍTULO 10 Y 11 ESTRUCTURA, FUNCIÓN Y REPLICACIÓN DE AND FACULTAD DE AGRONOMÍA CURSO DE BIOQUÍMICA INTRODUCCIÓN La transferencia de información biológica puede ser descrita con las leyes básicas de la
CAPÍTULO 10 Y 11 ESTRUCTURA, FUNCIÓN Y REPLICACIÓN DE AND FACULTAD DE AGRONOMÍA CURSO DE BIOQUÍMICA INTRODUCCIÓN La transferencia de información biológica puede ser descrita con las leyes básicas de la
La Célula. Membrana celular. UNIVERSIDAD NACIONAL DE GRAL. SAN MARTÍN ECyT BIOLOGÍA. Biología I
 La Célula. Membrana celular UNIVERSIDAD NACIONAL DE GRAL. SAN MARTÍN ECyT BIOLOGÍA Biología I Los seres vivos están formados por células Organismos unicelulares: bacterias, plantas (algas unicelulares),
La Célula. Membrana celular UNIVERSIDAD NACIONAL DE GRAL. SAN MARTÍN ECyT BIOLOGÍA Biología I Los seres vivos están formados por células Organismos unicelulares: bacterias, plantas (algas unicelulares),
Repaso Opción múltiple Macromoléculas Biológicas
 Repaso Opción múltiple Macromoléculas Biológicas 1. Por qué esta información sobre el carbono es tan importante para entender las moléculas de la vida? a. Es el esqueleto de las moléculas biológicas requeridas
Repaso Opción múltiple Macromoléculas Biológicas 1. Por qué esta información sobre el carbono es tan importante para entender las moléculas de la vida? a. Es el esqueleto de las moléculas biológicas requeridas
Biomoléculas Orgánicas II
 Biomoléculas Orgánicas II INTRODUCCIÓN Tal como se vio en la clase anterior, los elementos químicos se organizan de tal forma que aumentan su complejidad y desarrollan funciones que son específicas. En
Biomoléculas Orgánicas II INTRODUCCIÓN Tal como se vio en la clase anterior, los elementos químicos se organizan de tal forma que aumentan su complejidad y desarrollan funciones que son específicas. En
LA ORGANIZACIÓN DEL CUERPO HUMANO
 LA ORGANIZACIÓN DEL CUERPO HUMANO RICARDO, ALBERTO, PABLO Y JORGE 1º Los niveles de organización Todos los seres vivos estamos dotados de un conjunto de estructuras con sus funciones específicas. Ordenados
LA ORGANIZACIÓN DEL CUERPO HUMANO RICARDO, ALBERTO, PABLO Y JORGE 1º Los niveles de organización Todos los seres vivos estamos dotados de un conjunto de estructuras con sus funciones específicas. Ordenados
UNIDAD II. MECANISMOS CELULARES DE TRANSPORTE E INTEGRACIÓN DE SUSTANCIAS EXTRACELULARES
 UNIDAD II. MECANISMOS CELULARES DE TRANSPORTE E INTEGRACIÓN DE SUSTANCIAS EXTRACELULARES La membrana plasmática: Se encuentra rodeando a la célulac Delimita el territorio de la célula c y controla el
UNIDAD II. MECANISMOS CELULARES DE TRANSPORTE E INTEGRACIÓN DE SUSTANCIAS EXTRACELULARES La membrana plasmática: Se encuentra rodeando a la célulac Delimita el territorio de la célula c y controla el
SESIÓN 5 ESTRUCTURA DE LOS ÁCIDOS NUCLEICOS. Los Ácidos Nucleicos. Moléculas Esenciales Para La Vida
 SESIÓN 5 ESTRUCTURA DE LOS ÁCIDOS NUCLEICOS Los Ácidos Nucleicos. Moléculas Esenciales Para La Vida La secuencia de aminoácidos de un polipéptido está programada en una unidad heredable denominada gen.
SESIÓN 5 ESTRUCTURA DE LOS ÁCIDOS NUCLEICOS Los Ácidos Nucleicos. Moléculas Esenciales Para La Vida La secuencia de aminoácidos de un polipéptido está programada en una unidad heredable denominada gen.
I) Biomoléculas 6) Proteínas I-6 PROTEÍNAS
 I-6 PROTEÍNAS CONCEPTO Y CARACTERÍSTICAS Concepto: Se pueden definir como polímeros formados por la unión, mediante enlaces peptídicos, de unidades de menor masa molecular llamadas aminoácidos. Son moléculas
I-6 PROTEÍNAS CONCEPTO Y CARACTERÍSTICAS Concepto: Se pueden definir como polímeros formados por la unión, mediante enlaces peptídicos, de unidades de menor masa molecular llamadas aminoácidos. Son moléculas
4. El esquema adjunto representa la estructura de una molécula denominada lisozima.
 BLOQUE I : La base físico-química de la materia 1. a. Nombre y formule un monosacárido que contenga seis átomos de carbono. b. Indica esquemáticamente una diferencia estructural existente entre el almidón
BLOQUE I : La base físico-química de la materia 1. a. Nombre y formule un monosacárido que contenga seis átomos de carbono. b. Indica esquemáticamente una diferencia estructural existente entre el almidón
UD 5: LOS ÁCIDOS NUCLEICOS
 UD 5: LOS ÁCIDOS NUCLEICOS ÍNDICE: 1. COMPOSICIÓN QUÍMICA Y CLASIFICACIÓN 2. NUCLEÓTIDOS 3. ADN. COMPOSICIÓN QUÍMICA Y ESTRUCTURA Y PROPIEDADES. 4. ARN 1. ARN MENSAJERO 2. ARN TRANSFERENTE 3. OTROS ARNs
UD 5: LOS ÁCIDOS NUCLEICOS ÍNDICE: 1. COMPOSICIÓN QUÍMICA Y CLASIFICACIÓN 2. NUCLEÓTIDOS 3. ADN. COMPOSICIÓN QUÍMICA Y ESTRUCTURA Y PROPIEDADES. 4. ARN 1. ARN MENSAJERO 2. ARN TRANSFERENTE 3. OTROS ARNs
Células. 2ª Parte: Células procariotas. Tema 13 de Biología NS Diploma BI Curso
 Células 2ª Parte: Células procariotas Tema 13 de Biología NS Diploma BI Curso 2012-2014 Estructura de la célula procariota: Escherichia coli Las bacterias son las células procariotas típicas. Tienen pequeño
Células 2ª Parte: Células procariotas Tema 13 de Biología NS Diploma BI Curso 2012-2014 Estructura de la célula procariota: Escherichia coli Las bacterias son las células procariotas típicas. Tienen pequeño
Profesor(a): C.D. María Isabel Pérez Aguilar
 Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
TEMA 5: LOS ÁCIDOS NUCLEICOS
 TEMA 5: LOS ÁCIDOS NUCLEICOS 1. Características químicas 2. Nucleósidos y Nucleótidos 3. Estructura del ADN 4. Estructura y tipos de ARN 5. Importancia biológica de estos compuestos 1. CARACTERÍSTICAS
TEMA 5: LOS ÁCIDOS NUCLEICOS 1. Características químicas 2. Nucleósidos y Nucleótidos 3. Estructura del ADN 4. Estructura y tipos de ARN 5. Importancia biológica de estos compuestos 1. CARACTERÍSTICAS
PROTEÍNAS 1. PROTEÍNAS 2. ENZIMAS 1. PROTEÍNAS
 PROTEÍNAS 1. PROTEÍNAS Introducción Aminoácidos Estructura tridimensional de las proteínas Proteínas conjugadas Propiedades Funciones 2. ENZIMAS Introducción Estructura Clasificación Mecanismo de acción
PROTEÍNAS 1. PROTEÍNAS Introducción Aminoácidos Estructura tridimensional de las proteínas Proteínas conjugadas Propiedades Funciones 2. ENZIMAS Introducción Estructura Clasificación Mecanismo de acción
BIOQUIMICA Y FISIOLOGÍA MICROBIANA. Dra. Yenizey Merit Alvarez Cisneros
 BIOQUIMICA Y FISIOLOGÍA MICROBIANA Dra. Yenizey Merit Alvarez Cisneros Moléculas importantes para la vida Compuestos Orgánicos (contienen carbono e hidrógeno) y forma enlaces covalentes Azucares Aminoácidos
BIOQUIMICA Y FISIOLOGÍA MICROBIANA Dra. Yenizey Merit Alvarez Cisneros Moléculas importantes para la vida Compuestos Orgánicos (contienen carbono e hidrógeno) y forma enlaces covalentes Azucares Aminoácidos
Estructura tridimensional de proteínas
 Estructura tridimensional de proteínas 1. En solución acuosa, la conformación proteica esta determinada por dos factores prioritarios. Uno es la formación de un número máximo de enlaces de hidrógeno. El
Estructura tridimensional de proteínas 1. En solución acuosa, la conformación proteica esta determinada por dos factores prioritarios. Uno es la formación de un número máximo de enlaces de hidrógeno. El
INTRODUCCION A LA ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS
 INTRODUCCION A LA ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS Lic. Claudio Vidos Departamento de investigación de DEMIK Electromedicina Director del INSTITUTO CAV Rehabilitación Departamento de investigación
INTRODUCCION A LA ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS Lic. Claudio Vidos Departamento de investigación de DEMIK Electromedicina Director del INSTITUTO CAV Rehabilitación Departamento de investigación
COMPLEJO EDUCACIONAL JOAQUIN EDWARDS BELLO GUÍA REFORZAMIENTO 1 MEDIO
 COMPLEJO EDUCACIONAL JOAQUIN EDWARDS BELLO GUÍA REFORZAMIENTO 1 MEDIO NOMBRE: PJE. TOTAL: FECHA: CURSO: 1 MEDIO PJE. OBTENIDO: CALIFICACION: ASIGNATURA: BIOLOGIA UNIDAD: I - II OBJETIVO (S): CONTENIDO
COMPLEJO EDUCACIONAL JOAQUIN EDWARDS BELLO GUÍA REFORZAMIENTO 1 MEDIO NOMBRE: PJE. TOTAL: FECHA: CURSO: 1 MEDIO PJE. OBTENIDO: CALIFICACION: ASIGNATURA: BIOLOGIA UNIDAD: I - II OBJETIVO (S): CONTENIDO
01. INTRODUCCION. Conceptos previos. Verónica González Núñez Universidad de Salamanca
 01. INTRODUCCION. Conceptos previos Verónica González Núñez Universidad de Salamanca ESQUEMA. Introducción. Conceptos previos I. Principales grupos funcionales en Bioquímica II. Formación de compuestos
01. INTRODUCCION. Conceptos previos Verónica González Núñez Universidad de Salamanca ESQUEMA. Introducción. Conceptos previos I. Principales grupos funcionales en Bioquímica II. Formación de compuestos
Actividad introductoria: Aplicación en la industria de las fuerzas intermoleculares.
 Grado 10 Ciencias - Unidad 3 Cómo se relacionan los componentes del mundo? Tema Cómo afectan las fuerzas intermoleculares las propiedades de los compuestos? Curso: Nombre: Actividad introductoria: Aplicación
Grado 10 Ciencias - Unidad 3 Cómo se relacionan los componentes del mundo? Tema Cómo afectan las fuerzas intermoleculares las propiedades de los compuestos? Curso: Nombre: Actividad introductoria: Aplicación
Figura 1: Esquema de polímero
 Eje temático: Química: Fenómenos nucleares Polímeros Procesos químicos industriales Contenido: Tipos de polímeros y polimerización Nivel: Cuarto medio Polímeros. Polímeros sintéticos y naturales Polímeros
Eje temático: Química: Fenómenos nucleares Polímeros Procesos químicos industriales Contenido: Tipos de polímeros y polimerización Nivel: Cuarto medio Polímeros. Polímeros sintéticos y naturales Polímeros
La organización del cuerpo humano. Punto 1: Los niveles de organización.
 La organización del cuerpo humano Punto 1: Los niveles de organización. ATOMO MOLECULA Unidad constituyente más pequeña de la materia ordinaria. Conjunto de al menos dos átomos enlazados covalentes que
La organización del cuerpo humano Punto 1: Los niveles de organización. ATOMO MOLECULA Unidad constituyente más pequeña de la materia ordinaria. Conjunto de al menos dos átomos enlazados covalentes que
FISIOLOGÍA GENERAL Jesús Merino Pérez y María José Noriega Borge
 BIOMOLÉCULAS. PROTEÍNAS BIOMOLÉCULAS Los bioelementos se unen para formar biomoléculas, también denominadas principios inmediatos. En los seres vivos las moléculas se caracterizan por presentar una gran
BIOMOLÉCULAS. PROTEÍNAS BIOMOLÉCULAS Los bioelementos se unen para formar biomoléculas, también denominadas principios inmediatos. En los seres vivos las moléculas se caracterizan por presentar una gran
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA
 BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
1. Citosol 2. Citoesqueleto 3. Cilios y flagelos 4. El centrosoma. 1. El Citosol
 1. Citosol 2. Citoesqueleto 3. Cilios y flagelos 4. El centrosoma 1. El Citosol El Citosol, también denominado hialoplasma es el medio acuoso del citoplasma en el que se encuentran inmersos los orgánulos
1. Citosol 2. Citoesqueleto 3. Cilios y flagelos 4. El centrosoma 1. El Citosol El Citosol, también denominado hialoplasma es el medio acuoso del citoplasma en el que se encuentran inmersos los orgánulos
Tema 3. Tema 3. Péptidos.. Enlace Peptídico. Péptidos naturales de interés Biológico. Péptidos. Péptidos
 Tema 3 Tema 3 Péptidos.. Enlace Peptídico. Péptidos naturales de interés Biológico. Péptidos Enlace Peptídico Nomenclatura de péptidos Características estructurales del enlace peptídico Estéreoespecificidad
Tema 3 Tema 3 Péptidos.. Enlace Peptídico. Péptidos naturales de interés Biológico. Péptidos Enlace Peptídico Nomenclatura de péptidos Características estructurales del enlace peptídico Estéreoespecificidad
GENÉTICA MOLECULAR. El ADN, LA MOLÉCULA DE LA HERENCIA
 GENÉTICA MOLECULAR El ADN, LA MOLÉCULA DE LA HERENCIA INTRODUCCIÓN: COMENCEMOS PREGUNTÁNDONOS Qué significan estas dos palabras? GENÉTICA MOLECULAR Estudio de la genética (genes) desde el punto de vista
GENÉTICA MOLECULAR El ADN, LA MOLÉCULA DE LA HERENCIA INTRODUCCIÓN: COMENCEMOS PREGUNTÁNDONOS Qué significan estas dos palabras? GENÉTICA MOLECULAR Estudio de la genética (genes) desde el punto de vista
Proteínas. Tabla 1: Funciones de las proteínas
 Colegio Lectura Hispano Complementaria Americano Depto. de Ciencias - Biología Nivel: 4to medio Unidad I Proteínas 1 En las células, son las proteínas las macromoléculas más abundantes y las que constituyen
Colegio Lectura Hispano Complementaria Americano Depto. de Ciencias - Biología Nivel: 4to medio Unidad I Proteínas 1 En las células, son las proteínas las macromoléculas más abundantes y las que constituyen
Proteínas fibrosas. α-queratinas
 Hélices α entrecruzadas por puentes disulfuro Proteínas fibrosas α-queratinas Estructura Características Localización Estructuras resistentes e insolubles de dureza y flexibilidad variables Estructura
Hélices α entrecruzadas por puentes disulfuro Proteínas fibrosas α-queratinas Estructura Características Localización Estructuras resistentes e insolubles de dureza y flexibilidad variables Estructura
Tema 7: Características generales de los seres vivos
 Tema 7: Características generales de los seres vivos Constituyentes químicos Bioelementos-Elementos biogénicos: elementos que forman a los seres vivos. Primarios: (98%) C,H,O;N;P y S. Secundarios: Ca,
Tema 7: Características generales de los seres vivos Constituyentes químicos Bioelementos-Elementos biogénicos: elementos que forman a los seres vivos. Primarios: (98%) C,H,O;N;P y S. Secundarios: Ca,
HIDRATOS DE CARBONO Carbohidratos, sacáridos y glucidos
 1. Definición y clasificación HIDRATOS DE CARBONO Carbohidratos, sacáridos y glucidos Los carbohidratos o sacáridos (del griego: sakcharón, azúcar) Son compuestos esenciales de los organismos vivos y son
1. Definición y clasificación HIDRATOS DE CARBONO Carbohidratos, sacáridos y glucidos Los carbohidratos o sacáridos (del griego: sakcharón, azúcar) Son compuestos esenciales de los organismos vivos y son
Bloque II: Estructura y fisiología de la célula TEMA 10: LA CÉLULA EUCARIOTA: ESTRUCTURAS Y ORGÁNULOS NO MEMBRANOSOS.
 Bloque II: Estructura y fisiología de la célula TEMA 10: LA CÉLULA EUCARIOTA: ESTRUCTURAS Y ORGÁNULOS NO MEMBRANOSOS. PARED CELULAR Envoltura gruesa y rígida. En plantas, hongos, algas y bacterias. LA
Bloque II: Estructura y fisiología de la célula TEMA 10: LA CÉLULA EUCARIOTA: ESTRUCTURAS Y ORGÁNULOS NO MEMBRANOSOS. PARED CELULAR Envoltura gruesa y rígida. En plantas, hongos, algas y bacterias. LA
Actividades de los lípidos Tema 1
 Actividades de los lípidos Tema 1 parte 3 BLOQUE 1: TEST 1. Qué tipo de lípidos son los más abundantes en la membrana plasmática de la mayoría de las células? a) Fosfolípidos b) Acidos grasos esenciales
Actividades de los lípidos Tema 1 parte 3 BLOQUE 1: TEST 1. Qué tipo de lípidos son los más abundantes en la membrana plasmática de la mayoría de las células? a) Fosfolípidos b) Acidos grasos esenciales
Estructura celular. Teoría Celular. Cap. 4. Los organismos se componen de una o más células. La célula es la unidad más pequeña de la vida.
 Estructura celular Cap. 4 Teoría Celular Los organismos se componen de una o más células. Procesos metabólicos y de la herencia ocurren dentro de la célula. La célula es la unidad más pequeña de la vida.
Estructura celular Cap. 4 Teoría Celular Los organismos se componen de una o más células. Procesos metabólicos y de la herencia ocurren dentro de la célula. La célula es la unidad más pequeña de la vida.
