HIDROMORFONA (DCI) OROS
|
|
|
- Santiago Fernández Macías
- hace 6 años
- Vistas:
Transcripción
1 HIDROMORFONA (DCI) OROS Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Campus Universitario de Cartuja Cuesta del Observatorio, 4 Ap. Correos 2070, Granada España Telf , Fax Calificación(*): NO SUPONE AVANCE TERAPÉUTICO Fecha de evaluación: Junio, 2008 Nuevo principio activo Marca registrada (Laboratorio): JURNISTA (Janssen-Cilag) Presentación: 4 mg 30 comprimidos de liberación prolongada 8 mg 30 comprimidos de liberación prolongada 16 mg 30 comprimidos de liberación prolongada 32 mg 30 comprimidos de liberación prolongada Fecha autorización (procedimiento): Enero 2008 (reconocimiento mutuo) Grupo Terapéutico: N02AA03 - Analgésicos alcaloides naturales del opio Coste tratamiento/día comparativo: Principio activo...coste diario en euros - Hidromorfona OROS.4,12 - Morfina de liberación prolongada.....1,46 Fuente: Subdirección de Prestaciones. Servicio Andaluz de Salud Resumen: - Hidromorfona (HI) es un derivado semisintético de la morfina (MO) indicado para el tratamiento del dolor intenso, disponible en forma de liberación prolongada -HI OROS- que permite su administración una vez al día; siendo su factor de conversión de 1:5 (1 mg de HI equivale a 5 mg de MO). - No se ha publicado ningún ensayo clínico de HI OROS frente a MO de liberación prolongada; mientras que los resultados de un estudio de este tipo -no publicado- no han sido concluyentes. Respecto a los demás opioides, sólo se dispone de un estudio -no ciegofrente a oxicodona (OX) de liberación prolongada, cuyos resultados tampoco son concluyentes. No se dispone de ensayos que valoren HI OROS como estrategia de rotación de opioides. No obstante, de acuerdo a otros estudios disponibles con HI y a su experiencia de uso, la eficacia y el perfil de seguridad de HI se consideran similares al de MO y resto de los opioides. - Los analgésicos opioides mayores -morfina, fentanilo, oxicodona e hidromorfona- ocupan el tercer escalón en la escalera analgésica de la OMS, y son utilizados para tratar el dolor intenso. MO continúa considerándose de elección por su eficacia, flexibilidad de empleo y coste. Las formas de liberación prolongada suponen la ventaja de permitir una pauta más cómoda para el paciente.
2 - La elección de una alternativa a MO podría estar justificada cuando se presente intolerancia a la vía oral; aparición de ciertos efectos adversos; o, en su caso, por la preferencia del paciente por otra vía de administración más confortable (transdérmica). No obstante, la sustitución de MO motivada por un mal control del dolor, resulta poco frecuente y/o controvertida. - A la vista de la información disponible, la introducción de HI OROS no supone ventajas en eficacia, seguridad y pauta de administración a MO de liberación sostenida; si bien su coste es superior. Indicaciones: Hidromorfona (HI) es un derivado semisintético de la morfina (MO) indicado para el tratamiento del dolor intenso. HI, es un analgésico opioide mayor disponible en forma de liberación prolongada -HI OROS- que permite su administración una vez al día (1). Posología / Administración: La dosis depende de la naturaleza del dolor, así como de la situación clínica del paciente. Debido a la variabilidad interindividual en la respuesta a los opioides, se recomienda comenzar con una dosis baja, adecuada a la intensidad del dolor. Al inicio del tratamiento se deben considerar las medidas para prevenir las reacciones adversas conocidas (por ejemplo: estreñimiento, náuseas y vómitos), que pueden ser controladas reduciendo la dosis o mediante la administración de laxantes y/o antieméticos (1). Pacientes no sometidos a tratamiento regular con opioides: El ajuste de dosis hasta alcanzar la analgesia adecuada es más lento con las preparaciones de de liberación prolongada, por lo que puede ser aconsejable iniciar el tratamiento con preparaciones de liberación inmediata -en este caso, morfina (MO) de liberación inmediata ya que no está disponible la HI de liberación inmediata- y después convertirlas a la dosis diaria total apropiada de HI de liberación prolongada. El factor de conversión habitual HI OROS con respecto a MO es 1:5 (1). La dosis inicial en la mayoría de los pacientes de HI OROS debería ser 8 mg/ 24 h. En algunos pacientes pueden utilizarse una dosis inicial de titulación de 4 mg/ 24 h para mejorar la tolerabilidad. Si se requiere, la dosis de titulación puede aumentarse o disminuirse en 4 ó 8 mg/ 24 h, dependiendo de la respuesta y de los requerimientos analgésicos suplementarios (1). Pacientes sometidos a tratamiento regular con opioides: La dosis inicial de HI se debe basar en la dosis diaria del opioide anterior, usando el factor de conversión equianalgésico estándar, que es 1:5 para HI OROS respecto a MO. Para otros opioides, se calcula la dosis diaria total equivalente de MO, y se determina la dosis diaria total equivalente de HI OROS. Probablemente ningún factor de conversión resulta satisfactorio en todos los pacientes, debido a las diferencias interindividuales y de formulaciones, por lo que la posología se debería redondear a la baja, ajustándola a la dosis clínicamente más adecuada (1). Cuando se inicie el tratamiento con HI OROS, se debe interrumpir la administración de todos los analgésicos opioides cuya acción duración alcance 24 horas. HI OROS se puede usar de forma segura, junto con dosis habituales de analgésicos no opioides y analgésicos complementarios (1).
3 Analgesia adicional o de rescate: Además del tratamiento con HI OROS, los pacientes con dolor crónico pueden requerir preparaciones de liberación inmediata (MO de liberación inmediata) contra el dolor irruptivo. Las dosis individuales complementarias de MO de liberación inmediata no deben exceder el 10-25% de la dosis de HI de 24 horas (ver tabla) (1). Dosis de inicio recomendada para fármacos de rescate adicionales HI OROS (dosis diaria) MO liberación inmediata 4 mg 5 mg 8 mg 10 mg 16 mg mg 32 mg mg 64 mg mg Individualización de la dosis y tratamiento de mantenimiento: Los aumentos de dosis no se deben realizar en intervalos inferiores a 2 días, para que los efectos se estabilicen. Considerando en cada ajuste de dosis, incrementos del % de la dosis diaria de HI OROS administrada hasta ese momento (1). Suspensión del tratamiento Se debe ir reduciendo la dosis de HI OROS al 50% cada 2 días, hasta alcanzar la dosis más baja posible, momento en el que se puede interrumpir el tratamiento de forma segura (1). Mecanismo de acción: HI es un derivado semisintético de la MO que, como los analgésicos opioides, ejerce sus efectos farmacológicos principales sobre el SNC y el músculo liso. HI es principalmente un agonista de los receptores µ que también muestra una débil afinidad por los receptores κ. La analgesia ocurre como consecuencia de su unión a los receptores µ del SNC. Aunque las estimaciones varían (de 2 a 10 veces), parece que HI por vía oral es aproximadamente 5 veces más potente que MO (1 mg de HI equivale a 5 mg de MO) (1). Farmacocinética: Debido a las propiedades de liberación prolongada del sistema OROS, la HI se libera de manera constante y se absorbe de forma continuada durante aproximadamente 24 horas, lo que permite su administración una vez al día. La concentración estable se alcanza con la tercera dosis (1). Alternativas terapéuticas: Para el dolor grave o intenso se propone el uso de analgésicos opioides mayores o potentes, como: MO, fentanilo, oxicodona (OX) e HI. Siendo MO el opioide considerado de elección por su eficacia, flexibilidad de empleo y coste. El empleo de una alternativa podría estar justificada en caso de intolerancia a la vía oral (nauseas y vómitos); aparición de ciertos efectos adversos (agitación, confusión, acumulación de metabolitos por insuficiencia renal); o, en su caso, por la preferencia del paciente por otra vía de administración más confortable (transdérmica). No obstante, la sustitución de la MO como consecuencia de un mal control del dolor, resulta poco frecuente y/o controvertida (2).
4 Al inicio del tratamiento y para establecer la dosis, es preferible utilizar opioides de liberación rápida; una vez establecida ésta, puede administrarse una formulación de liberación prolongada (2). Comparador/es: MO de liberación prolongada Eficacia: HI es un opioide mayor que, tanto en forma de liberación inmediata como prolongada, se lleva utilizando muchos años en otros países. Este informe valora HI OROS que es una nueva formulación de liberación prolongada. Se dispone de una revisión sistemática sobre la utilización de HI en el tratamiento del dolor agudo y crónico, que incluye distintas vías de administración y formas farmacéuticas. La mayoría de los estudios incluidos se refieren a HI en administración parenteral, mientras que ninguno ha valorado la utilización de HI OROS. La revisión concluye que HI se muestra como un potente analgésico que, en términos de eficacia analgésica y tolerabilidad, se comporta como el resto de opioides mayores; considerándose la MO como la terapia de referencia (3). No se ha publicado ningún ensayo clínico aleatorizado que compare la eficacia de HI OROS frente a MO de liberación prolongada. Se dispone de los datos de un estudio no publicado (facilitado por el laboratorio) que incluía 200 pacientes con dolor crónico oncológico, que comparaba HI OROS frente a MO de liberación prolongada, durante 4 semanas. Se trata de un estudio de equivalencia cuya variable principal es la media de los 2 últimos valores medidos como peor dolor en las últimas 24 horas, según la escala BPI (Brief Pain Inventory) (4). Los resultados no son concluyentes, ya que: no se realiza el análisis por protocolo de la variable principal; no se alcanza el tamaño de muestra requerido en la rama tratada con HI OROS; y, dado el elevado porcentaje de pérdidas (49,5% de pacientes con HI OROS y 27,7% con MO). En cuanto a la comparación con otros opioides, únicamente se ha publicado un estudio de no inferioridad, aleatorizado, no ciego, comparativo frente OX de liberación prolongada. Se estudiaron 138 pacientes con artrosis (análisis de eficacia sobre 124) durante 6 semanas. La reducción media del alivio del dolor, según una escala -de 0 a 4- de las dos últimas medidas en la fase de mantenimiento fue de 2,3 tanto con HI como con OX; y, el tiempo transcurrido hasta el tercer día de alivio completo o moderado del dolor fue de 6,2 días con HI y de 5,5 días con OX. No obstante, los resultados no son concluyentes porque no se alcanza el tamaño de muestra requerido en la rama de OX (tras la exclusión de 14 pacientes del análisis de eficacia), y por el elevado porcentaje de pérdidas (39,1% con HI; 41,7% con OX) (5). Se dispone de algunos ensayos abiertos no comparativos (6-9), en pacientes con dolor oncológico y no oncológico, cuyo objetivo es confirmar el factor de conversión con otros opioides, así como la seguridad del cambio; no obstante, su metodología no permite extraer conclusiones sobre la eficacia de HI. Adicionalmente, no se dispone de ensayos que evalúen HI OROS como estrategia de rotación de opioides en aquellos pacientes en los que no se logra una analgesia adecuada con MO, o en los que ésta se ha de suspender por efectos adversos.
5 Seguridad: A dosis equianalgésicas, el perfil de efectos adversos de HI OROS es similar al de MO y el resto de los opioides. En los ensayos clínicos de HI OROS, las reacciones adversas más frecuentes fueron estreñimiento, náuseas, vómitos, somnolencia, mareos y astenia (1). Precauciones / Contraindicaciones / Uso en situaciones especiales / Interacciones: Debe utilizarse con extrema precaución en pacientes con: depresión o insuficiencia respiratoria o EPOC; traumatismo craneal e hipertensión intracraneal (1,10). Al igual que con los demás opioides, el desarrollo de dependencia psicológica o adicción, sólo ocurre en individuos predispuestos de algún modo, y no cabe esperar su desarrollo con las pautas de administración utilizadas para tratar el dolor (1). La administración de opioides junto a medicamentos IMAO puede producir excitación o depresión del SNC, hipotensión o hipertensión. El empleo concomitante de fármacos depresores del SNC tales como hipnóticos, sedantes, anestésicos generales, antipsicóticos y alcohol, puede producir efectos depresores aditivos, depresión respiratoria, hipotensión, sedación profunda o coma (1). En EEUU se retiró una forma de HI de liberación prolongada, diferente a HI OROS, porque su interacción con el alcohol aceleraba la liberación desde las cápsulas, lo que conllevaba riesgo de sobredosis y muerte (11). Se ha comprobado que esto no ocurre con HI OROS (1). Análisis comparativo: Fármaco comparador: MO DE LIBERACIÓN PROLONGADA Eficacia: SIMILAR A MO. Existen estudios de HI frente a otros opioides de los cuales se desprende que se comporta -en cuanto a su eficacia- como el resto de opioides mayores. Se dispone de un estudio no publicado de HI OROS frente a MO liberación prolongada en dolor crónico oncológico, cuyos resultados no han sido concluyentes. Con respecto a otros opioides, sólo se dispone de un estudio no ciego en artrosis frente a OX de liberación prolongada, cuyos resultados no son concluyentes. Seguridad: SIMILAR. HI es un opioide cuya seguridad está establecida ya que lleva muchos años comercializado en otros países. A dosis equianalgésicas, su perfil de efectos adversos es similar al de MO y el resto de opioides. Pauta: SIMILAR. HI OROS se administra en una dosis diaria. No se ha comercializado la forma de liberación inmediata, lo que supone un inconveniente para iniciar los tratamientos, y para la analgesia de rescate. Coste: SUPERIOR. Lugar en terapéutica: Los analgésicos opioides mayores ocupan el tercer escalón en la escalera analgésica de la OMS, y son los fármacos recomendados para tratar el dolor intenso. Las formas de liberación prolongada permiten una pauta más cómoda para el paciente (2,12). En este
6 contexto, MO de liberación prolongada es el tratamiento de elección del dolor crónico intenso (12). La eficacia y el perfil de seguridad de HI son similares al de MO y resto de los opioides. Los resultados del único estudio disponible de HI OROS frente a MO liberación prolongada en dolor crónico oncológico no son concluyentes (4). Una proporción de los pacientes con dolor oncológico que reciben MO oral sufren efectos adversos intolerables antes de alcanzar un control adecuado del dolor (13). En estos pacientes es una práctica establecida la sustitución de un opioide mayor por otro. Sin embargo, la información disponible para avalar esta práctica se basa únicamente en informes de casos y en estudios no controlados que concluyen que puede ser una estrategia útil para mejorar el control del dolor o reducir los efectos secundarios (14). En este sentido, tampoco se dispone de ensayos que valoren HI OROS como estrategia de rotación de opioides. A la vista de lo anterior, la utilización de MO oral continúa siendo el tratamiento de referencia en el tercer escalón de la escalera analgésica de la OMS (13). BIBLIOGRAFÍA 1- Ficha técnica de Jurnista. Disponible en: [consultado junio 2008] 2- Uso de opioides en el tratamiento del dolor oncológico. Bol Ter Andal 2007; 23(3): Quigley C. Hidromorfona para el dolor agudo y crónico (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus, Número 1. Oxford: Update Software Ltd. Disponible en: (Traducida de The Cochrane Library, 2008 Issue 1. Chichester, UK: John Wiley & Sons, Ltd.). [consultado junio 2008] 4- Estudio DO-118. Once a day controlled-release formulation of hydromorphone (OROS hydromorphone) versus sustained-release morphine in cancer pain. (Datos no publicados, facilitados por el laboratorio Janssen-Cilag). 5- Hale M et al. Efficacy and tolerability of once-daily OROS hydromorphone and twice-daily extended-release oxycodone in patients with chronic, moderate to severe osteoarthritis pain: results of a 6-week, randomized, open-label, noninferiority análisis. Clinical Therapeutics 2007; 29: Wallace M et al. Conversion from standard therapy to once-dayly oral extendedrelease hydromorphone in patients with chronic cancer pain. J Int Med Res 2008; 36: Wallace M et al. Efficacy and safety evaluation of once-daily OROS hydromorphone in patients with chronic low back pain: a pilot open-label study (DO-127) Curr Med Res Opin 2007; 23: Wallace M et al. Once-daily OROS hydromorphone for the management of chronic non-malignant pain: a dose-conversion and titration study. Int J Clin Pract 2007; 61:
7 9- Palangio M et al. Dose conversion and titration with a novel once-daily, OROS osmotic technology, extended-release hydromorphone formulation in the treatment of chronic malignant or non-malignant pain. J Pain Symptom Manage 2002; 23: Hydromorphone (Drug Evaluations). In: Klasko RK, editor. Drugdex System. Micromedex, Greenwood Village, Colorado (Vol Edition expires [09/2008]). 11- Palladone withdrawn. In brief. Med Let Drugs Therapeutics 2005; 47: Control of pain in patients with cancer. A National Clinical Guideline. Scottish Intercollegiate Guidelines Network (SIGN) June Disponible en: [consultado junio 2008] 13- Hanks GW et al. Morfina y opiáceos alternativos para el tratamiento del dolor oncológico: recomendaciones de la EAPC. Med Pal 2002; 9: Quigley C. Cambio de opiáceo para mejorar el alivio del dolor y la tolerancia del fármaco (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus, 2008 Número 1. Oxford: Update Software Ltd. Disponible en: (Traducida de The Cochrane Library, 2008 Issue 1. Chichester, UK: John Wiley & Sons, Ltd.). [consultado junio 2008] (*)CALIFICACIÓN No valorable: información insuficiente No supone avance terapéutico Aporta en situaciones concretas Modesta mejora terapéutica Importante mejora terapéutica DEFINICIÓN La bibliografía disponible sobre la novedad es insuficiente, poco concluyente o no se dispone de ensayos clínicos de calidad frente a comparadores adecuados, lo que no permite identificar su grado de aportación terapéutica La novedad no aporta ventajas frente a otros medicamentos ya disponibles en la indicación para la que ha sido autorizado La novedad puede ser de utilidad en alguna situación clínica y/o en un grupo determinado de pacientes La novedad aporta ventajas relacionadas con la comodidad posológica y/o el coste del tratamiento La novedad representa una clara ventaja en términos de eficacia y/o seguridad frente a las alternativas terapéuticas disponibles para la misma indicación o condición clínica. Este informe ha sido realizado de acuerdo con el Procedimiento Normalizado de Trabajo de los Comités de Evaluación de Nuevos Medicamentos de Andalucía, Aragón, Cataluña, Navarra y País Vasco; y revisado por el Grupo Multidisciplinar de Expertos en Uso Racional de Medicamentos del Servicio Andaluz de Salud.. La evaluación de novedades terapéuticas en el momento de su comercialización se apoya en información cuya validez puede verse limitada con el paso del tiempo, por lo que debe ser empleada con precaución.. Queda totalmente prohibido el uso de este documento con fines promocionales.
8 Referencia (Autor, publicación) INFORME DE HIDROMORFONA: TABLA RESUMEN DE ENSAYOS CLÍNICOS CONTROLADOS (ECR) Tipo de estudio Pauta de Comentarios y objetivo tratamiento Población estudiada (criterios de inclusión y exclusión) Variables de medida (endpoint) Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Campus Universitario de Cartuja Cuesta del Observatorio, 4 Ap. Correos 2070, Granada España Telf , Fax Resultados (tamaño / valores p / intervalos de confianza) Calidad del estudio (escala Jadad) (*) Estudio DO-118 (no publicado) proporcionado por el laboratorio Janssen-Cilag. (Fecha finalización estudio año 2001) Estudio de equivalencia, aleatorizado, multicéntrico, doble ciego con doble enmascaramiento y control activo Objetivo principal: demostrar la equivalencia clínica de la eficacia de HI LI y HI LP y de MO LI y MO LP en el tratamiento del dolor crónico oncológico 200 pacientes 18 años, con dolor oncológico en tratamiento con opioides mayores o en los que el tratamiento con opioides mayores 1vez/d resulte adecuado Estudio realizado en 2 fases: - Fase I: 2-9 días de titulación HI LI: n=99 MO LI: n=101 - Fase II: días mantenimiento HI LP: n=77 MO LP: n=86 Criterios de Fase I: titulación con opioides de LI, hasta alcanzar control del dolor durante 2 días consecutivos con la misma dosis de medicación y 3 dosis de medicación de rescate en las últimas 24 horas HI LI: MO LI: (Pauta cada 4 horas) Fase II: Se comienza con la dosis alcanzada en la fase anterior y las titulaciones se hacen cada 2 días. Media de los dos últimos valores, medidos como peor dolor en las últimas 24 horas de cada fase en la escala BPI (escala numérica de 0: no dolor, a 10: peor dolor). Los dos tratamientos se consideraron equivalentes si el 95% del IC de dos colas de la diferencia oscilaba entre -1,5 y 1,5 Fase I: -0,4 a 0,9 Se consideran equivalentes las 2 medicaciones de LI Fase II: -1,6 a -0,01 No se pueden considerar equivalentes, porque el -1,6 se sale de los límites prefijados. Variable principal: HI LI: 5 MO LI: 4,8 HI LP: 3,5 MO LP: 4,1 Medicación de rescate en los 2 últimos días: No se presentan los datos de la variable principal del análisis por protocolo Pérdidas: en la rama de HI, en la fase II, no se alcanza el tamaño de muestra requerido Total: 5 puntos Aleatorización:1 Doble ciego: 1 Pérdidas:1 Aleatorización adecuada: 1 Doble ciego adecuado:1
9 exclusión: norespondedores a opioides, que tras la aleatorización requieren otro analgésico opioide adicional a los del estudio, enfermedad gastrointestinal severa, situaciones en las que el riesgo potencial supera el beneficio como: tensión intracraneal elevada, hipotensión, hipotiroidismo, asma, hipertrofia prostática, insuficiencia hepática o renal, ancianos y debilitados, alteraciones convulsivas, enfermedad de Addison, etc. Se completa la fase tras al menos 10 días, si se obtienen dosis estables de control del dolor al menos los 2 últimos días HI LP: (Pauta cada 24 horas) MO LP: (Pauta cada 12 horas) Se ha considerado un ratio de equipotencia de 1:5 (MO:HI) Se permitió medicación de rescate en forma de LI HI LI: 2,1 MO LI: 1,4 (p=0,02) HI LP: 1,7 MO LP: 1,5 (p=0,52) Seguridad: Porcentaje de pacientes que sufre un efecto adverso (Fase II) : HI:79%; MO: 87%
10 Hale M, et al. Clinical Therapeutics. 2007; 29(5): EC aleatorizado, multicéntrico, abierto, de grupos paralelos, de no inferioridad Objetivo: comparar la eficacia y tolerabilidad de HI OROS 1 vez/d frente a OX LP 2 veces/d en pacientes con dolor crónico moderado a severo por artrosis 124 pacientes( a ) 18 años con osteoartrosis de rodilla o cadera desde al menos 3 meses antes de su reclutamiento y con dolor moderado a severo a pesar de tratamiento con AINE u otras terapias no opioides. Duración: 6 semanas (2 de titulación de dosis y estabilización y 4 de mantenimiento) Criterios de exclusión: Diagnóstico de otra artritis inflamatoria o gota, disfagia o incapacidad para tragar cápsulas, alteraciones gastrointestinales que puedan afectar la absorción o el tránsito de fármacos, reemplazo de la articulación afectada, uso de esteroides 90 días antes de la 1ª visita, etc. HI: n=64 D. inicial: 8 ; D. media de mantenimiento:16 OX: n=60 D.inicial: 10mg/12 h D.media de mantenimiento: 24 Variables principales: Reducción media en la puntuación del alivio del dolor (escala 0 a 4) Tiempo hasta obtener 3 días seguidos de alivio completo o moderado del dolor Se definió el margen de no inferioridad como δ: 0,46 HI: 2,3 OX: 2,3 IC 95%(-0,3 a ) HI: 6,2 (días) OX: 5,5 (días) IC 95% (-0,31 a ) RA relacionadas con el medicamento: HI:78,9% OX: 79,1% RA que llevaron al abandono: HI 35,2%; OX 32,8%. RA más frecuentes (HI, OX): Náuseas: (35,2%, 29,9%) Estreñimiento: (29,6%,25,4%;) somnolencia: (25,4%, 17,9%) Vómitos: (16,9%, 11,9%); mareos: (14,1%, 22,4%) dolor de cabeza: (5,6%,10,4%). ( a ) Aunque 138 pacientes reciben el tratamiento, el análisis de eficacia se hace sobre 124 pacientes ya que se excluyeron los 14 pacientes reclutados en uno de los centros (7 de cada rama). Esto, hace que en la rama de OX no se alcance el tamaño de muestra requerido (n=62). Pérdidas totales: 39,9% Total: 2 puntos Aleatorización:1 Doble ciego: 0 Pérdidas:1 Aleatorización adecuada: 0
11 AINE: Antiinflamatorio no esteroideo D: Dosis MO: morfina HI OROS: forma patentada de hidromorfona de liberación prolongada HI: Hidromorfona IC: Intervalo de confianza LI: Liberación inmediata LP: liberación prolongada OX: Oxicodona RA: Reacciones adversas BPI: Brief Pain Inventory (*) Rango de puntuación: 0-5. Estudio de baja calidad: puntuación < 3
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN Principio activo HIDROMORFONA OROS Nombre comercial y presentaciones Grupo terapéutico Condiciones de dispensación Procedimiento
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE ARAGÓN INFORME DE EVALUACIÓN Principio activo HIDROMORFONA OROS Nombre comercial y presentaciones Grupo terapéutico Condiciones de dispensación Procedimiento
Tabla de equivalencia aproximada entre opioides
 Tabla de equivalencia aproximada entre opioides Documentos www.1aria.com DOSIS EQUIPOTENTES BUPRENORFINA PARCHE TRANSDÉRMICO 8,75 µg/h (0,2 ) 17,5 µg/h (0,4 ) 35 µg/h (0,8 ) 52,5 µg/h (1,2 ) 70 µg/h (1,6
Tabla de equivalencia aproximada entre opioides Documentos www.1aria.com DOSIS EQUIPOTENTES BUPRENORFINA PARCHE TRANSDÉRMICO 8,75 µg/h (0,2 ) 17,5 µg/h (0,4 ) 35 µg/h (0,8 ) 52,5 µg/h (1,2 ) 70 µg/h (1,6
Anexo 6. Dosificación de opioides en el dolor
 Anexo 6. Dosificación de opioides en el dolor Equivalencia aproximada entre opioides El factor de conversión se expresa como fracción con respecto a morfina oral o en mg respecto a una dosis de 30 mg de
Anexo 6. Dosificación de opioides en el dolor Equivalencia aproximada entre opioides El factor de conversión se expresa como fracción con respecto a morfina oral o en mg respecto a una dosis de 30 mg de
PEDRO MESA RODRIGUEZ (Tutor: Dra Avellaneda) Dosis inicial 4-6h 30mg/ 6h v.o. Normal 5h Retard 14-24h
 ESCALERA ANALGÉSICA DE LA OMS 1º ESCALON 2º ESCALON 3º ESCALON Dolor leve Dolor moderado Dolor intenso Opioides potentes +/- coanalgésicos Opioides débiles +/- coanalgésicos ASCENSOR ANALGÉSICO Ascensor
ESCALERA ANALGÉSICA DE LA OMS 1º ESCALON 2º ESCALON 3º ESCALON Dolor leve Dolor moderado Dolor intenso Opioides potentes +/- coanalgésicos Opioides débiles +/- coanalgésicos ASCENSOR ANALGÉSICO Ascensor
Nuria Romero Laorden. Growing Up 14 de Febrero de 2012
 Nuria Romero Laorden R4 Oncología Médica HUFA Growing Up 14 de Febrero de 2012 1. Morfina 2. Oi Oxicodona 3. Fentanilo 4. Buprenorfina 5. Hidromorfona 6. Metadona OPIÁCEO: Sustancias que se extraen de
Nuria Romero Laorden R4 Oncología Médica HUFA Growing Up 14 de Febrero de 2012 1. Morfina 2. Oi Oxicodona 3. Fentanilo 4. Buprenorfina 5. Hidromorfona 6. Metadona OPIÁCEO: Sustancias que se extraen de
Calificación(*): APORTA EN SITUACIONES CONCRETAS. Marca/s registrada/s (Laboratorio/s): Relistor (Wyeth Europa Ltd).
 Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Campus Universitario de Cartuja Cuesta del Observatorio, 4 Ap. Correos 2070, Granada 18080. España Telf. +34 958 027 400, Fax 958
Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Campus Universitario de Cartuja Cuesta del Observatorio, 4 Ap. Correos 2070, Granada 18080. España Telf. +34 958 027 400, Fax 958
Oxicodona. . Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante.
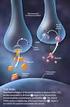 Oxicodona 1. Grupo Farmacoterapéutico:. Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante. 2.- Formas farmacéuticas registradas:. Comprimidos de 10mg
Oxicodona 1. Grupo Farmacoterapéutico:. Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante. 2.- Formas farmacéuticas registradas:. Comprimidos de 10mg
Aplicabilidad. Barreras. Indicadores para la. implantación
 Aplicabilidad. Barreras. Indicadores para la implantación 5 5. Aplicabilidad. Barreras. Indicadores para la implantación Aplicabilidad: Para facilitar la aplicación de las recomendaciones de la guía y
Aplicabilidad. Barreras. Indicadores para la implantación 5 5. Aplicabilidad. Barreras. Indicadores para la implantación Aplicabilidad: Para facilitar la aplicación de las recomendaciones de la guía y
Morera T, Jaureguizar N. OCW UPV/EHU Farmacología Aplicada en Odontología
 Morera T, Jaureguizar N. OCW UPV/EHU 2016 Farmacología Aplicada en Odontología 1. La ansiedad en la consulta odontológica 2. Prescripción de fármacos ansiolíticos A. Características farmacocinéticas B.
Morera T, Jaureguizar N. OCW UPV/EHU 2016 Farmacología Aplicada en Odontología 1. La ansiedad en la consulta odontológica 2. Prescripción de fármacos ansiolíticos A. Características farmacocinéticas B.
ESTRATEGIAS TERAPÉUTICAS EN EL DOLOR
 ESTRATEGIAS TERAPÉUTICAS EN EL DOLOR José Rufo Jiménez MIR UGC Luis Taracido 12 Abril 2013 Qué es el dolor? Experiencia sensorial asociada a una lesión tisular. Síntoma más frecuente. Frecuentemente se
ESTRATEGIAS TERAPÉUTICAS EN EL DOLOR José Rufo Jiménez MIR UGC Luis Taracido 12 Abril 2013 Qué es el dolor? Experiencia sensorial asociada a una lesión tisular. Síntoma más frecuente. Frecuentemente se
Aspectos prácticos en el tratamiento del dolor en el paciente oncológico Evaluación y manejo
 Aspectos prácticos en el tratamiento del dolor en el paciente oncológico Evaluación y manejo JM Campos S. Oncología Médica H. Arnau de Vilanova de Valencia DOLOR Indice de contenidos Dolor en el paciente
Aspectos prácticos en el tratamiento del dolor en el paciente oncológico Evaluación y manejo JM Campos S. Oncología Médica H. Arnau de Vilanova de Valencia DOLOR Indice de contenidos Dolor en el paciente
Efectos secundarios de sobredosis con tramadol
 Efectos secundarios de sobredosis con tramadol The Borg System is 100 % Efectos secundarios de sobredosis con tramadol Hola, Desde hace, al menos, 5 años tomo Tramadol para aliviarme los dolores persistentes
Efectos secundarios de sobredosis con tramadol The Borg System is 100 % Efectos secundarios de sobredosis con tramadol Hola, Desde hace, al menos, 5 años tomo Tramadol para aliviarme los dolores persistentes
Resumen de las recomendaciones
 Resumen de las recomendaciones 1. Cuál es el fármaco de primera elección para el tratamiento de pacientes en situación terminal con dolor moderado no controlado, o intenso? En pacientes en situación terminal,
Resumen de las recomendaciones 1. Cuál es el fármaco de primera elección para el tratamiento de pacientes en situación terminal con dolor moderado no controlado, o intenso? En pacientes en situación terminal,
FICHA DE INFORMACIÓN AL PACIENTE: DIHIDROCODEÍNA
 FICHA DE INFORMACIÓN AL PACIENTE: DIHIDROCODEÍNA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Analgésico opiáceo narcótico. Antitusígeno. 1.2 Cómo actúa este fármaco: La dihidrocodeína se une a unos receptores
FICHA DE INFORMACIÓN AL PACIENTE: DIHIDROCODEÍNA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Analgésico opiáceo narcótico. Antitusígeno. 1.2 Cómo actúa este fármaco: La dihidrocodeína se une a unos receptores
Efectos de tramadol en perros
 Search Search Efectos de tramadol en perros Únete a más de 15,000 usuarios! Y recibe nuestro boletin con ofertas, noticias y artículos interesantes sobre perros directo a tu email. El tramadol (nombre
Search Search Efectos de tramadol en perros Únete a más de 15,000 usuarios! Y recibe nuestro boletin con ofertas, noticias y artículos interesantes sobre perros directo a tu email. El tramadol (nombre
Analgésicos Opioides II. Según la OMS: clasificación clínica. Agonista potente. MORFINA Absorción Hidrosoluble: diferentes vías de administración
 Analgésicos Opioides II Dra. Teresa Pelissier Medicina 2011 Según la OMS: clasificación clínica Agonistas potentes Morfina Heroína: 3, 6 diacetil morfina Oxicodona Metadona Petidina Buprenorfina Fentanil
Analgésicos Opioides II Dra. Teresa Pelissier Medicina 2011 Según la OMS: clasificación clínica Agonistas potentes Morfina Heroína: 3, 6 diacetil morfina Oxicodona Metadona Petidina Buprenorfina Fentanil
Marca/s registrada/s (Laboratorio/s): INVEGA (Janssen-Cilag) Fecha autorización (procedimiento): Septiembre, 2007 (centralizado)
 PALIPERIDONA (DCI) Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Campus Universitario de Cartuja Cuesta del Observatorio, 4 Ap. Correos 2070, Granada 18080. España Telf. +34 958
PALIPERIDONA (DCI) Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Campus Universitario de Cartuja Cuesta del Observatorio, 4 Ap. Correos 2070, Granada 18080. España Telf. +34 958
MIELOMA MÚLTIPLE: Bortezomib 1/6
 MIELOMA MÚLTIPLE: Bortezomib 1/6 1. DENOMINACIÓN DEL ESQUEMA: BORTEZOMIB 2. USO TERAPÉUTICO (1) : Tratamiento de pacientes con mieloma múltiple que han recibido al menos dos tratamientos previos y que
MIELOMA MÚLTIPLE: Bortezomib 1/6 1. DENOMINACIÓN DEL ESQUEMA: BORTEZOMIB 2. USO TERAPÉUTICO (1) : Tratamiento de pacientes con mieloma múltiple que han recibido al menos dos tratamientos previos y que
A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN
 10 FENTANILO TRANSMUCOSA A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN 1. Denominación común internacional (DCI), denominación oficial española (DOE) o nombre genérico del principio activo. FENTANILO
10 FENTANILO TRANSMUCOSA A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN 1. Denominación común internacional (DCI), denominación oficial española (DOE) o nombre genérico del principio activo. FENTANILO
Calificación (*): NO SUPONE UN AVANCE TERAPÉUTICO
 MEDICAMENTO (DCI): ENALAPRIL (DCI) / LERCANIDIPINO (DCI) Calificación (*): NO SUPONE UN AVANCE TERAPÉUTICO Fecha de evaluación: Julio 2010 Nueva asociación Marca/s registrada/s (Laboratorio/s): Zanipress
MEDICAMENTO (DCI): ENALAPRIL (DCI) / LERCANIDIPINO (DCI) Calificación (*): NO SUPONE UN AVANCE TERAPÉUTICO Fecha de evaluación: Julio 2010 Nueva asociación Marca/s registrada/s (Laboratorio/s): Zanipress
NOMBRE DEL FÁRMACO e indicación clínica (Informe para la Comisión de Farmacia y Terapéutica del Hospital xxxxxxxxxx) Fecha xx/xx/xx
 NOMBRE DEL FÁRMACO e indicación clínica (Informe para la Comisión de Farmacia y Terapéutica del Hospital xxxxxxxxxx) Fecha xx/xx/xx 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Indicación
NOMBRE DEL FÁRMACO e indicación clínica (Informe para la Comisión de Farmacia y Terapéutica del Hospital xxxxxxxxxx) Fecha xx/xx/xx 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Indicación
INFORME DE EVALUACIÓN HIDROMORFONA OROS. Comparador: MORFINA DE LIBERACIÓN CONTROLADA NO SUPONE UN AVANCE TERAPÉUTICO. Lactosa
 INFORME DE EVALUACIÓN HIDROMORFONA OROS Comparador: MORFINA DE LIBERACIÓN CONTROLADA NO SUPONE UN AVANCE TERAPÉUTICO Principio activo Nombre comercial y presentaciones: HIDROMORFINA OROS JURNISTA (Janssen-Cilag)
INFORME DE EVALUACIÓN HIDROMORFONA OROS Comparador: MORFINA DE LIBERACIÓN CONTROLADA NO SUPONE UN AVANCE TERAPÉUTICO Principio activo Nombre comercial y presentaciones: HIDROMORFINA OROS JURNISTA (Janssen-Cilag)
FICHA TÉCNICA. Excipientes: Microgránulos de sacarosa y almidón de maíz, PEG 4000, Aquacoat ECD 30, Sebacato de dibutilo y Talco.
 1. NOMBRE DEL MEDICAMENTO SKENAN 10, 30, 60 y 100 FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA El contenido en principio activo para cada Especialidad es de: 10, 30, 60 ó 100 mg de Sulfato de
1. NOMBRE DEL MEDICAMENTO SKENAN 10, 30, 60 y 100 FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA El contenido en principio activo para cada Especialidad es de: 10, 30, 60 ó 100 mg de Sulfato de
Tema 13 Analgésicos opioides
 Tema 13 Analgésicos opioides Farmacología en fisioterapia OpenCourseWare UPV/EHU OCW-2017 Dr. Iván Manuel Vicente Dra. María Torrecilla Sesma Dpto. Farmacología UPV/EHU Resumen del contenido Generalidades:
Tema 13 Analgésicos opioides Farmacología en fisioterapia OpenCourseWare UPV/EHU OCW-2017 Dr. Iván Manuel Vicente Dra. María Torrecilla Sesma Dpto. Farmacología UPV/EHU Resumen del contenido Generalidades:
MARCAR CON UNA X LA RESPUESTA CORRECTA
 Unidad Didáctica 2. Test de evaluación MARCAR CON UNA X LA RESPUESTA CORRECTA 1. Ante un posible cuadro de dependencia y tolerancia, hay que tener en cuenta que: A. Nunca se deben administrar opioides
Unidad Didáctica 2. Test de evaluación MARCAR CON UNA X LA RESPUESTA CORRECTA 1. Ante un posible cuadro de dependencia y tolerancia, hay que tener en cuenta que: A. Nunca se deben administrar opioides
INFORME ETES-DAUM-DIGEMID/MINSA
 INFORME ETES-DAUM-DIGEMID/MINSA Proceso: Revisión y actualización del Petitorio Nacional Único de Medicamentos Esenciales (PNUME) Solicitante: Equipo Técnico para el proceso de revisión y actualización
INFORME ETES-DAUM-DIGEMID/MINSA Proceso: Revisión y actualización del Petitorio Nacional Único de Medicamentos Esenciales (PNUME) Solicitante: Equipo Técnico para el proceso de revisión y actualización
TRINITRATO DE GLICERILO (DCI) Marca registrada (Laboratorio): Rectogesic (ProStrakan Limited)
 Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Campus Universitario de Cartuja Cuesta del Observatorio, 4 Ap. Correos V 2070, Granada 18080. España Telf. +34 958 027 400, Fax 958
Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Campus Universitario de Cartuja Cuesta del Observatorio, 4 Ap. Correos V 2070, Granada 18080. España Telf. +34 958 027 400, Fax 958
FICHA TÉCNICA. Excipientes con efecto conocido: Cada comprimido contiene: 200 mg de sacarosa y 240 mg de sorbitol (E-420).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Simeticona Normon 40 mg comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Simeticona... 40 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Simeticona Normon 40 mg comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Simeticona... 40 mg Excipientes con efecto conocido:
Consentimiento informado para el uso de opioides potentes y de acción ultrarrápida fuera de las indicaciones autorizadas en su ficha técnica
 Consentimiento informado para el uso de opioides potentes y de acción ultrarrápida fuera de las indicaciones autorizadas en su ficha técnica DATOS DEL PACIENTE: Nombre Edad DATOS DEL FACULTATIVO QUE FACILITA
Consentimiento informado para el uso de opioides potentes y de acción ultrarrápida fuera de las indicaciones autorizadas en su ficha técnica DATOS DEL PACIENTE: Nombre Edad DATOS DEL FACULTATIVO QUE FACILITA
Symbicort. Down. Estudio SUND: Dosis ajustable de budesonida/formoterol en comparación con salmeterol/fluticasona en dosis fija
 Estudio SUND: Dosis ajustable de budesonida/formoterol en comparación con salmeterol/fluticasona en dosis fija Dr Francisco González Vargas Servicio de Neumología Jefe de Sección de la Unidad de Consultas
Estudio SUND: Dosis ajustable de budesonida/formoterol en comparación con salmeterol/fluticasona en dosis fija Dr Francisco González Vargas Servicio de Neumología Jefe de Sección de la Unidad de Consultas
TACROLIMUS de liberación prolongada
 TACROLIMUS de liberación prolongada Profilaxis rechazo transplante hepático Informe para la Comisión de Farmacia y Terapéutica del Hospital Universitario Central de Asturias Junio 2008 1.- IDENTIFICACIÓN
TACROLIMUS de liberación prolongada Profilaxis rechazo transplante hepático Informe para la Comisión de Farmacia y Terapéutica del Hospital Universitario Central de Asturias Junio 2008 1.- IDENTIFICACIÓN
DESARROLLO CLÍNICO DE LOS MEDICAMENTOS
 V EDICIÓN LA BUENA PRÁCTICA CLÍNICA EN LOS ENSAYOS CLÍNICOS 7-8 de ABRIL de 2015 DESARROLLO CLÍNICO DE LOS MEDICAMENTOS Dra. Dolores Ochoa Mazarro Servicio de Farmacología Clínica Hospital Universitario
V EDICIÓN LA BUENA PRÁCTICA CLÍNICA EN LOS ENSAYOS CLÍNICOS 7-8 de ABRIL de 2015 DESARROLLO CLÍNICO DE LOS MEDICAMENTOS Dra. Dolores Ochoa Mazarro Servicio de Farmacología Clínica Hospital Universitario
Conclusiones científicas
 Anexo II Conclusiones científicas y motivos para la revocación o modificación de los términos de las autorizaciones de comercialización y explicación detallada de las diferencias de la recomendación del
Anexo II Conclusiones científicas y motivos para la revocación o modificación de los términos de las autorizaciones de comercialización y explicación detallada de las diferencias de la recomendación del
MIELOMA MÚLTIPLE: MP 1/5. 1. DENOMINACIÓN DEL ESQUEMA: MP (Melfalán-Prednisona).
 MIELOMA MÚLTIPLE: MP 1/5 1. DENOMINACIÓN DEL ESQUEMA: MP (Melfalán-Prednisona). 2. USO TERAPÉUTICO (1). Mieloma múltiple. Tratamiento de primera línea cuando no está indicado el trasplante de células progenitoras
MIELOMA MÚLTIPLE: MP 1/5 1. DENOMINACIÓN DEL ESQUEMA: MP (Melfalán-Prednisona). 2. USO TERAPÉUTICO (1). Mieloma múltiple. Tratamiento de primera línea cuando no está indicado el trasplante de células progenitoras
Ficha técnica Página 1
 1. NOMBRE DEL MEDICAMENTO: Difur 120 mg cápsulas duras. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada cápsula contiene 120 mg de extracto seco de rizoma de Polypodium leucotomos L. (DER nativo 4-6:1)
1. NOMBRE DEL MEDICAMENTO: Difur 120 mg cápsulas duras. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada cápsula contiene 120 mg de extracto seco de rizoma de Polypodium leucotomos L. (DER nativo 4-6:1)
Hidromorfona (Jurnista ) Dolor intenso Informe para la Comisión de Farmacia y Terapéutica de Clínica Universitaria de Navarra Fecha 21/04/2009
 CLINICA UNIVERSITARIA Centro de Información de Medicamentos Servicio de Farmacia. Tfno. 948-25 54 00 ext. 4122 Hidromorfona (Jurnista ) Dolor intenso Informe para la Comisión de Farmacia y Terapéutica
CLINICA UNIVERSITARIA Centro de Información de Medicamentos Servicio de Farmacia. Tfno. 948-25 54 00 ext. 4122 Hidromorfona (Jurnista ) Dolor intenso Informe para la Comisión de Farmacia y Terapéutica
TOMES POR TU CUENTA MÁS DOSIS NI CON DISTINTA FRECUENCIA QUE LA QUE TE HAYA RECOMENDADO TU MÉDICO.
 Usos del tramadol The Borg System is 100 % Usos del tramadol TRAMADOL: Conoce con Onmeda los efectos secundarios que pueden derivar del uso de TRAMADOL. Consulta las interacciones de TRAMADOL antes de
Usos del tramadol The Borg System is 100 % Usos del tramadol TRAMADOL: Conoce con Onmeda los efectos secundarios que pueden derivar del uso de TRAMADOL. Consulta las interacciones de TRAMADOL antes de
VENLAFAXINA RETARD STADA EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA
 OBJETIVO VENLAFAXINA RETARD STADA RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA El Estudio de Bioequivalencia de Retard STADA se ha realizado siguiendo las Directrices que la Unión Europea recomienda para demostrar
OBJETIVO VENLAFAXINA RETARD STADA RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA El Estudio de Bioequivalencia de Retard STADA se ha realizado siguiendo las Directrices que la Unión Europea recomienda para demostrar
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
FENTANILO CITRATO (ABSTRAL / PROSTRAKAN LIMITED, S.A.)
 FENTANILO CITRATO (ABSTRAL / PROSTRAKAN LIMITED, S.A.) Presentación CN 662279: 100 mcg comp sublinguales E/30 CN 662281: 200 mcg comp sublinguales E/30 CN 662283: 300 mcg comp sublinguales E/30 CN 662285:
FENTANILO CITRATO (ABSTRAL / PROSTRAKAN LIMITED, S.A.) Presentación CN 662279: 100 mcg comp sublinguales E/30 CN 662281: 200 mcg comp sublinguales E/30 CN 662283: 300 mcg comp sublinguales E/30 CN 662285:
Dosis maxima diaria diazepam
 Cari untuk: Cari Cari Dosis maxima diaria diazepam Antidepresivos, ansiedad, pastillas para dormir Zolpidem, Xanax, Modafinil, Diazepam, Rivotril, Zoloft, Citalopram y mas en linea sin receta medica con
Cari untuk: Cari Cari Dosis maxima diaria diazepam Antidepresivos, ansiedad, pastillas para dormir Zolpidem, Xanax, Modafinil, Diazepam, Rivotril, Zoloft, Citalopram y mas en linea sin receta medica con
Uso del medicamento tramadol
 Cari untuk: Cari Cari Uso del medicamento tramadol Información relativa al paciente del fármaco tramadol en esta guía del medicamento. ha creado para uso del profesional de la salud y. El Tramadol clorhidrato
Cari untuk: Cari Cari Uso del medicamento tramadol Información relativa al paciente del fármaco tramadol en esta guía del medicamento. ha creado para uso del profesional de la salud y. El Tramadol clorhidrato
FICHA TÉCNICA. Supositorios incoloros semitransparentes envasados en blíster de aluminio-polietileno.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SUPOSITORIOS DE GLICERINA MICRALAX ADULTOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Supositorios incoloros semitransparentes envasados en
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SUPOSITORIOS DE GLICERINA MICRALAX ADULTOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1 Descripción general Supositorios incoloros semitransparentes envasados en
Diseños de No- inferioridad
 Diseños de No- inferioridad Ferran.Torres@uab.es 1 OBJETIVOS DEL ENSAYO CLÍNICO Demostración n de la eficacia y/o seguridad de un tratamiento (per se). ENSAYOS FRENTE A PLACEBO Evaluación n comparativa
Diseños de No- inferioridad Ferran.Torres@uab.es 1 OBJETIVOS DEL ENSAYO CLÍNICO Demostración n de la eficacia y/o seguridad de un tratamiento (per se). ENSAYOS FRENTE A PLACEBO Evaluación n comparativa
Anexo II. Conclusiones científicas y motivos para la modificación de los términos de la autorización de comercialización
 Anexo II Conclusiones científicas y motivos para la modificación de los términos de la autorización de comercialización 21 Conclusiones científicas Resumen general de la evaluación científica de Oxynal
Anexo II Conclusiones científicas y motivos para la modificación de los términos de la autorización de comercialización 21 Conclusiones científicas Resumen general de la evaluación científica de Oxynal
Actuación protocolizada del tratamiento del dolor irruptivo / incidental
 Actuación protocolizada del tratamiento del dolor irruptivo / incidental El tratamiento del dolor crónico oncológico debe contemplar el tratamiento analgésico basal y el uso de dosis extras de los analgésicos
Actuación protocolizada del tratamiento del dolor irruptivo / incidental El tratamiento del dolor crónico oncológico debe contemplar el tratamiento analgésico basal y el uso de dosis extras de los analgésicos
Tipología de Ensayos Clínicos
 Tipología de Ensayos Clínicos Ana Gallego CRA Novartis Definición Ensayo Clínico es toda evaluación experimental de una sustancia, medicamento, intervención terapéutica a través de su aplicación en seres
Tipología de Ensayos Clínicos Ana Gallego CRA Novartis Definición Ensayo Clínico es toda evaluación experimental de una sustancia, medicamento, intervención terapéutica a través de su aplicación en seres
FICHA DE INFORMACIÓN AL PACIENTE: MIANSERINA
 FICHA DE INFORMACIÓN AL PACIENTE: MIANSERINA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Antidepresivo, con intensa actividad sedante, ligera antihistamínica H-1 y escasa anticolinérgica. 1.2 Cómo actúa
FICHA DE INFORMACIÓN AL PACIENTE: MIANSERINA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Antidepresivo, con intensa actividad sedante, ligera antihistamínica H-1 y escasa anticolinérgica. 1.2 Cómo actúa
Departamento de Farmacología y Terapéutica 2013
 Departamento de Farmacología y Terapéutica 2013 Contribuir a preservar o mejorar la salud y bienestar del paciente. Maximizar la efectividad en el uso de los medicamentos. Minimizar los riesgos a los que
Departamento de Farmacología y Terapéutica 2013 Contribuir a preservar o mejorar la salud y bienestar del paciente. Maximizar la efectividad en el uso de los medicamentos. Minimizar los riesgos a los que
Principios activos Eficacia Seguridad Conveniencia Niveles 1 Paracetamol +++ +++ +++ 1-2-3. 2 Ibuprofeno +++ ++ ++ 1-2-3
 Título: DOLOR Codificación CIE 10 R52.0 dolor agudo R52.1 dolor crónico intratable R52.9 dolor, no especificado Problema: El dolor es un signo y un síntoma, una experiencia anormal sensorial producida
Título: DOLOR Codificación CIE 10 R52.0 dolor agudo R52.1 dolor crónico intratable R52.9 dolor, no especificado Problema: El dolor es un signo y un síntoma, una experiencia anormal sensorial producida
FICHA TÉCNICA. Excipientes con efecto conocido: 0,458 g de maltitol líquido (E965) y 1,830 g de isomalta (E953).
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor limón 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4 diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor limón 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4 diclorobencílico,
FICHA TÉCNICA. Normoreum 400 mg comprimidos recubiertos con película
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Normoreum 400 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principios activos: 400 mg de extracto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Normoreum 400 mg comprimidos recubiertos con película 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principios activos: 400 mg de extracto
ESOMEPRAZOL STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA
 OBJETIVO ESOMEPRAZOL STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA El Estudio de Bioequivalencia de Esomeprazol STADA se ha realizado siguiendo las Directrices que la Unión Europea recomienda
OBJETIVO ESOMEPRAZOL STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA El Estudio de Bioequivalencia de Esomeprazol STADA se ha realizado siguiendo las Directrices que la Unión Europea recomienda
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN
 COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN HIDROMORFONA OROS Comparador: MORFINA DE LIBERACIÓN CONTROLADA NO SUPONE UN AVANCE TERAPÉUTICO Nombre comercial y presentaciones:
COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS DE EUSKADI INFORME DE EVALUACIÓN HIDROMORFONA OROS Comparador: MORFINA DE LIBERACIÓN CONTROLADA NO SUPONE UN AVANCE TERAPÉUTICO Nombre comercial y presentaciones:
FENTANILO MATRIX STADA PARCHES TRANSDÉRMICOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA
 FENTANILO MATRIX STADA PARCHES TRANSDÉRMICOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA OBJETIVO El Estudio de Bioequivalencia de Fentanilo Matrix STADA se ha realizado siguiendo las Directrices que la
FENTANILO MATRIX STADA PARCHES TRANSDÉRMICOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA OBJETIVO El Estudio de Bioequivalencia de Fentanilo Matrix STADA se ha realizado siguiendo las Directrices que la
AVARIC (CITRATO DE FENTANILO) Comprimidos sublinguales GUÍA DE INFORMACIÓN PARA PROFESIONALES SANITARIOS
 AVARIC (CITRATO DE FENTANILO) Comprimidos sublinguales GUÍA DE INFORMACIÓN PARA PROFESIONALES SANITARIOS Información sobre medidas de prevención de riesgos autorizada por la Agencia Española de Medicamentos
AVARIC (CITRATO DE FENTANILO) Comprimidos sublinguales GUÍA DE INFORMACIÓN PARA PROFESIONALES SANITARIOS Información sobre medidas de prevención de riesgos autorizada por la Agencia Española de Medicamentos
ambroxol cinfa 15 mg / 5 ml jarabe EFG
 FICHA TÉCNICA ambroxol cinfa 15 mg / 5 ml jarabe EFG 1. NOMBRE DEL MEDICAMENTO ambroxol cinfa 15 mg/5 ml jarabe EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA 5 ml de jarabe contienen 15 mg de clorhidrato
FICHA TÉCNICA ambroxol cinfa 15 mg / 5 ml jarabe EFG 1. NOMBRE DEL MEDICAMENTO ambroxol cinfa 15 mg/5 ml jarabe EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA 5 ml de jarabe contienen 15 mg de clorhidrato
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Entero-Silicona 9 mg/ml emulsión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de emulsión oral contiene:
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Entero-Silicona 9 mg/ml emulsión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de emulsión oral contiene:
FICHA DE INFORMACIÓN AL PACIENTE: CITALOPRAM
 FICHA DE INFORMACIÓN AL PACIENTE: CITALOPRAM 1.1 Acción: Antidepresivo. 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.2 Cómo actúa este fármaco: Inhibe la recaptación de serotonina a nivel de la membrana neuronal,
FICHA DE INFORMACIÓN AL PACIENTE: CITALOPRAM 1.1 Acción: Antidepresivo. 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.2 Cómo actúa este fármaco: Inhibe la recaptación de serotonina a nivel de la membrana neuronal,
Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO bucomax pastillas para chupar sabor menta bucomax pastillas para chupar sabor fresa bucomax pastillas para chupar sabor miel y limón 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
1. NOMBRE DEL MEDICAMENTO bucomax pastillas para chupar sabor menta bucomax pastillas para chupar sabor fresa bucomax pastillas para chupar sabor miel y limón 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA. Excipientes con efecto conocido 1,38 g de sacarosa y 1,10 g glucosa. Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
Fecha de elaboración: julio 2004. Nueva asociación. Marca registrada (Laboratorio): Zaldiar (Grünental) Grupo Terapéutico: N02AX Otros opioides.
 Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Campus Universitario de Cartuja Cuesta del Observatorio, 4 Ap. Correos 2070, Granada 18080. España Telf. +34 958 027 400, Fax 958
Centro Andaluz de Documentación e Información de Medicamentos (CADIME) Campus Universitario de Cartuja Cuesta del Observatorio, 4 Ap. Correos 2070, Granada 18080. España Telf. +34 958 027 400, Fax 958
ITRACONAZOL STADA CÁPSULAS DURAS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA
 ITRACONAZOL STADA CÁPSULAS DURAS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA OBJETIVO El estudio de Bioequivalencia de Itraconazol STADA cápsulas se ha realizado siguiendo las Directrices que la Unión Europea
ITRACONAZOL STADA CÁPSULAS DURAS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA OBJETIVO El estudio de Bioequivalencia de Itraconazol STADA cápsulas se ha realizado siguiendo las Directrices que la Unión Europea
TABLA 5. Criterios de tratamiento potencialmente inapropiados
 TABLA 5. Criterios de tratamiento potencialmente inapropiados SISTEMA CARDIOVASCULAR Digoxina a dosis superiores a 0.5mg/día en tratamiento continuado en enfermos con alteraciones de la función renal (aclaramiento
TABLA 5. Criterios de tratamiento potencialmente inapropiados SISTEMA CARDIOVASCULAR Digoxina a dosis superiores a 0.5mg/día en tratamiento continuado en enfermos con alteraciones de la función renal (aclaramiento
Información y educación sobre dolor. Escalas de evaluación. Factores que influyen en el DAP
 Información y educación sobre dolor. Escalas de evaluación. Factores que influyen en el DAP HOSPITAL ABENTE Y LAGO S. López Álvarez. Puntos clave para el manejo del DAP 1.- Reconocer el derecho de los
Información y educación sobre dolor. Escalas de evaluación. Factores que influyen en el DAP HOSPITAL ABENTE Y LAGO S. López Álvarez. Puntos clave para el manejo del DAP 1.- Reconocer el derecho de los
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. SANODIN 20 mg/g pomada bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. Cada gramo de pomada bucal contiene:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SANODIN 20 mg/g pomada bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada bucal contiene: Carbenoxolona disódica. 20 mg Excipientes: Para consultar
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO SANODIN 20 mg/g pomada bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada bucal contiene: Carbenoxolona disódica. 20 mg Excipientes: Para consultar
Índice de contenidos DESCRIPCIÓN GENERAL. Ambroxol
 Ambroxol Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL El Ambroxol es un medicamento con propiedades
Ambroxol Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL El Ambroxol es un medicamento con propiedades
Cámara de inhalación versus nebulizadores para el tratamiento con β agonista en el asma agudo (1)
 Cámara de inhalación versus nebulizadores para el tratamiento con β agonista en el asma agudo (1) Colaboración Cochrane Antecedentes Las exacerbaciones agudas del asma son frecuentes y responsables de
Cámara de inhalación versus nebulizadores para el tratamiento con β agonista en el asma agudo (1) Colaboración Cochrane Antecedentes Las exacerbaciones agudas del asma son frecuentes y responsables de
Tramadol y codeina. Tramadol y codeina
 Tramadol y codeina The Borg System is 100 % Tramadol y codeina La combinacin de tramadol y paracetamol en dosis fijas es una alternativa atractiva para el tratamiento del dolor moderado a grave, que presenta
Tramadol y codeina The Borg System is 100 % Tramadol y codeina La combinacin de tramadol y paracetamol en dosis fijas es una alternativa atractiva para el tratamiento del dolor moderado a grave, que presenta
Para que es el tramadol 50 mg
 Para que es el tramadol 50 mg The Borg System is 100 % Para que es el tramadol 50 mg El Tramadol es un analgésico que se parece a la morfina y que tiene un efecto analgésico fuerte. Encargue oficialmente
Para que es el tramadol 50 mg The Borg System is 100 % Para que es el tramadol 50 mg El Tramadol es un analgésico que se parece a la morfina y que tiene un efecto analgésico fuerte. Encargue oficialmente
PIROXICAM ACCIONES: Analgésica Antiinflamatoria Antipirética Antitrombótica
 ÁCIDOS ENÓLICOS PIROXICAM ACCIONES: Analgésica Antiinflamatoria Antipirética Antitrombótica MECANISMO DE ACCIÓN de prostaglandinas. INHIBICIÓN DE LA COX Inhibe la migración de PMN y monocitos a lugar de
ÁCIDOS ENÓLICOS PIROXICAM ACCIONES: Analgésica Antiinflamatoria Antipirética Antitrombótica MECANISMO DE ACCIÓN de prostaglandinas. INHIBICIÓN DE LA COX Inhibe la migración de PMN y monocitos a lugar de
Tratamiento dolor crónico relacionado con el cáncer
 En el tratamiento del dolor crónico oncológico la OMS propone un esquema terapéutico, "la escalera analgésica". Ante el control insuficiente del dolor con los fármacos de un escalón se subirá al siguiente.
En el tratamiento del dolor crónico oncológico la OMS propone un esquema terapéutico, "la escalera analgésica". Ante el control insuficiente del dolor con los fármacos de un escalón se subirá al siguiente.
Enfermedad de Alzheimer - exploraciones PET muestran en los pacientes con Alzheimer leve y más en casos avanzados el metabolismo de glucosa se reduce
 Enfermedad de Alzheimer - exploraciones PET muestran en los pacientes con Alzheimer leve y más en casos avanzados el metabolismo de glucosa se reduce tanto en los lóbulos temporal y parietal. 1 Jefa de
Enfermedad de Alzheimer - exploraciones PET muestran en los pacientes con Alzheimer leve y más en casos avanzados el metabolismo de glucosa se reduce tanto en los lóbulos temporal y parietal. 1 Jefa de
MICOFENOLATO DE MOFETILO STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA
 MICOFENOLATO DE MOFETILO STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA OBJETIVO El Estudio de Bioequivalencia de Micofenolato de mofetilo STADA se ha realizado siguiendo las Directrices
MICOFENOLATO DE MOFETILO STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA OBJETIVO El Estudio de Bioequivalencia de Micofenolato de mofetilo STADA se ha realizado siguiendo las Directrices
Tabla de equivalencia aproximada entre opioides
 Tabla de equivalencia aproximada entre opioides Documentos www.1aria.com DOSIS EQUIPOTENTES BUPRENORFINA PARCHE TRANSDÉRMICO 8,75 (0,2 17,5 (0,4 35 (0,8 52,5 (1,2 70 (1,6 105 (2,4 122,5 (2,8 140 (3,2 -
Tabla de equivalencia aproximada entre opioides Documentos www.1aria.com DOSIS EQUIPOTENTES BUPRENORFINA PARCHE TRANSDÉRMICO 8,75 (0,2 17,5 (0,4 35 (0,8 52,5 (1,2 70 (1,6 105 (2,4 122,5 (2,8 140 (3,2 -
LISTADO DE MEDICAMENTOS ESENCIALES DEL INSTITUTO JALISCIENSE DE ALIVIO AL DOLOR Y CUIDADOS PALIATIVOS SEGUNDA EDICIÓN 2012
 DEL INSTITUTO JALISCIENSE DE ALIO AL DOLOR Y CUIDADOS PALIATOS PALIATOS POR IAHPC*/ 1 2500 ALPRAZOLAM 0.25 mg tabletas (caja con 30) Ansiolítico. $45.27 2 3305 AMITRIPTILINA 25 mg tabletas (caja con 20)
DEL INSTITUTO JALISCIENSE DE ALIO AL DOLOR Y CUIDADOS PALIATOS PALIATOS POR IAHPC*/ 1 2500 ALPRAZOLAM 0.25 mg tabletas (caja con 30) Ansiolítico. $45.27 2 3305 AMITRIPTILINA 25 mg tabletas (caja con 20)
MANIDIPINO STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA
 OBJETIVO MANIDIPINO STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA Los Estudios de Bioequivalencia de Manidipino STADA comprimidos EFG se han realizado siguiendo las Directrices que la Agencia
OBJETIVO MANIDIPINO STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA Los Estudios de Bioequivalencia de Manidipino STADA comprimidos EFG se han realizado siguiendo las Directrices que la Agencia
ALPRAZOLAM STADA comprimidos EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA
 OBJETIVO ALPRAZOLAM STADA comprimidos EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA El Estudio de Bioequivalencia de Alprazolam STADA comprimidos EFG se ha realizado siguiendo las Directrices que la Agencia
OBJETIVO ALPRAZOLAM STADA comprimidos EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA El Estudio de Bioequivalencia de Alprazolam STADA comprimidos EFG se ha realizado siguiendo las Directrices que la Agencia
MANEJO DEL DOLOR AGUDO EN EL ANCIANO
 MANEJO DEL DOLOR AGUDO EN EL ANCIANO Belén García Iglesias Complexo Hospitalario Juan Canalejo A Coruña Paciente Anciano Estrategia terapeútica Envejecimiento Proceso biológico que produce una pérdida
MANEJO DEL DOLOR AGUDO EN EL ANCIANO Belén García Iglesias Complexo Hospitalario Juan Canalejo A Coruña Paciente Anciano Estrategia terapeútica Envejecimiento Proceso biológico que produce una pérdida
3DOLOR AGUDO POSTOPERATORIO. ESTRATEGIA TERAPÉUTICA
 3DOLOR AGUDO POSTOPERATORIO. ESTRATEGIA TERAPÉUTICA IMPORTANCIA La importancia del dolor agudo postoperatorio radica en su alta frecuencia, en su inadecuado tratamiento y en las repercusiones que tiene
3DOLOR AGUDO POSTOPERATORIO. ESTRATEGIA TERAPÉUTICA IMPORTANCIA La importancia del dolor agudo postoperatorio radica en su alta frecuencia, en su inadecuado tratamiento y en las repercusiones que tiene
Boletín Terapéutico Distrito Sevilla
 Boletín Terapéutico Distrito Sevilla VOLUMEN 1, Nº 4 ABRIL 2009 Servicio de Farmacia. Distrito Sanitario Atención Primaria Sevilla MANEJO DEL DOLOR CRÓNICO NO ONCOLÓGICO EN PACIENTES CON ALGÚN FACTOR DE
Boletín Terapéutico Distrito Sevilla VOLUMEN 1, Nº 4 ABRIL 2009 Servicio de Farmacia. Distrito Sanitario Atención Primaria Sevilla MANEJO DEL DOLOR CRÓNICO NO ONCOLÓGICO EN PACIENTES CON ALGÚN FACTOR DE
Uso de Ketamina para procedimientos pediátricos. Alicia Llombart Vidal R3 Tutor: Luis Moral Gil 14 de Febrero del 2017
 Uso de Ketamina para procedimientos pediátricos Alicia Llombart Vidal R3 Tutor: Luis Moral Gil 14 de Febrero del 2017 Objetivos Conocer: Mecanismo de acción y principales efectos de la Ketamina Forma de
Uso de Ketamina para procedimientos pediátricos Alicia Llombart Vidal R3 Tutor: Luis Moral Gil 14 de Febrero del 2017 Objetivos Conocer: Mecanismo de acción y principales efectos de la Ketamina Forma de
QUETIAPINA STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA
 OBJETIVO QUETIAPINA STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA El Estudio de Bioequivalencia de Quetiapina STADA se ha realizado siguiendo las Directrices que la Unión Europea recomienda
OBJETIVO QUETIAPINA STADA COMPRIMIDOS EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA El Estudio de Bioequivalencia de Quetiapina STADA se ha realizado siguiendo las Directrices que la Unión Europea recomienda
Aproximación al dolor Oncológico. Zaragoza 22 de Noviembre 2014 Maria Pilar Acin Lazaro
 Aproximación al dolor Oncológico Zaragoza 22 de Noviembre 2014 Maria Pilar Acin Lazaro Manejo Farmacológico del Dolor Oncológico Seleccionar el Fármaco apropiado Prescribir la Dosis ajustada Administrarlo
Aproximación al dolor Oncológico Zaragoza 22 de Noviembre 2014 Maria Pilar Acin Lazaro Manejo Farmacológico del Dolor Oncológico Seleccionar el Fármaco apropiado Prescribir la Dosis ajustada Administrarlo
MARCAR CON UNA X LA RESPUESTA CORRECTA
 Unidad Didáctica 3. Test de evaluación MARCAR CON UNA X LA RESPUESTA CORRECTA 1. Cuál de las siguientes afirmaciones es correcta, en relación con antidepresivos tricíclicos? A. En una persona sana tiene
Unidad Didáctica 3. Test de evaluación MARCAR CON UNA X LA RESPUESTA CORRECTA 1. Cuál de las siguientes afirmaciones es correcta, en relación con antidepresivos tricíclicos? A. En una persona sana tiene
INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS
 INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS Principio activo: Nombre Comercial y presentación: FENTANILO ORAL TRANSMUCOSA (OT) ACTIQ (Ferrer Farma) 3 comprimidos para chupar con aplicador
INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS Principio activo: Nombre Comercial y presentación: FENTANILO ORAL TRANSMUCOSA (OT) ACTIQ (Ferrer Farma) 3 comprimidos para chupar con aplicador
1. DENOMINACIÓN DEL ESQUEMA: DOXORUBICINA LIPOSOMAL. Cáncer de ovario avanzado en mujeres en las que ha fallado un régimen de primera
 1. DENOMINACIÓN DEL ESQUEMA: DOXORUBICINA LIPOSOMAL 2. USO TERAPÉUTICO Cáncer de ovario avanzado en mujeres en las que ha fallado un régimen de primera línea conteniendo platino. 3. ESQUEMA (1) Medicamento
1. DENOMINACIÓN DEL ESQUEMA: DOXORUBICINA LIPOSOMAL 2. USO TERAPÉUTICO Cáncer de ovario avanzado en mujeres en las que ha fallado un régimen de primera línea conteniendo platino. 3. ESQUEMA (1) Medicamento
3. Cuidados Paliativos: Valoración y Plan de Actuación
 3. Cuidados Paliativos: Valoración y Plan de Actuación > Para dar respuesta a las necesidades que tiene una persona en situación terminal y su familia, es necesario realizar una valoración que permita
3. Cuidados Paliativos: Valoración y Plan de Actuación > Para dar respuesta a las necesidades que tiene una persona en situación terminal y su familia, es necesario realizar una valoración que permita
INFORME DE EVALUACIÓN DE MEDICAMENTOS PARA LA COMISIÓN DE FARMACIA Y TERAPÉUTICA Fecha: 19/02/09 Acta I/09
 . INFORME DE EVALUACIÓN DE MEDICAMENTOS PARA LA COMISIÓN DE FARMACIA Y TERAPÉUTICA Fecha: 19/02/09 Acta I/09 TRAMADOL + PARACETAMOL Tratamiento sintomático del dolor moderado a intenso 1. SOLICITUD Solicitado
. INFORME DE EVALUACIÓN DE MEDICAMENTOS PARA LA COMISIÓN DE FARMACIA Y TERAPÉUTICA Fecha: 19/02/09 Acta I/09 TRAMADOL + PARACETAMOL Tratamiento sintomático del dolor moderado a intenso 1. SOLICITUD Solicitado
TUSQUIM Paracetamol - Dextrometorfano bromhidrato - Fenilefrina clorhidrato Bromhexina clorhidrato Tabletas Recubiertas
 TUSQUIM Paracetamol - Dextrometorfano bromhidrato - Fenilefrina clorhidrato Bromhexina clorhidrato Tabletas Recubiertas TUSQUIM Comprimidos recubiertos Antitusivo Analgésico Antipirético Mucolítico COMPOSICION:
TUSQUIM Paracetamol - Dextrometorfano bromhidrato - Fenilefrina clorhidrato Bromhexina clorhidrato Tabletas Recubiertas TUSQUIM Comprimidos recubiertos Antitusivo Analgésico Antipirético Mucolítico COMPOSICION:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MICRALAX Macrogol 5,9 g polvo para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MICRALAX Macrogol 5,9 g polvo para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene 5,9 gramos de Macrogol 3350. Excipientes con efecto
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MICRALAX Macrogol 5,9 g polvo para solución oral. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre contiene 5,9 gramos de Macrogol 3350. Excipientes con efecto
HERBICIDAS DIPIRIDÍLICOS: Paraquat y diquat
 HERBICIDAS DIPIRIDÍLICOS: Paraquat y diquat Definición: El paraquat y el diquat son herbicidas de elevada eficacia, bajo coste y ausencia de acumulación en el medio ambiente. La ingesta oral de 10-20 ml
HERBICIDAS DIPIRIDÍLICOS: Paraquat y diquat Definición: El paraquat y el diquat son herbicidas de elevada eficacia, bajo coste y ausencia de acumulación en el medio ambiente. La ingesta oral de 10-20 ml
FICHA TÉCNICA. No exceder la dosis máxima de 480 mg de simeticona (4 comprimidos masticables) al día.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aero-red 120 mg comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Simeticona.. 120 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aero-red 120 mg comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Simeticona.. 120 mg Excipientes con efecto conocido:
FICHA TÉCNICA. No exceder la dosis máxima de 480 mg de simeticona (4 comprimidos masticables) al día.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aero-red 120 mg comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Simeticona.. 120 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aero-red 120 mg comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Simeticona.. 120 mg Excipientes con efecto conocido:
Anexo II. Conclusiones científicas
 Anexo II Conclusiones científicas 5 Conclusiones científicas Vale Pharmaceuticals presentó al Reino Unido una solicitud de autorización de comercialización, con arreglo al procedimiento descentralizado,
Anexo II Conclusiones científicas 5 Conclusiones científicas Vale Pharmaceuticals presentó al Reino Unido una solicitud de autorización de comercialización, con arreglo al procedimiento descentralizado,
Morfina o Fentanyl? bolo o infusion? Soledad Hernández Residente Neo 18 de junio 2014
 Morfina o Fentanyl? bolo o infusion? Soledad Hernández Residente Neo 18 de junio 2014 Introducción Dolor en RN tiene consecuencias a corto y largo plazo. Anand KJ, Pain and its effects in the human neonate
Morfina o Fentanyl? bolo o infusion? Soledad Hernández Residente Neo 18 de junio 2014 Introducción Dolor en RN tiene consecuencias a corto y largo plazo. Anand KJ, Pain and its effects in the human neonate
Tipos de Investigación Clínica. Investigación Clínica OBJETIVOS. mejorar la calidad y la expectativa de vida de los ciudadanos. aumentar su bienestar
 Tipos de Investigación Clínica Dra. Belén Sádaba Díaz de Rada Servicio de Farmacología Clínica Clínica Universidad de Navarra Investigación Clínica OBJETIVOS mejorar la calidad y la expectativa de vida
Tipos de Investigación Clínica Dra. Belén Sádaba Díaz de Rada Servicio de Farmacología Clínica Clínica Universidad de Navarra Investigación Clínica OBJETIVOS mejorar la calidad y la expectativa de vida
