Espectrometría de masas. Clase 4
|
|
|
- Milagros Camacho Quiroga
- hace 5 años
- Vistas:
Transcripción
1 Espectrometría de masas Clase 4
2 La espectrometría de masas (EM) no es una técnica espectroscópica en sentido estricto, puesto que no implica absorción de radiación electromagnética. La EM permite utilizar cantidades de muestra inferiores a los nanogramos (10-9 gramos).
3
4 En EI se introduce una molécula en la cámara de ionización y se bombardea con una corriente de electrones: La molécula se ioniza- pierde un electrón dando lugar a la formación de un ión-radical
5
6 La intensidad de los picos nos indica la cantidad relativa de iones que poseen dicha relación masa/carga.
7 La intensidad de los picos nos indica la cantidad relativa de iones que poseen dicha relación masa/carga. La separación de los diferentes iones se basa en la relación: m/z = 2 R 2 /2V es la intensidad del campo magnético; R el radio de deflexión del tubo analizador V es el potencial de aceleración utilizado. Como curiosidades indicaremos que la velocidad de los iones suele ser de unos 100 Km/seg, que el radio de deflexión (R) suele ser de unos cm y el tubo analizador suele ser un sector esférico de aproximadamente un metro de longitud.
8 El electrón que se pierde es el de menor potencial de ionización; así se obtendrán unas estructuras como las que se muestran:
9 Notación para los iones en EM etileno: C C ó C C 2 C C 2 ó Debe tenerse en cuenta que son más fáciles de remover los electrones π que los σ. etano: C C ó C C m/z = 30 m/z = 30 m/z = 30 ó C C Consideramos solo la ionización del enlace Carbono-Carbono La notación entre corchetes, si bien es muy utilizada no refleja la realidad pura, indica un total de 15 electrones sigma, mientras que las otras son algo más correctas al indicar solamente 13. benceno: ó ó ó + +
10 ciclohexanona: O ó O clorociclohexano: Cl ó Cl En los dos últimos ejemplos, los electrones n son los más fáciles de remover.
11 Sobre el ión molecular Generalmente es el ión con mayor masa de los que aparecen en el espectro sin tener en cuenta los picos isotópicos Debe contener todos los elementos presentes en sus fragmentos Debe corresponder al ión con el potencial de ionización más bajo Su relación m/z es: par cuando no posee Nitrógeno o posee un número par de ellos; impar cuando posee un número impar de átomos de Nitrógeno (Regla del nitrógeno) Las diferencias de masa entre el ión molecular y los fragmentos que aparecen en el espectro deben ser químicamente lógicas La abundancia relativa de los fragmentos depende de la naturaleza química del producto Cualitativa y aproximadamente la intensidad del ión molecular se relaciona con el grupo principal presente en la molécula : Compuestos aromáticos > olefinas conjugadas > compuestos alicíclicos > sulfuros > hidrocarburos lineales > mercaptanos > cetonas > aminas > esteres > éteres > ácidos carboxílicos > hidrocarburos ramificados > alcoholes
12 Cuando se obtiene un espectro de masas de alta resolución (RMS) es posible distinguir entre fórmulas de muy aproximadas En RMS se puede utilizar el ión molecular para determinar la fórmula molecular de la sustancia En la siguiente tabla se muestran algunas diferencias de masas de combinaciones atómicas para el pico de masa (redondeada) 43. Combinación atómica Masa exacta CNO C 2 3 O C 3 N C 2 5 N C
13 En esta tabla se muestra la causa de tales diferencias, que no es otra que la masa exacta de los elementos debido a la distribución isotópica de los mismos Elemento Peso Atómico Isótopos idrógeno Carbono C 13 C Nitrógeno N 15 N Oxígeno O 17 O 18 O Abundancia relativa (%) Masa atómica Fluor F Silicio Si 29 Si 30 Si Fósforo P Azufre S 33 S 34 S 36 S Cloro Cl 37 Cl Bromo Br 81 Br Iodo I
14 an sido compiladas tablas que listan todas las combinaciones razonables de C,, N y O para un peso molecular que varía en la tercera o cuarta cifra decimal ejemplo.. Fórmulas a partir de relaciones isotópicas: Aún con instrumentos de baja resolución que sólo discriminan entre iones que difieren en masa por un número entero de masa se puede acceder a la formula molecular de un compuesto analizando las relaciones isotópicas frente al M+ de los picos M+2, y M+1. La condición es que el pico M+ sea lo suficientemente intenso para que su altura y las alturas de los picos de los isótopos puedan determinarse con precisión.
15 Fraccionamiento del ión molecular Dependiendo del tipo de ruptura del enlace la fragmentación simple puede ser homolítica o heterolítica, siendo en ambos casos el resultado de la misma la formación de un radical (que no es detectado en el espectro de masas) y un catión:
16 A su vez los cationes formados en esta fragmentación pueden sufrir nuevas fragmentaciones bien por via homolítica (producirían radicales e iones radicales) o heterolítica (producirían moléculas neutras y otro catión).
17 Un caso algo especial es el de las moléculas cíclicas, pues cuando se rompe un enlace del anillo lo que se obtiene es un nuevo ión radical homólogo del ión molecular a partir de ambos tipos de ruptura, pero ahora lineal.
18 La vida media de las especies ionizadas En espectrometría de masas, algunos tipos de compuestos podrán acomodar mejor que otros la carga positiva y tener así un tiempo de vida mayor. Esto se observa cuando dicha carga puede deslocalizarse. En consecuencia: cuanto mayor es la vida media, mayor es la abundancia (mayor intensidad del pico)
19 Tabla las masas de los fragmentos más característicos y frecuentes (Estos fragmentos son característicos de iones pero también de perdidas del ión molecular) MASA ASIGNACIÓN 29 Etilo (C 2 5 ), formilo (CO) 30 Nitroso (NO) 31 Metoxilo (C 3 O), hidroximetilo (C 2 O) 39 Ciclopropenilo (C 3 3 ) 41 Alilo (C 2 C=C 2 ) 43 Propilo (C 3 7 ), acetilo (C 3 CO) 45 Carboxilo (COO) 46 Nitro (NO 2 ) 55 Butenilo (C 4 7 ) 56 C t-butilo (C 4 9 ), Propanoilo (C 3 C 2 CO) 60 Acido acético 65 Ciclopentadienilo (C 5 5 ) 77 Fenilo (C 6 5 ) 91 Bencilo (tropilio, Ph-C 2 ) 92 Metilenpiridina (azatropilio, C 5 5 N-C 2 ) 105 Benzoilo (Ph-CO) 127 Iodo
20 Reglas de fragmentación de los compuestos orgánicos Independientemente del tipo de ruptura las fragmentaciones responden a alguna de las cuatro reglas siguientes: 1ª REGLA: Los enlaces Carbono-Carbono se escinden con preferencia en los puntos de ramificación La carga positiva quedará sobre el carbocatión más estable, siendo la estabilidad de estos: Terciario > Secundario > Primario > Metilo
21 Reglas de fragmentación de los compuestos orgánicos 2ª REGLA: Los sistemas de dobles enlaces favorecen la escisión de los enlaces alílicos y bencílicos La carga positiva quedará normalmente formando un carbocatión alílico o bencílico En este ultimo caso debemos hacer notar que NO es un catión bencilo lo que se forma sino que se reagrupa formando el IÓN TROPÍLIO (C 7 7 +) que es aromático
22 Formación del Ión tropilio Ej. etilbenceno se fragmenta generando señales a m/z 91 y a m/z 77. C 2 C 3 C m / z =7 7 C 2 C 3 C 2 C 2... C 3 + m/z = 91 Este tipo de Clivaje se conoce como bencílico, pero la representación más correcta del fragmento a m/z 91 es como ión tropilio C 2 C ión tropilio m/ z =9 1
23
24 Reglas de fragmentación de los compuestos orgánicos Un caso especial lo constituye el caso de los cicloalquenos pues poseen dos enlaces en posición alílica, sufriendo la fragmentación simultánea de ambos enlaces, es lo que se conoce como reacción de RETRO DIELS-ALDER
25 Reglas de fragmentación de los compuestos orgánicos 3ª REGLA: Los heteroátomos favorecen la fragmentación de los enlaces del átomo de Carbono que soporta al heteroátomo y del enlace C-C en posición alfa
26 Ruptura enlace C-X Ruptura en alfa
27 35 Cl : 37 Cl 3 : 1
28 = = Br : 81 Br 50.5 : 49.5
29 Ruptura enlace C-X Ruptura en alfa
30 Alcoholes: Los iones moleculares de los alcoholes son muy pequeños o inexistentes Generalmente ocurren rupturas de enlaces C-C próximos al -O Son muy frecuentes las pérdidas de 2 O=18 unidades de masa
31 Si se trata de un grupo carbonilo (C=O), el ión más estable suele ser el ión acilo (RCO+).
32 Ácidos carboxílicos En ácidos de cadena corta dominan los picos provenientes de : Pérdida de O (M -17) Pérdida de COO (M - 45)
33
34 Reglas de fragmentación de los compuestos orgánicos 4º REGLA: Los dobles enlaces y los heteroátomos favorecen, como aceptores de idrógeno, la transposición de un hidrógeno a través de un estado cíclico de transición de seis miembros Se conoce como Transposición específica de idrógeno o Transposición de McLafferty
35 Reordenamiento o transposición McLafferty Para que se produzca debe existir un átomo de idrógeno en posición γ (gama) respecto al doble enlace aceptor de idrógeno. La experimentan compuestos insaturados de formula general: R' A B α γ D ββ C La transposición de McLafferty sobre un compuesto carbonílico da lugar a un alqueno y a una forma enólica de una nueva cetona.
36 Transposición de McLafferty Ejemplos: Una cetona con en posición gama fragmentación del catión-radical del 1-penteno: C C C 2 C 2 C 2 C C 3 C 2 + R uptura heterlítica C 2 C 2 C C 2 C 3 C 2 C C 2 C 2 C + R uptura homolítica C 2 C 2
37
38 Bibliografía básica sugerida -QUÍMICA ORGÁNICA. Vollhardt, K.P.C. / Schore, N.E. Editorial Omega QUÍMICA ORGÁNICA. John McMurry Paraninfo QUIMICA ORGANICA. Francis Carey. 6 Edición Ed. Mc Graw ill Bibliografía de consulta -ORGANIC STRUCTURES FROM SPECTRA. Field, Sternhell, Kalman. 4th Edition John Wiley & Sons Ltd. -MÉTODOS ESPECTROSCÓPICOS EN QUÍMICA ORGÁNICA. esse, Meier y Zeeh 1997, Editorial Síntesis -MÉTODOS ESPECTROSCÓPICOS EN QUÍMICA ORGÁNICA. Fleming y Williamms 1974, Urmo SA Ediciones -ORGANIC STRUCTURE DETERMINATION. D.J. Pasto, C.R. Johnson. Prentice-all-INC -INTRODUCTION TO ORGANIC SPECTROSCOPY. arwood y Clarige 1997, Oxford University Press -IDENTIFICACION ESPECTROMETRICA DE COMPUESTOS ORGANICOS. R.M. SILVERSTEIN, G.C. BASSLER Y T.C. MORILL Ed. Diana -STRUCTURE ELUCIDATION OF NATURAL PRODUCTS BY MASS ESPECTROMETRY, Vol. I, Vol.II.. BUDZIKIEWICZ, C. DJERASSI Y D.. WILLIAMS.olden-Day, INC
La espectrometría de masas (EM) no es una
 Espectrometría de masas La espectrometría de masas (EM) no es una técnica espectroscópica en sentido estricto, puesto que no implica absorción de radiación electromagnética. La EM permite utilizar cantidades
Espectrometría de masas La espectrometría de masas (EM) no es una técnica espectroscópica en sentido estricto, puesto que no implica absorción de radiación electromagnética. La EM permite utilizar cantidades
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS
 Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
Espectrometría de masas
 Espectrometría de masas La espectrometría de masas (EM) no es una técnica espectroscópica en sentido estricto, puesto que no implica absorción de radiación electromagnética. La EM permite utilizar cantidades
Espectrometría de masas La espectrometría de masas (EM) no es una técnica espectroscópica en sentido estricto, puesto que no implica absorción de radiación electromagnética. La EM permite utilizar cantidades
Espectrometría de masas
 Espectrometría de masas Qué compuesto orgánico responde a 16 unidades de masas? El metano (C 4 ) y ningún otro Qué compuesto orgánico responde a 32 unidades de masas? Rápidamente diríamos el metanol (C
Espectrometría de masas Qué compuesto orgánico responde a 16 unidades de masas? El metano (C 4 ) y ningún otro Qué compuesto orgánico responde a 32 unidades de masas? Rápidamente diríamos el metanol (C
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS
 Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
ESPECTROSCOPÍA ESPECTROMETRIA DE MASAS
 ESPECTROSCOPÍA ESPECTROMETRIA DE MASAS La espectrometría de masas es una técnica experimental que permite la medición de iones derivados de moléculas. El espectrómetro de masas es un instrumento que permite
ESPECTROSCOPÍA ESPECTROMETRIA DE MASAS La espectrometría de masas es una técnica experimental que permite la medición de iones derivados de moléculas. El espectrómetro de masas es un instrumento que permite
Espectrometría de masas. Complemento
 Espectrometría de masas Complemento Alcanos Se observan los iones moleculares, aunque con baja intensidad El patrónde fragmentación presenta picos que difieren en 14 unidades de masa (pérdida de CH 2
Espectrometría de masas Complemento Alcanos Se observan los iones moleculares, aunque con baja intensidad El patrónde fragmentación presenta picos que difieren en 14 unidades de masa (pérdida de CH 2
Espectrometría de Masa
 Espectrometría de Masa La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca de su estructura
Espectrometría de Masa La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca de su estructura
Espectrometría de masas
 Espectrometría de masas Información que puede obtenerse La masa molecular La fórmula molecular Algunas características estructurales del compuesto Espectrómetro de masas básico Técnica de Impacto de electrones
Espectrometría de masas Información que puede obtenerse La masa molecular La fórmula molecular Algunas características estructurales del compuesto Espectrómetro de masas básico Técnica de Impacto de electrones
Unidad IV: Espectrometría de Masas. Química Orgánica III Primer Semestre 2016 Facultad de CC.QQ. Y Farmacia USAC
 Unidad IV: Espectrometría de Masas Química Orgánica III Primer Semestre 2016 Facultad de CC.QQ. Y Farmacia USAC Identificación de un compuesto Orgánico Determinación de Propiedades Físicas Apariencia Olor
Unidad IV: Espectrometría de Masas Química Orgánica III Primer Semestre 2016 Facultad de CC.QQ. Y Farmacia USAC Identificación de un compuesto Orgánico Determinación de Propiedades Físicas Apariencia Olor
Espectrometría de Masas Interpretación de Espectros. Q. Georgina Duarte Lisci Facultad de Química UNAM
 Espectrometría de Masas Interpretación de Espectros Q Georgina Duarte Lisci Facultad de Química UNAM Regiones de Información en el Espectro de Masas %Abundancia Información General Series de Iones Información
Espectrometría de Masas Interpretación de Espectros Q Georgina Duarte Lisci Facultad de Química UNAM Regiones de Información en el Espectro de Masas %Abundancia Información General Series de Iones Información
Espectrometría de Masas Interpretación de Espectros. Q. Georgina Duarte Lisci Facultad de Química UNAM
 Espectrometría de Masas Interpretación de Espectros Q Georgina Duarte Lisci Facultad de Química UAM egiones de Información en el Espectro de Masas %Abundancia Información General Series de Iones Información
Espectrometría de Masas Interpretación de Espectros Q Georgina Duarte Lisci Facultad de Química UAM egiones de Información en el Espectro de Masas %Abundancia Información General Series de Iones Información
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS. Elucidación estructural: Ejemplo 1 Dados los siguientes espectros:
 ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
QUÍMICA DEL CARBONO 1. El enlace de carbono. 2. Grupos funcionales. 3. Isomería.
 QUÍMICA DEL CARBONO 1. El enlace de carbono. 2. Grupos funcionales. 3. Isomería. Química 2º bachillerato Química del carbono 1 0. CONOCIMIENTOS PREVIOS Los conocimientos previos que son necesarios dominar
QUÍMICA DEL CARBONO 1. El enlace de carbono. 2. Grupos funcionales. 3. Isomería. Química 2º bachillerato Química del carbono 1 0. CONOCIMIENTOS PREVIOS Los conocimientos previos que son necesarios dominar
ESPECTROMETRIA DE MASAS
 ESPECTROMETRIA DE MASAS Utilizando la espectrometría de masas (EM) podemos conocer la masa de una molécula. Ademas podemos obtener información sobre esa misma molécula utilizando una muestra mínima. Aunque
ESPECTROMETRIA DE MASAS Utilizando la espectrometría de masas (EM) podemos conocer la masa de una molécula. Ademas podemos obtener información sobre esa misma molécula utilizando una muestra mínima. Aunque
COLEGIO SAN JOSÉ - Hijas de María Auxiliadora C/ Emilio Ferrari, 87 - Madrid Departamento de Ciencias Naturales
 TEMA 3. FORMULACIÓN ORGÁNICA EJERCICIOS 3. Grupos funcionales 1. Se dan las siguientes moléculas utilizando su fórmula semidesarrollada. Indica a qué familia pertenecen y escribe la fórmula desarrollada
TEMA 3. FORMULACIÓN ORGÁNICA EJERCICIOS 3. Grupos funcionales 1. Se dan las siguientes moléculas utilizando su fórmula semidesarrollada. Indica a qué familia pertenecen y escribe la fórmula desarrollada
ANÁLISIS INSTRUMENTAL_UII_PARTE DOS. Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½
 RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
INTRODUCCION A LA NOMENCLATURA E ISOMERIA DE LOS COMPUESTOS ORGANICOS
 INTRODUCCION A LA NOMENCLATURA E ISOMERIA DE LOS COMPUESTOS ORGANICOS Extractado de la Guía de Problemas de Química Orgánica I por la Dra. Diana Bekerman Fórmulas y representación de estructuras químicas
INTRODUCCION A LA NOMENCLATURA E ISOMERIA DE LOS COMPUESTOS ORGANICOS Extractado de la Guía de Problemas de Química Orgánica I por la Dra. Diana Bekerman Fórmulas y representación de estructuras químicas
QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos.
 QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos. Química 1º bachillerato Química del carbono 1 1. EL CARBONO El carbono es una molécula muy especial capaz
QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos. Química 1º bachillerato Química del carbono 1 1. EL CARBONO El carbono es una molécula muy especial capaz
Química Química Orgánica
 2013 Fernando Brierley Felipe Salas Química Química Orgánica Fernando Brierley V. Felipe Salas B. 2013 La gran ciencia de la química se puede d ividir en d os grandes caminos; la química inorgánica, y
2013 Fernando Brierley Felipe Salas Química Química Orgánica Fernando Brierley V. Felipe Salas B. 2013 La gran ciencia de la química se puede d ividir en d os grandes caminos; la química inorgánica, y
REACCIONES ORGÁNICAS DE IMPORTANCIA
 Ruptura de enlace Reacciones en etapas y concertadas Reactivos de una reacción química orgánica Tipos de reacción REACCIONES ORGÁNICAS DE IMPORTANCIA Objetivo de la clase: Explicar la formación de los
Ruptura de enlace Reacciones en etapas y concertadas Reactivos de una reacción química orgánica Tipos de reacción REACCIONES ORGÁNICAS DE IMPORTANCIA Objetivo de la clase: Explicar la formación de los
Sencillo C C Doble C = C Triple C C
 FORMULACIÓN ORGÁNICA Existe un nº inmenso de compuestos del carbono, por lo que se impone una clasificación y sistematización para su estudio. Las causas de tan amplia variedad De compuestos la encontramos
FORMULACIÓN ORGÁNICA Existe un nº inmenso de compuestos del carbono, por lo que se impone una clasificación y sistematización para su estudio. Las causas de tan amplia variedad De compuestos la encontramos
TALLER DE ESPECTROSCOPIA
 TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
QUÍMICA ORGÁNICA PÁGS LIBRO
 QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
QUÍMICA ORGÁNICA PÁGS LIBRO
 QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
QUÍMICA ORGÁNICA PÁGS LIBRO
 QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
Grupos funcionales Series homólogas
 Grupos funcionales Series homólogas Grupo funcional: Es un átomo o grupo de átomos unidos de manera característica y que determinan, preferentemente, las propiedades del compuesto en que están presentes.
Grupos funcionales Series homólogas Grupo funcional: Es un átomo o grupo de átomos unidos de manera característica y que determinan, preferentemente, las propiedades del compuesto en que están presentes.
Sesión 28. Compuestos orgánicos, sus elementos y grupos funcionales
 Sesión 28 Compuestos orgánicos, sus elementos y grupos funcionales Introducción El elemento carbono forma un número inmenso de compuestos. Se conocen más de diez millones de compuestos que contienen carbono,
Sesión 28 Compuestos orgánicos, sus elementos y grupos funcionales Introducción El elemento carbono forma un número inmenso de compuestos. Se conocen más de diez millones de compuestos que contienen carbono,
Química. Hibridación de Orbitales Atómicos en el Carbono
 Química Hibridación de Orbitales Atómicos en el Carbono La estructura electrónica de los átomos que constituyen una molécula orgánica determina la estructura tridimensional de ésta y sus propiedades. sp
Química Hibridación de Orbitales Atómicos en el Carbono La estructura electrónica de los átomos que constituyen una molécula orgánica determina la estructura tridimensional de ésta y sus propiedades. sp
Reacciones de Adición
 Química Orgánica Química Orgánica Química Orgánica Química Orgánica Química Orgánica Reacciones de Adición ITESM-cq, Depto. C.B. Academia Química Reacciones de Adición Objetivos Diferenciar entre una reacción
Química Orgánica Química Orgánica Química Orgánica Química Orgánica Química Orgánica Reacciones de Adición ITESM-cq, Depto. C.B. Academia Química Reacciones de Adición Objetivos Diferenciar entre una reacción
Contenidos. Características del carbono Tipos de hibridación y enlace Formulación y nomenclatura de compuestos orgánicos
 QUIMICA ORGANICA Contenidos Características del carbono Tipos de hibridación y enlace Formulación y nomenclatura de compuestos orgánicos Características del Carbono Electronegatividad Enlace covalente
QUIMICA ORGANICA Contenidos Características del carbono Tipos de hibridación y enlace Formulación y nomenclatura de compuestos orgánicos Características del Carbono Electronegatividad Enlace covalente
Espectrometría de masas molecular EMM
 Espectrometría de masas molecular EMM Etapas de un análisis por EMM - Ionización - Conversión de las moléculas en un flujo de iones (generalmente +1) - Separación de los iones según relación masa/carga
Espectrometría de masas molecular EMM Etapas de un análisis por EMM - Ionización - Conversión de las moléculas en un flujo de iones (generalmente +1) - Separación de los iones según relación masa/carga
REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS
 REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS Reacciones Inorgánicas En general son rápidas y sencillas, especialmente las iónicas en solución acuosa porque los reactivos ya están listos para reaccionar. Reacciones
REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS Reacciones Inorgánicas En general son rápidas y sencillas, especialmente las iónicas en solución acuosa porque los reactivos ya están listos para reaccionar. Reacciones
Desplazamiento Químico. Dr. Jorge A. Palermo
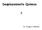 Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
FORMULACIÓN. Clasificación de los compuestos orgánicos. Hidrocarburos. Alcoholes y fenoles Éteres Aldehídos y cetonas Ácidos carboxílicos Esteres
 FORMULACIÓN Clasificación de los compuestos orgánicos Hidrocarburos. Alcoholes y fenoles Éteres Aldehídos y cetonas Ácidos carboxílicos Esteres CLASIFICACIÓN DE LOS COMPUESTOS ORGÁNICOS Clasificación de
FORMULACIÓN Clasificación de los compuestos orgánicos Hidrocarburos. Alcoholes y fenoles Éteres Aldehídos y cetonas Ácidos carboxílicos Esteres CLASIFICACIÓN DE LOS COMPUESTOS ORGÁNICOS Clasificación de
CICLO 6 QUÍMICA. Química orgánica. tiempo se conocen dos formas alotrópicas
 CICLO 6 QUÍMICA Química orgánica. La Química Orgánica se basa en el estudio de los compuestos de carbono. El carbono es el elemento 6 de la tabla periódica y puede formar más compuestos que ningún otro
CICLO 6 QUÍMICA Química orgánica. La Química Orgánica se basa en el estudio de los compuestos de carbono. El carbono es el elemento 6 de la tabla periódica y puede formar más compuestos que ningún otro
ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS
 ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS RESONANCIA MAGNÉTICA PROTÓNICA REGLAS BÁSICAS DE INTERPRETACIÓN Y TABLAS REGLAS BÁSICAS DE INTERPRETACIÓN DE RESONANCIA MAGNÉTICA PROTÓNICA
ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS RESONANCIA MAGNÉTICA PROTÓNICA REGLAS BÁSICAS DE INTERPRETACIÓN Y TABLAS REGLAS BÁSICAS DE INTERPRETACIÓN DE RESONANCIA MAGNÉTICA PROTÓNICA
TABLA I PASOS PARA LA INTERPRETACIÓN DE UN ESPECTRO DE MASAS
 TABLA I PASOS PARA LA INTERPRETACIÓN DE UN ESPECTRO DE MASAS 1. Examine el aspecto general del espectro para ver si es interpretable 2. Seleccione un candidato para el ion molecular (M + ). Base su selección
TABLA I PASOS PARA LA INTERPRETACIÓN DE UN ESPECTRO DE MASAS 1. Examine el aspecto general del espectro para ver si es interpretable 2. Seleccione un candidato para el ion molecular (M + ). Base su selección
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS ORGÁNICOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS ORGÁNICOS.Índice 1. Generalidades 2. Hidrocarburos: 2.1 Alcanos 2.2 Alquenos 2.3 Alquinos 2.4 Radicales 2.5 Hidrocarburos ramificados 2.6 Hidrocarburos cíclicos
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS ORGÁNICOS.Índice 1. Generalidades 2. Hidrocarburos: 2.1 Alcanos 2.2 Alquenos 2.3 Alquinos 2.4 Radicales 2.5 Hidrocarburos ramificados 2.6 Hidrocarburos cíclicos
VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES.
 VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES. ALCANOS NORMALES (LINEALES) En todos los alcanos normales o ramificados se espera encontrar solo estiramientos
VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES. ALCANOS NORMALES (LINEALES) En todos los alcanos normales o ramificados se espera encontrar solo estiramientos
Programa de Química Analítica Instrumental II (1803) Semestre 1/2016 Prof. Humberto Gómez Ruíz
 Programa de Química Analítica Instrumental II (1803) Semestre 1/2016 Prof. Humberto Gómez Ruíz Fecha Clase Comentarios lunes, 10 de agosto de 2015 1. INTRODUCCIÓN A LOS MÉTODOS ESPECTROSCÓPICOS. Programa
Programa de Química Analítica Instrumental II (1803) Semestre 1/2016 Prof. Humberto Gómez Ruíz Fecha Clase Comentarios lunes, 10 de agosto de 2015 1. INTRODUCCIÓN A LOS MÉTODOS ESPECTROSCÓPICOS. Programa
Metabolismo Reacciones en química orgánica Oxidaciones y reducciones Reacciones de formación y de ruptura de enlaces carbonocarbono.
 TEMA 5. Metabolismo Reacciones en química orgánica Oxidaciones y reducciones Reacciones de formación y de ruptura de enlaces carbonocarbono. Nucleofilia y electrofilia. Isomerizaciones y eliminaciones.
TEMA 5. Metabolismo Reacciones en química orgánica Oxidaciones y reducciones Reacciones de formación y de ruptura de enlaces carbonocarbono. Nucleofilia y electrofilia. Isomerizaciones y eliminaciones.
Existe un instante en el transcurso de la reacción en el que se rompe el enlace del reactivo y no se ha formado el enlace del producto.
 Las reacciones químicas transcurren por ruptura de determinados enlaces y formación de otros nuevos Existe un instante en el transcurso de la reacción en el que se rompe el enlace del reactivo y no se
Las reacciones químicas transcurren por ruptura de determinados enlaces y formación de otros nuevos Existe un instante en el transcurso de la reacción en el que se rompe el enlace del reactivo y no se
Tema 10 Sistemas insaturados conjugados
 Tema 10 Sistemas insaturados conjugados Sistemas alílicos. Estructura de los dienos conjugados. Calores de hidrogenación de dienos. Síntesis de dienos. Reactividad de los dienos conjugados. La reacción
Tema 10 Sistemas insaturados conjugados Sistemas alílicos. Estructura de los dienos conjugados. Calores de hidrogenación de dienos. Síntesis de dienos. Reactividad de los dienos conjugados. La reacción
5/31/2013 UNIVERSIDAD DE PUERTO RICO EN AGUADILLA ÁREA DE QUÍMICA. Laboratorio de Química Orgánica
 UNIVERSIDAD DE PUERTO RICO EN AGUADILLA ÁREA DE QUÍMICA Laboratorio de Química Orgánica Prof. Rafael A. Estremera Andújar, MS Dr. Carlos R. Ruiz Martínez, PhD. Dr. Carlos A. Nieves Marrero, PhD. JUNIO
UNIVERSIDAD DE PUERTO RICO EN AGUADILLA ÁREA DE QUÍMICA Laboratorio de Química Orgánica Prof. Rafael A. Estremera Andújar, MS Dr. Carlos R. Ruiz Martínez, PhD. Dr. Carlos A. Nieves Marrero, PhD. JUNIO
Programa de Química Analítica Instrumental II Semestre Prof. Humberto Gómez Ruíz
 Programa de Química Analítica Instrumental II Semestre 2- Prof. Humberto Gómez Ruíz Fecha Clase Comentarios 1. INTRODUCCIÓN. Antecedentes de las técnicas cromatográficas y su desarrollo. Programa Bibliografía
Programa de Química Analítica Instrumental II Semestre 2- Prof. Humberto Gómez Ruíz Fecha Clase Comentarios 1. INTRODUCCIÓN. Antecedentes de las técnicas cromatográficas y su desarrollo. Programa Bibliografía
Programa de Química Analítica Instrumental II Semestre 2/2014 Prof. Humberto Gómez Ruíz
 Programa de Química Analítica Instrumental II Semestre 2/ Prof. Humberto Gómez Ruíz Fecha Clase Comentarios lunes, 27 de enero de miércoles, 29 de enero de lunes, 03 de miércoles, 05 de lunes, 10 de miércoles,
Programa de Química Analítica Instrumental II Semestre 2/ Prof. Humberto Gómez Ruíz Fecha Clase Comentarios lunes, 27 de enero de miércoles, 29 de enero de lunes, 03 de miércoles, 05 de lunes, 10 de miércoles,
ANÁLISIS DE ESPECTROS
 EFECTOS DE CONJUGACIÓN Y TAMAÑO DE ANILLO EN C=O ALQUENOS Y AROMÁTICOS ( ESTIRAMIENTO C=C ) O-H 3600 N-H 3400 C-H 3000 C=N = 2250 C=C = 2150 C=O 1715 C=C 1650 C-O 1100 ANÁLISIS DE ESPECTROS CONJUGACIÓN
EFECTOS DE CONJUGACIÓN Y TAMAÑO DE ANILLO EN C=O ALQUENOS Y AROMÁTICOS ( ESTIRAMIENTO C=C ) O-H 3600 N-H 3400 C-H 3000 C=N = 2250 C=C = 2150 C=O 1715 C=C 1650 C-O 1100 ANÁLISIS DE ESPECTROS CONJUGACIÓN
CAPÍTULO 20 ESPECTROMETRÍA DE MASAS. Rosamil Rey, Ph.D. CHEM 4160
 CAPÍTULO 20 ESPECTROMETRÍA DE MASAS Rosamil Rey, Ph.D. CHEM 4160 INTRODUCCIÓN La espectrometría de masas no es una espectroscopia de absorción como IR, RMN y UV. Es el registro gráfico que sufre una molécula
CAPÍTULO 20 ESPECTROMETRÍA DE MASAS Rosamil Rey, Ph.D. CHEM 4160 INTRODUCCIÓN La espectrometría de masas no es una espectroscopia de absorción como IR, RMN y UV. Es el registro gráfico que sufre una molécula
Tema 1 Introducción. Universidad San Pablo CEU 1
 Tema 1 Introducción Revisión de nomenclatura de hidrocarburos. Estructura y nomenclatura de grupos funcionales. Principales tipos de reacciones orgánicas. Mecanismos de reacción. Rupturas homolíticas yheterolíticas.
Tema 1 Introducción Revisión de nomenclatura de hidrocarburos. Estructura y nomenclatura de grupos funcionales. Principales tipos de reacciones orgánicas. Mecanismos de reacción. Rupturas homolíticas yheterolíticas.
TEMA 3. Grupos funcionales con enlaces múltiples.
 TEMA 3. Grupos funcionales con enlaces múltiples. Alquenos. Alquinos. Compuestos aromáticos. El grupo carbonilo. Aldehídos. Cetonas. Ácidos carboxílicos. Ésteres. Anhídridos. Amidas Tioésteres, Fosfoésteres,
TEMA 3. Grupos funcionales con enlaces múltiples. Alquenos. Alquinos. Compuestos aromáticos. El grupo carbonilo. Aldehídos. Cetonas. Ácidos carboxílicos. Ésteres. Anhídridos. Amidas Tioésteres, Fosfoésteres,
Química orgánica. Cuarto Medio 25/06
 Química orgánica Cuarto Medio 25/06 CARBONO Es el elemento principal de las moléculas orgánicas. Debido a que este átomo, presenta una gran estabilidad. Dado que, tiene una baja tendencia a donar y quitar
Química orgánica Cuarto Medio 25/06 CARBONO Es el elemento principal de las moléculas orgánicas. Debido a que este átomo, presenta una gran estabilidad. Dado que, tiene una baja tendencia a donar y quitar
TEMA 3. Grupos funcionales con enlaces múltiples.
 TEMA 3. Grupos funcionales con enlaces múltiples. Alquenos. Alquinos. Compuestos aromáticos. El grupo carbonilo. Aldehídos. Cetonas. Ácidos carboxílicos. Ésteres. Anhídridos. Amidas Tioésteres, Fosfoésteres,
TEMA 3. Grupos funcionales con enlaces múltiples. Alquenos. Alquinos. Compuestos aromáticos. El grupo carbonilo. Aldehídos. Cetonas. Ácidos carboxílicos. Ésteres. Anhídridos. Amidas Tioésteres, Fosfoésteres,
Universidad de Puerto Rico-Humacao Departamento de Química QUIM 3032 (www.uprh.edu/~quimorg)
 1 Universidad de Puerto ico-umacao Departamento de Química QUIM 3032 (www.uprh.edu/~quimorg) Espectrometría de Masas Preparado por Prof. Jorge astillo evisión enero 2008 JS La espectrometría de masas es
1 Universidad de Puerto ico-umacao Departamento de Química QUIM 3032 (www.uprh.edu/~quimorg) Espectrometría de Masas Preparado por Prof. Jorge astillo evisión enero 2008 JS La espectrometría de masas es
CONTENIDOS MÍNIMOS septiembre
 DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
Química orgánica I: propiedades del carbono e hidrocarburos
 Química orgánica I: propiedades del carbono e hidrocarburos Aprendizajes esperados Conocer los tipos de compuestos orgánicos. Clasificar los distintos hidrocarburos. Conocer la nomenclatura orgánica de
Química orgánica I: propiedades del carbono e hidrocarburos Aprendizajes esperados Conocer los tipos de compuestos orgánicos. Clasificar los distintos hidrocarburos. Conocer la nomenclatura orgánica de
Unidad 1 (P.XVI) Reacciones Orgánicas Objetivos
 Unidad 1 (P.XVI) eacciones Orgánicas Objetivos 1. Diferencie la ruptura de enlaces homolítica de la heterolítica. 2. Identifique los diferentes tipos de reacciones orgánica: sustitución, eliminación, adición
Unidad 1 (P.XVI) eacciones Orgánicas Objetivos 1. Diferencie la ruptura de enlaces homolítica de la heterolítica. 2. Identifique los diferentes tipos de reacciones orgánica: sustitución, eliminación, adición
Resumen de la clase anterior
 Grupos Funcionales Resumen de la clase anterior sp 3 sp 2 sp Elemento de baja electronegatividad Capaz de hibridar electrones Carbono Hidrógeno Hidrocarburos Alifáticos Alicíclicos Aromáticos Alcanos Alquenos
Grupos Funcionales Resumen de la clase anterior sp 3 sp 2 sp Elemento de baja electronegatividad Capaz de hibridar electrones Carbono Hidrógeno Hidrocarburos Alifáticos Alicíclicos Aromáticos Alcanos Alquenos
clubdelquimico.blogspot.com
 clubdelquimico.blogspot.com Dadas las fórmulas siguientes: CH3OH, CH3CH2COOH, CH3COOCH3 y CH3CONH2 a. Diga cuál es el nombre del grupo funcional presente en cada una de las moléculas y nombre todos los
clubdelquimico.blogspot.com Dadas las fórmulas siguientes: CH3OH, CH3CH2COOH, CH3COOCH3 y CH3CONH2 a. Diga cuál es el nombre del grupo funcional presente en cada una de las moléculas y nombre todos los
Básico ( ) Profesional ( ) especializado ( x ) Horas de. Crédito s. Práctica ( )
 PROGRAMA DE ESTUDIO Nombre de la asignatura: TÉCNICAS ESPECTROSCÓPICAS. Clave: QUI15 Fecha de elaboración: Marzo 2015 Horas Semestre Horas semana Horas de Teoría Ciclo Formativo: Básico ( ) Profesional
PROGRAMA DE ESTUDIO Nombre de la asignatura: TÉCNICAS ESPECTROSCÓPICAS. Clave: QUI15 Fecha de elaboración: Marzo 2015 Horas Semestre Horas semana Horas de Teoría Ciclo Formativo: Básico ( ) Profesional
Unidad 1 (Parte V) Objetivos de la presentación:
 Unidad 1 (Parte V) Objetivos de la presentación: 1. onozca y maneje el tipo más adecuado de fórmula a utilizar cuando se representan compuestos orgánicos. 2. Identifique y clasifique los compuestos orgánicos
Unidad 1 (Parte V) Objetivos de la presentación: 1. onozca y maneje el tipo más adecuado de fórmula a utilizar cuando se representan compuestos orgánicos. 2. Identifique y clasifique los compuestos orgánicos
Nombre: Curso: Fecha:
 GUÍA ESTUDIO Nº1 PROPIEDADES DE HIDROCARBUROS Y FUNCIONES ORGÁNICAS PROPIEDADES DE LOS HIDROCARBUROS Propiedades de alcanos Subsector Profesor Química Paulina Gómez a) Propiedades físicas: Son menos densos
GUÍA ESTUDIO Nº1 PROPIEDADES DE HIDROCARBUROS Y FUNCIONES ORGÁNICAS PROPIEDADES DE LOS HIDROCARBUROS Propiedades de alcanos Subsector Profesor Química Paulina Gómez a) Propiedades físicas: Son menos densos
Acidez y Basicidad 16/10/2015. Dra. Ana M. Bruno 2015
 Acidez y Basicidad Dra. Ana M. Bruno 2015 Teorías ácido-base 1777 Lavoisier El oxígeno es el elemento presente en los ácidos (oxígeno en griego significa formador de ácidos ). 1810 Lavy El elemento común
Acidez y Basicidad Dra. Ana M. Bruno 2015 Teorías ácido-base 1777 Lavoisier El oxígeno es el elemento presente en los ácidos (oxígeno en griego significa formador de ácidos ). 1810 Lavy El elemento común
INSTITUTO DE QUÍMICA
 PONTIFICIA UNIVERSIDAD CATÓLICA DE VALPARAÍSO FUNDACION ISABEL CACES DE BROWN Avenida Brasil 2950, Valparaíso, Chile Teléfono (56-32) 273161 Fax (56-32) 273422 Casilla 4059 http://www.pucv.cl INSTITUTO
PONTIFICIA UNIVERSIDAD CATÓLICA DE VALPARAÍSO FUNDACION ISABEL CACES DE BROWN Avenida Brasil 2950, Valparaíso, Chile Teléfono (56-32) 273161 Fax (56-32) 273422 Casilla 4059 http://www.pucv.cl INSTITUTO
ESTRUCTURAS DE RESONANCIA
 1 ESTRUCTURAS DE RESONANCIA HIBRIDOS DE RESONANCIA CUANDO SON POSIBLES DOS O MÁS ESTRUCTURAS PARA REPRESENTAR LOS ENLACES DE UNA MOLÉCULA Y SÓLO DIFIENREN EN LA COLOCACIÓN DE LOS ELECTRONES LA MOLÉCULA
1 ESTRUCTURAS DE RESONANCIA HIBRIDOS DE RESONANCIA CUANDO SON POSIBLES DOS O MÁS ESTRUCTURAS PARA REPRESENTAR LOS ENLACES DE UNA MOLÉCULA Y SÓLO DIFIENREN EN LA COLOCACIÓN DE LOS ELECTRONES LA MOLÉCULA
Tema 9. Química Orgánica
 Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Espectrometría de Masa. Introducción. La espectrometría de masa crea partículas cargadas (iones).
 Espectrometría de Masa Introducción La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca
Espectrometría de Masa Introducción La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca
Tema 1 INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS EN LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS
 Tema 1 INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS EN LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS 1. Usando los datos de la siguiente tabla que ilustra el efecto de la electronegatividad del heteroátomo
Tema 1 INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS EN LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS 1. Usando los datos de la siguiente tabla que ilustra el efecto de la electronegatividad del heteroátomo
Química Orgánica y Biológica Apunte
 HIDROCARBUROS (dmonteci@exa.unicen.edu.ar) Son compuestos orgánicos que sólo contienen átomos de carbono y de hidrógeno. Tienen fórmulas muy variadas: CaHb. Los átomos de carbono se unen entre sí para
HIDROCARBUROS (dmonteci@exa.unicen.edu.ar) Son compuestos orgánicos que sólo contienen átomos de carbono y de hidrógeno. Tienen fórmulas muy variadas: CaHb. Los átomos de carbono se unen entre sí para
Espectrometría de Masa. Introducción. La espectrometría de masa crea partículas cargadas (iones).
 Espectrometría de Masa Introducción La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca
Espectrometría de Masa Introducción La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca
VOLUMENES ATOMICO Y MOLECULAR EN EL PUNTO DE EBULLICION NORMAL
 VOLUMENES ATOMICO Y MOLECULAR EN EL PUNTO DE EBULLICION NORMAL Volumen atómico x 10 3 ( m 3 / kg átomo ) Volumen molecular x 10 3 ( m 3 / kg mol ) Bromo 27,0 Aire 29,9 Carbono 14,8 Br 2 53,2 Cloro 24,6
VOLUMENES ATOMICO Y MOLECULAR EN EL PUNTO DE EBULLICION NORMAL Volumen atómico x 10 3 ( m 3 / kg átomo ) Volumen molecular x 10 3 ( m 3 / kg mol ) Bromo 27,0 Aire 29,9 Carbono 14,8 Br 2 53,2 Cloro 24,6
Alcoholes y halogenuros de alquilo
 Alcoholes y halogenuros de alquilo Resumén del capítulo Esta presentación es una introducción a las dos reacciones químicas y sus mecanismos que presentan los halogenuros de alquilo: (1) alcohol + halogenuro
Alcoholes y halogenuros de alquilo Resumén del capítulo Esta presentación es una introducción a las dos reacciones químicas y sus mecanismos que presentan los halogenuros de alquilo: (1) alcohol + halogenuro
Introducción a la Química Orgánica
 Introducción a la Química rgánica F. G. Calvo-Flores F. G. Calvo-Flores 1 Introducción F. G. Calvo-Flores 2 Configuración electrónca del carbono 2p 2s F. G. Calvo-Flores 3 ibridaciones del carbono Concepto
Introducción a la Química rgánica F. G. Calvo-Flores F. G. Calvo-Flores 1 Introducción F. G. Calvo-Flores 2 Configuración electrónca del carbono 2p 2s F. G. Calvo-Flores 3 ibridaciones del carbono Concepto
Departamento de Ciencias Profesores: Sergio Andrés Magdalena Loyola Curso: IIIº Medio QUÍMICA ORGÁNICA
 FUNDACIÓN EDUCACIONAL COLEGIO DE LOS SS.CC. Manquehue Departamento de Ciencias Profesores: Sergio Andrés Magdalena Loyola Curso: IIIº Medio Nombre: Curso: QUÍMICA ORGÁNICA CICLOALCANOS CnH2n Son cadenas
FUNDACIÓN EDUCACIONAL COLEGIO DE LOS SS.CC. Manquehue Departamento de Ciencias Profesores: Sergio Andrés Magdalena Loyola Curso: IIIº Medio Nombre: Curso: QUÍMICA ORGÁNICA CICLOALCANOS CnH2n Son cadenas
RECAPITULACIÓN 𝑀𝑎𝑠𝑎 𝑠𝑢𝑠𝑡𝑎𝑛𝑐𝑖𝑎 [𝑔] 𝑚𝑜𝑙 = 𝑀𝑎𝑠𝑎 𝑚𝑜𝑙𝑒𝑐𝑢𝑙𝑎𝑟 [𝑔/𝑚𝑜𝑙]
![RECAPITULACIÓN 𝑀𝑎𝑠𝑎 𝑠𝑢𝑠𝑡𝑎𝑛𝑐𝑖𝑎 [𝑔] 𝑚𝑜𝑙 = 𝑀𝑎𝑠𝑎 𝑚𝑜𝑙𝑒𝑐𝑢𝑙𝑎𝑟 [𝑔/𝑚𝑜𝑙] RECAPITULACIÓN 𝑀𝑎𝑠𝑎 𝑠𝑢𝑠𝑡𝑎𝑛𝑐𝑖𝑎 [𝑔] 𝑚𝑜𝑙 = 𝑀𝑎𝑠𝑎 𝑚𝑜𝑙𝑒𝑐𝑢𝑙𝑎𝑟 [𝑔/𝑚𝑜𝑙]](/thumbs/85/91585623.jpg) QUIMICA COMUN RECAPITULACIÓN RECAPITULACIÓN mol = Masa sustancia [g] Masa molecular [g/mol] QUÍMICA ORGÁNICA HIBRIDACIÓN CARBONO INTRODUCCIÓN La química orgánica, en simples palabras, es la química del
QUIMICA COMUN RECAPITULACIÓN RECAPITULACIÓN mol = Masa sustancia [g] Masa molecular [g/mol] QUÍMICA ORGÁNICA HIBRIDACIÓN CARBONO INTRODUCCIÓN La química orgánica, en simples palabras, es la química del
TÉCNICO SUPERIOR UNIVERSITARIO EN AGRICULTURA SUSTENTABLE Y PROTEGIDA EN COMPETENCIAS PROFESIONALES ASIGNATURA DE QUÍMICA ORGÁNICA
 TÉCNICO SUPERIOR UNIVERSITARIO EN AGRICULTURA SUSTENTABLE Y PROTEGIDA EN COMPETENCIAS PROFESIONALES ASIGNATURA DE QUÍMICA ORGÁNICA 1. Competencias Plantear y solucionar problemas con base en los principios
TÉCNICO SUPERIOR UNIVERSITARIO EN AGRICULTURA SUSTENTABLE Y PROTEGIDA EN COMPETENCIAS PROFESIONALES ASIGNATURA DE QUÍMICA ORGÁNICA 1. Competencias Plantear y solucionar problemas con base en los principios
Los compuestos químicos
 Los compuestos químicos Física y Química Compuestos formados por moléculas Oxford University Press España, S. A. Física y Química 3º ESO 2 Un compuesto químico es una sustancia pura formada por dos o más
Los compuestos químicos Física y Química Compuestos formados por moléculas Oxford University Press España, S. A. Física y Química 3º ESO 2 Un compuesto químico es una sustancia pura formada por dos o más
SEMANA No. 17 HIDROCARBUROS INSATURADOS
 SEMANA No. 17 HIDROCARBUROS INSATURADOS HIDROCARBUROS INSATURADOS Compuestos que contienen menos átomos de hidrógeno que los correspondientes alcanos. Por ser deficientes en hidrógeno se denominan INSATURADOS.
SEMANA No. 17 HIDROCARBUROS INSATURADOS HIDROCARBUROS INSATURADOS Compuestos que contienen menos átomos de hidrógeno que los correspondientes alcanos. Por ser deficientes en hidrógeno se denominan INSATURADOS.
CARACTERISTICAS QUE PRESENTA
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MEDICAS CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2015 SEMANA 15 INTRODUCCION A LA QUIMICA ORGÀNICA Elaborado por: Isabel Fratti
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MEDICAS CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2015 SEMANA 15 INTRODUCCION A LA QUIMICA ORGÀNICA Elaborado por: Isabel Fratti
QUÍMICA ORGÁNICA I (Parcial 1º)
 QUÍMICA ORGÁNICA I (Parcial 1º) 19-12-2013 Alumn@: DNI: 1 2 3 4 5 6 7 total calificación 1) Añadir los componentes que faltan (materiales de partida, reactivos o productos) de las siguientes reacciones:
QUÍMICA ORGÁNICA I (Parcial 1º) 19-12-2013 Alumn@: DNI: 1 2 3 4 5 6 7 total calificación 1) Añadir los componentes que faltan (materiales de partida, reactivos o productos) de las siguientes reacciones:
Ejercicios variados resueltos
 Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
QUÍMICA DEL CARBONO. Química 2º bachillerato Reacciones orgánicas 1
 QUÍMICA DEL CARBONO 1. Efectos electrónicos. 2. Reacciones orgánicas. 3. Reacción de sustitución. 4. Reacciones de adición. 5. Reacciones de eliminación. 6. Reacciones redox. 7. Ejemplos de reacciones.
QUÍMICA DEL CARBONO 1. Efectos electrónicos. 2. Reacciones orgánicas. 3. Reacción de sustitución. 4. Reacciones de adición. 5. Reacciones de eliminación. 6. Reacciones redox. 7. Ejemplos de reacciones.
Unidad IV: Espectrometría de Masas. Química Orgánica III Primer Semestre 2015 Facultad de CC.QQ. Y Farmacia USAC
 Unidad IV: Espectrometría de Masas Química Orgánica III Primer Semestre 2015 Facultad de CC.QQ. Y Farmacia USAC Identificación de un compuesto Orgánico Determinación de Propiedades Físicas Apariencia Olor
Unidad IV: Espectrometría de Masas Química Orgánica III Primer Semestre 2015 Facultad de CC.QQ. Y Farmacia USAC Identificación de un compuesto Orgánico Determinación de Propiedades Físicas Apariencia Olor
Efectos: inductivo, mesomérico,hiperconjugativo
 QUIMIA ORGANIA. Tema II. Efectos electrónicos. Efectos: inductivo, mesomérico,hiperconjugativo 1.Rotura de enlace covalente - homolítica - heterolítica 2. Intermedios de reacción: - radicales libres -
QUIMIA ORGANIA. Tema II. Efectos electrónicos. Efectos: inductivo, mesomérico,hiperconjugativo 1.Rotura de enlace covalente - homolítica - heterolítica 2. Intermedios de reacción: - radicales libres -
Introducción a la Química Orgánica
 Introducción a la Química Orgánica 2 Berzelius (1807) Compuestos Inorgánicos Orgánicos Sintetizados por los seres vivos Tienen Fuerza Vital 3 Friedrich Wölher (1828) Primera Síntesis orgánica: calor N
Introducción a la Química Orgánica 2 Berzelius (1807) Compuestos Inorgánicos Orgánicos Sintetizados por los seres vivos Tienen Fuerza Vital 3 Friedrich Wölher (1828) Primera Síntesis orgánica: calor N
GUÍA DOCENTE Química Orgánica II
 GUÍA DOCENTE 2015-2016 Química Orgánica II 1. Denominación de la asignatura: Química Orgánica II Titulación Grado en Química Código 5277 2. Materia o módulo a la que pertenece la asignatura: Química Orgánica
GUÍA DOCENTE 2015-2016 Química Orgánica II 1. Denominación de la asignatura: Química Orgánica II Titulación Grado en Química Código 5277 2. Materia o módulo a la que pertenece la asignatura: Química Orgánica
Espectroscopía Infraroja OBJETIVOS * 30/09/2010 * 1
 Espectroscopía Infraroja Carolina Jullian M. OBJETIVOS Adquirir principios y conceptos para la correcta formación de una base espectroscópica. Interpretación t adecuada d de los espectros para la obtención
Espectroscopía Infraroja Carolina Jullian M. OBJETIVOS Adquirir principios y conceptos para la correcta formación de una base espectroscópica. Interpretación t adecuada d de los espectros para la obtención
Problemas de Química 2.º Bachillerato Estructura atómica 13/11/2017 Pág. 1
 Problemas de Química 2.º Bachillerato Estructura atómica 3//207 Pág.. A y B son átomos de distintos elementos situados en el mismo período y que tienen 5 y 7 electrones de valencia, respectivamente. Responda,
Problemas de Química 2.º Bachillerato Estructura atómica 3//207 Pág.. A y B son átomos de distintos elementos situados en el mismo período y que tienen 5 y 7 electrones de valencia, respectivamente. Responda,
Criterio para aromaticidad
 Química Orgánica Paula Yurkanis Bruice Capítulos 14 y 15 Reacciones de SEA en el benceno Criterio para aromaticidad 1. Un compuesto debe tener una nube cíclica ininterrumpida de electrones π por arriba
Química Orgánica Paula Yurkanis Bruice Capítulos 14 y 15 Reacciones de SEA en el benceno Criterio para aromaticidad 1. Un compuesto debe tener una nube cíclica ininterrumpida de electrones π por arriba
MÉTODOS ACTUALES PARA EL ANÁLISIS DE SUSTANCIAS. Belén Cánovas Gómez Departamento Física y Química 1º BACHILLERATO Colegio Narval
 MÉTODOS ACTUALES PARA EL ANÁLISIS DE SUSTANCIAS Belén Cánovas Gómez Departamento Física y Química 1º BACHILLERATO Colegio Narval Para conocer la composición química de la materia, hay que llevar a cabo
MÉTODOS ACTUALES PARA EL ANÁLISIS DE SUSTANCIAS Belén Cánovas Gómez Departamento Física y Química 1º BACHILLERATO Colegio Narval Para conocer la composición química de la materia, hay que llevar a cabo
Guía Docente: QUÍMICA ORGÁNICA
 QUÍMICA ORGÁNICA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID CURSO 2014-2015 I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: NÚMERO DE CRÉDITOS 9 CARÁCTER: Obligatoria MATERIA: Química
QUÍMICA ORGÁNICA FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD COMPLUTENSE DE MADRID CURSO 2014-2015 I.- IDENTIFICACIÓN NOMBRE DE LA ASIGNATURA: NÚMERO DE CRÉDITOS 9 CARÁCTER: Obligatoria MATERIA: Química
QUÍMICA 2º Bachillerato Apuntes: Química Orgánica
 1(7) 1. GRUPO FUNCIONAL Y SERIE HOMÓLOGA 2. REACCIONES EN QUÍMICA ORGÁNICA 3. ISOMERÍA 1. GRUPO FUNCIONAL Y SERIE HOMÓLOGA Los compuestos orgánicos más sencillos son los hidrocarburos, que están constituidos
1(7) 1. GRUPO FUNCIONAL Y SERIE HOMÓLOGA 2. REACCIONES EN QUÍMICA ORGÁNICA 3. ISOMERÍA 1. GRUPO FUNCIONAL Y SERIE HOMÓLOGA Los compuestos orgánicos más sencillos son los hidrocarburos, que están constituidos
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUÍMICA ORGÁNICA III ACIDOS CARBOXILICOS
 Nombre: Mayra Morales Carrera: Bioquímica y Farmacia ACIDEZ UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUÍMICA ORGÁNICA III ACIDOS CARBOXILICOS Los ácidos carboxílicos son compuestos
Nombre: Mayra Morales Carrera: Bioquímica y Farmacia ACIDEZ UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUÍMICA ORGÁNICA III ACIDOS CARBOXILICOS Los ácidos carboxílicos son compuestos
Teoría Estructural 25/06/2012
 La Química Orgánica está a punto de enloquecerme. Se me figura como un bosque tropical primigenio, lleno de las cosas más notables, una selva infinita y terrible en la que uno no se atreve a penetrar porque
La Química Orgánica está a punto de enloquecerme. Se me figura como un bosque tropical primigenio, lleno de las cosas más notables, una selva infinita y terrible en la que uno no se atreve a penetrar porque
Royal American School QUIMICA 2º MEDIO Profesora: Jimena Hurtado Pereira GUÍA DE TRABAJO Nº1 QUIMICA ORGÁNICA NOMBRE: CURSO:
 Royal American School QUIMICA 2º MEDIO Profesora: Jimena Hurtado Pereira GUÍA DE TRABAJO Nº1 QUIMICA ORGÁNICA NOMBRE: CURSO: AE: Crear modelos del carbono y explicar sus propiedades como base para la formación
Royal American School QUIMICA 2º MEDIO Profesora: Jimena Hurtado Pereira GUÍA DE TRABAJO Nº1 QUIMICA ORGÁNICA NOMBRE: CURSO: AE: Crear modelos del carbono y explicar sus propiedades como base para la formación
ORGÁNICOS QUE POSEEN GRUPO FUNCIONAL CON ENLACE MULTIPLE CARBONO-HETEROÁTOMO
 Unidad IV: COMPUESTOS ORGÁNICOS QUE POSEEN GRUPO FUNCIONAL CON ENLACE MULTIPLE CARBONO-HETEROÁTOMO Química orgánica I Químicos Escuela de vacaciones junio 2016 Licda. Jaqueline Carrera. ENLACE DOBLE CARBONO-OXIGENO
Unidad IV: COMPUESTOS ORGÁNICOS QUE POSEEN GRUPO FUNCIONAL CON ENLACE MULTIPLE CARBONO-HETEROÁTOMO Química orgánica I Químicos Escuela de vacaciones junio 2016 Licda. Jaqueline Carrera. ENLACE DOBLE CARBONO-OXIGENO
