RECOMENDACIONES ARMONIZADAS PARA LA VALIDACIÓN DE MÉTODOS DE ANÁLISIS EN UN SOLO LABORATORIO (informe técnico)
|
|
|
- María Josefa Medina Franco
- hace 8 años
- Vistas:
Transcripción
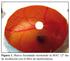
1 RECOMENDACIONES ARMONIZADAS PARA LA VALIDACIÓN DE MÉTODOS DE ANÁLISIS EN UN SOLO LABORATORIO (informe técnico) LA ASAMBLEA GENERAL En virtud del artículo 2 párrafo 2 iv del acuerdo sobre la creación de la Organización Internacional de la Viña y el Vino A propuesta de la Subcomisión de métodos de análisis y de valoración de los vinos, DECIDE crear un Anexo E en el Compendio Internacional de los Métodos de Análisis con el título Aseguramiento de la calidad en los laboratorios DECIDE: agrupar en este anexo E todas las resoluciones ya adoptadas relativas al aseguramiento de calidad en los laboratorios DECIDE introducir en el Anexo E de dicho Compendio las siguientes directivas: RECOMENDACIONES ARMONIZADAS PARA LA VALIDACIÓN DE MÉTODOS DE ANÁLISIS EN UN SOLO LABORATORIO (informe técnico) Síntesis La validación de métodos es una de las medidas universalmente reconocidas como parte necesaria de todo sistema completo de garantía de calidad en la química analítica. En el pasado ISO, IUPAC (Unión internacional de química pura y aplicada) y AOAC INTERNATIONAL han cooperado para elaborar protocolos o directivas comunes sobre Realización e Interpretación de Estudios de la eficiencia de los Métodos 1, sobre Ensayos de Aptitud de Laboratorios de Química Analítica) 2, sobre Control Interno de Calidad en Laboratorios de Química Analítica 3 y sobre Uso de Datos de Recuperación en las Mediciones Analíticas 4. La IUPAC ha encargado ahora al grupo de trabajo que elabore estos protocolos/directrices para establecer directrices de validación de métodos de análisis en un solo laboratorio. Dichas directrices ofrecen unas recomendaciones mínimas sobre los procedimientos que deben seguirse para garantizar una validación adecuada de los métodos analíticos. Se discutió un borrador de las directrices durante el Simposio Internacional sobre Armonización de Sistemas de Garantía de Calidad en Laboratorios Químicos, cuyas actas han sido publicadas por la Royal Society of Chemistry del Reino Unido. Resultados del Simposio sobre Armonización de Sistemas de Garantía de Calidad para Laboratorios Analíticos, Budapest, Hungría, 4-5 de noviembre de 1999 patrocinado por IUPAC, ISO y AOAC INTERNATIONAL 1
2 CONTENIDO 1 INTRODUCCIÓN 1.1 Antecedentes 1.2 Protocolos, normas y directrices existentes 2 DEFINICIONES Y TERMINOLOGÍA 2.1 Generales 2.2 Definiciones utilizadas en esta guía 3 Validación de métodos, incertidumbre y garantía de calidad 4 PRINCIPIOS BÁSICOS DE LA VALIDACIÓN DE MÉTODOS 4.1 Especificación y ámbito de validación 4.2 Hipótesis de ensayo 4.3 Fuentes de error en el análisis 4.4 Efectos del método y del laboratorio 5 Realización de estudios de validación 6 Alcance de los estudios de validación 6.1 El laboratorio debe utilizar un método completamente validado 6.2 El laboratorio debe utilizar un método completamente validado, pero con una nueva matriz 6.3 El laboratorio debe utilizar un método establecido, pero no estudiado de forma colectiva 6.4 El método ha sido publicado en la literatura científica especificando algunas características analíticas 6.5 El método ha sido publicado en la literatura científica sin especificación de sus características o ha sido desarrollado internamente 6.6 El método es empírico 6.7 El análisis es ad hoc 6.8 Cambios en el personal y el equipo 7 RECOMENDACIONES 8 REFERENCIAS 2
3 ANEXO A: NOTAS SOBRE LOS REQUISITOS DEL ESTUDIO DE LAS CARACTERÍSTICAS DEL RENDIMIENTO DEL MÉTODO. A1 A2 Aplicabilidad Selectividad A3 Calibrado y linealidad A3.1 Linealidad e intercepto A3.2 Ensayo del efecto de matriz general A3.3 Procedimiento final de calibrado A4 Veracidad A4.1 Estimación de la veracidad A4.2 Condiciones para las pruebas de veracidad A4.3 Valores de referencia para pruebas de veracidad A4.3.1 Materiales de referencia certificados (MRC) A4.3.2 Materiales de referencia A4.3.3 Uso de un método de referencia A4.3.4 Uso de adición/recuperación A5 A6 A7 A8 A9 A10 A11 A12 A13 Fidelidad Recuperación Rango Límite de detección Límite de determinación o límite de cuantificación Sensibilidad Robustez Adecuación al ensayo Variación de la matriz A14. Incertidumbre de la medición 3
4 ANEXO B. CONSIDERACIONES ADICIONALES PARA LA ESTIMACIÓN DE LA INCERTIDUMBRE EN ESTUDIOS DE VALIDACIÓN B1 B2 Análisis de sensibilidad Criterio profesional 4
5 1. INTRODUCCIÓN 1.1 ANTECEDENTES Se requieren métodos analíticos fiables para cumplir con las normativas nacionales e internacionales en todas las áreas de análisis. Por lo tanto, está admitido internacionalmente que un laboratorio deba tomar las medidas pertinentes para asegurarse de que es capaz de producir, y de que produce efectivamente, datos con el nivel necesario de calidad. Dichas medidas comprenden: utilización de métodos de análisis validados utilización de procedimientos internos de control de calidad participación en ensayos de aptitud; y obtención de la certificación según una norma internacional, habitualmente ISO/IEC Cabe resaltar que la certificación ISO/IEC concierne específicamente el establecimiento de la trazabilidad de las mediciones, al tiempo que fija un conjunto de otros requisitos técnicos y de gestión que incluyen todos los indicados anteriormente. Así, la validación de métodos es un componente esencial de las medidas que un laboratorio debe implementar para producir datos analíticos fiables. Otros aspectos de lo anteriormente dicho han sido tratados por el Grupo de Trabajo Interdivisional de la IUPAC sobre Armonización de Métodos de Garantía de Calidad para Laboratorios Analíticos, en particular mediante la elaboración de protocolos/directrices sobre los estudios (colectivos) de rendimiento de los métodos, 1 ensayos de aptitud, 2 y control interno de calidad. 3 En algunos sectores, y en particular en el análisis de los alimentos, la necesidad de utilizar métodos totalmente validados está estipulada por la legislación. 5,6 La validación total de un método analítico suele incluir un examen de las características del método mediante un estudio interlaboratorio del rendimiento del método (también conocido como estudio o ensayo colectivo). Se han elaborado protocolos internacionalmente aceptados para la validación completa de los métodos de análisis mediante ensayos colectivos, en especial el Protocolo Internacional Armonizado 1 y el procedimiento ISO. 7 Estos protocolos/estándares precisan que se incluyan en el ensayo colectivo un número mínimo de laboratorios y de materiales de ensayo sometidos al estudio inter-laboratorios para validar completamente el método analítico. Sin embargo, no siempre es práctico o necesario realizar una validación total de un método de análisis. En tales casos, puede resultar adecuado llevar a cabo una validación interna del método efectuada en un solo laboratorio. La validación del método en un solo laboratorio es pertinente en diferentes circunstancias, como por ejemplo: 5
6 para garantizar la viabilidad del método antes de realizar un costoso ensayo colectivo formal; para obtener pruebas de la fiabilidad de los métodos analíticos si no se dispone de datos de un ensayo colectivo o si no es posible realizar un ensayo colectivo formal; para garantizar que se utilizan correctamente los métodos validados estándares. Si se debe caracterizar un método internamente, es importante que el laboratorio determine y acuerde con el cliente qué características deben evaluarse exactamente. No obstante, en muchas situaciones estas características pueden afirmarse por ley (p.ej.: residuos de medicamentos veterinarios y pesticidas en los alimentos, en el sector de la alimentación). El contenido de la evaluación que llevan a cabo los laboratorios debe ajustarse a los requisitos de la legislación. No obstante, en algunas áreas analíticas un gran número de laboratorios utilizan el mismo método analítico para determinar componentes químicos estables en matrices definidas. Cabe observar que si es posible ofrecer a estos laboratorios un método estudiado de forma colectiva adecuado, el coste del ensayo colectivo para validar dicho método está plenamente justificado. El uso de un método estudiado de forma colectiva reduce considerablemente los esfuerzos que debe realizar un laboratorio, antes de utilizar el método de forma habitual, para llevar a cabo el conjunto de los trabajos de validación. Un laboratorio que emplee un método estudiado de forma colectiva que considere adecuado para sus propósitos sólo necesita demostrar que puede ofrecer las características de rendimiento estipuladas en el método. Dicha comprobación del uso correcto de un método es mucho menos costoso que una validación completa en un solo laboratorio. El coste total para la comunidad analítica de validar un método específico mediante un ensayo colectivo, validando posteriormente sus atributos de rendimiento en los laboratorios que deseen utilizarlo con frecuencia, suele ser inferior al coste que supone que muchos laboratorios realicen independientemente validaciones del mismo método en un solo laboratorio. 1.2 PROTOCOLOS, ESTÁNDARES Y GUÍAS EXISTENTES Se han elaborado varios protocolos y directrices 8-19 de validación de métodos e incertidumbres, principalmente por parte de AOAC INTERNATIONAL, la Conferencia Internacional de Armonización (ICH) y en documentos del Eurachem: El manual de estadística de la AOAC, que recomienda llevar a cabo estudios en un solo laboratorio antes de realizar ensayos colectivos 13 El texto 15 y la metodología 16 de la ICH, que prescriben los requisitos mínimos del estudio de validación para las pruebas utilizadas para presentación de medicamentos para su aprobación. La adecuación al propósito de los métodos analíticos: guía de laboratorio para la validación de métodos y temas relacionados (1998) 12 Cuantificación de la incertidumbre en las mediciones analíticas (2000) 9 6
7 La validación de métodos también se discutió ampliamente en una consulta conjunta a expertos de la FAO/IAEA, celebrada en diciembre de 1997, sobre la validación de métodos analíticos para el control alimentario, cuyo informe está disponible 19. Las presentes directrices recogen los principios científicos básicos de los documentos antes citados para ofrecer una información internacionalmente aceptada y, lo que es más importante, para indicar el camino de las mejores prácticas en la validación de métodos en un solo laboratorio. 2 DEFINICIONES Y TERMINOLOGÍA 2.1 DEFINICIONES GENERALES Los términos utilizados en el presente documento respetan en la medida de lo posible las definiciones de ISO y IUPAC. Los siguientes documentos contienen definiciones relevantes: i) IUPAC: Compendio de terminología química, 1987 ii) Vocabulario internacional de términos básicos y generales de metrología. ISO DEFINICIONES UTILIZADAS ESPECÍFICAMENTE EN ESTA GUÍA: Incertidumbre relativa: incertidumbre expresada como una desviación estándar relativa. Rango validado: parte del rango de concentración de un método analítico que ha sido objeto de una validación. 3 VALIDACIÓN DE MÉTODOS, INCERTIDUMBRE Y GARANTÍA DE CALIDAD La validación de métodos emplea un conjunto de pruebas que comprueban todas las hipótesis en las que se basa el método analítico, y establecen y documentan las características de rendimiento de un método, demostrando así si dicho método es adecuado para un propósito analítico particular. Las características de rendimiento de los métodos analíticos son: la aplicabilidad, la selectividad, el calibrado, la veracidad, la fidelidad, la recuperación, el rango de funcionamiento, el límite de cuantificación, el límite de detección, la sensibilidad y la robustez. Pueden añadirse la incertidumbre de la medición y la adecuación al propósito. 7
8 En términos estrictos, la validación debe hacer referencia a un sistema analítico, y no a un método analítico, ya que el sistema analítico incluye un protocolo de método definido, un rango de concentración definido para el analito y un tipo específico de material de prueba. Para los propósitos del presente documento, hablaremos de la validación de métodos en referencia al conjunto de un sistema analítico. Cuando el procedimiento analítico en sí esté establecido, lo denominaremos el protocolo. En el presente documento, la validación de métodos se considera diferente de las actividades que se realizan repetidamente, como el control de calidad interno (CCI) o los ensayos de aptitud. La validación de métodos se lleva a cabo una vez, o a intervalos relativamente infrecuentes, durante la vida útil de un método; nos indica qué rendimiento podemos esperar del método en el futuro. El CCI nos muestra cuál ha sido el comportamiento del método en el pasado, por cuyo motivo se trata como una actividad independiente en el Programa de Armonización del IUPAC. 3 En la validación de métodos, las características cuantitativas de interés tienen que ver con la fidelidad que probablemente ofrecerá el resultado. Por tanto, en general cabe afirmar que validar métodos equivale a estimar la incertidumbre de las mediciones. En la práctica de la validación, los diferentes aspectos del rendimiento del método se representan tradicionalmente mediante los elementos individuales antes indicados, modelo que en gran medida reproducen las presentes directrices. Sin embargo, debido al aumento de la confianza depositada en la incertidumbre de la medición como indicador clave de la adecuación al propósito y la fiabilidad de los resultados, los químicos analíticos cada vez realizan más validaciones de las mediciones para apoyar la estimación de la incertidumbre, y algunos profesionales desean que se haga inmediatamente. Así, la incertidumbre de la medición se trata brevemente en el Anexo A como una característica del rendimiento de un método analítico, mientras que el Anexo B ofrece información adicional sobre algunos procedimientos no tratados en otras partes del documento. 4 PRINCIPIOS BÁSICOS DE LA VALIDACIÓN DE MÉTODOS 4.1 ESPECIFICACIÓN Y ÁMBITO DE VALIDACIÓN La validación se aplica a un protocolo definido para determinar un analito específico y el rango de concentraciones en un tipo de material de prueba particular utilizado para un propósito específico. En general, la validación debe comprobar que el método se comporte de forma adecuada para la finalidad perseguida en todo el conjunto de concentraciones del analito y de materiales de ensayo a los que se aplica. Por consiguiente, estas características, junto con todos los criterios de adecuación al propósito, deben especificarse en su totalidad antes de realizar la validación. 8
9 4.2 HIPÓTESIS DE ENSAYO Además de facilitar las cifras de rendimiento que indican la adecuación al propósito, y que imperan en el uso práctico de los datos de validación, los estudios de validación actúan como una demostración objetiva de todas las hipótesis en las que se basa un método analítico. Por ejemplo, si debe calcularse un resultado a partir de una simple recta de calibrado, se supone implícitamente que el análisis está exento de sesgos significativos, que la respuesta es proporcional a la concentración de analito y que la dispersión de errores aleatorios es constante en todo el rango de interés. En la mayoría de casos, dichas hipótesis se establecen a partir de la experiencia acumulada durante el desarrollo del método o durante un largo período de tiempo, de manera que son razonablemente fiables. No obstante, la buena ciencia de las mediciones confía en hipótesis probadas. Por este motivo muchos estudios de validación se basan en pruebas de hipótesis estadísticas, cuyo objetivo es ofrecer una comprobación básica de que las hipótesis sobre los principios del método no contienen defectos graves. Esta nota aparentemente abstrusa reviste una importante implicación práctica: es más fácil comprobar una hipótesis fiable al principio que demostrar que una hipótesis particular es correcta. Así, cuando existe una largo historial de éxitos en el uso de una técnica analítica particular (como el análisis por cromatografía de gases o los métodos de digestión de ácidos) en un rango de analitos y matrices, las comprobaciones de validación se consideran justificadamente pequeñas pruebas preventivas. Al contrario, en ausencia de experiencia, el estudio de validación debe ofrecer pruebas claras de que las hipótesis tomadas son adecuadas para los casos particulares objeto del estudio, y, en general, es preciso estudiar todo el conjunto de circunstancias de manera detallada. Así pues, la extensión de los estudios de validación necesarios en un caso determinado dependerá, en parte, de la experiencia acumulada en la técnica analítica empleada. En los siguientes comentarios se dará por sentado que el laboratorio tiene una dilatada experiencia en la técnica en cuestión y que el propósito de cualquier prueba significativa es comprobar que no existen pruebas determinantes para descartar las hipótesis en las que se basa un protocolo particular. El lector deberá tener en cuenta que puede ser preciso realizar comprobaciones más exhaustivas si se emplean técnicas de medición menos conocidas o establecidas. 4.3 FUENTES DE ERROR EN EL ANÁLISIS Los errores en las mediciones analíticas surgen de diferentes fuentes * y a distintos niveles de organización. Una manera práctica de representar estas fuentes (para una concentración de analito específica) es la siguiente +24 : * En este documento no se tiene en cuenta la incertidumbre de muestreo en el sentido estricto de incertidumbre debida a la preparación de la muestra de laboratorio a partir del material a analizar a granel. La incertidumbre asociada a la toma de una porción de prueba de la muestra de laboratorio forma parte indisociable de la incertidumbre de medición y se incluye automáticamente a diferentes niveles de los análisis siguientes. + Existen muchos grupos o particiones de error posibles, y pueden ser útiles al estudiar fuentes de error particulares 9
10 error aleatorio de medición (repetibilidad); sesgo de ejecución; sesgo del laboratorio; sesgo del método; efecto de variación de la matriz. Aunque estas diferente fuentes no son necesariamente independientes, esta lista sirve para comprobar hasta qué punto un estudio de validación determinado estudia las fuentes de error. El término "repetibilidad" (durante la ejecución) incluye las contribuciones de cualquier parte del procedimiento que varía durante una ejecución, incluidas las contribuciones procedentes de errores gravimétricos y volumétricos conocidos, de la heterogeneidad del material de prueba y de la variación en las etapas de tratamiento químico del análisis, y se observa fácilmente en la dispersión de los análisis replicados. El efecto de ejecución se explica por las variaciones cotidianas en el sistema analítico, como los cambios de analistas o de lotes de reactivos, el recalibrado de los instrumentos y el entorno del laboratorio (p.ej.: cambios en la temperatura). En la validación en un solo laboratorio, el efecto de ejecución suele estimarse realizando un experimento diseñado con análisis replicados de un material apropiado en varias ejecuciones independientes. La variación entre laboratorios se deriva de factores como las variaciones en los estándares de calibrado, las diferencias entre las interpretaciones locales de un protocolo, los cambios en el equipo o los reactivos, o de factores del entorno, como las diferencias en las condiciones climáticas medias. La variación entre laboratorios se considera como una realidad evidente en los resultados de ensayos colectivos (estudios de rendimiento del método) y en los ensayos de aptitud. Además, en ocasiones sus resultados permiten detectar variaciones entre métodos. Generalmente, la repetibilidad, el efecto de ejecución y el efecto de laboratorio son de magnitud comparable, de modo que ninguno de ellos puede obviarse si se desea realizar una validación segura. En el pasado se tendía a despreciar algunos aspectos, en particular al estimar y plasmar la información sobre la incertidumbre. Esto provocaba unos intervalos de incertidumbre demasiado elevados. Por ejemplo, tal como se realiza normalmente, el ensayo colectivo no ofrece una imagen completa debido a que los factores de incertidumbre procedentes del sesgo del método y de la variación de la matriz no se estiman en los ensayos colectivos y deben estudiarse de forma independiente (en general, a priori en un estudio en un solo laboratorio). En la validación en un solo laboratorio existe el riesgo específico de no tener en cuenta el sesgo del laboratorio, y este elemento suele ser el mayor factor individual de incertidumbre de entre los anteriormente señalados. Por tanto, debe prestarse una especial atención al sesgo del laboratorio en la validación en un solo laboratorio. con más detalle o en una gama diferente de situaciones. Por ejemplo, el modelo estadístico ISO 5725 suele combinar los efectos de laboratorio y de ejecución, mientras que el procedimiento de valoración de la incertidumbre de la guía ISO GUM es idóneo para estudiar los efectos de cada influencia independiente y medible en el resultado. 10
11 Además de los problemas antes citados, la validación de un método se limita al ámbito de su aplicación, esto es, al método aplicado a una clase particular de material de prueba. Si existe una variación sustancial en los tipos de matriz dentro de la clase definida, puede existir una fuente adicional de variación debido al efecto de matriz dentro de la clase. Es evidente que si el método se utiliza posteriormente con materiales no pertenecientes a la clase definida (esto es, fuera del ámbito de la validación), el sistema analítico no puede considerarse validado, ya que se introduce un error adicional de magnitud desconocida en el proceso de medición. También es importante para los analistas tener en cuenta el modo en que varía el rendimiento de un método en función de la concentración del analito. En la mayoría de casos, la dispersión de los resultados aumenta claramente con la concentración y la recuperación puede diferir sustancialmente a altas y bajas concentraciones. Por tanto, la incertidumbre de la medición asociada a los resultados a menudo depende de estos dos factores y de otros factores dependientes de la concentración. Afortunadamente, suele ser razonable suponer una simple relación entre el rendimiento y la concentración del analito, ya que a menudo estos errores son proporcionales a la concentración del analito. * No obstante, cuando el rendimiento del método es de interés a concentraciones sustancialmente diferentes, es importante comprobar la supuesta relación entre rendimiento y concentración del analito. Esto suele hacerse comprobando el rendimiento en los extremos del rango probable, o a unos pocos niveles seleccionados. Las comprobaciones de linealidad también ofrecen información de este tipo. 4.4 EFECTOS DEL MÉTODO Y DEL LABORATORIO En la validación del método en un solo laboratorio es de suma importancia tener en cuenta el sesgo del método y el sesgo del laboratorio. Existen unos pocos laboratorios cuyas instalaciones permiten despreciar estos sesgos, pero se trata de casos excepcionales (sin embargo, si un solo laboratorio realiza un análisis particular, el sesgo del método y el sesgo del laboratorio adquieren una perspectiva distinta). Normalmente, los efectos del método y del laboratorio deben considerarse factores de incertidumbre, pero a menudo son más difíciles de estudiar que el error de repetibilidad y el efecto de ejecución. En general, para valorar las incertidumbres que producen es necesario utilizar información recabada independientemente del laboratorio. Las fuentes generalmente más útiles de dicha información son: (i) estadísticas derivadas de ensayos colectivos (no disponibles en muchas situaciones de validación de un método en un solo laboratorio), (ii) estadísticas derivadas de ensayos de aptitud y (iii) resultados de análisis de materiales de referencia certificados. Los ensayos colectivos estiman directamente la varianza de los sesgos entre laboratorios. Aunque teóricamente el diseño de estos ensayos puede presentar carencias, estas estimaciones de la varianza resultan útiles para muchos propósitos prácticos. En consecuencia, siempre es instructivo realizar una prueba de la validación en un solo laboratorio comparando las estimaciones de la incertidumbre * Puede no ser aplicable a concentraciones inferiores a 10 veces el límite de detección. 11
12 con las de la reproducibilidad a partir de ensayos colectivos. Si el resultado en un solo laboratorio es claramente menor, es probable que se hayan dejado de lado importantes fuentes de incertidumbre (también puede ser que un laboratorio particular trabaje con una incertidumbre menor que la hallada en ensayos colectivos: estos laboratorios deben tomar medidas especiales para justificar dicha postura). Si no se ha llevado a cabo ningún ensayo colectivo sobre la combinación método/material de prueba en cuestión, normalmente puede obtenerse una estimación de la desviación estándar de la reproducibilidad σ H a una concentración del analito c superior a unos 120 ppb mediante la función de Horwitz, σ H = 002c , con ambas variables expresadas como fracciones de masa (la estimación de Horwitz suele situarse dentro de un factor de, aproximadamente, dos de los resultados observados en el estudio colectivo). Se ha observado que la función de Horwitz es incorrecta a concentraciones inferiores a unos 120 ppb y que resulta más apropiado emplear una función modificada. 21, 25 Toda esta información puede aplicarse a un ensayo en un solo laboratorio produciendo unos cambios mínimos. Las estadísticas derivadas de ensayos de aptitud son particularmente interesantes porque ofrecen información general sobre la magnitud de los sesgos combinados de laboratorio y del método y, para el participante, información sobre el error total en ocasiones específicas. Las estadísticas, como la desviación estándar robusta de los resultados de los participantes para un analito en una serie de ensayos, puede utilizarse en principio de una forma similar a las desviaciones estándar de la reproducibilidad obtenidas de ensayos colectivos (p.ej.: para obtener un valor de referencia de la incertidumbre global y compararlo con estimaciones individuales obtenidas en una validación en un solo laboratorio). En la práctica, puede resultar más complicado explotar las estadísticas de los ensayos de aptitud, ya que no están sistemáticamente expresadas en tablas ni publicadas como los ensayos colectivos, sino que únicamente se comunican a los participantes. Obviamente, si deben utilizarse estas estadísticas, deben hacer referencia a la matriz y a la concentración del analito apropiadas. Los participantes individuales en programas de ensayos de aptitud también pueden valorar la validez de la incertidumbre estimada comparando sus resultados con los valores obtenidos en sucesivas ejecuciones 26. No obstante, esto es una actividad que se realiza de forma repetida y, por tanto, no entra estrictamente en la esfera de la validación en un solo laboratorio (que se realiza una sola vez). Si se dispone de un material de referencia certificado adecuado, un ensayo en un solo laboratorio permite al laboratorio valorar el sesgo del laboratorio y el sesgo del método combinados analizando el MRC varias veces. La estimación del sesgo combinado es la diferencia entre el resultado medio y el valor certificado. Pero no siempre se dispone de un material de referencia certificado adecuado, en cuyo caso deben emplearse otros materiales. En ocasiones pueden servir para este propósito los materiales restantes tras los ensayos de aptitud y, aunque los valores señalados de los materiales pueden tener incertidumbres cuestionables, su uso sin duda permite comprobar el sesgo global. Específicamente, suelen elegirse los valores indicados en los ensayos de aptitud para obtener una estimación con un sesgo mínimo, de manera que es importante realizar una prueba del sesgo significativo con este tipo de material. Otra alternativa es utilizar información de adición y 12
13 recuperación 4 para obtener estimaciones de estos sesgos, aunque puede haber fuentes de incertidumbre no medibles asociadas a estas técnicas. Actualmente, el efecto menos conocido en la validación es el debido a la variación de la matriz dentro de la clase de material de prueba definida. El requisito teórico para estimar este componente de incertidumbre es analizar en una única ejecución una gama representativa de materiales de prueba, estimar sus sesgos individuales y calcular la varianza de dichos sesgos. (El análisis en una sola ejecución implica que los sesgos elevados no tienen efectos sobre la varianza. Si se utiliza una amplia gama de concentraciones, debe tolerarse un cambio en el sesgo con la concentración). Si los materiales representativos son materiales de referencia certificados, los sesgos pueden estimarse directamente como diferencias entre los resultados y los valores de referencia, lo que redunda en beneficio de la claridad del procedimiento. En el caso más probable de que no existan suficientes materiales de referencia certificados, puede recurrirse a ensayos de recuperación con una gama habitual de materiales de prueba, con la debida precaución. Actualmente existe muy poca información cuantitativa sobre la magnitud de incertidumbres derivadas de esta fuente, aunque en algunos casos se sospecha que es grande. 5 REALIZACIÓN DE ESTUDIOS DE VALIDACIÓN En otros documentos se explica con detalle el diseño y la ejecución de estudios de validación de métodos, de manera que no lo repetiremos aquí. Sin embargo, cabe recordar los principios básicos: Es esencial que los estudios de validación sean representativos. Esto significa que, en la medida de lo posible, deberían realizarse los estudios necesarios para obtener una estimación realista del número y la gama de efectos que se producen durante el uso normal del método, al tiempo que deben analizar la gama de concentraciones y de tipos de muestra que abarca el método. Por ejemplo, si un factor (p.ej.: la temperatura ambiente) varía sustancialmente durante la realización de un experimento de fidelidad, los efectos de dicho factor aparecen directamente en la varianza observada y no precisan de un estudio adicional, a menos que se desee mejorar todavía más el método. En el contexto de la validación de métodos, una variación representativa significa que el factor debe tomar una distribución de valores adecuada para el rango previsto del parámetro en cuestión. Para los parámetros continuos medibles, puede ser un rango permitido, una incertidumbre determinada o un rango esperado; para los factores discontinuos, o factores con efectos impredecibles, como la matriz de la muestra, un rango representativo corresponde a los diferentes tipos o niveles de factor permitidos o hallados durante el uso normal del método. Idealmente, la representatividad abarca el rango de valores y también su distribución. Por desgracia, a menudo no es económicamente viable disponer de la variación completa de muchos factores a muchos niveles. No obstante, para propósitos prácticos los ensayos basados en extremos del rango esperado o en cambios mayores de lo previsto son un mínimo aceptable. 13
14 Al seleccionar los factores de la variación, es importante asegurarse de "ejercer" al máximo los mayores efectos. Por ejemplo, si la variación diaria (quizás a causa de los efectos del recalibrado) es sustancial comparada con la repetibilidad, dos determinaciones de cada una durante cinco días ofrecerá una mejor estimación de la fidelidad intermedia que cinco determinaciones de cada una durante dos días. Diez determinaciones individuales en días separados sería todavía mejor, aunque no ofrecería información adicional sobre la repetibilidad día a día. Al planificar comprobaciones de significación, los estudios deben tener suficiente potencia para detectar estos efectos antes de que lleguen a revestir una fuerte importancia práctica (comparable al mayor componente de incertidumbre). Además, cabe tener en cuenta las siguientes consideraciones: Si se sabe o se sospecha que los factores interactúan, es importante tener en cuenta el efecto de interacción. Esto puede lograrse realizando una selección aleatoria desde diferentes niveles de interacción de los parámetros o mediante un meticuloso diseño sistemático para obtener información de los efectos de interacción o de la covarianza. Al realizar estudios del sesgo global, es importante que los materiales y los valores de referencia sean relevantes para los materiales objeto de los ensayos rutinarios. 6 ALCANCE DE LOS ESTUDIOS DE VALIDACIÓN El alcance de la validación de un método nuevo, modificado o desconocido depende del estatus del método y de la competencia del laboratorio encargado de llevarla a cabo. A continuación se indican algunas sugerencias relativas a la validación y las mediciones de comprobación en diferentes circunstancias. Salvo indicación explícita, se supondrá que el método tendrá un uso periódico. 6.1 EL LABORATORIO DEBE UTILIZAR UN MÉTODO TOTALMENTE VALIDADO El método ha sido estudiado en un ensayo colectivo y el laboratorio debe comprobar si es capaz de alcanzar su rendimiento publicado (o si es capaz de cumplir los requisitos de las tareas analíticas). El laboratorio debe realizar estudios de la fidelidad, del sesgo (incluidos estudios de variación de la matriz) y posiblemente estudios de la linealidad, aunque puede omitir algunas pruebas, como por ejemplo la de robustez. 14
15 6.2 EL LABORATORIO DEBE UTILIZAR UN MÉTODO TOTALMENTE VALIDADO, PERO CON UNA NUEVA MATRIZ El método ha sido estudiado en un ensayo colectivo y el laboratorio debe comprobar que la nueva matriz no introduce nuevas fuentes de error en el sistema. Se precisa el mismo rango de validación que anteriormente. 6.3 EL LABORATORIO DEBE UTILIZAR UN MÉTODO BIEN ESTABLECIDO, PERO NO ESTUDIADO DE FORMA COLECTIVA Se precisa el mismo rango de validación que anteriormente. 6.4 EL MÉTODO HA SIDO PUBLICADO EN LA LITERATURA CIENTÍFICA JUNTO CON ALGUNAS CARACTERÍSTICAS ANALÍTICAS El laboratorio debe realizar estudios de la fidelidad, del sesgo (incluidos estudios de la variación de la matriz), de la robustez y de la linealidad. 6.5 EL MÉTODO HA SIDO PUBLICADO EN LA LITERATURA CIENTÍFICA SIN ESPECIFICACIÓN DE SUS CARACTERÍSTICAS O HA SIDO DESARROLLADO INTERNAMENTE El laboratorio debe realizar estudios de fidelidad, del sesgo (incluidos estudios de la variación de la matriz), de la robustez y de la linealidad. 6.6 EL MÉTODO ES EMPÍRICO Un método empírico se caracteriza porque la cantidad estimada es simplemente el resultado hallado tras aplicar el procedimiento. Esto difiere de las mediciones que valoran cantidades independientes del método, como la concentración de un analito particular en una muestra, en las que el sesgo del método es convencionalmente cero y la variación de la matriz (dentro de la clase definida) es irrelevante. No puede olvidarse el sesgo del laboratorio, pero probablemente sea difícil estimarlo mediante un ensayo en un solo laboratorio. Además, es improbable que haya materiales de referencia disponibles. En ausencia de datos de un ensayo colectivo, pueden obtenerse algunas estimaciones de la fidelidad interlaboratorio a partir de estudios de robustez específicamente diseñados o calculadas utilizando la función de Horwitz. 15
16 6.7 EL ANÁLISIS ES AD HOC En ocasiones es necesario utiliza análisis ad hoc para establecer el rango general de un valor sin que ello suponga un gasto importante y con baja criticidad. Por ello, el esfuerzo realizable de validación se ve estrictamente limitado. El sesgo debe estudiarse mediante métodos como la estimación de la recuperación o la adición de analito, y la fidelidad, por replicación. 6.8 CAMBIOS EN EL PERSONAL O EL EQUIPO Ejemplos más importantes: cambios en los principales instrumentos, nuevos lotes de reactivos muy variables (por ejemplo, anticuerpos policlonales), cambios realizados en el recinto del laboratorio, métodos utilizados por primera vez por nuevos empleados o un método validado utilizado tras un período de desuso. La acción esencial es demostrar que no se han producido cambios nocivos. La comprobación mínima es realizar una prueba de sesgo y un experimento a priori y a posteriori de los materiales de prueba o de control habituales. En general, las pruebas realizadas deben reflejar el posible impacto del cambio en el procedimiento analítico. 7 RECOMENDACIONES Recomendaciones relativas al uso de la validación de métodos en un solo laboratorio: Siempre que sea posible y práctico, el laboratorio debe utilizar un método de análisis cuyas características de rendimiento hayan sido evaluadas mediante un ensayo colectivo, de conformidad con un protocolo internacional. Si no se dispone de dicho método, el método debe validarse internamente antes de utilizarlo para generar datos analíticos para un cliente. La validación en un solo laboratorio precisa que el laboratorio seleccione las características a evaluar adecuadas, como por ejemplo: aplicabilidad, selectividad, calibrado, exactitud, fidelidad, rango, límite de cuantificación, límite de detección, sensibilidad, robustez y practicabilidad. El laboratorio debe tener en cuenta los requisitos del cliente al elegir las características a determinar. El laboratorio debe facilitar pruebas que demuestren que se han estudiado esas características, si así lo solicita el cliente. 16
17 8 REFERENCIAS 1. "Protocol for the Design, Conduct and Interpretation of Method Performance Studies", W Horwitz, Pure Appl. Chem., 1988, 60, , revisado W. Horwitz, Pure Appl. Chem., 1995, 67, The International Harmonised Protocol for the Proficiency Testing of (Chemical) Analytical Laboratories, M Thompson y R Wood, Pure Appl. Chem., 1993, 65, (También publicado en J. AOAC International, 1993, 76, Harmonised Guidelines For Internal Quality Control in Analytical Chemistry Laboratories, Michael Thompson y Roger Wood, J. Pure & Applied Chemistry, 1995, 67(4), Harmonised Guidelines for the Use of Recovery Information in Analytical Measurement, Michael Thompson, Stephen Ellison, Ales Fajgelj, Paul Willetts y Roger Wood, J. Pure & Applied Chemistry, 1999, 71(2), Council Directive 93/99/EEC on the Subject of Additional Measures Concerning the Official Control of Foodstuffs, O. J., 1993, L Procedural Manual of the Codex Alimentarius Commission, 10th Edition, FAO, Roma, Precision of Test Methods, Ginebra, 1994, ISO 5725, se publicaron ediciones anteriores en 1981 y Guide to the Expression of Uncertainty in Measurement, ISO, Ginebra, Quantifying Uncertainty in Analytical Measurement, Secretaría de EURACHEM, Laboratorio Químico Gubernamental, Teddington, Reino Unido, 1995, Guía de EURACHEM (en proceso de revisión). 10. International vocabulary of basic and general terms in metrology ISO, Ginebra Validation of Chemical Analytical Methods, Secretaría de NMKL, Finlandia, 1996, Procedimiento NMKL nº EURACHEM Guide: The fitness for purpose of analytical methods. A Laboratory Guide to method validation and related topics, LGC, Teddington También disponible en la Secretaría de EURACHEM y en el sitio Web. 13. Statistics manual of the AOAC, AOAC INTERNATIONAL, Gaithersburg, Maryland, EE.UU.,
18 14. An Interlaboratory Analytical Method Validation Short Course developed by the AOAC INTERNATIONAL, AOAC INTERNATIONAL, Gaithersburg, Maryland, EE.UU., Text on validation of analytical procedures Conferencia Internacional sobre Armonización. Federal Register, Vol. 60, 1 de marzo de 1995, páginas Validation of analytical procedures: Methodology Conferencia Internacional sobre Armonización. Federal Register, Vol. 62, No. 96, 19 de mayo de 1997, páginas Validation of Methods, Inspectorate for Health Protection, Rijswijk, Países Bajos, Informe A Protocol for Analytical Quality Assurance in Public Analysts Laboratories, Association of Public Analysts, 342 Coleford Road, Sheffield S9 5PH, Reino Unido, Validation of Analytical Methods for Food Control, Informe de Consulta Conjunta de Expertos FAO/IAEA, diciembre de 1997, Documento de la FAO sobre Alimentos y Nutrición nº. 68, FAO, Roma, Estimation and Expression of Measurement Uncertainty in Chemical Analysis, Secretaría de NMKL, Finlandia, 1997, Procedimiento NMKL nº M Thompson, PJ Lowthian, J AOAC Int, 1997, 80, Recomendación de IUPAC: Nomenclature in evaluation of analytical methods, including quantification and detection capabilities Pure and Applied Chem. 1995, ISO Capability of detection. (Several parts). International Standards Organisation, Ginebra. 24. M. Thompson, Analyst, 2000, 125, Recent trends in inter-laboratory precision at ppb and sub-ppb concentrations in relation to fitness for purpose criteria in proficiency testing M Thompson, Analyst, 2000, 125, How to combine proficiency test results with your own uncertainty estimate - the zeta score, Comité de Métodos Analíticos de la Royal Society of Chemistry, documentos técnicos de AMC, publicado por M. Thompson, AMC Technical Brief No. 2, 18
19 ANEXO A: NOTAS SOBRE LOS REQUISITOS DEL ESTUDIO DE LAS CARACTERÍSTICAS DEL RENDIMIENTO DEL MÉTODO Los requisitos generales de las características de rendimiento de un método son los siguientes. A1 APLICABILIDAD Tras la validación, la documentación debe reflejar, además de las especificaciones de rendimiento, los siguientes datos: La identidad del analito, incluida una especificación si es preciso (ejemplo: arsénico total ); el rango de concentración cubierto por la validación (ejemplo: 0-50 ppm ); una especificación del rango de matrices del material de prueba cubierto por la validación (ejemplo: marsico ); un protocolo que describa el equipo, los reactivos, el procedimiento (incluida la variación permitida en las instrucciones especificadas; p.ej.:, caliente a 100 ± 5 durante 30 ± 5 minutos ), los procedimientos de calibrado y calidad, y cualquier precaución de seguridad necesaria; la aplicación prevista y los umbrales de incertidumbre críticos (p.ej.: Análisis de alimentos para detección de enfermedades. La incertidumbre estándar u(c) del resultado c debe ser inferior a 0,1 c. ). A2 SELECTIVIDAD La selectividad es el grado en que un método puede cuantificar el analito con precisión en presencia de interferentes. Idealmente, la selectividad debería evaluarse para todos los interferentes importantes susceptibles de estar presentes. Es de especial importancia comprobar los interferentes susceptibles de responder a la prueba de acuerdo con los principios químicos. Por ejemplo, es previsible que las pruebas colorimétricas del amoniaco respondan a los aminos alifáticos primarios. Puede no ser viable considerar o probar cada uno de los interferentes potenciales; en tal caso, se recomienda comprobar los casos probablemente peores. Como principio general, la selectividad debe ser suficientemente buena para poder descartar cualquier interferencia. En muchos tipos de análisis, la selectividad es esencialmente un estudio cualitativo basado en la significación, o bien un conjunto de pruebas pertinentes de interferencia. Sin embargo, existen mediciones cuantitativas que pueden resultar útiles, como por ejemplo el índice de selectividad b an /b int, donde b an es la sensibilidad del método (función de la curva de calibrado) y b int la pendiente de la respuesta independientemente producida por un interferente potencial, que ofrece una medición cuantitativa de la interferencia. b int puede determinarse aproximadamente realizando el 19
20 procedimiento con una matriz blanca y añadiendo a la misma el interferente potencial a una concentración adecuada. Si no se dispone de una matriz blanca y en su lugar se emplea un material habitual, b int puede estimarse mediante un simple experimento con la única hipótesis de que no existen efectos de matriz mutuos. Cabe recordar que b int es más fácil de determinar en ausencia del analito porque el efecto puede confundirse con otro tipo de interferencias si la sensibilidad del analito se ve afectada por el interferente (efecto de matriz). A3 CALIBRADO Y LINEALIDAD Con la excepción de crasos errores en la preparación de los materiales de calibrado, los errores de calibrado suelen ser (aunque no siempre) un componente menor del total de la incertidumbre, y normalmente pueden incluirse con seguridad en otras categorías de errores establecidas por métodos top-down. Por ejemplo, los errores aleatorios resultantes del calibrado forman parte del sesgo de ejecución, que se valora en su conjunto, mientras que los errores sistemáticos procedentes de esta fuente se consideran parte del sesgo del laboratorio, que también se valora en su conjunto. No obstante, existen algunas características de calibrado que resulta útil conocer al principio de la validación de métodos dado que afectan a la estrategia de desarrollo óptimo del procedimiento. En esta clase se incluyen cuestiones como si la función de calibrado (a) es lineal, (b) si cruza el origen o (c) si no se ve afectada por la matriz del material de prueba. Los procedimientos aquí descritos hacen referencia a estudios de calibrado en validaciones, que deben ser más precisos que el calibrado realizado en análisis rutinarios. Por ejemplo, una vez establecido en la validación que una función de calibrado es lineal y que cruza el origen, puede emplearse una estrategia de calibrado mucho más simple para el uso normal (por ejemplo, un diseño repetido de dos puntos). En la validación, normalmente los errores procedentes de esta simple estrategia de calibrado se incluyen en un nivel superior de errores. A3.1 Linealidad e intercepto La linealidad puede probarse informalmente examinando un gráfico de los residuos producidos por regresión lineal de las respuestas a las concentraciones en un equipo de calibrado adecuado. Los modelos curvados sugieren una falta de adecuación al no ser lineal la función de calibrado. Puede realizarse una prueba de significación comparando la varianza de la inadecuación con la del error puro. No obstante, existen otras causas de inadecuación a parte de la no linealidad que pueden aparecer en algunos tipos de calibrado analítico, de manera que la prueba de significación debe utilizarse junto con un grafico residual. Pese a su uso actualmente extendido como indicador de la calidad de la adecuación, el coeficiente de correlación es engañoso e inapropiado para demostrar la linealidad y no debe utilizarse. El diseño es un elemento esencial en las pruebas de falta de adecuación, dado que es fácil confundir la no linealidad con desviaciones. Las mediciones replicadas son necesarias para ofrecer una estimación del error puro si no existen estimaciones independientes. En ausencia de directrices 20
21 específicas, debe aplicarse lo siguiente: RESOLUCIÓN OENO 8/2005 debe haber seis o más calibradores; los calibradores deben espaciarse de forma uniforme a lo largo del rango de concentración de interés; el rango debe abarcar del 0 al 150% o del 50 al 150% de la concentración susceptible de ser hallada, según cuál sea más adecuado; los calibradores deben ejecutarse al menos por duplicado y, preferiblemente, por triplicado o más, en orden aleatorio. Después de extrapolar la adecuación mediante la regresión lineal simple, deben examinarse los residuos para hallar modelos obvios. La heteroscedasticidad es bastante común en el calibrado analítico y un modelo que la sugiera significa que la mejor manera de tratar los datos calibrados es por regresión ponderada. La imposibilidad de utilizar una regresión ponderada en estas circunstancias podría dar origen a errores exagerados en la parte baja de la función de calibrado. La prueba de falta de adecuación puede llevarse a cabo con una regresión simple o ponderada. También puede realizarse una prueba de intercepto significativamente diferente de cero con estos datos si no hay una falta de adecuación significativa. A3.2 Ensayo del efecto de matriz general Simplifica enormemente el calibrado si los calibradores pueden prepararse como una simple solución del analito. Si debe adoptarse esta estrategia, deben estudiarse los efectos de un posible desemparejamiento general de la matriz en la validación. La prueba del efecto de matriz general puede efectuarse aplicando el método de adiciones de analito (también denominado de adiciones estándares ) a una solución de prueba derivada de un material de prueba habitual. La prueba debe realizarse de manera que ofrezca la misma dilución final que la que produce el procedimiento normal, y el rango de adiciones debe abarcar el mismo rango que la validación del calibrado definido por el procedimiento. Si el calibrado es lineal, las pendientes de la función de calibrado habitual y el gráfico de adiciones de analito pueden compararse para hallar diferencias significativas. La ausencia de significación indica que no existe un efecto de matriz general detectable. Si el calibrado no es lineal, puede emplearse un método más complejo para demostrar la significación, pero normalmente bastará con una comparación visual a iguales concentraciones. La ausencia de significación en esta prueba suele revelar la ausencia de variaciones en el efecto de matriz [Sección A13]. 21
22 A3.3 Procedimiento final de calibrado También puede ser preciso validar de forma independiente la estrategia de calibrado tal como está especificada en el procedimiento, aunque los errores que ello implique contribuirán a aumentar las incertidumbres estimadas. Lo importante aquí es que la incertidumbre de la evaluación estimada a partir de diseños específicos de linealidad, etc. sea inferior a la derivada del simple calibrado definido en el protocolo del procedimiento. A4 VERACIDAD A4.1 Estimación de la veracidad La veracidad es el grado de coincidencia entre el resultado de una prueba y el valor de referencia aceptado de la propiedad objeto de la medición. La veracidad se expresa cuantitativamente en términos de sesgo ; cuanto más pequeño es el sesgo, mayor veracidad indica. El sesgo suele determinarse comparando la respuesta del método a un material de referencia con el valor conocido asignado a ese material. Se recomienda realizar pruebas de significación. Si la incertidumbre del valor de referencia no es despreciable, la evaluación de los resultados debe tener en cuenta la incertidumbre del material de referencia y la variabilidad estadística. A4.2 Condiciones para las pruebas de veracidad El sesgo puede aparecer a diferentes niveles de la organización de un sistema analítico; por ejemplo, el sesgo de ejecución, el sesgo del laboratorio y el sesgo del método. Es importante recordar cuál se está analizando mediante los diferentes métodos de estudio del sesgo. En particular: La media de una serie de análisis de un material de referencia, realizados en su totalidad en una única ejecución, ofrece información sobre la suma del efecto del método, del laboratorio y de la ejecución en esa ejecución particular. Dado que se supone que el efecto de ejecución es aleatorio entre diferentes ejecuciones, el resultado variará de una ejecución a otra más de lo esperado a partir de la dispersión observable de los resultados, lo que debe tenerse en cuenta al evaluar los resultados (por ejemplo, realizando una prueba del sesgo medido respecto a la desviación estándar entre las ejecuciones, investigada por separado). La media de análisis repetidos de un material de referencia en varias ejecuciones mide el efecto combinado del método y del laboratorio en un laboratorio particular (salvo si se asigna el valor utilizando un método particular). 22
CRITERIOS ESPECÍFICOS PARA EVALUAR LA INCERTIDUMBRE EN PROCESOS DE MEDICIÓN EN LABORATORIOS QUIMICOS
 Página 1 de 6 TITULO: CRITERIOS ESPECIFICOS PARA EVALUAR LA INCERTIDUMBRE DE UN PROCESO DE MEDICIÓN EN LABORATORIOS QUÍMICOS Resumen: El presente documento contiene los criterios en lo referente a la evaluación
Página 1 de 6 TITULO: CRITERIOS ESPECIFICOS PARA EVALUAR LA INCERTIDUMBRE DE UN PROCESO DE MEDICIÓN EN LABORATORIOS QUÍMICOS Resumen: El presente documento contiene los criterios en lo referente a la evaluación
Validación de métodos de ensayo
 Validación de métodos de ensayo Validación verificación de que los requisitos especificados son adecuados para un uso determinado Ejemplo: Un procedimiento de medición ordinariamente usado para la medición
Validación de métodos de ensayo Validación verificación de que los requisitos especificados son adecuados para un uso determinado Ejemplo: Un procedimiento de medición ordinariamente usado para la medición
ASEGURAMIENTO DE LA CALIDAD EN LABORATORIO
 FUNDACION NEXUS ASEGURAMIENTO DE LA CALIDAD EN LABORATORIO Marzo de 2012 CALIDAD, CONTROL DE LA CALIDAD Y ASEGURAMIENTO DE LA CALIDAD El laboratorio de análisis ofrece a sus clientes un servicio que se
FUNDACION NEXUS ASEGURAMIENTO DE LA CALIDAD EN LABORATORIO Marzo de 2012 CALIDAD, CONTROL DE LA CALIDAD Y ASEGURAMIENTO DE LA CALIDAD El laboratorio de análisis ofrece a sus clientes un servicio que se
Validación de Métodos
 Validación de Métodos Francisco Rojo Callejas Validación de Métodos Definiciones Parámetros básicos Requisitos Validación de Métodos El proceso de definir las condiciones analíticas y confirmar que el
Validación de Métodos Francisco Rojo Callejas Validación de Métodos Definiciones Parámetros básicos Requisitos Validación de Métodos El proceso de definir las condiciones analíticas y confirmar que el
Requerimientos sobre Validación de Métodos en el marco de la Acreditación de Laboratorios según la norma ISO 17025
 Requerimientos sobre Validación de Métodos en el marco de la Acreditación de Laboratorios según la norma ISO 17025 Disertante: Lic. Pablo Álvarez Calidad y Competitividad INTI-Química Guías de referencia
Requerimientos sobre Validación de Métodos en el marco de la Acreditación de Laboratorios según la norma ISO 17025 Disertante: Lic. Pablo Álvarez Calidad y Competitividad INTI-Química Guías de referencia
INCERTIDUMBRE Y PRECISIÓN
 INCERTIDUMBRE Y PRECISIÓN Alicia Maroto, Ricard Boqué, Jordi Riu, F. Xavier Rius Departamento de Química Analítica y Química Orgánica Instituto de Estudios Avanzados Universitat Rovira i Virgili. Pl. Imperial
INCERTIDUMBRE Y PRECISIÓN Alicia Maroto, Ricard Boqué, Jordi Riu, F. Xavier Rius Departamento de Química Analítica y Química Orgánica Instituto de Estudios Avanzados Universitat Rovira i Virgili. Pl. Imperial
Validación y verificación de métodos de examen cuantitativos
 Temas selectos de Calidad en Serología (aplicación en el banco de sangre) Validación y verificación de métodos de examen cuantitativos Ignacio Reyes Ramírez entidad mexicana de acreditación, a.c. Introducción
Temas selectos de Calidad en Serología (aplicación en el banco de sangre) Validación y verificación de métodos de examen cuantitativos Ignacio Reyes Ramírez entidad mexicana de acreditación, a.c. Introducción
LA MEDIDA Y SUS ERRORES
 LA MEDIDA Y SUS ERRORES Magnitud, unidad y medida. Magnitud es todo aquello que se puede medir y que se puede representar por un número. Para obtener el número que representa a la magnitud debemos escoger
LA MEDIDA Y SUS ERRORES Magnitud, unidad y medida. Magnitud es todo aquello que se puede medir y que se puede representar por un número. Para obtener el número que representa a la magnitud debemos escoger
Técnicas de valor presente para calcular el valor en uso
 Normas Internacionales de Información Financiera NIC - NIIF Guía NIC - NIIF NIC 36 Fundación NIC-NIIF Técnicas de valor presente para calcular el valor en uso Este documento proporciona una guía para utilizar
Normas Internacionales de Información Financiera NIC - NIIF Guía NIC - NIIF NIC 36 Fundación NIC-NIIF Técnicas de valor presente para calcular el valor en uso Este documento proporciona una guía para utilizar
Evaluación de la capacidad óptima de medida y alcance de la acreditación de un laboratorio de calibración
 Evaluación de la capacidad óptima de medida y alcance de la acreditación de un laboratorio de calibración Fernández Pareja, Mª Teresa te_fer@topografia.upm.es Departamento de Ingeniería Topográfica y Cartografía
Evaluación de la capacidad óptima de medida y alcance de la acreditación de un laboratorio de calibración Fernández Pareja, Mª Teresa te_fer@topografia.upm.es Departamento de Ingeniería Topográfica y Cartografía
Curso Comparabilidad de resultados
 Curso Comparabilidad de resultados Director: Gabriel A. Migliarino. Docente: Evangelina Hernández. Agenda Introducción. n. Protocolos iniciales de comparación de métodos. m * EP9-A2. CLSI. * Comparación
Curso Comparabilidad de resultados Director: Gabriel A. Migliarino. Docente: Evangelina Hernández. Agenda Introducción. n. Protocolos iniciales de comparación de métodos. m * EP9-A2. CLSI. * Comparación
Trabajo lean (1): A que podemos llamar trabajo lean?
 Trabajo lean (1): A que podemos llamar trabajo lean? Jordi Olivella Nadal Director de Comunicación del Instituto Lean Management Este escrito inicia una serie de artículos sobre la organización en trabajo
Trabajo lean (1): A que podemos llamar trabajo lean? Jordi Olivella Nadal Director de Comunicación del Instituto Lean Management Este escrito inicia una serie de artículos sobre la organización en trabajo
COMO IMPLEMENTAR UN PROGRAMA DE ASEGURAMIENTO DE CALIDAD ANALÍTICO Dirección Redes en Salud Pública Subdirección Gestión de Calidad de LSP 2015-09-24
 COMO IMPLEMENTAR UN PROGRAMA DE ASEGURAMIENTO DE CALIDAD ANALÍTICO Dirección Redes en Salud Pública Subdirección Gestión de Calidad de LSP 2015-09-24 NTC-ISO/IEC17025:2005 ASEGURAMIENTO DE LA CALIDAD El
COMO IMPLEMENTAR UN PROGRAMA DE ASEGURAMIENTO DE CALIDAD ANALÍTICO Dirección Redes en Salud Pública Subdirección Gestión de Calidad de LSP 2015-09-24 NTC-ISO/IEC17025:2005 ASEGURAMIENTO DE LA CALIDAD El
Fecha Cargo Nombre Firma
 Código: OUADOC014 Revisión Nro. 10 Página 1 de 8 1. OBJETIVO Establecer los requisitos de carácter interpretativo de la UNIT- (equivalente a la ISO/IEC 17025) que los laboratorios de ensayo y calibración
Código: OUADOC014 Revisión Nro. 10 Página 1 de 8 1. OBJETIVO Establecer los requisitos de carácter interpretativo de la UNIT- (equivalente a la ISO/IEC 17025) que los laboratorios de ensayo y calibración
International Laboratory Accreditation Cooperation
 International Laboratory Accreditation Cooperation Servicios de ensayos, medida o calibración fiables La diferencia entre acreditación y certificación Qué buscar en un servicio de ensayo, medida o calibración?
International Laboratory Accreditation Cooperation Servicios de ensayos, medida o calibración fiables La diferencia entre acreditación y certificación Qué buscar en un servicio de ensayo, medida o calibración?
COMPARACION DE DOS METODOLOGIAS PARA LA DETERMINACION DE NITROGENO TOTAL EN ABONOS O FERTILIZANTES
 COMPARACION DE DOS METODOLOGIAS PARA LA DETERMINACION DE NITROGENO TOTAL EN ABONOS O FERTILIZANTES El método comunitario 2.6.1. para la determinación del nitrógeno total en los abonos, descrito en el anexo
COMPARACION DE DOS METODOLOGIAS PARA LA DETERMINACION DE NITROGENO TOTAL EN ABONOS O FERTILIZANTES El método comunitario 2.6.1. para la determinación del nitrógeno total en los abonos, descrito en el anexo
Control de Calidad en Laboratorios
 Metodos de control de calidad en laboratorios Funcionar bien en las pruebas de suficiencia (homologación). Funcionar bien en los ensayos de colaboración Un aspecto importante del sistema de gestión de
Metodos de control de calidad en laboratorios Funcionar bien en las pruebas de suficiencia (homologación). Funcionar bien en los ensayos de colaboración Un aspecto importante del sistema de gestión de
Validation. Validación Psicométrica. Validation. Central Test. Central Test. Centraltest CENTRAL. L art de l évaluation. El arte de la evaluación
 Validation Validación Psicométrica L art de l évaluation Validation Central Test Central Test Centraltest L art de l évaluation CENTRAL test.com El arte de la evaluación www.centraltest.com Propiedades
Validation Validación Psicométrica L art de l évaluation Validation Central Test Central Test Centraltest L art de l évaluation CENTRAL test.com El arte de la evaluación www.centraltest.com Propiedades
NOT CONTROLLED WHEN PRINTED. Protocolo para los Programas de Ensayos de Aptitud
 The Food and Environment Research Agency Agencia de Investigación en Alimentos y Medio Ambiente. Protocolo para los Programas de Ensayos de Aptitud Versión 3, Mayo 2014 Parte 2 FAPAS Crown Copyright 2014
The Food and Environment Research Agency Agencia de Investigación en Alimentos y Medio Ambiente. Protocolo para los Programas de Ensayos de Aptitud Versión 3, Mayo 2014 Parte 2 FAPAS Crown Copyright 2014
Gestión de Calidad de laboratorio clínico
 Gestión de Calidad de laboratorio clínico T.M. Luis Valenzuela Andrade Magíster en Aseguramiento de calidad en Laboratorio Clínicos, UNAB 2007 Product Manager Sistemas de Gestión de calidad Tecnigen Sistemas
Gestión de Calidad de laboratorio clínico T.M. Luis Valenzuela Andrade Magíster en Aseguramiento de calidad en Laboratorio Clínicos, UNAB 2007 Product Manager Sistemas de Gestión de calidad Tecnigen Sistemas
Covarianza y coeficiente de correlación
 Covarianza y coeficiente de correlación Cuando analizábamos las variables unidimensionales considerábamos, entre otras medidas importantes, la media y la varianza. Ahora hemos visto que estas medidas también
Covarianza y coeficiente de correlación Cuando analizábamos las variables unidimensionales considerábamos, entre otras medidas importantes, la media y la varianza. Ahora hemos visto que estas medidas también
NORMA INTERNACIONAL DE AUDITORÍA 520 PROCEDIMIENTOS ANALÍTICOS
 NORMA INTERNACIONAL DE AUDITORÍA 520 PROCEDIMIENTOS ANALÍTICOS (NIA-ES 520) (adaptada para su aplicación en España mediante Resolución del Instituto de Contabilidad y Auditoría de Cuentas, de 15 de octubre
NORMA INTERNACIONAL DE AUDITORÍA 520 PROCEDIMIENTOS ANALÍTICOS (NIA-ES 520) (adaptada para su aplicación en España mediante Resolución del Instituto de Contabilidad y Auditoría de Cuentas, de 15 de octubre
Calibración y control de calidad de instrumentos de análisis
 Calibración y control de calidad de instrumentos de análisis cĺınico. María Cecilia San Román Rincón Monografía vinculada a la conferencia del Dr. Horacio Venturino sobre Instrumental para laboratorio
Calibración y control de calidad de instrumentos de análisis cĺınico. María Cecilia San Román Rincón Monografía vinculada a la conferencia del Dr. Horacio Venturino sobre Instrumental para laboratorio
Análisis y cuantificación del Riesgo
 Análisis y cuantificación del Riesgo 1 Qué es el análisis del Riesgo? 2. Métodos M de Análisis de riesgos 3. Método M de Montecarlo 4. Modelo de Análisis de Riesgos 5. Qué pasos de deben seguir para el
Análisis y cuantificación del Riesgo 1 Qué es el análisis del Riesgo? 2. Métodos M de Análisis de riesgos 3. Método M de Montecarlo 4. Modelo de Análisis de Riesgos 5. Qué pasos de deben seguir para el
Metodología de la Investigación. Dr. Cristian Rusu cristian.rusu@ucv.cl
 Metodología de la Investigación Dr. Cristian Rusu cristian.rusu@ucv.cl 6. Diseños de investigación 6.1. Diseños experimentales 6.1.1. Diseños preexperimentales 6.1.2. Diseños experimentales verdaderos
Metodología de la Investigación Dr. Cristian Rusu cristian.rusu@ucv.cl 6. Diseños de investigación 6.1. Diseños experimentales 6.1.1. Diseños preexperimentales 6.1.2. Diseños experimentales verdaderos
8.1. Introducción... 1. 8.2. Dependencia/independencia estadística... 2. 8.3. Representación gráfica: diagrama de dispersión... 3. 8.4. Regresión...
 Tema 8 Análisis de dos variables: dependencia estadística y regresión Contenido 8.1. Introducción............................. 1 8.2. Dependencia/independencia estadística.............. 2 8.3. Representación
Tema 8 Análisis de dos variables: dependencia estadística y regresión Contenido 8.1. Introducción............................. 1 8.2. Dependencia/independencia estadística.............. 2 8.3. Representación
DD4B. ANEXO B CRITERIOS PARA LA ACREDITACIÓN DE LABORATORIOS QUE REALIZAN ENSAYOS FÍSICO-QUÍMICOS 2012 rev02
 Introducción DD4B QUE REALIZAN ENSAYOS FÍSICO-QUÍMICOS El presente anexo es una guía auxiliar, para los laboratorios y los evaluadores, de requisitos específicos que deben garantizarse al realizar ensayos
Introducción DD4B QUE REALIZAN ENSAYOS FÍSICO-QUÍMICOS El presente anexo es una guía auxiliar, para los laboratorios y los evaluadores, de requisitos específicos que deben garantizarse al realizar ensayos
IAP 1009 - TÉCNICAS DE AUDITORÍA APOYADAS EN ORDENADOR (TAAO)
 IAP 1009 - TÉCNICAS DE AUDITORÍA APOYADAS EN ORDENADOR (TAAO) Introducción 1. Como se indica en la Norma Internacional de Auditoría 401, "Auditoría en un contexto informatizado", los objetivos globales
IAP 1009 - TÉCNICAS DE AUDITORÍA APOYADAS EN ORDENADOR (TAAO) Introducción 1. Como se indica en la Norma Internacional de Auditoría 401, "Auditoría en un contexto informatizado", los objetivos globales
Equipos de medición. Intervalos de calibración e interpretación de Certificados de Calibración
 Equipos de medición. Intervalos de calibración e interpretación de Certificados de Calibración Equipos de Medición. Intervalos de calibración e interpretación de Certificados de Calibración Disertante:
Equipos de medición. Intervalos de calibración e interpretación de Certificados de Calibración Equipos de Medición. Intervalos de calibración e interpretación de Certificados de Calibración Disertante:
Validación de un Método Instrumental
 Validación Validación de un Método Instrumental Un Proceso de Validación Consiste de al menos las siguientes etapas: Validación del Software Validación del Hardware ( Instrumento) Validación del Método
Validación Validación de un Método Instrumental Un Proceso de Validación Consiste de al menos las siguientes etapas: Validación del Software Validación del Hardware ( Instrumento) Validación del Método
Traducción del. Our ref:
 Traducción del Documento: Our ref: Secretaría del ISO/TC 176/SC 2 Fecha: 15 de octubre de 2008 A los Miembros del ISO/TC 176/SC 2 - Gestión de la Calidad y Aseguramiento de la Calidad/ Sistemas de la Calidad
Traducción del Documento: Our ref: Secretaría del ISO/TC 176/SC 2 Fecha: 15 de octubre de 2008 A los Miembros del ISO/TC 176/SC 2 - Gestión de la Calidad y Aseguramiento de la Calidad/ Sistemas de la Calidad
-OPS/CEPIS/01.61(AIRE) Original: español Página 11 5. Estructura del programa de evaluación con personal externo
 Página 11 5. Estructura del programa de evaluación con personal externo 5.1 Introducción Esta sección presenta la estructura del programa de evaluación con personal externo. Describe las funciones y responsabilidades
Página 11 5. Estructura del programa de evaluación con personal externo 5.1 Introducción Esta sección presenta la estructura del programa de evaluación con personal externo. Describe las funciones y responsabilidades
La Directiva 98/79/CE sobre productos sanitarios para diagnóstico in vitro
 La Directiva 98/79/CE sobre productos sanitarios para diagnóstico in vitro F. Javier Gella Tomás División Reactivos BioSystems S.A. Barcelona Introducción Las directivas europeas son documentos legislativos,
La Directiva 98/79/CE sobre productos sanitarios para diagnóstico in vitro F. Javier Gella Tomás División Reactivos BioSystems S.A. Barcelona Introducción Las directivas europeas son documentos legislativos,
Capítulo 5: METODOLOGÍA APLICABLE A LAS NORMAS NE AI
 Capítulo 5: METODOLOGÍA APLICABLE A LAS NORMAS NE AI La segunda fase del NIPE corresponde con la adecuación de las intervenciones de enfermería del sistema de clasificación N.I.C. (Nursing Intervention
Capítulo 5: METODOLOGÍA APLICABLE A LAS NORMAS NE AI La segunda fase del NIPE corresponde con la adecuación de las intervenciones de enfermería del sistema de clasificación N.I.C. (Nursing Intervention
Norma Internacional de Contabilidad nº 10 (NIC 10) Hechos posteriores a la fecha del balance
 Norma Internacional de Contabilidad nº 10 (NIC 10) Hechos posteriores a la fecha del balance Esta Norma revisada sustituye a la NIC 10 (revisada en 1999) Hechos posteriores a la fecha del balance, y se
Norma Internacional de Contabilidad nº 10 (NIC 10) Hechos posteriores a la fecha del balance Esta Norma revisada sustituye a la NIC 10 (revisada en 1999) Hechos posteriores a la fecha del balance, y se
QUÉ ES LA ISO 14000? DIFERENCIAS ENTRE ISO 14001 Y EMAS. 1 Para Mayor información www.medicaindustrial.com.mx
 QUÉ ES LA ISO 14000? La ISO 14000 es una serie de normas internacionales para la gestión medioambiental. Es la primera serie de normas que permite a las organizaciones de todo el mundo realizar esfuerzos
QUÉ ES LA ISO 14000? La ISO 14000 es una serie de normas internacionales para la gestión medioambiental. Es la primera serie de normas que permite a las organizaciones de todo el mundo realizar esfuerzos
IAP 1005 - CONSIDERACIONES PARTICULARES SOBRE LA AUDITORÍA DE LAS EMPRESAS DE REDUCIDA DIMENSIÓN
 IAP 1005 - CONSIDERACIONES PARTICULARES SOBRE LA AUDITORÍA DE LAS EMPRESAS DE REDUCIDA DIMENSIÓN Introducción 1. Las Normas Internacionales de Auditoría (NIA) se aplican a la auditoría de la información
IAP 1005 - CONSIDERACIONES PARTICULARES SOBRE LA AUDITORÍA DE LAS EMPRESAS DE REDUCIDA DIMENSIÓN Introducción 1. Las Normas Internacionales de Auditoría (NIA) se aplican a la auditoría de la información
Sistemas de Gestión de Calidad. Control documental
 4 Sistemas de Gestión de Calidad. Control documental ÍNDICE: 4.1 Requisitos Generales 4.2 Requisitos de la documentación 4.2.1 Generalidades 4.2.2 Manual de la Calidad 4.2.3 Control de los documentos 4.2.4
4 Sistemas de Gestión de Calidad. Control documental ÍNDICE: 4.1 Requisitos Generales 4.2 Requisitos de la documentación 4.2.1 Generalidades 4.2.2 Manual de la Calidad 4.2.3 Control de los documentos 4.2.4
Curso TURGALICIA SISTEMA DE GESTIÓN DE SEGURIDAD Y SALUD EN EL TRABAJO OHSAS 18001:2.007
 Curso TURGALICIA SISTEMA DE GESTIÓN DE SEGURIDAD Y SALUD EN EL TRABAJO OHSAS 18001:2.007 C/Fernando Macías 13; 1º izda. 15004 A CORUÑA Tel 981 160 247. Fax 981 108 992 www.pfsgrupo.com DEFINICIONES: RIESGOS
Curso TURGALICIA SISTEMA DE GESTIÓN DE SEGURIDAD Y SALUD EN EL TRABAJO OHSAS 18001:2.007 C/Fernando Macías 13; 1º izda. 15004 A CORUÑA Tel 981 160 247. Fax 981 108 992 www.pfsgrupo.com DEFINICIONES: RIESGOS
ORGANIZACIÓN MUNDIAL DE LA PROPIEDAD INTELECTUAL GINEBRA
 OMPI IIM/2/3 ORIGINAL: Inglés FECHA: 14 de junio de 2005 ORGANIZACIÓN MUNDIAL DE LA PROPIEDAD INTELECTUAL GINEBRA S SEGUNDA REUNIÓN INTERGUBERNAMENTAL ENTRE PERÍODOS DE SESIONES SOBRE UN PROGRAMA DE LA
OMPI IIM/2/3 ORIGINAL: Inglés FECHA: 14 de junio de 2005 ORGANIZACIÓN MUNDIAL DE LA PROPIEDAD INTELECTUAL GINEBRA S SEGUNDA REUNIÓN INTERGUBERNAMENTAL ENTRE PERÍODOS DE SESIONES SOBRE UN PROGRAMA DE LA
ORGANIZACIÓN MUNDIAL DE LA PROPIEDAD INTELECTUAL GINEBRA
 S OMPI SCT/S2/4 ORIGINAL: Inglés FECHA: 29 de marzo de 2002 ORGANIZACIÓN MUNDIAL DE LA PROPIEDAD INTELECTUAL GINEBRA COMITÉ PERMANENTE SOBRE EL DERECHO DE MARCAS, DIBUJOS Y MODELOS INDUSTRIALES E INDICACIONES
S OMPI SCT/S2/4 ORIGINAL: Inglés FECHA: 29 de marzo de 2002 ORGANIZACIÓN MUNDIAL DE LA PROPIEDAD INTELECTUAL GINEBRA COMITÉ PERMANENTE SOBRE EL DERECHO DE MARCAS, DIBUJOS Y MODELOS INDUSTRIALES E INDICACIONES
global trust Razones por las cuales debería emplearse un Laboratorio Acreditado? International Laboratory Accreditation Cooperation
 International Laboratory Accreditation Cooperation Razones por las cuales debería emplearse un Laboratorio Acreditado? Qué deberia considerar al seleccionar un laboratorio? Al seleccionar un laboratorio
International Laboratory Accreditation Cooperation Razones por las cuales debería emplearse un Laboratorio Acreditado? Qué deberia considerar al seleccionar un laboratorio? Al seleccionar un laboratorio
0. Introducción. 0.1. Antecedentes
 ISO 14001:2015 0. Introducción 0.1. Antecedentes Conseguir el equilibrio entre el medio ambiente, la sociedad y la economía está considerado como algo esencial para satisfacer las necesidades del presente
ISO 14001:2015 0. Introducción 0.1. Antecedentes Conseguir el equilibrio entre el medio ambiente, la sociedad y la economía está considerado como algo esencial para satisfacer las necesidades del presente
Sistema de gestión de laboratorios IIQ- FI- UdelaR 2009
 Sistema de gestión de laboratorios IIQ- FI- UdelaR 2009 SGL- 2009 Introducción 1 Introducción SGL- 2009 Introducción 2 Objetivos del Curso a) Capacitar para la implementación de un sistema de gestión en
Sistema de gestión de laboratorios IIQ- FI- UdelaR 2009 SGL- 2009 Introducción 1 Introducción SGL- 2009 Introducción 2 Objetivos del Curso a) Capacitar para la implementación de un sistema de gestión en
Protección de los trabajadores contra los riesgos de la exposición a campos electromagnéticos 2
 CONTENIDO: 1 Protección de los trabajadores contra los riesgos de la exposición a campos electromagnéticos 2 1 Se prohíbe la reproducción total o parcial del contenido de este "Boletín Europa al Día" sin
CONTENIDO: 1 Protección de los trabajadores contra los riesgos de la exposición a campos electromagnéticos 2 1 Se prohíbe la reproducción total o parcial del contenido de este "Boletín Europa al Día" sin
Mantenimiento de Sistemas de Información
 de Sistemas de Información ÍNDICE DESCRIPCIÓN Y OBJETIVOS... 1 ACTIVIDAD MSI 1: REGISTRO DE LA PETICIÓN...4 Tarea MSI 1.1: Registro de la Petición... 4 Tarea MSI 1.2: Asignación de la Petición... 5 ACTIVIDAD
de Sistemas de Información ÍNDICE DESCRIPCIÓN Y OBJETIVOS... 1 ACTIVIDAD MSI 1: REGISTRO DE LA PETICIÓN...4 Tarea MSI 1.1: Registro de la Petición... 4 Tarea MSI 1.2: Asignación de la Petición... 5 ACTIVIDAD
Orientación acerca de los requisitos de documentación de la Norma ISO 9001:2000
 Orientación acerca de los requisitos de documentación de la Norma ISO 9001:2000 Documento: ISO/TC 176/SC 2/N 525R Marzo 2001 ISO Traducción aprobada el 2001-05-31 Prólogo de la versión en español Este
Orientación acerca de los requisitos de documentación de la Norma ISO 9001:2000 Documento: ISO/TC 176/SC 2/N 525R Marzo 2001 ISO Traducción aprobada el 2001-05-31 Prólogo de la versión en español Este
Capítulo 8. Tipos de interés reales. 8.1. Introducción
 Capítulo 8 Tipos de interés reales 8.1. Introducción A lo largo de los capítulos 5 y 7 se ha analizado el tipo de interés en términos nominales para distintos vencimientos, aunque se ha desarrollado más
Capítulo 8 Tipos de interés reales 8.1. Introducción A lo largo de los capítulos 5 y 7 se ha analizado el tipo de interés en términos nominales para distintos vencimientos, aunque se ha desarrollado más
ISO 9001 Auditing Practices Group Directriz en:
 International Organization for Standardization International Accreditation Forum ISO 9001 Auditing Practices Group Directriz en: Auditando los procesos de retroalimentación del cliente 1) Introducción
International Organization for Standardization International Accreditation Forum ISO 9001 Auditing Practices Group Directriz en: Auditando los procesos de retroalimentación del cliente 1) Introducción
Términos definiciones
 Términos y definiciones 3Claves para la ISO 9001-2015 Términos y definiciones: ISO9001 utiliza una serie de definiciones ligadas a la gestión de la calidad, que también deben ser comprendidas por la organización
Términos y definiciones 3Claves para la ISO 9001-2015 Términos y definiciones: ISO9001 utiliza una serie de definiciones ligadas a la gestión de la calidad, que también deben ser comprendidas por la organización
Media vs mediana vs moda Cual medida de tendencia central es mas adecuada? MEDIA conveniencias:
 Iniciar con las interpretaciones de las medidas MEDIA VS MEDIANA VS MODA CUAL ES LA MEDIDA ADECUADA TAREA MEDIA PONDERADA Actividad de Medidas de Localización Problema 1. El problema de las tasas de delito.
Iniciar con las interpretaciones de las medidas MEDIA VS MEDIANA VS MODA CUAL ES LA MEDIDA ADECUADA TAREA MEDIA PONDERADA Actividad de Medidas de Localización Problema 1. El problema de las tasas de delito.
DICTAMEN Nº 8. Página 1 de 5. # Nº. 8/1999, de 26 de enero.*
 Página 1 de 5 DICTAMEN Nº 8 # Nº. 8/1999, de 26 de enero.* Expediente relativo al proyecto de Decreto por el que se modifica el Reglamento de organización y funcionamiento del Consejo Asesor de Radio Televisión
Página 1 de 5 DICTAMEN Nº 8 # Nº. 8/1999, de 26 de enero.* Expediente relativo al proyecto de Decreto por el que se modifica el Reglamento de organización y funcionamiento del Consejo Asesor de Radio Televisión
Existen dos clases de observación: Observar científicamente Observación no científica
 La Observación Es una técnica que consiste en observar atentamente el fenómeno, hecho o caso, tomar información y registrarla para su posterior análisis. La observación es un elemento fundamental de todo
La Observación Es una técnica que consiste en observar atentamente el fenómeno, hecho o caso, tomar información y registrarla para su posterior análisis. La observación es un elemento fundamental de todo
Control interno de los métodos de análisis
 Aseguramiento de la Calidad Control interno de los métodos de análisis Universidad Nacional Sede Medellín Facultad de Ciencias Escuela de Geociencias Orlando Ruiz Villadiego, Químico MSc. Coordinador Laboratorio
Aseguramiento de la Calidad Control interno de los métodos de análisis Universidad Nacional Sede Medellín Facultad de Ciencias Escuela de Geociencias Orlando Ruiz Villadiego, Químico MSc. Coordinador Laboratorio
TIPOS DE MUESTREO. Jordi Casal 1, Enric Mateu RESUMEN
 TIPOS DE MUESTREO Jordi Casal 1, Enric Mateu CReSA. Centre de Recerca en Sanitat Animal / Dep. Sanitat i Anatomia Animals, Universitat Autònoma de Barcelona, 08193-Bellaterra, Barcelona RESUMEN Se discute
TIPOS DE MUESTREO Jordi Casal 1, Enric Mateu CReSA. Centre de Recerca en Sanitat Animal / Dep. Sanitat i Anatomia Animals, Universitat Autònoma de Barcelona, 08193-Bellaterra, Barcelona RESUMEN Se discute
EL ANÁLISIS DE LA VARIANZA (ANOVA) 1. Comparación de múltiples poblaciones
 EL ANÁLISIS DE LA VARIANZA (ANOVA) 1. Comparación de múltiples poblaciones Ricard Boqué, Alicia Maroto Grupo de Quimiometría y Cualimetría. Universitat Rovira i Virgili. Pl. Imperial Tàrraco, 1. 43005Tarragona
EL ANÁLISIS DE LA VARIANZA (ANOVA) 1. Comparación de múltiples poblaciones Ricard Boqué, Alicia Maroto Grupo de Quimiometría y Cualimetría. Universitat Rovira i Virgili. Pl. Imperial Tàrraco, 1. 43005Tarragona
PROCEDIMIENTO DE AUDITORÍAS INTERNAS DEL SISTEMA DE GESTIÓN DE CALIDAD
 Página : 1 de 12 PROCEDIMIENTO DE DEL SISTEMA DE GESTIÓN DE CALIDAD Esta es una copia no controlada si carece de sello en el reverso de sus hojas, en cuyo caso se advierte al lector que su contenido puede
Página : 1 de 12 PROCEDIMIENTO DE DEL SISTEMA DE GESTIÓN DE CALIDAD Esta es una copia no controlada si carece de sello en el reverso de sus hojas, en cuyo caso se advierte al lector que su contenido puede
DETERMINACIÓN DEL VOLUMEN DE PEDIDO.
 Lote económico de compra o Lote Optimo DETERMINACIÓN DEL VOLUMEN DE PEDIDO. Concepto que vemos en casi todos libros de aprovisionamiento, habitualmente la decisión de la cantidad a reaprovisionar en las
Lote económico de compra o Lote Optimo DETERMINACIÓN DEL VOLUMEN DE PEDIDO. Concepto que vemos en casi todos libros de aprovisionamiento, habitualmente la decisión de la cantidad a reaprovisionar en las
DIRECTRICES SOBRE LA INCERTIDUMBRE EN LA MEDICIÓN CAC/GL 54-2004
 CAC/GL 54-2004 Página 1 de 8 DIRECTRICES SOBRE LA INCERTIDUMBRE EN LA MEDICIÓN CAC/GL 54-2004 Introducción Es importante y es un requisito de la norma ISO/IEC 17025: 1999 que los analistas estén al corriente
CAC/GL 54-2004 Página 1 de 8 DIRECTRICES SOBRE LA INCERTIDUMBRE EN LA MEDICIÓN CAC/GL 54-2004 Introducción Es importante y es un requisito de la norma ISO/IEC 17025: 1999 que los analistas estén al corriente
Norma ISO 14001: 2004
 Norma ISO 14001: 2004 Sistema de Gestión Ambiental El presente documento es la versión impresa de la página www.grupoacms.com Si desea más información sobre la Norma ISO 14001 u otras normas relacionadas
Norma ISO 14001: 2004 Sistema de Gestión Ambiental El presente documento es la versión impresa de la página www.grupoacms.com Si desea más información sobre la Norma ISO 14001 u otras normas relacionadas
CMMI (Capability Maturity Model Integrated)
 CMMI (Capability Maturity Model Integrated) El SEI (software engineering institute) a mediados de los 80 desarrolló el CMM (modelo de madurez de la capacidad de software). CMMI: CMM integrado, una mezcla
CMMI (Capability Maturity Model Integrated) El SEI (software engineering institute) a mediados de los 80 desarrolló el CMM (modelo de madurez de la capacidad de software). CMMI: CMM integrado, una mezcla
Decisión: Indican puntos en que se toman decisiones: sí o no, o se verifica una actividad del flujo grama.
 Diagrama de Flujo La presentación gráfica de un sistema es una forma ampliamente utilizada como herramienta de análisis, ya que permite identificar aspectos relevantes de una manera rápida y simple. El
Diagrama de Flujo La presentación gráfica de un sistema es una forma ampliamente utilizada como herramienta de análisis, ya que permite identificar aspectos relevantes de una manera rápida y simple. El
L 320/8 Diario Oficial de la Unión Europea 17.11.2012
 L 320/8 Diario Oficial de la Unión Europea 17.11.2012 REGLAMENTO (UE) N o 1078/2012 DE LA COMISIÓN de 16 de noviembre de 2012 sobre un método común de seguridad en materia de vigilancia que deberán aplicar
L 320/8 Diario Oficial de la Unión Europea 17.11.2012 REGLAMENTO (UE) N o 1078/2012 DE LA COMISIÓN de 16 de noviembre de 2012 sobre un método común de seguridad en materia de vigilancia que deberán aplicar
CALIBRACIÓN DE EQUIPOS DE MEDIDA
 CALIBRACIÓN DE EQUIPOS DE MEDIDA Jordi Riu, Ricard Boqué, Alicia Maroto, F. Xavier Rius Departamento de Química Analítica y Química Orgánica Instituto de Estudios Avanzados Universitat Rovira i Virgili.
CALIBRACIÓN DE EQUIPOS DE MEDIDA Jordi Riu, Ricard Boqué, Alicia Maroto, F. Xavier Rius Departamento de Química Analítica y Química Orgánica Instituto de Estudios Avanzados Universitat Rovira i Virgili.
Enginyeria del Software III
 Enginyeria del Software III Sessió 3. L estàndard ISO/IEC 15504 Antònia Mas Pichaco 1 Introducción El proyecto SPICE representa el mayor marco de colaboración internacional establecido con la finalidad
Enginyeria del Software III Sessió 3. L estàndard ISO/IEC 15504 Antònia Mas Pichaco 1 Introducción El proyecto SPICE representa el mayor marco de colaboración internacional establecido con la finalidad
Capítulo 10. Estudio de un caso con parámetros reales: acuífero de Borden
 Capítulo 10. Estudio de un caso con parámetros reales: acuífero de Borden Tras la realización de muchos casos sintéticos y un estudio detallado de todos los parámetros que intervienen en el problema y
Capítulo 10. Estudio de un caso con parámetros reales: acuífero de Borden Tras la realización de muchos casos sintéticos y un estudio detallado de todos los parámetros que intervienen en el problema y
MATEMÁTICAS ESO EVALUACIÓN: CRITERIOS E INSTRUMENTOS CURSO 2014-2015 Colegio B. V. María (Irlandesas) Castilleja de la Cuesta (Sevilla) Página 1 de 7
 Página 1 de 7 1 CRITERIOS DE EVALUACIÓN 1.1 SECUENCIA POR CURSOS DE LOS CRITERIOS DE EVALUACION PRIMER CURSO 1. Utilizar números naturales y enteros y fracciones y decimales sencillos, sus operaciones
Página 1 de 7 1 CRITERIOS DE EVALUACIÓN 1.1 SECUENCIA POR CURSOS DE LOS CRITERIOS DE EVALUACION PRIMER CURSO 1. Utilizar números naturales y enteros y fracciones y decimales sencillos, sus operaciones
ORGANISMO DE ACREDITACIÓN ECUATORIANO - OAE CRITERIOS GENERALES ACREDITACION DE LABORATORIOS DE ENSAYO Y CALIBRACIÓN
 ORGANISMO DE ACREDITACIÓN ECUATORIANO OAE CRITERIOS GENERALES ACREDITACION DE LABORATORIOS DE ENSAYO Y CALIBRACIÓN NORMA NTE INENISO/IEC 17025: 2005 OAE CR GA01 R00 F PG01 01 R00 Página 1 de 11 ORGANISMO
ORGANISMO DE ACREDITACIÓN ECUATORIANO OAE CRITERIOS GENERALES ACREDITACION DE LABORATORIOS DE ENSAYO Y CALIBRACIÓN NORMA NTE INENISO/IEC 17025: 2005 OAE CR GA01 R00 F PG01 01 R00 Página 1 de 11 ORGANISMO
1. INTRODUCCIÓN 1.1 INGENIERÍA
 1. INTRODUCCIÓN 1.1 INGENIERÍA Es difícil dar una explicación de ingeniería en pocas palabras, pues se puede decir que la ingeniería comenzó con el hombre mismo, pero se puede intentar dar un bosquejo
1. INTRODUCCIÓN 1.1 INGENIERÍA Es difícil dar una explicación de ingeniería en pocas palabras, pues se puede decir que la ingeniería comenzó con el hombre mismo, pero se puede intentar dar un bosquejo
Ingeniería del Software I Clase de Testing Funcional 2do. Cuatrimestre de 2007
 Enunciado Se desea efectuar el testing funcional de un programa que ejecuta transferencias entre cuentas bancarias. El programa recibe como parámetros la cuenta de origen, la de cuenta de destino y el
Enunciado Se desea efectuar el testing funcional de un programa que ejecuta transferencias entre cuentas bancarias. El programa recibe como parámetros la cuenta de origen, la de cuenta de destino y el
Inter American Accreditation Cooperation ACREDITACIÓN DE LABORATORIOS O CERTIFICACIÓN ISO 9001?
 Este documento es una traducción al español preparada y endosada por IAAC del folleto de ILAC Laboratory Accreditation or ISO 9001 Certification? CLASIFICACIÓN Este documento está clasificado como un Documento
Este documento es una traducción al español preparada y endosada por IAAC del folleto de ILAC Laboratory Accreditation or ISO 9001 Certification? CLASIFICACIÓN Este documento está clasificado como un Documento
4.4.1 Servicio de Prevención Propio.
 1 Si se trata de una empresa entre 250 y 500 trabajadores que desarrolla actividades incluidas en el Anexo I del Reglamento de los Servicios de Prevención, o de una empresa de más de 500 trabajadores con
1 Si se trata de una empresa entre 250 y 500 trabajadores que desarrolla actividades incluidas en el Anexo I del Reglamento de los Servicios de Prevención, o de una empresa de más de 500 trabajadores con
Actualización de la Norma ISO 9001:2008
 Actualización de la Norma ISO 9001:2008 Porqué se actualiza la norma? Existe un ciclo para revisar las normas ISO para mantener las normas actualizadas. Se debe mantener la actualización con desarrollos
Actualización de la Norma ISO 9001:2008 Porqué se actualiza la norma? Existe un ciclo para revisar las normas ISO para mantener las normas actualizadas. Se debe mantener la actualización con desarrollos
Validación de los métodos microbiológicos PROTOCOLO DE VALIDACIÓN
 Validación de los métodos microbiológicos PROTOCOLO DE VALIDACIÓN Norma ISO 17025 Bqca. QM Alicia I. Cuesta, Consultora Internacional de la FAO Objetivos a desarrollar Validación de métodos: Intentamos
Validación de los métodos microbiológicos PROTOCOLO DE VALIDACIÓN Norma ISO 17025 Bqca. QM Alicia I. Cuesta, Consultora Internacional de la FAO Objetivos a desarrollar Validación de métodos: Intentamos
Test de Idioma Francés. Manual del evaluador
 Test de Idioma Francés Manual del evaluador 1 CONTENIDO Introducción Qué mide el Test de idioma francés? Qué obtienen el examinado y el examinador? Descripción de los factores Propiedades psicométricas
Test de Idioma Francés Manual del evaluador 1 CONTENIDO Introducción Qué mide el Test de idioma francés? Qué obtienen el examinado y el examinador? Descripción de los factores Propiedades psicométricas
SISTEMAS Y MANUALES DE LA CALIDAD
 SISTEMAS Y MANUALES DE LA CALIDAD NORMATIVAS SOBRE SISTEMAS DE CALIDAD Introducción La experiencia de algunos sectores industriales que por las características particulares de sus productos tenían necesidad
SISTEMAS Y MANUALES DE LA CALIDAD NORMATIVAS SOBRE SISTEMAS DE CALIDAD Introducción La experiencia de algunos sectores industriales que por las características particulares de sus productos tenían necesidad
TALLER: ISO 14001. Ocean. Alejandro Tonatiuh López Vergara Geog. Miriam Ruiz Velasco
 TALLER: ISO 14001 Ocean. Alejandro Tonatiuh López Vergara Geog. Miriam Ruiz Velasco Es un conjunto de partes o elementos organizados y relacionados que interactúan entre sí para lograr un objetivo. Sistemas
TALLER: ISO 14001 Ocean. Alejandro Tonatiuh López Vergara Geog. Miriam Ruiz Velasco Es un conjunto de partes o elementos organizados y relacionados que interactúan entre sí para lograr un objetivo. Sistemas
Control Estadístico del Proceso. Ing. Claudia Salguero Ing. Alvaro Díaz
 Control Estadístico del Proceso Ing. Claudia Salguero Ing. Alvaro Díaz Control Estadístico del Proceso Es un conjunto de herramientas estadísticas que permiten recopilar, estudiar y analizar la información
Control Estadístico del Proceso Ing. Claudia Salguero Ing. Alvaro Díaz Control Estadístico del Proceso Es un conjunto de herramientas estadísticas que permiten recopilar, estudiar y analizar la información
Preguntas que se hacen con frecuencia sobre los estudios clínicos
 Preguntas que se hacen con frecuencia sobre los estudios clínicos Son seguros? Todos los ensayos clínicos deben ser aprobados por el gobierno federal y deben cumplir con una reglamentación estricta que
Preguntas que se hacen con frecuencia sobre los estudios clínicos Son seguros? Todos los ensayos clínicos deben ser aprobados por el gobierno federal y deben cumplir con una reglamentación estricta que
Operación 8 Claves para la ISO 9001-2015
 Operación 8Claves para la ISO 9001-2015 BLOQUE 8: Operación A grandes rasgos, se puede decir que este bloque se corresponde con el capítulo 7 de la antigua norma ISO 9001:2008 de Realización del Producto,
Operación 8Claves para la ISO 9001-2015 BLOQUE 8: Operación A grandes rasgos, se puede decir que este bloque se corresponde con el capítulo 7 de la antigua norma ISO 9001:2008 de Realización del Producto,
NIC 39 Valor razonable
 NIC 39 Valor razonable Medición inicial y posterior de activos y pasivos financieros Se medirá por su valor razonable más, (si no se contabiliza al valor razonable con cambios en resultados) los costos
NIC 39 Valor razonable Medición inicial y posterior de activos y pasivos financieros Se medirá por su valor razonable más, (si no se contabiliza al valor razonable con cambios en resultados) los costos
Nota de Información al cliente Auditoría Multisede
 Nota de Información al cliente Auditoría Multisede La presente Nota de Información al Cliente explica las principales características de una Auditoría Multisede. Por lo general, las auditorías de certificación
Nota de Información al cliente Auditoría Multisede La presente Nota de Información al Cliente explica las principales características de una Auditoría Multisede. Por lo general, las auditorías de certificación
Tipos de Auditorías y objetivos básicos. Beneficios de las auditorías.
 16 Tipos de Auditorías y objetivos básicos. Beneficios de las auditorías. ÍNDICE: 16.1 Conceptos y definiciones 16.2 Tipos de auditorías 16.3 Certificación 16.4 Objetivos de las auditorías 16.5 Ventajas
16 Tipos de Auditorías y objetivos básicos. Beneficios de las auditorías. ÍNDICE: 16.1 Conceptos y definiciones 16.2 Tipos de auditorías 16.3 Certificación 16.4 Objetivos de las auditorías 16.5 Ventajas
Cómo mejorar la calidad del software a través de una gestión adecuada de la productividad de las pruebas
 Cómo mejorar la calidad del software a través de una gestión adecuada de la productividad de las pruebas Cuando una empresa contrata un proyecto de software a una consultora, realiza una inversión importante.
Cómo mejorar la calidad del software a través de una gestión adecuada de la productividad de las pruebas Cuando una empresa contrata un proyecto de software a una consultora, realiza una inversión importante.
Norma ISO 14001: 2015
 Norma ISO 14001: 2015 Sistema de Gestión Medioambiental El presente documento es la versión impresa de la página www.grupoacms.com Si desea más información sobre la Norma ISO 14001 u otras normas relacionadas
Norma ISO 14001: 2015 Sistema de Gestión Medioambiental El presente documento es la versión impresa de la página www.grupoacms.com Si desea más información sobre la Norma ISO 14001 u otras normas relacionadas
Este documento enumera los diferentes tipos de Diagramas Matriciales y su proceso de construcción. www.fundibeq.org
 DIAGRAMA MATRICIAL 1.- INTRODUCCIÓN Este documento enumera los diferentes tipos de Diagramas Matriciales y su proceso de construcción. Muestra su potencial, como herramienta indispensable para la planificación
DIAGRAMA MATRICIAL 1.- INTRODUCCIÓN Este documento enumera los diferentes tipos de Diagramas Matriciales y su proceso de construcción. Muestra su potencial, como herramienta indispensable para la planificación
Informe final de evaluación del seguimiento de la implantación de títulos oficiales GRADO EN TERAPIA OCUPACIONAL. Facultad de Medicina UCM
 Informe final de evaluación del seguimiento de la implantación de títulos oficiales 2013 GRADO EN TERAPIA OCUPACIONAL UCM INFORMACIÓN PUBLICA Valoración Final Uno de los compromisos esenciales que las
Informe final de evaluación del seguimiento de la implantación de títulos oficiales 2013 GRADO EN TERAPIA OCUPACIONAL UCM INFORMACIÓN PUBLICA Valoración Final Uno de los compromisos esenciales que las
Manual básico de gestión económica de las Asociaciones
 Manual básico de gestión económica de las Asociaciones El control económico de una Asociación se puede ver desde dos perspectivas: Necesidades internas de información económica para: * Toma de decisiones
Manual básico de gestión económica de las Asociaciones El control económico de una Asociación se puede ver desde dos perspectivas: Necesidades internas de información económica para: * Toma de decisiones
MEDICION DEL TRABAJO
 MEDICION DEL TRABAJO Habíamos dicho al comenzar el curso que habían 4 técnicas que permiten realizar una medición del trabajo 1 Técnicas Directas: - Estudio de tiempos con cronómetro - Muestreo del trabajo
MEDICION DEL TRABAJO Habíamos dicho al comenzar el curso que habían 4 técnicas que permiten realizar una medición del trabajo 1 Técnicas Directas: - Estudio de tiempos con cronómetro - Muestreo del trabajo
GUÍA TÉCNICA PARA LA DEFINICIÓN DE COMPROMISOS DE CALIDAD Y SUS INDICADORES
 GUÍA TÉCNICA PARA LA DEFINICIÓN DE COMPROMISOS DE CALIDAD Y SUS INDICADORES Tema: Cartas de Servicios Primera versión: 2008 Datos de contacto: Evaluación y Calidad. Gobierno de Navarra. evaluacionycalidad@navarra.es
GUÍA TÉCNICA PARA LA DEFINICIÓN DE COMPROMISOS DE CALIDAD Y SUS INDICADORES Tema: Cartas de Servicios Primera versión: 2008 Datos de contacto: Evaluación y Calidad. Gobierno de Navarra. evaluacionycalidad@navarra.es
OBJETIVOS GENERALES DE LA EMPRESA
 OBJETIVOS SMART y LOS KPI OBJETIVOS GENERALES DE LA EMPRESA Tras la realización del diagnóstico y el pronóstico del escenario, se decidirán los objetivos de la empresa que deberán alcanzarse en los próximos
OBJETIVOS SMART y LOS KPI OBJETIVOS GENERALES DE LA EMPRESA Tras la realización del diagnóstico y el pronóstico del escenario, se decidirán los objetivos de la empresa que deberán alcanzarse en los próximos
110º período de sesiones. Roma, 9 23 de septiembre de 2005. Financiación del pasivo del seguro médico después del cese en el servicio. I.
 Julio de 2005 S COMITÉ DE FINANZAS 110º período de sesiones Roma, 9 23 de septiembre de 2005 Financiación del pasivo del seguro médico después del cese en el servicio I. Introducción 1. El Comité de Finanzas
Julio de 2005 S COMITÉ DE FINANZAS 110º período de sesiones Roma, 9 23 de septiembre de 2005 Financiación del pasivo del seguro médico después del cese en el servicio I. Introducción 1. El Comité de Finanzas
2.11.1 CONTRATAS Y SUBCONTRATAS NOTAS
 NOTAS 1 Cuando en un mismo centro de trabajo desarrollen actividades trabajadores de dos o más empresas, éstas deberán cooperar en la aplicación de la normativa sobre prevención de riesgos laborales. A
NOTAS 1 Cuando en un mismo centro de trabajo desarrollen actividades trabajadores de dos o más empresas, éstas deberán cooperar en la aplicación de la normativa sobre prevención de riesgos laborales. A
ISO 9001:2015 Comprender los cambios clave. Lorri Hunt
 ISO 9001:2015 Comprender los cambios clave Lorri Hunt Exención de responsabilidad Si bien la información suministrada en esta presentación pretende explicar con precisión la actualización de la ISO 9001,
ISO 9001:2015 Comprender los cambios clave Lorri Hunt Exención de responsabilidad Si bien la información suministrada en esta presentación pretende explicar con precisión la actualización de la ISO 9001,
Sistema de Gestión de la Seguridad de la Información, UNE-ISO/IEC 27001
 Sistema de Gestión de la Seguridad de la Información, UNE-ISO/IEC 27001 Aníbal Díaz Gines Auditor de SGSI Certificación de Sistemas Applus+ Sistema de Gestión de la Seguridad de la Información, UNE-ISO/IEC
Sistema de Gestión de la Seguridad de la Información, UNE-ISO/IEC 27001 Aníbal Díaz Gines Auditor de SGSI Certificación de Sistemas Applus+ Sistema de Gestión de la Seguridad de la Información, UNE-ISO/IEC
GUIA SOBRE LOS REQUISITOS DE LA DOCUMENTACION DE ISO 9000:2000
 1 INTRODUCCIÓN Dos de los objetivos más importantes en la revisión de la serie de normas ISO 9000 han sido: desarrollar un grupo simple de normas que sean igualmente aplicables a las pequeñas, a las medianas
1 INTRODUCCIÓN Dos de los objetivos más importantes en la revisión de la serie de normas ISO 9000 han sido: desarrollar un grupo simple de normas que sean igualmente aplicables a las pequeñas, a las medianas
ISO 17025: 2005. Requisitos generales para la competencia de los laboratorios de ensayo y calibración
 ISO 17025: 2005 Requisitos generales para la competencia de los laboratorios de ensayo y calibración El presente documento es la versión impresa de la página www.grupoacms.com Si desea más información
ISO 17025: 2005 Requisitos generales para la competencia de los laboratorios de ensayo y calibración El presente documento es la versión impresa de la página www.grupoacms.com Si desea más información
Aseguramiento de la Calidad
 Aseguramiento de la Calidad El Aseguramiento de la Calidad consiste en tener y seguir un conjunto de acciones planificadas y sistemáticas, implantadas dentro del Sistema de Calidad de la empresa. Estas
Aseguramiento de la Calidad El Aseguramiento de la Calidad consiste en tener y seguir un conjunto de acciones planificadas y sistemáticas, implantadas dentro del Sistema de Calidad de la empresa. Estas
2. Redes de Medición de la Calidad del Aire
 2. Redes de Medición de la Calidad del Aire Una red de medición de la calidad del aire es parte de un Sistema de Medición de Calidad del aire, SMCA. Es importante mencionar que un SMCA puede incluir una
2. Redes de Medición de la Calidad del Aire Una red de medición de la calidad del aire es parte de un Sistema de Medición de Calidad del aire, SMCA. Es importante mencionar que un SMCA puede incluir una
Elementos requeridos para crearlos (ejemplo: el compilador)
 Generalidades A lo largo del ciclo de vida del proceso de software, los productos de software evolucionan. Desde la concepción del producto y la captura de requisitos inicial hasta la puesta en producción
Generalidades A lo largo del ciclo de vida del proceso de software, los productos de software evolucionan. Desde la concepción del producto y la captura de requisitos inicial hasta la puesta en producción
