Pegaptanib. Diseño: Son dos estudios prospectivos, randomizados, doble-ciego, multicéntricos y con diferentes dosis
|
|
|
- Lorenzo Alvarado Río
- hace 6 años
- Vistas:
Transcripción
1 Pegaptanib 1.- Identificación del fármaco: Nombre Comercial: Macugen Presentaciones: E/1 vial 0.3mg Laboratorio: Pfizer Precio adquisición: PVL+IVA: Grupo Terapéutico: S01XA17: Otros oftalmológicos 2.- Solicitud: Dr. Gallardo Galera. Jefe Sº Oftalmología. Fecha recepción de solicitud: 3 Noviembre Petición a título: Individual Consenso Servicio Consenso + Jefe de Servicio 3.- Farmacología 1 Indicaciones clínicas formalmente aprobadas en España: Tratamiento de la degeneración macular neovascular (exudativa) asociada a la edad (DMAE) Mecanismo de acción. Pegaptanib bloquea el VEGF, implicado en la neovascularización coroidea, inhibiendo la angiogénesis y reduciendo la permeabilidad vascular y la inflamación, que contribuiría a la progresión de la forma exudativa de la DMAE. Posología -Adultos: 0.3mg cada 6 semanas (9 administraciones al año) por inyección intravítrea en el ojo afectado. -Niños: No se ha evaluado en niños, por lo que no se recomienda su utilización. Farmacocinética. En animales, la absorción es la fase limitante para la disponibilidad. En humanos la semivida tras una dosis monoocular de 3mg es de 10±4 días. Se distribuye en plasma y no alcanza tejidos periféricos en cantidades apreciables. No se acumula en plasma si se administra de forma intravítrea cada 6 semanas. No requiere ajuste de dosis siempre que el aclaramiento de creatinina sea superior a 20ml/min. Por debajo de esto no se ha estudiado, y puede tener un incremento de hasta 2.3 veces el AUC. 4.- Evaluación de la eficacia Informe preliminar del Servicio de Farmacia Ventajas argumentadas por el solicitante Está indicado para todos los subtipos angiográficos de lesión, independientemente de la localización y el tamaño. Frente a esto, Verteporfin está indicado en lesiones predominantemente clásicas y ocultas, disminuyendo su eficacia en lesiones de gran tamaño. Verteporfin destruye la membrana neovascular una vez formada, pero no previene la formación de nuevos vasos al no actuar sobre el VEGF. Los efectos adversos de Verteporfin son sistémicos debido a su vía de administración intravenosa Ensayos Clínicos Comparativos Se han desarrollado 2 ensayos clínicos fase II/III, ampliamente comentados en el informe EPAR 2 de la EMEA además de estar ya publicados 3,4. Son los estudios EOP1003 y EOP1004: Diseño: Son dos estudios prospectivos, randomizados, doble-ciego, multicéntricos y con diferentes dosis Población: Se incluyeron un total de 1186 pacientes mayores de 50 años, con DMAE con neovascularción coroidea (en subfóvea) y un rango de agudeza visual de 20/40 a 20/320 en el ojo de estudio y 20/800 ó mejor en el otro ojo. Se incluyeron todos los subtipos de lesiones angiográficas, con un área de lesión de hasta 12 discos ópticos (1 disco=2.54 mm 2 ) 1
2 Tratamiento: Los pacientes se randomizaron a recibir de forma doble ciego 3 dosis diferentes de Pegaptanib: 0.3mg, 1mg ó 3mg) o placebo, cada 6 semanas y durante 48 semanas. Se permitió terapia fotodinámica con Verteporfin en el tratamiento de pacientes con lesiones clásicas, a criterio del oftalmólogo. Variable principal: % pacientes que perdían <15 letras de agudeza visual desde el inicio hasta la semana 54. Resultados: Variables Pegaptanib 0.3mg (n=294) Pegaptanib 1mg (n=300) Pegapatanib 3mg (n=296) Placebo (n=296) p (0.3mg vs placebo) % pac. con pérdida de <15 letras 70% 71% 65% 55% <0.001 % pac. con pérdida de >30 letras 10% 8% 14% 22% <0.001 % pac. con ganancia de >0 letras 33% 37% 31% 23% =0.003 % pac. con ganancia de >5 letras 22% 23% 17% 12% =0.004 % pac. ganancia de >10 letras 11% 14% 10% 6% =0.02 % pac. ganancia de >15 letras 6% 7% 4% 2% =0.04 Tamaño total de la lesión Basal Sem 54 Tamaño total de la neovascularización coroidea Basal Sem 54 Tamaño total de fugas Basal Sem (ns) < Ns Ns Resultados de otras variables: La evaluación de la calidad de vida por los pacientes no favoreció, después de todo, a los grupos de tratamiento activo 2 La EMEA solicitó información de los resultados del 2º año de tratamiento. En el 2º año, los pacientes que habían recibido tratamiento activo se re-randomizaban 1:1 a discontinuar o a seguir con su tratamiento, y los de placebo se re-randomizaban 1:1:1:1:1 a discontinuar, seguir con placebo o seguir con tratamiento activo. Se encontró que no existía diferencia entre los respondedores de los distintos grupos, y tampoco la había en el empeoramiento de agudeza visual entre placebo y pegaptanib 0.3 mg, en el estudio 1003, mayoritario en Europa. Seguridad: La discontinuación fue del 1% en Pegaptanib y 1% en placebo. La mayoría de los EA se atribuyeron al procedimiento más que al fármaco en sí. Se encontraron reacciones adversas oculares comunes con mayor frecuencia en el grupo de Pegaptanib (dolor en el ojo, cataratas, queratitis, opacidad vítrea, inflamación, molestias visuales y edema corneal). Además existe un mayor riesgo de desarrollar endoftalmitis con Pegaptanib intravítreo, por lo que se aconseja la utilización de este fármaco por personal médico con experiencia en este tipo de administraciones. Discusión: En el informe de la EMEA se indica que es claro que tras hasta 54 semanas de tratamiento, la enfermedad está aún activa; el nuevo fármaco consigue un menor incremento en el tamaño de la lesión y la revascularización coroidea que el grupo placebo, pero el tratamiento es sintomático y no curativo, y se desconoce el número total de inyecciones intravítreas que podrían ser toleradas antes de que haya un incremento inaceptable de efectos adversos graves. En la misma línea apunta un editorial, señalando que aunque es positivo que se abra una puerta al tratamiento de esta enfermedad basado en la angiogénesis, la magnitud del efecto del tratamiento es similar al conseguido con la terapia fotodinámica 5. Otra limitación del estudio es que se compara a placebo. 2
3 Conclusiones: Pegaptanib mejora de forma estadísticamente significativa, pero comparado con placebo, la mayoría de las variables descritas, en una diversa población de pacientes con DMAE tras 1 año. Los EA que puedan producirse requieren una especial vigilancia. Dado que esta enfermedad progresa con los años, se necesitan estudios a mayor largo plazo para conocer su verdadera eficacia y seguridad. La EMEA acaba considerando el balance beneficio/riesgo positivo, dada la gravedad de la enfermedad, aunque el beneficio absoluto de enlentecer la pérdida de agudeza visual resulta modesto y menos convincente tras los resultados del 2º año de tratamiento. RESULTADOS CON OTROS FÁRMACOS ANTIANGIOGÉNICOS Bevacizumab Se trata de una indicación no aprobada, pero autorizada a través del uso compasivo en España para pacientes de forma individual, habiéndose realizado varios estudios de corta duración a nivel internacional. Bevacizumab se comercializó para el tratamiento del cáncer metastásico colorrectal, y es un anticuerpo monoclonal humanizado completo, de 149 KD. No hay ningún dato exploratorio de ventajas o inconvenientes frente a Ranibizumab, fármaco que se registrará próximamente en esta indicación. Podría o no ser superior. Por ejemplo, el ser una molécula 3 veces más grande le haría permanecer en el ojo durante más tiempo y reducir la frecuencia de administración 6. Además tiene 2 sitios de unión al VEGF. Sin embargo, Ranibizumab también tendría argumentos para ser mejor. Es un fragmento Fab humanizado, con mayor afinidad por el VEGF y al tener menor tamaño podría llegar mejor a todas las capas 6. En caso de pasar a circulación, tiene una menor semivida, por lo que los efectos sistémicos serían menores 6, aunque Bevacizumab parece seguro, incluso a dosis altas ensayadas 7. De nada de esto hay realmente datos. La limitación en experiencia con Bevacizumab es que los estudios publicados son con pocos pacientes y a 3 meses, y algunos de estos estudios son retrospectivos No obstante la eficacia y seguridad del fármaco parecen muy adecuadas, y desde la publicación de los resultados de los primeros casos 11-12, su uso se ha ido extendiendo de forma continua. Una de las grandes ventajas supone poder disponer de un fármaco de nueva generación a un coste muy bajo, ya que de cada vial de 100mg de Bevacizumab se pueden obtener 25 dosis de inyecciones intravítreas 13, con estudios de estabilidad de hasta 6 meses evaluando la forma refrigerada y la posibilidad de congelación 14. De esta forma, administrar la dosis de 1.25mg por paciente y cada 4 semanas tendría un coste de 14 euros. Ranibizumab Ranibizumab es un fragmento de anticuerpo monoclonal anti VEGF diseñado para obtener una mayor afinidad por el VEGF, con un peso molecular de 48KD. Su eficacia y seguridad se han evaluado en 2 ensayos clínicos. El estudio MARINA 15, que evalúa las dosis de 0.3mg y 0.5mg frente a placebo, y el estudio ANCHOR 16, que lo hace frente a Verteporfin. En ambos estudios el resultado principal de eficacia (% de pacientes con pérdida de menos de 15 letras de agudeza visual al año) favorece a Ranibizumab. Aunque los estudios no son idénticos, en ambos la eficacia de Ranibizumab 0.3mg en esta variable se repite (94%), siendo algo sorprendente la similar tasa de respuesta del comparador; placebo en uno de ellos (62.2%) y Verteporfin en el otro (64.3%). El principal efecto adverso grave es el riesgo de endoftalmitis, uveitis e inflamación ocular, así como hemorragia no ocular. Nuevos estudios se están desarrollando en fase I/II evaluando la eficacia y seguridad de asociaciones de Ranibizumab+Verteporfin vs Verteporfin (estudio FOCUS 17 ), con resultados similares a los descritos. Lo que más interesaría sería un comparativo entre Bevacizumab y Ranibizumab, algo que ya algunos autores demandan que se realice para aclarar el tratamiento óptimo. La realización de otro tipo de estudios donde se varíen pautas, dosis, etc, sólo vendría a aportar confusión 18. Mientras tanto, la utilización fuera de indicación de Bevacizumab se postula como la opción más eficiente y atractiva, ya que muchos pacientes y sistemas de salud podrían permitirse un tratamiento de nueva generación a un coste muy asequible 13. 3
4 5. Evaluación de la seguridad 1 Se administró Pegaptanib a 892 pacientes en estudios controlados durante un año (número total de inyecciones = 7.545, promedio de inyecciones/paciente = 8,5) a las dosis de 0,3, 1,0 y 3,0 mg. Las tres dosis compartieron un perfil de seguridad similar. De los 295 pacientes que fueron tratados con la dosis recomendada de 0,3 mg durante un año (número total de inyecciones = 2.478, promedio de inyecciones/paciente = 8,4): - un 84% de los pacientes experimentó un acontecimiento adverso atribuido por los investigadores como relacionado con el procedimiento de inyección, - un 3% de los pacientes experimentó un acontecimiento adverso grave potencialmente relacionado con el procedimiento de inyección, - y un 1% experimentó un acontecimiento adverso que conllevó la interrupción del tratamiento del estudio y que fue potencialmente relacionado con el procedimiento de inyección. - Un 27% de los pacientes experimentó un acontecimiento adverso atribuido por los investigadores como relacionado con el medicamento en estudio. - Dos pacientes (0,7%) experimentaron acontecimientos adversos graves relacionados potencialmente con el medicamento en estudio. Uno de ellos presentó un aneurisma aórtico; el otro tuvo un desprendimiento de retina y una hemorragia retiniana, que conllevaron la interrupción del tratamiento. Los acontecimientos adversos oculares graves notificados en pacientes tratados con Pegaptanib incluyeron endoftalmitis (12 casos, 1%), hemorragia retiniana (3 casos, <1%), hemorragia del vítreo (2 casos, <1%) y desprendimiento de retina (4 casos, <1%). Trastornos oculares Estas reacciones adversas oculares fueron consideradas como potencialmente relacionadas con el tratamiento con Pegaptanib 0.3mg (bien debidas al procedimiento de inyección o bien debidas al fármaco), estando la mayoría consideradas como relacionadas con el procedimiento de la inyección. Muy frecuentes: inflamación de la cámara anterior, dolor ocular, aumento de la presión intraocular, queratitis puntiforme, partículas flotantes en el vítreo y opacidades del vítreo Frecuentes: sensación anormal en el ojo, catarata, hemorragia conjuntival, hiperemia conjuntival, edema conjuntival, conjuntivitis, distrofia corneal, defecto del epitelio corneal, trastorno del epitelio de la córnea, edema corneal, ojo seco, endoftalmitis, secreción ocular, inflamación ocular, irritación ocular, prurito ocular, ojo rojo, hinchazón ocular, edema palpebral, lagrimación aumentada, degeneración macular, midriasis, molestia ocular, hipertensión ocular, hematoma periorbital, fotofobia, fotopsia, hemorragia retiniana, visión borrosa, disminución de la agudeza visual, deterioro visual, desprendimiento del cuerpo vítreo y trastorno del cuerpo vítreo. Poco frecuentes: astenopia, blefaritis, conjuntivitis alérgica, depósitos corneales, hemorragia ocular, prurito palpebral, queratitis, hemorragia del vítreo, reflejo pupilar alterado, abrasión corneal, exudados retinianos, ptosis palpebral, cicatriz retiniana, chalazión, erosión corneal, disminución de la presión intraocular, reacción en la zona de inyección, vesículas en la zona de inyección, desprendimiento de retina, alteración corneal, oclusión arterial retiniana, desgarro retiniano, ectropión, trastorno de los movimientos oculares, irritación palpebral, hifema, trastorno pupilar, trastorno del iris, ictericia ocular, uveítis anterior, depósito en el ojo, iritis, excavación del nervio óptico, deformidad pupilar, oclusión cutánea, prurito, sudoración nocturna 374 pacientes recibieron un tratamiento continuo con Pegaptanib durante un periodo de 2 años (128 a 0,3 mg, 126 a 1 mg, y 120 a 3 mg). Los datos de seguridad globales fueron concordantes con los datos de seguridad a un año, no detectándose ninguna nueva señal de seguridad. En los 128 pacientes tratados con la dosis recomendada de 0,3 mg durante 2 años (número total de inyecciones en el segundo año = 913, promedio de inyecciones en el segundo año = 6,9), no hubo ningún aumento significativo en la frecuencia de acontecimientos adversos en comparación con los que se vieron durante el primer año. Experiencia post-comercialización: raramente se han notificado casos de anafilaxia/reacciones anafilactoides, incluyendo angioedema, en las horas siguientes a la administración de Pegaptanib junto a otros medicamentos que forman parte del procedimiento de preparación de la inyección. 4
5 6.- Area económica FARMACO Presentaciones Posología Coste fco/sesión Coste fco/año Verteporfin Vial 15mg 15 mg/3 meses Pegaptanib Vial 0.3mg 0.3 mg/6 semanas Bevacizumab Vial 100mg 1.25mg/4 semanas Ranibizumab Vial 0.5mg 0.5mg/4 semanas 1950 $ $ 7.- Conclusiones Pegaptanib es el primero de los fármacos implicados en la angiogénesis registrado para la degeneración macular asociada a la edad. Está indicado para todos los subtipos angiográficos de lesión, independientemente de la localización y el tamaño. En dos estudios fase III, Pegaptanib comparado frente a placebo fue superior en casi todas las variables a un año. Sin embargo, tras el año de tratamiento el fármaco resulta ser sintomático y no curativo, logrando un menor incremento en el tamaño de la lesión y la revascularización coroidea que el placebo, pero la enfermedad permanece aún activa. En uno de los dos estudios, durante el segundo año de tratamiento no se encontró diferencia entre los respondedores de los distintos grupos, ni diferencia en empeoramiento de agudeza visual entre placebo y Pegaptanib 0.3mg. Otras limitaciones de los resultados son que el resultado en la calidad de vida de los pacientes es similar entre los dos grupos, y que los resultados de eficacia son similares a los que obtenía Verteporfin en sus estudios iniciales. En seguridad, se desconoce el número total de inyecciones intravítreas que podrían ser toleradas antes de que haya un incremento inaceptable de efectos adversos graves. El efecto adverso más grave registrado es la aparición de endolftalmitis; también hemorragia retiniana, hemorragia del vítreo y desprendimiento de retina. Ya que la magnitud del efecto lograda con Pegaptanib parece ser similar a la alcanzada con Verteporfin, otras opciones son la utilización de otros antiangiogénicos bloqueantes del VEGF. De ellos, lo más eficiente es utilizar intravítreas de Bevacizumab, mediante su aprobación como uso compasivo. Esta opción, que puede tramitarse desde el Sº Farmacia fácilmente, se posiciona como la más eficiente, por poder utilizar un fármaco de nueva generación a un precio asumible. El Sº Farmacia propone no incluir Pegaptanib en la GFT, ofreciendo emplear la opción de Bevacizumab como alternativa a éste tras la terapia fotodinámica en caso de lesiones predominantemente clásicas y incluso como alternativa a la misma en otras situaciones. 8.- Bibliografía 1. Ficha técnica Macugen (Lab Pfizer) actualizada a Sept Committee for Medicinal Medical Products. European Public Assessment Report (EPAR). Macugen En 3. Gragoudas E, Adamis A, Cunningham A, Feinsod M and Guyer D. Pegaptanib for neovascular age-relates macular degeneration. N Engl J Med 2004; 351 (24): The VEGF inhibition study in ocular neovascularization (V.I.S.I.O.N.) Clinical Trial Group. Enhanced efficacy associated with early treatment of neovascular age-related macular degeneration with Pegaptanib Sodium: An exploratory analysis. Retina 2005; 25 (7): Ferris III, F. A new treatment for ocular neovascularizatioin. N Eng J Med 2004; 351 (27): Steinbrook R. The price of sight: Ranibizumab, Bevacizumab, and the treatment of macular degeneration. N Eng J Med 2006; 355 (14): Bashshur ZF, Bazarbachi A, Schakal A, Haddad ZA, El Haibi CP, Noureddin BN. Intravitreal bevacizumab for the management of choroideal neovascularization in age-related macular degeneration. Am J Ophtalmol 2006; 142 (1): Rich RM, Rosenfeld PJ, Puliafito CA et al. Short-term safety and efficacy of intravitreal bevacizumab (Avastin) for neovascular age-related macular degeneration. Retina 2006; 26 (5): Spaide RF, Laud K, Fine HF et al. Intravitreal bevacizumab treatment of choroidal neovascularization secondary to age-related macular degeneration. Retina 2006; 26 (4): Avery RL, Pieramici DJ, Rabena MD, Castellarin AA, Nasir MA and Giust MJ. Intravitreal bevacizumab (Avastin) for neovascular age-related macular degeneration. Ophthalmology 2006; 113 (3): Rosenfeld PJ, Fung AE, Pulfiato CA. Optical coherence tomography findings after an intravitreal injection of bevacizumab (Avastin) for macular edema from central retinal vein occlusion. Ophtalmic Surg Lasers Imaging 2005; 36:
6 12. Rosenfeld PJ, Moshfeghi AA, Pulfiato CA. Optical coherence tomography findings after an intravitreal injection of bevacizumab (Avastin) for neovascular age-related macular degeneration. Ophtalmic Surg Lasers Imaging 2005; 36: Rosenfeld PJ.Intravitreal Avastin: The low cost alternative to Lucentis? Am J Ophtalmol 2006; 142 (1): Bakri SJ, Snyder MR, Pulido JS, McCannel CA, Weiss WT and Singh RJ. Six-month stability of bevacizumab (Avastin) binding to vascular endothelial growth factor withdrawal into a syringe and refrigeration or freezing. Retina 2006; 26 (5): Rosenfeld PJ, Brown DM, Heier JS et al (MARINA Study Group). Ranibizumab for neovascular age-related macular degeneration. N Eng J Med 2006; 355 (14): Brown DM, Kaiser PK, Michels M et al (ANCHOR Study Group). Ranibizumab versus Verteporfin for neovascular age-related macular degeneration. N Eng J Med 2006; 355 (14): Heier JS, Boyer DS, Ciulla TA et al (FOCUS Study Group). Ranibizumab combined with Verteporfin Photodynamic Therapy in nevascular age-related macular degeneration. Arch Ophthalmol 2006; 124: Stone EM. A very effective treatment for neovascular macular degeneration. N Eng J Med 2006; 355 (14):
RANIBIZUMAB. (Novartis) LUCENTIS?
 RANIBIZUMAB LUCENTIS? (Novartis) DEGENERACIÓN MACULAR ASOCIADA A LA EDAD (DMAE) Es una enfermedad que afecta la mácula, la zona central de la retina que tiene un mayor poder de discriminación de la visión
RANIBIZUMAB LUCENTIS? (Novartis) DEGENERACIÓN MACULAR ASOCIADA A LA EDAD (DMAE) Es una enfermedad que afecta la mácula, la zona central de la retina que tiene un mayor poder de discriminación de la visión
Comisión de Evaluación de Medicamentos RANIBIZUMAB. Degeneración macular asociada a la edad (DMAE) neovascular (exudativa)
 Comisión de Evaluación de Medicamentos RANIBIZUMAB Degeneración macular asociada a la edad (DMAE) neovascular (exudativa) 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Ranibizumab (Lucentis
Comisión de Evaluación de Medicamentos RANIBIZUMAB Degeneración macular asociada a la edad (DMAE) neovascular (exudativa) 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Ranibizumab (Lucentis
4.5 Características comparadas con otros medicamentos con la misma indicación disponibles en el Hospital
 RANIBIZUMAB Degeneración macular asociada a la edad (Informe para la Comisión de Farmacia y Terapéutica del Hospital Universitario Central de Asturias) Fecha 01/08/2007 1.- IDENTIFICACIÓN DEL FÁRMACO Y
RANIBIZUMAB Degeneración macular asociada a la edad (Informe para la Comisión de Farmacia y Terapéutica del Hospital Universitario Central de Asturias) Fecha 01/08/2007 1.- IDENTIFICACIÓN DEL FÁRMACO Y
URGENCIAS EN OFTALMOLOGÍA
 URGENCIAS EN OFTALMOLOGÍA OJO ROJO NO DOLOROSO 99% de casos: HEMORRAGIA SUBCONJUNTIVAL. NIVEL 1 Actitud: Control de TA por su médico de cabecera; si se repite varias veces en poco tiempo, búsqueda sistémica
URGENCIAS EN OFTALMOLOGÍA OJO ROJO NO DOLOROSO 99% de casos: HEMORRAGIA SUBCONJUNTIVAL. NIVEL 1 Actitud: Control de TA por su médico de cabecera; si se repite varias veces en poco tiempo, búsqueda sistémica
INFORME FINAL RESULTADOS VISUALES EN PACIENTES
 INFORME FINAL RESULTADOS VISUALES EN PACIENTES CON MEMBRANA NEOVASCULAR ASOCIADA A LA EDAD TRATADOS CON BEVACIZUMAB EN EL INSTITUTO NACIONAL DE OFTALMOLOGIA JULIO A DICIEMBRE DEL 2011 TRABAJO PRESENTADO
INFORME FINAL RESULTADOS VISUALES EN PACIENTES CON MEMBRANA NEOVASCULAR ASOCIADA A LA EDAD TRATADOS CON BEVACIZUMAB EN EL INSTITUTO NACIONAL DE OFTALMOLOGIA JULIO A DICIEMBRE DEL 2011 TRABAJO PRESENTADO
Dra. Jaysi Pastrana Arias Oftalmología Especialista en Retina y Vítreo
 Dra. Jaysi Pastrana Arias Oftalmología Especialista en Retina y Vítreo Medicina Oftalmología Retina y Vítreo Universidad de Cartagena Universidad de Panamá Caja del Seguro Social Universidad Autónoma de
Dra. Jaysi Pastrana Arias Oftalmología Especialista en Retina y Vítreo Medicina Oftalmología Retina y Vítreo Universidad de Cartagena Universidad de Panamá Caja del Seguro Social Universidad Autónoma de
INFORME TÉCNICO UTILIZACIÓN DE FÁRMACOS INHIBIDORES DEL FACTOR DE CRECIMIENTO DEL ENDOTELIO VASCULAR POR VÍA INTRAVÍTREA
 INFORME TÉCNICO UTILIZACIÓN DE FÁRMACOS INHIBIDORES DEL FACTOR DE CRECIMIENTO DEL ENDOTELIO VASCULAR POR VÍA INTRAVÍTREA 2012 UTILIZACIÓN DE FÁRMACOS INHIBIDORES DEL FACTOR DE CRECIMIENTO DEL ENDOTELIO
INFORME TÉCNICO UTILIZACIÓN DE FÁRMACOS INHIBIDORES DEL FACTOR DE CRECIMIENTO DEL ENDOTELIO VASCULAR POR VÍA INTRAVÍTREA 2012 UTILIZACIÓN DE FÁRMACOS INHIBIDORES DEL FACTOR DE CRECIMIENTO DEL ENDOTELIO
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Macugen 0,3 mg solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Una jeringa precargada proporciona
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Macugen 0,3 mg solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Una jeringa precargada proporciona
Manual CTO de Medicina y Cirugía. 9.ª edición. Oftalmología. Autor. Julio González Martín-Moro
 Manual CTO de Medicina y Cirugía 9.ª edición Oftalmología Autor Julio González Martín-Moro NOTA La medicina es una ciencia sometida a un cambio constante. A medida que la investigación y la experiencia
Manual CTO de Medicina y Cirugía 9.ª edición Oftalmología Autor Julio González Martín-Moro NOTA La medicina es una ciencia sometida a un cambio constante. A medida que la investigación y la experiencia
CIME CENTRO DE INFORMACIÓN DE MEDICAMENTOS
 CIME CENTRO DE INFORMACIÓN DE MEDICAMENTOS FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD NACIONAL DE CÓRDOBA Ranibizumab y Bevacizumab en la degeneración macular asociada a la edad Caffaratti, M.; Real, J.P;
CIME CENTRO DE INFORMACIÓN DE MEDICAMENTOS FACULTAD DE CIENCIAS QUÍMICAS UNIVERSIDAD NACIONAL DE CÓRDOBA Ranibizumab y Bevacizumab en la degeneración macular asociada a la edad Caffaratti, M.; Real, J.P;
AMBOS SEXOS - De H00 a H59
 H00. Orzuelo y calacio H01. Otras inflamaciones del párpado H02. Otros trastornos de los párpados H04. Trastornos del aparato lagrimal H05. Trastornos de la órbita H10. Conjuntivitis H11. Otros trastornos
H00. Orzuelo y calacio H01. Otras inflamaciones del párpado H02. Otros trastornos de los párpados H04. Trastornos del aparato lagrimal H05. Trastornos de la órbita H10. Conjuntivitis H11. Otros trastornos
Tratamientos para la Degeneración Macular
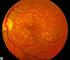 Tratamientos para la Degeneración Macular La mayoría de los tratamientos más comunes que se describen aquí impactan la degeneración macular húmeda relacionada a la edad (DMRE). Es importante señalar que
Tratamientos para la Degeneración Macular La mayoría de los tratamientos más comunes que se describen aquí impactan la degeneración macular húmeda relacionada a la edad (DMRE). Es importante señalar que
Oclusiones Venosas Retinales
 Oclusiones Venosas Retinales RETINAL VEIN OCCLUSION Dr. Alejandro Lutz H. (1), DR. PATRICIO MARTÍNEZ R. 1. Departamento de Oftalmología. Clínica las Condes. 2. Hospital del Salvador. Email: alejandrolutz@mi.cl
Oclusiones Venosas Retinales RETINAL VEIN OCCLUSION Dr. Alejandro Lutz H. (1), DR. PATRICIO MARTÍNEZ R. 1. Departamento de Oftalmología. Clínica las Condes. 2. Hospital del Salvador. Email: alejandrolutz@mi.cl
deterioro de la visión causado por un edema macular provocado por la diabetes;
 EMA/677928/2015 EMA/H/C/002392 Resumen del EPAR para el público general aflibercept El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo el Comité de Medicamentos
EMA/677928/2015 EMA/H/C/002392 Resumen del EPAR para el público general aflibercept El presente documento resume el Informe Público Europeo de Evaluación (EPAR) de. En él se explica cómo el Comité de Medicamentos
Ranibizumab, Bevacizumab y Aflibercept para Degeneración Macular asociada a la edad
 Ranibizumab, Bevacizumab y Aflibercept para Degeneración Macular asociada a la edad DOCUMENTO DE EVALUACIÓN DE TECNOLOGÍAS SANITARIAS Nro. 88 Esta es una Actualización del Documento de Evaluación de Tecnologías
Ranibizumab, Bevacizumab y Aflibercept para Degeneración Macular asociada a la edad DOCUMENTO DE EVALUACIÓN DE TECNOLOGÍAS SANITARIAS Nro. 88 Esta es una Actualización del Documento de Evaluación de Tecnologías
GPC. Guía de Referencia Rápida. Diagnóstico y Tratamiento del Trauma de Conjuntiva y Abrasión Corneal. Guía de Práctica Clínica
 Guía de Referencia Rápida Diagnóstico y Tratamiento del Trauma de Conjuntiva y Abrasión Corneal GPC Guía de Práctica Clínica Catálogo maestro de guías de práctica clínica: IMSS-520-11 Guía de Referencia
Guía de Referencia Rápida Diagnóstico y Tratamiento del Trauma de Conjuntiva y Abrasión Corneal GPC Guía de Práctica Clínica Catálogo maestro de guías de práctica clínica: IMSS-520-11 Guía de Referencia
DG de Farmacia y Productos Sanitarios PAISE
 Plan de Gestión riesgos para la administración de fármacos antiangiogénicos en la degeneración macular asociada a la edad, edema macular diabético, edema macular secundario a la oclusión de la vena retiniana,
Plan de Gestión riesgos para la administración de fármacos antiangiogénicos en la degeneración macular asociada a la edad, edema macular diabético, edema macular secundario a la oclusión de la vena retiniana,
PRESENTACIÓN GANFORT
 PRESENTACIÓN GANFORT PRESENTACIÓN GANFORT John J. Aristizábal Gómez Jefe Oftalmología H.P.T.U Docente Postgrado U.P.B Alcanzando la PIO meta Tratando el glaucoma de manera intensiva Abordaje terapéutico
PRESENTACIÓN GANFORT PRESENTACIÓN GANFORT John J. Aristizábal Gómez Jefe Oftalmología H.P.T.U Docente Postgrado U.P.B Alcanzando la PIO meta Tratando el glaucoma de manera intensiva Abordaje terapéutico
GUÍAS DE PRÁCTICA CLÍNICA DE LA SERV: TRATAMIENTO DE LA DEGENERACIÓN MACULAR ASOCIADA A LA EDAD (DMAE) EXUDATIVA
 ARCH SOC ESP OFTALMOL 2009; 84: 333-344 REVISIÓN GUÍAS DE PRÁCTICA CLÍNICA DE LA SERV: TRATAMIENTO DE LA DEGENERACIÓN MACULAR ASOCIADA A LA EDAD (DMAE) EXUDATIVA GUIDELINES OF CLINICAL PRACTICE OF THE
ARCH SOC ESP OFTALMOL 2009; 84: 333-344 REVISIÓN GUÍAS DE PRÁCTICA CLÍNICA DE LA SERV: TRATAMIENTO DE LA DEGENERACIÓN MACULAR ASOCIADA A LA EDAD (DMAE) EXUDATIVA GUIDELINES OF CLINICAL PRACTICE OF THE
FLORA BACTERIANA EN AGUJAS DE INYECCION DE RANIBIZUMAB EN LA FUNDACIÓN OFTALMOLOGICA NACIONAL
 2º. Curso Anual Institucional Fundación Oftalmológica Nacional y Sociedad de Cirugía Ocular 32º.Curso Anual de educación Continuada de la Fundación Oftalmológica Nacional FLORA BACTERIANA EN AGUJAS DE
2º. Curso Anual Institucional Fundación Oftalmológica Nacional y Sociedad de Cirugía Ocular 32º.Curso Anual de educación Continuada de la Fundación Oftalmológica Nacional FLORA BACTERIANA EN AGUJAS DE
*Ranibizumab es un fragmento de anticuerpo monoclonal humanizado producido en células de Escherichia coli mediante tecnología de ADN recombinante.
 NOMBRE DEL MEDICAMENTO Lucentis 10 mg/ml solución inyectable Lucentis 10 mg/ml solución inyectable en jeringa precargada COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 10 mg de ranibizumab*. *Ranibizumab
NOMBRE DEL MEDICAMENTO Lucentis 10 mg/ml solución inyectable Lucentis 10 mg/ml solución inyectable en jeringa precargada COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 10 mg de ranibizumab*. *Ranibizumab
PROGRAMA DE LECCIONES TEÓRICAS: OFTALMOLOGIA (4º) curso BASES ANATOMOFISIOLOGICAS DEL SISTEMA VISUAL
 PROGRAMA DE LECCIONES TEÓRICAS: OFTALMOLOGIA (4º) curso 2013-14 Las clases se impartirán en el AULA 6. BASES ANATOMOFISIOLOGICAS DEL SISTEMA VISUAL 1. PRESENTACION DEL CURSO El globo ocular. (I) Lunes,
PROGRAMA DE LECCIONES TEÓRICAS: OFTALMOLOGIA (4º) curso 2013-14 Las clases se impartirán en el AULA 6. BASES ANATOMOFISIOLOGICAS DEL SISTEMA VISUAL 1. PRESENTACION DEL CURSO El globo ocular. (I) Lunes,
Plan de Gestión riesgos para la administración de fármacos antiangiogénicos en la degeneración macular asociada a la edad.
 Plan de Gestión riesgos para la administración de fármacos antiangiogénicos en la degeneración macular asociada a la edad. (Adaptado de la plantilla Doc.Ref. EMEA/192632/2006) 1 Objeto Definir el plan
Plan de Gestión riesgos para la administración de fármacos antiangiogénicos en la degeneración macular asociada a la edad. (Adaptado de la plantilla Doc.Ref. EMEA/192632/2006) 1 Objeto Definir el plan
Dr. Felipe Centeno Rodríguez Oftalmología Hospital San Vicente de Paúl Oftalmología Hospital México Profesor Posgrado Oftalmología UCR
 Emergencias en Oftalmología Dr. Felipe Centeno Rodríguez Oftalmología Hospital San Vicente de Paúl Oftalmología Hospital México Profesor Posgrado Oftalmología UCR Es cualquier condición aguda que, de no
Emergencias en Oftalmología Dr. Felipe Centeno Rodríguez Oftalmología Hospital San Vicente de Paúl Oftalmología Hospital México Profesor Posgrado Oftalmología UCR Es cualquier condición aguda que, de no
Anti - VEGF: Adyuvantes - prequirúrgicos
 . Anti-VEGF: Aporta ventajas en la cirugía del glaucoma? Mª Isabel Canut 44º Congrés Societat Catalana d Oftalmologia Barcelona, 29 de Mayo 2013 Anti - VEGF: Adyuvantes - prequirúrgicos Bevacizumab (Avastin
. Anti-VEGF: Aporta ventajas en la cirugía del glaucoma? Mª Isabel Canut 44º Congrés Societat Catalana d Oftalmologia Barcelona, 29 de Mayo 2013 Anti - VEGF: Adyuvantes - prequirúrgicos Bevacizumab (Avastin
La importancia social y económica de esta enfermedad queda resumida en algunos datos:
 Domingo, 14 de marzo de 2010 De 11:30 a 13:00 horas Auditorio (N-103+N-104) La degeneración macular asociada a la edad (DMAE) es una enfermedad frecuente y grave, con un elevado coste social, económico
Domingo, 14 de marzo de 2010 De 11:30 a 13:00 horas Auditorio (N-103+N-104) La degeneración macular asociada a la edad (DMAE) es una enfermedad frecuente y grave, con un elevado coste social, económico
2013 GUIA DE MANEJO OJO ROJO CLINICA OFTALMOLÓGICADE TULUÁ ALFONSO MONDRAGÓN GIRALDO GERENTE GENERAL
 2013 GUIA DE MANEJO OJO ROJO CLINICA OFTALMOLÓGICADE TULUÁ ALFONSO MONDRAGÓN GIRALDO GERENTE GENERAL Páginas: 1 de 5 DEFINICION El ojo rojo es uno de los problemas oftalmológicos más frecuentes. Dentro
2013 GUIA DE MANEJO OJO ROJO CLINICA OFTALMOLÓGICADE TULUÁ ALFONSO MONDRAGÓN GIRALDO GERENTE GENERAL Páginas: 1 de 5 DEFINICION El ojo rojo es uno de los problemas oftalmológicos más frecuentes. Dentro
INFORMACIÓN DE SEGURIDAD PARA EL PROFESIONAL SANITARIO
 INFORMACIÓN DE SEGURIDAD PARA EL PROFESIONAL SANITARIO RECOMENDACIONES PARA EL TRATAMIENTO MEDIANTE INYECCIÓN INTRAVÍTREA (aflibercept) Material informativo autorizado por la Agencia Española de Medicamentos
INFORMACIÓN DE SEGURIDAD PARA EL PROFESIONAL SANITARIO RECOMENDACIONES PARA EL TRATAMIENTO MEDIANTE INYECCIÓN INTRAVÍTREA (aflibercept) Material informativo autorizado por la Agencia Española de Medicamentos
Valor del examen 28 puntos, nota mínima para acreditar 20 puntos
 COD. NOMBRE DEL PARTICIPANTE: 27 DE ABRIL 2013 NOMBRE DE LA ACTIVIDAD: SEMINARIO DE OFTALMOLOGIA FECHA: NÚMERO DE PREGUNTAS CORRECTAS APROBÓ SÍ NO Valor del examen 28 puntos, nota mínima para acreditar
COD. NOMBRE DEL PARTICIPANTE: 27 DE ABRIL 2013 NOMBRE DE LA ACTIVIDAD: SEMINARIO DE OFTALMOLOGIA FECHA: NÚMERO DE PREGUNTAS CORRECTAS APROBÓ SÍ NO Valor del examen 28 puntos, nota mínima para acreditar
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Lucentis 10 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 10 mg de ranibizumab*.
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Lucentis 10 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 10 mg de ranibizumab*.
MONOGRAFÍA DE PRODUCTO
 MONOGRAFÍA DE PRODUCTO UNA NUEVA MIRADA EN OFTALMOLOGÍA CONTENIDOS I. resumen ejecutivo 04 II. fundamentos 08 A) Información general sobre la enfermedad DMAE húmeda 09 A) El peso de la enfermedad (ceguera,
MONOGRAFÍA DE PRODUCTO UNA NUEVA MIRADA EN OFTALMOLOGÍA CONTENIDOS I. resumen ejecutivo 04 II. fundamentos 08 A) Información general sobre la enfermedad DMAE húmeda 09 A) El peso de la enfermedad (ceguera,
Titulación(es) Titulación Centro Curso Periodo 1204 - Grado de Medicina FACULTAT DE MEDICINA I ODONTOLOGIA
 FICHA IDENTIFICATIVA Datos de la Asignatura Código 34485 Nombre Oftalmología Ciclo Grado Créditos ECTS 4.5 Curso académico 2015-2016 Titulación(es) Titulación Centro Curso Periodo 1204 - Grado de Medicina
FICHA IDENTIFICATIVA Datos de la Asignatura Código 34485 Nombre Oftalmología Ciclo Grado Créditos ECTS 4.5 Curso académico 2015-2016 Titulación(es) Titulación Centro Curso Periodo 1204 - Grado de Medicina
1 I Tratamiento de la Degeneración Macular Asociada a la Edad (DMAE) exudativa
 Guías de práctica clínica de la SERV 1 I Tratamiento de la Degeneración Macular Asociada a la Edad (DMAE) exudativa Sociedad Española de Retina y Vitreo Guías de práctica clínica de la SERV 1 I Tratamiento
Guías de práctica clínica de la SERV 1 I Tratamiento de la Degeneración Macular Asociada a la Edad (DMAE) exudativa Sociedad Española de Retina y Vitreo Guías de práctica clínica de la SERV 1 I Tratamiento
CONTROVERSIAS HIPERTENSION PULMONAR
 CONTROVERSIAS HIPERTENSION PULMONAR Mª Carmen Torreiro Penas Hospital Xeral-Calde Lugo Eficacia/precio de los fármacos f aprobados? Es necesario evaluar los fármacos f aprobados? TRATAMIENTO Importantes
CONTROVERSIAS HIPERTENSION PULMONAR Mª Carmen Torreiro Penas Hospital Xeral-Calde Lugo Eficacia/precio de los fármacos f aprobados? Es necesario evaluar los fármacos f aprobados? TRATAMIENTO Importantes
Información sobre La Degeneración Macular Asociada a la Edad (DMAE)
 Información sobre La Degeneración Macular Asociada a la Edad (DMAE) Consulte a su oftalmólogo Por gentileza de: QUÉ ES LA DMAE? La DMAE es una patología que genera la pérdida progresiva de la visión y
Información sobre La Degeneración Macular Asociada a la Edad (DMAE) Consulte a su oftalmólogo Por gentileza de: QUÉ ES LA DMAE? La DMAE es una patología que genera la pérdida progresiva de la visión y
Rev Mex Oftalmol; Mayo-Junio 2009; 83(3):
 medigraphic Artemisa en línea ; Mayo-Junio 2009; 83(3):162-166 Cubas-Lorenzo y cols. Hallazgos en el electrorretinograma multifocal (ERGmf) posterior a la aplicación de bevacizumab (Avastin) intravítreo
medigraphic Artemisa en línea ; Mayo-Junio 2009; 83(3):162-166 Cubas-Lorenzo y cols. Hallazgos en el electrorretinograma multifocal (ERGmf) posterior a la aplicación de bevacizumab (Avastin) intravítreo
Fondo de Ojos. Examen de Fondo de Ojos
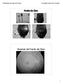 Fondo de Ojos Examen de Fondo de Ojos 1 Retina Fondo de Ojos Papila Mácula Vena retinal Arteríola retinal Fondo de Ojos: Papila Excavada por Glaucoma 2 Fondo de Ojos: Edema de Papila Fondo de Ojos: Edema
Fondo de Ojos Examen de Fondo de Ojos 1 Retina Fondo de Ojos Papila Mácula Vena retinal Arteríola retinal Fondo de Ojos: Papila Excavada por Glaucoma 2 Fondo de Ojos: Edema de Papila Fondo de Ojos: Edema
Tratamiento de una hemorragia subretiniana con r-tpa, SF 6 y ranibizumab
 Vol. 85 Marzo 2010 Núm. 3 Editorial OHTS 13 años después Artículos originales Vitrectomía vía pars plana e implante simultáneo de dispositivo de drenaje para glaucoma Detección automática de vasos en retinografías
Vol. 85 Marzo 2010 Núm. 3 Editorial OHTS 13 años después Artículos originales Vitrectomía vía pars plana e implante simultáneo de dispositivo de drenaje para glaucoma Detección automática de vasos en retinografías
Informe Ultrarrápido de Evaluación de Tecnología Sanitaria (IURETS)
 Informe Ultrarrápido de Evaluación de Tecnología Sanitaria (IURETS) Título Bevacizumab en el tratamiento de la retinopatía del prematuro (ROP) Autor/es Programa ETS Fecha de Inicio 16-02-2016 Fecha de
Informe Ultrarrápido de Evaluación de Tecnología Sanitaria (IURETS) Título Bevacizumab en el tratamiento de la retinopatía del prematuro (ROP) Autor/es Programa ETS Fecha de Inicio 16-02-2016 Fecha de
Eylea debe ser administrado únicamente por un médico cualificado con experiencia en la administración de inyecciones intravítreas.
 Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones
Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones
Conjuntiva: Tarsal. Cuerpo Extraño Tarsal + Ulcera Corneal. Conjuntiva: Hemorragia Sub-Conjuntival
 Conjuntiva: Tarsal Cuerpo Extraño Tarsal + Ulcera Corneal Conjuntiva: Hemorragia Sub-Conjuntival 1 Conjuntiva: Ojo Rojo Superficial indica inflamación de la conjuntiva Ojo Rojo Profundo indica inflamación
Conjuntiva: Tarsal Cuerpo Extraño Tarsal + Ulcera Corneal Conjuntiva: Hemorragia Sub-Conjuntival 1 Conjuntiva: Ojo Rojo Superficial indica inflamación de la conjuntiva Ojo Rojo Profundo indica inflamación
PROTOCOLO DE CIRUGÍA DEL PTERIGIÓN
 PROTOCOLO DE CIRUGÍA DEL PTERIGIÓN ÍNDICE 1. Objetivos y ámbito del protocolo 2. Definición 3. Diagnóstico y evaluación 4. Tratamiento Técnica quirúrgicas Tratamiento coadyuvante 5. Complicaciones 6. Cuidados
PROTOCOLO DE CIRUGÍA DEL PTERIGIÓN ÍNDICE 1. Objetivos y ámbito del protocolo 2. Definición 3. Diagnóstico y evaluación 4. Tratamiento Técnica quirúrgicas Tratamiento coadyuvante 5. Complicaciones 6. Cuidados
GENESIS-SEFH. Informe Base Página: 1
 GENESISSEFH Versión: 4. Programa MADRE versión 4. Fecha: 711213 Informe Base Página: 1 AFLIIBERCEPT DEGENERACIÓN MACULAR ASOCIADA A LA EDAD (Informe para la Comisión Regional de Farmacia y Terapéutica
GENESISSEFH Versión: 4. Programa MADRE versión 4. Fecha: 711213 Informe Base Página: 1 AFLIIBERCEPT DEGENERACIÓN MACULAR ASOCIADA A LA EDAD (Informe para la Comisión Regional de Farmacia y Terapéutica
Hay dos tipos de DMRE: seca y húmeda. Es posible que una persona sufra de ambas condiciones y además que la enfermedad avance lenta o rápidamente.
 La degeneración macular relacionada con la edad (DMRE) es una enfermedad común del ojo que provoca un deterioro de la mácula, el área central de la retina. La retina es un tejido parecido a un papel fino
La degeneración macular relacionada con la edad (DMRE) es una enfermedad común del ojo que provoca un deterioro de la mácula, el área central de la retina. La retina es un tejido parecido a un papel fino
RETINOPATÍA DIABÉTICA
 Qué es la retinopatía diabética? Las personas con diabetes pueden tener una enfermedad ocular llamada retinopatía diabética. Esta enfermedad ocurre porque los niveles altos de azúcar en la sangre causan
Qué es la retinopatía diabética? Las personas con diabetes pueden tener una enfermedad ocular llamada retinopatía diabética. Esta enfermedad ocurre porque los niveles altos de azúcar en la sangre causan
GPC. Guía de Referencia Rápida. Diagnóstico y Manejo del Orzuelo y Chalazión
 Guía de Referencia Rápida Diagnóstico y Manejo del Orzuelo y Chalazión GPC Guía de Práctica Clínica Número de Registro ESPACIO PARA SER LLENADO POR CENETEC Guía de Referencia Rápida H00 Orzuelo y Chalazión
Guía de Referencia Rápida Diagnóstico y Manejo del Orzuelo y Chalazión GPC Guía de Práctica Clínica Número de Registro ESPACIO PARA SER LLENADO POR CENETEC Guía de Referencia Rápida H00 Orzuelo y Chalazión
INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS BECAPLERMINA
 INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS Principio activo: BECAPLERMINA Nombre Comercial y presentación: REGRANEX (Vita) 0,01% 15 g gel (351,69 ) Conservación: Entre 2ºC y 8ºC.
INFORME DE EVALUACIÓN COMITÉ DE EVALUACIÓN DE NUEVOS MEDICAMENTOS Principio activo: BECAPLERMINA Nombre Comercial y presentación: REGRANEX (Vita) 0,01% 15 g gel (351,69 ) Conservación: Entre 2ºC y 8ºC.
METASTASIS COROIDEA DE CANCER DE MAMA. *Prof. Adjunta, Curso de Oftalmología, Área Medicina Interna. Facultad de
 METASTASIS COROIDEA DE CANCER DE MAMA Ceballos M*, De Merolis F**, Paredes G***. *Prof. Adjunta, Curso de Oftalmología, Área Medicina Interna. Facultad de Ciencias Médicas. Universidad Nacional de Cuyo.
METASTASIS COROIDEA DE CANCER DE MAMA Ceballos M*, De Merolis F**, Paredes G***. *Prof. Adjunta, Curso de Oftalmología, Área Medicina Interna. Facultad de Ciencias Médicas. Universidad Nacional de Cuyo.
Ojo Rojo y Urgencias Oftalmológicas
 Ojo Rojo y Urgencias Oftalmológicas Eugenio Maul Fonseca Outline 1. Emergencias vs Urgencias Oftalmológicas 2. Claves del examen 3. Tipos de Ojo Rojo Superficial vs Profundo 4. Cuadros frecuentes y diagnóstico
Ojo Rojo y Urgencias Oftalmológicas Eugenio Maul Fonseca Outline 1. Emergencias vs Urgencias Oftalmológicas 2. Claves del examen 3. Tipos de Ojo Rojo Superficial vs Profundo 4. Cuadros frecuentes y diagnóstico
Monitorización de niveles de vancomicina en Pediatría
 Monitorización de niveles de vancomicina en Pediatría Chevorn Suzette Adams (R3 Pediatría) María Luz Boquera Ferrer (R4 Farmacia Hospitalaria) Tutor: Dr. Luis Moral 3 febrero, 2016, HGUA. Objetivo Repasar
Monitorización de niveles de vancomicina en Pediatría Chevorn Suzette Adams (R3 Pediatría) María Luz Boquera Ferrer (R4 Farmacia Hospitalaria) Tutor: Dr. Luis Moral 3 febrero, 2016, HGUA. Objetivo Repasar
OJO ROJO TRAUMATICO. Dra Valeria C. Zampieri Hosp. De Niños R. Gutierrez Servicio de Oftalmología 2010
 OJO ROJO TRAUMATICO Dra Valeria C. Zampieri Hosp. De Niños R. Gutierrez Servicio de Oftalmología 2010 TRAUMA OCULAR EN LA INFANCIA Public health issue Incremento incidencia últimos años Significante morbilidad
OJO ROJO TRAUMATICO Dra Valeria C. Zampieri Hosp. De Niños R. Gutierrez Servicio de Oftalmología 2010 TRAUMA OCULAR EN LA INFANCIA Public health issue Incremento incidencia últimos años Significante morbilidad
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Lucentis 10 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 10 mg de ranibizumab.
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Lucentis 10 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene 10 mg de ranibizumab.
Vacuna frente al papilomavirus humano. (Comentarios a las fichas técnicas)
 Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
Guía de Referencia Rápida. Diagnóstico y Tratamiento de la Contusión Ocular y Orbitaria GPC. Guía de Práctica Clínica. Número de Registro: IMSS-424-10
 Guía de Referencia Rápida Diagnóstico y Tratamiento de la Contusión Ocular y Orbitaria GPC Guía de Práctica Clínica Número de Registro: IMSS-424-10 Guía de Referencia Rápida S05.1 Contusión ocular y orbitaria
Guía de Referencia Rápida Diagnóstico y Tratamiento de la Contusión Ocular y Orbitaria GPC Guía de Práctica Clínica Número de Registro: IMSS-424-10 Guía de Referencia Rápida S05.1 Contusión ocular y orbitaria
COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS
 COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS 1. SOLICITUD DEL FÁRMACO Principio activo solicitado: (erbitux
COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS 1. SOLICITUD DEL FÁRMACO Principio activo solicitado: (erbitux
DEGEnERACIÓn MACUlAR ASoCIADA A la EDAD
 DEGEnERACIÓn MACUlAR ASoCIADA A la EDAD TRATAMIEnTo Problemas para distinguir los contornos de los objetos o de los rostros, visión distorsionada de las líneas rectas Los síntomas de la degeneración macular
DEGEnERACIÓn MACUlAR ASoCIADA A la EDAD TRATAMIEnTo Problemas para distinguir los contornos de los objetos o de los rostros, visión distorsionada de las líneas rectas Los síntomas de la degeneración macular
GPC. Guía de Referencia Rápida. Diagnóstico de Catarata Congénita en el Recién Nacido. Guía de Práctica Clínica
 Guía de Referencia Rápida Diagnóstico de Catarata Congénita en el Recién Nacido GPC Guía de Práctica Clínica Catálogo maestro de guías de práctica clínica: IMSS-363-13 CIE-10: Q12.0 Catarata congénita
Guía de Referencia Rápida Diagnóstico de Catarata Congénita en el Recién Nacido GPC Guía de Práctica Clínica Catálogo maestro de guías de práctica clínica: IMSS-363-13 CIE-10: Q12.0 Catarata congénita
GUÍA DE MANEJO DEGENERACION MACULAR RELACIONADA CON LA EDAD DEPARTAMENTO OFTALMOLOGIA
 PÀGINA 1 de 5 GUÍA DE MANEJO DEGENERACION MACULAR DEPARTAMENTO OFTALMOLOGIA Revisión y adaptación de las guías de manejo elaboradas por el Servicio de oftalmología del Hospital de San José departamento
PÀGINA 1 de 5 GUÍA DE MANEJO DEGENERACION MACULAR DEPARTAMENTO OFTALMOLOGIA Revisión y adaptación de las guías de manejo elaboradas por el Servicio de oftalmología del Hospital de San José departamento
SENTIDO DE LA VISTA VALORACIÓN MÉDICO-LEGAL J.A. GONZÁLEZ GARCÍA. IMLC - Barcelona. Es una patología traumática? Valoración por un no especialista.
 SENTIDO DE LA VISTA VALORACIÓN MÉDICO-LEGAL J.A. GONZÁLEZ GARCÍA IMLC - Barcelona Es una patología traumática? Valoración por un no especialista. Valoración de un informe clínico o asistencial La importancia
SENTIDO DE LA VISTA VALORACIÓN MÉDICO-LEGAL J.A. GONZÁLEZ GARCÍA IMLC - Barcelona Es una patología traumática? Valoración por un no especialista. Valoración de un informe clínico o asistencial La importancia
TRATAMIENTO DEL EDEMA MACULAR PROVOCADO POR OCLUSIÓN VENOSA RETINIANA OZURDEX LUCENTIS
 TRTMIENTO DEL EDEM MCULR PROVOCDO POR OCLUSIÓN VENOS RETININ OZURDEX LUCENTIS Informe de evaluación de tecnologías sanitarias elaborado por el Servicio de Evaluación y Planificación a petición de la Dirección
TRTMIENTO DEL EDEM MCULR PROVOCDO POR OCLUSIÓN VENOS RETININ OZURDEX LUCENTIS Informe de evaluación de tecnologías sanitarias elaborado por el Servicio de Evaluación y Planificación a petición de la Dirección
Signos-síntomas-características: Dolor. Fotofobia. Lagrimeo. Disminución de la visión, sobre todo a distancia. Opacidad corneal.
 Afecciones Oculares 1. Anomalías que afectan a la córnea QUERATITIS Descripción: Inflamación de la córnea asociada a traumatismos, infecciones, trastornos de la nutrición corneal, exposiciones prolongadas
Afecciones Oculares 1. Anomalías que afectan a la córnea QUERATITIS Descripción: Inflamación de la córnea asociada a traumatismos, infecciones, trastornos de la nutrición corneal, exposiciones prolongadas
AFLIBERCEPT EN DEGENERACIÓN MACULAR ASOCIADA A LA EDAD Y EDEMA MACULAR ASOCIADO A OVCR
 Informe Base Página: 1 AFLIBERCEPT EN DEGENERACIÓN MACULAR ASOCIADA A LA EDAD Y EDEMA MACULAR ASOCIADO A OVCR (Informe para la CEMAI) Octubre 2014. Glosario: - ATA: acontecimientos tromboembólicos arteriales.
Informe Base Página: 1 AFLIBERCEPT EN DEGENERACIÓN MACULAR ASOCIADA A LA EDAD Y EDEMA MACULAR ASOCIADO A OVCR (Informe para la CEMAI) Octubre 2014. Glosario: - ATA: acontecimientos tromboembólicos arteriales.
Consideraciones prácticas en oftalmología dirigidas a las clínicas de primera asistencia A. Carbonell, R Torró umivale ( Valencia )
 Consideraciones prácticas en oftalmología dirigidas a las clínicas de primera asistencia A. Carbonell, R Torró umivale ( Valencia ) Se trata de recordar las cosas más esenciales que pueden encontrarse
Consideraciones prácticas en oftalmología dirigidas a las clínicas de primera asistencia A. Carbonell, R Torró umivale ( Valencia ) Se trata de recordar las cosas más esenciales que pueden encontrarse
Novedades en el diagnóstico de la superficie ocular: Keratograph 5M
 Novedades en el diagnóstico de la superficie ocular: Keratograph 5M Patología superficie ocular Efecto adverso de medicamentos. Enfermedades cutáneas que afectan a los párpados (Rosácea). Disfunción de
Novedades en el diagnóstico de la superficie ocular: Keratograph 5M Patología superficie ocular Efecto adverso de medicamentos. Enfermedades cutáneas que afectan a los párpados (Rosácea). Disfunción de
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox
 TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
(S-2844/10) PROYECTO DE LEY CAPÍTULO I DEL TÍTULO
 Senado de la Nación Secretaria Parlamentaria Dirección General de Publicaciones (S-2844/10) PROYECTO DE LEY El Senado y Cámara de Diputados,... CAPÍTULO I DEL TÍTULO Artículo 1 : Institúyese, a partir
Senado de la Nación Secretaria Parlamentaria Dirección General de Publicaciones (S-2844/10) PROYECTO DE LEY El Senado y Cámara de Diputados,... CAPÍTULO I DEL TÍTULO Artículo 1 : Institúyese, a partir
Lourdes Betegon 1 ; Cristina Canal 1 ; Marina De Salas-Cansado 2
 Análisis de Costes No Farmacológicos y Eventos Evitados en el Tratamiento de la Fibrilación Auricular en España: Apixaban Frente a Otros Fármacos Anticoagulantes Lourdes Betegon 1 ; Cristina Canal 1 ;
Análisis de Costes No Farmacológicos y Eventos Evitados en el Tratamiento de la Fibrilación Auricular en España: Apixaban Frente a Otros Fármacos Anticoagulantes Lourdes Betegon 1 ; Cristina Canal 1 ;
Glaucoma. Lente cristalino. Córnea. Iris. Humor vítreo
 Glaucoma Introducción El glaucoma es un grupo de enfermedades que afectan al ojo y que pueden llevar a la ceguera si no se recibe tratamiento adecuado. El glaucoma de ángulo abierto, la forma de glaucoma
Glaucoma Introducción El glaucoma es un grupo de enfermedades que afectan al ojo y que pueden llevar a la ceguera si no se recibe tratamiento adecuado. El glaucoma de ángulo abierto, la forma de glaucoma
Taller de Oftalmología. Exploración oftalmológica en la consulta de Pediatría; anomalías de la visión, fondo de ojo y urgencias oftalmológicas
 MADRID 16 A 18 DE OCTUBRE DE 2003 Taller OFTALMOLOGÍA Exploración oftalmológica en la consulta de Pediatría; anomalías de la visión, fondo de ojo y urgencias oftalmológicas Moderador: Ramón Ugarte Libano
MADRID 16 A 18 DE OCTUBRE DE 2003 Taller OFTALMOLOGÍA Exploración oftalmológica en la consulta de Pediatría; anomalías de la visión, fondo de ojo y urgencias oftalmológicas Moderador: Ramón Ugarte Libano
Protocolo de uso de agentes antiangiogénicos y corticoides intravítreos en patología ocular
 2015 Protocolo de uso de agentes antiangiogénicos y corticoides intravítreos en patología ocular [Escriba aquí una descripción breve del documento. Una descripción breve es un resumen corto del contenido
2015 Protocolo de uso de agentes antiangiogénicos y corticoides intravítreos en patología ocular [Escriba aquí una descripción breve del documento. Una descripción breve es un resumen corto del contenido
Guía Farmacoterapéutica de Hospital Sistema Sanitario Público de Andalucía GRUPO S
 Guía Farmacoterapéutica de Hospital Sistema Sanitario Público de Andalucía GRUPO S ÓRGANOS DE LOS SENTIDOS S S01 S01AA ÓRGANOS DE LOS SENTIDOS OFTALMOLÓGICOS ANTIBIÓTICOS S01AA11 GENTAMICINA Blefaritis,
Guía Farmacoterapéutica de Hospital Sistema Sanitario Público de Andalucía GRUPO S ÓRGANOS DE LOS SENTIDOS S S01 S01AA ÓRGANOS DE LOS SENTIDOS OFTALMOLÓGICOS ANTIBIÓTICOS S01AA11 GENTAMICINA Blefaritis,
LEVETIRACETAM SOLUCION INTRAVENOSA EN EPILEPSIA (Informe para la Comisión de Farmacia y Terapéutica del Hospital Son LLátzer) Fecha Abril 2008
 LEVETIRACETAM SOLUCION INTRAVENOSA EN EPILEPSIA (Informe para la Comisión de Farmacia y Terapéutica del Hospital Son LLátzer) Fecha Abril 2008 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco:
LEVETIRACETAM SOLUCION INTRAVENOSA EN EPILEPSIA (Informe para la Comisión de Farmacia y Terapéutica del Hospital Son LLátzer) Fecha Abril 2008 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco:
SERPIENTES Definición:
 SERPIENTES Definición: Las serpientes u ofidios son reptiles caracterizados por la ausencia de extremidades y un cuerpo muy alargado. En España hay solo dos familias de serpientes venenosas: las víboras
SERPIENTES Definición: Las serpientes u ofidios son reptiles caracterizados por la ausencia de extremidades y un cuerpo muy alargado. En España hay solo dos familias de serpientes venenosas: las víboras
I- EXAMEN OFTALMOLOGICO EN EL NIÑO. Debe hacerse de rutina (según AAO y AAPOS): En el recién nacido. A los 6 meses. A los 3 años. A los 5 años.
 I- EXAMEN OFTALMOLOGICO EN EL NIÑO Debe hacerse de rutina (según AAO y AAPOS): En el recién nacido. A los 6 meses. A los 3 años. A los 5 años. 1. EXAMEN EN EL RECIEN NACIDO Hay dos grupos de patologías
I- EXAMEN OFTALMOLOGICO EN EL NIÑO Debe hacerse de rutina (según AAO y AAPOS): En el recién nacido. A los 6 meses. A los 3 años. A los 5 años. 1. EXAMEN EN EL RECIEN NACIDO Hay dos grupos de patologías
Qué es y dónde está la mácula? Defectos Centrales. Síntomas de Enfermedad Macular DEFINICION. Patología a Degenerativa de la Retina.
 50 40 30 20 10 0 41 2 5 11 14 3 3 RP 5 RD 1 16 Qué es y dónde está la mácula? Patología a Degenerativa de la Retina Dra. RM Coco Martín Unidad de Mácula y Degeneraciones Retinianas Para qué sirve la mácula?
50 40 30 20 10 0 41 2 5 11 14 3 3 RP 5 RD 1 16 Qué es y dónde está la mácula? Patología a Degenerativa de la Retina Dra. RM Coco Martín Unidad de Mácula y Degeneraciones Retinianas Para qué sirve la mácula?
TRABAJO DE INVESTIGACIÓN
 ESTUDIO COMPARATIVO ENTRE RANIBIZUMAB Y BEVACIZUMAB EN EL TRATAMIENTO DE DEGENERACIÓN MACULAR ASOCIADA A LA EDAD TIPO EXUDATIVO Departamento de cirugía UAB Autor:Dra. Idoia Rodríguez Maiztegui Director:
ESTUDIO COMPARATIVO ENTRE RANIBIZUMAB Y BEVACIZUMAB EN EL TRATAMIENTO DE DEGENERACIÓN MACULAR ASOCIADA A LA EDAD TIPO EXUDATIVO Departamento de cirugía UAB Autor:Dra. Idoia Rodríguez Maiztegui Director:
ABORDAJE DEL OJO ROJO EN ATENCIÓN PRIMARIA
 ABORDAJE DEL OJO ROJO EN ATENCIÓN PRIMARIA Carlos Navarro Cueva, R3 MFyC del CS Rafalafena Tutorizado por Mª Dolores Aicart Bort Castelló de la Plana, Junio de 2015 De qué hablamos? es la manifestación
ABORDAJE DEL OJO ROJO EN ATENCIÓN PRIMARIA Carlos Navarro Cueva, R3 MFyC del CS Rafalafena Tutorizado por Mª Dolores Aicart Bort Castelló de la Plana, Junio de 2015 De qué hablamos? es la manifestación
(Leyes 26.529-26742 y Decreto Reglamentario 1089 / 2012)
 CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE BEVACIZUMAB (AVASTÍN) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ( HUMEDA Ó NEOVASCULAR) (Leyes 26.529-26742 y Decreto Reglamentario
CONSENTIMIENTO INFORMADO PARA LA INYECCIÓN INTRAOCULAR DE BEVACIZUMAB (AVASTÍN) EN LA DEGENERACIÓN MACULAR RELACIONADA CON LA EDAD EXUDATIVA ( HUMEDA Ó NEOVASCULAR) (Leyes 26.529-26742 y Decreto Reglamentario
INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) INSULINAS
 Centro de Información de Medicamentos. Servicio de Farmacia. INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) Datos del solicitante INSULINAS Dr. Pedro José Pines Corrales, FEA del servicio
Centro de Información de Medicamentos. Servicio de Farmacia. INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) Datos del solicitante INSULINAS Dr. Pedro José Pines Corrales, FEA del servicio
FISIOPATOLOGÍA OCULAR.
 FISIOPATOLOGÍA OCULAR http://labibliotecademaverick.blogspot.com/ Recordemos casa grande Iris casa Párpado superior casa grande casa casa grande casa Medial Párpado casa grande inferior casa casa Pupila
FISIOPATOLOGÍA OCULAR http://labibliotecademaverick.blogspot.com/ Recordemos casa grande Iris casa Párpado superior casa grande casa casa grande casa Medial Párpado casa grande inferior casa casa Pupila
Bevacizumab en el tratamiento del edema macular cistoideo postcirugía de catarata: a propósito de un caso clínico bilateral
 ARCH. SOC. CANAR. OFTAL., 2010; 21: 60-64 CASO CLÍNICO Bevacizumab en el tratamiento del edema macular cistoideo postcirugía de catarata: a propósito de un caso clínico bilateral Bevacizumab in cystoid
ARCH. SOC. CANAR. OFTAL., 2010; 21: 60-64 CASO CLÍNICO Bevacizumab en el tratamiento del edema macular cistoideo postcirugía de catarata: a propósito de un caso clínico bilateral Bevacizumab in cystoid
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita
Anexo I. Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización
 Anexo I Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización 1 Conclusiones científicas Teniendo en cuenta lo dispuesto en el Informe
Anexo I Conclusiones científicas y motivos para la modificación de las condiciones de la(s) autorización(es) de comercialización 1 Conclusiones científicas Teniendo en cuenta lo dispuesto en el Informe
Cada ml contiene levocabastina (como hidrocloruro) equivalente a 0,5 mg de levocabastina.
 1. NOMBRE DEL MEDICAMENTO Bilina 0,5 mg/ml colirio en suspensión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene levocabastina (como hidrocloruro) equivalente a 0,5 mg de levocabastina. Excipiente
1. NOMBRE DEL MEDICAMENTO Bilina 0,5 mg/ml colirio en suspensión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene levocabastina (como hidrocloruro) equivalente a 0,5 mg de levocabastina. Excipiente
ARCHIVOS DE LA SOCIEDAD ESPAÑOLA DE OFTALMOLOGÍA
 Vol. 87 Diciembre 2012 Extraordinario 1 Lucentis. Cinco años de experiencia: de los ensayos clínicos a la práctica clínica Introducción Ranibizumab frente a bevacizumab. Consideraciones farmacológicas
Vol. 87 Diciembre 2012 Extraordinario 1 Lucentis. Cinco años de experiencia: de los ensayos clínicos a la práctica clínica Introducción Ranibizumab frente a bevacizumab. Consideraciones farmacológicas
SALUD OCULAR CAUSAS Y EFECTOS EFECTOS DE UNA MALA CAUSAS DE UNA MALA SALUD OCULAR SALUD OCULAR ESTRÉS ENROJECIMIENTO. CANSANCIO y DOLOR OCULAR
 SALUD 1. CAUSAS Y EFECTOS CAUSAS DE UNA MALA SALUD ESTRÉS POLUCIÓN EFECTOS DE UNA MALA SALUD ENROJECIMIENTO CANSANCIO y DOLOR Mala ALIMENTACIÓN Menor SECRECIÓN LAGRIMAL SOBREEXPOSICIÓN con DISPOSITIVOS
SALUD 1. CAUSAS Y EFECTOS CAUSAS DE UNA MALA SALUD ESTRÉS POLUCIÓN EFECTOS DE UNA MALA SALUD ENROJECIMIENTO CANSANCIO y DOLOR Mala ALIMENTACIÓN Menor SECRECIÓN LAGRIMAL SOBREEXPOSICIÓN con DISPOSITIVOS
DEL HEMANGIOMA INFANTIL
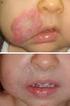 COMUNICACIÓN CIENTÍFICA PROPRANOLOL ORAL EN EL TRATAMIENTO DEL HEMANGIOMA INFANTIL Martínez Roca C 1, Yáñez Gómez P 1, Gómez Tellado M 2, Vilaboa Pedrosa C 1, Calleja Chuclá T 1, Martín Herranz MI 1. 1
COMUNICACIÓN CIENTÍFICA PROPRANOLOL ORAL EN EL TRATAMIENTO DEL HEMANGIOMA INFANTIL Martínez Roca C 1, Yáñez Gómez P 1, Gómez Tellado M 2, Vilaboa Pedrosa C 1, Calleja Chuclá T 1, Martín Herranz MI 1. 1
TABLA DE EVIDENCIAS BZM INTRA VÍTREO EN RETINOPATIA DEL PREMATURO
 TABLA DE EVIDENCIAS BZM INTRA VÍTREO EN RETINOPATIA DEL PREMATURO Estudio Diseño/población/número/ Intervención/comparador Puntos intermedios Resultados/ Conclusiones Fortalezas/Limitaciones de la evidencia
TABLA DE EVIDENCIAS BZM INTRA VÍTREO EN RETINOPATIA DEL PREMATURO Estudio Diseño/población/número/ Intervención/comparador Puntos intermedios Resultados/ Conclusiones Fortalezas/Limitaciones de la evidencia
Patología Oftalmológica en la Infancia
 Patología Oftalmológica en la Infancia Alejandra S. Tártara Servicio de Oftalmología HNRG-Buenos Aires Argentina Oftalmopediatría Desarrollo Visual del Niño Estímulos: Luz - Forma - Color Para Aprender
Patología Oftalmológica en la Infancia Alejandra S. Tártara Servicio de Oftalmología HNRG-Buenos Aires Argentina Oftalmopediatría Desarrollo Visual del Niño Estímulos: Luz - Forma - Color Para Aprender
CONCLUSIONES. 2. La mayoría de pacientes presentó mal control metabólico con niveles altos de glicemia y hemoglobina glicosilada.
 CONCLUSIONES 1. Confirmamos en el Instituto Nacional de Ojos que la Población de mayor prevalencia proceden de Lima 39.2 % en comparación con el 60.8% procedente de los demás departamentos del país predominando
CONCLUSIONES 1. Confirmamos en el Instituto Nacional de Ojos que la Población de mayor prevalencia proceden de Lima 39.2 % en comparación con el 60.8% procedente de los demás departamentos del país predominando
CIRCUITO ASISTENCIAL DE INTERCONSULTA ENTRE ATENCIÓN PRIMARIA Y OFTALMOLOGIA
 CIRCUITO ASISTENCIAL DE INTERCONSULTA ENTRE ATENCIÓN PRIMARIA Y OFTALMOLOGIA Borrador a mayo de2007 Contenido: - Problemas oftalmológicos que requieren atención especializada: o Urgencias oftalmológicas.
CIRCUITO ASISTENCIAL DE INTERCONSULTA ENTRE ATENCIÓN PRIMARIA Y OFTALMOLOGIA Borrador a mayo de2007 Contenido: - Problemas oftalmológicos que requieren atención especializada: o Urgencias oftalmológicas.
UNA LUCHA OPTIMISTA 3 - BARCELONA MACULA FOUNDATION: RESEARCH FOR VISION
 ESP UNA LUCHA OPTIMISTA OPTIMISMO. Esta es la palabra que más nos gusta usar a los oftalmólogos que hemos decidido apostar por la investigación internacional en la lucha contra la ceguera. Los avances
ESP UNA LUCHA OPTIMISTA OPTIMISMO. Esta es la palabra que más nos gusta usar a los oftalmólogos que hemos decidido apostar por la investigación internacional en la lucha contra la ceguera. Los avances
Adaptarse para seguir activos. ONCE. Valladolid
 Adaptarse para seguir activos. ONCE. Valladolid Un programa para facilitar la adaptación a la deficiencia visual Algunas cifras sobre deficiencia visual en personas mayores El 16% de los mayores de 80
Adaptarse para seguir activos. ONCE. Valladolid Un programa para facilitar la adaptación a la deficiencia visual Algunas cifras sobre deficiencia visual en personas mayores El 16% de los mayores de 80
Especialista en Urgencias Oftalmológicas
 Titulación certificada por EUROINNOVA BUSINESS SCHOOL Especialista en Urgencias Oftalmológicas Especialista en Urgencias Oftalmológicas Duración: 200 horas Precio: 260 * Modalidad: Online * Materiales
Titulación certificada por EUROINNOVA BUSINESS SCHOOL Especialista en Urgencias Oftalmológicas Especialista en Urgencias Oftalmológicas Duración: 200 horas Precio: 260 * Modalidad: Online * Materiales
El edema macular es la hinchazón o engrosamiento de la mácula del ojo, la parte del ojo responsable por la visión central y detallada.
 Qué Es un Edema Macular? El edema macular es la hinchazón o engrosamiento de la mácula del ojo, la parte del ojo responsable por la visión central y detallada. La mácula es un área muy pequeña en el centro
Qué Es un Edema Macular? El edema macular es la hinchazón o engrosamiento de la mácula del ojo, la parte del ojo responsable por la visión central y detallada. La mácula es un área muy pequeña en el centro
KETOCONAZOLE IN THE TREATMENT OF CHRONIC IDIOPATHIC CENTRAL SEROUS CHORIORETINOPATHY
 KETOCONAZOLE IN THE TREATMENT OF CHRONIC IDIOPATHIC CENTRAL SEROUS CHORIORETINOPATHY CATHERINE B. MEYERLE, MD, K. BAILEY FREUND, MD, PAWAN BHATNAGAR, MD, VIRAL SHAH, MD, LAWRENCE A. YANNUZZI, MD LuEsther
KETOCONAZOLE IN THE TREATMENT OF CHRONIC IDIOPATHIC CENTRAL SEROUS CHORIORETINOPATHY CATHERINE B. MEYERLE, MD, K. BAILEY FREUND, MD, PAWAN BHATNAGAR, MD, VIRAL SHAH, MD, LAWRENCE A. YANNUZZI, MD LuEsther
Boletín Brasileño de Evaluación de Tecnologías en Salud
 06BRATS ISSN 1983-7003 Año III nº 6 Diciembre de 2008 INHIBIDORES DE LA ANGIOGENESIS PARA EL TRATAMIENTO DE LA DEGENERACIÓN MACULAR RELACIONADA A LA EDAD Resumen La degeneración macular relacionada a la
06BRATS ISSN 1983-7003 Año III nº 6 Diciembre de 2008 INHIBIDORES DE LA ANGIOGENESIS PARA EL TRATAMIENTO DE LA DEGENERACIÓN MACULAR RELACIONADA A LA EDAD Resumen La degeneración macular relacionada a la
RETINOPATIA LEUCEMICA
 RETINOPATIA LEUCEMICA Retinopatia Leucemica 1996, 27.600 casos leucemia USA. Sx oftalmologicos Dx. Enf. Sistemica. El ojo refleja el estado de la enf en el cuerpo Examen oftalmologico Extension Pronostico.
RETINOPATIA LEUCEMICA Retinopatia Leucemica 1996, 27.600 casos leucemia USA. Sx oftalmologicos Dx. Enf. Sistemica. El ojo refleja el estado de la enf en el cuerpo Examen oftalmologico Extension Pronostico.
Melasma. Andrea Albuja, Nicolás Almeida, Danilo Noboa UIDE
 Melasma Andrea Albuja, Nicolás Almeida, Danilo Noboa UIDE Es la terapia triple la mejor opción de tratamiento en pacientes con melasma? Primer articulo 2003 Criterios Inclusion: muestra de 641 pacientes
Melasma Andrea Albuja, Nicolás Almeida, Danilo Noboa UIDE Es la terapia triple la mejor opción de tratamiento en pacientes con melasma? Primer articulo 2003 Criterios Inclusion: muestra de 641 pacientes
Marca/s registrada/s (Laboratorio/s): Saflutan (MSD España, S.A. ) Fecha autorización (procedimiento): septiembre 2008 (reconocimiento mutuo)
 Información de Medicamentos (CADIME) Campus Universitario de Cartuja TAFLUPROST (DCI) Calificación(*): NO SUPONE UN AVANCE TERAPÉUTICO Fecha de evaluación: febrero 2010 Fecha de reevaluación: junio 2011
Información de Medicamentos (CADIME) Campus Universitario de Cartuja TAFLUPROST (DCI) Calificación(*): NO SUPONE UN AVANCE TERAPÉUTICO Fecha de evaluación: febrero 2010 Fecha de reevaluación: junio 2011
