MATERIALES Y METODOS. El presente trabajo se desarrolló en el Laboratorio de. Investigación del Departamento de Ciencias Químico Biológicas de
|
|
|
- Eugenia Aranda Villalobos
- hace 5 años
- Vistas:
Transcripción
1 19 MATERIALES Y METODOS El presente trabajo se desarrolló en el Laboratorio de Investigación del Departamento de Ciencias Químico Biológicas de la Universidad de Sonora Unidad Regional Norte campus Caborca. Se utilizó un sistema para electroforesis Mini -Protean 3 (Bio-Rad). (Figura 2) para medir los volúmenes con alta precisión se u tilizaron micro pipetas de volumen variable ( µL y µL) de la marca comercial Rainin Instrument (SL1000 y SL100) y sus respectivas puntas desechables para micro pipetas. Las muestras fueron preparadas en tubos Eppendorf de 2 ml. En todo el trab ajo se utilizó agua bidestilada y des ionizada. Los reactivos fueron grado analítico especiales para electroforesis todos de la Marca SIGMA-ALDRICH, Acrilamida (cat. A-3553), Trizma base (cat. T1503), N;N -methylen-bis-acrilamida (cat. M-7279), Azul brillante coomassie R-250 (cat ), Azul de bromo fenol (cat. B5525), glicina (cat. G-8898), SDS (cat. L3771) Persulfato de amonio (cat A3678).Los procedimientos para la preparación de soluciones se encuentran descritos en el ANEXO A.
2 20 Figura 2. Componentes para la preparación de geles de electroforesis SDS del Sistema Mini-Protean 3 (Bio-Rad) a) Fuente de poder, b) tanque para corridas, c) soportes para elaboración de geles, d) moldes de cristal para formación de geles, e) soportes para tanque de corrida, f) peines para formación de pocillos, g) Guía para carga de muestra.
3 21 En la Figura 2 se observa el sistema Mini-Protean 3 de Bio- Rad. En este sistema se fabrican los geles o se puede utilizar geles comerciales prefabricados. Este sistema inclu ye placas de cristal con el espaciador (0.75mm) unido en forma permanente que simplifica el manejo de los moldes. El empleo de reactivos de alta calidad y agua desionizada es un prerrequisito para hacer geles reproducibles y de alta resolución, en particular esto es muy importante para la acrilamida, ya que es el constituyente más abundante del gel y sus principales impurezas son acido acrílica residual (que puede retardar la actividad electroforética de algunas proteínas), poliacrilamida lineal e iones 10. Preparación de Geles de Poliacrilamida Los geles de poliacrilamida (PAGE) son los soportes de elección para la electroforesis, porque son químicamente inertes y se forman con facilidad mediante polimerización de la acrilamida. Además, escogiendo distin tas cantidades de acrilamida y metilen - bis-acrilamida (un reactivo que realiza enlaces cruzados) y, variando los tiempos de polimerización, se pueden conseguir tamaños de poro controlados 11, que servirán como tamices moleculares que potencian la separación. Se ha planteado que la resolución de moléculas generalmente aumenta con la disminución
4 22 del grosor del gel 12. Los geles de poliacrilamida utilizados, constan de dos partes y se preparan sobre moldes verticales de vidrio. El gel superior (gel concentrador) tiene alrededor de 2 cm de longitud y los pocillos para aplicar las muestras. El gel inferio r (gel separador) tiene un recorrido de unos 6 cm. Se debe tener especial precaución debido a que la acrilamida es un compuesto químico neurotóxico, mientras que la poliacrilamida no lo es; por lo que para la preparación de geles es necesario del uso de guantes de látex. Ensamblado de los moldes Previamente al ensamble de los moldes para la preparación de geles el material se lavó con una solución de extrán al 2% y enjuagados con agua desionizada. Se dejan secar en una estufa para secado de material (100 C, 1h), y posteriormente se enjuagaron con etanol al 70% procurando manipular los vidrios solamente por los bordes para evitar cualquier contaminación, una vez secos se procede a realizar el ensamble del molde para la formación de geles. Se utilizaron los vidrios con espaciador de 0.75 mm de espesor, se colocan en el soporte para los moldes y se verificó que no existieran fugas agregando agua hasta el borde superior de los moldes dejando por unos minutos para asegurar de que no existan fugas. Después se descartó el agua inclinando el soporte con los moldes ensamblados (Figura 3)
5 23 a b c d Figura 3. Ensamblado de cristales para formar el molde para geles de electroforesis PAGE. a) Alineado de vidrios para geles con espaciador de 0.75mm de espesor, b) introducción de vidrios en el marco, c) Emparejamiento y ajuste de vidrios en el marco. d) Colocación y aseguramiento del marco en la base de soporte.
6 24 Polimerización del gel de poliacrilamida En la Tabla 1 se describen las cantidades de soluciones requeridas para la formación de geles para el sistema Mini- Protean 3 de Bio-Rad con 12% de entrecruzamiento. Estas cantidades pueden adaptarse para otras cámaras de diversa capacidad, conservando las proporciones. En el anexo B se dan las concentraciones para otros porcentajes de entrecruzamiento. En un tubo Falcon se mezclaron los reactivos para la preparación del gel separador y en otro tubo para el gel concentrador en las cantidades descritas en la Tabla 1: El persulfato de amonio al 10 %, se agregó un instante antes de vaciar la mezcla en los moldes (agregar los geles). En la Figura 4 se observa el procedimiento para la preparación de los geles. Primeramente se descartó el agua de los moldes una vez que se verificó que no existían fugas. Al agregar el persulfato de amonio a la mezcla de reactivos para gel separador, se agregó la mezcla al interior de los moldes hasta alcanzar tres cuartas partes del volumen. Después se agregó agua desionizada para eliminar cualquier burbuja que se hubiera formado, además que esta reacción es fuertemente inhibida por altos niveles de oxigeno. 2 Se permitió la polimerización durante un tiempo de 20 min aproximadamente.
7 25 Tabla 1. Volumen de soluciones (microlitros) requeridas para la preparación del gel de poliacrilamida al 12%, para el sistema Mini - Protean 3 de Bio-Rad. Soluciones Gel Separador Gel Concentrador Acrilamida/Bis-acrilamida (30%/0.8%) x Trizma HCl/SDS Agua des ionizada Persulfato de amonio (10%) TEMED La solución de persulfato de amonio (10%) se agrega antes de chorrear los geles ya que este es el que inicia la reacción de polimerización.
8 26 a b c d Figura 4. Preparación del gel separador y concentrador. a) Agregar el gel separador en el molde, b) Nivelación de la superficie del gel con agua, c) Agregar el gel concentrador, d) Colocación de peines para formar los pozos.
9 27 Una vez que polimerizó la mezcla se descartó el agua inclinando el molde ensamblado. Posteriormente, se agregó el persulfato de amonio a la mezcla correspondiente al gel concentrador. Inmediatamente después se agregó la mezcla en el interior de los moldes y se colocaron los peines para la formación de los pocillos para la carga de las muestras. Se dejaron polimerizar durante 20 minutos aproximadamente. Una vez que polimerizó el gel concentrador se retiraron los peines deslizándolos suavemente hacia arriba. Los geles formados se enjuagaron depositando agua desionizada en el interior del casete para eliminar los residuos no polimerizados. Aplicación de Muestra y Desarrollo Electroforético En el caso de la SDS-PAGE es necesario lograr una completa desnaturalización de las proteínas, para evitar la aparición de bandas fantasmas en la electroforesis. Las muestras de proteína se disolvieron en una solución reguladora con ph de 6.8 (búfer de muestra 2x) en el que contiene SDS, 2-mercaptoetanol para reducir los puentes disulfuro, azul de bromo fenol y glicerol. Se prepara colocando 2µL de muestra por 80µL de búfer de muestra 2x.
10 28 Una vez polimerizados los geles se realizó la carga de las muestras. En la Figura 5 se describe el procedimiento usado para el montaje, carga de muestra y corrida electroforética. Los casetes con los geles polimerizados se desmontaron y se colocaron en el soporte con electrodos. Después se insertó la guía para la carga de muestra, las cuales fueron agregadas en cada pocillo utilizando una micropipeta con puntillas especiales para cargar la muestra colocando hasta 20 µl. Una vez cargadas las muestras, el soporte se colocó dentro de la cámara de corrida y se llenó, incluyendo el interior del soporte de los geles, con solución búfer reguladora la cual contiene glicina (concentraciones en anexo A), Trizma base y SDS (búfer para corrida 1x). Los electrodos se conectaron a la fuente de poder después de colocar la tapa sobre la cámara de desarrollo. Para iniciar el desarrollo electroforético, se energizó l a fuente de poder aplicando una corriente eléctrica de 100 Volts, manteniéndola constante durante 2 h. aproximadamente o hasta que el frente de la corrida alcanzó el borde inferior del gel. Es importantela uniformidad de temperatura a través del gel mientr as ocurre la corrida electroforética, generalmente elimina el efecto de deformación de las bandas en forma de sonrisa 10.
11 29 a b c d e f Figura 5. Montaje, carga de muestra y desarrollo electroforético. a) desmontado de los casetes del marco, b) colocación del casete en el soporte con electrodos, c) introducción del porta electrodos en el bastidor, d) colocación de guías y carga de muestra, e) montaje del bastidor dentro del mini tanque, f) llenado de la cámara de desarrollo y conexión de electrodos para iniciar la corrida.
12 30 Revelado de los Geles de SDS-PAGE Una rápida tinción, destinción y fijación son esenciales en el caso de las proteínas pequeñas para evitar su elución, la omisión del metanol de la solución de tinción es beneficiosa ya que se reduce el tiempo de tinción y evita el hinchamiento de los geles. 14. Cuando se ha completado una electroforesis, las moléculas más pequeñas han llegado al ánodo, entonces se pueden 'revelar' mediante la adición de un colorante específico para hacerlas visibles. Se emplean compuestos como el bromuro de etidio, para los ácidos nucléicos, o tinción de plata, azul de COOMASSIE o tinción fluorescente, para las proteínas. El colorante azul de COOMASSIE es generalmente el más aceptado para el revelado de geles de ele ctroforesis. se une a las proteínas y la intensidad de coloración es relativamente hasta cierto punto independiente de la concentración y naturaleza química de las proteínas, de esta forma cuando se tiene que cuantificar una proteína es el colorante mas recomendado. Por otra parte la tinción con nitrato de plata tiene una detección de concentraciones más pequeñas que varía entre 2 a 5
13 31 ɳg. sin embargo detección con plata es exclusivamente cualitativa y no puede ser utilizada para cuantificar proteínas. Para la tinción con Azul de COOMASSIE se utilizó una solución de tinción compuesta por metanol (50%), ácido acético (10%), agua destilada (40%) y 0.05 % p/v de Azul de COOMASSIE, mientras que la solución uno para desteñido consistió de la misma mezcla con excepción del colorante, y la solución dos para desteñido consistió de una mezcla de agua des ionizada (88%) ácido acético (7%) y metanol (5%). Una vez concluida la corrida electroforética, se inició el procedimiento de revelado de los geles como se muestra en la Figura 6. Primeramente se retiraron los geles de los cristales depositándolos en un recipiente de plástico descartando el gel concentrador y dejando el gel separador para su tinción. Se agregó la solución para tinción de Azul de COOMASSIE procurando que el gel quedará totalmente sumergido. Para evitar los gases y olores que se desprenden, el recipiente de plástico se tapó y se colocó sobre la placa de agitación orbital, y agitándose por 12h o dejándolo por un periodo de 12 h (overnight).
14 32 Después del tiempo transcurrido se procedió a realizar el desteñido de los geles. Primeramente se retiró la solución de tinción y se agregó la solución uno de desteñido. Se agitó por espacio de 30 min y posteriormente se cambió la solución uno de desteñido por la solución dos de desteñido, dejándose en agitación por 30 min. en agitador orbital hasta que se observó el gel transparente.
15 33 a b c d e Figura 6. Procedimiento para el revelado de los geles. a) Sumergido de los geles en colorante para la tinción, b) Agitación de los geles en agitador orbital, c) Introducción de los geles teñidos en solución para desteñir, d) Agitación de los geles en agitador orbital, e) Enmicado de los geles en papel celofán dulce listo para su escanear y analizar.
16 34 Una vez terminado el revelado se colocan los geles en papel celofán tranparente en forma de emparedado esto permitirá que el gel se seque sin causar ruptura, deformación, perdida de la transparencia y sin necesidad de emplear calor o presión reducida ni ningún aparato especial para su manipulación, escaneo y almacenaje. 15 Una vez escaneado se hace la comparación con los estándares adecuados. Diseño de la Investigación En este trabajo se evaluaron distintos procedimientos para el revelado de los geles de electroforesis utilizando los colorantes Violeta de Genciana (cloruro de hexametildisilazano -p-rosanilina), Azure A (N',N'-dimethylphenothiazin-5-ium-3,7-diamine), Azul Indigo 23 (2,2'-Bis(2,3-dihydro-3- oxoindolyliden), con el fin de investigar la capacidad de resolución en el revelado de geles SDS-PAGE. Como colorante control se utilizó al Azul d e COOMASSIE, ya que es que describe el método de referencia para poder lograr su comparación. En la Tabla 2 se describen las características de los colorantes utilizados en la presente investigación.
17 35 Tabla 2. Características de los colorantes utilizados Nombre del colorante Estructura química Formula Molecular color Solubilidad Azul de coomassie Azul brillante Etanol C 45 H 44 N 3 NaO 7 S 2 Violeta de genciana C 24 H 28 N 3 Cl Violeta intenso Agua Azure A C 14 H 14 ClN 3 S Café obscuro Agua Azul mezclilla 23 C 16 H 10 N 2 O 2 Azul cristalino Agua
18 36 Análisis de Muestras de Suero Con la finalidad de trabajar con muestras de interés clínico, se utilizaron muestras de suero sanguíneo, probando la gran cantidad de resultados que se pueden obtener a partir de este tipo de muestras, ya sea en los laboratorios clínicos o de investigación. Las muestras de suero fresco, se desnaturalizaron mediante calentamiento en baño maría por un tiempo de 30 segundos. Se trasvasa una alícuota de 2 L a un tubo de Eppendorf y se adicionó 80 L el búfer de muestra 2x. Experimentos de Validación de la Metodología Una vez definida la técnica para el desarrollo y tinción de muestras de proteína por SDS-PAGE se procedió a la validación del método establecido aplicando las siguientes pruebas de control de calidad. Linealidad Con el fin de obtener el intervalo dinámico lineal, en este trabajo se realizaron corridas con muestras de suero humano (5
19 37 %v/v) y BSA (0.625 mg/ml) a diferentes volúmenes de carga (0, 5, 8, 10, 15 y 20 L) para la detección de las bandas de proteínas respectivamente. Para estos experimentos se utilizaron los distintos colorantes antes descritos, siguiendo los mismos procedimientos de tinción. Los geles fueron escaneados y analizados por densitocolorimetría en el programa de cómputo Image J (NIH, institute), determinando el área bajo la curva de los respectivos electrograma. Posteriormente los datos fueron analizados por regresión lineal en el programa Excel (Microsoft Office 2010). Límite de detección Las cantidades de proteína cargadas en cada pozo fueron del orden de microgramos. Para estos experimentos se utilizaron los distintos colorantes antes descritos, siguiendo los mismos procedimientos de tinción para determinar la cantidad mínima detectable por cada uno de los colorantes. Se analizó la capacidad de detección del método de tinción a diferentes concentraciones de muestra utilizando suero humano y BSA a distintas concentraciones indicando una relación lineal a las diferentes concentraciones. Cuando el análisis densito colorimétrico no produjo un pico cuantificable se estableció la cantidad mínima detectable.
20 38 Reproducibilidad Con el fin de lograr una reproducibilidad comparable con otros métodos, además de que se arrojen resultados confiables. Se realizaron corridas utilizando diferentes concentraciones de muestra con distintos colorantes. Se analizo la capacidad de reproducibilidad del método a diferentes concentraciones de muestra y colorantes, obteniendo resultados iguales en la s repeticiones realizadas, de esta forma se logra realizar la reproducibilidad de este método, logrando un análisis confiable en la detección de proteínas por medio de revelados de geles de electroforesis SDS-PAGE.
RESULTADOS Y DISCUSIONES. El análisis por medio de electroforesis a demostrado ser uno de los
 39 RESULTADOS Y DISCUSIONES El análisis por medio de electroforesis a demostrado ser uno de los mejores métodos de separación para complejos proteicos, además de necesitar cantidades muy pequeñas de muestra.
39 RESULTADOS Y DISCUSIONES El análisis por medio de electroforesis a demostrado ser uno de los mejores métodos de separación para complejos proteicos, además de necesitar cantidades muy pequeñas de muestra.
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE 1. FUNDAMENTO TEÓRICO La electroforesis es una técnica de
Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE 1. FUNDAMENTO TEÓRICO La electroforesis es una técnica de
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa
 MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa.
 MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa. Qué es la electroforesis? Es la técnica que permite la
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa. Qué es la electroforesis? Es la técnica que permite la
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 1. FUNDAMENTO TEÓRICO ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE Departamento de Bioquímica La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo
1. FUNDAMENTO TEÓRICO ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE Departamento de Bioquímica La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo
Monitoreo de un proceso de purificación de proteínas. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa
 Monitoreo de un proceso de purificación de proteínas Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
Monitoreo de un proceso de purificación de proteínas Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
ANEXOS A: Procedimientos experimentales
 ANEXOS 1 ANEXOS A: Procedimientos experimentales SDS-TRIS-GLICINA-PAGE Procedimiento A.1. Descripción del método de preparación de geles de poliacrilamida. Se trata de un sistema vertical de electroforesis,
ANEXOS 1 ANEXOS A: Procedimientos experimentales SDS-TRIS-GLICINA-PAGE Procedimiento A.1. Descripción del método de preparación de geles de poliacrilamida. Se trata de un sistema vertical de electroforesis,
Introducción. Electroforesis zonal Campo aplicado a un soporte estabilizante Muestra dispuesta sobre una zona reducida del soporte
 Introducción Técnica analítica separativa: Transporte de moléculas cargadas bajo la acción de un campo eléctrico Movilidad electroforética depende de: La carga de la molécula Depende del medio ph Fuerza
Introducción Técnica analítica separativa: Transporte de moléculas cargadas bajo la acción de un campo eléctrico Movilidad electroforética depende de: La carga de la molécula Depende del medio ph Fuerza
Electroforesis de proteínas en geles de poliacrilamida
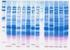 Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 1 Virología y Micología Veterinaria Trabajo Práctico No. 4 ELECTROFORESIS La electroforesis es una técnica utilizada para separar grandes moléculas por tamaño a través de la aplicación de un campo eléctrico
1 Virología y Micología Veterinaria Trabajo Práctico No. 4 ELECTROFORESIS La electroforesis es una técnica utilizada para separar grandes moléculas por tamaño a través de la aplicación de un campo eléctrico
Diagnóstico Avanzado en Enfermedades Tropicales
 Diagnóstico Avanzado en Enfermedades Tropicales Máster universitario en Enfermedades Tropicales Código 302731 (3 créditos ECTS) Área de Parasitología Departamento de Biología Animal, Parasitología, Ecología,
Diagnóstico Avanzado en Enfermedades Tropicales Máster universitario en Enfermedades Tropicales Código 302731 (3 créditos ECTS) Área de Parasitología Departamento de Biología Animal, Parasitología, Ecología,
Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon.
 Biología Celular y Molecular para Medicina Jorge Contreras Pineda Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon. GENERALIDADES La electroforesis es una técnica de laboratorio
Biología Celular y Molecular para Medicina Jorge Contreras Pineda Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon. GENERALIDADES La electroforesis es una técnica de laboratorio
ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B
 ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B 2 0 1 7 Que es la electroforesis? Qué permite analizar? Que factores influyen? Separar y analizar
ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B 2 0 1 7 Que es la electroforesis? Qué permite analizar? Que factores influyen? Separar y analizar
BIOLOGIA CELULAR Y MOLECULAR. LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE)
 BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE) 1. INTRODUCCIÓN Uno de los métodos que permite la purificación y separación de proteínas de un organismo
BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE) 1. INTRODUCCIÓN Uno de los métodos que permite la purificación y separación de proteínas de un organismo
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987)
 EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS. Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo (+)
 GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS Electroforésis Separación de especies cargadas (anión (-) y catión (+) ) Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo
GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS Electroforésis Separación de especies cargadas (anión (-) y catión (+) ) Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo
 TRABAJO PRACTICO Nº 3. PROTEINAS Y ENZIMAS. www.fcn.unp.edu.ar/sitio/farmacognosia/ Objetivo - Utilizar reacciones generales y técnicas de extracción y separación adecuadas para el análisis de proteínas
TRABAJO PRACTICO Nº 3. PROTEINAS Y ENZIMAS. www.fcn.unp.edu.ar/sitio/farmacognosia/ Objetivo - Utilizar reacciones generales y técnicas de extracción y separación adecuadas para el análisis de proteínas
Evaluación de Procedimientos de Tinción para el Análisis de Proteínas por Electroforesis (SDS-PAGE)
 INVURNUS En busca del conocimiento Universidad de Sonora Campus Centro Campus Caborca Volumen 8 No. 1 (Enero-Junio 2013): 19-26 INVESTIGACIÓN Evaluación de Procedimientos de Tinción para el Análisis de
INVURNUS En busca del conocimiento Universidad de Sonora Campus Centro Campus Caborca Volumen 8 No. 1 (Enero-Junio 2013): 19-26 INVESTIGACIÓN Evaluación de Procedimientos de Tinción para el Análisis de
TP3: Electroforesis en gel de poliacrilamida
 TP3: Electroforesis en gel de poliacrilamida Objetivos Comparar las fracciones de proteínas obtenidas en el TP Nº2 mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas.
TP3: Electroforesis en gel de poliacrilamida Objetivos Comparar las fracciones de proteínas obtenidas en el TP Nº2 mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas.
METODOLOGÍA EXPERIMENTAL. Los reactivos utilizados en este trabajo fueron los siguientes y las soluciones se
 METODOLOGÍA EXPERIMENTAL Materiales y reactivos: Los reactivos utilizados en este trabajo fueron los siguientes y las soluciones se prepararon con agua desionizada: Acetato de celulosa (AC), marca Aldrich;
METODOLOGÍA EXPERIMENTAL Materiales y reactivos: Los reactivos utilizados en este trabajo fueron los siguientes y las soluciones se prepararon con agua desionizada: Acetato de celulosa (AC), marca Aldrich;
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDS-PAGE. Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE)
 ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
Electroforesis de proteínas
 Electroforesis de proteínas Introducción general La electroforesis es un método de separación basado en la tasa diferencial de migración de especies cargadas al estar en un campo eléctrico de DC La electroforesis
Electroforesis de proteínas Introducción general La electroforesis es un método de separación basado en la tasa diferencial de migración de especies cargadas al estar en un campo eléctrico de DC La electroforesis
MATERIALES Y MÉTODOS. Tipo de Estudio. Muestra
 MATERIALES Y MÉTODOS Tipo de Estudio Experimental. Este tipo de estudio tiene como característica primordial el poder manipular y controlar las variables, siendo en este caso la fuerza iónica y el ph.
MATERIALES Y MÉTODOS Tipo de Estudio Experimental. Este tipo de estudio tiene como característica primordial el poder manipular y controlar las variables, siendo en este caso la fuerza iónica y el ph.
qprotein (BCA) Kit para cuantificar proteinas totales PB-L Productos Bio-Lógicos
 qprotein () Kit para cuantificar proteinas totales PB-L http://www.pb-l.com.ar qprotein () Cat. no. RA03 CONTENIDO Componentes RA0301 RA0302 Buffer A 250 ml 500 ml Buffer B 5 ml 10 ml Proteína Patrón 5
qprotein () Kit para cuantificar proteinas totales PB-L http://www.pb-l.com.ar qprotein () Cat. no. RA03 CONTENIDO Componentes RA0301 RA0302 Buffer A 250 ml 500 ml Buffer B 5 ml 10 ml Proteína Patrón 5
Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS
 Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS DICIEMBRE 2006 Tratamiento de Imágenes por Computadora Proyecto
Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS DICIEMBRE 2006 Tratamiento de Imágenes por Computadora Proyecto
TP3: Electroforesis en gel de poliacrilamida
 Objetivos TP3: Electroforesis en gel de poliacrilamida Comparar los perfiles proteicos obtenidos mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas. Introducción La
Objetivos TP3: Electroforesis en gel de poliacrilamida Comparar los perfiles proteicos obtenidos mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas. Introducción La
ESPECTROSCOPIA UV-VISIBLE
 ESPECTROSCOPIA UV-VISIBLE FUNDAMENTOS INSTRUMENTACION FUNCIONAMIENTO APLICACIONES FUNDAMENTOS La espectroscopia UV-Vis está basada en el proceso de absorción de la radiación ultravioleta-visible (radiación
ESPECTROSCOPIA UV-VISIBLE FUNDAMENTOS INSTRUMENTACION FUNCIONAMIENTO APLICACIONES FUNDAMENTOS La espectroscopia UV-Vis está basada en el proceso de absorción de la radiación ultravioleta-visible (radiación
Determinación de Sulfatos en Aguas
 QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Sulfatos en Aguas Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 22/09/2013 Descripción del método de determinación de
QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Sulfatos en Aguas Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 22/09/2013 Descripción del método de determinación de
DETERMINACIÓN DEL PESO MOLECULAR DE PROTEÍNAS
 DETERMINACIÓN DEL PESO MOLECULAR DE PROTEÍNAS 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar el conocimiento de la estructura de las proteínas y determinar
DETERMINACIÓN DEL PESO MOLECULAR DE PROTEÍNAS 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar el conocimiento de la estructura de las proteínas y determinar
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar
 4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
Baños de bloque Bloques Electroforesis Otros Biología Molecular PCR Separación y recogida de células. Cromakit, S.L. Biologia Molecular
 Baños de bloque Bloques Electroforesis Otros Biología Molecular PCR Separación y recogida de células Cromakit, S.L. Biologia Molecular Contenido Baños de bloque 4 Bloques 6 Electroforesis 10 Cubetas electroforesis
Baños de bloque Bloques Electroforesis Otros Biología Molecular PCR Separación y recogida de células Cromakit, S.L. Biologia Molecular Contenido Baños de bloque 4 Bloques 6 Electroforesis 10 Cubetas electroforesis
PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA
 INTRODUCCIÓN PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA La electroforesis es una técnica que permite separar moléculas cargadas eléctricamente, entre las cuales se encuentran los ácidos nucleicos (DNA
INTRODUCCIÓN PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA La electroforesis es una técnica que permite separar moléculas cargadas eléctricamente, entre las cuales se encuentran los ácidos nucleicos (DNA
Electroforesis. Dr. Héctor L. Ayala del Río AMGEN Bruce Wallace Program Departamento de Biología UPR-Humacao VER VIDEO CARGADO GEL
 Electroforesis Dr. Héctor L. Ayala del Río AMGEN Bruce Wallace Program Departamento de Biología UPR-Humacao VER VIDEO CARGADO GEL 1 Electroforesis l Método utilizado para separar y purificar macromoléculas:
Electroforesis Dr. Héctor L. Ayala del Río AMGEN Bruce Wallace Program Departamento de Biología UPR-Humacao VER VIDEO CARGADO GEL 1 Electroforesis l Método utilizado para separar y purificar macromoléculas:
Guía de TP Nro. 5 Actividad Proteolítica Celular
 Biología Celular y Molecular Guía de TP Nro. 5 Actividad Proteolítica Celular Introducción La actividad proteolítica secretada por las células es un elemento indispensable para la proliferación y migración
Biología Celular y Molecular Guía de TP Nro. 5 Actividad Proteolítica Celular Introducción La actividad proteolítica secretada por las células es un elemento indispensable para la proliferación y migración
PRÁCTICA # 01 PREPARACIÓN DE DISOLUCIONES
 REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
TÉCNICAS DE ANÁLISIS GENÉTICO: Extracción de ADN.
 Trabajo Práctico 2.2 TÉCNICAS DE ANÁLISIS GENÉTICO: Extracción de ADN. Desde el reconocimiento del ADN como "la molécula de la vida", se conoce que en ella se encuentran cifradas las instrucciones que
Trabajo Práctico 2.2 TÉCNICAS DE ANÁLISIS GENÉTICO: Extracción de ADN. Desde el reconocimiento del ADN como "la molécula de la vida", se conoce que en ella se encuentran cifradas las instrucciones que
ELECTROFORESIS. Objetivo de la clase. *fundamentos *procedimientos *algunas aplicaciones. Conocer los métodos electroforéticos
 ELECTROFORESIS Objetivo de la clase Conocer los métodos electroforéticos *fundamentos *procedimientos *algunas aplicaciones Definición de electroforesis Proceso de separación que se basa en la diferente
ELECTROFORESIS Objetivo de la clase Conocer los métodos electroforéticos *fundamentos *procedimientos *algunas aplicaciones Definición de electroforesis Proceso de separación que se basa en la diferente
PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG. 1 de 20 2 de 10 1 moneda de 1 10 monedas monedas monedas de 0.
 PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG Para saber lo que tengo debo separar las partes y cuantificar 1 de 20 2 de 10 1 moneda de 1 10 monedas 0.20 4 monedas 0.10 3 monedas
PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG Para saber lo que tengo debo separar las partes y cuantificar 1 de 20 2 de 10 1 moneda de 1 10 monedas 0.20 4 monedas 0.10 3 monedas
Ensayos de restricción
 Ensayos de restricción Vector con inserto= Vector recombinante 6500pb Objetivos de ensayos de restricción de plásmidos Conocer el principio de separación y detección de ácidos nucleicos en geles de agarosa.
Ensayos de restricción Vector con inserto= Vector recombinante 6500pb Objetivos de ensayos de restricción de plásmidos Conocer el principio de separación y detección de ácidos nucleicos en geles de agarosa.
Laboratorio: Deteccio n de biomole culas orga nicas (Carbohidratos, Proteí nas, Grasas)
 Laboratorio: Deteccio n de biomole culas orga nicas (Carbohidratos, Proteí nas, Grasas) Introducción Las biomoléculas son las moléculas constituyentes de los seres vivos. Los seis elementos o bioelementos
Laboratorio: Deteccio n de biomole culas orga nicas (Carbohidratos, Proteí nas, Grasas) Introducción Las biomoléculas son las moléculas constituyentes de los seres vivos. Los seis elementos o bioelementos
ANEXOS. Anexo 1. Solución Reguladora de Acetato 0.1 M, ph 4.0 y metanol al 2% (v/v).
 ANEXOS Anexo 1 Solución Reguladora de Acetato 0.1 M, ph 4.0 y metanol al 2% (v/v). 1. Tomar 6.011mL de ácido acético y aforar a 1L de agua HPLC. 2. Pesar 13.609 g de acetato de sodio y aforar a 1L de agua
ANEXOS Anexo 1 Solución Reguladora de Acetato 0.1 M, ph 4.0 y metanol al 2% (v/v). 1. Tomar 6.011mL de ácido acético y aforar a 1L de agua HPLC. 2. Pesar 13.609 g de acetato de sodio y aforar a 1L de agua
Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa
 Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa OBJETIVO: -Realizar electroforesis de las proteínas presentes en suero utilizando acetato de celulosa
Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa OBJETIVO: -Realizar electroforesis de las proteínas presentes en suero utilizando acetato de celulosa
Determinación de Fósforo Asimilable en Suelos Método de Bray Kurtz
 QUÍMICA ANALITICA APLICADA INORGÁNICA QMC-613 Determinación de Fósforo Asimilable en Suelos Método de Bray Kurtz Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 21/10/2013 Método de
QUÍMICA ANALITICA APLICADA INORGÁNICA QMC-613 Determinación de Fósforo Asimilable en Suelos Método de Bray Kurtz Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 21/10/2013 Método de
Separación e identificación de lípidos de membrana
 Separación e identificación de lípidos de membrana Objetivos Separación e identificación de especies de fosfolípidos por cromatografía de capa fina (TLC, Thin Layer Chromatography) TLC monodimensional
Separación e identificación de lípidos de membrana Objetivos Separación e identificación de especies de fosfolípidos por cromatografía de capa fina (TLC, Thin Layer Chromatography) TLC monodimensional
ELECTROFORESIS AVANZADA
 Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
5 DESARROLLO EXPERIMENTAL
 5 DESARROLLO EXPERIMENTAL 5.1 SÍNTESIS DE NANOFIBRAS DE TIO2 Para la síntesis de las nanofibras de TiO2 se ocuparon dos métodos distintos, en la cual la variante principal era el peso molecular y la proporción
5 DESARROLLO EXPERIMENTAL 5.1 SÍNTESIS DE NANOFIBRAS DE TIO2 Para la síntesis de las nanofibras de TiO2 se ocuparon dos métodos distintos, en la cual la variante principal era el peso molecular y la proporción
III. ESTUDIO DE CASO: INDUSTRIA PAPELERA
 III. ESTUDIO DE CASO: INDUSTRIA PAPELERA 3.1 Proceso de Fabricación más común del Papel La industria para la producción de papel se realiza a partir de la madera, mediante su trituración, tanto mecánica
III. ESTUDIO DE CASO: INDUSTRIA PAPELERA 3.1 Proceso de Fabricación más común del Papel La industria para la producción de papel se realiza a partir de la madera, mediante su trituración, tanto mecánica
Código: KIT-005 Ver: 1 MTHFR C677T
 Sistema para detección de la alteración C677T en el gene que codifica para la Metilen-tetrahidrofolato reductasa humana 1 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598)
Sistema para detección de la alteración C677T en el gene que codifica para la Metilen-tetrahidrofolato reductasa humana 1 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598)
MATERIALES Y MÉTODOS. Cepa de Mycobacterium tuberculosis
 MATERIALES Y MÉTODOS Cepa de Mycobacterium tuberculosis Se utilizó una cepa de referencia de Mycobacterium tuberculosis H37Rv tipificada en el Instituto Nacional de Diagnóstico y Referencia Epidemiológica
MATERIALES Y MÉTODOS Cepa de Mycobacterium tuberculosis Se utilizó una cepa de referencia de Mycobacterium tuberculosis H37Rv tipificada en el Instituto Nacional de Diagnóstico y Referencia Epidemiológica
FICHA TÉCNICA RESINA ACRÍLICA AUTOPOLIMERIZABLE DPFTPT-020
 1 GENERALIDADES DEL PRODUCTO Los polímeros de metacrilato han tenido gran popularidad en la odontología porque se procesan con facilidad utilizando técnicas relativamente sencillas, tienen la capacidad
1 GENERALIDADES DEL PRODUCTO Los polímeros de metacrilato han tenido gran popularidad en la odontología porque se procesan con facilidad utilizando técnicas relativamente sencillas, tienen la capacidad
Biología Celular y Molecular. Guía de TP Nro. 5. Actividad proteolítica celular.
 Biología Celular y Molecular. Guía de TP Nro. 5 Actividad proteolítica celular. Introducción La actividad proteolítica secretada por las células es un elemento indispensable para la proliferación y migración
Biología Celular y Molecular. Guía de TP Nro. 5 Actividad proteolítica celular. Introducción La actividad proteolítica secretada por las células es un elemento indispensable para la proliferación y migración
PRACTICA DE LABORATORIO SEMANA 19 y 20 PROPIEDADES FÍSICAS Y QUÍMICAS DE ALCOHOLES Y FENOLES Elaborado por: Licda. Lilian Judith Guzmán Melgar
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MEDICAS-CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO PRACTICA DE LABORATORIO 2016 SEMANA 19 y 20 PROPIEDADES FÍSICAS Y QUÍMICAS DE ALCOHOLES Y FENOLES
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MEDICAS-CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO PRACTICA DE LABORATORIO 2016 SEMANA 19 y 20 PROPIEDADES FÍSICAS Y QUÍMICAS DE ALCOHOLES Y FENOLES
OBJETIVO LINEAMIENTOS DE OPERACIÓN
 OBJETIVO ESTRATEGICO: Coadyuvar a la disminución de accidentes en las vías generales de comunicación, mediante la implementación de políticas, normas y programas en materia de protección y medicina preventiva
OBJETIVO ESTRATEGICO: Coadyuvar a la disminución de accidentes en las vías generales de comunicación, mediante la implementación de políticas, normas y programas en materia de protección y medicina preventiva
DETERMINACIÓN POR DESTILACIÓN DEL LIGANTE RESIDUAL Y DEL FLUIDIFICANTE EN LAS EMULSIONES BITUMINOSAS UNE-EN 1431:2009
 DETERMINACIÓN POR DESTILACIÓN DEL LIGANTE RESIDUAL Y DEL FLUIDIFICANTE EN LAS EMULSIONES BITUMINOSAS UNE-EN 1431:2009 PT-03 Rev. 0 Fecha: Junio 2017 Redactado GT1 ATEB Aprobado COMITÉ TÉCNICO ATEB Página
DETERMINACIÓN POR DESTILACIÓN DEL LIGANTE RESIDUAL Y DEL FLUIDIFICANTE EN LAS EMULSIONES BITUMINOSAS UNE-EN 1431:2009 PT-03 Rev. 0 Fecha: Junio 2017 Redactado GT1 ATEB Aprobado COMITÉ TÉCNICO ATEB Página
MMP. MÉTODOS DE MUESTREO Y PRUEBA DE MATERIALES
 LIBRO: PARTE: TÍTULO: CAPÍTULO: MMP. MÉTODOS DE MUESTREO Y PRUEBA DE MATERIALES 2. MATERIALES PARA ESTRUCTURAS 02. Materiales para Concreto Hidráulico 026. Impurezas Orgánicas en Agregados Finos A. CONTENIDO
LIBRO: PARTE: TÍTULO: CAPÍTULO: MMP. MÉTODOS DE MUESTREO Y PRUEBA DE MATERIALES 2. MATERIALES PARA ESTRUCTURAS 02. Materiales para Concreto Hidráulico 026. Impurezas Orgánicas en Agregados Finos A. CONTENIDO
Código: IDK-006 Ver: 1 MTHFR A1298C. Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa
 Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa Reg. MSP 21199 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336
Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa Reg. MSP 21199 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336
CYP 2C9 A1075C CYP2C9*3
 CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
Código: IDK-003 Ver: 1. Factor V Leiden
 Sistema para detección de la alteración G1691A en el gene que codifica para el Factor V de la coagulación humana Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71
Sistema para detección de la alteración G1691A en el gene que codifica para el Factor V de la coagulación humana Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71
velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz porosa
 INTRODUCCIÓN En general, la electroforesis es una técnica que separa las moléculas en base a sus diferentes velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz
INTRODUCCIÓN En general, la electroforesis es una técnica que separa las moléculas en base a sus diferentes velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz
Los principales mecanismos que intervienen en la separación cromatográfica son:
 TP 8 CROMATOGRAFIA EN PAPEL, Introducción Los métodos cromatográficos son un conjunto de técnicas empleadas para separar compuestos químicos de una mezcla. Su nombre significa escribir con color ya que
TP 8 CROMATOGRAFIA EN PAPEL, Introducción Los métodos cromatográficos son un conjunto de técnicas empleadas para separar compuestos químicos de una mezcla. Su nombre significa escribir con color ya que
FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA ÁREA QUÍMICA GENERAL
 FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA ÁREA QUÍMICA GENERAL PRUEBAS DE CARACTERIZACIÓN DE ALCOHOLES Guía No: 07 Páginas: 1 a 7 1. INTRODUCCIÓN El grupo funcional
FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA ÁREA QUÍMICA GENERAL PRUEBAS DE CARACTERIZACIÓN DE ALCOHOLES Guía No: 07 Páginas: 1 a 7 1. INTRODUCCIÓN El grupo funcional
COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE
 COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE PRACTICA # 1 CAMBIOS QUÍMICOS OBJETIVO DE LA PRÁCTICA: Identificar que los cambios químicos están acompañados
COLEGIO DE BACHILLERES PLANTEL 5 SATÉLITE PRÁCTICAS DE LABORATORIO QUÍMICA II TERCER SEMESTRE PRACTICA # 1 CAMBIOS QUÍMICOS OBJETIVO DE LA PRÁCTICA: Identificar que los cambios químicos están acompañados
INTRODUCCIÓN: Las proteínas son precipitadas de sus soluciones por ciertos ácidos tales como Zn +++, Hg ++, Fe ++, Cu ++ y Pb ++.
 INTRODUCCIÓN: Las proteínas pueden formar soluciones estables debido a las cargas de hidratación de las moléculas de proteína y a las cargas eléctricas que ellas poseen. Las proteínas ligan agua por formación
INTRODUCCIÓN: Las proteínas pueden formar soluciones estables debido a las cargas de hidratación de las moléculas de proteína y a las cargas eléctricas que ellas poseen. Las proteínas ligan agua por formación
Práctica 15. Cinética química.
 Materiales Vasos de precipitados Vidrio de reloj Varilla agitadora Matraces aforados Tubos de ensayo Tapones Gradilla Balanza Placa calefactora Reactivos Bisulfato sódico Agua destilada Almidón soluble
Materiales Vasos de precipitados Vidrio de reloj Varilla agitadora Matraces aforados Tubos de ensayo Tapones Gradilla Balanza Placa calefactora Reactivos Bisulfato sódico Agua destilada Almidón soluble
CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:
 CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:55-2231189 WWW.LICEOINDUSTRIALEGM.CL GUÍA DE APRENDIZAJE Profesor Asignatura Objetivo de Aprendizaje
CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:55-2231189 WWW.LICEOINDUSTRIALEGM.CL GUÍA DE APRENDIZAJE Profesor Asignatura Objetivo de Aprendizaje
UNIVERSIDAD TECNOLÓGICA EQUINOCCIAL Laboratorio de Química. MEDICIÓN DEL ph DE ÁCIDOS, BASES Y SALES 2. INTRODUCCIÓN
 UNIVERSIDAD TECNOLÓGICA EQUINOCCIAL Laboratorio de Química 1 MEDICIÓN DEL ph DE ÁCIDOS, BASES Y SALES 1. OBJETIVOS. Reconocer la acidez o basicidad de una sustancia mediante el uso de indicadores. Relacionar
UNIVERSIDAD TECNOLÓGICA EQUINOCCIAL Laboratorio de Química 1 MEDICIÓN DEL ph DE ÁCIDOS, BASES Y SALES 1. OBJETIVOS. Reconocer la acidez o basicidad de una sustancia mediante el uso de indicadores. Relacionar
CARRERA DE ESPECIALIZACION EN BIOTECNOLOGIA INDUSTRIAL FCEyN-INTI Materia de Especialización CEBI_E1b Técnicas de análisis en biotecnología
 CARRERA DE ESPECIALIZACION EN BIOTECNOLOGIA INDUSTRIAL FCEyN-INTI Materia de Especialización CEBI_E1b Técnicas de análisis en biotecnología Macromoléculas Docente a cargo: SANTAGAPITA, Patricio CEBI_E1b_2
CARRERA DE ESPECIALIZACION EN BIOTECNOLOGIA INDUSTRIAL FCEyN-INTI Materia de Especialización CEBI_E1b Técnicas de análisis en biotecnología Macromoléculas Docente a cargo: SANTAGAPITA, Patricio CEBI_E1b_2
Evaluación de la metodología analítica utilizada para determinar Fósforo Extraíble en muestras de Suelos Ing. Agr. Valeria Bortolotti
 Evaluación de la metodología analítica utilizada para determinar Fósforo Extraíble en muestras de Suelos Ing. Agr. Valeria Bortolotti Comisión de Suelos A.L.A.P. Asociación de Laboratorios Agropecuarios
Evaluación de la metodología analítica utilizada para determinar Fósforo Extraíble en muestras de Suelos Ing. Agr. Valeria Bortolotti Comisión de Suelos A.L.A.P. Asociación de Laboratorios Agropecuarios
ANÁLISIS DE CLORUROS
 Página 1 de 6 1. OBJETIVO Realizar el análisis de cloruros en el agua cruda (Río Guadalajara), en los tanques de almacenamiento que distribuyen agua a la red de distribución y en los puntos fijos de la
Página 1 de 6 1. OBJETIVO Realizar el análisis de cloruros en el agua cruda (Río Guadalajara), en los tanques de almacenamiento que distribuyen agua a la red de distribución y en los puntos fijos de la
REALIZACION DE CURVAS DE CALIBRACIÓN PARA PROTEÍNAS Y AZÚCARES REDUCTORES.
 REALIZACION DE CURVAS DE CALIBRACIÓN PARA PROTEÍNAS Y AZÚCARES REDUCTORES. INTRODUCCIÓN Existen dos facetas de calibración en el análisis cualitativo, la calibración instrumental y la calibración metodológica.
REALIZACION DE CURVAS DE CALIBRACIÓN PARA PROTEÍNAS Y AZÚCARES REDUCTORES. INTRODUCCIÓN Existen dos facetas de calibración en el análisis cualitativo, la calibración instrumental y la calibración metodológica.
Taller de la ronda de aptitud LACOMET-DMF
 Taller de la ronda de aptitud LACOMET-DMF-003-2015 1 Temas a Revisar 1. Antecedentes 2. Objetivos 3. Aspectos Generales de la calibración 1. Características de los equipos a calibrar 2. Equipos y patrones
Taller de la ronda de aptitud LACOMET-DMF-003-2015 1 Temas a Revisar 1. Antecedentes 2. Objetivos 3. Aspectos Generales de la calibración 1. Características de los equipos a calibrar 2. Equipos y patrones
LA ELECTRÓLISIS DE DISOLUCIONES SALINAS (II)
 LA ELECTRÓLISIS DE DISOLUCIONES SALINAS (II) Se van a presentar tres electrólisis en diferentes condiciones y con distintos electrodos, a fin de observar la influencia de estas condiciones en sus resultados
LA ELECTRÓLISIS DE DISOLUCIONES SALINAS (II) Se van a presentar tres electrólisis en diferentes condiciones y con distintos electrodos, a fin de observar la influencia de estas condiciones en sus resultados
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-499-1987. INGENIOS AZUCAREROS. DETERMINACIÓN DE PLOMO EN AZÚCARES BLANCOS Y AZÚCAR MASCABADO O CRUDO. SUGAR MILLS. DETERMINATION OF LEAD IN WHITE SUGARS AND MUSCOVADO SUGAR (RAW SUGAR). NORMAS MEXICANAS.
NMX-F-499-1987. INGENIOS AZUCAREROS. DETERMINACIÓN DE PLOMO EN AZÚCARES BLANCOS Y AZÚCAR MASCABADO O CRUDO. SUGAR MILLS. DETERMINATION OF LEAD IN WHITE SUGARS AND MUSCOVADO SUGAR (RAW SUGAR). NORMAS MEXICANAS.
III. EXPERIMENTACIÓN
 III. EXPERIMENTACIÓN 8. OBJETIVO Se colectaron muestras de aceite vegetal de diferentes negocios de comida rápida con el fin de determinar el costo de producción del biodiesel a partir de éstos y el comportamiento
III. EXPERIMENTACIÓN 8. OBJETIVO Se colectaron muestras de aceite vegetal de diferentes negocios de comida rápida con el fin de determinar el costo de producción del biodiesel a partir de éstos y el comportamiento
DETERMINACIÓN DE FÓSFORO TOTAL EN ALIMENTOS. Método Espectrofotométrico del molibdato de amonio (Basado en Método AOAC N ) ME-711.
 07.05.2009 18.12.2014 Página 1 de 5 OBJETIVO Determinar el contenido de fósforo total en alimentos e ingredientes alimentarios. 1. CAMPO DE APLICACIÓN Y ALCANCE El método es aplicable a alimentos en general,
07.05.2009 18.12.2014 Página 1 de 5 OBJETIVO Determinar el contenido de fósforo total en alimentos e ingredientes alimentarios. 1. CAMPO DE APLICACIÓN Y ALCANCE El método es aplicable a alimentos en general,
Tapas de cajas de petri de plástico de 2 ml o vidrios de reloj de 5 cm de diámetro Puntas para las micropipetas (amarillas y azules)
 Biología Celular y Molecular Médica I Jorge Contreras Pineda Práctica: El uso de las micropipetas OBJETIVO: Conocer las partes y el funcionamiento de las micropipetas; adquirir destreza en la utilización
Biología Celular y Molecular Médica I Jorge Contreras Pineda Práctica: El uso de las micropipetas OBJETIVO: Conocer las partes y el funcionamiento de las micropipetas; adquirir destreza en la utilización
REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA
 REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo de micropipetas
REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo de micropipetas
PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA
 PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo
PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo
Capítulo 4.- Materiales y Proceso de Síntesis
 Capítulo.- Materiales y Proceso de Síntesis..- Descripción general La síntesis química de las nanopartículas tanto metálicas, como semiconductoras, se realiza en soluciones acuosas, controlando variables
Capítulo.- Materiales y Proceso de Síntesis..- Descripción general La síntesis química de las nanopartículas tanto metálicas, como semiconductoras, se realiza en soluciones acuosas, controlando variables
DESARROLLO COGNOSCITIVO Y APRENDIZAJE
 Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
12. POLIFENOLES TOTALES
 42 12. POLIFENOLES TOTALES Introducción Los polifenoles están formados por una o más moléculas de fenol y contribuyen de forma notable en las características organolépticas del vino (color, astringencia,
42 12. POLIFENOLES TOTALES Introducción Los polifenoles están formados por una o más moléculas de fenol y contribuyen de forma notable en las características organolépticas del vino (color, astringencia,
OBJETIVO INTRODUCCIÓN MATERIALES DE MUESTREO. 2. Bolsas plásticas autoclavables. Envases de muestreo 1. Frascos PROGRAMA DE MUESTREO Y MEDICIÓN
 INTRODUCCIÓN CHARLAS TECNICAS Gobierno Regional de Cajamarca TÉCNICAS MICROBIOLÓGICAS PARA LA TOMA DE MUESTRAS DE AGUA DE CONSUMO Blga. Carmen Vargas García Asesora ANEPSSA PERÚ Asesora en Laboratorios
INTRODUCCIÓN CHARLAS TECNICAS Gobierno Regional de Cajamarca TÉCNICAS MICROBIOLÓGICAS PARA LA TOMA DE MUESTRAS DE AGUA DE CONSUMO Blga. Carmen Vargas García Asesora ANEPSSA PERÚ Asesora en Laboratorios
Purificaciónde Inmunoglobulina A, a partir deleche materna para su posible estabilización in vitro
 4 Encuentro de Jóvenes Investigadores CONACYT 11 Coloquio de Jóvenes Talentos en la Investigación Acapulco, Guerrero 21, 21 y 23 de septiembre 2016 Memorias Purificaciónde Inmunoglobulina A, a partir deleche
4 Encuentro de Jóvenes Investigadores CONACYT 11 Coloquio de Jóvenes Talentos en la Investigación Acapulco, Guerrero 21, 21 y 23 de septiembre 2016 Memorias Purificaciónde Inmunoglobulina A, a partir deleche
Laboratorio de Agroindustria II. Calidad de Leche
 Laboratorio de Agroindustria II. Calidad de Leche Medio de cultivo: Caldo lactosado biliado verde brillante (Brilliant Green Bile Lactose: BGBL) Composición - Peptona 10 g. - Lactosa 10 g. - Bilis de buey
Laboratorio de Agroindustria II. Calidad de Leche Medio de cultivo: Caldo lactosado biliado verde brillante (Brilliant Green Bile Lactose: BGBL) Composición - Peptona 10 g. - Lactosa 10 g. - Bilis de buey
Guía de laboratorio: Reconocimiento de moléculas orgánicas.
 Departamento de Ciencias / Biología Primeros medios Prof. Daniela Gutiérrez G. Instrucciones generales: Guía de laboratorio: Reconocimiento de moléculas orgánicas. - Lean con detención cada una de las
Departamento de Ciencias / Biología Primeros medios Prof. Daniela Gutiérrez G. Instrucciones generales: Guía de laboratorio: Reconocimiento de moléculas orgánicas. - Lean con detención cada una de las
PROPIEDADES FÍSICAS Y QUÍMICAS
 PROPIEDADES FÍSICAS Y QUÍMICAS Guía de Química EXPERIMENTO N 5 E.5 Q PROPIEDADES FÍSICAS Y QUÍMICAS OBJETIVO: Identificar las propiedades que presentan los elementos azufre y hierro. EQUIPOS Y REACTIVOS.
PROPIEDADES FÍSICAS Y QUÍMICAS Guía de Química EXPERIMENTO N 5 E.5 Q PROPIEDADES FÍSICAS Y QUÍMICAS OBJETIVO: Identificar las propiedades que presentan los elementos azufre y hierro. EQUIPOS Y REACTIVOS.
TRABAJO PRACTICO Nº 3. PROTEINAS Y ENZIMAS.
 UNIVERSIDAD NACIONAL DE LA PATAGONIA SAN JUAN BOSCO FACULTAD DE CIENCIAS NATURALES DEPARTAMENTO DE FARMACIA CATEDRA DE FARMACOGNOSIA TRABAJO PRACTICO Nº 3. PROTEINAS Y ENZIMAS. Objetivo - Utilizar reacciones
UNIVERSIDAD NACIONAL DE LA PATAGONIA SAN JUAN BOSCO FACULTAD DE CIENCIAS NATURALES DEPARTAMENTO DE FARMACIA CATEDRA DE FARMACOGNOSIA TRABAJO PRACTICO Nº 3. PROTEINAS Y ENZIMAS. Objetivo - Utilizar reacciones
JULIO FASE ESPECÍFICA QUÍMICA. OPCIÓN A
 JULIO 2011. FASE ESPECÍFICA 1. (2,5 puntos) QUÍMICA. OPCIÓN A Calcule la entalpía estándar de formación del metanol líquido a partir de los siguientes datos: ΔHº f [H 2 O(l)] = - 285,5 kj/mol; ΔHº f [CO
JULIO 2011. FASE ESPECÍFICA 1. (2,5 puntos) QUÍMICA. OPCIÓN A Calcule la entalpía estándar de formación del metanol líquido a partir de los siguientes datos: ΔHº f [H 2 O(l)] = - 285,5 kj/mol; ΔHº f [CO
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO
 UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE QUÍMICA ORGÁNICA DETERMINACIÓN DE HALÓGENOS TRABAJO PRÁCTICO Nº:... NOMBRE Y APELLIDO:... FECHA:...
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE QUÍMICA ORGÁNICA DETERMINACIÓN DE HALÓGENOS TRABAJO PRÁCTICO Nº:... NOMBRE Y APELLIDO:... FECHA:...
MATERIALES Y MÉTODOS
 MATERIALES Y MÉTODOS Determinación de las Disoluciones de Análisis y sus Concentraciones Parte I: In 2 S 3 Esta sección del presente trabajo se elaboró en base a la formulación química desarrollada por
MATERIALES Y MÉTODOS Determinación de las Disoluciones de Análisis y sus Concentraciones Parte I: In 2 S 3 Esta sección del presente trabajo se elaboró en base a la formulación química desarrollada por
CROMATOGRAFÍA DE AMINOÁCIDOS
 CROMATOGRAFÍA DE AMINOÁCIDOS Electroforesis.- Es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar aminoácidos (y otras biomoléculas) según su
CROMATOGRAFÍA DE AMINOÁCIDOS Electroforesis.- Es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar aminoácidos (y otras biomoléculas) según su
SEMANA 8 PREPARACIÓN DE SOLUCIONES Elaborado por: Licda. Bárbara Jannine Toledo Chaves
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA QUÍMICA, PRIMER AÑO I. INTRODUCCIÓN PRACTICA DE LABORATORIO 2015 SEMANA 8 PREPARACIÓN DE SOLUCIONES Elaborado por:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA QUÍMICA, PRIMER AÑO I. INTRODUCCIÓN PRACTICA DE LABORATORIO 2015 SEMANA 8 PREPARACIÓN DE SOLUCIONES Elaborado por:
Preparación de agua de dilución :
 La determinación de la Demanda Bioquímica de Oxígeno es una prueba en la que se determina los requerimientos relativos de oxígeno en aguas contaminadas tal como aguas residuales domésticas e industriales,,
La determinación de la Demanda Bioquímica de Oxígeno es una prueba en la que se determina los requerimientos relativos de oxígeno en aguas contaminadas tal como aguas residuales domésticas e industriales,,
UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE AGRONOMIA DEPARTAMENTO DE QUIMICA Y TECNOLOGÍA ASIGNATURA QUIMICA ANALITICA
 UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE AGRONOMIA DEPARTAMENTO DE QUIMICA Y TECNOLOGÍA ASIGNATURA QUIMICA ANALITICA INFORME DE LABORATORIO PRACTICA DE DETERMINACION DE CONDUCTIVIDAD DE ELECTROLITOS
UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE AGRONOMIA DEPARTAMENTO DE QUIMICA Y TECNOLOGÍA ASIGNATURA QUIMICA ANALITICA INFORME DE LABORATORIO PRACTICA DE DETERMINACION DE CONDUCTIVIDAD DE ELECTROLITOS
CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO. Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión
 EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
DETERMINACIÓN DE LA MASA MOLECULAR POR ELEVACIÓN DEL PUNTO DE EBULLICIÓN DE UNA DISOLUCIÓN
 DETERMINACIÓN DE LA MASA MOLECULAR POR ELEVACIÓN DEL PUNTO DE EBULLICIÓN DE UNA DISOLUCIÓN OBJETIVO El alumno determinará la masa molecular de un compuesto puro, por elevación del punto de ebullición de
DETERMINACIÓN DE LA MASA MOLECULAR POR ELEVACIÓN DEL PUNTO DE EBULLICIÓN DE UNA DISOLUCIÓN OBJETIVO El alumno determinará la masa molecular de un compuesto puro, por elevación del punto de ebullición de
ELECTROLISIS DEL CLORURO DE ESTAÑO(II) Fotografía 1
 ELECTROLISIS DEL CLORURO DE ESTAÑO(II) Introducción En esta web, en la sección de Química a la gota y en el apartado electrolisis salinas V (ubicada en el almacén) se ha expuesto, mediante fotografía digital,
ELECTROLISIS DEL CLORURO DE ESTAÑO(II) Introducción En esta web, en la sección de Química a la gota y en el apartado electrolisis salinas V (ubicada en el almacén) se ha expuesto, mediante fotografía digital,
5012 Síntesis de ácido acetilsalicílico (aspirina) a partir de ácido salicílico y anhidrido acético
 NP 5012 Síntesis de ácido acetilsalicílico (aspirina) a partir de ácido salicílico y anhidrido acético CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2)
NP 5012 Síntesis de ácido acetilsalicílico (aspirina) a partir de ácido salicílico y anhidrido acético CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2)
