Módulo I: Moléculas pequeñas. Módulo II: Macromoléculas.
|
|
|
- María del Carmen Ortega Farías
- hace 5 años
- Vistas:
Transcripción
1 CARRERA DE ESPECIALIZACION EN BIOTECNOLOGIA INDUSTRIAL FCEyN-INTI Materia de Especialización CEBI_E1 Técnicas de análisis en biotecnología Módulo I: Moléculas pequeñas. Módulo II: Macromoléculas. Docente a cargo: SANTAGAPITA, Patricio CEBI_E1_9: Resonancia magnética nuclear
2 Técnicas de análisis estructural Espectrometría de masa Espectroscopia RMN Patricio Santagapita_CEBI_E1
3 Espectroscopía Estudio de la interacción entre la radiación electromagnética y la materia, con absorción o emisión de energía radiante T E R M I N O L O G I A Composición: átomos presentes y su proporción (formula molecular) Constitución: uniones entre los átomos (grupos funcionales y subestructuras) Configuración: disposición espacial de los átomos Conformación: disposición espacial de la molécula (rotación o giro de los enlaces simples) Patricio Santagapita_CEBI_E1
4 Patricio Santagapita_CEBI_E1
5 Rayos X/g UV/Vis IR Microondas Radiofrecuencia l Transición de e - internos Transición de e - de valencia Vibración molecular Rotación molecular Spin nuclear Espectroscopía UV Espectroscopía de abs. atómica Espectroscopía IR Espectroscopía RMN Espectroscopía de absorción (o emisión), como IR o UV. Detecta la absorción de radiofrequencias (radiación electromagnética) por ciertos núcleos en una molécula.. Patricio Santagapita_CEBI_E1
6 Espectroscopía TÉCNICA Rayos X Ultravioleta-Visible Infrarrojo Espectrometría de masas* Resonancia magnética nuclear INFORMACIÓN OBTENIDA Estructura total de la molécula incluída la estereoquímica (posiciones relativas de los átomos) Existencia de cromóforos y/o conjugación en la molécula (absorciones) Grupos funcionales (absorciones) Formula molecular y subestructuras (relación m/z). Grupos funcionales, subestructuras, conectividades, estereoquímica, etc (desplazamiento químico, áreas de los picos y constantes de acoplamiento) * No es una técnica espectroscópica en el sentido que estamos viendo pues no existe irradiación electromagnética de la sustancia y no se produce absorción de dicha radiación. Patricio Santagapita_CEBI_E1
7 Por qué estudiar RMN? Elucidación estructural Química de los productos naturales. Síntesis orgánica. Método analítico para elegir las condiciones de reacción Estudio de procesos dinámicos Cinética de reacciones. Estudio del equilibrio (químico y estructural). Estructura (tri-dimensional) Proteinas. ADN. Complejos proteína/adn Polisacáridos Diseño de drogas Relación Estructura Actividad por RMN Medicina MRI (Imágenes) Patricio Santagapita_CEBI_E1
8 RMN: Aplicaciones Análisis cualitativo (determinación estructural) y cuantitativo de las moléculas, orgánicas o inorgánicas, que componen la muestra Determinación estructural de moléculas (productos naturales o sintéticos) propiedades que poseen los núcleos atómicos Análisis de macromoléculas biológicas en condiciones similares a las naturales Estudio de la composición de muestras de origen natural (aceites, vinos, etc). Control de calidad en la industria química, industria de alimentos, industria farmacológica y en síntesis química. Determinación de constantes físicas y químicas (termodinámicas y cinéticas) Patricio Santagapita_CEBI_E1
9 RMN: fenómeno Núcleos atómicos: espacios ocupados por partículas subatómicas (protón y neutrón). Rodeados de capas de e - (modelo eléctricamente neutro) Núcleo + - protones 0 neutrones electrones orbitando ESPÍN (rotación alrededor del eje) MOMENTO ANGULAR (Cantidad de movimiento de rotación) Patricio Santagapita_CEBI_E1
10 Protón girando Un protón girando genera un campo magnético (momento magnético). Este campo magnético (B) se asemeja al de un imán (dipolo magnético). Qué espín tienen los núcleos? Núcleo está constituido por p protones y n neutrones Espín del núcleo: vector combinación del espín de todos sus p 1. p y n pares proporcionan espín nulo (I = 0): 4 He, 12 C, 16 O, 2. p y n impares dan espín entero: I = 1 2 D, 14 N; I = 3 10 B; 3. p + n = impar espín semientero: I = 1/2 1 H, 13 C; I = 5/2 17 O; TODO NÚCLEO CON ESPÍN NO NULO (I 0) ES SENSIBLE A RMN Patricio Santagapita_CEBI_E1
11 Los estados de spin del nucleo (m) estan cuantizados: m = I, (I - 1), (I - 2),, -I m es el número cuántico magnético. Para 1 H, 13 C, 15 N, 31 P : m = 1/2, -1/2 Esto significa que solo existen dos estados (niveles E) para ese núcleo Patricio Santagapita_CEBI_E1
12 En un núcleo con espín no nulo (I 0): Los dipolos magnéticos están dispuestos al azar Qué le ocurre bajo un campo magnético externo (B 0 )? El campo intenta alinear los dipolos de los núcleos en su misma dirección pero: 1. El momento magnético forma un ángulo con B 0 2. Existe más de una orientación del momento respecto a B 0 Patricio Santagapita_CEBI_E1
13 El momento magnético del núcleo rota alrededor del eje de B 0 con una frecuencia de precesión (w o u): Se comporta como un trompo o giroscopio Patricio Santagapita_CEBI_E1
14 Modelo de giróscopo del spin nuclear : B o m = -1/2 Nucleo rotando La cuantización de la componente según z del spin nuclear resulta en un ángulo = 54.73º para spin ½ o de 45º para spin 1.
15 Para un núcleo de I = ½ Dos estados energéticos posibles: a favor o en contra del campo B o B o = 0 B o > 0 b a La energía necesaria para pasar de un estado de espin al otro está determinada por: E = h = g h B 0 / 2 0 = g B 0 / 2 ECUACIÓN DE LARMOR E: relacionado con la intensidad del campo externo (B 0 ) y con la frecuencia de precesión ( ) El cambio de orientación se realiza absorbiendo o emitiendo radiación a la misma frecuencia ( ) Patricio Santagapita_CEBI_E1
16 Bajo un B 0 qué ocurrirá si suministramos E por otra fuente? Irradiando una radiofrecuencia ( ) los núcleos entran en RESONANCIA: absorben E y cambian de orientación Cambio de orientación crea un voltaje que puede ser registrado Patricio Santagapita_CEBI_E1
17 Magnetización macroscópica M o es directamente proporcional a la diferencia de población (N a - N b ), en la cual se promedian las contribuciones de los diferentes ms : z z x M o x y B o y B o Si descomponemos la contribución de los m en contribución sobre z y en el plano <xy>. Los componentes en el plano <xy> estan distribuidos al azar y se cancelan. Para los del eje z, tenemos una magnetizacion proporcional a N a - N b. Esto es mas o menos la situacion en una muestra macroscópica, usamos M o Diferencia importante entre m y M o. El primero está cuantizado y puede adoptar sólo uno de dos estados (a o b), El ultimo es la población total de spins (es un número continuo de estados).
18 Interpretación gráfica
19 RESONANCIA MAGNÉTICA NUCLEAR radiofrecuencia (bobina) propiedad del núcleo (espín I) campo magnético externo (B 0 ) (imán) Detector (bobina) para registrar el cambio de orientación Patricio Santagapita_CEBI_E1
20 Al dejar de irradiar con la frecuencia de resonancia la distribución vuelve al estado basal (relajación) La señal depende del exceso de núcleos que viene fijado por E: E ghb 0 2 h 1. Constante giroscópica del núcleo (g) 2. Campo magnético externo (B 0 ) A mayor B 0 : 1. Mayor exceso en N i (más señal o sensibilidad) 2. Mayor 0 (más resolución) Patricio Santagapita_CEBI_E1
21 1 millón - 64 El exceso de población con el que se trabaja es muy pequeño 2 millones 1 millón millón -8 m = 16 m = 64 m = millón + 8 E 1 millón + 32 B 0 (Tesla) 0 T 2.35 T (100 MHz) 1 millón T 18.8 T (400 MHz) (800 MHz) Patricio Santagapita_CEBI_E1
22 Influencia de B 0 en la calidad del espectro Espectros RMN 1 H de santonina 90 MHz 500 MHz A mayor B 0 MAYOR RESOLUCIÓN DE MULTIPLETES
23
24 Para cada tipo de núcleo la frecuencia de Larmor puede sufrir pequeñas variaciones que dependen del entorno molecular: Los electrones de los alrededores producen pequeños campos magnéticos que se agregan a B 0 Desplazamiento Químico (ppm de la frecuencia) Los núcleos de los alrededores con momento magnético dan lugar a desplazamientos simétricos de las frecuencias Acoplamiento spin-spin:j (Hz) Patricio Santagapita_CEBI_E1
25 Qué información se puede obtener de un espectro RMN 1 H? Número de señales: relacionada con el número de 1 H diferentes de la muestra Frecuencia de las señales ( ) : relacionada con el entorno molecular del núcleo. Área de las señales (integral): relacionada con la cantidad de cada tipo de 1 H. Multiplicidad de cada señal: relacionada con el número de 1 H vecinos de cada tipo. Constantes de acoplamiento (J): brinda información estereoquímica. Intercambio de 1 H : indica la presencia de cierto tipo de grupos funcionales (-COOH, -OH, -NH 2 ) Patricio Santagapita_CEBI_E1
26 constantes de acoplamiento: J (Hz) integrales frecuencia ( ) triplete multiplete triplete Multiplicidad de señales Patricio Santagapita_CEBI_E1
27 Escala de RMN (, ppm) 0 = g B 0 / 2 ECUACIÓN DE LARMOR La frecuencia de Larmor de un núcleo depende de B 0 No se puede definir ni utilizar una escala de frecuencias absoluta en RMN Ej: en un equipo de 90 MHz, la señal de CH 3 Br aparece a Hz, la de CH 2 Br 2 a y la de CHBr 3 a Hz Se define una escala relativa y sin unidades: desplazamiento químico (, ppm) utilizando una sustancia de referencia = muestra - ref. X 10 6 ref. Se expresa en partes por millón (ppm) es independiente de B 0 para un dado núcleo, su será el mismo en cualquier equipo.
28 Desplazamiento CH 3 H 3 C Si CH 3 CH 3 Tetrametilsilano = TMS. Referencia más usada. Soluble en la mayor parte de los solventes, inerte, volátil, da una señal intensa (12H) y suele estar a menores que la mayor parte de los compuestos orgánicos Por definición: TMS = 0 El TMS se agrega al solvente deuterado en el que se prepara la muestra
29 Escalas de 1 H : ~ 15 ppm Acidos, Aldehidos Alcoholes, protones a Aromaticos a cetonas Olefinas Alifáticos ppm 13 C : ~ 220 ppm TMS C=O de cetonas Aromaticos,olefinas Alifaticos CH 3, CH 2, CH ppm TMS C=O de Acidos, Carbonos unidos a grupos oxigenados y derivados de ácido
30 Desplazamiento El electrón tiene I = ½ posee momento magnético y éste es mucho más intenso que el de 1 H En una molécula, un núcleo está rodeado por una nube electrónica el B ef sobre el núcleo es la suma de B 0 y el campo generado por los electrones, B loc Como el electrón tiene carga negativa, el campo se opone al B 0 B ef < B o la nube electrónica apantalla
31 Desplazamiento 31 e - que rodean al nucleo tienen carga opuesta al 1 H, entonces pueden generar un campo magnético opuesto a B 0 Desapantallamiento Factores que disminuyen la densidad electrónica permiten al núcleo ver más a B 0 Resonancia a > energía Apantallamiento Factores que aumentan la densidad electrónica no dejan ver al núcleo a B 0 Resonancia a < energía
32 RMN de protones < apantallamiento campos bajos > δ > apantallamiento campos altos < δ Campo bajo Protección Aumenta el campo magnético Aumenta la frecuencia Campo alto Desprotección
33 Factores que afectan al desplazamiento Efecto inductivo: Si un átomo más electronegativo retira densidad de carga eléctrica, el B loc que se oponía a B 0 disminuye, en consecuencia la resonancia se produce con un campo externo menos intenso. Ojo! Se produce a mayor frecuencia, más a la izquierda Cuanto mayor es la diferencia de electronegatividad, mayor es el desapantallamiento/protección
34 Factores que afectan al desplazamiento Anisotropía magnética de los sistemas : Cuando los sistemas de electrones son sometidos a B 0 inducen otro campo que se opone al anterior. Aromáticos: el campo magnético efectivo que sienten los protones aumenta δ Otros sistemas con electrones
35 Factores que afectan al desplazamiento Puentes de hidrógeno: Los protones que pueden formar enlaces por puentes de hidrógeno (alcoholes, aminas) disminuyen fuertemente la densidad electrónica alrededor del 1 H. A medida que aumentan los puentes aumenta también el desplazamiento químico. RMN del hidrógeno ácido del fenol a distintas concentraciones
36 Multiplicidad El 1 H que observamos sufre está sometido a dos B ef diferentes: En uno B 0 se refuerza por el 50% de los núcleos alineados con él 2) En el otro, B 0 sufre una pequeña merma por el 50% de los núcleos que están en su contra. El 1 H aparece como un doblete debido a la influencia del protón vecino. La separación entre las señales es la constante de acoplamiento J y se mide en Hz.
37 Generalizando: la señal de un núcleo acoplado a n spins equivalentes constará de n + 1 líneas 8 Las intensidades de las líneas siguen el triángulo de Pascal s d t q qn
38 Patrones de acoplamiento más comunes X CH 3 X Metilo: singulete Etilo: cuarteto - triplete X X tert-butilo: singulete iso-propilo: septeto - doblete
39
40 Patrones de acoplamiento más comunes Alquenos La multiplicidad observada para H a es un doble doblete H c 2 J gem = 0 1 Hz X C H a C H b 3 J trans = Hz 3 J AC 3 J AB 3 J AB 3 J cis = 6-15 Hz
41 INTERPRETACIÓN DE UN ESPECTRO 1 H-RMN Número de señales: relacionada con el número de 1 H diferentes Frecuencia de las señales ( ) : relacionada con el entorno molecular del núcleo. Tipo de 1 H diferentes Área de las señales (integral): cantidad de cada tipo de 1 H diferentes Multiplicidad de cada señal: relacionada con el número de 1 H vecinos de cada tipo. Constantes de acoplamiento (J): brinda información estereoquímica Intercambio de 1 H : indica la presencia de cierto tipo de grupos funcionales (-COOH, -OH, -NH 2 )
42 INTERPRETACIÓN DE UN ESPECTRO 1 H-RMN FM=C 4 H 8 O 2 IR C=O Tabla Señal Multip. y J total 40 40/8=5 14/5=2.8~3 11/5=2.2~2 15/5=3 Estructura?? integral
43 INTERPRETACIÓN DE UN ESPECTRO 1 H-RMN FM=C 4 H 8 O 2 IR C=O Tabla Señal Multip. y J total 40 40/8=5 14/5=2.8~3 11/5=2.2~2 15/5=3 Estructura?? integral
44 INTERPRETACIÓN 1 H-RMN su isómero
45 Como preparar una muestra? Para un 1 H se utilizan unos pocos mg Cuidados:5-10 mg para moléculas promedio. La muestra: soluble en un solvente deuterado. Por qué? La señal del deuterio se utiliza para la estabilización del campo y como referencia. Cuánto? alrededor de 0,5 ml de solvente No disolver en recipientes grandes La solución no debe contener sólidos en suspensión (polvo, sílica, fibras, etc.) Filtrar a través (algodón o lana de vidrio). Evitar la presencia de metales (limaduras, restos de granallas, etc.) La solución debe ser homogénea en todo el tubo Evitar excesiva manipulación del material
46 Cuantificación por RMN Cuantificación relativa similar a un CG pero el factor de respuesta es conocido en forma exacta RMN es el método más usado para la determinación relativa de isómeros, diasterómeros y enantiómeros Cuantificación absoluta Se agrega un estándar a una masa conocida de mezcla RMN es un método primario de medición (con la más alta calidad metrológica y cuyos resultados son aceptados sin referencia a un estándar de la cantidad que se está midiendo)
47 Cuantificación absoluta: Uso de patrón interno El área no depende de la molécula en que se encuentran (la respuesta se relaciona con la cantidad de núcleos) No requiere separación previa ni establecimiento del factor de respuesta. Condiciones para un patrón Tener por lo menos un núcleo en común con la muestra Ser soluble en el mismo solvente No interferir con la muestra (no dar señales próximas, preferentemente una única, ni reaccionar químicamente con ella) Obtenerse con alto grado de pureza y título confiable Sustancia estable, no volátil, preferentemente sólida
48 Patrones más comunes
49 A B C D E F G S: integral, N: nro. de núcleos, m: masa, M: PM, p: pureza
50 Ventajas y desventajas Ventajas No requiere de determinación del factor de respuesta => NO son necesarios estándares de TODOS los analitos No requiere mantenimiento del sistema de detección (sangrado de columnas, carbonización en inyectores, etc.) No requiere de separación previa y puede cuantificarse más de un compuesto en el mismo espectro. Pueden cuantificarse impurezas inesperadas. Es simple, preciso y no destructivo. El costo de mantenimiento es fijo (se use o no el espectrómetro). Desventajas El costo de mantenimiento es el mismo. El costo del equipo de altos campos es 20 o 30 veces el de un CG o un HPLC La utilización del equipo requiere de personal entrenado Requiere de la utilización de He y N 2 líquidos, y su consumo es permanente.
51
52 y = 45º se observan todas las señales y = 90º se observan sólo los CH y = 135º se observan por un lado CH y CH 3 y por otro los CH 2, con fases opuestas
53 DEPT 45: CH 3, CH 2 y CH H Me O DEPT 90: solo CH DEPT 135: CH 3, CH, CH 2
54 Programa de análisis
55 Instrumentación en RMN B o N S Imán B 1 Generador de Frecuencia Registrador Detector Imán - Normalmente un superconductor. Algunos electroimanes e imanes permanentes (EM-360, EM-390) quedan. Generador de Frequencia Crea la corriente alterna (a w o ) que induce B 1. De onda continua o pulsado. Detector Resta la frecuencia base (una frecuencia constante muy cercana a w o ) de la frecuencia de salida. Da una frecuencia baja mucho más facil de manejar. Registrador - XY ploter, osciloscopio, computadora, etc., etc.
56 Free Induction Decay (FID) (decaimiento libre de la inducción Estamos interesados en analizar la señal que aparece en la espira receptora despues de poner la magnetización en el plano <xy> ( / 2 pulso). Dijimos que la muestra retornará al equilibrio precesionando (z). En el sistema rotante, la frecuencia de esta precesión es w - w o. La relajación de M o en el plano <xy> es exponencial (más la clase que sigue). Entonces, la espira receptora detecta una señal que decae y es cosinusoidal (para un spin sólo): w = w o M xy w - w o > 0 M xy time time
57 FID En una muestra real tenemos cientos de sistemas de spin, todos con frecuencias diferentes de la de B 1 (o frequencia carrier). Como hemos usado un pulso y efectivamente excitado todas las frequencias al mismo tiempo, veremos una combinación de todas en la espira receptora y esto se llama Free Induction Decay (o FID): La FT de esta función nos da el espectro de RMN en frecuencias:
58 RMN de proteínas Guías prácticas: Las proteínas grandes (> 150 residuos) dan peores resultados que las pequeñas, y generalmente NO se pueden asignar todos los picos. RMN > 750 MHz Los espectros son MUY complejos RMN 2D
59 RMN de proteínas Los espectros son MUY complejos Imposibles de interpretar!
60 RMN 2D Si los núcleos son iguales: Las señales fuera de la diagonal son las interesantes, por que son las de los protones (x ej) que si intercambiaron información durante el t1.
61 Si se miden protones en ambas dimensiones, igual siguen siendo complejos!
62
63 Actuales
64 Comparación MS vs NMR en Metabolómica
65 Comparación MS vs NMR en Metabolómica Gran diferencia de espacio
66 Comparación MS vs NMR en Metabolómica
67 LF-NMR (bajo campo)
68 LF-NMR (bajo campo) Free Induction Decay (FID) (decaimiento libre de la inducción w = w o M xy time
69 Enlace interesante m
Desplazamiento Químico. Dr. Jorge A. Palermo
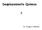 Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR
 ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR La Espectroscopía de Resonancia Magnética Nuclear (RMN) es la herramienta de determinación estructural más potente del químico orgánico. Mediante el RMN podemos
ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR La Espectroscopía de Resonancia Magnética Nuclear (RMN) es la herramienta de determinación estructural más potente del químico orgánico. Mediante el RMN podemos
Información IR EM RMN UV DC
 Técnicas de determinación estructural Información IR EM RMN UV DC Fórmula molecular Grupos funcionales - XXX X - - XXX X XX X - Conectividad X X XXX X - Geometría/ - - XXX - X estereoquímica Quiralidad
Técnicas de determinación estructural Información IR EM RMN UV DC Fórmula molecular Grupos funcionales - XXX X - - XXX X XX X - Conectividad X X XXX X - Geometría/ - - XXX - X estereoquímica Quiralidad
Resonancia Magnética Nuclear
 Resonancia Magnética Nuclear Química Orgánica I 2013 1H 4.29 4.28 4.28 4.27 4.26 4.26 4.25 4.24 4.23 4.22 4.22 4.21 4.20 4.18 4.18 4.16 4.16 4.14 3.85 3.80 3.75 2.82 2.81 2.80 2.77 2.76 2.75 2.72 2.71
Resonancia Magnética Nuclear Química Orgánica I 2013 1H 4.29 4.28 4.28 4.27 4.26 4.26 4.25 4.24 4.23 4.22 4.22 4.21 4.20 4.18 4.18 4.16 4.16 4.14 3.85 3.80 3.75 2.82 2.81 2.80 2.77 2.76 2.75 2.72 2.71
Para un resorte: E p =1/2 K (r-r 0 ) 2
 El enlace en analogía con un resorte!! Para un resorte: E p =1/2 K (r-r 0 ) 2 Cual es la energía potencial cuando r=r 0?? Que pasa con la energía potencial del resorte cuando lo estiro? Graficando la ecuación
El enlace en analogía con un resorte!! Para un resorte: E p =1/2 K (r-r 0 ) 2 Cual es la energía potencial cuando r=r 0?? Que pasa con la energía potencial del resorte cuando lo estiro? Graficando la ecuación
Resonancia Magnética Nuclear. Algunos núcleos atómicos, como por ejemplo el hidrógeno, tienen una propiedad denominada momento magnético
 Resonancia Magnética Nuclear Algunos núcleos atómicos, como por ejemplo el hidrógeno, tienen una propiedad denominada momento magnético Los hidrógenos de un compuesto se comportan como minúsculos imanes
Resonancia Magnética Nuclear Algunos núcleos atómicos, como por ejemplo el hidrógeno, tienen una propiedad denominada momento magnético Los hidrógenos de un compuesto se comportan como minúsculos imanes
Instrumentación en Resonancia Magnética Nuclear: el espectrómetro
 Instrumentación en Resonancia Magnética Nuclear: el espectrómetro Un imán que genere un campo magnético fijo y estable. Generalmente se identifica cada espectrómetro por la frecuencia de resonancia del
Instrumentación en Resonancia Magnética Nuclear: el espectrómetro Un imán que genere un campo magnético fijo y estable. Generalmente se identifica cada espectrómetro por la frecuencia de resonancia del
TEMARIO DE LOS EXÁMENES DE ADMISIÓN PARA INGRESO AL PROGRAMA DE MAESTRÍA EN CIENCIA DE MATERIALES DE LA UNIVERSIDAD DE SONORA
 TEMARIO DE LOS EXÁMENES DE ADMISIÓN PARA INGRESO AL PROGRAMA DE MAESTRÍA EN CIENCIA DE MATERIALES DE LA UNIVERSIDAD DE SONORA Examen de Química Química Orgánica Orbitales híbridos. Propiedades de los enlaces
TEMARIO DE LOS EXÁMENES DE ADMISIÓN PARA INGRESO AL PROGRAMA DE MAESTRÍA EN CIENCIA DE MATERIALES DE LA UNIVERSIDAD DE SONORA Examen de Química Química Orgánica Orbitales híbridos. Propiedades de los enlaces
J H,H pequeño. Equivalencia química y equivalencia magnética
 La magnitud de J para 1 H, 1 H varía entre -20 y 20 Hz J a 2 enlaces 2 J H,H 10-15 Hz J a 3 enlaces 3 J H,H 3-10 Hz J a larga distancia H-C-C-C-H 4 J H,H pequeño Los J heteronucleares son mas grandes,
La magnitud de J para 1 H, 1 H varía entre -20 y 20 Hz J a 2 enlaces 2 J H,H 10-15 Hz J a 3 enlaces 3 J H,H 3-10 Hz J a larga distancia H-C-C-C-H 4 J H,H pequeño Los J heteronucleares son mas grandes,
ESPECTROSCOPÍA DE RESONANCIA MAGNÉTICA NUCLEAR DE PROTONES
 ESPETROSOPÍA DE RESONANIA MAGNÉTIA NULEAR DE PROTONES La resonancia magnética nuclear es posible porque los núcleos de ciertos átomos, aquellos que tienen número de espín diferente de cero, (I ) se comportan
ESPETROSOPÍA DE RESONANIA MAGNÉTIA NULEAR DE PROTONES La resonancia magnética nuclear es posible porque los núcleos de ciertos átomos, aquellos que tienen número de espín diferente de cero, (I ) se comportan
TALLER DE ESPECTROSCOPIA
 TALLER DE ESPECTROSCOPIA RESONANCIA MAGNÉTICA PROTONICA OBJETIVOS a) Que el alumno reciba la una orientación teórica básica sobre la técnica analítica denominada Resonancia Magnética Protonica b) El alumno
TALLER DE ESPECTROSCOPIA RESONANCIA MAGNÉTICA PROTONICA OBJETIVOS a) Que el alumno reciba la una orientación teórica básica sobre la técnica analítica denominada Resonancia Magnética Protonica b) El alumno
Introducción Espectroscopía RMN
 Introducción Espectroscopía RMN +½ -½ +½ -½ Espín Nuclear + + +1/2 1/2 Un núcleo se comporta como un imán diminuto En ausencia de Mext: distribución al azar + + + + + Un campo o externo provoca momentos
Introducción Espectroscopía RMN +½ -½ +½ -½ Espín Nuclear + + +1/2 1/2 Un núcleo se comporta como un imán diminuto En ausencia de Mext: distribución al azar + + + + + Un campo o externo provoca momentos
Introducción Espectroscopía RMN
 Introducción Espectroscopía RMN +½ -½ +½ -½ Espín Nuclear + + +1/2 1/2 Un núcleo se comporta como un imán diminuto En ausencia de Mext: distribución al azar + + + + + Un campo o externo provoca momentos
Introducción Espectroscopía RMN +½ -½ +½ -½ Espín Nuclear + + +1/2 1/2 Un núcleo se comporta como un imán diminuto En ausencia de Mext: distribución al azar + + + + + Un campo o externo provoca momentos
Momento angular de espín
 Momento angular de espín 14 Ene 04 Reson 1 Estado de espín de un electrón: Ŝ 2 χ(σ) = s(s + 1) 2 χ(σ) Ŝ z χ(σ) = m s χ(σ) Donde s = 1/2 y hay dos orientaciones: m s = 1/2, 1/2 Estado de espín de un núcleo:
Momento angular de espín 14 Ene 04 Reson 1 Estado de espín de un electrón: Ŝ 2 χ(σ) = s(s + 1) 2 χ(σ) Ŝ z χ(σ) = m s χ(σ) Donde s = 1/2 y hay dos orientaciones: m s = 1/2, 1/2 Estado de espín de un núcleo:
(( )) Tema 5: Técnicas espectroscópicas: Espectrofotometría. visible Infrarrojo. Ultravioleta. Espectro de emisión de los cuerpos en equilibrio
 Tema 5: Técnicas espectroscópicas: Espectrofotometría 0 22 Hz Frecuencia 0 4 Hz 0 3 Hz γ X UV IR micro radio Rayos γ (gamma) λ < pm Rayos X pm-0nm Visible 400-800nm Ultravioleta 0-400 nm Longitud de onda
Tema 5: Técnicas espectroscópicas: Espectrofotometría 0 22 Hz Frecuencia 0 4 Hz 0 3 Hz γ X UV IR micro radio Rayos γ (gamma) λ < pm Rayos X pm-0nm Visible 400-800nm Ultravioleta 0-400 nm Longitud de onda
LICENCIATURA DE QUÍMICO EN ALIMENTOS. Química Analítica III. Tipo de Asignatura: Teórico-Práctico Área de Conocimiento: Básica Propedéutica
 LICENCIATURA DE QUÍMICO EN ALIMENTOS Química Analítica III Tipo de Asignatura: Teórico-Práctico Área de Conocimiento: Básica Propedéutica 106 1. DATOS GENERALES DE IDENTIFICACIÓN Nombre de la asignatura
LICENCIATURA DE QUÍMICO EN ALIMENTOS Química Analítica III Tipo de Asignatura: Teórico-Práctico Área de Conocimiento: Básica Propedéutica 106 1. DATOS GENERALES DE IDENTIFICACIÓN Nombre de la asignatura
RESONANCIA MAGNÉTICA NUCLEAR
 RESONANCIA MAGNÉTICA NUCLEAR SPIN DEL NUCLEO El nucleo de algunos átomos poseen SPIN. Estos núcleos se comportan como si estuvieran girando... no sabemos si realmente giran! Es como la propiedad de un
RESONANCIA MAGNÉTICA NUCLEAR SPIN DEL NUCLEO El nucleo de algunos átomos poseen SPIN. Estos núcleos se comportan como si estuvieran girando... no sabemos si realmente giran! Es como la propiedad de un
Resonancia Magnética Nuclear
 Clase 4 152.952 147.290 123.188 117.525 114.209 113.216 76.850 55.678 48.146 41.562 40.012 33.361 32.113 23.659 20.654 19.816 19.720 190 180 170 160 150 140 130 120 110 100 90 80 70 60 50 40 30 20 10 ppm
Clase 4 152.952 147.290 123.188 117.525 114.209 113.216 76.850 55.678 48.146 41.562 40.012 33.361 32.113 23.659 20.654 19.816 19.720 190 180 170 160 150 140 130 120 110 100 90 80 70 60 50 40 30 20 10 ppm
EJERCICIOS DE INTERPRETACIÓN PARTE 2
 EJERCICIOS DE INTERPRETACIÓN PARTE 2 7 Ácido -Bromobutírico NMR 09 CH 3 CH 2 CH O C OH 3 1 Br 1 2 8 Feniletil Acetato NMR 14 5 O CH 2 CH 2 O C CH 3 3 2 2 9 Etil Succinato NMR 18 O O CH 3 CH 2 O C CH 2
EJERCICIOS DE INTERPRETACIÓN PARTE 2 7 Ácido -Bromobutírico NMR 09 CH 3 CH 2 CH O C OH 3 1 Br 1 2 8 Feniletil Acetato NMR 14 5 O CH 2 CH 2 O C CH 3 3 2 2 9 Etil Succinato NMR 18 O O CH 3 CH 2 O C CH 2
TEMA 2: Resonancia Magnética Nuclear RMN-1H y 13C Fundamentos
 Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
ANÁLISIS INSTRUMENTAL_UII_PARTE DOS. Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½
 RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
INTRODUCCION (2) espectroscopía de absorción Espectroscopía de Emisión RMN Espectrometría de Masas espectrometría de fragmentación
 INTRODUCCION (1) Una de las labores más difíciles dentro de la Química Orgánica es la elucidación estructural. En algunos casos es suficiente con algunos datos mínimos. Utilizando algunas propiedades Fisico-Químicas
INTRODUCCION (1) Una de las labores más difíciles dentro de la Química Orgánica es la elucidación estructural. En algunos casos es suficiente con algunos datos mínimos. Utilizando algunas propiedades Fisico-Químicas
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS. Elucidación estructural: Ejemplo 1 Dados los siguientes espectros:
 ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
SERVICIO DE APOYO A LA INVESTIGACIÓN (SAI) SECCIÓN UNIVERSITARIA DE INSTRUMENTACIÓN CIENTÍFICA (SUIC)
 SERVICIO DE APOYO A LA INVESTIGACIÓN (SAI) SECCIÓN UNIVERSITARIA DE INSTRUMENTACIÓN CIENTÍFICA (SUIC) Murcia, 30 de Octubre de 2013 http://suicsaiumu.wordpress.com/ 1 La RMN es un tipo de Espectroscopía
SERVICIO DE APOYO A LA INVESTIGACIÓN (SAI) SECCIÓN UNIVERSITARIA DE INSTRUMENTACIÓN CIENTÍFICA (SUIC) Murcia, 30 de Octubre de 2013 http://suicsaiumu.wordpress.com/ 1 La RMN es un tipo de Espectroscopía
QUIMICA ORGANICA DE BIOPROCESOS. CEBI_A3_ 4: Espectroscopía (1º parte)
 CARRERA DE ESPECIALIZACION EN BIOTECNOLOGIA INDUSTRIAL FCEyN-INTI Materia de Articulación CEBI_A3 QUIMICA ORGANICA DE BIOPROCESOS Docente a cargo: Dra. Silvia Flores CEBI_A3_ 4: Espectroscopía (1º parte)
CARRERA DE ESPECIALIZACION EN BIOTECNOLOGIA INDUSTRIAL FCEyN-INTI Materia de Articulación CEBI_A3 QUIMICA ORGANICA DE BIOPROCESOS Docente a cargo: Dra. Silvia Flores CEBI_A3_ 4: Espectroscopía (1º parte)
Espectroscopía RMN: Un poco de historia
 Espectroscopía RMN: Un poco de historia 1924 Wolfang Pauli propuso las bases teóricas de RMN. Sugirió que ciertos núcleos atómicos tienen propiedades de spin y momento magnético 1924 W. Stern y O. Gerlach
Espectroscopía RMN: Un poco de historia 1924 Wolfang Pauli propuso las bases teóricas de RMN. Sugirió que ciertos núcleos atómicos tienen propiedades de spin y momento magnético 1924 W. Stern y O. Gerlach
Elucidación estructural: Resonancia Magnética Nuclear (Introducción)
 Elucidación estructural: Resonancia Magnética Nuclear (Introducción) Antes de comenzar a entender el fenómeno de la Resonancia magnética debemos considerar cuales son las propiedades que poseen los núcleos
Elucidación estructural: Resonancia Magnética Nuclear (Introducción) Antes de comenzar a entender el fenómeno de la Resonancia magnética debemos considerar cuales son las propiedades que poseen los núcleos
SISTEMAS PROTÓNICOS EN RESONANCIA MAGNÉTICO NUCLEAR DE 1 H. Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato
 SISTEMAS PROTÓNICOS EN RESONANCIA MAGNÉTICO NUCLEAR DE 1 H Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato Clasificación de los sistemas protónicos Sistema A2 Sistema AX Sistema
SISTEMAS PROTÓNICOS EN RESONANCIA MAGNÉTICO NUCLEAR DE 1 H Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato Clasificación de los sistemas protónicos Sistema A2 Sistema AX Sistema
Interacciones intermoleculares: Espectroscopia
 Interacciones intermoleculares: Espectroscopia Presentado por: Wilmer E. Vallejo Narváez 13 de Octubre de 2014 1 Contenido Introducción Espectroscopia Uv vis Espectroscopia IR Espectroscopia RMN 2 Introducción
Interacciones intermoleculares: Espectroscopia Presentado por: Wilmer E. Vallejo Narváez 13 de Octubre de 2014 1 Contenido Introducción Espectroscopia Uv vis Espectroscopia IR Espectroscopia RMN 2 Introducción
Resonancia Magnetica Nuclear Avanzada
 Resonancia Magnetica Nuclear Avanada Ala-Arg-Pro-Tr-Asn-Phe-Cpa-Leu-NH 2 Cpa Ala Pro Facultad De Quimica Que es la espectroscopia? Sin aprender griego o latin, la espectroscopia es el estudio de las interacciones
Resonancia Magnetica Nuclear Avanada Ala-Arg-Pro-Tr-Asn-Phe-Cpa-Leu-NH 2 Cpa Ala Pro Facultad De Quimica Que es la espectroscopia? Sin aprender griego o latin, la espectroscopia es el estudio de las interacciones
TEMA 6: Espectroscopía de Resonancia Paramagnética Electrónica. El espín electrónico
 TEMA 6: Espectroscopía de Resonancia Paramagnética Electrónica. El espín electrónico - Evidencia experimental 1. Líneas espectrales del átomo de H poseen estructura fina. 2. Experimento de Stern-Gerlach.
TEMA 6: Espectroscopía de Resonancia Paramagnética Electrónica. El espín electrónico - Evidencia experimental 1. Líneas espectrales del átomo de H poseen estructura fina. 2. Experimento de Stern-Gerlach.
UNIVERSIDAD SANTO TOMAS SECCIONAL BUCARAMANGA. División de Ingenierías - Facultad de Química Ambiental
 UNIVERSIDAD SANTO TOMAS SECCIONAL BUCARAMANGA División de Ingeniería Facultad de Química Ambiental Nombre de Asignatura: QUÍMICA INSTRUMENTAL II Àrea: Básicas de Química / Química Analítica Créditos: 4
UNIVERSIDAD SANTO TOMAS SECCIONAL BUCARAMANGA División de Ingeniería Facultad de Química Ambiental Nombre de Asignatura: QUÍMICA INSTRUMENTAL II Àrea: Básicas de Química / Química Analítica Créditos: 4
Movimiento vibracional
 ESPECTROSCOPÍA Movimiento vibracional El oscilador armónico como modelo de la vibración molecular Los sistemas que vibran a nivel molecular incluyen las vibraciones internas de una molécula y las vibraciones
ESPECTROSCOPÍA Movimiento vibracional El oscilador armónico como modelo de la vibración molecular Los sistemas que vibran a nivel molecular incluyen las vibraciones internas de una molécula y las vibraciones
Departamento: Química Industrial y Aplicada Contenido Vigencia: Sem. A/80
 Prelaciones: IQ-7151 Intensidad:2T+1P+4L= 4U Departamento: Química Industrial y Aplicada Semestre: Octavo Contenido Vigencia: Sem. A/80 1.- Introducción.- 1.1. Propiedades físicas útiles en el análisis.
Prelaciones: IQ-7151 Intensidad:2T+1P+4L= 4U Departamento: Química Industrial y Aplicada Semestre: Octavo Contenido Vigencia: Sem. A/80 1.- Introducción.- 1.1. Propiedades físicas útiles en el análisis.
1 ANÁLISIS DE COMPUESTOS ORGÁNICOS
 1 ANÁLISIS DE COMPUESTOS ORGÁNICOS 1.1. EL ANÁLISIS DE COMPUESTOS ORGÁNICOS Una de las actividades más apasionantes que realiza el químico, es cuando se encuentra con una sustancia desconocida; inmediatamente
1 ANÁLISIS DE COMPUESTOS ORGÁNICOS 1.1. EL ANÁLISIS DE COMPUESTOS ORGÁNICOS Una de las actividades más apasionantes que realiza el químico, es cuando se encuentra con una sustancia desconocida; inmediatamente
Trabajo Practico nº2
 Trabajo Practico nº2 Espectroscopía de Resonancia Paramagnética Electrónica (RPE). Introducción La Resonancia Paramagnética Electrónica (RPE, en inglés EPR: Electron Paramagnetic Resonance) es una técnica
Trabajo Practico nº2 Espectroscopía de Resonancia Paramagnética Electrónica (RPE). Introducción La Resonancia Paramagnética Electrónica (RPE, en inglés EPR: Electron Paramagnetic Resonance) es una técnica
UNIVERSIDAD NACIONAL DEL SUR 1
 UNIVERSIDAD NACIONAL DEL SUR 1 PROGRAMA DE: CODIGO: 393 H O R A S D E C L A S E P R O F E S O R R E S P O N S A B L E T E O R I C A S P R A C T I C A S Dra. Alicia B. Chopa Por semana Por cuatrimestre
UNIVERSIDAD NACIONAL DEL SUR 1 PROGRAMA DE: CODIGO: 393 H O R A S D E C L A S E P R O F E S O R R E S P O N S A B L E T E O R I C A S P R A C T I C A S Dra. Alicia B. Chopa Por semana Por cuatrimestre
ESPECTROSCOPÍA INFRARROJA
 MÉTODOS 2: ESPECTROSCOPÍA INFRARROJA Universidad Pedagógica Nacional Facultad de Ciencia y Tecnología Departamento de Química Julie Benavides Melo 2 CONTENIDOS 3 CONTENIDOS 4 CONTENIDOS ÁREAS TEMÁTICAS
MÉTODOS 2: ESPECTROSCOPÍA INFRARROJA Universidad Pedagógica Nacional Facultad de Ciencia y Tecnología Departamento de Química Julie Benavides Melo 2 CONTENIDOS 3 CONTENIDOS 4 CONTENIDOS ÁREAS TEMÁTICAS
E = h = h B 0. Un núcleo con numero atómico impar o numero másico impar tiene spin nuclear.
 ESPETRSPIA 1 -RMN Un núcleo con numero atómico impar o numero másico impar tiene spin nuclear. La carga del núcleo al girar genera un campo magnético uando se aplica un campo magnético externo La carga
ESPETRSPIA 1 -RMN Un núcleo con numero atómico impar o numero másico impar tiene spin nuclear. La carga del núcleo al girar genera un campo magnético uando se aplica un campo magnético externo La carga
MATERIAL 06. TEMA: MÉTODOS ESPECTROSCÓPICOS DE ANÁLISIS
 MATERIAL 06. TEMA: MÉTODOS ESPECTROSCÓPICOS DE ANÁLISIS La espectroscopia es el estudio de las interacciones de las radiaciones electromagnéticas con la materia (átomos y moléculas). Los métodos analíticos
MATERIAL 06. TEMA: MÉTODOS ESPECTROSCÓPICOS DE ANÁLISIS La espectroscopia es el estudio de las interacciones de las radiaciones electromagnéticas con la materia (átomos y moléculas). Los métodos analíticos
La espectroscopia de resonanc resonan ia magnética nuclear (RMN) es un fenóme fenóm no
 Resonancia Magnética Nuclear de Sólidos y su aplicación ala caracterización de polímeros Carlos García Aparicio Madrid, 2012 La espectroscopia de resonancia magnética nuclear (RMN) es un fenómeno que ocurre
Resonancia Magnética Nuclear de Sólidos y su aplicación ala caracterización de polímeros Carlos García Aparicio Madrid, 2012 La espectroscopia de resonancia magnética nuclear (RMN) es un fenómeno que ocurre
GUÍA DOCENTE DETERMINACIÓN ESTRUCTURAL. JOSE SEPÚLVEDA ARQUES Departamento de Química Orgànica Universitad de Valencia
 45 GUÍA DOCENTE DETERMINACIÓN ESTRUCTURAL Curso 2006-2007 JOSE SEPÚLVEDA ARQUES Departamento de Química Orgànica Universitad de Valencia 46 I. Datos iniciales de identificación Nombre de la asignatura:
45 GUÍA DOCENTE DETERMINACIÓN ESTRUCTURAL Curso 2006-2007 JOSE SEPÚLVEDA ARQUES Departamento de Química Orgànica Universitad de Valencia 46 I. Datos iniciales de identificación Nombre de la asignatura:
CONOCIMIENTO DE TÉCNICAS ANALÍTICAS PARTE I: FUNDAMENTOS DE ESPECTROFOTOMETRÍA.
 CONOCIMIENTO DE TÉCNICAS ANALÍTICAS PARTE I: FUNDAMENTOS DE ESPECTROFOTOMETRÍA. I. OBJETIVO GENERAL Conocer y aplicar los fundamentos de la ESPECTROFOTOMETRÍA para la determinación de concentraciones en
CONOCIMIENTO DE TÉCNICAS ANALÍTICAS PARTE I: FUNDAMENTOS DE ESPECTROFOTOMETRÍA. I. OBJETIVO GENERAL Conocer y aplicar los fundamentos de la ESPECTROFOTOMETRÍA para la determinación de concentraciones en
ESPECTROSCOPÍA INTERACCIÓN RADIACIÓN-MATERIA. Es el laboratorio de la química cuántica
 ESPECTROSCOPÍA INTERACCIÓN RADIACIÓN-MATERIA Es el laboratorio de la química cuántica RADIACIÓN ELECTROMAGNÉTICA E = h n c = nl La energía aumenta Cómo interactúa con la materia la radiación según su energía
ESPECTROSCOPÍA INTERACCIÓN RADIACIÓN-MATERIA Es el laboratorio de la química cuántica RADIACIÓN ELECTROMAGNÉTICA E = h n c = nl La energía aumenta Cómo interactúa con la materia la radiación según su energía
Problemas. Módulo 2. Espectroscopía de IR y RMN
 Problemas. Módulo 2. Espectroscopía de IR y RMN 1. Dadas las estructuras de cinco isómeros de fórmula molecular C 4 H 8 Oy los espectros IR identificados como A, B, C, D y E, indique de manera razonada
Problemas. Módulo 2. Espectroscopía de IR y RMN 1. Dadas las estructuras de cinco isómeros de fórmula molecular C 4 H 8 Oy los espectros IR identificados como A, B, C, D y E, indique de manera razonada
Práctica 5 APLICACIONES DE LA ESPECTROSCOPÍA DE RESONANCIA MAGNÉTICA NUCLEAR
 Práctica 5 APLICACIONES DE LA ESPECTROSCOPÍA DE RESONANCIA MAGNÉTICA NUCLEAR 1. Objetivo El objetivo de la presente práctica es la identificación cualitativa de compuestos orgánicos mediante la técnica
Práctica 5 APLICACIONES DE LA ESPECTROSCOPÍA DE RESONANCIA MAGNÉTICA NUCLEAR 1. Objetivo El objetivo de la presente práctica es la identificación cualitativa de compuestos orgánicos mediante la técnica
Carrera: Químico Farmacobiólogo. Asignatura: Análisis instrumental II. Área del Conocimiento: Análisis Instrumental II
 Carrera: Químico Farmacobiólogo Asignatura: Análisis instrumental II Área del Conocimiento: Generales de la Asignatura: Nombre de la Asignatura: Clave Asignatura: Nivel: Carrera: Frecuencia (h/semana)
Carrera: Químico Farmacobiólogo Asignatura: Análisis instrumental II Área del Conocimiento: Generales de la Asignatura: Nombre de la Asignatura: Clave Asignatura: Nivel: Carrera: Frecuencia (h/semana)
Colegio San Lorenzo - Copiapó - Región de Atacama Per Laborem ad Lucem
 TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
Espectrometría de luminiscencia molecular Cap.15
 Espectrometría de luminiscencia molecular Cap.15 Luz cuyo origen no radica exclusivamente en las altas temperaturas Se da en sustancias que pueden absorber energía, excitándose a niveles mayores y emitirla
Espectrometría de luminiscencia molecular Cap.15 Luz cuyo origen no radica exclusivamente en las altas temperaturas Se da en sustancias que pueden absorber energía, excitándose a niveles mayores y emitirla
Tema 7. Espectroscopia para el estudio de la materia. 1. Introducción. 1. Introducción. 1. Introducción
 1 Tema 7. Espectroscopia para el estudio de la materia 1801: Thomas Young. Naturaleza dual de la radiación y la materia. Interacción Radiación-materia. Ley de Lambert-Beer 3. Espectroscopía InfraRojos
1 Tema 7. Espectroscopia para el estudio de la materia 1801: Thomas Young. Naturaleza dual de la radiación y la materia. Interacción Radiación-materia. Ley de Lambert-Beer 3. Espectroscopía InfraRojos
PRÁCTICA DE ESPECTROSCOPIA INFRARROJA
 PRÁCTICA DE ESPECTROSCOPIA INFRARROJA PREPARACIÓN DE MUESTRAS Tu profesor te enseñará el manejo del equipo de infrarrojo y las técnicas de preparación de muestra: disolución, película, pastilla, y suspensión.
PRÁCTICA DE ESPECTROSCOPIA INFRARROJA PREPARACIÓN DE MUESTRAS Tu profesor te enseñará el manejo del equipo de infrarrojo y las técnicas de preparación de muestra: disolución, película, pastilla, y suspensión.
UNIVERSIDAD NACIONAL DE EDUCACIÓN A DISTANCIA
 UNIVERSIDAD NACIONAL DE EDUCACIÓN A DISTANCIA NOMBRE... APELLIDOS... CALLE... POBLACIÓN... PROVINCIA... C.P.... ESPECTROSCOPIA MOLECULAR PRUEBA DE EVALUACIÓN A DISTANCIA 2013 2014 095354 Prueba Objetiva
UNIVERSIDAD NACIONAL DE EDUCACIÓN A DISTANCIA NOMBRE... APELLIDOS... CALLE... POBLACIÓN... PROVINCIA... C.P.... ESPECTROSCOPIA MOLECULAR PRUEBA DE EVALUACIÓN A DISTANCIA 2013 2014 095354 Prueba Objetiva
Determinación estructural
 Determinación estructural Qué queremos saber? 1- Composición (Fórmula molecular) ( C 15 22 3 ) Masas, 13 C-RMN + DEPT +IR 2- Constitución (Conectividad) 1 -RMN, 13 C-RMN + DEPT, CSY, /C, /C larga dist.
Determinación estructural Qué queremos saber? 1- Composición (Fórmula molecular) ( C 15 22 3 ) Masas, 13 C-RMN + DEPT +IR 2- Constitución (Conectividad) 1 -RMN, 13 C-RMN + DEPT, CSY, /C, /C larga dist.
TALLER DE ESPECTROSCOPIA
 TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
Básico ( ) Profesional ( ) especializado ( x ) Horas de. Crédito s. Práctica ( )
 PROGRAMA DE ESTUDIO Nombre de la asignatura: TÉCNICAS ESPECTROSCÓPICAS. Clave: QUI15 Fecha de elaboración: Marzo 2015 Horas Semestre Horas semana Horas de Teoría Ciclo Formativo: Básico ( ) Profesional
PROGRAMA DE ESTUDIO Nombre de la asignatura: TÉCNICAS ESPECTROSCÓPICAS. Clave: QUI15 Fecha de elaboración: Marzo 2015 Horas Semestre Horas semana Horas de Teoría Ciclo Formativo: Básico ( ) Profesional
Espectroscopía. Qué es la espectroscopía? 18/10/2013
 Espectroscopía Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar la frecuencia de
Espectroscopía Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar la frecuencia de
Tema 1 INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS EN LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS
 Tema 1 INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS EN LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS 1. Usando los datos de la siguiente tabla que ilustra el efecto de la electronegatividad del heteroátomo
Tema 1 INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS EN LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS 1. Usando los datos de la siguiente tabla que ilustra el efecto de la electronegatividad del heteroátomo
Práctica 4. Espectroscopia IR y Análisis elemental
 Laboratorio de Química de Coordinación Práctica 4. Espectroscopia IR y Análisis elemental Parte II: Las técnicas Tarea previa 1. Leer los fundamentos teóricos de la práctica 2. La molécula de agua (H2O)
Laboratorio de Química de Coordinación Práctica 4. Espectroscopia IR y Análisis elemental Parte II: Las técnicas Tarea previa 1. Leer los fundamentos teóricos de la práctica 2. La molécula de agua (H2O)
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS
 Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
Resonancia Magnética Nuclear
 RMN 01 MÉTODOS ESPECTROSCÓPICOS APLICADOS A DETERMINACIÓN DE ESTRUCTURAS MOLECULARES Resonancia Magnética Nuclear Resonancia Magnética Nuclear Espectroscopía de RMN es una forma de espectroscopia de Absorción.
RMN 01 MÉTODOS ESPECTROSCÓPICOS APLICADOS A DETERMINACIÓN DE ESTRUCTURAS MOLECULARES Resonancia Magnética Nuclear Resonancia Magnética Nuclear Espectroscopía de RMN es una forma de espectroscopia de Absorción.
S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS
 S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS NOMBRE DE LA ASIGNATURA: QUIMICA ANALITICA II (4-2-10) NIVEL: LICENCIATURA. CARRERA: INGENIERIA BIOQUIMICA INGENIERIA QUIMICA CLAVE: ACC-9331
S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS NOMBRE DE LA ASIGNATURA: QUIMICA ANALITICA II (4-2-10) NIVEL: LICENCIATURA. CARRERA: INGENIERIA BIOQUIMICA INGENIERIA QUIMICA CLAVE: ACC-9331
ESPECTROSCOPíA INFRARROJA
 ESPECTROSCOPíA INFRARROJA Química Orgánica 1 Facultad de Farmacia y Bioquímica UBA 2016 Autor: Dra. Isabel Perillo 1 Espectro electromagnético Unidades de l usadas: para UV-visible: nm (mm): 10-9 m para
ESPECTROSCOPíA INFRARROJA Química Orgánica 1 Facultad de Farmacia y Bioquímica UBA 2016 Autor: Dra. Isabel Perillo 1 Espectro electromagnético Unidades de l usadas: para UV-visible: nm (mm): 10-9 m para
ESTRUCTURA ATÓMICA, SISTEMA PERIÓDICO Y ENLACE QUÍMICO 1
 ESTRUCTURA ATÓMICA, SISTEMA PERIÓDICO Y ENLACE QUÍMICO CUESTIONES Los números atómicos deben consultarse en la tabla periódica de los elementos 1. (1988) El cobre natural está compuesto por cobre 63 y
ESTRUCTURA ATÓMICA, SISTEMA PERIÓDICO Y ENLACE QUÍMICO CUESTIONES Los números atómicos deben consultarse en la tabla periódica de los elementos 1. (1988) El cobre natural está compuesto por cobre 63 y
MATERIA SERES VIVOS QUE ES LA MATERIA? UNIDAD 2 PARTE 1 LA MATERIA ES TODO AQUELLO QUE OCUPA UN LUGAR EN EL ESPACIO, ES DECIR TIENE MASA Y VOLUMEN
 UNIDAD 2 COMPOSICIÓN N QUÍMICA DE LOS SERES VIVOS PARTE 1 MATERIA QUE ES LA MATERIA? LA MATERIA ES TODO AQUELLO QUE OCUPA UN LUGAR EN EL ESPACIO, ES DECIR TIENE MASA Y VOLUMEN Puede estar en diferentes
UNIDAD 2 COMPOSICIÓN N QUÍMICA DE LOS SERES VIVOS PARTE 1 MATERIA QUE ES LA MATERIA? LA MATERIA ES TODO AQUELLO QUE OCUPA UN LUGAR EN EL ESPACIO, ES DECIR TIENE MASA Y VOLUMEN Puede estar en diferentes
CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH.
 Pag:1 CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH. En química orgánica, el índice de deficiencia de hidrógeno (IDH) es utilizado para ayudar a dibujar estructuras químicas. La fórmula permite determinar
Pag:1 CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH. En química orgánica, el índice de deficiencia de hidrógeno (IDH) es utilizado para ayudar a dibujar estructuras químicas. La fórmula permite determinar
Tema 6. Espectroscopia para el estudio de la materia
 Tema 6. Espectroscopia para el estudio de la materia 1. Introducción. Naturaleza dual de la radiación y la materia 2. Interacción Radiación-materia. Ley de Lambert-Beer 3. Espectroscopía InfraRojo 4. Espectroscopía
Tema 6. Espectroscopia para el estudio de la materia 1. Introducción. Naturaleza dual de la radiación y la materia 2. Interacción Radiación-materia. Ley de Lambert-Beer 3. Espectroscopía InfraRojo 4. Espectroscopía
Introducción a la Resonancia Magnética Nuclear. Química Orgánica III Primer Semestre 2014
 Introducción a la Resonancia Magnética Nuclear Química Orgánica III Primer Semestre 2014 Referencias empleadas en esta presentación: McMurry, John. Química Orgánica. 8ª. Edición. CENGAGE. Wade, L.J. Química
Introducción a la Resonancia Magnética Nuclear Química Orgánica III Primer Semestre 2014 Referencias empleadas en esta presentación: McMurry, John. Química Orgánica. 8ª. Edición. CENGAGE. Wade, L.J. Química
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO. Lola Castelao
 ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
Los átomos constituyen la unidad básica de todos los materiales de ingeniería. La estructura de los átomos Están constituidos por las siguientes partí
 Capítulo 2: Estructura atómica Los átomos constituyen la unidad básica de todos los materiales de ingeniería. La estructura de los átomos Están constituidos por las siguientes partículas subatómicas: Protones
Capítulo 2: Estructura atómica Los átomos constituyen la unidad básica de todos los materiales de ingeniería. La estructura de los átomos Están constituidos por las siguientes partículas subatómicas: Protones
ÍNDICE 1 Introducción 2 Átomos, moléculas y iones 3 Estequiometría 4 Reacciones en disolución acuosa
 ÍNDICE Lista de animaciones... xvii Prefacio... xix Sugerencia para el estudiante... xxvii 1 Introducción... 1 1.1 El estudio de la química... 2 1.2 El método científico... 2 1.3 Clasificación de la materia...
ÍNDICE Lista de animaciones... xvii Prefacio... xix Sugerencia para el estudiante... xxvii 1 Introducción... 1 1.1 El estudio de la química... 2 1.2 El método científico... 2 1.3 Clasificación de la materia...
Tema 7: Espectroscopia Vibracional (IR)
 Tabla 1. El espectro electromagnético Región Longitud de onda Energía de excitación Tipo de excitación Rayos x, rayos cósmicos 286 (Kcal/mol) Ultravioleta Visible Infrarrojo próximo Infrarrojo
Tabla 1. El espectro electromagnético Región Longitud de onda Energía de excitación Tipo de excitación Rayos x, rayos cósmicos 286 (Kcal/mol) Ultravioleta Visible Infrarrojo próximo Infrarrojo
Prefacio... ix COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3
 ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA
 PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo
PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo
PLANIFICACIÓN DE ASIGNATURA
 PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUÍMICA DEPARTAMENTO CIENCIAS DEL AMBIENTE ASIGNATURA QUIMICA ORGANICA I CÓDIGO 66114 PRERREQUISITOS Química General I y
PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUÍMICA DEPARTAMENTO CIENCIAS DEL AMBIENTE ASIGNATURA QUIMICA ORGANICA I CÓDIGO 66114 PRERREQUISITOS Química General I y
REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA
 REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo de micropipetas
REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo de micropipetas
MÉTODOS ACTUALES PARA EL ANÁLISIS DE SUSTANCIAS. Belén Cánovas Gómez Departamento Física y Química 1º BACHILLERATO Colegio Narval
 MÉTODOS ACTUALES PARA EL ANÁLISIS DE SUSTANCIAS Belén Cánovas Gómez Departamento Física y Química 1º BACHILLERATO Colegio Narval Para conocer la composición química de la materia, hay que llevar a cabo
MÉTODOS ACTUALES PARA EL ANÁLISIS DE SUSTANCIAS Belén Cánovas Gómez Departamento Física y Química 1º BACHILLERATO Colegio Narval Para conocer la composición química de la materia, hay que llevar a cabo
TEMA 5 ESPECTROSCOPÍA
 TEMA 5 ESPECTROSCOPÍA ORIGEN DEL PROBLEMA Durante el siglo XIX, antes que existieran las técnicas analíticas actuales, el químico orgánico podía determinar la fórmula molecular de una sustancia pura a
TEMA 5 ESPECTROSCOPÍA ORIGEN DEL PROBLEMA Durante el siglo XIX, antes que existieran las técnicas analíticas actuales, el químico orgánico podía determinar la fórmula molecular de una sustancia pura a
SANTIAGO V. LUIS C.U. Química Orgánica U.J.I. Despacho TC1424DD, 4º piso Dpto. Q. Inorgánica y Orgánica
 SANTIAGO V. LUIS C.U. Química Orgánica U.J.I. Despacho TC1424DD, 4º piso Dpto. Q. Inorgánica y Orgánica Tutorías: Martes, Miércoles, Jueves: 10:00-11:00 1 ELUCIDACIÓN ESTRUCTURAL EN COMPUESTOS ORGÁNICOS
SANTIAGO V. LUIS C.U. Química Orgánica U.J.I. Despacho TC1424DD, 4º piso Dpto. Q. Inorgánica y Orgánica Tutorías: Martes, Miércoles, Jueves: 10:00-11:00 1 ELUCIDACIÓN ESTRUCTURAL EN COMPUESTOS ORGÁNICOS
1.- Fundamentos básicos
 1.- Fundamentos básicos - Algunos núcleos tienen espín: La circulación de carga genera un campo magnético a lo largo del eje de giro ( 1 H, 7 Li, 11 B, 13 C, 14 N, 19 F, 23 Na, 27 Al, 29 Si, 31 P, 33 S,
1.- Fundamentos básicos - Algunos núcleos tienen espín: La circulación de carga genera un campo magnético a lo largo del eje de giro ( 1 H, 7 Li, 11 B, 13 C, 14 N, 19 F, 23 Na, 27 Al, 29 Si, 31 P, 33 S,
ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS
 ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS RESONANCIA MAGNÉTICA PROTÓNICA REGLAS BÁSICAS DE INTERPRETACIÓN Y TABLAS REGLAS BÁSICAS DE INTERPRETACIÓN DE RESONANCIA MAGNÉTICA PROTÓNICA
ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS RESONANCIA MAGNÉTICA PROTÓNICA REGLAS BÁSICAS DE INTERPRETACIÓN Y TABLAS REGLAS BÁSICAS DE INTERPRETACIÓN DE RESONANCIA MAGNÉTICA PROTÓNICA
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS
 Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
TEMA 10. ESPECTROSCOPIA DE RESONANCIA MAGNÉTICA NUCLEAR
 TEMA 10. ESPETROSOPIA DE RESONANIA MAGNÉTIA NULEAR 1. Fundamentos físicos de la espectroscopia de RMN. 2. El espectrómetro de resonancia magnética nuclear. 3. Resonancia magnética nuclear de 1. Apantallamiento
TEMA 10. ESPETROSOPIA DE RESONANIA MAGNÉTIA NULEAR 1. Fundamentos físicos de la espectroscopia de RMN. 2. El espectrómetro de resonancia magnética nuclear. 3. Resonancia magnética nuclear de 1. Apantallamiento
Temario: Temario: SEMINARIO1 hora lectiva (2 grupos) martes y jueves. SEMINARIO1 hora lectiva (2 grupos) martes y jueves
 PROFESORES PARTICIPANTES: DRA. CAROLINA JULLIAN M. DR. ERNAN PESSOA M. COORDINADOR CATEDRA 2 horas lectivas SEMINARIO1 hora lectiva (2 grupos) martes y jueves Temario: ESPECTROSCOPIA NOMENCLATURA ESTRUCTURA
PROFESORES PARTICIPANTES: DRA. CAROLINA JULLIAN M. DR. ERNAN PESSOA M. COORDINADOR CATEDRA 2 horas lectivas SEMINARIO1 hora lectiva (2 grupos) martes y jueves Temario: ESPECTROSCOPIA NOMENCLATURA ESTRUCTURA
DETERMINACIÓN ESTRUCTURAL (Teoría) CURSO , GRUP A 9 de febrero Apellidos... Nombre...
 DETERMINAIÓN ESTRUTURAL (Teoría) URS 2003-2004, GRUP A 9 de febrero 2004 Apellidos... Nombre... 1.- Que diferencias espera encontrar entre el 3 - y el 3 -D. a) en sus espectros de masas. El ión molecular
DETERMINAIÓN ESTRUTURAL (Teoría) URS 2003-2004, GRUP A 9 de febrero 2004 Apellidos... Nombre... 1.- Que diferencias espera encontrar entre el 3 - y el 3 -D. a) en sus espectros de masas. El ión molecular
INDICE DE DEFICIENCIA DE HIDRÓGENO TEORIA BÁSICA DE ESPECTROSCOPÍA INFRAROJA
 INDIE DE DEFIIENIA DE HIDRÓGENO Y TEORIA BÁSIA DE ESPETROSOPÍA INFRAROJA QUE SE PUEDE SABER DE UNA FÓRMULA MÍNIMA DE UN OMPUESTO? SE PUEDE DETERMINAR EL NUMERO DE ANILLOS Y DOBLES ENLAES. Hidrucarburos
INDIE DE DEFIIENIA DE HIDRÓGENO Y TEORIA BÁSIA DE ESPETROSOPÍA INFRAROJA QUE SE PUEDE SABER DE UNA FÓRMULA MÍNIMA DE UN OMPUESTO? SE PUEDE DETERMINAR EL NUMERO DE ANILLOS Y DOBLES ENLAES. Hidrucarburos
DIVISIÓN CIENCIAS BÁSICAS E INGENIERÍA
 PROGRAMA DE ESTUDIOS UNIVERSIDAD AUTÓNOMA METROPOLITANA UNIDAD: IZTAPALAPA NIVEL: EN LICENCIATURA QUÍMICA : HORAS TEORÍA: 3 HORAS PRÁCTICA: 3 DIVISIÓN CIENCIAS BÁSICAS E INGENIERÍA UNIDAD DE ENSEÑANZA
PROGRAMA DE ESTUDIOS UNIVERSIDAD AUTÓNOMA METROPOLITANA UNIDAD: IZTAPALAPA NIVEL: EN LICENCIATURA QUÍMICA : HORAS TEORÍA: 3 HORAS PRÁCTICA: 3 DIVISIÓN CIENCIAS BÁSICAS E INGENIERÍA UNIDAD DE ENSEÑANZA
Métodos Espectrofotométricos. Capítulos 24 y 25 de Fundamentos de Química Analítica Skoog-West-Holler-Crouch (octava Ed.)
 Métodos Espectrofotométricos Capítulos 24 y 25 de Fundamentos de Química Analítica Skoog-West-Holler-Crouch (octava Ed.) 1 Radiación electromagnética Longitud de onda : Frecuencia en s -1 Hertz Numero
Métodos Espectrofotométricos Capítulos 24 y 25 de Fundamentos de Química Analítica Skoog-West-Holler-Crouch (octava Ed.) 1 Radiación electromagnética Longitud de onda : Frecuencia en s -1 Hertz Numero
MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA
 MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA y EL VISIBLE La espectroscopia de absorción molecular en el ultravioleta y visible se emplea en el análisis cuantitativo y es
MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA y EL VISIBLE La espectroscopia de absorción molecular en el ultravioleta y visible se emplea en el análisis cuantitativo y es
A) FUNDAMENTOS DE QUÍMICA B) DATOS BÁSICOS DEL CURSO C) OBJETIVOS DEL CURSO
 UNIVERSIDAD AUTÓNOMA DE SAN LUIS POTOSI Facultad de Ciencias Programas Analíticos de los primeros dos semestres de la licenciatura en Biofísica. 1) NOMBRE DE CADA CURSO O ACTIVIDAD CURRICULAR A) FUNDAMENTOS
UNIVERSIDAD AUTÓNOMA DE SAN LUIS POTOSI Facultad de Ciencias Programas Analíticos de los primeros dos semestres de la licenciatura en Biofísica. 1) NOMBRE DE CADA CURSO O ACTIVIDAD CURRICULAR A) FUNDAMENTOS
La teoría atómica de Dalton (1808)
 EL ÁTOMO Evolución de los modelos atómicos, partículas atómicas, masa y número atómico, mol, elementos e isótopos, modelo atómico contemporáneo, números cuánticos, principio de aufbau, principio de Pauli,
EL ÁTOMO Evolución de los modelos atómicos, partículas atómicas, masa y número atómico, mol, elementos e isótopos, modelo atómico contemporáneo, números cuánticos, principio de aufbau, principio de Pauli,
Fundación H. A. Barceló Facultad de Medicina Licenciatura en Nutrición ISOMERÍA
 ISOMERÍA El término isomería procede del griego (isos = igual; meros = parte) y se refiere a la propiedad que presentan algunos compuestos, particularmente los orgánicos, de poseer la misma fórmula molecular,
ISOMERÍA El término isomería procede del griego (isos = igual; meros = parte) y se refiere a la propiedad que presentan algunos compuestos, particularmente los orgánicos, de poseer la misma fórmula molecular,
CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH.
 Pag:1 Ya hemos visto cómo podemos averiguar la fórmula empírica y molecular de un compuesto. En este tema conoceremos varias técnicas analíticas que combinadas nos podrán ayudar a identificar la fórmula
Pag:1 Ya hemos visto cómo podemos averiguar la fórmula empírica y molecular de un compuesto. En este tema conoceremos varias técnicas analíticas que combinadas nos podrán ayudar a identificar la fórmula
Electrón: LAS PARTÍCULAS SUBATÓMICAS. Electrón: e - Carga eléctrica: 1,602x10-19 C Masa: 9,109x10-31 C
 ENLACE QUÍMICO 1. Repaso de los Conceptos Básicos: Las partículas del átomo: Electrón, Protón y neutrón Número atómico, número másico, Isótopos 2. Modelos atómicos: Repaso de los modelos atómicos Modelo
ENLACE QUÍMICO 1. Repaso de los Conceptos Básicos: Las partículas del átomo: Electrón, Protón y neutrón Número atómico, número másico, Isótopos 2. Modelos atómicos: Repaso de los modelos atómicos Modelo
COLEGIO SAN JOSÉ - Hijas de María Auxiliadora C/ Emilio Ferrari, 87 - Madrid Departamento de Ciencias Naturales
 TEMA 3. FORMULACIÓN ORGÁNICA EJERCICIOS 3. Grupos funcionales 1. Se dan las siguientes moléculas utilizando su fórmula semidesarrollada. Indica a qué familia pertenecen y escribe la fórmula desarrollada
TEMA 3. FORMULACIÓN ORGÁNICA EJERCICIOS 3. Grupos funcionales 1. Se dan las siguientes moléculas utilizando su fórmula semidesarrollada. Indica a qué familia pertenecen y escribe la fórmula desarrollada
ANTECEDENTES Métodos generales de extracción y purificación
 ANTECEDENTES El estudio de los Agaves es de gran importancia debido a su uso tradicional como medicamento en diferentes culturas como la de la India y México. Los Agaves se utilizan como diuréticos, antisifilítico,
ANTECEDENTES El estudio de los Agaves es de gran importancia debido a su uso tradicional como medicamento en diferentes culturas como la de la India y México. Los Agaves se utilizan como diuréticos, antisifilítico,
BIOLOGIA. Unidad 0.- Conceptos básicos de química para biología. - Los átomos constituyen la unidad más pequeña de la materia ( aprox cm).
 .- Conceptos básicos de química para biología. 1. Los átomos. - Los átomos constituyen la unidad más pequeña de la materia ( aprox. 10-8 cm). - Los átomos están formados por partículas sub-atómicas denominadas
.- Conceptos básicos de química para biología. 1. Los átomos. - Los átomos constituyen la unidad más pequeña de la materia ( aprox. 10-8 cm). - Los átomos están formados por partículas sub-atómicas denominadas
Colegio San Agustín de Atacama Copiapó TEMARIO QUÍMICA. Séptimo Básico:
 UNIDAD CERO: Sustancias puras y mezclas Séptimo Básico: Describir los estados de la materia a nivel macroscópico y molecular. Comprender que toda la materia está constituida por un número reducido de elementos
UNIDAD CERO: Sustancias puras y mezclas Séptimo Básico: Describir los estados de la materia a nivel macroscópico y molecular. Comprender que toda la materia está constituida por un número reducido de elementos
