Resonancia Magnética Nuclear
|
|
|
- Inés Ortega Navarrete
- hace 6 años
- Vistas:
Transcripción
1 RMN 01 MÉTODOS ESPECTROSCÓPICOS APLICADOS A DETERMINACIÓN DE ESTRUCTURAS MOLECULARES Resonancia Magnética Nuclear
2 Resonancia Magnética Nuclear Espectroscopía de RMN es una forma de espectroscopia de Absorción. La mayoría de las espectroscopias requieren transiciones de electrones (p.ej. UV- Visible e Infrarrojo) En RMN, son los núcleos de los átomos los que producen la respuesta. Es necesario aplicar un campo magnético para que se produzcan los niveles energéticos que se lugar a las transiciones que por absorción de energía.
3 Aparición de estados energéticos de núcleos en presencia de un campo magnético. Nucleo de espín½ = Barra Magnética
4 Aparición de estados energeticos de núcleos en presencia de un campo magnético. Nucleo de espín½ = Barra Magnética
5 Poblaciones de niveles energéticos para núcleos de 1 (espín ½) en un campo magnético Campo magnético aplicado B o E a E hv0 Sin la aplicación de un campo magnético, no existe división de energia
6 Estados energéticos de los núcleos en presencia de campos magnéticos Los núcleos como los electrones tienen la propiedad de espín, que está caracterizada por: p I momento angular cuantizado en unidades de h/(2π) número cuántico de espin toma valores enteros o semienteros p I I 1 h 2 El momento angular esta relacionado directamente con el momento dipolar magnético μ, a través de p I I 1 h 2 γ constante giromagnética, depende del tipo de núcleo
7 Estados energéticos de los núcleos en presencia de campos magnéticos Existen 2I+1 estados energéticos discretos: I I-1 I-2 -I Este es llamado el estado magnético cuántico, m I. La situación mas simple se da para un sistema con dos estados de energía, p.ej. I = ½. Este es el caso de 1, 13 C, 19 F y 31 P que tiene espín ½, por lo tanto tienen: ½ -½
8 Descripción mecano-cuántica de la RMN El momento angular está cuantizado Niveles nucleares de Zeeman I es un número cuántico de espín que viene determinado principalmente por el número de protones y neutrones desapareados.
9 Descripción mecano-cuántica de la RMN Los núcleos con I = 0, L= 0, lo que implica que =0 y no son activos en RMN o no dan señal RMN.
10 Nucleos magnéticamente activos I A Z Z es par y A es par I = 0 C 12 6 O 16 8 S I A Z Z es par o impar y A es impar I = ½, 3/2, 5/2 1 1 C 13 6 P Todos 1/2 I A Z Z es impar y A es par I = entero 1,2, Li 6 3 N 14 7 Todos 1 I = 0 inactivo I > ½ Núcleo cuadrupolar (poseen momento eléctrico cuadrupolar, -carga nuclear no esferica-posee rápida relajación) I = ½ nucleo activo
11 Propiedades Magnéticas de los cuatro núcleos mas comúnmente usados en RMN. Núcleo Cte giromagnetica (radian T -1 s -1 ) Sensibilidad Relativa Frecuencia de absorción (Mz) x C x F x P x Todos estos nucleos tiene spin I = ½!
12 Nucleos magnéticamente activos
13 Poblaciones de niveles energéticos para núcleos de 1 (espín ½) en un campo magnético Energía Potencial, E, y la diferencia de diferencia entre los dos estados : E 1 2 h 4 B 0 0 Campo magnético aplicado B o E h 2 B 0 E 1 2 h 4 B 0
14 Poblaciones de niveles energéticos para núcleos de 1 (espín ½) en un campo magnético La población relativa depende de la ecuación de Boltmann
15 Poblaciones de niveles energéticos para núcleos de 1 (espín ½) en un campo magnético En general, la energía potencial, E, de una energía estado/orientación esta relacionado al número cuántico: mh E m 2 B 0
16 Transiciones de energía en estados de los núcleos Ecuación de Planck relación entre ΔE y la frecuencia aplicada ν 0 E hv or 2 2 B E v B v B h B h v h E v 0 2 B mh E m
17 Relación entre frecuencia de resonancia y la fuerza del campo aplicado v E 0 B 0 400Mz 9.4Tesla v B 1 01 v2 11.7Tesla v B v 2 500Mz v v 400Mz 500Mz 13 v Mz v C C 13 v v C 13 C125Mz
18 Poblaciones de niveles energéticos para núcleos de 1 (espín ½) en un campo magnético
19 El experimento de onda continua
20 El experimento de onda continua B 0 B 0 ω 0 ω μ θ μ Z Absorción* Emisión ω ω 0 μ θ μ Z m=+1/2 *radiación circularmente polarizada m=-1/2 μ Z μ θ Vector de campo magnetico marco de referencia rotante espin axial del núcleo ángulo entre vector magnetico y el eje de espian de la particual
21 Primer espectro de un compuesto sólido Purcell
22 Primer espectro de un compuesto líquido - Bloch
23 Premio Nobel en Física 1952 Felix Bloch y Edward Mills Purcell Por el desarrollo de un nuevo método para medir mediante un método preciso la resonancia magnética y los descubrimientos asociados " Stanford University, Stanford, CA, USA arvard University, Cambridge, MA, USA
24 Primer espectro de RMN observado por Bloch
25 Instrumentación Primero equipos
26 Primer espectro de un compuesto líquido - Bloch
27 El experimento de onda continua
28 El experimento de onda continua
29 Cuando la explicación cuántica termina, comienza la clásica
30 El experimento de transformada de Fourier z z y M 0 y x x Sistema de referencia del Laboratorio (estático) B 0 B 0 Sistema de referencia rotante
31 El experimento de transformada de Fourier
32 El experimento de transformada de Fourier
33 El experimento de transformada de Fourier Rotating Frame of Reference z M 0 y x B 0
34 Pulse Delay El experimento de transformada de Fourier time Delay Acquisition time
35 El experimento de transformada de Fourier time z z 90º M 0 RF y M 0 y B 1 x B 0 x B 0
36 El experimento de transformada de Fourier z z RF α M 0 M z y y M y B 1 B 1 x B 0 x B 0 1 B α angle of rotation in radians γ magnetogyric ratio (radians T -1 s -1 ) B 1 induced magnetic field (T) τ pulse width (s) M y M 0 cos
37 El experimento de transformada de Fourier time z M 0 y x B 0
38 El experimento de transformada de Fourier 0 time z z z z M 0 y y y M 0 y x x M 0 x M 0 x
39 Relajación de M xy durante FT-RMN Respuesta debido a T 1 y T 2
40 Las bases de la RMN con transformada de Fourier: El decaimiento inducido libre Free induction decay
41 Mejora de la relación señal-ruido Con la acumulación digital de FIDs, S n N n S N n n n n n n S N n Donde n es el número total de scans adquiridos
42 El experimento de transformada de Fourier
43 El experimento de transformada de Fourier
44 El experimento de transformada de Fourier
45 El experimento de transformada de Fourier
46 El experimento de transformada de Fourier
47 El experimento de transformada de Fourier
48 El experimento de transformada de Fourier
49 Instrumentación RMN: Imán superconductor Diseño standard magneto de equipos de Mz
50 S N Directional Coupler Instrumentación: Componentes principales del equipo Preamp RF Amplifier RF Transmitter Phase Sensitive Detector IG SPEED Data Recorder Pulse Switch Computer to Perform FT Frequency Synthesizer Output (Video/ard Copy)
51 Instrumentación: Equipos de alto campo Mz
52 Desplazamiento químico () - Terminología Etapa 1: Definición de un Punto de refencia En RMN de 1 el standard interno es el tetrametil silano (TMS), oos grupos metilo están islados, y todos protones son magneticamente equivalentes. La contante de apantallamiento del TMS es mayor que la mayoria de los protones presente en compuestos orgánicos. Etapa 2: Definición de una escala La frecuencia de resonancia es dependiente de la magnitud de campo magnético aplicado, debido a esto es necesaria una escala que permita comparar espectros independientemente del equipo en que fueron adquiridos (independiente del campo magnético) vs v v r r ν r frecuencia de resonancia de referencia (TMS para RMN de 1 ) ν s frecuencia de resonancia del nucleo
53 r s r r s r r r s s r r s r s s s r r r r s k k v v v k k k v v k v k v v v v Debido a lo que sabemos (para RMN de 1 NMR para espectro de TMS como estandar interno) σ r << 1, entonces s r r r s v v v Desplazamiento químico () - Terminología
54 Desplazamiento químico () - Terminología Etapa 2: Definición de una escala (cont.) Para que los valores de desplazamiento tengas magnitudes manejables,se aplica la sieguiente definición. v s v v r r r s Skoog, et al., definieron el Desplazamiento químico con la letra δ según 6 r 10 s Y se expresa en unidades de ppm (partes por millón)
55 Desplazamiento químico () v s v v r r 1.00 ppm z
56 Desplazamiento químico () ppm Frecuencia de resonancia 6 10
57 Origen del apantallamiento y las diferencias en el desplazameinto químico 1. Los electrones cercanos al núcleo The closest electrons to a nucleus are those that bond the nucleus to its neighboring atoms. 2. Bajo al influencia del campo magnético, los electrones de enlaces tiene a precesar en un plano perpendicular al campo aplicado. Electrones circulantes B 0 Campo magnético opuesto σb 0 3. Cualquier factor que afecta la distribución de estos electrones de enlace también afectará el grado de apantallamiento que el núcleo experimenta. Por lo tanto, la electronegatividad de los enlaces de los átomos cercanos son extremadamente importantes.
58 Diferencias en el desplazamiento químico Compuesto C 3 X C 3 C 3 I C 3 Br C 3 Cl C 3 F Elemento X I Br Cl F Electronegatividad X Desplazamiento qco (δ)
59 Diferencias en el desplazamiento químico Verde Azul
60 Diferencias en el desplazamiento químico
61 Increasing Electronegativity Diferencias en el desplazamiento químico δ C C C C C C 3 0.9
62 Diferencias en el desplazamiento químico Circulation of electrons within molecular orbitals results in local magnetic fields that oppose the applied magnetic field. A higher shielding of the nuclear results in a lower B eff for the nucleus of interest. A smaller value for B means a slightly lower energy of transition.
63 Diferencias en el desplazamiento químico Corriende de anillo B 0 σb 0 σb 0 Campo magnético
64 Increasing Electronegativity Diferencias en el desplazamiento químico δ C C C C C C 3 0.9
65 Diferencias en el desplazamiento químico B 0 C C C B 0 C
66
67
68
69 Corriente de anillo en alquinos 69
70 Corrientes de anillo en compuestos carbonílicos 70
71 Anisotropia de compuestos aromáticos La anisotropía (opuesta de isotropía) es la propiedad general de la materia según la cual cualidades como: elasticidad, temperatura, conductividad, velocidad de propagación de la luz, etc. varían según la dirección en que son examinadas. Corriente de anillo B 0 σb 0 σb 0 Campo magnético 71
72 Anisotropia de compuestos aromáticos C 3 ring ppm Me ppm C 3 ring ppm Me ppm OUTSIDE 9.28 ppm INSIDE ppm 72
73 Anisotropia de compuestos aromáticos 73
74 Anisotropia de compuestos aromáticos 74
75 Anisotropia de compuestos aromáticos 75
76 Efectos electrónicos 2 C O + 2 C Desprotección O - O 3 C 3 C COOEt COOEt 7.10 ppm O 6.28 ppm 6.83 ppm O COOEt EtOOC O 6.10 ppm O 5.93 ppm 7.07 ppm 6.38 ppm 7.71 ppm 6.28 ppm 76
77 Efectos electrónicos conjugación con carbonilo. O O
78 Efectos electrónicos conjugación con carbonilo. O 1 desprotección
79 Efectos electrónicos enoles O O + C - protegido S 6.06 ppm S 5.81 ppm 5.48 ppm O 6.22 ppm O 5.78 ppm 4.82 ppm 79
80 Efectos electrónicos enoles 4 O
81 Efectos electrónicos enoles 4 O protegido
82 Efectos electronicos: conjugación con carbonilo o m O C 3 p desprotegido desprotegido
83 Efectos electrónicos: conjugación con heteroátomo 3 C O protegido protegido m p o
84 Efectos electrónicos: conjugación con heteroátomo 3 C N m p o Protegido Protegido
85 Enlace hidrógeno 85
86 Efectos electrónicos: grupo carbonilo 86
87 Efectos electrónicos: grupo carbonilo 87
88 Efectos electrónicos: grupo alquino 88
89
90 Origen del desdoblamiento espin-espin El desdoblamiento espin-espin occurre cuando el momento magnético de un núcleo (µ A ) interacciona con el momento magnético del núcleo adyancente (µ B, µ C, etc.). A X Interacciones Polarizantes : Los momentos magnéticos son transmitidos a través de los electrones de los enlaces. El acoplamiento puede transmitirse a traves de enlaces lejanos y poder producir un efecto visible, generando un desdoblamiento. La constante de acoplamiento es INDEPENDIENTE del campo aplicado debido a que se transmite por los electrones. El cambio del campo en un espectro cambia el patron pero no el desplazamiento químico.
91 Origen del desdoblamiento espin-espin
92 Origen del desdoblamiento espin-espin
93 Origen del desdoblamiento espin-espin C 3 -C 2 -O
94 Energy Origen del desdoblamiento espin-espin C 3 -C 2 -O B 0
95 Origen del desdoblamiento espin-espin Energy C 3 -C 2 -O Because the neighboring nuclei oppose B 0, the magnetic field felt by the methyl protons is lessened. B 0
96 Origen del desdoblamiento espin-espin Energy II C 3 -C 2 -O III I I II B 0 III
97 Energy Origen del desdoblamiento espin-espin Ejemplo: etanol C 3 -C 2 -O B 0
98 Origen del desdoblamiento espin-espin Energy C 3 -C 2 -O I II III B 0 IV
99 Constantes de acoplamiento en diferentes campos ν 0 = Mz A B C D
100 Constantes de acoplamiento en diferentes campos ν 0 = Mz A B J AB J BA
101 Constantes de acoplamiento en diferentes campos ν 0 = Mz A J AB J AC J AC
102 Constantes de acoplamiento en diferentes campos ν 0 = Mz 10 z 4 z 4 z 10 z ν 0 = Mz 4 z 4 z
103 Constantes de acoplamiento en diferentes campos ν 0 = Mz 10 z 4 z 4 z 12.5 z ν 0 = Mz 4 z 4 z
104 Constantes de acoplamiento en diferentes campos pico n
105 Reglas para la interpretación de espectros de primer orden En los espectros de primer orden el valor de desplazamiento químico de los núcleos que interaccionan es más grande que las cosntante de acoplamiento, J. Para garantizar conducta de primer orden se debe tener δ/j > 8. En la mayoría de los casos se usan valores mayores para tener primer orden Se debe tener en cuenta que: Núcleos equivalentes no producen desdoblamiento Las constantes de acoplamiento disminuyen con la distancia, es raro ver acoplamientos a mas de 4 enlaces. La regla n + 1 aplica cuando n es el numero de núcleos magnéticamente equivalentes
106
107 Patrones de acoplamiento: Triangulo de Pascal Contante de acoplamiento iguales Singlete Doblete Triplete Cuarteto Multipletes n=2 n=3 n=4 n=5 n=6
108 Acoplamiento escalar: ejemplos a b a b C C C C b b a b b a b C C b b C C C b b a b b b C C C
109 Acoplamiento escalar n = b 2n + 1 lineas C 3 b C 3 a a doublete septeto
110 Acoplamiento escalar n = m 2n + 1 lineas o p m o b a Br p a 2 x triplete b
111 Acoplamiento escalar n = n + 1 lineas c b a 2 x triplete 1 quinteto a c Br b
112 Acoplamiento escalar n = Triplete: 2 C3 Roof effect 0.9 ppm C (ppm) Int mult J (z) COMMENT triplete 7 C3->(C2) triplete 7 C3->(C2) sextuplete 7 C2 (C3, C2) quintuplete 7 C2 (C2, C2) cuatriplete7 =C- C2 (C3) triplete 7 C2 -O (C2) C2 C2 O O cuatriplete C2 2.3 C x triplete 3 3 C7 14 O2 I = 7-14/2 + 1 = 1 2n + 1 lines 2 Quintuplete 2 Multiplete:
113 Acoplamiento escalar n = Triplete: C nI + 1 lines 4 O 5 O Cuartriplete: 5 C 3 6 Quintuplete: 3 Multiplete: 2 2 x triplete
114 Acoplamiento geminal 2J-
115 Acoplamiento geminal 2 J - Orientación del enlace Efecto de electronegatividad del sustituyente
116 3 J Acoplamiento vecinal 3 J -
117 Acoplamiento escalar: ejemplos J ab = J ab c a b a b C C b J ab J ab C qd C C b b b a b C C C J ab td c a b b a b C C C C C C b b
118 Acoplamiento vecinal 3J-
119 Acoplamiento vecinal 3 J - Curva acoplamiento vecinal en cicloalcanos. Ecuación de Bothner-By
120 Acoplamiento vecinal 3 J - a Las constantes de acoplamiento vecinal de pueden usar para estrablecer la esteriquímica de compuestos cíclicos J ad J ab J ac
121 Acoplamiento a larga distancia 4J- y 4J-
122 Acoplamiento a larga distancia 4 J - y 4 J - 4 N 5 4 J 1-3 = 1.07 z 5 J 1-4 = 1.21 z 5 J 1-5 = 0.95 z 5 J 4-7 = 0.67 z C C C 4 J - = 9 z 1 7 C C C C 5 J - = 3 z 4 J - = 1-2 z C C C 4 J - = 3 z 4 J - = 1.1 z C C C C 5 J - = 3 z
123 300 Mz ¹ NMR In C D C l Sigma -A ldric h C o. A LL R IG TS R ESER V ED
124
125 300 Mz ¹ NMR In C D C l3 300 Mz ¹ NMR In C D C l3 1,40 1,35 1,30 1,25 1,20 1,15 1,10 1,05 1,00 0,95 0,90 0,85 0,80 Sigma -Aldrich C o. A LL R IG TS R ESER V ED Sigma -A ldric h C o. A LL R IG TS R ESER V ED
126 300 Mz ¹ NMR In C D C l Sigma -A ldric h C o. A LL R IG TS R ESER V ED
127 300 Mz ¹ NMR In C D C l Sigma -A ldric h C o. A LL R IG TS R ESER V ED
128 300 Mz ¹ NMR In C D C l Sigma -A ldric h C o. A LL R IG TS R ESER V ED
RESONANCIA MAGNÉTICA NUCLEAR
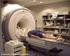 RESONANCIA MAGNÉTICA NUCLEAR SPIN DEL NUCLEO El nucleo de algunos átomos poseen SPIN. Estos núcleos se comportan como si estuvieran girando... no sabemos si realmente giran! Es como la propiedad de un
RESONANCIA MAGNÉTICA NUCLEAR SPIN DEL NUCLEO El nucleo de algunos átomos poseen SPIN. Estos núcleos se comportan como si estuvieran girando... no sabemos si realmente giran! Es como la propiedad de un
TEMA 2: Resonancia Magnética Nuclear RMN-1H y 13C Fundamentos
 Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
Resonancia Magnética Nuclear
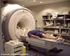 Resonancia Magnética Nuclear Por qué algunas señales aparecen como señales múltiples (multipletes)? Dos átomos que se encuentren contiguos interaccionan modificándose mutuamente. La forma de la señal depende
Resonancia Magnética Nuclear Por qué algunas señales aparecen como señales múltiples (multipletes)? Dos átomos que se encuentren contiguos interaccionan modificándose mutuamente. La forma de la señal depende
J H,H pequeño. Equivalencia química y equivalencia magnética
 La magnitud de J para 1 H, 1 H varía entre -20 y 20 Hz J a 2 enlaces 2 J H,H 10-15 Hz J a 3 enlaces 3 J H,H 3-10 Hz J a larga distancia H-C-C-C-H 4 J H,H pequeño Los J heteronucleares son mas grandes,
La magnitud de J para 1 H, 1 H varía entre -20 y 20 Hz J a 2 enlaces 2 J H,H 10-15 Hz J a 3 enlaces 3 J H,H 3-10 Hz J a larga distancia H-C-C-C-H 4 J H,H pequeño Los J heteronucleares son mas grandes,
Tema 3.-Espectroscopía de biomoléculas
 Tema 3.Espectroscopía de biomoléculas Tema 3.Espectroscopía de biomoléculas 3..El espectro electromagnético 3.2.Espectros de absorción y de emisión (espontánea y estimulada) 3.2..Momento dipolar de transición:
Tema 3.Espectroscopía de biomoléculas Tema 3.Espectroscopía de biomoléculas 3..El espectro electromagnético 3.2.Espectros de absorción y de emisión (espontánea y estimulada) 3.2..Momento dipolar de transición:
TEMA 10. ESPECTROSCOPIA DE RESONANCIA MAGNÉTICA NUCLEAR
 TEMA 10. ESPETROSOPIA DE RESONANIA MAGNÉTIA NULEAR 1. Fundamentos físicos de la espectroscopia de RMN. 2. El espectrómetro de resonancia magnética nuclear. 3. Resonancia magnética nuclear de 1. Apantallamiento
TEMA 10. ESPETROSOPIA DE RESONANIA MAGNÉTIA NULEAR 1. Fundamentos físicos de la espectroscopia de RMN. 2. El espectrómetro de resonancia magnética nuclear. 3. Resonancia magnética nuclear de 1. Apantallamiento
Conceptos de relajación en RMN
 Conceptos de relajación en RMN Oscar Millet Unidad de Biología Estructural CICbioGUNE Curso Avanzado de Resonancia Magnética Nuclear, Jaca 2009 Relajación: retorno de la magnetización a la situación de
Conceptos de relajación en RMN Oscar Millet Unidad de Biología Estructural CICbioGUNE Curso Avanzado de Resonancia Magnética Nuclear, Jaca 2009 Relajación: retorno de la magnetización a la situación de
Resonancia Magnética Nuclear
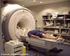 Víctor Moreno de la Cita Jesús J. Fernández Romero 25 de mayo de 2010 1 Base teórica 2 Medicina Química y análisis no destructivo Computación cuántica 3 4 Notación que emplea Kittel: µ = Momento magnético
Víctor Moreno de la Cita Jesús J. Fernández Romero 25 de mayo de 2010 1 Base teórica 2 Medicina Química y análisis no destructivo Computación cuántica 3 4 Notación que emplea Kittel: µ = Momento magnético
1.- Fundamentos básicos
 1.- Fundamentos básicos - Algunos núcleos tienen espín: La circulación de carga genera un campo magnético a lo largo del eje de giro ( 1 H, 7 Li, 11 B, 13 C, 14 N, 19 F, 23 Na, 27 Al, 29 Si, 31 P, 33 S,
1.- Fundamentos básicos - Algunos núcleos tienen espín: La circulación de carga genera un campo magnético a lo largo del eje de giro ( 1 H, 7 Li, 11 B, 13 C, 14 N, 19 F, 23 Na, 27 Al, 29 Si, 31 P, 33 S,
RADIACIÓN ELECTROMAGNÉTICA Y ESPECTROS ATÓMICOS. Tipos de radiaciones electromagnéticas según λ.
 RADIACIÓN ELECTROMAGNÉTICA Y ESPECTROS ATÓMICOS λ Tipos de radiaciones electromagnéticas según λ. Rayos γ Rayos X Rayos UV Radiación visible. Rayos IR Microondas Ondas de radio Ondas de radar Ondas de
RADIACIÓN ELECTROMAGNÉTICA Y ESPECTROS ATÓMICOS λ Tipos de radiaciones electromagnéticas según λ. Rayos γ Rayos X Rayos UV Radiación visible. Rayos IR Microondas Ondas de radio Ondas de radar Ondas de
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO. Lola Castelao
 ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
ESTRUCTURA DE LA MATERIA Y SISTEMA PERIÓDICO DALTON: el átomo es indivisible. MODELOS ATÓMICOS THOMSON: el átomo es una especie de pudín, formado por una masa cargada positivamente, dentro del cual se
Resonancia Magnetica Nuclear Avanzada
 Resonancia Magnetica Nuclear Avanada Ala-Arg-Pro-Tr-Asn-Phe-Cpa-Leu-NH 2 Cpa Ala Pro Facultad De Quimica Que es la espectroscopia? Sin aprender griego o latin, la espectroscopia es el estudio de las interacciones
Resonancia Magnetica Nuclear Avanada Ala-Arg-Pro-Tr-Asn-Phe-Cpa-Leu-NH 2 Cpa Ala Pro Facultad De Quimica Que es la espectroscopia? Sin aprender griego o latin, la espectroscopia es el estudio de las interacciones
CURSO DE RESONANCIA MAGNETICA NUCLEAR
 CURSO DE RESONANCIA MAGNETICA NUCLEAR El espectro electromagnético y su aplicación en el diagnóstico por imágenes Lic. Carlos R. Sánchez Qué es el espectro electromagnético? Se conoce como espectro de
CURSO DE RESONANCIA MAGNETICA NUCLEAR El espectro electromagnético y su aplicación en el diagnóstico por imágenes Lic. Carlos R. Sánchez Qué es el espectro electromagnético? Se conoce como espectro de
DETERMINACIÓN ESTRUCTURAL (Teoría) CURSO , GRUP A 9 de febrero Apellidos... Nombre...
 DETERMINAIÓN ESTRUTURAL (Teoría) URS 2003-2004, GRUP A 9 de febrero 2004 Apellidos... Nombre... 1.- Que diferencias espera encontrar entre el 3 - y el 3 -D. a) en sus espectros de masas. El ión molecular
DETERMINAIÓN ESTRUTURAL (Teoría) URS 2003-2004, GRUP A 9 de febrero 2004 Apellidos... Nombre... 1.- Que diferencias espera encontrar entre el 3 - y el 3 -D. a) en sus espectros de masas. El ión molecular
Capítulo 1. Antecedentes de la Química Cuántica y primeras Teorías Atómicas
 Capítulo 1. Antecedentes de la Química Cuántica y primeras Teorías Atómicas Objetivos: Recordar y actualizar los conocimientos sobre las características de electrones, protones y neutrones Describir la
Capítulo 1. Antecedentes de la Química Cuántica y primeras Teorías Atómicas Objetivos: Recordar y actualizar los conocimientos sobre las características de electrones, protones y neutrones Describir la
UNIVERSIDAD SANTO TOMAS SECCIONAL BUCARAMANGA. División de Ingenierías - Facultad de Química Ambiental
 UNIVERSIDAD SANTO TOMAS SECCIONAL BUCARAMANGA División de Ingeniería Facultad de Química Ambiental Nombre de Asignatura: QUÍMICA INSTRUMENTAL II Àrea: Básicas de Química / Química Analítica Créditos: 4
UNIVERSIDAD SANTO TOMAS SECCIONAL BUCARAMANGA División de Ingeniería Facultad de Química Ambiental Nombre de Asignatura: QUÍMICA INSTRUMENTAL II Àrea: Básicas de Química / Química Analítica Créditos: 4
UNIVERSIDAD NACIONAL DEL SUR 1
 UNIVERSIDAD NACIONAL DEL SUR 1 PROGRAMA DE: CODIGO: 393 H O R A S D E C L A S E P R O F E S O R R E S P O N S A B L E T E O R I C A S P R A C T I C A S Dra. Alicia B. Chopa Por semana Por cuatrimestre
UNIVERSIDAD NACIONAL DEL SUR 1 PROGRAMA DE: CODIGO: 393 H O R A S D E C L A S E P R O F E S O R R E S P O N S A B L E T E O R I C A S P R A C T I C A S Dra. Alicia B. Chopa Por semana Por cuatrimestre
RADIACIÓN ELECTROMAGNÉTICA
 FACULTAD DE CIENCIAS QUÍMICAS Espectrometría Objeto de Estudio Nº 1 LECTURA N 1 RADIACIÓN ELECTROMAGNÉTICA Bibliografía: SKOOG, D.A.; Leary J.J.; ANÁLISIS INSTRUMENTAL, 4 ed.; Ed. McGraw-Hill (1994), págs.
FACULTAD DE CIENCIAS QUÍMICAS Espectrometría Objeto de Estudio Nº 1 LECTURA N 1 RADIACIÓN ELECTROMAGNÉTICA Bibliografía: SKOOG, D.A.; Leary J.J.; ANÁLISIS INSTRUMENTAL, 4 ed.; Ed. McGraw-Hill (1994), págs.
Experimento 12 LÍNEAS ESPECTRALES. Objetivos. Teoría. Postulados de Bohr. El átomo de hidrógeno, H
 Experimento 12 LÍNEAS ESPECTRALES Objetivos 1. Describir el modelo del átomo de Bohr 2. Observar el espectro del H mediante un espectrómetro de rejilla 3. Medir los largos de onda de las líneas de la serie
Experimento 12 LÍNEAS ESPECTRALES Objetivos 1. Describir el modelo del átomo de Bohr 2. Observar el espectro del H mediante un espectrómetro de rejilla 3. Medir los largos de onda de las líneas de la serie
Práctica 6 ANÁLISIS DE CONTAMINANTES MEDIANTE TÉCNICAS DE RESONANCIA MAGNÉTICA NUCLEAR, GASES/MASAS E INFRARROJO
 Práctica 6 ANÁLISIS DE CONTAMINANTES MEDIANTE TÉCNICAS DE RESONANCIA MAGNÉTICA NUCLEAR, GASES/MASAS E INFRARROJO 1. Objetivo El objetivo de la presente práctica es la identificación cualitativa de compuestos
Práctica 6 ANÁLISIS DE CONTAMINANTES MEDIANTE TÉCNICAS DE RESONANCIA MAGNÉTICA NUCLEAR, GASES/MASAS E INFRARROJO 1. Objetivo El objetivo de la presente práctica es la identificación cualitativa de compuestos
El ÁTOMO de HIDRÓGENO
 El ÁTOMO de HIDRÓGENO Dr. Andres Ozols Dra. María Rebollo FIUBA 006 Dr. A. Ozols 1 ESPECTROS DE HIDROGENO espectros de emisión espectro de absorción Dr. A. Ozols ESPECTROS DE HIDROGENO Secuencias de las
El ÁTOMO de HIDRÓGENO Dr. Andres Ozols Dra. María Rebollo FIUBA 006 Dr. A. Ozols 1 ESPECTROS DE HIDROGENO espectros de emisión espectro de absorción Dr. A. Ozols ESPECTROS DE HIDROGENO Secuencias de las
Operador de densidad y operadores producto en resonancia magnética nuclear
 Operador de densidad y operadores producto en resonancia magnética nuclear Juan Carlos Paniagua Dep. de Química Física & Institut de Química Teòrica i Computacional - Universitat de Barcelona Presentación
Operador de densidad y operadores producto en resonancia magnética nuclear Juan Carlos Paniagua Dep. de Química Física & Institut de Química Teòrica i Computacional - Universitat de Barcelona Presentación
Modelo Atómico. Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran embebidos los electrones con carga (-)
 Modelo Atómico 1 Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran embebidos los electrones con carga () Electrón Conceptos:» Neutralidad eléctrica» Carga elemental del
Modelo Atómico 1 Thompson (1898): Esfera uniforme de materia con carga (+) en la cual se encuentran embebidos los electrones con carga () Electrón Conceptos:» Neutralidad eléctrica» Carga elemental del
Elucidación Estructural de Biomoléculas utilizando Resonancia Magnética Nuclear
 Universidad de Los Andes Facultad de Ciencias Postgrado Interdisciplinario en Química Aplicada Mención Estudio de Materiales Elucidación Estructural de Biomoléculas utilizando Resonancia Magnética Nuclear
Universidad de Los Andes Facultad de Ciencias Postgrado Interdisciplinario en Química Aplicada Mención Estudio de Materiales Elucidación Estructural de Biomoléculas utilizando Resonancia Magnética Nuclear
S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS
 S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS NOMBRE DE LA ASIGNATURA: QUIMICA ANALITICA II (4-2-10) NIVEL: LICENCIATURA. CARRERA: INGENIERIA BIOQUIMICA INGENIERIA QUIMICA CLAVE: ACC-9331
S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS NOMBRE DE LA ASIGNATURA: QUIMICA ANALITICA II (4-2-10) NIVEL: LICENCIATURA. CARRERA: INGENIERIA BIOQUIMICA INGENIERIA QUIMICA CLAVE: ACC-9331
ESPECTROSCOPIA DE RESONANCIA MAGNÉTICA NUCLEAR
 ESPECTROSCOPIA DE RESONANCIA MAGNÉTICA NUCLEAR La espectroscopia de resonancia magnética nuclear (RMN) se basa en la medida de la absorción de la radiación electromagnética en la región de las radiofrecuencias
ESPECTROSCOPIA DE RESONANCIA MAGNÉTICA NUCLEAR La espectroscopia de resonancia magnética nuclear (RMN) se basa en la medida de la absorción de la radiación electromagnética en la región de las radiofrecuencias
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica
 Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Ultima actualización 3 de febrero de 205 Índice. Aproximación
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Ultima actualización 3 de febrero de 205 Índice. Aproximación
RESONANCIA MAGNÉTICA NUCLEAR (NMR) Larraona Puy, M. Manjavacas Arévalo, A.
 Si ahora aplicamos un pulso electromagnético de radiofrecuencia a la frecuencia de resonancia, polarizado en una dirección perpendicular al plano de B, se inducirán transiciones por la absorción de fotones
Si ahora aplicamos un pulso electromagnético de radiofrecuencia a la frecuencia de resonancia, polarizado en una dirección perpendicular al plano de B, se inducirán transiciones por la absorción de fotones
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS FUNDAMENTOS ESPECTROSCOPICOS
 UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS FUNDAMENTOS ESPECTROSCOPICOS Alexis Lema Jueves 10-12 ESPECTROSCOPIA UV-VIS. COMBINACIÓN LINEAL DE ORBITALES ATOMICOS (CLOA). ORBITALES ATOMICOS
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS FUNDAMENTOS ESPECTROSCOPICOS Alexis Lema Jueves 10-12 ESPECTROSCOPIA UV-VIS. COMBINACIÓN LINEAL DE ORBITALES ATOMICOS (CLOA). ORBITALES ATOMICOS
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León.
 Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Espectroscopía Clase integradora
 Espectroscopía Clase integradora Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar
Espectroscopía Clase integradora Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar
EXTRUCTURA ATOMICA ACTUAL
 ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS. Partícula Masa (g) Carga (Coulombs) Carga unitaria. Electrón
 MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
Tema 7.- Principios de fotoquímica
 Tema 7.- Principios de fotoquímica Introducción La rama de la química que estudia las transformaciones de las moléculas producidas por la absorción de energía electromagnética Muchas especies en la atmósfera
Tema 7.- Principios de fotoquímica Introducción La rama de la química que estudia las transformaciones de las moléculas producidas por la absorción de energía electromagnética Muchas especies en la atmósfera
Unidad 1 Estructura atómica de la materia. Teoría cuántica
 Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Prefacio... ix COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3
 ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
RADIACIÓN ELECTROMAGNÉTICA Y TÉCNICAS DE OBSERVACIÓN. Curso Introducción a la Astronomía 1
 RADIACIÓN ELECTROMAGNÉTICA Y TÉCNICAS DE OBSERVACIÓN Curso 2011-12 Introducción a la Astronomía 1 Brillo Magnitud aparente El ojo detecta la luz de forma logarítmica, es decir, detecta cambios no de manera
RADIACIÓN ELECTROMAGNÉTICA Y TÉCNICAS DE OBSERVACIÓN Curso 2011-12 Introducción a la Astronomía 1 Brillo Magnitud aparente El ojo detecta la luz de forma logarítmica, es decir, detecta cambios no de manera
El átomo: sus partículas elementales
 El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS. Elucidación estructural: Ejemplo 1 Dados los siguientes espectros:
 ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
SIMETRIAS Y LEYES DE CONSERVACION
 SIMETRIAS Y LEYES DE CONSERVACION 1. Introducción 2. Conservación de la energía y el momento 3. Conservación del momento angular 4. Paridad 5. Isospín 6. Extrañeza 7. Conjugación de carga 8. Inversión
SIMETRIAS Y LEYES DE CONSERVACION 1. Introducción 2. Conservación de la energía y el momento 3. Conservación del momento angular 4. Paridad 5. Isospín 6. Extrañeza 7. Conjugación de carga 8. Inversión
Espectroscopía vibracional y rotacional
 Espectroscopía vibracional y rotacional Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Ultima actualización 19 de marzo de 2015 Índice 1. Interacción de la radiación con la materia
Espectroscopía vibracional y rotacional Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Ultima actualización 19 de marzo de 2015 Índice 1. Interacción de la radiación con la materia
INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3.
 El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
Tema 6: Espectroscopia electrónica
 1.- Introducción -El color es uno de los aspectos más llamativos de los compuestos de coordinación. -Desde antiguo se conocen compuestos de coordinación que se usan como colorantes: Azul de prusia Fe 4
1.- Introducción -El color es uno de los aspectos más llamativos de los compuestos de coordinación. -Desde antiguo se conocen compuestos de coordinación que se usan como colorantes: Azul de prusia Fe 4
EL ÁTOMO 1. El átomo. 2. Modelos atómicos. 3. Núcleo atómico. 4. Espectros atómicos. 5. Modelo atómico cuántico.
 EL ÁTOMO 1. El átomo. 2. Modelos atómicos. 3. Núcleo atómico. 4. Espectros atómicos. 5. Modelo atómico cuántico. Química 1º bachillerato El átomo 1 El átomo no es una partícula indivisible, sino que está
EL ÁTOMO 1. El átomo. 2. Modelos atómicos. 3. Núcleo atómico. 4. Espectros atómicos. 5. Modelo atómico cuántico. Química 1º bachillerato El átomo 1 El átomo no es una partícula indivisible, sino que está
Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA
 Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA 1. Objetivo Familiarizarse con los fundamentos de la identificación de moléculas a partir de su espectro de absorción infrarrojo.
Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA 1. Objetivo Familiarizarse con los fundamentos de la identificación de moléculas a partir de su espectro de absorción infrarrojo.
INTERACCIONES Y MATERIALES MAGNÉTICOS
 INTERACCIONES Y MATERIALES MAGNÉTICOS G U T I É R R E Z N Ú Ñ E Z D E B O R A H V A L E R I A I S L A S B A U T I S T A J O S É A L F R E D O L O E R A R U B A L C A V A J E S S I C A R I V E R O T R E
INTERACCIONES Y MATERIALES MAGNÉTICOS G U T I É R R E Z N Ú Ñ E Z D E B O R A H V A L E R I A I S L A S B A U T I S T A J O S É A L F R E D O L O E R A R U B A L C A V A J E S S I C A R I V E R O T R E
RMN DE SÓLIDOS. Teresa Blasco. Escuela de Jaca, Junio Instituto de Tecnología Química (UPV-CSIC) Valencia
 RMN DE SÓLIDOS Teresa Blasco Instituto de Tecnología Química (UPV-CSIC) Valencia Escuela de Jaca, Junio 2009 RMN de sólidos Es un método extremadamente útil en la caracterización de materiales sólidos
RMN DE SÓLIDOS Teresa Blasco Instituto de Tecnología Química (UPV-CSIC) Valencia Escuela de Jaca, Junio 2009 RMN de sólidos Es un método extremadamente útil en la caracterización de materiales sólidos
Radiación. Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler. L. Infante 1
 Radiación Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler L. Infante 1 Cuerpo Negro: Experimento A medida que el objeto se calienta, se hace más brillante ya que emite más radiación
Radiación Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler L. Infante 1 Cuerpo Negro: Experimento A medida que el objeto se calienta, se hace más brillante ya que emite más radiación
TALLER DE ESPECTROSCOPIA
 TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
DETERMINACIÓN ESTRUCTURAL DE COMPUESTOS ORGÁNICOS (660016)
 DETERMINACIÓN ESTRUCTURAL DE COMPUESTOS ORGÁNICOS (660016) Grado en Química Universidad de Alcalá Curso Académico 2015/2016 3 er Curso 1º Cuatrimestre GUÍA DOCENTE Nombre de la asignatura: DETERMINACIÓN
DETERMINACIÓN ESTRUCTURAL DE COMPUESTOS ORGÁNICOS (660016) Grado en Química Universidad de Alcalá Curso Académico 2015/2016 3 er Curso 1º Cuatrimestre GUÍA DOCENTE Nombre de la asignatura: DETERMINACIÓN
Espectro Electromagnético
 1 Espectro Electromagnético La luz es radiación electromagnética y está compuesta por una parte eléctrica y otra magnética. Las particulas subatómicas, electrones y fotones, tienen propiedades de partículas
1 Espectro Electromagnético La luz es radiación electromagnética y está compuesta por una parte eléctrica y otra magnética. Las particulas subatómicas, electrones y fotones, tienen propiedades de partículas
E n 1946, dos grupos de investigadores
 1. INTRODUCCIÓN HISTÓRICA E n 1946, dos grupos de investigadores dirigidos por F. Bloch y E.M. Purcell observaron, por primera vez e independientemente, una señal de resonancia magnética nuclear. Bloch
1. INTRODUCCIÓN HISTÓRICA E n 1946, dos grupos de investigadores dirigidos por F. Bloch y E.M. Purcell observaron, por primera vez e independientemente, una señal de resonancia magnética nuclear. Bloch
Colegio San Lorenzo - Copiapó - Región de Atacama Per Laborem ad Lucem
 TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
Moléculas poliatómicas con dobles enlaces conjugados en la aproximación de electrones libres
 aterial didáctico para el curso de Química Cuántica Andrés Cedillo Departamento de Química, UA-I arzo de 1991 oléculas poliatómicas con dobles enlaces conjugados en la aproximación de electrones libres
aterial didáctico para el curso de Química Cuántica Andrés Cedillo Departamento de Química, UA-I arzo de 1991 oléculas poliatómicas con dobles enlaces conjugados en la aproximación de electrones libres
Gradientes de Campo Magnético en experimentos de RMN
 VIII Escuela de Verano RMN Jaca 16-junio junio-2009 Gradientes de Campo Magnético en experimentos de RMN Teodor Parella SeRMN UAB Secuencia de pulsos, Espectro y Estructura Experimento RMN: Secuencia de
VIII Escuela de Verano RMN Jaca 16-junio junio-2009 Gradientes de Campo Magnético en experimentos de RMN Teodor Parella SeRMN UAB Secuencia de pulsos, Espectro y Estructura Experimento RMN: Secuencia de
Características físicas del sonido
 Características físicas del sonido Sonido? Propagación de cambios en la densidad de partículas en un medio elástico producto de una perturbación mecánica Transferencia de energía al desplazarse una perturbación
Características físicas del sonido Sonido? Propagación de cambios en la densidad de partículas en un medio elástico producto de una perturbación mecánica Transferencia de energía al desplazarse una perturbación
Ondas. Prof. Jesús Hernández Trujillo Facultad de Química, UNAM. Ondas/J. Hdez. T p. 1
 Ondas Prof. Jesús Hernández Trujillo Facultad de Química, UNAM Ondas/J. Hdez. T p. 1 Introducción Definición: Una onda es una perturbación que se propaga en el tiempo y el espacio Ejemplos: Ondas en una
Ondas Prof. Jesús Hernández Trujillo Facultad de Química, UNAM Ondas/J. Hdez. T p. 1 Introducción Definición: Una onda es una perturbación que se propaga en el tiempo y el espacio Ejemplos: Ondas en una
Propiedades Nucleares.
 Curso 00-00 Propiedades Nucleares.. El radio nuclear Distribución de carga eléctrica Distribución de materia nuclear. Las masas de los núcleos 3. Energía de enlace nuclear 4. Espín y paridad de los núcleos
Curso 00-00 Propiedades Nucleares.. El radio nuclear Distribución de carga eléctrica Distribución de materia nuclear. Las masas de los núcleos 3. Energía de enlace nuclear 4. Espín y paridad de los núcleos
Espectros de emisión y absorción.
 Espectros de emisión y absorción. Los espectros de emisión y absorción de luz por los átomos permitieron la justificación y ampliación del modelo cuántico. Espectros de emisión: Calentar un gas a alta
Espectros de emisión y absorción. Los espectros de emisión y absorción de luz por los átomos permitieron la justificación y ampliación del modelo cuántico. Espectros de emisión: Calentar un gas a alta
TÉCNICAS INSTRUMENTALES FISICOQUÍMICAS
 DPTO. CIENCIAS Y TÉCNICAS FISICOQUÍMICAS 2ª Prueba de Evaluación a Distancia de TÉCNICAS INSTRUMENTALES FISICOQUÍMICAS Curso 2009-2010 Técnicas Instrumentales Fisicoquímicas. 2ª PED (2009-10) 1 Instrucciones
DPTO. CIENCIAS Y TÉCNICAS FISICOQUÍMICAS 2ª Prueba de Evaluación a Distancia de TÉCNICAS INSTRUMENTALES FISICOQUÍMICAS Curso 2009-2010 Técnicas Instrumentales Fisicoquímicas. 2ª PED (2009-10) 1 Instrucciones
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica
 Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Curso 2015-2016 Problema 1 La línea principal del espectro
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Curso 2015-2016 Problema 1 La línea principal del espectro
Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro:
 RESPUESTAS BLOQUE III Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro: Tipo de raciación Partículas Carga eléctrica Masa(uma) Alfa α +2 4
RESPUESTAS BLOQUE III Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro: Tipo de raciación Partículas Carga eléctrica Masa(uma) Alfa α +2 4
QUÍMICA de 2º de BACHILLERATO ESTRUCTURA DE LA MATERIA
 QUÍMICA de 2º de BACHILLERATO ESTRUCTURA DE LA MATERIA EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013)
QUÍMICA de 2º de BACHILLERATO ESTRUCTURA DE LA MATERIA EJERCICIOS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2013)
UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO METROPOLITANO FACULTAD CIENCIAS Y TECNOLOGIA DEPARTAMENTO DE CIENCIAS NATURALES PRONTUARIO
 [Type text] UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO METROPOLITANO FACULTAD CIENCIAS Y TECNOLOGIA DEPARTAMENTO DE CIENCIAS NATURALES PRONTUARIO I. INFORMACION GENERAL Título del Curso: Determinación
[Type text] UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO METROPOLITANO FACULTAD CIENCIAS Y TECNOLOGIA DEPARTAMENTO DE CIENCIAS NATURALES PRONTUARIO I. INFORMACION GENERAL Título del Curso: Determinación
Enlace químico II: geometría molecular e hibridación de orbitales atómicos
 Enlace químico II: geometría e hibridación de orbitales atómicos Capítulo 10 Modelo de la repulsión de los pares de electrones de la capa de valencia (): Predice la geometría de la molécula a partir de
Enlace químico II: geometría e hibridación de orbitales atómicos Capítulo 10 Modelo de la repulsión de los pares de electrones de la capa de valencia (): Predice la geometría de la molécula a partir de
Unidad 1: Materia, estructura y Periodicidad Base experimental de la teoría cuántica y estructura atómica.
 Unidad 1: Materia, estructura y Periodicidad 1.7. Base experimental de la teoría cuántica y estructura atómica. Modelo de Dalton En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia
Unidad 1: Materia, estructura y Periodicidad 1.7. Base experimental de la teoría cuántica y estructura atómica. Modelo de Dalton En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia
INDICE 22. La carga eléctrica Resumen, preguntas, problemas 23. El campo eléctrico Resumen, preguntas, problemas Resumen, preguntas, problemas
 INDICE 22. La carga eléctrica 22-1. las propiedades de la materia con carga 646 22-2. la conservación y cuantización de la carga 652 22-3. la ley de Colulomb 654 22-4. las fuerzas en las que intervienen
INDICE 22. La carga eléctrica 22-1. las propiedades de la materia con carga 646 22-2. la conservación y cuantización de la carga 652 22-3. la ley de Colulomb 654 22-4. las fuerzas en las que intervienen
Unidad 1: Teoría Cuántica y Estructura Atómica. 1.2 Base experimental de la teoría cuántica
 Unidad 1: Teoría Cuántica y Estructura Atómica 1.2 Base experimental de la teoría cuántica Thompson Dalton Rutherford Demócrito Naturaleza eléctrica de la materia La naturaleza de la luz CUANTOS Descubrimiento
Unidad 1: Teoría Cuántica y Estructura Atómica 1.2 Base experimental de la teoría cuántica Thompson Dalton Rutherford Demócrito Naturaleza eléctrica de la materia La naturaleza de la luz CUANTOS Descubrimiento
Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos
 Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos INTEGRANTES: * Nazate Amuy Ana * Veloz Hidalgo Polet TEMA: Combinación Lineal de Orbitales Atómicos ORBITAL ATÓMICO
Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos INTEGRANTES: * Nazate Amuy Ana * Veloz Hidalgo Polet TEMA: Combinación Lineal de Orbitales Atómicos ORBITAL ATÓMICO
Espectro Electromagnético
 Espectro Electromagnético En las moléculas orgánicas se observan vibraciones moleculares con energías que corresponden a la porción del infrarrojo del espectro electromagnético. Describiendo de la forma
Espectro Electromagnético En las moléculas orgánicas se observan vibraciones moleculares con energías que corresponden a la porción del infrarrojo del espectro electromagnético. Describiendo de la forma
INDICE Capitulo 27. La Carga Eléctrica y la Ley de Coulomb Capitulo 28. El Campo Eléctrico Capitulo 29. La Ley de Gauss
 INDICE Capitulo 27. La Carga Eléctrica y la Ley de Coulomb 1 27.1. Electromagnetismo. Un estudio preliminar 1 27.2. La carga eléctrica 2 27.3. Conductores y aislantes 3 27.4. La Ley de Coulomb 4 27.5.
INDICE Capitulo 27. La Carga Eléctrica y la Ley de Coulomb 1 27.1. Electromagnetismo. Un estudio preliminar 1 27.2. La carga eléctrica 2 27.3. Conductores y aislantes 3 27.4. La Ley de Coulomb 4 27.5.
ENLACE COVALENTE. Z = 1 Hidrógeno H: 1s 1 Z = 6 Carbono C: 1s 2 2s 2 2p 2 Z = 7 Nitrógeno N: 1s 2 2s 2 2p 3 Z = 8 Oxígeno O: 1s 2 2s 2 2p 4 H H H 2
 ENLACE COVALENTE Si los átomos que se enfrentan son ambos electronegativos (no metales), ninguno de los dos cederá electrones. Una manera de adquirir la configuración de gas noble en su última capa es
ENLACE COVALENTE Si los átomos que se enfrentan son ambos electronegativos (no metales), ninguno de los dos cederá electrones. Una manera de adquirir la configuración de gas noble en su última capa es
Robert A. MILLIKAN ( )
 Robert A. MILLIKAN (1906 1914) Modelo atómico de Rutherford - Todo átomo está formado por un núcleo y corteza. - El núcleo, muy pesado, y de muy pequeño tamaño, formado por un número de protones igual
Robert A. MILLIKAN (1906 1914) Modelo atómico de Rutherford - Todo átomo está formado por un núcleo y corteza. - El núcleo, muy pesado, y de muy pequeño tamaño, formado por un número de protones igual
UNIVERSIDAD DE PUERTO RICO RECINTO DE RÍO PIEDRAS DEPARTAMENTO DE QUÍMICA. QUíMICA 3031
 UNVERSDAD DE PUERT RC RECNT DE RÍ PEDRAS DEPARTAMENT DE QUÍMCA QUíMCA 3031 17 DE DCEMBRE DE 2004 NMBRE EXAMEN FNAL SECCÓN DE CNFERENCA Este examen se compone de 40 preguntas de selección múltiple. Se incluye
UNVERSDAD DE PUERT RC RECNT DE RÍ PEDRAS DEPARTAMENT DE QUÍMCA QUíMCA 3031 17 DE DCEMBRE DE 2004 NMBRE EXAMEN FNAL SECCÓN DE CNFERENCA Este examen se compone de 40 preguntas de selección múltiple. Se incluye
radiación electromagnética
 radiación electromagnética ondas propagándose en el espacio con velocidad c crestas amplitud l valles longitud de onda [ l]=cm, nm, μm, A Frecuencia=n=c/l [ n ]=HZ=1/s l= numero de ondas por unidad de
radiación electromagnética ondas propagándose en el espacio con velocidad c crestas amplitud l valles longitud de onda [ l]=cm, nm, μm, A Frecuencia=n=c/l [ n ]=HZ=1/s l= numero de ondas por unidad de
Indique razonadamente si son ciertas o falsas cada una de las siguientes afirmaciones:
 Considere las configuraciones electrónicas en el estado fundamental: 1ª) 1s 2 2s 2 2p 7 ; 2ª ) 1s 2 2s 3 ; 3ª ) 1s 2 2s 2 2p 5 ; 4ª ) 1s 2 2s 2 2p 6 3s 1 a) Razone cuáles cumplen el principio de exclusión
Considere las configuraciones electrónicas en el estado fundamental: 1ª) 1s 2 2s 2 2p 7 ; 2ª ) 1s 2 2s 3 ; 3ª ) 1s 2 2s 2 2p 5 ; 4ª ) 1s 2 2s 2 2p 6 3s 1 a) Razone cuáles cumplen el principio de exclusión
Estructura de la materia y Sistema Periódico
 Estructura de la materia y Sistema Periódico 1 - Respecto el número cuántico «n» que aparece en el modelo atómico de Bohr indicar de manera razonada cuáles de las siguientes frases son correctas y cuáles
Estructura de la materia y Sistema Periódico 1 - Respecto el número cuántico «n» que aparece en el modelo atómico de Bohr indicar de manera razonada cuáles de las siguientes frases son correctas y cuáles
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica
 Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
El átomo. Rafael Molina Fernández Científico Titular Instituto de Estructura de la Materia Consejo Superior de Investigaciones Científicas
 El átomo Rafael Molina Fernández Científico Titular Instituto de Estructura de la Materia Consejo Superior de Investigaciones Científicas Qué es un átomo? Cantidad mínima de un elemento químico que mantiene
El átomo Rafael Molina Fernández Científico Titular Instituto de Estructura de la Materia Consejo Superior de Investigaciones Científicas Qué es un átomo? Cantidad mínima de un elemento químico que mantiene
Tema 2: Propiedades y medición de la radiación electromagnética
 Tema 2: Propiedades y medición de la radiación electromagnética Espectro de la radiación electromagnética Conceptos básicos para la medición: Densidad de flujo Luminosidad Intensidad Brillo superficial
Tema 2: Propiedades y medición de la radiación electromagnética Espectro de la radiación electromagnética Conceptos básicos para la medición: Densidad de flujo Luminosidad Intensidad Brillo superficial
FÍSICA 4 PRIMER CUATRIMESTRE DE 2015 GUÍA 9: POTENCIALES EN 2-D Y 3-D, MOMENTO ANGULAR, ÁTOMO DE HIDRÓGENO, ESPÍN
 FÍSICA 4 PRIMER CUATRIMESTRE DE 2015 GUÍA 9: POTENCIALES EN 2-D Y 3-D, MOMENTO ANGULAR, ÁTOMO DE HIDRÓGENO, ESPÍN 1. Considere el siguiente potencial (pozo infinito): { 0 x a; y b y z c V(x)= sino Escribiendo
FÍSICA 4 PRIMER CUATRIMESTRE DE 2015 GUÍA 9: POTENCIALES EN 2-D Y 3-D, MOMENTO ANGULAR, ÁTOMO DE HIDRÓGENO, ESPÍN 1. Considere el siguiente potencial (pozo infinito): { 0 x a; y b y z c V(x)= sino Escribiendo
ANTECEDENTES Métodos generales de extracción y purificación
 ANTECEDENTES El estudio de los Agaves es de gran importancia debido a su uso tradicional como medicamento en diferentes culturas como la de la India y México. Los Agaves se utilizan como diuréticos, antisifilítico,
ANTECEDENTES El estudio de los Agaves es de gran importancia debido a su uso tradicional como medicamento en diferentes culturas como la de la India y México. Los Agaves se utilizan como diuréticos, antisifilítico,
LAS LEYES DE LA RADIACIÓN EN LA TIERRA Y EN EL ESPACIO OBJETIVO RESUMEN. GENERACIÓN DE LINEAS: Leyes de Kirchhoff
 LAS LEYES DE LA RADIACIÓN EN LA TIERRA Y EN EL ESPACIO OBJETIVO Aproximarnos a los procesos que absorben y generan radiación electromagnética en la Tierra y en el espacio. Basada en presentación de Tabaré
LAS LEYES DE LA RADIACIÓN EN LA TIERRA Y EN EL ESPACIO OBJETIVO Aproximarnos a los procesos que absorben y generan radiación electromagnética en la Tierra y en el espacio. Basada en presentación de Tabaré
Unidad I: Propiedades Periódicas: Masa y Enlace
 Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
UNIVERSIDAD SIMÓN BOLÍVAR Vicerrectorado Académico
 UNIVERSIDAD SIMÓN BOLÍVAR Vicerrectorado Académico 1.Departamento: FÍSICA 2. Asignatura: FISICA MODERNA I 3. Código de la asignatura: FS-3411 No. de unidades-crédito: 4 No. de horas semanales: Teoría 4
UNIVERSIDAD SIMÓN BOLÍVAR Vicerrectorado Académico 1.Departamento: FÍSICA 2. Asignatura: FISICA MODERNA I 3. Código de la asignatura: FS-3411 No. de unidades-crédito: 4 No. de horas semanales: Teoría 4
Bloque 2. INTERACCIÓN GRAVITATORIA.
 Teniendo en cuenta los diferentes apartados de cada bloque temático, se indican a continuación algunos de los conceptos que tienen mayor relevancia en cada apartado, tal y como se ponen de manifiesto en
Teniendo en cuenta los diferentes apartados de cada bloque temático, se indican a continuación algunos de los conceptos que tienen mayor relevancia en cada apartado, tal y como se ponen de manifiesto en
Thompson (1898) Rutherford (1911) Bohr (1913) Schrödinger (1926) NUMEROS CUANTICOS
 Thompson (1898) Modelo Atómico Rutherford (1911) Bohr (1913) Propiedad corpuscular de las onda (PLANCK) Propiedad ondulatoria de las partículas (De Broglie) Schrödinger (1926) Números cuánticos 1 NUMEROS
Thompson (1898) Modelo Atómico Rutherford (1911) Bohr (1913) Propiedad corpuscular de las onda (PLANCK) Propiedad ondulatoria de las partículas (De Broglie) Schrödinger (1926) Números cuánticos 1 NUMEROS
Las estructura electrónica de los átomos
 Las estructura electrónica de los átomos Al preguntarnos por las diferencias entre las propiedades químicas y físicas de los elementos, así como, su forma de enlazarse y la forma en la cual emiten o absorben
Las estructura electrónica de los átomos Al preguntarnos por las diferencias entre las propiedades químicas y físicas de los elementos, así como, su forma de enlazarse y la forma en la cual emiten o absorben
Detectores de Partículas
 Detectores de Partículas Física de Astropartículas Master de Física Fundamental Juan Abel Barrio, Curso 12/13 Universidad Complutense de Madrid 1 Detección de radiación Radiación Detector Señal Amplificación
Detectores de Partículas Física de Astropartículas Master de Física Fundamental Juan Abel Barrio, Curso 12/13 Universidad Complutense de Madrid 1 Detección de radiación Radiación Detector Señal Amplificación
Técnicas Avanzadas de Resonancia Magnética Nuclear GUÍA DOCENTE Curso
 Técnicas Avanzadas de Resonancia Magnética Nuclear GUÍA DOCENTE Curso 2009-2010 Titulación: Máster en Química Avanzada Código Asignatura: Técnicas Avanzadas de Resonancia Magnética Nuclear Código Materia:
Técnicas Avanzadas de Resonancia Magnética Nuclear GUÍA DOCENTE Curso 2009-2010 Titulación: Máster en Química Avanzada Código Asignatura: Técnicas Avanzadas de Resonancia Magnética Nuclear Código Materia:
Tema 2: Estructura atómica (I): Estructura nuclear del átomo
 Primeros experimentos sobre la estructura atómica Tema : Estructura atómica (I): Estructura nuclear del átomo. Primeros modelos atómicos. Isótopos.3 Radiación y materia: propiedades ondulatorias de la
Primeros experimentos sobre la estructura atómica Tema : Estructura atómica (I): Estructura nuclear del átomo. Primeros modelos atómicos. Isótopos.3 Radiación y materia: propiedades ondulatorias de la
El Átomo de Bohr. Descripción mecánico-cuántica de los electrones alrededor del núcleo: orbitales atómicos
 Descripción mecánico-cuántica de los electrones alrededor del núcleo: orbitales atómicos El Átomo de Bohr 1.Los electrones orbitan el átomo en niveles discretos y cuantizados de energía, es decir, no todas
Descripción mecánico-cuántica de los electrones alrededor del núcleo: orbitales atómicos El Átomo de Bohr 1.Los electrones orbitan el átomo en niveles discretos y cuantizados de energía, es decir, no todas
2. APARICIÓN DE NUEVOS HECHOS: ESPECTROS ATÓMICOS E HIPÓTESIS DE PLANCK 6. CONFIGURACIONES ELECTRÓNICAS: PRINCIPIO DE AUFBAU
 ÍNDICE 1. MODELO ATÓMICO DE RUTHERFORD 2. APARICIÓN DE NUEVOS HECHOS: ESPECTROS ATÓMICOS E HIPÓTESIS DE PLANCK 3. MODELO ATÓMICO DE BORH 4. CONCEPTO DE ORBITAL ATÓMICO 5. NÚMERO CUÁNTICOS Y SU SIGNIFICADO
ÍNDICE 1. MODELO ATÓMICO DE RUTHERFORD 2. APARICIÓN DE NUEVOS HECHOS: ESPECTROS ATÓMICOS E HIPÓTESIS DE PLANCK 3. MODELO ATÓMICO DE BORH 4. CONCEPTO DE ORBITAL ATÓMICO 5. NÚMERO CUÁNTICOS Y SU SIGNIFICADO
INTRODUCCIÓN A LA TELEDETECCIÓN CUANTITATIVA
 INTRODUCCIÓN A LA TELEDETECCIÓN CUANTITATIVA Haydee Karszenbaum Veronica Barrazza haydeek@iafe.uba.ar vbarraza@iafe.uba.ar Clase 1.2: ondas y leyes de la radiación Teledetección cuantitativa 1 Características
INTRODUCCIÓN A LA TELEDETECCIÓN CUANTITATIVA Haydee Karszenbaum Veronica Barrazza haydeek@iafe.uba.ar vbarraza@iafe.uba.ar Clase 1.2: ondas y leyes de la radiación Teledetección cuantitativa 1 Características
ESTRUCTURA DE LA MATERIA
 ESTRUCTURA DE LA MATERIA 1. Naturaleza de la materia (el átomo). 2. Modelos atómicos clásicos. 3. Modelo mecánico cuántico. 4. Mecánica ondulatoria de Schrödinger. 5. Números cuánticos. 6. Orbitales atómicos.
ESTRUCTURA DE LA MATERIA 1. Naturaleza de la materia (el átomo). 2. Modelos atómicos clásicos. 3. Modelo mecánico cuántico. 4. Mecánica ondulatoria de Schrödinger. 5. Números cuánticos. 6. Orbitales atómicos.
Ondas. Vasili Kandinsky: Puntos, oleo, 110 x 91,8 cm, 1920
 Ondas Vasili Kandinsky: Puntos, oleo, 110 x 91,8 cm, 1920 Este documento contiene material multimedia. Requiere Adobe Reader 7.1 o superior para poder ejecutarlo. Las animaciones fueron realizadas por
Ondas Vasili Kandinsky: Puntos, oleo, 110 x 91,8 cm, 1920 Este documento contiene material multimedia. Requiere Adobe Reader 7.1 o superior para poder ejecutarlo. Las animaciones fueron realizadas por
EL MODELO ATOMICO DE BOHR
 EL MODELO ATOMICO DE BOHR En 1913, Niels Bohr ideó un modelo atómico que explica perfectamente los espectros determinados experimentalmente para átomos hidrogenoides. Estos son sistemas formados solamente
EL MODELO ATOMICO DE BOHR En 1913, Niels Bohr ideó un modelo atómico que explica perfectamente los espectros determinados experimentalmente para átomos hidrogenoides. Estos son sistemas formados solamente
ESTRUCTURA DEL ÁTOMO - RESUMEN
 TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
ATOMO DE HIDROGENO. o = permitividad al vacío = 8.85 X C 2 N -1 cm -1. = metros. F = Newtons 2. Ó (3)
 ATOMO DE HIDROGENO I. Atomo de hidrógeno A. Descripción del sistema: Dos partículas que interaccionan por atracción de carga eléctrica y culómbica. 1. Ley de coulomb: a. En el sistema cgs en unidades de
ATOMO DE HIDROGENO I. Atomo de hidrógeno A. Descripción del sistema: Dos partículas que interaccionan por atracción de carga eléctrica y culómbica. 1. Ley de coulomb: a. En el sistema cgs en unidades de
