UNIDAD 2 - CROMATOGRAFIA COMPLEMENTO TEORICO
|
|
|
- Fernando Crespo Ríos
- hace 5 años
- Vistas:
Transcripción
1 UNIDAD 2 - CROMATOGRAFIA COMPLEMENTO TEORICO 1- CROMATOGRAFIA DE ADSORCION EN COLUMNA La separación se realiza entre una fase móvil líquida (o gaseosa en el caso de cromatografía instrumental) y una fase estacionaria constituida por un sólido finamente dividido y sobre el cual se produce la adsorción de los componentes a separar. La separación de los solutos por cromatografía sólido - líquido (o sólido - gas) depende de: a - el establecimento del equilibrio en la interfase entre la fase estacionaria y la solución aplicada (muestra a separar), que resulta de la competencia solvente fase estacionaria para el soluto disuelto; b - la relativa solubilidad del soluto en el solvente eluente. El soluto es adsorbido de la solución por la fase estacionaria, y más tarde, desadsorbido pasando a la fase móvil. Cuando hay más de un soluto, aquél que se una más fuerte al adsorbente será eluido más lentamente, y será el que corre o se desplaza menos. La posición relativa que los solutos toman en la columna dependerá de su fuerza de adsorción y las velocidades de pasaje a la fase móvil dependerá de sus respectivas velocidades de desadsorción. La cromatografía de adsorción en columna tradicional de laboratorio se lleva a cabo generalmente en tubos de vidrio verticales, que se llenará con la fase estacionaria adecuada, donde se incorpora la mezcla de sustancias a separar. La mezcla a analizar se siembra sobre la parte superior del adsorbente. La mezcla es adsorbida por la columna y luego es progresivamente eluida con solventes de polaridad creciente, los que alojan o desalojan o desadsorben las sustancias adsorbidas desde el extremo de la columna hacia abajo. A medida que los solutos pasan hacia abajo, a zonas de adsorbente fresco, se establecen menos equilibrios entre el adsorbente, los solutos y el solvente. Como el número de partículas de adsorbente es grande, como están estrechamente empaquetadas y como continuamente se agrega solvente nuevo, el número de equilibrios entre adsorbente y el solvente es enorme. A medida que los componentes de la mezcla se separan, comienzan a formar bandas o zonas móviles, donde cada banda debe contener un componente. Si la columna es suficientemente larga y se eluye correctamente, las bandas se separan unas de otras, dejando espacios entre ellas de solvente puro. A medida que cada banda sale de la columna, puede ser recogida totalmente antes de que salga la próxima banda. Si la operación no es correcta, las distintas bandas se superponen y salen mezcladas, entonces la separación será pobre o nula. Los compuestos menos adsorbidos serán recogidos primero en el extremo de la columna. 1
2 Parámetros que afectan a la separación 1- Fase estacionaria. Se debe tener en cuenta: a- Actividad o poder adsorbente: la actividad máxima está dada por un mínimo contenido de moléculas de agua sobre la superficie del adsorbente (idealmente 0 %, aunque en general se tiene un 5 %). A medida que aumenta el % disminuye la actividad del adsorbente ya que numerosos sitios activos de su superficie están bloqueados por moléculas de agua. b- Inercia química: el adsorbente no debe reaccionar con las sustancias a separar. Pueden haber reacciones indeseables de hidrólisis de ésteres, condensaciones aldólicas (con alúmina), lactonizaciones (con sílice), formación de sales (entre alúmina básica con componentes ácidos, o entre sílica que posee características ácidas con componentes básicos), deshidrataciones de grupos funcionales lábiles o catálisis de descomposición, transposición o isomerización. c- Solubilidad del adsorbente: debe ser totalmente insoluble en el solvente de desarrollo. d- Color: deberá ser incolora. e- Composición: uniforme. f- Tamaño del gránulo: mientras más fina sea la división del adsorbente, mayor es la superficie de contacto y mayor la adsorción. El tamaño del gránulo debe ser entre 60 y 200 micrones. Menos no es conveniente porque el empacado se hace muy denso y el pasaje de solvente lento. g- Empaquetamiento: debe ser homogéneo, de lo contrario habría un descenso rápido de las bandas en zonas menos densas de relleno y el frente de elución sería desparejo, saliendo los componentes mezclados. Tampoco deben quedar canales, ya que por ellos correrían más rápidamente las bandas ocasionando el mismo error. ADSORBENTES CELULOSA ALMIDON AZUCARES SILICATO DE MG SILICA GEL COMPONENTES DE LA MUESTRA Para separar compuestos polifuncionales muy sensibles a interacciones ácido-base. Azúcares acetilados, aceites esenciales esteroles. Hidrocarburos,alcoholes, cetonas, ésteres, ácidos, aminas, azo-compuestos. ACIDA Acidos carboxílicos, aminoácidos. ALUMINA BASICA Aminas. NEUTRA Compuestos varios neutros. 2
3 2- Soluto. La absorbabilidad del soluto depende de su polarizabilidad y su capacidad para formar uniones puente hidrógeno. Los grupos más polares son los adsorbidos más fuertemente. Orden creciente: ácidos y bases, alcoholes y tioles, aldehídos y cetonas, halogenuros de alquilo y ésteres, hidrocarburos insaturados e hidrocarburos saturados. En general el poder de adsorción aumenta con el incremento de grupos funcionales unidos a la misma molécula, pero existen casos en los cuales dos grupos funcionales presentes pueden formar uniones puente de hidrógeno y de esta forma adsorberse menos. 3- Solventes. Por lo general se comienza la elución con un solvente no polar para remover compuestos relativamente poco polares de la columna, y luego, gradualmente, aumentar la polaridad del solvente para forzar a los compuestos de mayor polaridad a descender de la columna, es decir a eluir. Cuando la polaridad del solvente debe ser cambiada, este paso debe ser gradual, agregando pequeños porcentajes del nuevo solvente, hasta que el porcentaje alcance el valor deseado. Si no se procede así, se pueden formar canales o quiebras en la columna. Es fundamental el uso de solventes anhidros y miscibles. Polaridad creciente de los solventes más comunes utilizados: 4- Velocidad de elución. ETER DE PETROLEO CICLOHEXANO TETRACLORURO DE CARBONO BENCENO CLORURO DE METILENO CLOROFORMO ETER ETILICO ACETATO DE ETILO ACETONA PIRIDINA ETANOL METANOL AGUA Debe ser lo suficientemente lenta para permitir alcanzar el equilibrio adsorción desadsorción, pero no al extremo, pues si la muestra difunde más rápidamente que la velocidad a la cual se escurre hacia abajo en la columna, las bandas se ensanchan. La velocidad ideal es de 2 ml/min. 3
4 5- Tamaño de la columna. La relación altura/diámetro debe ser del órden de 8:1. 6- Cantidad de adsorbente. Debe ser de 25 a 30 veces en peso respecto de la cantidad del material a separar. 7- Temperatura. Afecta la volatilidad y la solubilidad de los solventes, por lo tanto debe mantenerse constante a lo largo de la operación y debe ser homogénea en toda la columna. APLICACIONES. Se la prefiere para escala preparativa. Se pueden separar los componentes de extractos de plantas; productos de reacción de trabajos de síntesis. También permite el estudio de cada fracción obtenida. Algunas ventajas: 1- Cambio secuencial de la polaridad del solvente de elución. 2- Desplazamiento ilimitado del frente de solvente. 2- CROMATOGRAFIA PLANAR EN PAPEL La cromatografía en papel es de partición en donde se mantiene una fase líquida inmóvil (fase estacionaria) sobre un soporte activo (el papel) y una segunda fase líquida inmiscible con la primera puede fluir sobre ella (fase móvil). Las dos fases estarán en contacto, en una gran interfase, lo que permite una rápida obtención de una distribución de equilibrio del soluto entre las dos fases. Si la muestra problema está formada por más de un soluto, éstos se separan por sus diferentes coeficientes de partición. La realización de la cromatografía en papel implica la siembra de la muestra problema en un trozo de papel de buena calidad Whatman 1 (ó 3 para cromatografía preparativa), que luego se introducirá en una cuba de desarrollo de modo que el solvente (fase móvil) ascienda por capilaridad (técnica ascendente) o descienda por gravedad (técnica descendente). La fase estacionaria es un complejo celulosa-agua que tiene un poder de resolución diferente que el del agua pura. ETAPAS DE LA CROMATOGRAFIA EN PAPEL 1- Siembra: se aplican muestras en solución a no menos de 1,5 cm del borde inferior de una tira rectangular de papel, y a no menos de 1,5 cm de los bordes laterales, manteniendo a su vez, entre mancha y mancha una distancia no menor de 1 cm. La siembra es puntual para fines analíticos, y en banda para fines preparativos. 2-Desarrollo: las formas más usuales son: a- Ascendente: el solvente se coloca en el fondo de la cuba y el papel se suspende por algún artificio colocado en la parte superior de ésta. Dan mejores resultados con solventes muy volátiles, lo que constituye una ventaja. Un inconveniente es que los compuestos con Rf muy bajo se separan incompletamente. 4
5 b- Descendente: el solvente se coloca en un depósito inerte ubicado en la parte superior de la cuba cromatográfica. En el fondo de la cuba se coloca también un poco de solvente para asegurar la saturación con el vapor. La parte superior del papel se sumerge en el disolvente y se tapa herméticamente la cuba (al igual que en la técnica ascendente). La siembra quedará en la parte superior del papel, en este caso. c- Bidimensional: se corre el papel en una dirección y luego del desarrollo y secado, se gira 90º y se corre con otro solvente. 3- Revelado: si los compuestos de la mezcla son coloreados, las manchas son visibles directamente. De lo contrario hay que revelarlas: a- Con luz U.V.: si los compuestos absorben radiaciones en esta frecuencia. Las manchas se verán entonces con fluorescencia. b- Con reactivos de color: especiales para cada compuesto. Se deberá tener en cuenta que no se pueden utilizar reveladores que destruyan el papel, tales como el ácido sulfúrico o el calor. c- Vapores de yodo sublimado: es un revelador universal. 4- Evaluación: se efectúa el cálculo del Rf para cada componente de la mezcla por separado. APLICACIONES. Se utiliza generalmente para compuestos muy polares o polifuncionales. El uso más común es para azúcares, aminoácidos y pigmentos naturales. Consideraciones generales. - El desplazamiento depende de la temperatura y de la saturación de la cuba. - Las sustancias más polares quedarán más retenidas, y serán más desplazadas las menos polares. - Las operaciones pueden ser con fines analíticos o preparativos: a- Fines analíticos: para conocer la composición o pureza de una muestra, identificar una sustancia dada, etc. También sirve para la valoración de muestras, en cuyo caso los volúmenes a sembrar deben ser conocidos, las diluciones conocidas, tanto de la sustancia incógnita como la de un testigo. b- Fines preparativos: la siembra se efectúa en banda. El papel usado es más poroso. Luego del desarrollo se ubican las sustancias separadas por coloración, o fluorescencia. Se cortan tiras de papes de ambos lados y se revelan. Luego se colocan esas bandas a los lados del cromatograma y se delinean los componentes separados con un lápiz. Las áreas dibujadas se cortan y se extraen con un solvente propuesto para cada caso, por maceración o percolación. 5
6 2.2- CROMATOGRAFIA EN CAPA DELGADA. También llamada en capa fina. Es una técnica muy importante para la separación rápida y el análisis cualitativo de muestras en pequeña cantidad. Es semejante a una cromatografía en columna invertida, en donde el solvente asciende por capilaridad por un soporte que tiene adherido el adsorbente (cromatografía de adsorción en capa fina) o la celulosa microcristalina (cromatografía de partición en capa fina). Se usan soportes de vidrio, aluminio o plástico. Sobre ellos se extiende una capa pareja de adsorbente (o de celulosa) de espesor variable según la placa sea analítica o preparativa (100 m a 2 mm). En un extremo de la placa se siembra la muestra. La siembra es puntual si es con fines analíticos (A) y en banda si es con fines preparativos (P). En ambos casos pueden hacerse varias siembras superpuestas para aumentar la cantidad de muestra. A P La placa se introduce en una cuba que contiene el solvente de desarrollo el cual asciende y permite que se lleven a cabo los equilibrios de adsorción -desadsorción vistos en cromatografía en columna, o los de partición. La placa se deja hasta que el solvente llegue al extremo superior. De igual modo que en la cromatografia en columna, los componentes más polares serán más retenidos por la fase estacionaria ( corren menos ) y los menos polares migrarán más con el solvente. Terminado el desarrollo, se retira la placa, se seca, revela y evalúa. El siguiente esquema permite visualizar el proceso: frente o o o -- origen testigo muestra o es la sustancia más retenida (la más polar); es la que más corrió (la menos polar). emigró en forma intermedia. Podría tratarse de la misma sustancia que la muestra patrón porque posee desplazamiento semejante. 6
7 PARAMETROS QUE AFECTAN LA SEPARACION Son similares a los vistos en cromatografía en columna, si bien presentan algunas variantes. 1- ADSORBENTE Tiene un agregado de CaCO 3 (yeso) que permite que el adsorbente se adhiera al soporte. La granulometría es menor de 10 a 40 m de diámetro aproximadamente. Es primordial el espesor de adsorbente en la placa, una capa irregular ocasionará recorridos más rápidos en zonas más delgadas o más lentos en zonas de mayor espesor. 2- SOLVENTES La diferencia que hay con la cromatografía en columna es que aquí se emplea un solvente o una combinación de solventes fija, no se cambia durante el desarrollo del cromatograma. Deberá ser tal que los componentes de la muestra no corran con el frente del solvente, ni queden retenidos en el lugar de siembra. 3- SATURACION DE LA CUBA La cuba cromatográfica deberá estar saturada con el o los solventes de desarrollo antes de introducir la placa, de lo contrario, el solvente en vez de ascender por capilaridad continuamente, tenderá a evaporarse de la capa de adsorbente para equilibrar al líquido con su presión de vapor. Eso implicaría un ascenso no homogéneo del frente de solvente. Cuando se utiliza una mezcla de solventes, el problema se agrava, ya que las volatilidades relativas de los solventes pueden ser distintas (el más volátil se evaporaría mas). APLICACIONES 1.- Permite establecer si dos compuestos analizados son indénticos (para ello deben correr igual en iguales condiciones, es decir en idénticos sistemas cromatográficos). 2.- Se utiliza para determinar el número de componentes de una mezcla (por el número de manchas que salen de la placa). 3.- Para determinar el solvente apropiado para una separación en columna. 4.- Para seguir una separación por cromatografía en columna. Para ello se usa como solvente de desarrollo la combinación de solventes con que salió la banda de la columna. 5.- Para probar la efectividad de una separación realizada por columna, cristalización o extracción. 6.- Para separar los componentes de una mezcla (en este caso deben utilizarse placas preparativas pudiendo usarse muestras de hasta 500 mg). 7.- Para seguir el proceso de una reacción realizada. 7
8 La cromatografia en capa delgada con fines analíticos permite detectar hasta 10 g. Este método tiene la desventaja de que no se pueden sembrar componentes volátiles, pues se evaporarían de la placa. PREPARACION DE LA PLACA FINA DE ADSORCION A.- Placas de uso inmediato: se suspende el adsorbente en una mezcla de cloruro de metileno - metanol (9:1), o cloroformo - metanol (9:1). La cantidad de adsorbente y solvente serán tales que quede sobre el soporte una capa delgada y uniforme. Las placas (soportes) perfectamente limpias y desengrasadas con etanol, se sostienen de a dos y se las sumerge en la suspensión del adsorbente hasta las 3/4 partes de su altura. Se las retira, se limpian los bordes y una vez secas se pueden utilizar. Conviene realizar la activación de las mismas en estufa a C (dependerá del adsorbente) antes de utilizarlas, aún cuando previamente el adsorbente hubiera sido activado. B.- Técnica de suspensión con agua: Se suspende el adsorbente en agua según la relación: Sílica gel: 30 g ml de agua Alúmina: 50 g ml de agua Celulosa microcristalina: 35 g ml de agua Se colocan los soportes sobre una base que actúa como una corredera y la suspensión en un carro donde se regula el espesor del adsorbente según la placa sea para fines analiticos o preparativos. Se desliza el carro sobre la corredera. Las placas se dejan a temperatura ambiente 1-2 horas y luego se activan en estufa durante 20 minutos, para eliminar toda la humedad. ETAPAS DEL PROCESO 1) SIEMBRA Se disuelve (o suspende) la muestra en un solvente adecuado preferentemente volátil, y la siembra se efectúa con un capilar cargado, a 1,5 cm del borde de la placa. Se hace un toque, se evapora el solvente, se hace otro toque, así sucesivamente hasta lograr la concentración deseada. Se debe cuidar que las siembras no sean demasiado grandes (un diámentro no mayor de 0,2 cm). Si se hacen varias siembras deben estar separadas una de otras por lo menos 1 cm. 2) DESARROLLO La placa sembrada se introduce en la cuba previamente saturada con el solvente de modo que el solvente toque la placa, pero no la zona de siembra. 8
9 La cuba se tapa y se deja que el solvente ascienda por capilaridad, hasta 2 cm. antes del borde superior. En este momento se retira la placa y se deja secar. >1,0 cm ,5 cm 1,5 cm 0,2 cm Analítica Preparativa 3) REVELADO Si los componentes de la muestra son coloreados, las manchas serán visibles. De lo contrario hay que revelarlas. Reveladores: 1.- Luz UV: cuando los componentes toman radiaciones de esta frecuencia. En este caso observará fluorescencia. 2.- I2: es un revelador universal. Se coloca la placa en una cuba que tenga I2 sublimado. Este es volátil y se fija por uniones dipolo inducido a las zonas donde están los compuestos dando manchas marrones o amarillentas. La ventaja de este método es que quitada la placa de la cámara de iodo (o del contacto con los vapores) comienza a decolorarse por la volatilización del iodo. 3.- H2SO4 con calor: este método es destructivo. Se rocía la placa con ácido sulfúrico concentrado y se coloca en estufa por unos minutos. Aparecerán manchas con colores diversos. 4.- Reactivos de color: reactivos particulares para cada compuesto. Si la placa es preparativa no pueden usarse reveladores destructivos o si se los usa hacerlo en el extremo de la placa frente de solvente siembra
10 Placa sembrada Placa revelada Luego se raspa el adsorbente del soporte y se extrae la/s sustancia/s con el solvente adecuado. Se centrifuga tomando el sobrenadante o bien se filtra, se evapora el solvente y obtenemos así compuestos puros. Se raspa en. Cada banda se coloca por separado con el solvente elegido c b evaporar filtrar solvente a a b c solv + muestra muestra siembra (a, b, ó c) 4) EVALUACION La evaluación se hace calculando los Rf que son característicos para cada compuesto en condiciones constantes (adsorbente, grosor de la capa, temperatura, solventes, altura de desarrollo, etc). distancia recorrida por el compuesto desde el origen Rf= distancia recorrida por el solvente desde el origen Origen= punto de siembra frente de solvente 6,5 cm 5 cm Rf = 2 cm Rf = 5 cm 2 cm 6,5 cm 6,5 cm origen El Rf toma valores entre 0-1 y puede ser usado para la identificación de los componentes de una muestra. 10
11 El número de manchas reveladas nos indica el grado de pureza de la muestra. Si variando los solventes de desarrollo aparece una única mancha en todos los casos es muy probable que la muestra consista en una sustancia pura. 11
Los principales mecanismos que intervienen en la separación cromatográfica son:
 TP 8 CROMATOGRAFIA EN PAPEL, Introducción Los métodos cromatográficos son un conjunto de técnicas empleadas para separar compuestos químicos de una mezcla. Su nombre significa escribir con color ya que
TP 8 CROMATOGRAFIA EN PAPEL, Introducción Los métodos cromatográficos son un conjunto de técnicas empleadas para separar compuestos químicos de una mezcla. Su nombre significa escribir con color ya que
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN. Ingeniería Ambiental
 TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
CROMATOGRAFIA. Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA
 CROMATOGRAFIA Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA 1 CROMATOGRAFIA Se basa en el principio general de distribución de un compuesto entre dos fases, una fija o estacionaria (FE) y
CROMATOGRAFIA Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA 1 CROMATOGRAFIA Se basa en el principio general de distribución de un compuesto entre dos fases, una fija o estacionaria (FE) y
CROMATOGRAFÍA EN PLACA FINA
 CROMATOGRAFÍA EN PLACA FINA Fundamento La cromatografía en capa fina (en inglés thin layer chromatography o TLC) es una técnica analítica rápida y sencilla, muy utilizada en un laboratorio de Química Orgánica.
CROMATOGRAFÍA EN PLACA FINA Fundamento La cromatografía en capa fina (en inglés thin layer chromatography o TLC) es una técnica analítica rápida y sencilla, muy utilizada en un laboratorio de Química Orgánica.
tipo fase estacionaria fase movil sólido inerte como gel de sílice o alúmina resina cambiadora líquido adsorbido en un soporte sólido
 Cromatografía La cromatografía es una técnica de separación extraordinariamente versátil que presenta distintas variantes. En toda separación cromatográfica hay dos fases (sólida, líquida o gas) una móvil
Cromatografía La cromatografía es una técnica de separación extraordinariamente versátil que presenta distintas variantes. En toda separación cromatográfica hay dos fases (sólida, líquida o gas) una móvil
Unidad II: Cromatografía. Contenidos mínimos. Guía de estudio
 Universidad Nacional de Quilmes Departamento de Ciencia y Tecnología Química Orgánica I Unidad II: Cromatografía Contenidos mínimos Fundamentos de las técnicas cromatográficas. Fenómenos de adsorción y
Universidad Nacional de Quilmes Departamento de Ciencia y Tecnología Química Orgánica I Unidad II: Cromatografía Contenidos mínimos Fundamentos de las técnicas cromatográficas. Fenómenos de adsorción y
Cromatografía. Producto 1 Producto 2 Producto 3. Figura 1
 Cromatografía La cromatografía es una técnica muy versátil que puede utilizarse con fines analíticos para identificar los componentes de una mezcla por comparación con patrones o con fines preparativos
Cromatografía La cromatografía es una técnica muy versátil que puede utilizarse con fines analíticos para identificar los componentes de una mezcla por comparación con patrones o con fines preparativos
Principios: Se basa en los diferentes tamaños de las moléculas cuando pasan a través de una columna rellena con un gel
 Clasificación de los métodos cromatográficos en columna (4) Cromatografía líquido sólido: permeación en geles Principios: Se basa en los diferentes tamaños de las moléculas cuando pasan a través de una
Clasificación de los métodos cromatográficos en columna (4) Cromatografía líquido sólido: permeación en geles Principios: Se basa en los diferentes tamaños de las moléculas cuando pasan a través de una
1311 Laboratorio Química Orgánica I Prof. Mario Alfredo García Carrillo Semestre 2017-I
 GUIA DE ESTUDIOS PARA EL SEGUNDO EXAMEN. 1. Se tiene una mezcla de dos moléculas I y II en diclorometano (las moléculas se muestran abajo). Si se pretende separar por extracción selectiva dicha mezcla,
GUIA DE ESTUDIOS PARA EL SEGUNDO EXAMEN. 1. Se tiene una mezcla de dos moléculas I y II en diclorometano (las moléculas se muestran abajo). Si se pretende separar por extracción selectiva dicha mezcla,
Informe del trabajo práctico nº3
 Informe del trabajo práctico nº3 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Trabajo Práctico Nº3 1. Conocer
Informe del trabajo práctico nº3 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Trabajo Práctico Nº3 1. Conocer
Trabajo Práctico 10 : Evaluación de colesterol total y fraccionado por una técnica de cromatografía en capa fina.
 Trabajo Práctico 10 : Evaluación de colesterol total y fraccionado por una técnica de cromatografía en capa fina. OBJETIVO: -Determinar colesterol libre y esterificado en sangre mediante una técnica de
Trabajo Práctico 10 : Evaluación de colesterol total y fraccionado por una técnica de cromatografía en capa fina. OBJETIVO: -Determinar colesterol libre y esterificado en sangre mediante una técnica de
Separaciones Químicas Introducción
 Separaciones Químicas Introducción Destilación Extracción con solventes Cromatografía A. Martínez 1 Cromatografía Un método físico de separación Partición de componentes de una mezcla (soluto) entre dos
Separaciones Químicas Introducción Destilación Extracción con solventes Cromatografía A. Martínez 1 Cromatografía Un método físico de separación Partición de componentes de una mezcla (soluto) entre dos
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía.
 1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
CROMATOGRAFÍA LÍQUIDA DE ADSORCIÓN EN COLUMNA (CC) Y CAPA FINA (TLC)
 PRÁCTICA 10: CROMATOGRAFÍA LÍQUIDA DE ADSORCIÓN EN COLUMNA (CC) Y CAPA FINA (TLC) 1. INTRODUCCIÓN La cromatografía es un método físico de separación basado en la diferencia de distribución de los componentes
PRÁCTICA 10: CROMATOGRAFÍA LÍQUIDA DE ADSORCIÓN EN COLUMNA (CC) Y CAPA FINA (TLC) 1. INTRODUCCIÓN La cromatografía es un método físico de separación basado en la diferencia de distribución de los componentes
CROMATOGRAFIA EN COLUMNA
 PRACTICA IX CROMATOGRAFIA EN COLUMNA I. OBJETIVOS a) Utillizar las técnicas de la cromatografía en capa fina y columna e identificar los factores que intervienen en ellas. b) Utilizar la cromatografía
PRACTICA IX CROMATOGRAFIA EN COLUMNA I. OBJETIVOS a) Utillizar las técnicas de la cromatografía en capa fina y columna e identificar los factores que intervienen en ellas. b) Utilizar la cromatografía
CROMATOGRAFÍA SOBRE CAPA FINA MÉTODO DE SCREENING SISTEMA MTTLC ESTRUCTURA GENERAL. Análisis de medicamentos, Doping y drogas de abuso
 CROMATOGRAFÍA SOBRE CAPA FINA Análisis de medicamentos, Doping y drogas de abuso Q.F. Sergio Salas Ibáñez Laboratorio de Análisis Antidoping/Drogas de Abuso Facultad de Ciencias Químicas y Farmacéuticas
CROMATOGRAFÍA SOBRE CAPA FINA Análisis de medicamentos, Doping y drogas de abuso Q.F. Sergio Salas Ibáñez Laboratorio de Análisis Antidoping/Drogas de Abuso Facultad de Ciencias Químicas y Farmacéuticas
Curso Química Analítica Cualitativa
 TERMINOLOGÍA CROMATOGRÁFICA Curso Química Analítica Cualitativa Jorge Yáñez S Depto. de Química Analítica e Inorgánica Facultad de Ciencias Químicas Universidad de Concepción 1 TERMINOLOGÍA CROMATOGRÁFICA
TERMINOLOGÍA CROMATOGRÁFICA Curso Química Analítica Cualitativa Jorge Yáñez S Depto. de Química Analítica e Inorgánica Facultad de Ciencias Químicas Universidad de Concepción 1 TERMINOLOGÍA CROMATOGRÁFICA
Separación e identificación de lípidos de membrana
 Separación e identificación de lípidos de membrana Objetivos Separación e identificación de especies de fosfolípidos por cromatografía de capa fina (TLC, Thin Layer Chromatography) TLC monodimensional
Separación e identificación de lípidos de membrana Objetivos Separación e identificación de especies de fosfolípidos por cromatografía de capa fina (TLC, Thin Layer Chromatography) TLC monodimensional
LABORATORIO DE QUÍMICA INGENIERÍA FORESTAL-RÉGIMEN ANUAL. Prof. Fidel Muñoz Pinto Laboratorio de Polímeros Departamento de Química 2016
 LABORATORIO DE QUÍMICA INGENIERÍA FORESTAL-RÉGIMEN ANUAL PRÁCTICA Nº 7 CROMATOGRAFÍA EN PAPEL Y CAPA FINA Prof. Fidel Muñoz Pinto Laboratorio de Polímeros Departamento de Química 2016 Marco teórico. Las
LABORATORIO DE QUÍMICA INGENIERÍA FORESTAL-RÉGIMEN ANUAL PRÁCTICA Nº 7 CROMATOGRAFÍA EN PAPEL Y CAPA FINA Prof. Fidel Muñoz Pinto Laboratorio de Polímeros Departamento de Química 2016 Marco teórico. Las
INTRODUCCIÓN. Separación de biomoléculas. análisis y purificación. CROMATOGRAFIA (chroma-color y graphein-escribir)
 INTRODUCCIÓN CROMATOGRAFIA (chroma-color y graphein-escribir) Separación de biomoléculas proteínas péptidos aminoácidos lípidos ADN/ARN Mikhail Tswett 1906 en función de su diferente distribución en dos
INTRODUCCIÓN CROMATOGRAFIA (chroma-color y graphein-escribir) Separación de biomoléculas proteínas péptidos aminoácidos lípidos ADN/ARN Mikhail Tswett 1906 en función de su diferente distribución en dos
cromatografía 03/07/2012 INTRODUCCIÓN Etapas de un análisis cuantitativo Curso: Química Analítica II Loreto Ascar 2012 Proceso Analítico
 cromatografía Curso: Química Analítica II Loreto Ascar 2012 INTRODUCCIÓN Cómo determinar un analito en una muestra problema? X Proceso Analítico Etapas de un análisis cuantitativo Elección del método Obtención
cromatografía Curso: Química Analítica II Loreto Ascar 2012 INTRODUCCIÓN Cómo determinar un analito en una muestra problema? X Proceso Analítico Etapas de un análisis cuantitativo Elección del método Obtención
CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN
 CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN Curso: Química Analítica II Loreto Ascar 2012 Esquema de las bases de la separación en cromatografía de: (a)absorción, (b) partición, (c) Intercambio iónico y (d)
CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN Curso: Química Analítica II Loreto Ascar 2012 Esquema de las bases de la separación en cromatografía de: (a)absorción, (b) partición, (c) Intercambio iónico y (d)
CROMATOGRAFÍA EN CAPA FINA
 CROMATOGRAFÍA EN CAPA FINA OBJETIVOS a) Conocer la técnica de cromatografía en capa fina, c.c.f., sus características y los factores que en ella intervienen. b) Calcular valores de r.f. de varias sustancias
CROMATOGRAFÍA EN CAPA FINA OBJETIVOS a) Conocer la técnica de cromatografía en capa fina, c.c.f., sus características y los factores que en ella intervienen. b) Calcular valores de r.f. de varias sustancias
Sustituir fotografía. Sustituir texto
 Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
Definición. Definición (IUPAC) graphein = escribir. chroma = color INTERACCIÓN. Mikhail Tswett, 1906
 Definición Definición (IUPAC) La cromatografía es un método físico de separación en el cual los componentes a separar se distribuyen entre dos fases, una que es estacionaria (fase estacionaria) mientras
Definición Definición (IUPAC) La cromatografía es un método físico de separación en el cual los componentes a separar se distribuyen entre dos fases, una que es estacionaria (fase estacionaria) mientras
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN. Ingeniería Ambiental
 TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
ANTECEDENTES Métodos generales de extracción y purificación
 ANTECEDENTES El estudio de los Agaves es de gran importancia debido a su uso tradicional como medicamento en diferentes culturas como la de la India y México. Los Agaves se utilizan como diuréticos, antisifilítico,
ANTECEDENTES El estudio de los Agaves es de gran importancia debido a su uso tradicional como medicamento en diferentes culturas como la de la India y México. Los Agaves se utilizan como diuréticos, antisifilítico,
CROMATOGRAFIA EN CAPA FINA
 I. OBJETIVOS PRACTICA VIII CROMATOGRAFIA EN CAPA FINA a) Conocer la técnica de cromatografía en capa fina, c.c.f., sus características y los factores que en ella intervienen. b) Calcular valores de r.f.
I. OBJETIVOS PRACTICA VIII CROMATOGRAFIA EN CAPA FINA a) Conocer la técnica de cromatografía en capa fina, c.c.f., sus características y los factores que en ella intervienen. b) Calcular valores de r.f.
Juárez Martínez Julio César Reporte Práctica no. 8. Cromatografía en Capa Fina. Cromatografía de tinta negra de plumón en papel toalla en rollo
 Cromatografía en Capa Fina Objetivo: Conocer dos diferentes tecnicas de cromatografia como medios complementarios en la separación y análisis de compuestos químicos. Resultados: Cromatografía de tinta
Cromatografía en Capa Fina Objetivo: Conocer dos diferentes tecnicas de cromatografia como medios complementarios en la separación y análisis de compuestos químicos. Resultados: Cromatografía de tinta
CROMATOGRAFIA EN CAPA FINA. a) Conocer la técnica de cromatografía en capa fina, (c.c.f.), sus características y los factores que en ella intervienen.
 CROMATOGRAFIA EN CAPA FINA I. OBJETIVOS a) Conocer la técnica de cromatografía en capa fina, (c.c.f.), sus características y los factores que en ella intervienen. b) Calcular valores de r.f. de varias
CROMATOGRAFIA EN CAPA FINA I. OBJETIVOS a) Conocer la técnica de cromatografía en capa fina, (c.c.f.), sus características y los factores que en ella intervienen. b) Calcular valores de r.f. de varias
Curso interactivo de cromatografía de líquidos. Módulo 1 parte A. Dr. Juan Carlos Vázquez Lira Abril 2016
 Curso interactivo de cromatografía de líquidos Módulo 1 parte A Dr. Juan Carlos Vázquez Lira Abril 2016 Bases de la cromatografía CROMATOGRAFÍA Separación Determinación La cromatografía es una técnica
Curso interactivo de cromatografía de líquidos Módulo 1 parte A Dr. Juan Carlos Vázquez Lira Abril 2016 Bases de la cromatografía CROMATOGRAFÍA Separación Determinación La cromatografía es una técnica
TRABAJO PRÁCTICO Nº 2
 República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Química Orgánica Año: 5 A, B y C Prof. Luis Aguilar
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Química Orgánica Año: 5 A, B y C Prof. Luis Aguilar
INSTITUTO NACIONAL DE MEDICAMENTOS (INAME) FARMACOPEA ARGENTINA
 INSTITUTO NACIONAL DE MEDICAMENTOS (INAME) FARMACOPEA ARGENTINA AV. CASEROS 2161 1264 BUENOS AIRES FAX 5411-4340-0853 R E P U B L I C A A R G E N T I N A ÁCIDO SALICÍLICO Sustancia de Referencia para Ensayos
INSTITUTO NACIONAL DE MEDICAMENTOS (INAME) FARMACOPEA ARGENTINA AV. CASEROS 2161 1264 BUENOS AIRES FAX 5411-4340-0853 R E P U B L I C A A R G E N T I N A ÁCIDO SALICÍLICO Sustancia de Referencia para Ensayos
10. Cromatografía en papel de aminoácidos
 10. romatografía en papel de aminoácidos José Peinado Peinado, Fermín Toribio Meléndez-Valdés Departamento de Bioquímica y Biología Molecular, ampus Universitario de Rabanales, Edificio Severo choa, 14071-órdoba
10. romatografía en papel de aminoácidos José Peinado Peinado, Fermín Toribio Meléndez-Valdés Departamento de Bioquímica y Biología Molecular, ampus Universitario de Rabanales, Edificio Severo choa, 14071-órdoba
COMPLEMENTO TEORICO. CROMATOGRAFIAS ESPECIALES
 UNIVERSIDAD NACIONAL DE LA KM 4, 9000, COMODORO RIVADAVIA PATAGONIA SAN JUAN BOSCO CHUBUT, ARGENTINA FACULTAD DE CIENCIAS NATURALES TEL/FAX: (++54-297)4550339 CARRERA DE FARMACIA CATEDRA DE FARMACOGNOSIA
UNIVERSIDAD NACIONAL DE LA KM 4, 9000, COMODORO RIVADAVIA PATAGONIA SAN JUAN BOSCO CHUBUT, ARGENTINA FACULTAD DE CIENCIAS NATURALES TEL/FAX: (++54-297)4550339 CARRERA DE FARMACIA CATEDRA DE FARMACOGNOSIA
La materia se puede definir como todo aquello que tiene masa y ocupa un volumen.
 Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
LABORATORIO DE QUÍMICA ORGANICA GUÍA No 4: METODOS DE SEPARACIÓN POR CROMATOGRAFÍA Y ESPECTROFOTOMETRIA ULTRAVIOLETA
 LABORATORIO DE QUÍMICA ORGANICA 502502 GUÍA No 4: METODOS DE SEPARACIÓN POR CROMATOGRAFÍA Y ESPECTROFOTOMETRIA ULTRAVIOLETA I. EL PROBLEMA Separar e identificar los aminoácidos presentes en el extracto
LABORATORIO DE QUÍMICA ORGANICA 502502 GUÍA No 4: METODOS DE SEPARACIÓN POR CROMATOGRAFÍA Y ESPECTROFOTOMETRIA ULTRAVIOLETA I. EL PROBLEMA Separar e identificar los aminoácidos presentes en el extracto
QUÍMICA BIOLÓGICA. DEPARTAMENTO DE BQCA. FCN Y CS. UNPSJB 2017
 QUÍMICA BIOLÓGICA. DEPARTAMENTO DE BQCA. FCN Y CS. UNPSJB 2017 CROMATOGRAFIA (chroma-color y graphein-escribir) Separación de biomoléculas en función de su diferente distribución en dos FASES ( siempre!)
QUÍMICA BIOLÓGICA. DEPARTAMENTO DE BQCA. FCN Y CS. UNPSJB 2017 CROMATOGRAFIA (chroma-color y graphein-escribir) Separación de biomoléculas en función de su diferente distribución en dos FASES ( siempre!)
Análisis Funcional Orgánico. Cromatografía Líquida de Alta Resolución (HPLC/CLAR)
 Análisis Funcional Orgánico Cromatografía Líquida de Alta Resolución (HPLC/CLAR) PARTE A Introducción Técnicas instrumentales cromatográficas 1. Gaseosa líquida (CGL) o sólida (CGS) 2. Líquida de Alta
Análisis Funcional Orgánico Cromatografía Líquida de Alta Resolución (HPLC/CLAR) PARTE A Introducción Técnicas instrumentales cromatográficas 1. Gaseosa líquida (CGL) o sólida (CGS) 2. Líquida de Alta
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
CROMATOGRAFÍA LÍQUIDA DE ADSORCIÓN EN COLUMNA (CC) Y CAPA FINA (TLC)
 PRÁCTICA 9: CROMATOGRAFÍA LÍQUIDA DE ADSORCIÓN EN COLUMNA (CC) Y CAPA FINA (TLC) 1. INTRODUCCIÓN La cromatografía es un método físico de separación basado en la diferencia de distribución de los componentes
PRÁCTICA 9: CROMATOGRAFÍA LÍQUIDA DE ADSORCIÓN EN COLUMNA (CC) Y CAPA FINA (TLC) 1. INTRODUCCIÓN La cromatografía es un método físico de separación basado en la diferencia de distribución de los componentes
cromatografía 03/07/2012 Tipos de cromatografía en columnas Curso: Química Analítica II Loreto Ascar 2012 LIQUIDO SUPERCRITICO
 cromatografía Curso: Química Analítica II Loreto Ascar 2012 GASES FLUIDO SUPERCRITICO LIQUIDO CROMATOGRAFIA GAS - SOLIDO CROMATOGRAFIA GAS - LIQUIDO COLUMNA PLANAR LSC BPC IEC SEC TLC PC BPC - RP BPC -
cromatografía Curso: Química Analítica II Loreto Ascar 2012 GASES FLUIDO SUPERCRITICO LIQUIDO CROMATOGRAFIA GAS - SOLIDO CROMATOGRAFIA GAS - LIQUIDO COLUMNA PLANAR LSC BPC IEC SEC TLC PC BPC - RP BPC -
CARACTERISTICAS DE LAS DISOLUCIONES Mezcla: unión de dos o mas sustancias, que no se combinan químicamente
 CARACTERISTICAS DE LAS DISOLUCIONES Mezcla: unión de dos o mas sustancias, que no se combinan químicamente Las mezclas están formadas por una sustancia que se encuentra en mayor proporción llamada fase
CARACTERISTICAS DE LAS DISOLUCIONES Mezcla: unión de dos o mas sustancias, que no se combinan químicamente Las mezclas están formadas por una sustancia que se encuentra en mayor proporción llamada fase
CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO. Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión
 EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
Tema 2: Tratamiento de muestras y técnicas de separación de analitos. Tratamiento de muestras (algunas directrices) ecosistema ( contaminado?
 Tema 2: Tratamiento de s y técnicas de separación de analitos. Tratamiento de s (algunas directrices) ecosistema ( contaminado?) toma y preparación, técnica analítica 1) Toma de una representativa: réplica
Tema 2: Tratamiento de s y técnicas de separación de analitos. Tratamiento de s (algunas directrices) ecosistema ( contaminado?) toma y preparación, técnica analítica 1) Toma de una representativa: réplica
PROCESOS INDUSTRIALES. Ing. Carlos H. Gómez R. Msc.
 PROCESOS INDUSTRIALES Ing. Carlos H. Gómez R. Msc. QUE ES UN PROCESO? PRODUCCION DE AMONIACO QUE ES UN PROCESO? PRODUCCION DE ACIDO CLORHIDRICO PRODUCCION DE HIDROXIDO DE SODIO Producción de detergentes
PROCESOS INDUSTRIALES Ing. Carlos H. Gómez R. Msc. QUE ES UN PROCESO? PRODUCCION DE AMONIACO QUE ES UN PROCESO? PRODUCCION DE ACIDO CLORHIDRICO PRODUCCION DE HIDROXIDO DE SODIO Producción de detergentes
filosofiatotal.blogspot.com depcienat1.blogspot.com
 www.alambiques.info filosofiatotal.blogspot.com depcienat1.blogspot.com www.panreac.es Ahhhh! Un vaso de limonada helada es muy refrescante en un día caluroso. La limonada es una combinación de jugo de
www.alambiques.info filosofiatotal.blogspot.com depcienat1.blogspot.com www.panreac.es Ahhhh! Un vaso de limonada helada es muy refrescante en un día caluroso. La limonada es una combinación de jugo de
CLASIFICACIONES DE LA MATERIA. Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia.
 CLASIFICACIONES DE LA MATERIA Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia. LA MATERIA Es todo aquello que ocupa un sitio en el espacio, se puede tocar,
CLASIFICACIONES DE LA MATERIA Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia. LA MATERIA Es todo aquello que ocupa un sitio en el espacio, se puede tocar,
Clasificación. Según geometría del tren separador
 Clasificación Según geometría del tren separador la fase estacionaria está contenida en un tubo estrecho y se fuerza el paso de la fase móvil por gravedad o presión En columna Lecho abierto o plana la
Clasificación Según geometría del tren separador la fase estacionaria está contenida en un tubo estrecho y se fuerza el paso de la fase móvil por gravedad o presión En columna Lecho abierto o plana la
INTRODUCCIÓN A LA CROMATOGRAFÍA
 INTRODUCCIÓN A LA CROMATOGRAFÍA Curso Química Analítica Cualitativa Jorge Yáñez S Depto. de Química Analítica e Inorgánica Facultad de Ciencias Químicas Universidad de Concepción CROMATOGRAFÍA Método físico
INTRODUCCIÓN A LA CROMATOGRAFÍA Curso Química Analítica Cualitativa Jorge Yáñez S Depto. de Química Analítica e Inorgánica Facultad de Ciencias Químicas Universidad de Concepción CROMATOGRAFÍA Método físico
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
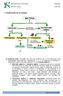 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
FASES DEL PROCESO CROMATOGRÁFICO
 Apéndice CROMATOGRAFíA La cromatografía agrupa un importante grupo de técnicas que permiten separar componentes de mezclas complejas. En todas las separaciones cromatográficas la muestra que se desea separar
Apéndice CROMATOGRAFíA La cromatografía agrupa un importante grupo de técnicas que permiten separar componentes de mezclas complejas. En todas las separaciones cromatográficas la muestra que se desea separar
TRANSFERENCIA DE MASA II EXTRACCION LIQUIDA-LIQUIDA
 TRANSFERENCIA DE MASA II EXTRACCION LIQUIDA-LIQUIDA La Extracción Líquido- Líquido es una operación de separación muy importante en ingeniería química. Se aplica para llevar a cabo la separación de mezclas
TRANSFERENCIA DE MASA II EXTRACCION LIQUIDA-LIQUIDA La Extracción Líquido- Líquido es una operación de separación muy importante en ingeniería química. Se aplica para llevar a cabo la separación de mezclas
Parte B Módulo 1 y 2. Abril 2016
 Parte B Módulo 1 y 2 Abril 2016 La longitud de una columna en la que el soluto experimenta un equilibrio completo entre las dos fases Eficiencia de una separación cromatográfica número de platos teóricos
Parte B Módulo 1 y 2 Abril 2016 La longitud de una columna en la que el soluto experimenta un equilibrio completo entre las dos fases Eficiencia de una separación cromatográfica número de platos teóricos
SELECCIÓN DE COLUMNAS Y ORDEN DE ELUCIÓN
 SELECCIÓN DE COLUMNAS Y ORDEN DE ELUCIÓN 1. Con base en la polaridad de los siguientes compuestos, indique el orden de elución en un proceso de separación cromatográfico de gases: a).- Columna SE-30 Versamid
SELECCIÓN DE COLUMNAS Y ORDEN DE ELUCIÓN 1. Con base en la polaridad de los siguientes compuestos, indique el orden de elución en un proceso de separación cromatográfico de gases: a).- Columna SE-30 Versamid
Agua y Soluciones SEMANA 07. Licda. Lilian Judith Guzmán M.
 Agua y Soluciones SEMANA 07 Licda. Lilian Judith Guzmán M. AGUA El agua es el compuesto químico más abundante en los seres vivos y en nuestro planeta, lo cual lo hace ser uno de los compuestos más extraordinarios.
Agua y Soluciones SEMANA 07 Licda. Lilian Judith Guzmán M. AGUA El agua es el compuesto químico más abundante en los seres vivos y en nuestro planeta, lo cual lo hace ser uno de los compuestos más extraordinarios.
EXTRACCIÓN SÓLIDO - LÍQUIDO. Se le llama también: Lixiviación. Lavado. Percolación Infusión. Decantación por sedimentación
 LIXIVIACIÓN Es la disolución preferente de uno o más componentes de una mezcla sólida por contacto con un disolvente líquido. Es la eliminación de una fracción soluble, en forma de solución, a partir de
LIXIVIACIÓN Es la disolución preferente de uno o más componentes de una mezcla sólida por contacto con un disolvente líquido. Es la eliminación de una fracción soluble, en forma de solución, a partir de
CÓMO SE SEPARAN LOS COMPONENTES DE UNA MEZCLA? 2. TÉCNICAS DE SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA.
 1. INTRODUCCIÓN. CÓMO SE SEPARAN LOS COMPONENTES DE UNA MEZCLA? Cuando una sustancia cualquiera contiene a otra distribuida en su seno como partículas muy pequeñas, se habla de un sistema disperso o de
1. INTRODUCCIÓN. CÓMO SE SEPARAN LOS COMPONENTES DE UNA MEZCLA? Cuando una sustancia cualquiera contiene a otra distribuida en su seno como partículas muy pequeñas, se habla de un sistema disperso o de
T r a b a j o P r á c t i c o N r o. 2 : C r o m a t o g r a f í a d e a d s o r c i ó n 1
 T r a b a j o P r á c t i c o N r o. 2 : C r o m a t o g r a f í a d e a d s o r c i ó n 1 Fundamentos Teóricos La cromatografía es una técnica que permite separar los componentes de una mezcla. Esta separación
T r a b a j o P r á c t i c o N r o. 2 : C r o m a t o g r a f í a d e a d s o r c i ó n 1 Fundamentos Teóricos La cromatografía es una técnica que permite separar los componentes de una mezcla. Esta separación
FÍSICA Y QUÍMICA 2º ESO Tema 2: LA MATERIA Mezclas y Soluciones. Sustancias puras y mezclas
 Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
TRABAJO PRACTICO Nº 4: SEPARACIÓN DE FOSFOLÍPIDOS INDIVIDUALES DESCRIPCIÓN DE LOS MÉTODOS UTILIZADOS. Preparación de extractos en solventes orgánicos
 TRABAJO PRACTICO Nº 4: SEPARACIÓN DE FOSFOLÍPIDOS INDIVIDUALES DESCRIPCIÓN DE LOS MÉTODOS UTILIZADOS Preparación de extractos en solventes orgánicos Los lípidos son sustancias que presentan muy baja solubilidad
TRABAJO PRACTICO Nº 4: SEPARACIÓN DE FOSFOLÍPIDOS INDIVIDUALES DESCRIPCIÓN DE LOS MÉTODOS UTILIZADOS Preparación de extractos en solventes orgánicos Los lípidos son sustancias que presentan muy baja solubilidad
APÉNDICE II DESECACIÓN Y AGENTES DESECANTES DESECACIÓN
 259 APÉNDICE II DESECACIÓN Y AGENTES DESECANTES DESECACIÓN La desecación se emplea para extraer la humedad de los líquidos, soluciones y sustancias sólidas. El grado de desecación de una sustancia depende
259 APÉNDICE II DESECACIÓN Y AGENTES DESECANTES DESECACIÓN La desecación se emplea para extraer la humedad de los líquidos, soluciones y sustancias sólidas. El grado de desecación de una sustancia depende
Universidad Iberoamericana
 Universidad Iberoamericana Ingeniería Química Laboratorio de Química General Grupo R Equipo 1 : Extracción y Cristalización por Francisco José Guerra Millán Prof. Celia Margarita del Valle Méndez I Extracción
Universidad Iberoamericana Ingeniería Química Laboratorio de Química General Grupo R Equipo 1 : Extracción y Cristalización por Francisco José Guerra Millán Prof. Celia Margarita del Valle Méndez I Extracción
INSTITUTO NACIONAL DE MEDICAMENTOS (INAME) FARMACOPEA ARGENTINA
 INSTITUTO NACIONAL DE MEDICAMENTOS (INAME) FARMACOPEA ARGENTINA AV. CASEROS 2161 1264 BUENOS AIRES FAX 5411-4340-0853 R E P U B L I C A A R G E N T I N A DEXAMETASONA Sustancia de Referencia para Ensayos
INSTITUTO NACIONAL DE MEDICAMENTOS (INAME) FARMACOPEA ARGENTINA AV. CASEROS 2161 1264 BUENOS AIRES FAX 5411-4340-0853 R E P U B L I C A A R G E N T I N A DEXAMETASONA Sustancia de Referencia para Ensayos
Unidad 13. Mix. Sustancias puras y mezclas
 Unidad 13. Mix. Sustancias puras y mezclas La materia y su clasificación Recuerda que materia es todo aquello que tiene masa y ocupa un volumen. Según su composición la materia se puede clasificar en sustancias
Unidad 13. Mix. Sustancias puras y mezclas La materia y su clasificación Recuerda que materia es todo aquello que tiene masa y ocupa un volumen. Según su composición la materia se puede clasificar en sustancias
Métodos de separación de sistemas materiales sencillos
 Métodos de separación de sistemas materiales sencillos SISTEMAS MATERIALES Mezclas Separación física Sustancias Puras no Son uniformes? si si Pueden descomponerse por reacciones químicas? no Mezclas heterogéneas
Métodos de separación de sistemas materiales sencillos SISTEMAS MATERIALES Mezclas Separación física Sustancias Puras no Son uniformes? si si Pueden descomponerse por reacciones químicas? no Mezclas heterogéneas
Juan Rolando Vázquez Miranda
 Juan Rolando Vázquez Miranda CROMATOGRAFIA Un método físico utilizado para la separación de los componentes de una muestra en la cual los componentes se distribuyen en dos fases, una de las cuales es estacionaria,
Juan Rolando Vázquez Miranda CROMATOGRAFIA Un método físico utilizado para la separación de los componentes de una muestra en la cual los componentes se distribuyen en dos fases, una de las cuales es estacionaria,
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
CROMATOGRAFÍA. En la siguiente tabla se observan diferentes fases móviles y fases estacionarias en diferentes técnicas de cromatografía:
 CROMATOGRAFÍA La palabra cromatografía significa gráfica de colores y fue diseñada por Michael Tswett en el 1903. Tswett llevó a cabo una extracción de una mezcla de pigmentos de hojas verdes y luego pasó
CROMATOGRAFÍA La palabra cromatografía significa gráfica de colores y fue diseñada por Michael Tswett en el 1903. Tswett llevó a cabo una extracción de una mezcla de pigmentos de hojas verdes y luego pasó
PRÁCTICAS TÉCNICAS DE SEPARACIÓN Y PREPARACIÓN DE DISOLUCIONES FÍSICA Y QUÍMICA 2º
 PRÁCTICAS TÉCNICAS DE SEPARACIÓN Y PREPARACIÓN DE DISOLUCIONES FÍSICA Y QUÍMICA 2º CURSO: NOMBRE: COMPAÑEROS QUE FORMAN TU GRUPO: 1 FILTRACIÓN DE AGUA Y ARENA La filtración es la separación de las partículas
PRÁCTICAS TÉCNICAS DE SEPARACIÓN Y PREPARACIÓN DE DISOLUCIONES FÍSICA Y QUÍMICA 2º CURSO: NOMBRE: COMPAÑEROS QUE FORMAN TU GRUPO: 1 FILTRACIÓN DE AGUA Y ARENA La filtración es la separación de las partículas
LOGO. Soluciones. M. C. Rita Paz Samaniego
 LOGO Soluciones M. C. Rita Paz Samaniego Contenido Qué es una solución Terminología de solubilidad Solubilidad de compuestos Unidades de concentración de soluciones Qué es una solución? Una solución es
LOGO Soluciones M. C. Rita Paz Samaniego Contenido Qué es una solución Terminología de solubilidad Solubilidad de compuestos Unidades de concentración de soluciones Qué es una solución? Una solución es
Disoluciones. Química General II 2011
 Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO I)
 PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO I) Las preguntas de este tipo constan de un enunciado y de cuatro posibilidades de respuesta entre las cuales debe escoger la que considere correcta
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO I) Las preguntas de este tipo constan de un enunciado y de cuatro posibilidades de respuesta entre las cuales debe escoger la que considere correcta
PREPARACIÓN DE SOLUCIONES
 PRÁCTICA 4 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las soluciones Preparar soluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO. Las
PRÁCTICA 4 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las soluciones Preparar soluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO. Las
Métodos para la determinación de grasas
 Practica 4 Métodos para la determinación de grasas Antecedentes Los lípidos se encuentran ampliamente distribuidos en animales y vegetales, formado parte fundamental de membranas celulares. En los alimentos
Practica 4 Métodos para la determinación de grasas Antecedentes Los lípidos se encuentran ampliamente distribuidos en animales y vegetales, formado parte fundamental de membranas celulares. En los alimentos
INSTITUTO NACIONAL DE MEDICAMENTOS (INAME) FARMACOPEA ARGENTINA
 INSTITUTO NACIONAL DE MEDICAMENTOS (INAME) FARMACOPEA ARGENTINA AV. CASEROS 2161 1264 BUENOS AIRES FAX 5411-4340-0853 R E P U B L I C A A R G E N T I N A IBUPROFENO Sustancia de Referencia para Ensayos
INSTITUTO NACIONAL DE MEDICAMENTOS (INAME) FARMACOPEA ARGENTINA AV. CASEROS 2161 1264 BUENOS AIRES FAX 5411-4340-0853 R E P U B L I C A A R G E N T I N A IBUPROFENO Sustancia de Referencia para Ensayos
MI PEQUEÑO ARCOIRIS. Título del trabajo SÍLICE. Pseudónimo de integrantes. Química. Área. Local. Categoría. Investigación Experimental.
 MI PEQUEÑO ARCOIRIS Título del trabajo SÍLICE Pseudónimo de integrantes Química Área Local Categoría Investigación Experimental Modalidad 3852291 Folio de Inscripción 1 Resumen El presente trabajo describe
MI PEQUEÑO ARCOIRIS Título del trabajo SÍLICE Pseudónimo de integrantes Química Área Local Categoría Investigación Experimental Modalidad 3852291 Folio de Inscripción 1 Resumen El presente trabajo describe
IDENTIFICACION DE COLORANTES ORGANICOS SINTETICOS HIDROSOLUBLES EN ALIMENTOS Método Cualitativo Cromatografía en papel Basado en Schmidt-Hebbel, 1973
 Basado en Schmidt-Hebbel, 1973 Página 1 de 5 1. OBJETIVO Identificar colorantes orgánicos hidrosolubles en alimentos por método cualitativo utilizando cromatografía en papel. 2. CAMPO DE APLICACIÓN Y ALCANCE
Basado en Schmidt-Hebbel, 1973 Página 1 de 5 1. OBJETIVO Identificar colorantes orgánicos hidrosolubles en alimentos por método cualitativo utilizando cromatografía en papel. 2. CAMPO DE APLICACIÓN Y ALCANCE
Análisis de ácido salicílico en agua destinada al consumo humano.
 Trabajo Práctico N 11 EL PROCESO DE MEDIDA QUÍMICA Proceso Analítico Total (PAT) Análisis de ácido salicílico en agua destinada al consumo humano. Objetivo: Aplicar un método de preconcentración (extracción
Trabajo Práctico N 11 EL PROCESO DE MEDIDA QUÍMICA Proceso Analítico Total (PAT) Análisis de ácido salicílico en agua destinada al consumo humano. Objetivo: Aplicar un método de preconcentración (extracción
CAPITULO 4. LA OPERACIÓN UNITARIA COMO PROCESO DE TRANSFERENCIA DE MASA, ENERGÍA Y/O CANTIDAD DE MOVIMIENTO PROF. JOSE MAYORGA
 UNIVERSIDAD DE LOS ANDES FACULTAD DE INGENIERIA INGENIERIA QUIMICA INTRODUCCIÓN A LA INGENIERIA QUIMICA CAPITULO 4. LA OPERACIÓN UNITARIA COMO PROCESO DE TRANSFERENCIA DE MASA, ENERGÍA Y/O CANTIDAD DE
UNIVERSIDAD DE LOS ANDES FACULTAD DE INGENIERIA INGENIERIA QUIMICA INTRODUCCIÓN A LA INGENIERIA QUIMICA CAPITULO 4. LA OPERACIÓN UNITARIA COMO PROCESO DE TRANSFERENCIA DE MASA, ENERGÍA Y/O CANTIDAD DE
LA DIVERSIDAD DE LA MATERIA
 Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
Unidad 2. La materia
 Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
MEZCLAS Y DISOLUCIONES. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
Parámetros cromatográficos
 Parámetros cromatográficos El detector registra cambios en alguna propiedad de eluyente. Los cambios son registrados en función del tiempo. El diagrama de la respuesta del detector en función del tiempo
Parámetros cromatográficos El detector registra cambios en alguna propiedad de eluyente. Los cambios son registrados en función del tiempo. El diagrama de la respuesta del detector en función del tiempo
DETERMINACIÓN DE PUNTO DE FUSIÓN
 DETERMINACIÓN DE PUNTO DE FUSIÓN La pureza e identidad de una sustancia orgánica puede quedar establecida cuando sus constantes físicas (punto de fusión, punto de ebullición, color, densidad, índice de
DETERMINACIÓN DE PUNTO DE FUSIÓN La pureza e identidad de una sustancia orgánica puede quedar establecida cuando sus constantes físicas (punto de fusión, punto de ebullición, color, densidad, índice de
Cuantificación del porcentaje de grasa cruda, extracto lipídico, extracto etéreo o fracción lipídica
 1 PRACTICA N 9 Cuantificación del porcentaje de grasa cruda, extracto lipídico, extracto etéreo o fracción lipídica I. Introducción: La cuantificación del contenido de grasa cruda es otra de las determinaciones
1 PRACTICA N 9 Cuantificación del porcentaje de grasa cruda, extracto lipídico, extracto etéreo o fracción lipídica I. Introducción: La cuantificación del contenido de grasa cruda es otra de las determinaciones
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
E.T. Nro. 27 Hipólito Yrigoyen TRABAJOS PRÁCTICOS DE QUÍMICA ORGÁNICA l. Trabajo Práctico Nro. 2: Cromatografía de ad sorción 1
 Trabajo Práctico Nro. 2: Cromatografía de ad sorción 1 Fundamentos Teóricos La cromatografía es una técnica que permite separar los componentes de una mezcla. Esta separación se logra utilizando un sistema
Trabajo Práctico Nro. 2: Cromatografía de ad sorción 1 Fundamentos Teóricos La cromatografía es una técnica que permite separar los componentes de una mezcla. Esta separación se logra utilizando un sistema
4.- Métodos de separación de mezclas: filtración, evaporación y sublimación
 4.- Métodos de separación de mezclas: filtración, evaporación y sublimación Marco teórico En la naturaleza, las sustancias se encuentran en forma de mezclas y sustancias puras; cuando se trabaja con mezclas,
4.- Métodos de separación de mezclas: filtración, evaporación y sublimación Marco teórico En la naturaleza, las sustancias se encuentran en forma de mezclas y sustancias puras; cuando se trabaja con mezclas,
Cromatografía de Líquidos
 Cromatografía de Líquidos Elba Rojas Escudero ERE Ab o Ad??? Fundamentos Temario Definiciones básicas Aspectos teóricos Instrumentación Elementos básicos Columnas Inyectores Detectores y sistemas acoplados
Cromatografía de Líquidos Elba Rojas Escudero ERE Ab o Ad??? Fundamentos Temario Definiciones básicas Aspectos teóricos Instrumentación Elementos básicos Columnas Inyectores Detectores y sistemas acoplados
Tema 5: Disoluciones. (Químic General) Disoluciones 6 de noviembre de / 38
 Tema 5: Disoluciones Tipos de disoluciones. Concentración. Solubilidad de gases. Diagramas de fases de dos componentes. Propiedades coligativas: presión osmótica, disminución del punto de fusión y aumento
Tema 5: Disoluciones Tipos de disoluciones. Concentración. Solubilidad de gases. Diagramas de fases de dos componentes. Propiedades coligativas: presión osmótica, disminución del punto de fusión y aumento
SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA
 PRÁCTICA Nº 3 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de diversas muestras problema. I. FUNDAMENTOS
PRÁCTICA Nº 3 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de diversas muestras problema. I. FUNDAMENTOS
Soluciones y unidades de concentración
 MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
Soluciones y unidades de concentración
 Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
Estados de la materia y cambios de fase
 3 Año de Química: Sistemas Materiales Prof. Javier Ponce Qué es Ciencia? Ciencia (en latíns cientia, de scire, conocer ), término que en su sentido más amplio se emplea para referirse al conocimiento sistematizado
3 Año de Química: Sistemas Materiales Prof. Javier Ponce Qué es Ciencia? Ciencia (en latíns cientia, de scire, conocer ), término que en su sentido más amplio se emplea para referirse al conocimiento sistematizado
Usando el nomograma presión-temperatura de la figura 1, contesta las siguientes preguntas:
 GUIA DE ESTUDIOS PARA EL SEGUNDO EXAMEN. Usando el nomograma presión-temperatura de la figura 1, contesta las siguientes preguntas: 1. Cuál es el punto normal de ebullición (a 760 mmhg), para un compuesto
GUIA DE ESTUDIOS PARA EL SEGUNDO EXAMEN. Usando el nomograma presión-temperatura de la figura 1, contesta las siguientes preguntas: 1. Cuál es el punto normal de ebullición (a 760 mmhg), para un compuesto
Componentes de una disolución. El disolvente El soluto Concentración de una disolución. concentración solubilidad
 Componentes de una disolución. Todas las disoluciones tienen dos componentes: El disolvente es el componente que se encuentra en mayor proporción. Este componente no cambia de estado. El soluto es el componente
Componentes de una disolución. Todas las disoluciones tienen dos componentes: El disolvente es el componente que se encuentra en mayor proporción. Este componente no cambia de estado. El soluto es el componente
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
