ANÁLISIS DEL VIH 1/2 SURE CHECK
|
|
|
- Luis Vidal Villanueva
- hace 6 años
- Vistas:
Transcripción
1 REF Kit de 25 pruebas ANÁLISIS DEL VIH 1/2 SURE CHECK Lea el prospecto del producto completamente antes de usarlo. Siga cuidadosamente las instrucciones cuando realice la prueba, ya que el no hacerlo puede proporcionar resultados de la prueba inexactos. Los usuarios de esta prueba deben seguir las precauciones universales de los CDC para la prevención de la transmisión del virus de la inmunodeficiencia humana, del virus de la hepatitis B y otros patógenos sanguíneos. 1 Complejidad según las CLIA: exenta para sangre completa por punción dactilar y sangre completa por punción venosa. Toda modificación hecha por el laboratorio a las instrucciones del sistema de análisis o sistema de prueba por la administración de alimentos y medicamentos (Fonda and Drupa Administrativo, FA) ocasionará que la prueba ya no cumpla con los requisitos para la categoría exenta. Complejidad según las CLIA: moderada para muestras de suero y plasma. ALMACENAMIENTO: Almacenar entre 8 y 30 C (46 y 86 F) Nombre y uso previsto El análisis del VIH 1/2 SURE CHECK de Chembio es una prueba inmunocromatográfica de un solo uso para la detección de los anticuerpos contra el virus de la inmunodeficiencia humana tipo 1 (VIH-1) y tipo 2 (VIH-2) en sangre completa por punción dactilar, sangre completa por punción venosa y muestras de suero o plasma. El análisis del VIH 1/2 SURE CHECK de Chembio tiene un uso previsto como análisis de diagnóstico inmediato para ayudar en el diagnóstico de la infección por el VIH-1 y VIH-2. Esta prueba es adecuada para utilizarse en los algoritmos de múltiples pruebas diseñadas para la validación estadística de los resultados de la prueba rápida del VIH. Cuando están disponibles múltiples pruebas rápidas del VIH, esta prueba deberá utilizarse en los algoritmos de múltiples pruebas adecuadas. Restricciones La venta del análisis del VIH 1/2 SURE CHECK de Chembio se limita a laboratorios clínicos que tienen un programa de control de calidad adecuado, que incluye actividades sistemáticas planificadas que brindan una confianza adecuada de que se cumplirán los requisitos de calidad y garantizan que los operadores recibirán y usarán los materiales instructivos. El análisis del VIH 1/2 SURE CHECK de Chembio está aprobado para su uso solo por un agente de un laboratorio clínico. Los centros de análisis no clínicos que ofrecen análisis de VIH rápidos exentos deben tener su propio certificado de exención de CLIA o tener un contrato de trabajo según el certificado de CLIA de un laboratorio existente. Los sujetos de la prueba deben recibir la notificación de información del sujeto antes de la recolección de la muestra e información adecuada cuando se proporcionan los resultados de la prueba. El análisis del VIH 1/2 SURE CHECK de Chembio no está aprobado para el uso de selección de donantes de sangre, plasma, células o tejidos. Resumen y explicación de la prueba Descubierto en 1983, el virus de la inmunodeficiencia humana (VIH) es un retrovirus identificado como agente etiológico del síndrome de inmunodeficiencia adquirida (SIDA) y un complejo relacionado con el SIDA. 2 El SIDA se caracteriza por cambios en la población de linfocitos T que desempeñan un papel fundamental en el sistema de defensa inmunitario. En las personas infectadas, el virus reduce la subpoblación de linfocitos T conocidos como linfocitos T cooperadores, lo que deja a estos pacientes susceptibles de sufrir infecciones oportunistas y ciertos tipos de tumores malignos. Las vías principales de transmisión son el contacto sexual, la exposición a sangre o hemoderivados infectados (que incluye el uso compartido de jeringas y agujas infectadas) y la transmisión maternofilial. 3-5 A pesar de que la tasa de infección ha disminuido en ciertos países, la cantidad de personas infectadas por el VIH en todo el mundo ha seguido aumentando. A finales de 2005, había aproximadamente 40.3 millones de personas infectadas por el VIH o SIDA, un aumento de casi 37.5 millones en En 2005, casi 5 millones de personas se infectaron por primera vez por el VIH. Ese mismo año, más de 3 millones de personas murieron por enfermedades relacionadas con el SIDA; más de 500,000 eran niños. 6 La infección por el VIH, el SIDA y el complejo relacionado con el SIDA se convirtieron en la causa principal de enfermedad y muerte en los Estados Unidos en las últimas dos décadas. A partir de diciembre de 2001, se informó que un total de 774,467 personas sufrían de SIDA y 448,060 de estas personas habían muerto. Aproximadamente entre 800,000 y 900,000 personas en los Estados Unidos están infectadas por el VIH y aproximadamente entre 80,000 y 280,000 de estas personas pueden no ser conscientes de su estado infectado. 7 El virus del VIH consta de una molécula de ARN genómica protegida por una cápside y una envoltura. La envoltura del VIH es el objetivo principal de la respuesta inmunitaria humoral. La presencia del virus en los pacientes activa la producción de anticuerpos por el sistema inmunitario. La detección de estos anticuerpos se puede usar como una herramienta de diagnóstico. Página 1 de 16
2 En la actualidad se dispone de enzimoinmunoanálisis (Enzyme Immunoassays, EIA), Western Blots (WB), análisis de amplificación de ácidos nucleicos (Nucleic Amplification Test, NAT) y varios otros sistemas de prueba para la detección de la infección por el VIH-1 y VIH El análisis del VIH 1/2 SURE CHECK de Chembio usa antígenos inmovilizados para la detección de los anticuerpos contra el VIH-1 y VIH-2, y es un análisis de diagnóstico inmediato para ayudar en el diagnóstico de la infección por el VIH-1 y VIH-2. Principios biológicos de la prueba El análisis del VIH 1/2 SURE CHECK de Chembio usa una combinación única de una proteína específica de unión a anticuerpos conjugada con partículas de colorante de oro coloidal y antígenos del VIH 1/2 unidos a la membrana de fase sólida. La sangre completa venosa o capilar (punción dactilar), el suero o el plasma se aplican en la punta capilar del muestreador del dispositivo de prueba. El muestreador se introduce en el amortiguador, que se proporciona en un envase sellado. El amortiguador facilita el flujo lateral de la muestra y los reactivos de la prueba y promueve la unión de los anticuerpos al antígeno. La mezcla de la muestraamortiguador migra en la tira reactiva mediante acción capilar, lo que reconstituye el conjugado. Si hay anticuerpos presentes, estos se unen a la proteína de unión a anticuerpos conjugada con oro coloidal. En una muestra reactiva, el complejo inmunitario conjugado con el colorante migra a la membrana de nitrocelulosa, donde es capturado por los antígenos inmovilizados en el área de PRUEBA lo que genera una línea de color rosa/morado. Ante la ausencia de anticuerpos contra el VIH-1 y VIH-2, no se forma una línea de color rosa/morado en el área de PRUEBA. La muestra sigue migrando a lo largo de la membrana y genera una línea de color rosa/morado en el área de CONTROL, que contiene antígenos de inmunoglobulina G. Este control del procedimiento permite demostrar que las muestras y los reactivos se han aplicado y han migrado correctamente a través del dispositivo. Materiales proporcionados Cada kit contiene los componentes para realizar 25 pruebas: 1 prospecto del producto del análisis del VIH 1/2 SURE CHECK 25 copias de notificación de información al sujeto 25 bases para prueba desechables (A) 25 bolsas, cada una con: 1 muestreador con una tira reactiva en su interior (B) 1 tubo con amortiguador unido al muestreador (~350μl) (C) 1 lanceta de seguridad estéril (D) 1 apósito (E) 1 paquete secante (F) MATERIALES NECESARIOS Y DISPONIBLES COMO ACCESORIO PARA EL KIT Controles no reactivos o reactivos del VIH de Chembio (número de catálogo ). Cada paquete contiene: 1 control reactivo del VIH 1 (0.25 ml) 1 control reactivo del VIH 2 (0.25 ml) 1 control no reactivo (0.25 ml) 1 prospecto del producto para controles reactivos o no reactivos de Chembio MATERIALES NECESARIOS PERO NO SUMINISTRADOS: Reloj, cronómetro u otro dispositivo para medir el tiempo Pipeta capaz de dispensar una muestra de 2.5 μl (para todas las muestras con excepción de las muestras de sangre completa por punción dactilar o venosa) Guantes desechables Gasa estéril Toallitas húmedas antisépticas Recipiente para residuos de riesgo biológico Dispositivos de recolección de muestras con excepción de las muestras de sangre completa por punción dactilar. Página 2 de 16
3 Advertencias Para uso diagnóstico IN VITRO 1. lea el prospecto del producto completamente antes de usar este análisis. Siga cuidadosamente las instrucciones, ya que el no hacerlo puede proporcionar resultados de la prueba inexactos. 2. los usuarios de esta prueba deben seguir las precauciones universales de los Centros para el Control y la Prevención de Enfermedades (Centers for Disease Control and Prevention, CDC) para la prevención de la transmisión del virus de la inmunodeficiencia humana, del virus de la hepatitis B y otros patógenos sanguíneos El uso de este kit de prueba con tipos de muestras que no sean aquellas específicamente aprobadas para el uso con este dispositivo puede ocasionar resultados de prueba inexactos. 4. Esta prueba está exenta de las CLIA para el uso solo con muestras de sangre completa por punción dactilar o sangre completa por punción venosa. 5. esta prueba se debe realizar entre 18 y 30 C (64 y 86 F). Si se almacena refrigerada, asegúrese de que la bolsa alcance la temperatura de funcionamiento antes de realizar la prueba. 6. si el kit de pruebas se almacena a temperaturas distintas de la temperatura de almacenamiento de 8 a 30 C (46 a 86 F) o se usa a una temperatura fuera del intervalo de 18 a 30 C (64 a 86 F), use los controles del kit para asegurar un desempeño adecuado de la prueba. 7. las personas infectadas por el VIH-1 o VIH-2 que estén recibiendo un tratamiento antirretrovírico de gran actividad (TARGA) pueden tener resultados negativos falsos. PRECAUCIONES Precauciones de seguridad 1. manipule las muestras y los materiales en contacto con las muestras como si fueran capaces de transmitir la infección. 2. no coma, beba ni fume en el área donde se manipulan las muestras y los reactivos del kit. Evite todo contacto con las manos, los ojos o la boca durante la prueba y la recolección de muestras. 3. use ropa de protección como batas de laboratorio, guantes desechables y protección ocular cuando se manipulen muestras. 4. deseche todas las muestras y materiales usados en el procedimiento de prueba en un recipiente de residuos de riesgo biológico. Las lancetas se deben colocar en un recipiente resistente a las punciones antes de desecharlas. El método recomendado para el desecho de residuos de riesgo biológico es esterilización en autoclave durante un mínimo de 1 hora a 121 C. Los materiales desechables se pueden incinerar. Los desperdicios líquidos se pueden mezclar con desinfectantes químicos adecuados. Se recomienda usar una solución recién preparada de lejía al 10 % (solución al 0.5 % de hipoclorito de sodio). Deje transcurrir 60 minutos para lograr una descontaminación eficaz. NOTA: No esterilice en autoclave soluciones que contengan lejía. 5. Para obtener información adicional sobre bioseguridad, consulte Precauciones universales para la prevención de la transmisión del virus de la inmunodeficiencia humana, virus de la hepatitis B y otros patógenos sanguíneos. 1 Y Actualización de las pautas del servicio de salud pública de Estados Unidos para el manejo de la exposición profesionales al VHB, VHC y VIH, y recomendaciones para la profilaxis posterior a la exposición) Use lejía al 10 % u otros desinfectantes adecuados para limpiar los derrames. La solución de lejía debe estar recién preparada todos los días. Precauciones de manipulación 1. el dispositivo para análisis del VIH 1/2 SURE CHECK de Chembio tiene un filtro para muestras en la parte inferior del dispositivo y una almohadilla absorbente en la parte superior del dispositivo dentro del tubo que envuelve la tira reactiva. Confirme la presencia del filtro para muestras y la almohadilla absorbente antes de realizar la prueba. Si falta alguno de ellos, NO USE EL DISPOSITIVO. 2. no use ningún dispositivo si la bolsa se perforó. No use el dispositivo si falta el paquete secante. 3. Cada dispositivo es para un solo uso únicamente. 4. no use reactivos después de la fecha de vencimiento impresa en la bolsa. Siempre compruebe la fecha de vencimiento antes de realizar la prueba. 5. No mezcle los reactivos de diferentes números de lotes de los kits. 6. A fin de garantizar que los resultados de la prueba sean precisos, el muestreador se debe introducir en el tubo del amortiguador inmediatamente después de la aplicación de la muestra. 7. Se requiere iluminación adecuada para leer los resultados de la prueba. Almacenamiento El análisis del VIH 1/2 SURE CHECK de Chembio se debe almacenar en una bolsa sin abrir entre 8 y 30 C (46 y 86 F). No la congele. No abra la bolsa hasta que esté listo para realizar la prueba. Cuando lo almacene como se indica, los dispositivos de prueba son estables hasta la fecha de vencimiento marcada en la bolsa. RECOLECCIÓN DE MUESTRAS Antes de la recolección de muestras, proporcióneles a los sujetos de la prueba una notificación de información del sujeto y asesoramiento previo a la prueba de acuerdo con las pautas de CDC para realizar una prueba de VIH rápida. 7 El análisis del VIH 1/2 SURE CHECK de Chembio se realiza en sangre completa por punción dactilar, sangre completa por punción venosa, muestras de suero o plasma. Sangre completa por punción dactilar: Prepárese para realizar el procedimiento de recolección de sangre por punción dactilar. Limpie el dedo de la persona que se someterá a la prueba con una toallita húmeda antiséptica. Espere a que el dedo esté completamente seco o séquelo con una gasa estéril. Con una lanceta Página 3 de 16
4 estéril, perfore la piel justo fuera del centro del dedo y limpie la primera gota con la gasa estéril y evite apretar la yema del dedo para acelerar el sangrado, ya que esto puede diluir la sangre con exceso de líquido tisular. Recolecte la muestra de la segunda gota, para lo cual deberá tocar la punta del muestreador del dispositivo con la gota de sangre hasta que la punta del muestreador esté llena. Realice la prueba de inmediato, siguiendo las instrucciones del procedimiento de la prueba. Sangre completa venosa: Extraiga la sangre siguiendo los procedimientos de laboratorio para la obtención de sangre venosa. Recolecte la muestra en un tubo que contenga citrato, heparina o EDTA. Asegúrese de mezclar bien el tubo de sangre. Suero o plasma: Nota: El suero y el plasma solo se deben analizar en laboratorios certificados para realizar pruebas de complejidad moderadas. Extraiga sangre siguiendo los procedimientos de laboratorio para obtener muestras de suero o plasma. Recolecte la muestra en un tubo que no contenga ningún anticoagulante (suero) y en un tubo que contenga citrato, heparina o EDTA (plasma). Recolecte la muestra en un recipiente limpio siguiendo los procedimientos de laboratorio estándar. Las muestras de sangre completa venosa, suero y plasma se pueden analizar de inmediato después de la recolección. Si las muestras no se analizan de inmediato, refrigérelas entre 2 y 8 C (36 y 46 F) luego de la recolección. Estas muestras se deben analizar en un plazo de 3 días de la recolección. Si las muestras no se analizan en un plazo de 3 días de la recolección, las muestras de suero o plasma se deben congelar a -20 C (-4 F) o a una temperatura más baja. NO CONGELE LA SANGRE COMPLETA. Envío de la muestra Si se enviarán las muestras, se deben embalar en cumplimiento con las regulaciones que cubren el transporte de agentes etiológicos. La sangre completa venosa y las muestras de suero y plasma se deben enviar refrigeradas con compresas frías o hielo común. PROCEDIMIENTO DE PRUEBA PARA ENTORNOS EXENTOS DE CLIA Y MODERADOS DE CLIA Preparación del componente del kit Todos los componentes del análisis del VIH 1/2 SURE CHECK de Chembio están listos para usarse según se suministraron. Siga las instrucciones según se indican. Si la muestra que se evaluará está refrigerada, retírela del refrigerador y deje que llegue a una temperatura de 18 a 30 C (64 a 86 F) antes de realizar la prueba. 1 ABRA LA BOLSA, RETIRE E IDENTIFIQUE LOS COMPONENTES. filtro para muestras almohadilla absorbente SURECHECK Dispositivo de prueba Tapa del amortiguador Base para la prueba (transparente) Identifique el dispositivo de prueba, la tapa del amortiguador y la base para la prueba. Nota: Si falta el paquete secante o la almohadilla absorbente (en la parte superior del muestreador) o si falta el filtro para muestras (en la parte inferior del muestreador), NO USE EL DISPOSITIVO. Deseche el dispositivo y use uno nuevo. ESCRIBA EL NÚM. DE ID DEL PACIENTE EN LA BASE. SEPARE LA TAPA DEL AMORTIGUADOR DEL DISPOSITIVO DE PRUEBA. COLOQUE LA TAPA DEL AMORTIGUADOR EN LA BASE PARA LA PRUEBA. SURECHECK Tapa del amortiguador Base para la prueba Sobre una superficie firme, deje caer la tapa del amortiguador en la muestra de prueba Página 4 de 16
5 5 APLICACIÓN DE MUESTRA PROCEDIMIENTOS EXENTOS Para sangre completa por punción dactilar, toque la gota de sangre con la punta del muestreador hasta que la punta esté llena. O De manera alternativa, levante una gota de sangre completa del interior de la tapa del tubo de sangre. O 5 APLICACIÓN DE MUESTRA PROCEDIMIENTO MODERADAMENTE COMPLEJO Para sangre completa por punción venosa, suero o plasma, invierta el muestreador y vierta 2.5 μl de muestra con pipeta dentro de la punta del muestreador. 6 COMIENCE LA PRUEBA. Con la tapa del amortiguador en la base, presione firmemente la punta del dispositivo a través de la cubierta de aluminio. Empuje con fuerza hasta que el dispositivo esté completamente asentado en la tapa del amortiguador. Se escucharán 3 chasquidos cuando esté correctamente asentado. Chasquido 1: al traspasar el aluminio Chasquido 2: al ingresar en la tapa Chasquido 3: al quedar completamente asentado PRESIONE CON FIRMEZA 7 CONFIRME QUE EL DISPOSITIVO ESTÉ COMPLETAMENTE ASENTADO. a. La línea azul que se encuentra directamente por encima de las flechas se debe alinear con la línea transparente en la base. b. Observará que la solución de amortiguador rosa o morada comienza a subir. SI NO OBSERVA QUE LA SOLUCIÓN ROSA/MORADA SUBE A LOS 3 MINUTOS, EMPUJE NUEVAMENTE. (luego inicie el cronómetro) INCORRECTO Confirme la solución rosa/ morada aquí CORRECTO Línea dentro de la ventana transparente Página 5 de 16
6 8 COMIENCE A CRONOMETRAR - ESPERE QUE TRANSCURRAN 15 MINUTOS. NOTA: El tubo con muestreador/amortiguador se debe mantener de forma vertical en la base para la prueba. 15 minutos LEA LOS RESULTADOS DE LA PRUEBA. Lea la prueba una vez transcurridos entre 15 y 20 minutos. NOTA: Los resultados de prueba reactivos (consulte la sección Interpretación de los resultados de la prueba) se pueden observar y leer antes de los 15 minutos. Para verificar un resultado de prueba no reactivo, espere que transcurran los 15 minutos completos después de comenzar la prueba. Área de control Área de prueba No lea los resultados después de 20 minutos. CONTROL DE CALIDAD Característica de control integrada La línea de control sirve como control interno integrado y brinda una confirmación de la adición de la muestra y un desempeño de prueba adecuado. Una línea de color rosa/morado aparecerá en el área de CONTROL si la prueba se realizó correctamente y el dispositivo funciona adecuadamente (consulte la sección: Interpretación de los resultados de la prueba). Control de calidad externo Las buenas prácticas de laboratorio (Good Laboratory Practices, GLP) necesitan un material de control externo de prueba junto con las muestras de prueba a fin de garantizar un desempeño adecuado del kit de prueba. Los controles reactivos/no reactivos de Chembio (n. de catálogo ) están disponibles por separado con el análisis del VIH 1/2 SURE CHECK de Chembio. Los controles del VIH se usan para verificar la capacidad del operador de realizar la prueba adecuadamente y de interpretar los resultados. Cada control reactivo producirá un resultado de la prueba REACTIVO y fue fabricado para producir una línea tenue en el área de PRUEBA. El control no reactivo producirá un resultado de prueba NO REACTIVO. Ejecute los controles según el PROCEDIMIENTO DE PRUEBA y siga las instrucciones como se describen en las secciones INTERPRETACIÓN DE LOS RESULTADOS DE LA PRUEBA de este prospecto del producto. Es responsabilidad de cada centro usar el análisis del VIH 1/2 SURE CHECK para establecer un programa de control de calidad adecuado para garantizar el desempeño del dispositivo según ubicaciones específicas y las condiciones de uso. Ejecute los controles del kit en las siguientes circunstancias: Cada operador nuevo antes de llevar a cabo pruebas en las muestras de pacientes Cuando se abra un nuevo lote de kits de pruebas Cada vez que se reciba un nuevo envío de kits de pruebas Si la temperatura del área de almacenamiento de la prueba es diferente de 8 a 30 C (46 a 86 F) Si la temperatura del área de la prueba es diferente de 18 a 30 C (64 a 86 F) En intervalos periódicos como lo indica el centro del usuario Si los reactivos de control del VIH no producen los resultados esperados, comuníquese con el Servicio de Atención al Cliente de Chembio Diagnostic Systems, ya sea al o gratuitamente al INTERPRETACIÓN DE LOS RESULTADOS DE LA PRUEBA PARA ENTORNOS MODERADOS DE CLIA Y EXENTOS DE CLIA Cuando el análisis del VIH 1/2 SURE CHECK de Chembio se realiza correctamente, las líneas de color rosa/ morado adecuadas se harán visibles. Estas son: 1. la LÍNEA DE CONTROL: que aparece más cerca de la parte superior de la tira reactiva, indica que la muestra se aplicó de forma adecuada, y que hubo hidratación y migración correctas de los reactivos. La línea de control se hará visible dentro de los 15 minutos siguientes al inicio de la prueba independientemente del estado del anticuerpo de VIH de la muestra. 2. la LÍNEA DE LA PRUEBA: que aparece más próxima a la parte inferior de la tira reactiva (debajo de la línea de control) indica la presencia de anticuerpos específicos del VIH. La línea de la prueba solo se hará visible dentro de los 15 minutos siguientes al inicio de una prueba válida cuando los anticuerpos específicos del VIH estén presentes a niveles detectables en la muestra. Página 6 de 16
7 Área de control Área de prueba NO REACTIVO 1 línea REACTIVO 2 líneas INVÁLIDO No está la línea de control o está fuera del área INVÁLIDO Línea de prueba fuera del área NO REACTIVO (diagrama 1): Una línea de color rosa/morado en el área de CONTROL, sin una línea en el área de PRUEBA, indica un resultado de prueba NO REACTIVO. Un resultado de prueba NO REACTIVO significa que no se detectaron anticuerpos contra el VIH-1 y VIH-2 en la muestra. El resultado de la prueba se interpreta como NEGATIVO para los anticuerpos contra el VIH-1 y VIH-2. Sin embargo, esto no excluye una posible infección por el VIH. 7, 14 Siga las pautas de CDC para informarle al sujeto de la prueba el resultado de la prueba y su interpretación. REACTIVO (diagrama 2): Dos líneas de color rosa/morado, una en el área de PRUEBA y otra en el área de CONTROL, indican un resultado de prueba REACTIVO. La línea en el área de PRUEBA puede lucir diferente de la línea en el área de CONTROL. Las intensidades de las líneas de prueba y control pueden variar. El resultado de la prueba con líneas visibles en las áreas de PRUEBA y CONTROL, sin importar la intensidad, se considera REACTIVO. Un resultado de prueba REACTIVO significa que se detectaron anticuerpos contra el VIH-1 o VIH-2 en la muestra. El resultado de la prueba se interpreta como POSITIVO de manera preliminar para los anticuerpos contra el VIH-1 o VIH-2. Siga las pautas de CDC para informarle al sujeto de la prueba el resultado de la prueba y su 7, 14 interpretación. INVÁLIDA (diagrama 3): Siempre debe aparecer una línea de color rosa/morado en el área de CONTROL, ya sea que aparezca o no una línea en el área de PRUEBA. Si no se distingue una línea de color rosa/morado visible en el área de CONTROL (consulte los diagramas 1 y 2), la prueba es INVÁLIDA. Toda línea que aparezca fuera del área de prueba o de control (consulte el diagrama 3) es una prueba INVÁLIDA. No se puede interpretar una prueba INVÁLIDA. Se recomienda que la prueba INVÁLIDA se repita con un dispositivo nuevo. INVÁLIDA (diagrama 4): Si aparece una línea rosa o morada dentro del área de CONTROL, con la línea de la prueba fuera del área de prueba, entonces la prueba es INVÁLIDA. Se recomienda que la prueba INVÁLIDA se repita con un dispositivo nuevo. Limitaciones del procedimiento 1. la prueba VIH 1/2 SURE CHECK de Chembio se debe usar de acuerdo con las instrucciones que aparecen en este prospecto del producto para obtener resultados exactos. 2. el análisis del VIH 1/2 SURE CHECK de Chembio se debe usar con sangre completa venosa o capilar (punción dactilar), suero o plasma únicamente. El uso de otros tipos de muestras o prueba de muestras de sangre completa por punción venosa recolectadas con un tubo que contenga un anticoagulante que no sea el citrato, la heparina o EDTA puede no brindar resultados exactos. Para las muestras de suero, recopile sangre sin anticoagulante. 3. la lectura de resultados de prueba no reactivos antes de los 15 minutos o todo resultado de prueba posterior a los 20 minutos puede brindar resultados erróneos. 4. No abra la bolsa de aluminio sellada hasta justo antes de usarla. 5. no use el contenido del kit después de la fecha de vencimiento etiquetada. 6. Para la recolección de la muestra de sangre completa por punción dactilar, asegúrese de que el dedo esté completamente seco antes de realizar la punción dactilar. 7. lea los resultados en un área bien iluminada. 8. el resultado de prueba reactivo con la prueba VIH 1/2 SURE CHECK de Chembio sugiere la presencia de anticuerpos contra el VIH-1 o VIH-2 en la muestra. El análisis del VIH 1/2 SURE CHECK de Chembio se usa como una ayuda para el diagnóstico de la infección por el VIH-12. El SIDA o las afecciones relacionadas con el SIDA son síndromes clínicos y sus diagnósticos solo se pueden establecer clínicamente. 9. Para un resultado de prueba reactivo, la intensidad de la línea de la prueba no necesariamente se correlaciona con el valor del anticuerpo en la muestra. 10. una persona que tiene anticuerpos contra el VIH-1 o VIH-2 se supone que está infectada por el virus, excepto una persona que haya participado en un estudio de vacuna contra el VIH que pueda presentar anticuerpos contra la vacuna y puede o no estar infectada por el VIH. 11. Un resultado de prueba no reactivo no excluye la posibilidad de exposición al VIH o infección por el VIH. Puede llevar varios meses que una respuesta de anticuerpo a una exposición reciente logre niveles detectables. 12. este análisis no fue evaluado para una selección de recién nacidos, muestras de sangre del cordón umbilical o personas menores de 13 años de edad. Página 7 de 16
8 CARACTERÍSTICAS DE DESEMPEÑO El análisis del VIH 1/2 SURE CHECK de Chembio se evaluó en estudios clínicos prospectivos en cuatro centros geográficamente distintos. Las muestras se evaluaron de tres grupos de personas: quienes saben que están infectados por el VIH-1, quienes se encuentran con un alto riesgo de contraer la infección por el VIH-1 y quienes se encuentran con un bajo riesgo de contraer la infección por el VIH-1. El análisis del VIH 1/2 SURE CHECK de Chembio se evaluó en paralelo en sangre completa por punción dactilar, sangre completa por punción venosa, matrices de muestras de suero y plasma. No se obtuvo un resultado discorde de todas las matrices de muestras. Las muestras de suero o plasma de los sujetos del estudio también se evaluaron con un enzimoinmunoanálisis (EIA) autorizado por la FDA. Las muestras con resultados discordes se evaluaron aún más con el análisis de Western Blot autorizado por la FDA o NAT aprobado por la FDA. Sensibilidad La sensibilidad del análisis del VIH 1/2 SURE CHECK de Chembio para detectar la infección por el VIH-1 se evaluó con 614 muestras de personas que sabían que estaban infectadas por el VIH-1 y de 776 personas que se encontraban con un alto riesgo de contraer la infección por el VIH-1 (Tabla 1). Se identificaron 648 personas con resultado positivo de la infección por el VIH-1 con un análisis de confirmación autorizado o análisis de NAT aprobado por la FDA. De estos, 646 muestras se evaluaron reactivas en el análisis del VIH 1/2 SURE CHECK de Chembio. La sensibilidad calculada del análisis del VIH 1/2 SURE CHECK de Chembio en estos estudios fue del 99.7 % ( = 99.7 % con un intervalo de confianza [IC] del 95 % = 98.9 % %). Tabla 1 Detección del anticuerpo contra el VIH-1 en muestras de personas que sabían que estaban infectadas por el VIH-1 Población del estudio Positivo conocido Muestras Análisis del VIH 1/2 SURE CHECK reactivo EIA autorizado por la FDA Repetidamente reactivo WB autorizado reactivo Verdadero positivo Alto riesgo 776 TOTAL Según los resultados de los análisis NAT y WB autorizados (cuando son positivos y EIA es repetidamente reactivo). 2. Dos muestras fueron indeterminadas por Western Blot (una fue inicialmente reactiva solo en el EIA y no reactiva en el VIH 1/2 SURE CHECK ). 3. Una muestra fue repetidamente reactiva en el EIA y reactiva en el VIH 1/2 SURE CHECK, indeterminada en WB y positiva en NAT. La sensibilidad del análisis del VIH 1/2 SURE CHECK de Chembio para detectar el anticuerpo contra el VIH-2 se determinó evaluando simultáneamente 202 muestras de suero o plasma que fueron positivas para los anticuerpos contra el VIH-2 únicamente. Estas muestras se obtuvieron de las fuentes del depósito. También se evaluó un total de 488 muestras de un área endémica para la infección por el VIH-2 (Tabla 2). Todas las muestras reactivas con el análisis del VIH 1/2 SURE CHECK de Chembio en estos estudios también fueron reactivas mediante un EIA de VIH-12 autorizado. La sensibilidad del análisis del VIH 1/2 SURE CHECK para la detección de anticuerpos contra el VIH-2 en estos estudios se calculó que es del 100 % (203/203 = 100 % con un IC del 95 % = 98.2 % %). Tabla 2 Detección del anticuerpo contra el VIH-2 en muestras reactivas del VIH-2 conocidas y muestras endémicas Población del estudio Muestras Análisis del VIH 1/2 SURE CHECK reactivo VIH-2 verdadero positivo únicamente 1 VIH-2 positivo conocido Muestras endémicas TOTAL Confirmación según los resultados con el uso en investigación de Western Blot del VIH de estas 27 muestras reactivas del EIA del VIH-1 y EIA del VIH-2, 23 fueron reactivas en el WB del VIH-1 únicamente, tres fueron reactivas en el WB del VIH-1 y VIH-2 y una fue indeterminada en el WB del VIH-1 y reactiva en el WB del VIH-2. REACTIVIDAD CON MUESTRAS DE VIH-1 DE VARIAS REGIONES GEOGRÁFICAS DE TODO EL MUNDO Para evaluar la sensibilidad del análisis del VIH 1/2 SURE CHECK para las muestras del VIH-1 de varias regiones geográficas de todo el mundo, se obtuvieron 750 muestras positivas del anticuerpo contra el VIH confirmadas. De las 715 muestras evaluadas de África, Asia, América Latina, Europa y Bélgica, 712 fueron reactivas con el análisis del VIH 1/2 SURE CHECK de Chembio. Se evaluaron las 35 muestras positivas confirmadas restantes de los dos paneles mundiales, que consistieron en dos muestras plasmáticas que ocurrieron naturalmente de diversas ubicaciones geográficas (España, Ghana, Costa de Marfil, Mozambique, Uganda, Zimbabue, China, Tailandia, India, Estados Unidos y Argentina con subtipos VIH-1: A, B, C, D, E, F, G, O, BD y VIH-2). Los 35 resultados fueron reactivos con un análisis del VIH 1/2 SURE CHECK de Chembio. REACTIVIDAD CON PANELES DE SEROCONVERSIÓN El análisis del VIH 1/2 SURE CHECK de Chembio se evaluó en 15 paneles de seroconversión diferentes. Cada panel consistió en recolecciones secuenciales de una única persona que era seroconvertida. Las muestras se confirmaron con Western Blot (WB) y dos pruebas de EIA autorizadas. Como se muestra en la Tabla 3, la prueba VIH 1/2 SURE CHECK de Chembio funcionó de manera similar a los análisis actualmente autorizados para la detección de la seroconversión. La tabla presenta los días transcurridos desde la fecha del sangrado inicial hasta la primera muestra positiva. Página 8 de 16
9 Tabla 3 Comparación del análisis del VIH 1/2 SURE CHECK de Chembio con dos análisis de EIA autorizados y Western Blot en la detección de la seroconversión. (Donde NR = no reactivo, RR = repetidamente reactivo, IND = indeterminado, ND = no disponible) Panel Día relativo de sangrado Análisis SURE CHECK de Chembio EIA 1 EIA 2 WB PRB-927 (AB) 0 NR NR NR NR 28 NR RR NR NR 33 NR RR NR NR 35 R RR NR NR 40 R RR RR R PRB-928 (AC) 0 NR NR NR NR 111 NR RR RR NR 120 R RR RR R 125 R RR RR R 130 R RR RR R PRB-930 (AE) 0 NR NR NR NR 3 NR NR NR NR 7 NR RR NR NR 10 NR RR RR IND PRB-931 (AF) 0 NR NR NR NR 2 NR NR NR NR 7 NR NR NR NR 9 NR NR NR NR 15 NR NR NR NR 28 R RR NR NR 33 R RR RR IND 35 R RR RR R 42 R RR RR R PRB-934 (AI) 0 NR NR NR NR 7 R RR NR IND 11 R RR RR IND PRB-938 (AM) 0 NR NR NR NR 3 NR NR NR NR 9 NR NR NR IND PRB-944 (AT) 0 NR NR NR NR 2 NR NR NR NR 7 NR NR NR NR 9 NR NR NR NR 14 R RR NR IND 16 R RR NR IND PRB-959 (BI) 0 NR NR NR NR 7 NR NR NR NR 9 NR RR NR NR 14 R RR RR R 19 R RR RR R 21 R RR RR R 26 R RR RR R Página 9 de 16
10 Panel Día relativo de sangrado Análisis SURE CHECK de Chembio EIA 1 EIA 2 WB PRB-904 (D) 0 NR NR NR NR 21 NR NR NR NR 49 NR NR NR NR 92 R RR RR R 99 R RR RR R PRB-910 (J) 0 NR NR NR NR 14 R NR NR NR 26 R RR RR R 28 R RR RR R 32 R RR RR R 35 R RR RR R 40 R RR RR R PRB-914 (N) 0 R RR NR IND 4 R RR RR IND 7 R RR RR IND 25 R RR RR R 31 R RR RR R PRB-916 (P) 0 NR NR NR NR 4 NR NR NR NR 9 NR NR NR NR 15 NR NR NR NR 30 R RR RR R 35 R RR RR R PRB-917 (Q) 0 NR NR NR NR 53 NR NR NR NR 57 NR NR NR NR 60 ND* RR NR NR 65 R RR NR IND 67 R RR NR IND 72 ND* RR RR R PRB-919 (S) 0 NR NR NR NR 9 R RR NR R 11 R RR RR R PRB-922 (V) 0 NR RR NR NR *ND: NO DISPONIBLE 4 NR RR NR NR 7 R RR NR NR 11 R RR NR R REACTIVIDAD CON PANELES DE VALORES BAJOS DEL VIH-1 Se usó un total de 30 muestras de dos paneles de valores bajos caracterizados para evaluar la capacidad del análisis del VIH 1/2 SURE CHECK de Chembio para detectar anticuerpos contra el VIH-1. Los resultados de la prueba se presentan en la Tabla 4 y demuestran que el análisis del VIH 1/2 SURE CHECK de Chembio detectó la presencia del anticuerpo de manera similar a uno o ambos de los EIA autorizados. Página 10 de 16
11 Tabla 4 Comparación del análisis del VIH 1/2 SURE CHECK de Chembio con dos análisis del EIA autorizados y Western Blot con paneles de valores bajos. (Donde NR = no reactivo, RR = repetidamente reactivo) Panel Análisis SURE EIA 1 EIA 2 WB CHECK de Chembio PRB107-1 NR RR NR NR PRB107-2 NR RR RR IND PRB107-3 NR RR NR NR PRB107-4 NR RR RR NR PRB107-5 NR NR NR NR PRB107-6 R RR RR NR PRB107-7 NR RR NR NR PRB107-8 NR RR RR NR PRB107-9 NR RR NR NR PRB R RR RR NR PRB R RR RR R PRB NR RR NR NR PRB NR RR NR IND PRB R RR RR R PRB R RR RR IND PRB108-1 R RR RR R PRB108-2 NR NR NR NR PRB108-3 NR RR RR IND PRB108-4 R RR RR R PRB108-5 R RR RR R PRB108-6 R RR RR IND PRB108-7 R RR RR R PRB108-8 R RR RR R PRB108-9 R RR RR R PRB NR RR NR IND PRB R RR RR R PRB NR RR NR NR PRB NR RR NR IND PRB NR RR NR NR PRB R RR RR IND REACTIVIDAD CON PANELES DE VALORES MIXTOS DEL VIH-1 La sensibilidad del análisis del VIH 1/2 SURE CHECK de Chembio se evaluó mediante la prueba de tres paneles bien caracterizados compuestos de muestras que oscilaron desde no reactivos hasta reactivos fuertes para el anticuerpo contra el VIH-1. Los resultados se presentan en la Tabla 5 e indican que el análisis del VIH 1/2 SURE CHECK de Chembio pudo detectar anticuerpos contra el VIH-1 de manera similar al EIA y WB autorizados. Tabla 5 Comparación del análisis del VIH 1/2 SURE CHECK de Chembio con dos análisis del EIA autorizados y Western Blot con paneles de valores bajos. (Donde NR = no reactivo, RR = repetidamente reactivo) Panel Análisis SURE EIA 1 EIA 2 WB CHECK de Chembio PRB202-1 NR RR RR IND PRB202-2 R RR RR R Página 11 de 16
12 Panel Análisis SURE EIA 1 EIA 2 WB CHECK de Chembio PRB202-3 R RR RR R PRB202-4 R RR RR R PRB202-5 R RR RR R PRB202-6 R RR RR R PRB202-7 R NR RR R PRB202-8 R RR RR R PRB202-9 NR NR NR NR PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB NR NR NR NR PRB R RR RR R PRB NR RR NR IND PRB R RR RR R PRB R RR RR R PRB203-1 R RR RR R PRB203-2 R RR RR R PRB203-3 NR NR NR NR PRB203-4 NR RR NR IND PRB203-5 R RR RR R PRB203-6 R RR RR R PRB203-7 R RR RR R PRB203-8 R RR RR R PRB203-9 R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB NR RR NR NR PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB NR NR NR NR PRB R RR RR R PRB R RR RR R PRB R RR RR R Página 12 de 16
13 Panel Análisis SURE EIA 1 EIA 2 WB CHECK de Chembio PRB R RR RR R PRB R RR RR R PRB204-1 NR RR NR NR PRB204-2 R RR RR R PRB204-3 NR NR NR NR PRB204-4 R RR RR R PRB204-5 R RR RR R PRB204-6 R RR RR R PRB204-7 R RR RR R PRB204-8 R RR RR R PRB204-9 NR RR NR NR PRB R RR RR IND PRB R RR RR R PRB R RR RR R PRB NR RR RR IND PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR IND PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB R RR RR R PRB NR NR NR NR PRB NR RR NR IND PRB NR RR NR IND ESPECIFICIDAD La especificidad del análisis del VIH 1/2 SURE CHECK de Chembio se evaluó mediante muestras de pruebas de poblaciones con bajo riesgo y alto riesgo de contraer infección por el VIH-1 de tres centros de estudios clínicos dentro de EE. UU. Los resultados se resumen en la Tabla 6. Tabla 6 Desempeño del análisis del VIH 1/2 SURE CHECK de Chembio en las muestras de las personas que supuestamente son negativas para infección por el VIH-1 Población del estudio Bajo riesgo Alto riesgo Muestras Análisis del VIH 1/2 SURE CHECK no reactivo EIA autorizadas no reactivo TOTAL Confirmación realizada por Western Blot, prueba de inmunofluorescencia (Immunofluorescence Assay, IFA) o NAT del VIH-1 autorizados. Una muestra fue repetidamente reactiva según EIA, indeterminada según WB y positiva según NAT. Una muestra fue repetidamente reactiva según EIA e indeterminada según WB. Estas dos muestras no se incluyeron en los cálculos de especificidad. 2. Cuatro muestras fueron repetidamente reactivas en EIA y no reactivas en el análisis del VIH 1/2 SURE CHECK de Chembio y Western Blot. 3. Cinco muestras fueron repetidamente reactivas en EIA y no reactivas en el análisis del VIH 1/2 SURE CHECK de Chembio y Western Blot. Según estos estudios, la especificidad de VIH 1/2 SURE CHECK de Chembio en estos estudios se calculó que es de un 99.9 % ( = 99.9 % con un IC del 95 % 99.6 % %) Verdadero negativo Página 13 de 16
14 EFECTO DE SUSTANCIAS QUE INTERFIEREN POTENCIALMENTE Y AFECCIONES MÉDICAS NO RELACIONADAS Para evaluar la influencia de afecciones médicas no relacionadas o sustancias que interfieren en la especificidad y sensibilidad del análisis del VIH 1/2 SURE CHECK de Chembio, se evaluaron 208 muestras que representan afecciones médicas no relacionadas y 110 muestras que representan sustancias de potencial interferencia (Tabla 7). Las muestras fueron enriquecidas con una solución salina (no reactiva) o con una muestra de suero reactiva del VIH-1 a un nivel bajo de reactividad. Todas las muestras enriquecidas de VIH-1 dieron resultados reactivos mientras que todas las muestras no enriquecidas, con la excepción de una muestra con nivel elevado de albúmina y 14 muestras de sífilis, dieron resultados no reactivos. La única muestra con nivel elevado de albúmina y las 14 muestras de sífilis no enriquecidas con resultados reactivos se confirmaron posteriormente que estaban infectadas por el VIH-1 con un análisis de Western Blot autorizado. Se evaluaron diez muestras adicionales de VIH-1 reconocidas como no reactivas y las muestras reactivas de sífilis dieron resultados esperados. Tabla 7 Reactividad del análisis del VIH 1/2 SURE CHECK de Chembio contra las muestras de afecciones médicas no relacionadas o que contienen sustancias de potencial interferencia. ANÁLISIS DEL VIH 1/2 SURE CHECK DE CHEMBIO Descripción Solución salina (no reactiva) VIH-12 (reactivo débil) Cirrosis 20/20 20/20 CITOMEGALOVIRUS IgM 20/20 20/20 Vacuna contra la gripe reciente 1 11/11 11/11 VHB 21/21 21/21 VHC 19/19 19/19 VLTH-I 11/11 11/11 VLTH-II 10/10 10/10 Multípara 9/9 9/9 Mieloma 10/10 10/10 Factor reumatoide 10/10 10/10 Sífilis 2 15/29 29/29 Tuberculosis 38/38 38/38 Niveles elevados de albúmina 3 9/10 10/10 Niveles elevados de bilirrubina 10/10 10/10 Citrato 10/10 10/10 ADN 10/10 10/10 EDTA 10/10 10/10 Hemolizados 10/10 10/10 Heparina 10/10 10/10 Ictérico 10/10 10/10 Lipémico 10/10 10/10 Niveles elevados de proteínas 10/10 10/10 Niveles elevados de triglicéridos 10/10 10/10 1 Recolectadas en un período de 6 meses de la vacunación 2 Catorce muestras se confirmaron reactivas con un análisis de WB autorizado. 3 Se confirmó que una muestra contenía anticuerpos contra el VIH con un análisis de WB autorizado. Estudios de reproducibilidad La reproducibilidad se evaluó en tres centros independientes con tres lotes del análisis del VIH 1/2 SURE CHECK de Chembio. Se ejecutó un panel de cinco muestras enmascaradas que representan no reactivo, VIH-1 reactivo bajo, VIH-2 reactivo bajo, VIH-1 reactivo alto y VIH-2 reactivo alto en tres días separados por tres técnicos separados en cada centro. La prueba se realizó de acuerdo con el prospecto del producto de la prueba VIH 1/2 SURE CHECK de Chembio. Los resultados se leyeron en 15 minutos. Los resultados se leyeron de manera semicuantitativa con una escala de evaluación de tiras común. Se obtuvo un total de 405 puntos de datos. Hubo una reproducibilidad del 100 % (405405) en todos los parámetros. Página 14 de 16
15 RESULTADOS DEL ESTUDIO DEL USUARIO NO CAPACITADO Se llevó a cabo un estudio de usuario no capacitado en el cual los participantes recibieron solo las instrucciones escritas de la prueba y se les pidió que realizaran la prueba en un panel enmascarado de seis muestras de sangre completa preparadas en tres niveles diferentes (reactividad del análisis del VIH 1/2 SURE CHECK de Chembio negativa, positiva baja y positiva fuerte). Los participantes del estudio no recibieron instrucciones ni capacitación orales ni de otro tipo. El protocolo del estudio estipuló que se excluyera la participación del personal del laboratorio médico capacitado profesionalmente o las personas con experiencia previa en el uso del análisis del VIH 1/2 SURE CHECK de Chembio. Un total de 111 participantes se inscribieron de un total de cuatro centros, lo que representó una demografía heterogénea (educativa, edad, sexo, origen étnico, etc.). Para ayudar a evaluar la facilidad de uso y la claridad de las instrucciones de prueba y la interpretación de los resultados, se le pidió a cada participante que completara un cuestionario y ofreciera comentarios acerca de su experiencia con la prueba. La tasa general de los resultados correctos fue de un 99.1 % (636642). Los resultados del estudio por tipo de muestra se resumen a continuación en la Tabla 8. La tasa general de resultados no válidos de los cuatro centros fue del 3.5 %. Tabla 8 Tasa de usuarios no capacitados de resultados correctos No reactivo Reactivo bajo Reactivo alto General 99.1 % (213215) 98.1 % (206210) 100 % (217217) 99.1 % (636642) IC del 95 % = 96.7 % % IC del 95 % = 95.2 % % IC del 95 % = 98.3 % % IC del 95 % = 98.0 % % Referencias 1. centers for Disease Control and Prevention (CDC) Universal Precautions for prevention of transmission of human immunodeficiency virus, hepatitis B virus, and other bloodborne pathogens in health-care settings. (Precauciones universales de los Centros para el Control y la Prevención de Enfermedades [CDC] para la prevención del virus de la inmunodeficiencia humana, virus de la hepatitis B y otros patógenos sanguíneos en entornos de atención médica). MMWR 1988; 37(24): Essex, M. (1999) Human immunodeficiency viruses in the developing world. (Virus de la inmunodeficiencia humana en los países en vías de desarrollo). Adv Virus Res 53: Kanki, P.J., Hopper, J.R. and Essex, M. (1987) The origins of HIV-1 and HTLV-4HIV2. (Orígenes del VIH-1 y el VLTH-4VIH2). Ann N Y Acad Sci 511: nicoll, A., Gill, O.N. (1999) The global impact of HIV infection and disease. (Repercusiones mundiales de la infección y la enfermedad causadas por el VIH). Commun Dis Publ Health 2: valdiserri R.O., Holtgrave, D.R., West, G.R. (1999) Promoting early diagnosis and entry into care. (Promoción del diagnóstico y el inicio del tratamiento de manera anticipada). AIDS 13: unaids, Joint United Nations Programme on HIVAIDS, 2008 Report on the Global AIDS Epidemic (Programa conjunto de las Naciones Unidas sobre el VIHSIDA ONUSIDA, Informe sobre Epidemia Mundial de SIDA 2008) 2008: cdc, Revised Guidelines for HIV Counseling, Testing and Referral and Revised Recommendations for HIV Screening of Pregnant Women. (Centros para el Control y la Prevención de Enfermedades [CDC], Pautas revisadas para el asesoramiento, la prueba y la remisión sobre el VIH y recomendaciones revisadas para la detección del VIH en mujeres embarazadas) MMWR 2001; 50 (19); Essex, M., Kanki, P. J., Marlink, R., et al. (1990) Antigenic characterization of the human immunodeficiency viruses. (Caracterización antigénica del virus de la inmunodeficiencia humana). J Am Acad Dermatol 22: Essex, M., McLane, M.F., Lee, T.H. et al. (1983) Antibodies to cell membrane antigens associated with human T-cell leukemia virus in patients with AIDS. (Anticuerpos contra antígenos de la membrana celular asociados al virus de la leucemia de linfocitos T en pacientes con SIDA). Science 220: gallo, R.C., Saluahuddin, S.Z., Popovic, M., et al. (1984) Frequent detection and isolation of cytopathic retroviruses (HTLV-III) from patients with AIDS and at risk for AIDS. (Detección y aislamiento frecuentes de retrovirus citopáticos [VLTH-III] de pacientes con SIDA o riesgo de SIDA). Science 224: Kenealy, W., Reed, D., Cybulsky, R., et.al. (1987) Analysis of human serum antibodies to human immunodeficiency virus (HIV) using recombinant ENV and GAG antigens. (Análisis de anticuerpos séricos humanos contra el virus de la inmunodeficiencia humana [VIH] utilizando los antígenos recombinantes ENV y GAG). AIDS Res Human Retrovir 3: Kovacs, A., Xu, J., Rasheed, S., et al. (1995) Comparison of a rapid non-isotopic polymerase chain reaction assay with four commonly used methods for the early diagnosis of human Immunodeficiency Virus type 1 infection in neonates and children. (Comparación de un análisis rápido no isotópico de reacción en cadena de la polimerasa con cuatro métodos de uso común para el diagnóstico anticipado de la infección por el virus de la inmunodeficiencia humana tipo 1 en neonatos y niños). Pediatr Infect Dis J 14: CDC:Updated U.S. Public Health Service Guidelines for the Management of Occupational Exposures to HBV, HCV and HIV Recommendations for Postexposure Prophylaxis. (CDC: Actualización de las pautas del servicio de salud pública de Estados Unidos para el manejo de las exposiciones profesionales al VHB, VHC y VIH, y recomendaciones para la profilaxis posterior a la exposición). MMWR 2001; 50(RR-11): CDC: Approval of a New Rapid Test for HIV Antibody. (CDC: Aprobación de una prueba rápida nueva del anticuerpo contra el VIH). MMWR 2002; 51(46): Página 15 de 16
16 REF REF CHEMBIO DIAGNOSTIC SYSTEMS, INC HORSEBLOCK ROAD MEDFORD, NY EE. UU. Teléfono: Teléfono: (631) Fax: (631) Correo electrónico: Sitio web: INFORMACIÓN DE PEDIDOS Análisis DEL VIH 1/2 SURE CHECK de Chembio ACCESORIOS DISPONIBLES Controles reactivos o no reactivos de Chembio LEYENDA DE SÍMBOLOS CONSULTE EL MANUAL ANTES DE USAR PRECAUCIÓN, CONSULTE LA DOCUMENTACIÓN ADJUNTA. NO REUTILIZABLE PARA USAR DENTRO DE LOS LÍMITES DE TEMPERATURA DISPOSITIVO SANITARIO PARA DIAGNÓSTICO IN VITRO CÓDIGO DE LOTE NÚMERO DE CATÁLOGO DEL PRODUCTO IDENTIFICACIÓN DEL FABRICANTE FECHA DE FABRICACIÓN FECHA DE CADUCIDAD Fabricado por Chembio Diagnostic Systems, Inc., Medford, NY EE. UU. bajo la licencia de Alere con la patente de EE. UU. n. 6,485,982, que es propiedad o está autorizada por el grupo de empresas de Alere. Análisis del VIH 1/2 SURE CHECK Página 16 de 16
ANÁLISIS DEL VIH 1/2 STAT-PAK
 REF 60-9505-1 Kit de 20 pruebas ANÁLISIS DEL VIH 1/2 STAT-PAK Lea el prospecto del producto completamente antes de usarlo. Siga cuidadosamente las instrucciones cuando realice la prueba, ya que el no hacerlo
REF 60-9505-1 Kit de 20 pruebas ANÁLISIS DEL VIH 1/2 STAT-PAK Lea el prospecto del producto completamente antes de usarlo. Siga cuidadosamente las instrucciones cuando realice la prueba, ya que el no hacerlo
LIMITACIONES El HIV 1/2 STAT-PAK no está aprobado para el uso en la selección de donantes de tejidos, células, plasma o sangre.
 N.º catálogo HIV101 20 pruebas HIV 1/2 STAT-PAK PARA USO DIAGNÓSTICO IN VITRO PARA USO PROFESIONAL SOLAMENTE Kit de prueba de selección cualitativa para la detección de anticuerpos para el VIH-1/2 en la
N.º catálogo HIV101 20 pruebas HIV 1/2 STAT-PAK PARA USO DIAGNÓSTICO IN VITRO PARA USO PROFESIONAL SOLAMENTE Kit de prueba de selección cualitativa para la detección de anticuerpos para el VIH-1/2 en la
TIRAS REACTIVAS PARA VIH 1/2 STAT-PAK
 TIRAS REACTIVAS PARA VIH 1/2 STAT-PAK HIV303 30 pruebas por kit Kit de pruebas de cribado cualitativas para la detección de anticuerpos anti-vih 1/2 en suero, plasma o sangre completa humanos SOLO PARA
TIRAS REACTIVAS PARA VIH 1/2 STAT-PAK HIV303 30 pruebas por kit Kit de pruebas de cribado cualitativas para la detección de anticuerpos anti-vih 1/2 en suero, plasma o sangre completa humanos SOLO PARA
ALMACENAMIENTO: ALMACENAR DE +8 C a +30 C
 HIV 1 /2 STAT-PAK ASSAY Lea completamente este inserto del producto antes de su uso. Siga cuidadosamente las instrucciones cuando realice la prueba ya que el no hacerlo puede proporcionar Resultados de
HIV 1 /2 STAT-PAK ASSAY Lea completamente este inserto del producto antes de su uso. Siga cuidadosamente las instrucciones cuando realice la prueba ya que el no hacerlo puede proporcionar Resultados de
Fortel PROSTATE (PSA)
 Fortel PROSTATE (PSA) Test para Screening Simple, realizable y confidencial [Seleccione la fecha] Un test visual fácil, para detectar niveles anormales del Antígeno Prostático Específico (PSA), sobre rango
Fortel PROSTATE (PSA) Test para Screening Simple, realizable y confidencial [Seleccione la fecha] Un test visual fácil, para detectar niveles anormales del Antígeno Prostático Específico (PSA), sobre rango
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt
 Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
PROYECTO DE MARBETE CAJA SURE CHECK HIV 1/2 REF HIV 201 25 PRUEBAS
 PROYECTO DE MARBETE CAJA SURE CHECK HIV 1/2 REF HIV 201 25 PRUEBAS Prueba para la detección cualitativa de anticuerpos del Virus de lnmunodeficiencia Humana tipo 1 y 2 en suero, plasma o sangre total.
PROYECTO DE MARBETE CAJA SURE CHECK HIV 1/2 REF HIV 201 25 PRUEBAS Prueba para la detección cualitativa de anticuerpos del Virus de lnmunodeficiencia Humana tipo 1 y 2 en suero, plasma o sangre total.
PRINCIPIO DE LA PRUEBA: USO PREVISTO:
 ESPECIFICACIONES DEL KIT: Cat. No Cantidad Reactivo Almacenamiento ADRT0011 1 x 20 PRUEBAS 1 x 3 ml Diluente USO PREVISTO: HIV 2-30 C El HIV-1/2 Plus Combo Rapid Test es un inmunoensayo de flujo lateral
ESPECIFICACIONES DEL KIT: Cat. No Cantidad Reactivo Almacenamiento ADRT0011 1 x 20 PRUEBAS 1 x 3 ml Diluente USO PREVISTO: HIV 2-30 C El HIV-1/2 Plus Combo Rapid Test es un inmunoensayo de flujo lateral
Uni-Gold Recombigen HIV-1/2
 Uni-Gold Recombigen 1206506 ESPAÑOL Antes de usar el producto, lea el prospecto completo. Siga las instrucciones con cuidado. No hacerlo puede ocasionar que el resultado de la prueba sea incorrecto. Antes
Uni-Gold Recombigen 1206506 ESPAÑOL Antes de usar el producto, lea el prospecto completo. Siga las instrucciones con cuidado. No hacerlo puede ocasionar que el resultado de la prueba sea incorrecto. Antes
50 kits de recolección de muestras con torunda multitest Aptima (N.º de catálogo PRD-03546) Cada kit contiene:
 Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
ENSAYO DE HIV 1/2 STAT-PAK
 NÚM. DE PRODUCTO HIV102 20 exámenes ENSAYO DE HIV 1/2 Lea completamente este Inserto del Producto antes de usarlo. Siga las instrucciones con cuidado al realizar el examen pues de lo contrario puede obtener
NÚM. DE PRODUCTO HIV102 20 exámenes ENSAYO DE HIV 1/2 Lea completamente este Inserto del Producto antes de usarlo. Siga las instrucciones con cuidado al realizar el examen pues de lo contrario puede obtener
SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA
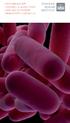 SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA Aplicación El análisis de sangre ImmuView Legionella de Statens Serum Institute se ha creado para el diagnóstico de una infección
SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA Aplicación El análisis de sangre ImmuView Legionella de Statens Serum Institute se ha creado para el diagnóstico de una infección
Reducción de la transmisión vertical del VIH en Colombia. Proyecto Madre-Hijo. Diagnóstico y seguimiento por laboratorio
 Reducción de la transmisión vertical del VIH en Colombia. Proyecto Madre-Hijo. Diagnóstico y seguimiento por laboratorio El VIRUS PRUEBAS PRESUNTIVAS ELISA: es la prueba convencional para la detección
Reducción de la transmisión vertical del VIH en Colombia. Proyecto Madre-Hijo. Diagnóstico y seguimiento por laboratorio El VIRUS PRUEBAS PRESUNTIVAS ELISA: es la prueba convencional para la detección
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS
 HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
Prueba rápida de detección de anticuerpos anti VIH-1/2 OraQuick ADVANCE Carta al cliente
 Prueba rápida de detección de anticuerpos anti VIH-1/2 OraQuick ADVANCE Carta al cliente Estimado cliente: Le agradecemos que haya decido usar la prueba rápida de detección de anticuerpos anti VIH-1/2
Prueba rápida de detección de anticuerpos anti VIH-1/2 OraQuick ADVANCE Carta al cliente Estimado cliente: Le agradecemos que haya decido usar la prueba rápida de detección de anticuerpos anti VIH-1/2
One Step Dengue IgG/IgM Antibody Test
 One Step Dengue IgG/IgM Antibody Test Instrucciones de uso Formato: Cassette Espécimen: Suero/Plasma y Sangre Entera Numero de Catalogo: A03-08- 322 * Por favor, lea atentamente las instrucciones antes
One Step Dengue IgG/IgM Antibody Test Instrucciones de uso Formato: Cassette Espécimen: Suero/Plasma y Sangre Entera Numero de Catalogo: A03-08- 322 * Por favor, lea atentamente las instrucciones antes
WITNESS RELAXIN (plasma, serum) RLX RLX u d 9 n n ersio V X RLX L R -W IO B S
 WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
NycoCard CRP Single Test
 NycoCard CRP Single Test ES DESCRIPCION DEL PRODUCTO Aplicaciones NycoCard CRP Single Test es un test de diagnóstico in vitro para medir de una forma rápida la proteína C reactiva (CRP) en la sangre humana.
NycoCard CRP Single Test ES DESCRIPCION DEL PRODUCTO Aplicaciones NycoCard CRP Single Test es un test de diagnóstico in vitro para medir de una forma rápida la proteína C reactiva (CRP) en la sangre humana.
GenPE: estudio Internacional de Genética en Preeclampsia
 GenPE: estudio Internacional de Genética en Preeclampsia INSTRUCTIVO Toma de muestra proyecto GenPE PAQUETE PARA CAPTACIÓN DE PACIENTE Y TOMA DE MUESTRA. Cuando llegue a su institución la caja del proyecto
GenPE: estudio Internacional de Genética en Preeclampsia INSTRUCTIVO Toma de muestra proyecto GenPE PAQUETE PARA CAPTACIÓN DE PACIENTE Y TOMA DE MUESTRA. Cuando llegue a su institución la caja del proyecto
ALMACENAMIENTO: Almacenar entre 2 y 30 C (36 a 86 F)
 20 Kits de Prueba 61-1000-0 INSERTO DEL PRODUCTO Ensayo DPP VIH-SÍFILIS PRECAUCIÓN-Dispositivo de Investigación. Limitado por Ley Federal (o Estados Unidos) para uso de investigación PARA USO DIAGNÓSITICO
20 Kits de Prueba 61-1000-0 INSERTO DEL PRODUCTO Ensayo DPP VIH-SÍFILIS PRECAUCIÓN-Dispositivo de Investigación. Limitado por Ley Federal (o Estados Unidos) para uso de investigación PARA USO DIAGNÓSITICO
Diagnóstico microbiológico de la infección por HIV
 Diagnóstico microbiológico de la infección por HIV Juan Carlos Rodríguez Díaz S. Microbiología Hospital General Universitario de Alicante E-mail: rodriguez_juadia@gva.es http://microbiología-alicante.umh.es
Diagnóstico microbiológico de la infección por HIV Juan Carlos Rodríguez Díaz S. Microbiología Hospital General Universitario de Alicante E-mail: rodriguez_juadia@gva.es http://microbiología-alicante.umh.es
Introducción Principio del test
 El equipo ImmunoComb II VIH 1 & 2 TriSpot Ag-Ab es una prueba Inmuno Ensayo Enzimático para la determinación cualitativa y diferencial de anticuerpos contra el virus de inmunodeficiencia humano tipo 1
El equipo ImmunoComb II VIH 1 & 2 TriSpot Ag-Ab es una prueba Inmuno Ensayo Enzimático para la determinación cualitativa y diferencial de anticuerpos contra el virus de inmunodeficiencia humano tipo 1
PRUEBAS DE DIAGNOSTICO. Hospital Roosevelt Laboratorio Clínica de Enfermedades Infecciosas Septiembre 2013
 PRUEBAS DE DIAGNOSTICO Hospital Roosevelt Laboratorio Clínica de Enfermedades Infecciosas Septiembre 2013 DIAGNÓSTICO DE LA INFECCIÓN POR EL VIH El diagnóstico definitivo de la infección por el VIH sólo
PRUEBAS DE DIAGNOSTICO Hospital Roosevelt Laboratorio Clínica de Enfermedades Infecciosas Septiembre 2013 DIAGNÓSTICO DE LA INFECCIÓN POR EL VIH El diagnóstico definitivo de la infección por el VIH sólo
ILUSTRE CONSEJO GENERAL DE COLEGIOS DE DENTISTAS DE ESPAÑA
 2010 ILUSTRE CONSEJO GENERAL DE COLEGIOS DE DENTISTAS DE ESPAÑA Qué es un accidente biológico (AB) Cuales son los riesgos de transmisión? Para el VHB (hepatitis B) Para el VHC (hepatitis C) Para el VIH
2010 ILUSTRE CONSEJO GENERAL DE COLEGIOS DE DENTISTAS DE ESPAÑA Qué es un accidente biológico (AB) Cuales son los riesgos de transmisión? Para el VHB (hepatitis B) Para el VHC (hepatitis C) Para el VIH
Contacto con Sangre y otros líquidos corporales.
 CAPÍTULO 8 Contacto con Sangre y otros líquidos corporales. Transfusiones de sangre La transfusión de sangre es una intervención que salva vidas y mejora la salud siempre que se realice correctamente.
CAPÍTULO 8 Contacto con Sangre y otros líquidos corporales. Transfusiones de sangre La transfusión de sangre es una intervención que salva vidas y mejora la salud siempre que se realice correctamente.
Muestra. Membrana Inmunoreactiva Material Absorbente. Figura 1: Tecnología en Plataforma de Flujo Rápido MedMira
 Prueba Rápida de Anticuerpos VIH Para Suero, Plasma y Sangre Completa Folleto Anexo INTENCION DE USO La Prueba Rápida del Anticuerpo VIH MiraCare es una prueba de inmunoensayo cualitativo de un solo uso
Prueba Rápida de Anticuerpos VIH Para Suero, Plasma y Sangre Completa Folleto Anexo INTENCION DE USO La Prueba Rápida del Anticuerpo VIH MiraCare es una prueba de inmunoensayo cualitativo de un solo uso
GUÍA DE ATENCIÓN PARA RECIÉN NACIDOS DE MADRES CON INFLUENZA Y MENORES DE UN AÑO
 GUÍA DE ATENCIÓN PARA RECIÉN NACIDOS DE MADRES CON INFLUENZA Y MENORES DE UN AÑO Las mujeres embarazadas son consideradas grupo de alto riesgo para presentar complicaciones graves y muerte por influenza,
GUÍA DE ATENCIÓN PARA RECIÉN NACIDOS DE MADRES CON INFLUENZA Y MENORES DE UN AÑO Las mujeres embarazadas son consideradas grupo de alto riesgo para presentar complicaciones graves y muerte por influenza,
PRUEBA DE VIH. Universidad de Panamá USAID Proyecto Capacity Centroamérica
 PRUEBA DE VIH Universidad de Panamá USAID Proyecto Capacity Centroamérica Es la prueba de detección que produce los resultados rápidamente, en aproximadamente 20 minutos y utiliza sangre de una vena o
PRUEBA DE VIH Universidad de Panamá USAID Proyecto Capacity Centroamérica Es la prueba de detección que produce los resultados rápidamente, en aproximadamente 20 minutos y utiliza sangre de una vena o
GEBRAX DIVISION DIAGNÓSTICA
 GEBRAX T h e r a p e u t i c s & D i a g n o s t i c s DIVISION DIAGNÓSTICA Se recomienda que el prospecto deba ser leído antes de comenzar el procedimiento de prueba. Aunque el ensayo está diseñado para
GEBRAX T h e r a p e u t i c s & D i a g n o s t i c s DIVISION DIAGNÓSTICA Se recomienda que el prospecto deba ser leído antes de comenzar el procedimiento de prueba. Aunque el ensayo está diseñado para
SensPERT TM TM Ehrlichia Test Kit
 SensPERT TM TM Ehrlichia Test Kit Distribuidor en España: Pº Pontones 7 tlf 914745799 Madrid 28005 Ehrlichia Test Kit Descripción : Detección específica de anticuerpos de E. canis en 10 minutos Principio
SensPERT TM TM Ehrlichia Test Kit Distribuidor en España: Pº Pontones 7 tlf 914745799 Madrid 28005 Ehrlichia Test Kit Descripción : Detección específica de anticuerpos de E. canis en 10 minutos Principio
5-MARCO DE REFERENCIA
 5-MARCO DE REFERENCIA Para hablar de pruebas diagnosticas es necesario el conocimiento de ciertos términos que a continuación se describen. Sensibilidad: Es la probabilidad de obtener una prueba positiva
5-MARCO DE REFERENCIA Para hablar de pruebas diagnosticas es necesario el conocimiento de ciertos términos que a continuación se describen. Sensibilidad: Es la probabilidad de obtener una prueba positiva
Algoritmos diagnósticos para VIH
 Algoritmos diagnósticos para VIH ALGORITMOS DIAGNÓSTICOS PARA VIH Los avances tecnológicos de los distintos ensayos para el tamizaje y diagnóstico de la infección por VIH, conjuntamente con la necesidad
Algoritmos diagnósticos para VIH ALGORITMOS DIAGNÓSTICOS PARA VIH Los avances tecnológicos de los distintos ensayos para el tamizaje y diagnóstico de la infección por VIH, conjuntamente con la necesidad
PROTOCOLO EN CASO DE ACCIDENTE OCUPACIONAL
 PROTOCOLO EN CASO DE ACCIDENTE OCUPACIONAL I. INTRODUCCIÓN Los trabajadores de la salud no están exentos de accidentes ocupacionales aún cuando se ciñan a la aplicación de las normas universales y específicas
PROTOCOLO EN CASO DE ACCIDENTE OCUPACIONAL I. INTRODUCCIÓN Los trabajadores de la salud no están exentos de accidentes ocupacionales aún cuando se ciñan a la aplicación de las normas universales y específicas
 Carta de Trámite 3 de junio de 2016 Estimado Proveedor: Re: Orden Administrativa 337 del Departamento de Salud de Puerto Rico Relacionada al Nuevo Algoritmo de Pruebas para el Diagnóstico de la Infección
Carta de Trámite 3 de junio de 2016 Estimado Proveedor: Re: Orden Administrativa 337 del Departamento de Salud de Puerto Rico Relacionada al Nuevo Algoritmo de Pruebas para el Diagnóstico de la Infección
Pruebas rápidas r. Estrategias preventivas. Propuesta de nuevas estrategias preventivas
 XV ENCUENTRO ESTATAL PARA ONG s Madrid, 1-3 de Octubre 2009 Diagnóstico tardío o. Pruebas rápidas r Dra Carmen Rodríguez Centro Sanitario Sandoval Madrid Estrategias preventivas La prevención de nuevas
XV ENCUENTRO ESTATAL PARA ONG s Madrid, 1-3 de Octubre 2009 Diagnóstico tardío o. Pruebas rápidas r Dra Carmen Rodríguez Centro Sanitario Sandoval Madrid Estrategias preventivas La prevención de nuevas
HIV TIPS Número 1 Octubre de 2009
 HIV TIPS Número 1 Octubre de 2009 Sabía usted que El VIH es un virus perteneciente a la familia Retroviridae, subfamilia Lentiviridae 4,5. Existen dos formas semejantes: VIH 1 y VIH 2, pero difieren en
HIV TIPS Número 1 Octubre de 2009 Sabía usted que El VIH es un virus perteneciente a la familia Retroviridae, subfamilia Lentiviridae 4,5. Existen dos formas semejantes: VIH 1 y VIH 2, pero difieren en
TEMA 14. Métodos inmunológicos para la identificación microbiana
 TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
EL KIT CONTIENE: EL KIT CONTIENE: Jeringa de diluyente precargada. Adaptador del vial en su envase. Vial con el fármaco en polvo. Vástago del émbolo
 ALPROLIX Factor IX de coagulación (recombinante), proteína de fusión a Fc INSTRUCCIONES DE USO Lea las Instrucciones de uso antes de comenzar a usar el ALPROLIX y cada vez que obtenga un suministro nuevo
ALPROLIX Factor IX de coagulación (recombinante), proteína de fusión a Fc INSTRUCCIONES DE USO Lea las Instrucciones de uso antes de comenzar a usar el ALPROLIX y cada vez que obtenga un suministro nuevo
Ficha técnica del producto. Agente Floculante Aquabase Plus P P Agente Floculante Base agua
 Ficha técnica del producto MASTER INTERNACIONAL Agente Floculante Aquabase Plus P872-1000 Producto Descripción P872-1000 Agente Floculante Base agua Descripción del producto P872-1000 se ha desarrollado
Ficha técnica del producto MASTER INTERNACIONAL Agente Floculante Aquabase Plus P872-1000 Producto Descripción P872-1000 Agente Floculante Base agua Descripción del producto P872-1000 se ha desarrollado
OBTENCIÓN, PREPARACIÓN Y ENVÍO DE MUESTRAS DE SANGRE
 1 de 7 MANUAL DE PROCEDIMIENTOS OBTENCIÓN, PREPARACIÓN Y ENVÍO DE MUESTRAS DE SANGRE CONTROLADA Nº DESTINATARIO FECHA ENTREGA ENTREGADO POR Nombre Firma NO CONTROLADA ENTRADA EN REVISIÓN REALIZADO FECHA
1 de 7 MANUAL DE PROCEDIMIENTOS OBTENCIÓN, PREPARACIÓN Y ENVÍO DE MUESTRAS DE SANGRE CONTROLADA Nº DESTINATARIO FECHA ENTREGA ENTREGADO POR Nombre Firma NO CONTROLADA ENTRADA EN REVISIÓN REALIZADO FECHA
Preguntas de Selectividad sobre inmunología.
 Preguntas de Selectividad sobre inmunología. 1. Existen virus que producen en los humanos enfermedades mortales por inmunodeficiencia. Sin embargo, la muerte del individuo no es provocada directamente
Preguntas de Selectividad sobre inmunología. 1. Existen virus que producen en los humanos enfermedades mortales por inmunodeficiencia. Sin embargo, la muerte del individuo no es provocada directamente
PROSPECTO. Para uso diagnóstico in vitro. Para uso en la preparación y aislamiento de linfocitos purificados directamente de sangre entera.
 Para uso en la preparación y aislamiento de linfocitos purificados directamente de sangre entera. PROSPECTO Para uso diagnóstico in vitro PI-TT.610-ES-V5 Información e instrucciones Uso previsto El reactivo
Para uso en la preparación y aislamiento de linfocitos purificados directamente de sangre entera. PROSPECTO Para uso diagnóstico in vitro PI-TT.610-ES-V5 Información e instrucciones Uso previsto El reactivo
HIV 1&2 BiSpot. Introducción. Principio de la Prueba. Figura 1. Principio de la Prueba
 S inmunoglobulina humana del punto superior (Control Interno). Los componentes no unidos son eliminados con un lavado en la fila B. En la fila C y D, el capturado en los dientes reacciona con los anticuerpos
S inmunoglobulina humana del punto superior (Control Interno). Los componentes no unidos son eliminados con un lavado en la fila B. En la fila C y D, el capturado en los dientes reacciona con los anticuerpos
NOCIONES DE EPIDEMIOLOGÍA Y DIAGNOSTICO DE HIV. Dra G Carballal Laboratorio de Virología Clínica CEMIC, 2009
 NOCIONES DE EPIDEMIOLOGÍA Y DIAGNOSTICO DE HIV Dra G Carballal Laboratorio de Virología Clínica CEMIC, 2009 La Pandemia de SIDA Personas que viven con el HIV/SIDA Total 40 millones Adultos 38 Niños 2 Nuevas
NOCIONES DE EPIDEMIOLOGÍA Y DIAGNOSTICO DE HIV Dra G Carballal Laboratorio de Virología Clínica CEMIC, 2009 La Pandemia de SIDA Personas que viven con el HIV/SIDA Total 40 millones Adultos 38 Niños 2 Nuevas
Código: IDX-016 Ver: 1 TOXO. Sistema para la detección de la presencia de ADN de Toxoplasma gondii. Reg. MSP 21205
 Sistema para la detección de la presencia de ADN de Toxoplasma gondii Reg. MSP 21205 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. info@atgen.com.uy www.atgen.com.uy
Sistema para la detección de la presencia de ADN de Toxoplasma gondii Reg. MSP 21205 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. info@atgen.com.uy www.atgen.com.uy
La Patología a Molecular y el Control de Calidad
 UNIDAD DIDÁCTICA 7: LOS PROCESOS EN ANATOMÍA PATOLÓGICA La Patología a Molecular y el Control de Calidad Asunción n Olmo Sevilla Master Diagnóstica S. L. Patología Molecular: Patología del futuro X Personal:
UNIDAD DIDÁCTICA 7: LOS PROCESOS EN ANATOMÍA PATOLÓGICA La Patología a Molecular y el Control de Calidad Asunción n Olmo Sevilla Master Diagnóstica S. L. Patología Molecular: Patología del futuro X Personal:
Contenido. Bioseguridad Chile Ltda., Septiembre 2014i www.bioseguridadchile.cl nfo@bioseguridadchile.cl 1
 Contenido Control de Infecciones, Recolección y Manejo de Muestras... 2 Recomendaciones para la evaluación de los riesgos para el personal... 2 Recomendaciones para la recogida de muestras por parte del
Contenido Control de Infecciones, Recolección y Manejo de Muestras... 2 Recomendaciones para la evaluación de los riesgos para el personal... 2 Recomendaciones para la recogida de muestras por parte del
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO
 SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO FACULTAD DE MEDICINA Y NUTRICIÓN Unidad Médica de Simulación Clínica "Dr. José Jorge Talamas Márquez"
 LICENCIATURA EN NUTRICIÓN Practica #10 TOMA DE MUESTRA DE GLUCOSA CAPILAR OBJETIVOS: Al concluir la práctica el alumno será capaz de: 1. Definir y conocer la técnica de toma de muestra de glucosa capilar
LICENCIATURA EN NUTRICIÓN Practica #10 TOMA DE MUESTRA DE GLUCOSA CAPILAR OBJETIVOS: Al concluir la práctica el alumno será capaz de: 1. Definir y conocer la técnica de toma de muestra de glucosa capilar
Toma de Muestras Microbiológicas
 Toma de Muestras Microbiológicas MICROBIOLOGÍA CLÍNICA DIAGNÓSTICO DE ENFERMEDADES INFECCIOSAS MUESTRA AISLAMIENTO IDENTIFICACIÓN SENSIBILIDAD A ANTIMICROBIANOS Detección de anticuerpos, antígenos y ácidos
Toma de Muestras Microbiológicas MICROBIOLOGÍA CLÍNICA DIAGNÓSTICO DE ENFERMEDADES INFECCIOSAS MUESTRA AISLAMIENTO IDENTIFICACIÓN SENSIBILIDAD A ANTIMICROBIANOS Detección de anticuerpos, antígenos y ácidos
6 INFECCIÓN POR EL VIRUS DE LA INMUNODEFICIENCIA HUMANA (VIH) Y SIDA. TRATAMIENTO Y PREVENCIÓN DE LAS INFECCIONES OPORTUNISTAS ASOCIADAS
 6 INFECCIÓN POR EL VIRUS DE LA INMUNODEFICIENCIA HUMANA (VIH) Y SIDA. TRATAMIENTO Y PREVENCIÓN DE LAS INFECCIONES OPORTUNISTAS ASOCIADAS Introducción.................... 663 Clasificación de la infección
6 INFECCIÓN POR EL VIRUS DE LA INMUNODEFICIENCIA HUMANA (VIH) Y SIDA. TRATAMIENTO Y PREVENCIÓN DE LAS INFECCIONES OPORTUNISTAS ASOCIADAS Introducción.................... 663 Clasificación de la infección
Presentación Del Entrenamiento De Seguridad
 Presentación Del Entrenamiento De Seguridad Patógeno De Bloodborne 29 CFR 1910.1030 Directorio Revisado De la Conformidad Los Patógeno del Osha Bloodborne(CPL2-2.44D) Podría usted contraer una enfermedad
Presentación Del Entrenamiento De Seguridad Patógeno De Bloodborne 29 CFR 1910.1030 Directorio Revisado De la Conformidad Los Patógeno del Osha Bloodborne(CPL2-2.44D) Podría usted contraer una enfermedad
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
GARANTIAS MINIMAS DE CALIDAD Y SEGURIDAD EXIGIBLES PARA LA UTILIZACION DE PLASMA RICO EN PLAQUETAS (PRP) EN LA COMUNIDAD AUTONOMA DE LA REGION DE
 GARANTIAS MINIMAS DE CALIDAD Y SEGURIDAD EXIGIBLES PARA LA UTILIZACION DE PLASMA RICO EN PLAQUETAS (PRP) EN LA COMUNIDAD AUTONOMA DE LA REGION DE MURCIA 1 GARANTIAS MINIMAS DE CALIDAD Y SEGURIDAD EXIGIBLES
GARANTIAS MINIMAS DE CALIDAD Y SEGURIDAD EXIGIBLES PARA LA UTILIZACION DE PLASMA RICO EN PLAQUETAS (PRP) EN LA COMUNIDAD AUTONOMA DE LA REGION DE MURCIA 1 GARANTIAS MINIMAS DE CALIDAD Y SEGURIDAD EXIGIBLES
PRUEBA RAPIDA EN EMBARAZADAS (n=62,214 2009-Junio 2010) NO REACTIVO n=218 REACTIVO INDETERMINADO. Tabla 9: Resultados Prueba rápida
 11-RESULTADOS 11.1-Interpretación y análisis de resultados Un total de de 62,214 mujeres embarazadas se realizaron la prueba rápida de VIH durante años 2009 hasta junio 2010 (Tabla 9). De ellas, 61,808
11-RESULTADOS 11.1-Interpretación y análisis de resultados Un total de de 62,214 mujeres embarazadas se realizaron la prueba rápida de VIH durante años 2009 hasta junio 2010 (Tabla 9). De ellas, 61,808
Riesgos laborales de los puestos de trabajo
 MANUAL INFORMATIVO Riesgos laborales de los puestos de trabajo TRABAJO SEGURO PARA LA PREVENCIÓN DE ACCIDENTES BIOLÓGICOS Salud Laboral Un objetivo compartido Presentación Como complemento al MANUAL INFORMATIVO
MANUAL INFORMATIVO Riesgos laborales de los puestos de trabajo TRABAJO SEGURO PARA LA PREVENCIÓN DE ACCIDENTES BIOLÓGICOS Salud Laboral Un objetivo compartido Presentación Como complemento al MANUAL INFORMATIVO
HIV 1 & 2 TriSpot Ag-Ab
 S HIV 1 & 2 TriSpot Ag-Ab Para comenzar la prueba, se agregan muestras de suero o plasma al diluyente en los pocillos de la fila A de la Bandeja de desarrollo. Luego el peine se inserta en los pocillos
S HIV 1 & 2 TriSpot Ag-Ab Para comenzar la prueba, se agregan muestras de suero o plasma al diluyente en los pocillos de la fila A de la Bandeja de desarrollo. Luego el peine se inserta en los pocillos
APLICACIONES DEL LABORATORIO DE BIOLOGIA MOLECULAR. Javier Sfalcin Líder de Biología Molecular CIBIC - Rosario - Argentina
 APLICACIONES DEL LABORATORIO DE BIOLOGIA MOLECULAR Javier Sfalcin Líder de Biología Molecular CIBIC - Rosario - Argentina BiologÍa Molecular: es una disciplina que se enfoca principalmente en el estudio
APLICACIONES DEL LABORATORIO DE BIOLOGIA MOLECULAR Javier Sfalcin Líder de Biología Molecular CIBIC - Rosario - Argentina BiologÍa Molecular: es una disciplina que se enfoca principalmente en el estudio
PRECAUCIONES ESTÁNDAR DEFINICIÓN:
 PRECAUCIONES ESTÁNDAR DEFINICIÓN: Son las precauciones que deben aplicarse a todos los pacientes independientemente de su diagnóstico, a fin de minimizar el riesgo de transmisión de cualquier tipo de microorganismo,
PRECAUCIONES ESTÁNDAR DEFINICIÓN: Son las precauciones que deben aplicarse a todos los pacientes independientemente de su diagnóstico, a fin de minimizar el riesgo de transmisión de cualquier tipo de microorganismo,
Instrucciones de uso. Módulo del filtro MBT Galaxy
 Instrucciones de uso Módulo del filtro MBT Galaxy Número de referencia de Bruker 1819125 Filtro de combinación que proporciona un entorno de humedad controlada para la preparación de muestras y el uso
Instrucciones de uso Módulo del filtro MBT Galaxy Número de referencia de Bruker 1819125 Filtro de combinación que proporciona un entorno de humedad controlada para la preparación de muestras y el uso
Instrucciones. Kit de Recoleccion. para proveedor de atención médica. (800) 786-7235 Cryo-Cell.com. mantenga estas instrucciones dentro del kit
 Instrucciones para proveedor de atención médica mantenga estas instrucciones dentro del kit IMPORTANTE: Antes de la recolección, asegurarse que los requisitos de elegibilidad de los donantes han sido cumplidos
Instrucciones para proveedor de atención médica mantenga estas instrucciones dentro del kit IMPORTANTE: Antes de la recolección, asegurarse que los requisitos de elegibilidad de los donantes han sido cumplidos
DIAGNÓSTICO MOLECULAR CMV Y EBV
 DIAGNÓSTICO MOLECULAR CMV Y EBV DIAGNÓSTICO MOLECULAR REACCIÓN EN CADENA DE LA POLIMERASA (PCR) ALTA SENSIBILIDAD Y ESPECIFICIDAD DIAGNÓSTICO MOLECULAR REACCIÓN EN CADENA DE LA POLIMERASA (PCR) PCR PUNTO
DIAGNÓSTICO MOLECULAR CMV Y EBV DIAGNÓSTICO MOLECULAR REACCIÓN EN CADENA DE LA POLIMERASA (PCR) ALTA SENSIBILIDAD Y ESPECIFICIDAD DIAGNÓSTICO MOLECULAR REACCIÓN EN CADENA DE LA POLIMERASA (PCR) PCR PUNTO
LINEAMIENTOS DE LA UTILIZACION DEL DIAGNÓSTICO Y VIGILANCIA DE LABORATORIO PARA LA ENFERMEDAD DE ZIKA, CHIKUNGUNYA Y DENGUE
 LINEAMIENTOS DE LA UTILIZACION DEL DIAGNÓSTICO Y VIGILANCIA DE LABORATORIO PARA LA ENFERMEDAD DE ZIKA, CHIKUNGUNYA Y DENGUE LABORATORIO NACIONAL DE SALUD Unidad Central de Referencia para la Vigilancia
LINEAMIENTOS DE LA UTILIZACION DEL DIAGNÓSTICO Y VIGILANCIA DE LABORATORIO PARA LA ENFERMEDAD DE ZIKA, CHIKUNGUNYA Y DENGUE LABORATORIO NACIONAL DE SALUD Unidad Central de Referencia para la Vigilancia
EL VIRUS DE INMUNODEFICIENCIA ADQUIRIDA HUMANA Y SIDA. (VIH Y SIDA).
 EL VIRUS DE INMUNODEFICIENCIA ADQUIRIDA HUMANA Y SIDA. (VIH Y SIDA). 2 Qué es el VIH? y el sida? El VIH es el virus de la inmunodeficiencia humana, que se transmite de diferentes maneras, y que, en su
EL VIRUS DE INMUNODEFICIENCIA ADQUIRIDA HUMANA Y SIDA. (VIH Y SIDA). 2 Qué es el VIH? y el sida? El VIH es el virus de la inmunodeficiencia humana, que se transmite de diferentes maneras, y que, en su
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS
 PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
RIESGOS DERIVADOS DE LA INCORRECTA CLASIFICACIÓN
 1. Riesgo de pinchazo o corte Situación 1: Deshacer elementos punzantes y cortantes en contenedores no destinados a tal fin. Ejemplo: Desechar un elemento cortante o punzante en contenedores de 30 y 60
1. Riesgo de pinchazo o corte Situación 1: Deshacer elementos punzantes y cortantes en contenedores no destinados a tal fin. Ejemplo: Desechar un elemento cortante o punzante en contenedores de 30 y 60
Utilidad clínica de la prueba de Captura de Híbridos en la detección del Cáncer del Cuello Uterino
 Utilidad clínica de la prueba de Captura de Híbridos en la detección del Cáncer del Cuello Uterino Alejandro García Carrancá, PhD Jefe del Laboratorio de Virus y Cáncer Unidad de Investigación Biomédica
Utilidad clínica de la prueba de Captura de Híbridos en la detección del Cáncer del Cuello Uterino Alejandro García Carrancá, PhD Jefe del Laboratorio de Virus y Cáncer Unidad de Investigación Biomédica
Cómo agregar heparina a la solución de diálisis
 Cómo agregar heparina a la solución de diálisis #1594/1428s Por qué? La heparina (heparina de sodio) es un medicamento que evita los coágulos de sangre (anticoagulante). Podría usarse para evitar la formación
Cómo agregar heparina a la solución de diálisis #1594/1428s Por qué? La heparina (heparina de sodio) es un medicamento que evita los coágulos de sangre (anticoagulante). Podría usarse para evitar la formación
DIAPOSITIVA 1 Esta presentación tratará sobre los Diagnósticos In Vitro (o IVDs, por sus siglas en inglés) de Análisis de Sangre.
 Diagnósticos In Vitro de Análisis de Sangre (OBRR) DIAPOSITIVA 1 Esta presentación tratará sobre los Diagnósticos In Vitro (o IVDs, por sus siglas en inglés) de Análisis de Sangre. DIAPOSITIVA 2 Para la
Diagnósticos In Vitro de Análisis de Sangre (OBRR) DIAPOSITIVA 1 Esta presentación tratará sobre los Diagnósticos In Vitro (o IVDs, por sus siglas en inglés) de Análisis de Sangre. DIAPOSITIVA 2 Para la
Analizador portátil til CD4. Solución innovadora y revolucionaria para el seguimiento de pacientes HIV positivos
 Analizador portátil til CD4 Solución innovadora y revolucionaria para el seguimiento de pacientes HIV positivos Qué es PIMA? Es la primer solución point-of-care para el análisis de CD4. Diseñado para desempeñarse
Analizador portátil til CD4 Solución innovadora y revolucionaria para el seguimiento de pacientes HIV positivos Qué es PIMA? Es la primer solución point-of-care para el análisis de CD4. Diseñado para desempeñarse
PROCEDIMIENTO 8 PROCEDIMIENTO PARA LA TOMA, PROCESAMIENTO Y TRANSPORTE DE MUESTRAS DE LABORATORIO EN IPS DESIGNADAS
 PROCEDIMIENTO 8 PROCEDIMIENTO PARA LA TOMA, PROCESAMIENTO Y TRANSPORTE DE MUESTRAS DE LABORATORIO EN IPS DESIGNADAS MINISTERIO DE SALUD Y PROTECCIÓN SOCIAL Bogotá, Octubre de 2014 SIG-F05 VERSIÓN 1 (6
PROCEDIMIENTO 8 PROCEDIMIENTO PARA LA TOMA, PROCESAMIENTO Y TRANSPORTE DE MUESTRAS DE LABORATORIO EN IPS DESIGNADAS MINISTERIO DE SALUD Y PROTECCIÓN SOCIAL Bogotá, Octubre de 2014 SIG-F05 VERSIÓN 1 (6
1. Revisar que se hayan seguido las medidas higiénicas inmediatas:
 PROTOCOLO DE ACTUACIÓN EN EL SERVICIO DE URGENCIAS EN CASO DE ACCIDENTE CON RIESGO BIOLÓGICO Autores: Alvarez Erviti, Susana; Asenjo Redín, Belén Servicio de Prevención de Riesgos Laborales. SNS-Osasunbidea
PROTOCOLO DE ACTUACIÓN EN EL SERVICIO DE URGENCIAS EN CASO DE ACCIDENTE CON RIESGO BIOLÓGICO Autores: Alvarez Erviti, Susana; Asenjo Redín, Belén Servicio de Prevención de Riesgos Laborales. SNS-Osasunbidea
HIV 1 & 2 TriSpot Ag-Ab
 S HIV 1 & 2 TriSpot Ag-Ab Para comenzar la prueba, se agregan muestras de suero o plasma al diluyente en los pocillos de la fila A de la Bandeja de desarrollo. Luego el peine se inserta en los pocillos
S HIV 1 & 2 TriSpot Ag-Ab Para comenzar la prueba, se agregan muestras de suero o plasma al diluyente en los pocillos de la fila A de la Bandeja de desarrollo. Luego el peine se inserta en los pocillos
ENFERMEDAD POR EL VIRUS DEL ÉBOLA (EVE) PROTOCOLO PARA EL DIAGNÓSTICO POR LABORATORIO Noviembre. 2014
 1 Tabla de contenido Introducción... 3 Objetivo... 3 Alcance... 3 Diagnóstico de Enfermedad por el Virus del Ébola... 3 Tipos de prueba de laboratorio... 4 Toma de la muestra... 5 Consideraciones generales...
1 Tabla de contenido Introducción... 3 Objetivo... 3 Alcance... 3 Diagnóstico de Enfermedad por el Virus del Ébola... 3 Tipos de prueba de laboratorio... 4 Toma de la muestra... 5 Consideraciones generales...
VIH/SIDA SAN MARCOS 13 DE MAYO 2003 PREVENIR EL SIDA ES RESPONSABILIDAD DE TODOS Y TODAS
 VIH/SIDA SAN MARCOS 13 DE MAYO 2003 ANTECEDENTES SIDA identificado en 1981 1,983 se aisla el VIH por el equipo del Dr. Luc Montacnier. Desde 1994 a 2002 en Guatemala se han reportado 4369 casos ( 37 por
VIH/SIDA SAN MARCOS 13 DE MAYO 2003 ANTECEDENTES SIDA identificado en 1981 1,983 se aisla el VIH por el equipo del Dr. Luc Montacnier. Desde 1994 a 2002 en Guatemala se han reportado 4369 casos ( 37 por
AISLAMIENTO UNIVERSAL
 AISLAMIENTO UNIVERSAL OBJETIVO: Llevar a cabo las medidas de protección que deben observarse de forma sistemática y generalizada en el ámbito hospitalario. 1 EQUIPAMIENTO NECESARIO: Jabón antiséptico y
AISLAMIENTO UNIVERSAL OBJETIVO: Llevar a cabo las medidas de protección que deben observarse de forma sistemática y generalizada en el ámbito hospitalario. 1 EQUIPAMIENTO NECESARIO: Jabón antiséptico y
PAMI 8: Diagnóstico de la infección por VIH
 PAMI 8: Diagnóstico de la infección por VIH SITUACIÓN ACTUAL DEL DIAGNÓSTICO EN ESPAÑA NUEVOS DIAGNÓSTICOS DE LA INFECCIÓN A finales del año 2013 la tasa anual de nuevos diagnósticos fue de 70,4/100.000.000
PAMI 8: Diagnóstico de la infección por VIH SITUACIÓN ACTUAL DEL DIAGNÓSTICO EN ESPAÑA NUEVOS DIAGNÓSTICOS DE LA INFECCIÓN A finales del año 2013 la tasa anual de nuevos diagnósticos fue de 70,4/100.000.000
Validación del proceso de desinfección
 Validación del proceso de desinfección Silvia I. Acosta-Gnass Prevención y Control de Infecciones Riverside County Regional Medical Center Moreno Valley, California, EEUU Pan American Health Organization
Validación del proceso de desinfección Silvia I. Acosta-Gnass Prevención y Control de Infecciones Riverside County Regional Medical Center Moreno Valley, California, EEUU Pan American Health Organization
VIH y BOMBEROS. Preguntas y respuestas
 VIH y BOMBEROS Preguntas y respuestas Por qué hablamos sobre el VIH y bomberos? Aunque no existe ninguna evidencia que muestre una especial vinculación entre el VIH y nuestro trabajo como bomberas y bomberos,
VIH y BOMBEROS Preguntas y respuestas Por qué hablamos sobre el VIH y bomberos? Aunque no existe ninguna evidencia que muestre una especial vinculación entre el VIH y nuestro trabajo como bomberas y bomberos,
Haga la prueba fácil y cómodamente - Asegure resultados completos y precisos -
 PRESENTACIÓN Haga la prueba fácil y cómodamente - La única prueba rápida del VIH para usar con: Muestras de fluído oral Sangre completa obtenida por venopunción Sangre completa obtenida por pinchazo de
PRESENTACIÓN Haga la prueba fácil y cómodamente - La única prueba rápida del VIH para usar con: Muestras de fluído oral Sangre completa obtenida por venopunción Sangre completa obtenida por pinchazo de
-Test Inmunodeficiecia Felina
 -Test Inmunodeficiecia Felina Ref: AI04 DECRIPCIÓN Detección de Anticuerpos P24 del virus de Inmunoteficiencia Felina en suero, plasma o sangre en 10 minutos. PRINCIPIO Ensayo Inmunocromatográfico en un
-Test Inmunodeficiecia Felina Ref: AI04 DECRIPCIÓN Detección de Anticuerpos P24 del virus de Inmunoteficiencia Felina en suero, plasma o sangre en 10 minutos. PRINCIPIO Ensayo Inmunocromatográfico en un
SISTEMA INTEGRADO DE GESTIÓN -SSYMA-
 Página 1 de 5 1. OBJETIVO Establecer los lineamientos para identificar los peligros y evaluar y controlar los riesgos relacionados a la Seguridad y Salud Ocupacional asociados a la exposición de patógenos
Página 1 de 5 1. OBJETIVO Establecer los lineamientos para identificar los peligros y evaluar y controlar los riesgos relacionados a la Seguridad y Salud Ocupacional asociados a la exposición de patógenos
Propuesta de nuevos algoritmos para el diagnóstico de VIH
 Propuesta de nuevos algoritmos para el diagnóstico de VIH Propuesta de nuevos algoritmos para el diagnóstico de VIH Autores Bioq. María Belén Bouzas Jefa de División Análisis Clínicos. Hospital de Infecciosas
Propuesta de nuevos algoritmos para el diagnóstico de VIH Propuesta de nuevos algoritmos para el diagnóstico de VIH Autores Bioq. María Belén Bouzas Jefa de División Análisis Clínicos. Hospital de Infecciosas
CENTRO NACIONAL DE VIGILANCIA EPIDEMIOLOGICA INSTITUTO DE DIAGNOSTICO Y REFERENCIA EPIDEMIOLOGICOS
 CENTRO NACIONAL DE VIGILANCIA EPIDEMIOLOGICA INSTITUTO DE DIAGNOSTICO Y REFERENCIA EPIDEMIOLOGICOS DIAGNOSTICO POR LABORATORIO DEL VIRUS DEL OESTE DEL NILO Participantes José Carmen Gudiño Rita Flores
CENTRO NACIONAL DE VIGILANCIA EPIDEMIOLOGICA INSTITUTO DE DIAGNOSTICO Y REFERENCIA EPIDEMIOLOGICOS DIAGNOSTICO POR LABORATORIO DEL VIRUS DEL OESTE DEL NILO Participantes José Carmen Gudiño Rita Flores
La mayoría de exposiciones no ocasionan una infección. Después de una exposición, el riesgo de infección depende de factores como los siguientes:
 Exposición a la sangre Lo que deben saber los trabajadores de la salud Departamento de Salud y Servicios Humanos Centros para el Control y la Prevención de Enfermedades Exposiciones ocupacionales a la
Exposición a la sangre Lo que deben saber los trabajadores de la salud Departamento de Salud y Servicios Humanos Centros para el Control y la Prevención de Enfermedades Exposiciones ocupacionales a la
PROTOCOLO DE PROFILAXIS POST-EXPOSICIÓN FRENTE A VIH
 PROTOCOLO DE PROFILAXIS POST-EXPOSICIÓN FRENTE A VIH Ante paciente que acude por posible contacto con VIH, o personal sanitario en contacto potencial con el virus, se recomienda seguir el siguiente algoritmo
PROTOCOLO DE PROFILAXIS POST-EXPOSICIÓN FRENTE A VIH Ante paciente que acude por posible contacto con VIH, o personal sanitario en contacto potencial con el virus, se recomienda seguir el siguiente algoritmo
Norma/Política Precauciones, estándares y uso adecuado de desinfectantes
 01.00 de / Modificación: 01/00 Fecha de Vigencia: 27/12/13 Responsable de Gestión de la norma/política: Dra. Inés Staneloni/ Int. 8165 Mail: maria.staneloni@hospitalitaliano.org.ar Estándar: PCI.9 Referencias:
01.00 de / Modificación: 01/00 Fecha de Vigencia: 27/12/13 Responsable de Gestión de la norma/política: Dra. Inés Staneloni/ Int. 8165 Mail: maria.staneloni@hospitalitaliano.org.ar Estándar: PCI.9 Referencias:
FeLV Ag / FIV Ab Test Kit
 SensPERT FeLV Ag / FIV Ab Test Kit CONCEPTO SENSPERT La línea de diagnóstico SensPERT de Rapid Test proporciona una solución rápida, específica y fiable para los médicos veterinarios en su práctica clínica
SensPERT FeLV Ag / FIV Ab Test Kit CONCEPTO SENSPERT La línea de diagnóstico SensPERT de Rapid Test proporciona una solución rápida, específica y fiable para los médicos veterinarios en su práctica clínica
Definición de caso confirmado de VIH. En mayores de 18 meses: 2 pruebas presuntivas positivas y western Blot positivo
 Página: 1 de 14 Objetivo: Evitar la transmisión vertical y determinar la ruta de atención de las Gestantes con diagnostico o sospecha de diagnostico de VIH o Hepatitis B Medidas de Prevención: Captación
Página: 1 de 14 Objetivo: Evitar la transmisión vertical y determinar la ruta de atención de las Gestantes con diagnostico o sospecha de diagnostico de VIH o Hepatitis B Medidas de Prevención: Captación
Mat. Natalia Torres D.Educadora Roche Diabetes Care
 Mat. Natalia Torres D.Educadora Roche Diabetes Care Objetivos Definir Glicemia capilar Identificar los objetivos del control de glicemia capilar Conocer la historia toma de muestra de glicemia capilar
Mat. Natalia Torres D.Educadora Roche Diabetes Care Objetivos Definir Glicemia capilar Identificar los objetivos del control de glicemia capilar Conocer la historia toma de muestra de glicemia capilar
VIH Y EMBARAZO TALLER NACIONAL DE LA ELIMINACIÓN MATENRO INFANTIL DEL VIH D R A. C L A U D I A M A Z A R I E G O S
 VIH Y EMBARAZO TALLER NACIONAL DE LA ELIMINACIÓN MATENRO INFANTIL DEL VIH D R A. C L A U D I A M A Z A R I E G O S Guatemala 2 de marzo de 2016 PERSONAS CON EL VIH CON ACCESO AL TRATAMIENTO RICO En junio
VIH Y EMBARAZO TALLER NACIONAL DE LA ELIMINACIÓN MATENRO INFANTIL DEL VIH D R A. C L A U D I A M A Z A R I E G O S Guatemala 2 de marzo de 2016 PERSONAS CON EL VIH CON ACCESO AL TRATAMIENTO RICO En junio
DuPont Protección de Cultivos Seguimiento de Etiquetas México
 Comunicado MACC DCP-02062014 DuPont Protección de Cultivos Junio 2014 DuPont Protección de Cultivos Seguimiento de Etiquetas México Estimados clientes: La presente comunicación quiere resaltar la importancia
Comunicado MACC DCP-02062014 DuPont Protección de Cultivos Junio 2014 DuPont Protección de Cultivos Seguimiento de Etiquetas México Estimados clientes: La presente comunicación quiere resaltar la importancia
COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS
 DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
22/01/2009 NOM-050-SCFI-2004 INFORMACION COMERCIAL- ETIQUETADO GENERAL DE PRODUCTOS BSL. Todos los Derechos reservados
 1 15 de abril de 2004, Comité Consultivo Nacional de Normalización de Seguridad al Usuario, Información Comercial y Prácticas de Comercio. EMPRESAS E INSTITUCIONES: - ALMACENADORA ACCEL, S.A. - ASOCIACION
1 15 de abril de 2004, Comité Consultivo Nacional de Normalización de Seguridad al Usuario, Información Comercial y Prácticas de Comercio. EMPRESAS E INSTITUCIONES: - ALMACENADORA ACCEL, S.A. - ASOCIACION
Nuevos enfoques diagnósticos de la infección por VIH
 Nuevos enfoques diagnósticos de la infección por VIH Santiago Estrada M.D Laboratorio Clínico VID Agosto 28 de 2015 Hoja informativa para los pacientes que solicitan una prueba de VIH Recomendaciones para
Nuevos enfoques diagnósticos de la infección por VIH Santiago Estrada M.D Laboratorio Clínico VID Agosto 28 de 2015 Hoja informativa para los pacientes que solicitan una prueba de VIH Recomendaciones para
Kit artus EBV QS-RGQ. Características de rendimiento. Mayo Sample & Assay Technologies. Sensibilidad analítica (plasma)
 Kit artus EBV QS-RGQ Características de rendimiento Kit artus EBV QS-RGQ, versión 1, 4501363 Compruebe la disponibilidad de nuevas revisiones electrónicas de las especificaciones en www.qiagen.com/products/artusebvpcrkitce.aspx
Kit artus EBV QS-RGQ Características de rendimiento Kit artus EBV QS-RGQ, versión 1, 4501363 Compruebe la disponibilidad de nuevas revisiones electrónicas de las especificaciones en www.qiagen.com/products/artusebvpcrkitce.aspx
Diagnóstico del Dengue
 Solución Total: Todo lo que usted necesita saber acerca del Diagnóstico del Dengue Prueba Rápida Dengue Duo ( + Ab Combo) Dengue IgG/IgM ELISA Dengue IgM capture ELISA Dengue IgG capture ELISA ELISA 2
Solución Total: Todo lo que usted necesita saber acerca del Diagnóstico del Dengue Prueba Rápida Dengue Duo ( + Ab Combo) Dengue IgG/IgM ELISA Dengue IgM capture ELISA Dengue IgG capture ELISA ELISA 2
FORMULARIO DE INVESTIGACIÓN DE EAV Sólo para Eventos Adversos Serios Atribuidos a la Vacunación
 Página 1 de 9 Sólo para Eventos Adversos Serios Atribuidos a la ción SECCIÓN A DETALLES BÁSICOS Estado Distrito ID Lugar de la vacunación Centro de salud pública Centro de salud privado Otro (Especificar)
Página 1 de 9 Sólo para Eventos Adversos Serios Atribuidos a la ción SECCIÓN A DETALLES BÁSICOS Estado Distrito ID Lugar de la vacunación Centro de salud pública Centro de salud privado Otro (Especificar)
HIGIENE EN EL MEDIO HOSPITALARIO
 HIGIENE EN EL MEDIO HOSPITALARIO Código Nombre Categoría SN_0079 HIGIENE EN EL MEDIO HOSPITALARIO SANIDAD Duración 30 HORAS Modalidad ONLINE Audio SI Vídeo SI Objetivos OFRECER AL PERSONAL DEL CENTRO SANITARIO
HIGIENE EN EL MEDIO HOSPITALARIO Código Nombre Categoría SN_0079 HIGIENE EN EL MEDIO HOSPITALARIO SANIDAD Duración 30 HORAS Modalidad ONLINE Audio SI Vídeo SI Objetivos OFRECER AL PERSONAL DEL CENTRO SANITARIO
