Se van a purificar dos proteínas, una de origen animal, la lisozima de la clara de huevo y otra vegetal la galactosidasa de hojas de espinaca.
|
|
|
- Isabel Ponce Maldonado
- hace 6 años
- Vistas:
Transcripción
1 PRÁCTICA 1 PURIFICACIÓN DE ENZIMAS OBJETIVO: Extraer y purificar enzimas mediante cromatografía de intercambio iónico utilizando SP Sepharose y Q Sepharose, para posteriormente cuantificarlas en las diferentes fracciones y ver sus actividades. Se van a purificar dos proteínas, una de origen animal, la lisozima de la clara de huevo y otra vegetal la galactosidasa de hojas de espinaca. La cromatografía de intercambio iónico se fundamenta en las propiedades ácido-base de las proteínas. Una proteína, a ph menor de su pi (punto isoeléctrico), tendrá carga positiva y a ph mayor de su pi presentará carga negativa. Por lo que, en el primer caso, se unirá a una resina con carga negativa (SP Sepharose) y en el segundo a una resina con carga positiva (Q Sepharose). Una vez unida la proteína a las resinas, estas se pueden eluir de dos formas distintas: 1) variando el ph del medio hasta alcanzar el pi 2) mediante un gradiente iónico añadiendo el contraión correspondiente (Na + en el caso de intercambio catiónico o Cl - para el intercambio aniónico)
2 A.- PURIFICACIÓN DE LA LISOZIMA Dado que el pi de la lisozima es de 11, dos unidades de ph superior al del resto de las proteínas de la clara del huevo, a un ph de 9,5-10 la lisozima es prácticamente la única proteína con carga positiva neta. Ello permite separar esta enzima del resto de proteínas mediante la utilización de resinas intercambiadoras de cationes. Materiales: *Huevos de gallina *Tampón A: glicina/naoh 100 mm, ph 10 * Tampón B: glicina/naoh 100 mm, ph 10, conteniendo 0.6 M NaCl Protocolo: 1.- Recoger la clara procedente de un huevo. Diluirla 1/5 (vol/vol) con Tampón A. Tomar 10 ml de la muestra anterior en un tubo de 15 ml (Fracción 0, F0). Se separa 1 ml para cuantificar. 2.- Al resto del extracto proteico, añadir 4 ml de SP Sepharose y agitar suavemente durante 15 minutos para que la lisozima se adhiera a la resina. 3.- Al finalizar la incubación, centrifugar la muestra a 1500 g durante 3 minutos. Guardar el sobrenadante (F1). 4.- Añadir a la resina 10 ml de tampón. Agitar suavemente y centrifugar de nuevo. Recoger el sobrenadante (F2). 5.- Repetir el lavado anterior y desechar el sobrenadante. 6.- Resuspender la SP Sepharose con 3 ml de tampón B e incubar, agitando suavemente durante 10 minutos. Centrifugar y recoger el líquido (F3 que correspondería con la lisozima purificada).
3 B.- PURIFICACIÓN DE GALACTOSIDASA En las plantas podemos encontrar distintos tipos de galactosidasas con diferentes pesos moleculares (entre 38 y 58 kd) y también con pi que varían entre 6.9 y 5.2. En esta práctica vamos a intentar purificar distintas fracciones proteicas del extracto de hojas de espinacas utilizando en este caso una resina de intercambio aniónico (Q Sepharose), de manera que las proteínas estén ionizadas negativamente por medio de un ph superior al pi. Materiales: *3 g de hojas de espinacas *Tampón A: Fosfato Sódico 50 mm, ph 7.5 * Tampón B: Fosfato Sódico 50 mm, ph 6 * Tampón C: Acético/Acetato Sódico 50 mm, ph 4.5 Protocolo: 1.- Se homogenizan las hojas en un mortero (puede emplearse N 2 líquido que facilita este proceso). 2.- Añadir 10 ml de Tampón A, recoger la mezcla y filtrarla a vacío con ayuda de una muselina o de papel de filtro (F0). Separar 1 ml para cuantificar. 3.- A los 9 ml restantes se le añaden 4 ml de resina Q Sepharose y se continúa el proceso igual que en el apartado A (purificación de lisozima), pero lavando una sola vez y eluyendo con los tampones B y C sucesivamente.
4 PRÁCTICA 2 DETERMINACIÓN DE PROTEÍNAS OBJETIVO: Calcular la concentración total de proteínas contenida en una disolución. Con este fin, utilizaremos las muestras obtenidas en la práctica de purificación y seguiremos dos métodos, el colorimétrico Bradford y el espectofotométrico. A.- MÉTODO BRADFORD Basado en la unión directa del colorante azul de Coomassie Blue G-250 a la estructura terciaria de las proteínas y aminoácidos específicos. Esta unión se realiza a través de grupos ionizados y consiste en la medición de la extinción provocada por el cambio en el espectro visible del colorante cuando éste se une a la proteína (absorbiendo a 595 nm), así el colorante cambiaría de color de marrón a azul proporcionalmente en función del contenido proteico de la muestra. Para determinar la cantidad de proteína, es necesaria la comparación del valor de la absorbancia de la muestra con los valores obtenidos a partir de cantidades conocidas de proteínas, con lo que se construye una curva de calibración. Recta de Calibrado Se realiza en microplacas con BSA comercial (Seroalbúmina Bovina). 1.- La concentración de la que partimos es 2 mg/ml y se hacen diluciones con el tampón de elución empleado en cada caso de 1 y 0.5 mg/ml, en tubo eppendorf. 2.- Hacer un blanco con 5L del tampón y por triplicado. 3.- Se pipetean 5L de cada dilución de BSA y se añaden a un pocillo de la microplaca por triplicado. Muestras Añadir, por triplicado, volúmenes variados de cada muestra, entre 1 y 5 L. Los extractos crudos al tener mucha concentración de proteína probablemente saturen el ensayo con lo que se aconseja hacer una dilución ó variar el volumen. Ensayo 1.- A todos los pocillos de le añaden 300L de Reactivo Bradford, repipeteando con cuidado para que la mezcla quede bien homogenizada. 2.- Esperar 15 minutos para que desarrolle el color. 3.- Medir la absorbancia a 595nm. 4.- Calcular la concentración de proteína en la muestra. Se puede emplear una hoja de cálculo como la que se adjunta.
5 B.- MÉTODO ESPECTROFOTOMÉTRICO Desarrollado en múltiples variantes, aunque la más recomendada es la de Scopes. Se basa en la propiedad de las proteínas de tener un máximo de absorción a 280 nm debido al contenido en los aminoácidos tirosina y triptófano y fenilalanina. La variabilidad en estos aminoácidos en diferentes proteínas obliga a añadir un factor de corrección aportado por la absorbancia del enlace peptídico a 205 nm. Así: [Prot](mg/mL) = A 205 [27!120[ A 280 A 205 ]] La mayoría de equipos modernos ya actualizan el factor de corrección.
6 PRÁCTICA 3 MEDIDA DE LA ACTIVIDAD ENZIMATICA A.- MEDIDA DE LA ACTIVIDAD DE LA LISOZIMA DE LAS FRACCIONES PURIFICADAS La medida de la actividad lisozima se realiza utilizando una suspensión de agregados de pared celular del microorganismo Micrococcus lysodeikticus en concentración suficientemente elevada para atenuar, por dispersión, la transmisión de luz monocromática a través de la cubeta de un espectrofotómetro. Al incubar esta suspensión con lisozima, los fragmentos de pared celular se hidrolizan, originando otros más pequeños, lo que reduce la dispersión de la luz, que se manifiesta en una reducción en la absorbancia a una longitud de onda fija de 450 nm. La actividad enzimática es proporcional a la disminución de la absorbancia a 450 nm. Por definición, en condiciones estándar (25ºC, ph 6,2 y 0,1 M fosfato), se considera que 1 unidad de actividad enzimática de lisozima (U) produce una disminución en la absorbancia de 0,001 en 1 minuto. METODO DE MEDIDA: 1. En una cubeta de espectrofotómetro, añadir 3 ml de suspensión de pared bacteriana. Meterla en el espectrofotómetro y anotar la densidad óptica (D.O.). Esta medida constituye el tiempo cero y hay que hacerlo para cada medida. 2. Añadir 25 µl de la fracción correspondiente a ensayar, tomar el tiempo por el reloj, agitar e introducir la cubeta en el espectrofotómetro y anotar la absorbancia observada al primer minuto y al segundo minuto. Calcular la variación de absorbancia al primer minuto (ΔA 1 /min) y al segundo (ΔA 2 /min). Hacer la media de las dos medidas. Anotar los resultados en la tabla siguiente: Volumen (ml) Absorbanci a tº 0 Absorbanci a tº 1 Absorbanci a tº 2 ΔA 1 /mi n ΔA 2 /mi n ΔA/min Actividad (U) F 0 F 1 F 2 F 3
7 CALCULOS: 1. Actividad de cada fracción 2. % Retención de la resina: Actividad F 0 Actividad F 1 x 100 Actividad F 0 3. % de Recuperación: Actividad F 3 x 100 Actividad Fo
8 B.- EFECTO DE LA TEMPERATURA Y DE LA REDUCCIÓN DE LOS PUENTES DISULFURO SOBRE LA ACTIVIDAD DE LA LISOZIMA OBJETIVO: estudiar la contribución de los enlaces disulfuro y puentes de hidrógeno a la conformación del centro activo de la lisozima y su efecto sobre la actividad de la enzima. La lisozima es una proteína globular constituida por una sola cadena polipeptídica, su estructura presenta 4 hélices α y 1 hoja extendida β. Esta proteína presenta cuatro puentes disulfuro cruzados que contribuyen a su elevada estabilidad. El DTT (ditiotreitrol) es un reductor de puente disulfuro. Por tanto, su adición en concentración suficiente, reducirá los -S-S- de la lisozima y producirá cambios en la estructura terciaria de la proteína. Estos cambios pueden afectar a la actividad enzimática de la lisozima. Por otra parte, los puentes de hidrógeno también están implicados en el mantenimiento de la estructura de las proteínas. Estos puentes de hidrógenos se pueden romper fácilmente por tratamiento con calor. Del mismo modo al caso anterior, la modificación de la estructura de la proteína por rotura de los puentes de hidrógeno puede modificar la actividad del enzima PROTOCOLO El estudio se lleva a cabo en la fracción F3 purificada en la práctica anterior 1. Preparar 4 tubos eppendorf numerados del 1 al 4 y pipetear las cantidades adecuadas según se indica en la tabla siguiente:
9 Tubo Fracción F 3 DTT (0.5 M)* 50 C/30min 1 200μl μl 20μl μl μl 20μl + * La concentración de DTT de 0.5M es concentración inicial (75 mg/1000 ml) Los tubos 1 y 2 se mantienen a temperatura ambiente Los tubos 3 y 4 se calientan a 50ºC durante 30 min. 2. Medir la actividad como se indicó en la práctica anterior. Anotar los resultados en la tabla siguiente: TUBO Volumen (ml) Absorbancia tº 0 Absorbanci a tº 1 Absorbancia tº 2 ΔA 1/min ΔA 2/min ΔA/min Actividad (U)
10 PRÁCTICA 4 ELECTROFORESIS: Separación de proteínas en geles de poliacrilamida OBJETIVO: utilizar la técnica de la electroforesis en gel para analizar la purificación de la enzima lisozima. Se analizará la composición proteica de las distintas fracciones y se constatará el grado de pureza de la lisozima. FUNDAMENTO La electroforesis es la migración de iones en un campo eléctrico. Es una de las técnicas analíticas más importantes dentro de la Bioquímica. Las moléculas biológicas (ADN, proteínas, vitaminas, etc.) poseen cargas eléctricas, y por tanto poseen esta propiedad de movilidad en un campo eléctrico. La movilidad dependerá de la carga que presentan al ph que trabajemos. La electroforesis en gel es el método más conveniente para realizar separaciones de macromoléculas (ADN y Proteínas). El soporte de la electroforesis (el gel) es un entramado tridimensional que impide o reduce la difusión. Este gel ha de ser compatible con los tampones usados y debe permitir la entrada del líquido en los poros (reticulados hidratables). Los soportes pueden ser más o menos restrictivos según que el tamaño de poros limite o impida el paso de las moléculas. Los más restrictivos, como los geles de acrilamida- bisacrilamida, oponen impedimento al paso de las moléculas, participando así en el proceso de separación. Entre los menos restrictivos está la agarosa. El tamaño de poro que da unas dimensiones moleculares de criba de los geles puede ser establecido previamente. El gel en la electroforesis retarda, en mayor o menor medida, a las moléculas mayores respecto a las de menor tamaño. Las separaciones moleculares están pues basadas en el tamizado molecular junto a la movilidad electroforética de las moléculas que van a ser separadas. Para llevar a cabo la electroforesis se necesita: A. Una fuente de Tensión que proporciona campo eléctrico, mediante dos electrodos, positivo (ánodo) y negativo (cátodo), entre los que seestablece la diferencia de potencial. B. Una cubeta o recipiente, en cuyos extremos se sitúan los electrodos. C. Un soporte electroforético. D. El tampón de electroforesis: durante la electroforesis se produce electrolisis del agua, generándose protones en la proximidad del ánodo e iones hidroxilos en la proximidad del cátodo; el tampón evitará que el entorno anódico se acidifique y el catódico se haga más básico a lo largo de la electroforesis
11 El polímero utilizado para la formación del gel es la acrilamida y la bisacrilamida, los cuales se polimerizan mediante la adición de catalizadores (persulfato amónico, TEMED). En nuestro caso, la separación de las proteínas se verá condicionada sólo por su tamaño y no por su carga ya que previamente las proteínas serán desnaturalizadas utilizando un detergente (SDS), el cual despliega a las proteínas y se queda pegado a su superficie confiriéndole una gran carga negativa. Esa gran carga negativa enmascara la carga intrínseca de la proteína, y las proteínas una vez tratadas con SDS presentan todas la misma carga, y la separación será debida solamente a la masa molecular de la proteína. PROTOCOLO La separación electroforética se lleva a cabo según el método descrito por Laemmli en geles de poliacrilamida Gel de separación: poliacrilamida 15% (Para 2 geles) - Acrilamida- Bis-acrilamida(40%)(37.5:1) 4.32 ml - Tampón 1.5 m TrisHCl ph %SDS 2.8 ml - H ml - TEMED 9.2 µl - Persulfato amónico 10% 40 µl Verter, cuidadosamente, la acrilamida entre los cristales. Cubrir, cuidadosamente con 2-Butanol (utilizar una pipeta Pasteur) para delimitar el frente. Esperar a que el gel polimerice. Gel concentrador: poliacrilamida 3% - Acrilamida- Bis-acrilamida (40%) 0.75 ml - Tampón 0.5MTrisHCl ph %SDS 2.5 ml - H ml - TEMED 10 µl - Persulfato amónico 10% 100 µl Retirar el agua. Verter, cuidadosamente, la acrilamida entre los cristales. Colocar los peines y esperar a que polimerice.
12 Retirar los peines. El volumen final de los geles es aproximadamente 11 ml, para la preparación de 2 cristales. A 25 µl de cada fracción de la Práctica 1 se le añaden, en un eppendorf, 5 µl de tampón de carga 4X y 0.4 µl de agente reductor DTT 1M Calentar las muestras a 90ºC durante 5 min. Cargar en pocillos 20 µl de F y 10 µl del estándar de proteínas Correr la electroforesis en tampón Tris-HCl 0,025 M, ph 8,8, glicina 0,192 M y SDS 0,1% (TGS), a una voltaje constante de 30 ma hasta que el azul de bromofenol esté aproximadamente, a 1 mm del extremo inferior del gel. Desmontar el gel y teñirlo con metanol/acético/h20 (5/1/5) con azul de Coomassie (1 g/l). Desteñir el gel en metanol/acético/h20 (10/10/80).
13 PRÁCTICA 5 ELECTROFORESIS DE HEMOGLOBINAS Existen muchos tipos diferentes de hemoglobina (Hb) y los más comunes son HbA, HbA2, HbF, HbS, HbC, Hb H y Hgb M. Los adultos sanos sólo tienen niveles significativos de HbA y HbA2. Algunas personas también pueden tener pequeñas cantidades de HbF (que es el tipo principal de hemoglobina en el cuerpo de un recién nacido). Asimismo, ciertas enfermedades están asociadas con niveles altos de HbF (cuando la HbF corresponde a más del 2% de la hemoglobina total). La HbS es una forma anormal de hemoglobina asociada con la anemia drepanocítica. En las personas con esta afección, los glóbulos rojos algunas veces tienen una forma de luna creciente o falciforme. Estas células se descomponen fácilmente o pueden obstruir pequeños vasos sanguíneos. La HbC es una forma anormal de hemoglobina asociada con una anemia hemolítica y los síntomas son mucho más leves que los de la anemia drepanocítica. Reactivos Solución salina: 0.85% w/v NaCl Reactivo de hemolisis: 0.005M EDTA, 0.175% w/v saponina y 0.1% azida sódica como conservante; almacenar a RT; cuidado con la azida!!! 50 ml de 1.5M Tris ph 9.2 (MW Tris ): Pesar g de Tris, añadir 40 ml de agua. Agitar y ajustar a ph 9.2 con HCl. Completar hasta 50 ml. Tampón de muestra 4X: 8 ml glicerol, 4 ml de 1.5 M Tris ph 9.2, 14 ml de agua destilada, 0.01 g de azul de bromofenol (670 Da). Tampón de electroforesis 5X (sólo hay que diluirlo a 1x para ser utilizado): Para 2L pesar 160 g de Tris y 72 g de glicina. Añadir 1800 ml de dh2o, disolver y completar hasta 2 L. El ph debe de quedar entre 8.9 y 9.2. Preparación del gel: 1. Preparar y sellar un molde del tamaño apropiado. 2. Mezclar 1 g de agarosa en 100 ml de 1X tampón de electroforesis. 3. Disolver la agarosa en microondas. 4. Dejar enfriar a 55 ºC. 5. Depositar la agarosa en el molde. 6. Insertar el peine y dejar solidificar. 7. Una vez solidificado colocar el gel en la carcasa de electroforesis horizontal. 8. Rellenar con 1X tampón de electroforesis hasta 1-2 mm por encima del gel. Electroforesis de hemoglobinas:
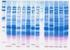
14 1. Sangre completa tratada con anticoagulante (heparinizada, EDTA) o buffy coat (se observará mejor la banda de leucocitos). Puede almacenarse la sangre completa o las células empaquetadas de 1-2 semanas a 6ºC. 2. Centrifugar 200 L de la sangre anticoagulada durante 10 minutos 2500 xg (5500 rpm) para separar las células del plasma. Eliminar el plasma y la capa superior del pellet, que se corresponderá con los leucocitos (apenas visible en sangre normal, pero muy evidente en muestras de buffy coats). 3. Lavar las células empaquetadas (pellet) con 5 volúmenes de solución salina (0.85% w/v NaCl). Centrifugar a 3500 rpm (1000xg) 5 minutos y aspirar el sobrenadante como antes. Repetir 2-3 veces para eliminar todas las proteínas del suero. 4. Preparar los hemolisados mezclando 10 l de eritrocitos empaquetados con 100 L de reactivo de hemolisis. Vortex vigoroso durante 15 segundos. Centrifugar a 10,000 xg durante 15 min para eliminar los fantasmas eritrocitarios. El sobrenadante preaclarado, que contiene la Hb (y por ello será de color rojo), se pasa a un tubo nuevo y se le añade 37 L de tampón de muestra 4X. Se cargarán sólo 20 l de lisado con tampón de muestra en cada canal. 5. Electroforesis: 100 voltios. Resultado de la electroforesis de hemoglobinas: 1 y 5: estándares de hemoglobina 2: Sangre de adulto normal 3: Sangre de recién nacido 4: Paciente #2 6: Padre paciente #2 7: Paciente #3 8: Madre paciente
15 PRÁCTICA 6 Electroforesis de proteínas del plasma El plasma sanguíneo es una solución muy compleja que contiene un gran número de proteínas, su concentración media es de 70g/L. Entre las funciones principales están el mantenimiento de la volemia, la capacidad amortiguadora, transporte de sustancias endógenas y exógenas, participación en la coagulación e inmunidad. La técnica más común para la separación de proteínas del suero es la electroforesis. En el caso del proteinograma electroforético, las proteínas migran en función de de la carg, independientemente de su tamaño. Para ello los soportes comúnmente usados son la agarosa y el acetato de celulosa. Empleando la técnica de separación con agarosa se pueden separar 6 bandas: prealbúmina y albúmina (que por ser la molécula más pequeña y con mayor número de grupos cargados negativamente, migra con mayor rapidez) seguida por las globulinas α1, α2, β1,β2, y γ OBJETIVO: Preparar el suero fisiológico normal y patológico de manera tal que la electroforesis nos permita identificar las diferentes proteínas que encontramos en estos.
16 MATERIALES Muestras de suero. Solución tampón TBE (TRIS, Borato EDTA). Tampón de carga. Gel de agarosa al 0,8%. Tinción Coomassie. PROTOCOLO Hacer dos diluciones en el tampón TBE de cada una de las distintas muestras de suero, de manera que la cantidad de cada una sea de 30 y 100µg Añadir el tampón de carga 4x Correr el gel Teñir con Coomassie.
Electroforesis de proteínas en geles de poliacrilamida
 Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo
 Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
Técnicas de Estudio de las células
 Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
ELECTROFORESIS AVANZADA
 Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS
 ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS Marcelo Castillo Navarrrete, T.M. MsCs (C) Facultad de Medicina Carrera Tecnología Médica 18 de Noviembre de 2004 Fundamentos de Electroforesis Alta
ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS Marcelo Castillo Navarrrete, T.M. MsCs (C) Facultad de Medicina Carrera Tecnología Médica 18 de Noviembre de 2004 Fundamentos de Electroforesis Alta
4. CURVAS DE TITULACION DE AMINOACIDOS
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 4. CURVAS DE TITULACION DE AMINOACIDOS ESQUEMA - Curvas de titulación de los aminoácidos Curva de titulación de un aminoácido
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 4. CURVAS DE TITULACION DE AMINOACIDOS ESQUEMA - Curvas de titulación de los aminoácidos Curva de titulación de un aminoácido
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA
 PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 1 Virología y Micología Veterinaria Trabajo Práctico No. 4 ELECTROFORESIS La electroforesis es una técnica utilizada para separar grandes moléculas por tamaño a través de la aplicación de un campo eléctrico
1 Virología y Micología Veterinaria Trabajo Práctico No. 4 ELECTROFORESIS La electroforesis es una técnica utilizada para separar grandes moléculas por tamaño a través de la aplicación de un campo eléctrico
TRABAJO PRÁCTICO Nº 2 CUANTIFICACIÓN DE PROTEÍNAS POR EL MÉTODO DE BRADFORD.
 AÑO 2010 PRIMER SEMESTRE LABORATORIO ASIGNATURA DE BIOQUÍMICA. PLAN COMÚN AGRONOMÍA E INGENIERÍA FORESTAL FACULTAD CIENCIAS SILVOAGROPECUARIAS TRABAJO PRÁCTICO Nº 2 CUANTIFICACIÓN DE PROTEÍNAS POR EL MÉTODO
AÑO 2010 PRIMER SEMESTRE LABORATORIO ASIGNATURA DE BIOQUÍMICA. PLAN COMÚN AGRONOMÍA E INGENIERÍA FORESTAL FACULTAD CIENCIAS SILVOAGROPECUARIAS TRABAJO PRÁCTICO Nº 2 CUANTIFICACIÓN DE PROTEÍNAS POR EL MÉTODO
TP2: Extracción y cuantificación de proteínas
 TP2: Extracción y cuantificación de proteínas Objetivos Obtener un extracto crudo de proteínas a partir de distintos órganos. Realizar un fraccionamiento a partir de una precipitación con Sulfato de Amonio.
TP2: Extracción y cuantificación de proteínas Objetivos Obtener un extracto crudo de proteínas a partir de distintos órganos. Realizar un fraccionamiento a partir de una precipitación con Sulfato de Amonio.
Anexo Conservar a 4 o C.
 Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
Purificación de proteínas
 Purificación de proteínas Purificación Proceso que cuenta con varias etapas cuyo objetivo es lograr la concentración diferencial de la proteína o molécula de interés Condiciones generales a evaluar Calidad
Purificación de proteínas Purificación Proceso que cuenta con varias etapas cuyo objetivo es lograr la concentración diferencial de la proteína o molécula de interés Condiciones generales a evaluar Calidad
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
 EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
METODOLOGÍA DE EXTRACCIÓN Y PURIFICACIÓN DE INHIBIDORES DE PROTEASAS EN Opuntia streptacantha
 METODOLOGÍA DE EXTRACCIÓN Y PURIFICACIÓN DE INHIBIDORES DE PROTEASAS EN Opuntia streptacantha RESUMEN Estudiante: Jannet Alejandra Vargas Sánchez Instituto Tecnológico de Roque jannettitajm@hotmail.com
METODOLOGÍA DE EXTRACCIÓN Y PURIFICACIÓN DE INHIBIDORES DE PROTEASAS EN Opuntia streptacantha RESUMEN Estudiante: Jannet Alejandra Vargas Sánchez Instituto Tecnológico de Roque jannettitajm@hotmail.com
ANEXOS. Anexo 1 Transformación mediante electroporación
 Anexo 1 Transformación mediante electroporación ANEXOS En este método de transformación de E. coli se requieren células electrocompetentes. La preparación de estas células consta de los siguientes pasos:
Anexo 1 Transformación mediante electroporación ANEXOS En este método de transformación de E. coli se requieren células electrocompetentes. La preparación de estas células consta de los siguientes pasos:
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDS-PAGE. Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE)
 ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
PRACTICAS DE ENSAYOS BIOTECNOLOGICOS (CFGS LABORATORIO DE ANALISIS Y DE CONTROL DE CALIDAD)
 PRACTICAS DE ENSAYOS BIOTECNOLOGICOS (CFGS LABORATORIO DE ANALISIS Y DE CONTROL DE CALIDAD) Introducción Se presentan 4 prácticas de laboratorio para ser desarrolladas dentro del segundo curso del nuevo
PRACTICAS DE ENSAYOS BIOTECNOLOGICOS (CFGS LABORATORIO DE ANALISIS Y DE CONTROL DE CALIDAD) Introducción Se presentan 4 prácticas de laboratorio para ser desarrolladas dentro del segundo curso del nuevo
DESARROLLO COGNOSCITIVO Y APRENDIZAJE
 Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
PRÁCTICAS AMPLIACIÓN DE MICROBIOLOGÍA
 PRÁCTICAS AMPLIACIÓN DE MICROBIOLOGÍA Día 1º.- EXPLICACIÓN GENERAL. TRANSFORMACIONES: E. coli, Streptomyces Día 2º.- INOCULAR MINIPREPS (8:45 de la mañana). OBTENCIÓN DE PLÁSMIDO ( MINIPREPS, Lisis alcalina)
PRÁCTICAS AMPLIACIÓN DE MICROBIOLOGÍA Día 1º.- EXPLICACIÓN GENERAL. TRANSFORMACIONES: E. coli, Streptomyces Día 2º.- INOCULAR MINIPREPS (8:45 de la mañana). OBTENCIÓN DE PLÁSMIDO ( MINIPREPS, Lisis alcalina)
ELECTROFORESIS Fundamento.
 ELECTROFORESIS La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar biomoleculas según su tamaño y carga eléctrica a través
ELECTROFORESIS La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar biomoleculas según su tamaño y carga eléctrica a través
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
TP3: Electroforesis en gel de poliacrilamida
 TP3: Electroforesis en gel de poliacrilamida Objetivos Comparar las fracciones de proteínas obtenidas en el TP Nº2 mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas.
TP3: Electroforesis en gel de poliacrilamida Objetivos Comparar las fracciones de proteínas obtenidas en el TP Nº2 mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas.
PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS.
 PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS. OBJETIVOS En esta práctica se tratarán aspectos de interés relacionados con los equilibrios
PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS. OBJETIVOS En esta práctica se tratarán aspectos de interés relacionados con los equilibrios
TÍTULO: Determinación colorimétrica de fenoles en agua por el método de la 4- aminoantipirina
 Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
Material elaborado por F. Agius, O. Borsani, P.Díaz, S. Gonnet, P. Irisarri, F. Milnitsky y J. Monza. Bioquímica. Facultad de Agronomía.
 AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas.
 La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS
 ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo PARTE I. EXTRACCIÓN Y PRECIPITACIÓN POR SALADO. Las proteínas se purifican mediante
ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo PARTE I. EXTRACCIÓN Y PRECIPITACIÓN POR SALADO. Las proteínas se purifican mediante
Inmunohematología. Dra. Ana Cecilia Haro
 Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN
 DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar un conocimiento del mapaje de ADN determinando
DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar un conocimiento del mapaje de ADN determinando
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN
 5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
MATERIALES Y MÉTODOS. Tipo de Estudio. Muestra
 MATERIALES Y MÉTODOS Tipo de Estudio Experimental. Este tipo de estudio tiene como característica primordial el poder manipular y controlar las variables, siendo en este caso la fuerza iónica y el ph.
MATERIALES Y MÉTODOS Tipo de Estudio Experimental. Este tipo de estudio tiene como característica primordial el poder manipular y controlar las variables, siendo en este caso la fuerza iónica y el ph.
TÍTULO: Determinación colorimétrica de fenoles solubles en material vegetal mediante el reactivo de Folin-Ciocalteu
 Página 1 de 7 1.- INTRODUCCIÓN El presente método colorimétrico permite el análisis de compuestos orgánicos que presenten anillos aromáticos hidroxilados (polifenoles, ácido tánico, taninos, ácido clorogénico,
Página 1 de 7 1.- INTRODUCCIÓN El presente método colorimétrico permite el análisis de compuestos orgánicos que presenten anillos aromáticos hidroxilados (polifenoles, ácido tánico, taninos, ácido clorogénico,
Métodos para la determinación de grasas
 Practica 4 Métodos para la determinación de grasas Antecedentes Los lípidos se encuentran ampliamente distribuidos en animales y vegetales, formado parte fundamental de membranas celulares. En los alimentos
Practica 4 Métodos para la determinación de grasas Antecedentes Los lípidos se encuentran ampliamente distribuidos en animales y vegetales, formado parte fundamental de membranas celulares. En los alimentos
TRABAJO PRÁCTICO Nº 5 ESTUDIO DE ANEMIAS. Emilse Ledesma Achem
 TRABAJO PRÁCTICO Nº 5 ESTUDIO DE ANEMIAS Emilse Ledesma Achem - 2016 - EVALUACIÓN CLÍNICA: Cuándo fue el último análisis sin anemia? Origen étnico Antecedentes personales y heredofamiliares ESTUDIO DE
TRABAJO PRÁCTICO Nº 5 ESTUDIO DE ANEMIAS Emilse Ledesma Achem - 2016 - EVALUACIÓN CLÍNICA: Cuándo fue el último análisis sin anemia? Origen étnico Antecedentes personales y heredofamiliares ESTUDIO DE
PRACTICA Nº 6 GLUCÓSIDOS CARDIOTÓNICOS Y SAPONINAS
 PRACTICA Nº 6 GLUCÓSIDOS CARDIOTÓNICOS Y SAPONINAS GLICÓSIDOS CARDIOTÓNICOS La valoración de glicósidos se puede realizar por los siguientes métodos: Por pesada directa del glicósido aislado, Por colorimetría,
PRACTICA Nº 6 GLUCÓSIDOS CARDIOTÓNICOS Y SAPONINAS GLICÓSIDOS CARDIOTÓNICOS La valoración de glicósidos se puede realizar por los siguientes métodos: Por pesada directa del glicósido aislado, Por colorimetría,
Proteínas: Métodos para su Estudio
 Proteínas: Métodos para su Estudio Propiedades Espectroscópicas Todos los aminoácidos absorben luz en la región infraroja Sólo Phe, Tyr, & Trp absorben UV Absorbancia a 280 nm es un buen diagnóstico para
Proteínas: Métodos para su Estudio Propiedades Espectroscópicas Todos los aminoácidos absorben luz en la región infraroja Sólo Phe, Tyr, & Trp absorben UV Absorbancia a 280 nm es un buen diagnóstico para
Taller Ciencia para Jóvenes CIMAT 2012 Bachillerato julio 8 14 Cinvestav Campus Guanajuato
 Introducción Taller Ciencia para Jóvenes CIMAT 2012 Bachillerato julio 8 14 Cinvestav Campus Guanajuato Visita al CINVESTAV - Irapuato. 19 julio, 2012. Las bacterias son los organismos más abundantes que
Introducción Taller Ciencia para Jóvenes CIMAT 2012 Bachillerato julio 8 14 Cinvestav Campus Guanajuato Visita al CINVESTAV - Irapuato. 19 julio, 2012. Las bacterias son los organismos más abundantes que
CROMATOGRAFÍA DE FILTRACIÓN EN GEL
 1.- FUNDAMENTO TEÓRICO CROMATOGRAFÍA DE FILTRACIÓN EN GEL Filtración en gel - 1 (Farmacia) La cromatografía de exclusión o filtración en gel es una clase de cromatografía sólido-líquido que permite la
1.- FUNDAMENTO TEÓRICO CROMATOGRAFÍA DE FILTRACIÓN EN GEL Filtración en gel - 1 (Farmacia) La cromatografía de exclusión o filtración en gel es una clase de cromatografía sólido-líquido que permite la
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE FUNDAMENTO TEÓRICO La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo eléctrico. Las moléculas se separan
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE FUNDAMENTO TEÓRICO La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo eléctrico. Las moléculas se separan
Unidad 6: ELECTROQUIMICA
 Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
Unidad 6: ELECTROQUIMICA REACCIONES DE OXIDACION-REDUCCION Las reacciones redox son aquellas en las cuales hay intercambio de electrones entre las sustancias que intervienen en la reacción. Oxidación:
Determinación de constantes de ionización
 Capítulo 5. Determinación de constantes de ionización Se determinaron las constantes de ionización de diversos compuestos mediante curvas de titulación ácido-base empleando métodos espectrofotométricos
Capítulo 5. Determinación de constantes de ionización Se determinaron las constantes de ionización de diversos compuestos mediante curvas de titulación ácido-base empleando métodos espectrofotométricos
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
PREPARACION DE MEDIOS DE CULTIVO
 PREPARACION DE MEDIOS DE CULTIVO MEDIOS DE CULTIVO Un medio de cultivo es un conjunto de nutrientes, factores de crecimiento y otros componentes que crean las condiciones necesarias para el desarrollo
PREPARACION DE MEDIOS DE CULTIVO MEDIOS DE CULTIVO Un medio de cultivo es un conjunto de nutrientes, factores de crecimiento y otros componentes que crean las condiciones necesarias para el desarrollo
Proyecto de Fin de Cursos
 Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
Grado en Química. 4º Curso Bioquímica. Guión de Prácticas
 Grado en Química 4º Curso Bioquímica Guión de Prácticas UTILES A TRAER POR EL ALUMNO Bata Gafas de Seguridad Cuaderno de Laboratorio NORMAS DE TRABAJO Antes de empezar Antes de empezar cada práctica, el
Grado en Química 4º Curso Bioquímica Guión de Prácticas UTILES A TRAER POR EL ALUMNO Bata Gafas de Seguridad Cuaderno de Laboratorio NORMAS DE TRABAJO Antes de empezar Antes de empezar cada práctica, el
QUÍMICA BIOLÓGICA GUÍA DE PROBLEMAS Nº3 VI-CINÉTICA ENZIMÁTICA
 QUÍMICA BIOLÓGICA GUÍA DE PROBLEMAS Nº3 VI-CINÉTICA ENZIMÁTICA 1. Para estudiar una reacción enzimática se preparó una serie de tubos con diferentes concentraciones de sustrato y una cantidad constante
QUÍMICA BIOLÓGICA GUÍA DE PROBLEMAS Nº3 VI-CINÉTICA ENZIMÁTICA 1. Para estudiar una reacción enzimática se preparó una serie de tubos con diferentes concentraciones de sustrato y una cantidad constante
QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A
 1. (2,5 puntos) QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A Las entalpías estándar de combustión del C(s), H 2 (g) y propano gas, C 3 H 8 (g), son -394, -286 y -2220 kj/mol, respectivamente: i. Calcule la entalpía
1. (2,5 puntos) QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A Las entalpías estándar de combustión del C(s), H 2 (g) y propano gas, C 3 H 8 (g), son -394, -286 y -2220 kj/mol, respectivamente: i. Calcule la entalpía
38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa
 38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa José Luis Caballero Repullo, Enriqueta Moyano, Juan Muñoz Blanco Departamento de Bioquímica y Biología Molecular, Campus
38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa José Luis Caballero Repullo, Enriqueta Moyano, Juan Muñoz Blanco Departamento de Bioquímica y Biología Molecular, Campus
Sistema Integrado de Gestión RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS PROGRAMAS DE DEPORTE Y FISIOTERAPIA GUIA PRÁCTICA N 6
 Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
Inmunología Clínica T.P.Nº4 2009
 Inmunología Clínica T.P.Nº4 2009 Separación de Inmunoglobulinas Separación n de Inmunoglobulinas Métodos basados en la diferencia de solubilidad Métodos basados en el tamaño molecular Métodos basados en
Inmunología Clínica T.P.Nº4 2009 Separación de Inmunoglobulinas Separación n de Inmunoglobulinas Métodos basados en la diferencia de solubilidad Métodos basados en el tamaño molecular Métodos basados en
ELABORACIÓN N DE MEZCLA PARA PCR. Raquel Asunción Lima Cordón
 ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
DETERMINACIÓN CUANTITATIVA DE PROTEINAS
 DETERMIAIÓ UATITATIVA DE PRTEIAS bjetivos: Al finalizar este trabajo práctico los alumnos estarán en capacidad de: - onocer el principio que rige la espectrofotometría. - Interpretar el basamento químico
DETERMIAIÓ UATITATIVA DE PRTEIAS bjetivos: Al finalizar este trabajo práctico los alumnos estarán en capacidad de: - onocer el principio que rige la espectrofotometría. - Interpretar el basamento químico
MANUAL DE PRÁCTICAS DE LABORATORIO
 MANUAL DE PRÁCTICAS DE LABORATORIO INGENIERIA ENBIOTECNOLOGÍA INGENIERÍA GENÉTICA FICHA TECNICA FICHA TÉCNICA SEMINARIO DE BIOTECNOLOGÍA MÉDICO-FARMACÉUTICA Fecha: Nombre del catedrático: 10-Julio-2012
MANUAL DE PRÁCTICAS DE LABORATORIO INGENIERIA ENBIOTECNOLOGÍA INGENIERÍA GENÉTICA FICHA TECNICA FICHA TÉCNICA SEMINARIO DE BIOTECNOLOGÍA MÉDICO-FARMACÉUTICA Fecha: Nombre del catedrático: 10-Julio-2012
Trabajo Práctico N 3. Reconocimiento de sustancias ácidas, básicas y neutras. mediante el empleo de indicadores químicos.
 Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
Conceptos y técnicas en ecología fluvial
 Conceptos y técnicas en ecología fluvial Edición a cargo de: ARTURO ELOSEGI Profesor titular de Ecología en la Universidad del País Vasco SERGI SABATER Catedrático de Ecología en la Universidad de Girona
Conceptos y técnicas en ecología fluvial Edición a cargo de: ARTURO ELOSEGI Profesor titular de Ecología en la Universidad del País Vasco SERGI SABATER Catedrático de Ecología en la Universidad de Girona
CARPETA DE TRABAJOS PRÁCTICOS DE QUÍMICA BIOLÓGICA II
 CARPETA DE TRABAJOS PRÁCTICOS DE QUÍMICA BIOLÓGICA II Profesor: Dr. Osvaldo León Córdoba J.T.P: Bioq. María Andrea Abalos Aux. 1ra: Bioq. Mónica Beatriz Becerra REGLAMENTO DE QUIMICA BIOLOGICA II 2010
CARPETA DE TRABAJOS PRÁCTICOS DE QUÍMICA BIOLÓGICA II Profesor: Dr. Osvaldo León Córdoba J.T.P: Bioq. María Andrea Abalos Aux. 1ra: Bioq. Mónica Beatriz Becerra REGLAMENTO DE QUIMICA BIOLOGICA II 2010
Electroforesis en gel de poliacrilamida y electrotransferencia
 Electroforesis en gel de poliacrilamida y electrotransferencia INDICE ELECTROFORESIS Fundamento y características Tipos de electroforesis: libre y de zona Electroforesis en papel, acetato de celulosa Electroforesis
Electroforesis en gel de poliacrilamida y electrotransferencia INDICE ELECTROFORESIS Fundamento y características Tipos de electroforesis: libre y de zona Electroforesis en papel, acetato de celulosa Electroforesis
CONTENIDO DE HIERRO EN LAS LECHES DE FORMULA EMPLEADAS EN LA ALIMENTACIÓN INFANTIL: DISTRIBUCION EN EL SUERO LACTEO Y EN LA GRASA
 CONTENIDO DE HIERRO EN LAS LECHES DE FORMULA EMPLEADAS EN LA ALIMENTACIÓN INFANTIL: DISTRIBUCION EN EL SUERO LACTEO Y EN LA GRASA R. Domínguez 3,1, J.M. Fraga 1,2, J.A. Cocho 1,2, P. Bermejo 3, A. Bermejo
CONTENIDO DE HIERRO EN LAS LECHES DE FORMULA EMPLEADAS EN LA ALIMENTACIÓN INFANTIL: DISTRIBUCION EN EL SUERO LACTEO Y EN LA GRASA R. Domínguez 3,1, J.M. Fraga 1,2, J.A. Cocho 1,2, P. Bermejo 3, A. Bermejo
Manual de Uso (Ref /2)
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu Diseñado para la purificación
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu Diseñado para la purificación
PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERMINACIÓN DE LA MASA MOLECULAR DE UN SOLUTO PROBLEMA POR CRIOSCOPIA
 PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERINACIÓN DE LA ASA OLECULAR DE UN SOLUTO PROBLEA POR CRIOSCOPIA OBJETIVOS: El objetivo de la práctica es el estudio del efecto que produce la adición de un soluto
PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERINACIÓN DE LA ASA OLECULAR DE UN SOLUTO PROBLEA POR CRIOSCOPIA OBJETIVOS: El objetivo de la práctica es el estudio del efecto que produce la adición de un soluto
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
Reacciones redox espontáneas
 Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
Celda galvánica o voltaica o electroquímica Pila galvánica o voltaica o electroquímica Cuba galvánica o voltaica o electroquímica Cada una de las partes se denomina: semicelda o semipila o electrodo Pila
EXTRACCIÓN Y CUANTIFICACION DEL ARN DE LA LEVADURA
 EXTRACCIÓN Y CUANTIFICACION DEL ARN DE LA LEVADURA Objetivos: Al finalizar el trabajo práctico los cursantes estarán en capacidad de: - Extraer ARN a partir de células de levadura. - Realizar la hidrólisis
EXTRACCIÓN Y CUANTIFICACION DEL ARN DE LA LEVADURA Objetivos: Al finalizar el trabajo práctico los cursantes estarán en capacidad de: - Extraer ARN a partir de células de levadura. - Realizar la hidrólisis
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS
 PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
Electroforesis de proteínas en geles de poliacrilamida. Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica
 Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
3.1. Cuantificación de proteínas totales. 3.2. Técnicas de separación de proteínas. Análisis de proteínas específicas.
 TEMA 3: Métodos para el análisis de proteínas 3.1. Cuantificación de proteínas totales. 3.2. Técnicas de separación de proteínas. Análisis de proteínas específicas. INTRODUCCIÓN A lo largo de este tema
TEMA 3: Métodos para el análisis de proteínas 3.1. Cuantificación de proteínas totales. 3.2. Técnicas de separación de proteínas. Análisis de proteínas específicas. INTRODUCCIÓN A lo largo de este tema
MANUAL FAR 516 L DEL PERFIL
 BENEMÉRITA UNIVERSIDAD AUTÓNOMAA DE PUEBLA FACULTAD DE CIENCIAS QUÍMICAS LICENCIATURA: FARMACIAA ÁREA ESPECÍFICA DE: FARMACIA NOMBRE DE LA ASIGNATURA: CÓDIGO: FECHA DE ELABORACIÓN: NIVEL EN EL MAPA CURRICULAR:
BENEMÉRITA UNIVERSIDAD AUTÓNOMAA DE PUEBLA FACULTAD DE CIENCIAS QUÍMICAS LICENCIATURA: FARMACIAA ÁREA ESPECÍFICA DE: FARMACIA NOMBRE DE LA ASIGNATURA: CÓDIGO: FECHA DE ELABORACIÓN: NIVEL EN EL MAPA CURRICULAR:
EL AGUA Y LAS SALES MINERALES
 EL AGUA Y LAS SALES MINERALES 1. EL AGUA DE LA MATERIA VIVA El agua es la molécula más abundante de la materia viva La cantidad de agua en los seres vivos es variable Según el tipo de tejido: más agua
EL AGUA Y LAS SALES MINERALES 1. EL AGUA DE LA MATERIA VIVA El agua es la molécula más abundante de la materia viva La cantidad de agua en los seres vivos es variable Según el tipo de tejido: más agua
TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS. DOCENTES: Dr. Andrés Ciochinni, Dra. Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR
 TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DOCENTES: Dr. Andrés Ciochinni, Dra. Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR Purificación de ácido desoxiribonucleico (ADN). El ADN es un polímero
TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DOCENTES: Dr. Andrés Ciochinni, Dra. Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR Purificación de ácido desoxiribonucleico (ADN). El ADN es un polímero
Titulaciones en Química Analítica. Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D.
 Titulaciones en Química Analítica Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D. Introducción En el análisis volumétrico, la concentración se determina midiendo su capacidad de reaccionar con un reactivo
Titulaciones en Química Analítica Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D. Introducción En el análisis volumétrico, la concentración se determina midiendo su capacidad de reaccionar con un reactivo
PRÁCTICO Nº 4 GLUCOGENOLISIS
 UNIVERSIDAD MAY ESCUELA DE TECNLGIA MEDICA 1 PRÁCTIC Nº 4 GLUCGENLISIS I.- INTRDUCCIÓN La molécula de Hidrato de Carbono más importante desde el punto de vista fisiológico es la Glucosa, la cual se clasifica
UNIVERSIDAD MAY ESCUELA DE TECNLGIA MEDICA 1 PRÁCTIC Nº 4 GLUCGENLISIS I.- INTRDUCCIÓN La molécula de Hidrato de Carbono más importante desde el punto de vista fisiológico es la Glucosa, la cual se clasifica
31. Extracción y ensayo de la actividad invertasa de levadura de panadería
 31. Extracción y ensayo de la actividad invertasa de levadura de panadería Manuel Tena Aldave, Jesús V. Jorrín Novo Departamento de Bioquímica y Biología Molecular, Campus Universitario de Rabanales, Edificio
31. Extracción y ensayo de la actividad invertasa de levadura de panadería Manuel Tena Aldave, Jesús V. Jorrín Novo Departamento de Bioquímica y Biología Molecular, Campus Universitario de Rabanales, Edificio
EJERCICIOS DE BIOQUÍMICA: BIOELEMENTOS. AGUA Y SALES MINERALES
 EJERCICIOS DE BIOQUÍMICA: BIOELEMENTOS. AGUA Y SALES MINERALES 1) El siguiente cuadro representa el % de agua de ciertos organismos, qué deduces de ello? Por qué crees que es tan bajo el % de agua en las
EJERCICIOS DE BIOQUÍMICA: BIOELEMENTOS. AGUA Y SALES MINERALES 1) El siguiente cuadro representa el % de agua de ciertos organismos, qué deduces de ello? Por qué crees que es tan bajo el % de agua en las
TEMA 3: Equilibrios redox
 TEMA 3: Equilibrios redox Índice 1) Concepto potencial redox. 2) Pila galvánica. 3) Ecuación de Nernst. 4) Espontaneidad y equilibrio. 5) Influencia del ph en el potencial de electrodo. 6) Reacciones de
TEMA 3: Equilibrios redox Índice 1) Concepto potencial redox. 2) Pila galvánica. 3) Ecuación de Nernst. 4) Espontaneidad y equilibrio. 5) Influencia del ph en el potencial de electrodo. 6) Reacciones de
Determinación de la concentración micelar crítica (cmc) y grado de disociación (α) de un tensioactivo iónico mediante medidas de conductividad
 Determinación de la concentración micelar crítica (cmc) y grado de disociación (α) de un tensioactivo iónico mediante medidas de conductividad OBJETIVO: Determinación de la concentración micelar crítica
Determinación de la concentración micelar crítica (cmc) y grado de disociación (α) de un tensioactivo iónico mediante medidas de conductividad OBJETIVO: Determinación de la concentración micelar crítica
EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS
 EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS 1) Qué es un tetrapéptido?. Construye uno, formado por los siguientes aminoácidos: Ala, Cys, Ser y Tyr. 2) Haz corresponder los elementos de las dos columnas: -Cys -Hormona
EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS 1) Qué es un tetrapéptido?. Construye uno, formado por los siguientes aminoácidos: Ala, Cys, Ser y Tyr. 2) Haz corresponder los elementos de las dos columnas: -Cys -Hormona
Investigando los genes FRAUDE CANINO
 FRAUDE CANINO Ahora vamos a actuar como policías científicos. No se trata de un caso humano, sino de perros. El protocolo seguido es similar al de la Huella Genética o Huella de ADN, es decir, vamos a
FRAUDE CANINO Ahora vamos a actuar como policías científicos. No se trata de un caso humano, sino de perros. El protocolo seguido es similar al de la Huella Genética o Huella de ADN, es decir, vamos a
TRBAJO PRÁCTICO N 5: ph. Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes.
 QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRBAJO PRÁCTICO N 5: ph Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes. Fundamentos Teóricos: La mayoría de las reacciones químicas
QUÍMICA GENERAL Y TECNOLÓGICA 2010 TRBAJO PRÁCTICO N 5: ph Objetivo: Determinar el ph de soluciones ácidas y básicas de concentraciones diferentes. Fundamentos Teóricos: La mayoría de las reacciones químicas
CINÉTICA QUÍMICA DETERMINACIÓN DEL ORDEN DE REACCIÓN Y ENERGÍA DE ACTIVACIÓN
 II PRÁCTICA 2 CINÉTICA QUÍMICA DETERMINACIÓN DEL ORDEN DE REACCIÓN Y ENERGÍA DE ACTIVACIÓN En esta experiencia comprobaremos la influencia de la concentración de los reactivos, de la temperatura, y de
II PRÁCTICA 2 CINÉTICA QUÍMICA DETERMINACIÓN DEL ORDEN DE REACCIÓN Y ENERGÍA DE ACTIVACIÓN En esta experiencia comprobaremos la influencia de la concentración de los reactivos, de la temperatura, y de
PRÁCTICA HIGIENE, INSPECCIÓN Y CONTROL DE LA MIEL
 PRÁCTICA HIGIENE, INSPECCIÓN Y CONTROL DE LA MIEL Determinación del contenido de humedad Determinación gravimétrica del contenido de sólidos insolubles en agua Conductividad eléctrica Determinación del
PRÁCTICA HIGIENE, INSPECCIÓN Y CONTROL DE LA MIEL Determinación del contenido de humedad Determinación gravimétrica del contenido de sólidos insolubles en agua Conductividad eléctrica Determinación del
UNIVERSIDAD TECNOLÓGICA METROPOLITANA INGENIERIA EN QUIMICA LABORATORIO ANALISIS INSTRUMENTAL. INFORME N 1: ESPECTROFOTOMETRÍA UV VISIBLE INTRODUCCION
 UNIVERSIDAD TECNOLÓGICA METROPOLITANA INGENIERIA EN QUIMICA LABORATORIO ANALISIS INSTRUMENTAL. INFORME N 1: ESPECTROFOTOMETRÍA UV VISIBLE INTRODUCCION En este laboratorio utilizaremos el método de la espectrofotometría
UNIVERSIDAD TECNOLÓGICA METROPOLITANA INGENIERIA EN QUIMICA LABORATORIO ANALISIS INSTRUMENTAL. INFORME N 1: ESPECTROFOTOMETRÍA UV VISIBLE INTRODUCCION En este laboratorio utilizaremos el método de la espectrofotometría
Estrategias de evaluación de antioxidantes en extractos vegetales
 Estrategias de evaluación de antioxidantes en extractos vegetales Dr. Gustavo E. Zúñiga Laboratorio de Fisiología y Biotecnología Vegetal Departamento de Biología Facultad de Química y Biología Universidad
Estrategias de evaluación de antioxidantes en extractos vegetales Dr. Gustavo E. Zúñiga Laboratorio de Fisiología y Biotecnología Vegetal Departamento de Biología Facultad de Química y Biología Universidad
TEMA 6. PURIFICACIÓN DE PROTEÍNAS
 TEMA 6. PURIFICACIÓN DE PROTEÍNAS 1. Introducción 2. Métodos de rotura celular y extracción de proteínas 3. Métodos cromatográficos 4. Métodos electroforéticos 1. Introducción La mayor parte de las investigaciones
TEMA 6. PURIFICACIÓN DE PROTEÍNAS 1. Introducción 2. Métodos de rotura celular y extracción de proteínas 3. Métodos cromatográficos 4. Métodos electroforéticos 1. Introducción La mayor parte de las investigaciones
AMINOÁCIDOS SE PUEDEN UNIR POR ENLACES PEPTÍDICOS
 Tema 4. Proteínas: funciones biológicas y estructura primaria. Enlace peptídico. Péptidos y proteínas. Diversidad de funciones biológicas. Niveles de organización estructural de las proteínas. Separación
Tema 4. Proteínas: funciones biológicas y estructura primaria. Enlace peptídico. Péptidos y proteínas. Diversidad de funciones biológicas. Niveles de organización estructural de las proteínas. Separación
PRÁCTICA 4: ANÁLISIS DE PROTEÍNAS
 PRÁCTICA 4: ANÁLISIS DE PROTEÍNAS 1. DETERMINACIÓN DE LA PROTEÍNA BRUTA POR EL MÉTODO DE KJELDAHL. 1.1. FUNDAMENTO: En los análisis de rutina se suele determinar el contenido de nitrógeno total y expresar
PRÁCTICA 4: ANÁLISIS DE PROTEÍNAS 1. DETERMINACIÓN DE LA PROTEÍNA BRUTA POR EL MÉTODO DE KJELDAHL. 1.1. FUNDAMENTO: En los análisis de rutina se suele determinar el contenido de nitrógeno total y expresar
IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006
 IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006 REACCION EN CADENA DE LA POLIMERASA (PCR) EN EL DIAGNOSTICO DE Campylobacter jejuni/coli Viernes 19 de mayo María Rosa Viñas Servicio
IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006 REACCION EN CADENA DE LA POLIMERASA (PCR) EN EL DIAGNOSTICO DE Campylobacter jejuni/coli Viernes 19 de mayo María Rosa Viñas Servicio
Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a
 Introducción Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a los investigadores verificar la expresión de una proteína, determinar la cantidad relativa
Introducción Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a los investigadores verificar la expresión de una proteína, determinar la cantidad relativa
CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO. Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión
 EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
PRACTICO N 1: ESPECTROFOTOMETRIA
 UNIVERSIDAD MAYOR FACULTAD DE MEDICINA ESCUELA DE TECNOLOGIA MEDICA BIOQUIMICA PRACTICO N 1: ESPECTROFOTOMETRIA 1.- INTRODUCCIÓN Utilizando términos quizás excesivamente simplistas puede definirse la espectrofotometría
UNIVERSIDAD MAYOR FACULTAD DE MEDICINA ESCUELA DE TECNOLOGIA MEDICA BIOQUIMICA PRACTICO N 1: ESPECTROFOTOMETRIA 1.- INTRODUCCIÓN Utilizando términos quizás excesivamente simplistas puede definirse la espectrofotometría
Cuantificación de Clorofila a
 Cuantificación de Clorofila a Clorofilas Las clorofilas son una familia de pigmentos de color verde que se encuentran en las cianobacterias y en todos aquellos organismos que contienen cloroplastos en
Cuantificación de Clorofila a Clorofilas Las clorofilas son una familia de pigmentos de color verde que se encuentran en las cianobacterias y en todos aquellos organismos que contienen cloroplastos en
TRABAJO PRACTICO Nº2 RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS
 1 TRABAJO PRACTICO Nº2 RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS I) Péptidos Los aminoácidos pueden condesarse entre sí, uniéndose a través del grupo carboxilo de un aminoácido al grupo amino de otro
1 TRABAJO PRACTICO Nº2 RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS I) Péptidos Los aminoácidos pueden condesarse entre sí, uniéndose a través del grupo carboxilo de un aminoácido al grupo amino de otro
15. Electroforesis: electroforesis en papel de proteínas séricas
 15. Electroforesis: electroforesis en papel de proteínas séricas Isaac Túnez Fiñana Departamento de Bioquímica y Biología Molecular, Facultad de Medicina, Universidad de Córdoba, Avda. Menéndez Pidal s/n,
15. Electroforesis: electroforesis en papel de proteínas séricas Isaac Túnez Fiñana Departamento de Bioquímica y Biología Molecular, Facultad de Medicina, Universidad de Córdoba, Avda. Menéndez Pidal s/n,
ANEXO I. Inmunofenotipificación Celular por Citometría de Flujo
 ANEXO I Inmunofenotipificación Celular por Citometría de Flujo Reactivos Anticuerpos monoclonales fluoromarcados (BD Bioscience Pharmingen) Medio DMEM con 0.02% de azida de sodio Paraformaldehido (PFA)
ANEXO I Inmunofenotipificación Celular por Citometría de Flujo Reactivos Anticuerpos monoclonales fluoromarcados (BD Bioscience Pharmingen) Medio DMEM con 0.02% de azida de sodio Paraformaldehido (PFA)
BIOQUÍMICA ESTRUCTURAL Y BIOLÓGICA José Carlos Rodríguez Rey, Javier León Serrano, Mª Dolores Delgado Villar y Jesús Navas Méndez
 PRÁCTICA 3 VALORACIÓN DE LA DIABETES: DETERMINACIÓN DE LA GLUCEMIA Y HEMOGLOBINAS GLUCOSILADAS 1. Introducción general El mantenimiento de la glucemia, (concentración de glucosa en suero o plasma) dentro
PRÁCTICA 3 VALORACIÓN DE LA DIABETES: DETERMINACIÓN DE LA GLUCEMIA Y HEMOGLOBINAS GLUCOSILADAS 1. Introducción general El mantenimiento de la glucemia, (concentración de glucosa en suero o plasma) dentro
1. CROMATOGRAFÍA EN DEAE-CELULOSA para purificar la glutamina sintetasa.
 INTRODUCCIÓN En el primer módulo de la asignatura Técnicas Experimentales en Bioquímica llevaremos a cabo el estudio de una proteína determinada, para ello se realizará el protocolo de laboratorio habitual
INTRODUCCIÓN En el primer módulo de la asignatura Técnicas Experimentales en Bioquímica llevaremos a cabo el estudio de una proteína determinada, para ello se realizará el protocolo de laboratorio habitual
Módulo 1 Biología Molecular Genética Molecular II 2009. Módulo 1. Amplificación de un fragmento de ADN genómico por PCR
 Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
DANAGENE RNA PURIFICATION KIT
 DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
CARACTERIZACIÓN CINÉTICA DE LA ENZIMA FOSFATASA ÁCIDA DEL EXTRACTO CRUDO DE PAPA
 FACULTAD CIENCIAS SILVOAGROPECUARIAS LABORATORIO ASIGNATURA DE BIOQUÍMICA. PLAN COMÚN AGRONOMÍA E INGENIERÍA FORESTAL TRABAJO PRÁCTICO Nº3 CARACTERIZACIÓN CINÉTICA DE LA ENZIMA FOSFATASA ÁCIDA DEL EXTRACTO
FACULTAD CIENCIAS SILVOAGROPECUARIAS LABORATORIO ASIGNATURA DE BIOQUÍMICA. PLAN COMÚN AGRONOMÍA E INGENIERÍA FORESTAL TRABAJO PRÁCTICO Nº3 CARACTERIZACIÓN CINÉTICA DE LA ENZIMA FOSFATASA ÁCIDA DEL EXTRACTO
