EFECTO IN VIVO DE PROLACTINA Y EL COPEPTIN DE ISOTOCINA SOBRE LA RESPUESTA DE Salmo salar AL PATOGENO BACTERIANO Piscirickettsia salmonis
|
|
|
- José Manuel Cordero Méndez
- hace 8 años
- Vistas:
Transcripción
1 Profesor Patrocinante Dr. Jaime Figueroa V. Instituto de Bioquímica y microbiología Facultad de Ciencias EFECTO IN VIVO DE PROLACTINA Y EL COPEPTIN DE ISOTOCINA SOBRE LA RESPUESTA DE Salmo salar AL PATOGENO BACTERIANO Piscirickettsia salmonis Tesis de Grado presentada como parte de los requisitos para optar al grado de Licenciado en Bioquímica y Título Profesional de Bioquímico MARINA LORENA OJEDA OJEDA VALDIVIA - CHILE 2011
2 II AGRADECIMIENTOS Al Dr. Jaime Figueroa, por acogerme en su laboratorio, por todo su tiempo, paciencia y conocimientos que me brindó durante el desarrollo de esta tesis, además de su estímulo, comprensión y apoyo en esta etapa de mi vida. Agradezco también al Dr. Alejandro Reyes y Dr. Hugo Folch Vilches, por acceder a formar parte de mi comisión evaluadora. A mis compañeros (as) y amigos (as) de laboratorio quienes me entregaron de una u otra forma su apoyo y experiencia en el desarrollo de este trabajo. La presente tesis se llevó a cabo en el Laboratorio de Biología Molecular de Peces del Instituto de Bioquímica y microbiología, Facultad de Ciencias, Universidad Austral de Chile y fue financiado por los proyectos FONDECYT
3 III..Dedico esta tesis a mis padres que me han dado todo en la vida, a mis hermanos por ayudarme y acompañarme siempre. A mí amado Alexei que siempre me ha apoyado. A mi pequeño hijo que me brinda su incondicional amor y es para mí la persona que más admiro, por su fuerza, valor y entereza para enfrentar la vida, sorprendiéndome siempre
4 IV INDICES DE CONTENIDOS 1 RESUMEN 1 SUMMARY 2 2 INTRODUCCION 3 3 MATERIALES Y METODOS Materiales Reactivos Soluciones Softwares Anticuerpos Anticuerpo anti-igm de Salmón/Trucha Anti copeptin de carpa (Cyprinus Carpio) hecho en conejo, Lab. Biología Molecular Peces Anticuerpo anti-prl METODOS Purificación de copeptin de Salmo salar Obtención de las hipófisis de Salmo salar (para purificar copeptin) Extracción Ácida Cromatografía de filtración en gel Cromatografía de intercambio iónico. 19
5 V Cuantificación de proteínas mediante el método de Bradford Electroforesis en geles de poliacrilamida Análisis por Western Blot Evaluación in vivo de PRL, copéptido de Isotocina y PBS sobre la respuesta de S.salar frente a P. salmonis Animales de experimentación Extracción de macrófagos renales Elaboración del gradiente discontinuo de Percoll Separación de las fracciones celulares Conteo y evaluación de la viabilidad de los leucocitos Evaluación de la producción del anión superoxido Extracción de plasma Electroforesis en geles de poliacrilamida condiciones nativas Análisis de electrotransferencia para geles de poliacrilamida en condiciones nativas Cuantificación de inmunorreactividad Ensayo de actividad de lizosimas Inmunohistoquímica Material biológico Fijación de los cortes histológicos. 26
6 VI Inmunohistoquímica cromogénica Cuantificación de la inmunorreacción RESULTADOS Purificación del copeptin de Salmo salar Expresión diferencial del copeptin asociado a Isotocina en hipófisis de S. salar desafiados con patógenos bacterianos Expresión de prolactina en hipófisis de salmones sanos y desafiados a patógenos Expresión del copeptin en hipófisis de salmones sanos y desafiados a patógenos Evaluación in vivo de PRL, Copéptido de Isotocina y PBS sobre la respuesta de Salmo salar frente a P. salmonis Efecto in vivo de PRL en macrófagos de cabeza de riñón de S. salar Evaluación de los niveles plasmáticos de IgM de peces inyectados con PRL, copeptin, PBS y desafiados con P. salmonis Evaluación de los niveles plasmáticos de lizosima en peces inyectados con PRL, copeptido y PBS desafiados con Piscirickettsia salmonis DISCUSION BIBLIOGRAFIA 62
7 VII INDICE DE FIGURAS Figura 1.- Esquema demostrativo de la composición del precursor de Isotocina. 11 Figura 2.- Esquema explicativo de la precipitación del copeptin con solventes orgánicos y medio acido. 29 Figura 3.- Cromatografía de filtración en gel (Sephadex G-25). 30 Figura 4.- Cromatografía de intercambio aniónico en DEAE-Celulosa. 31 Figura 5.- Electroforesis en gel de poliacrilamida en condiciones denaturantes de neurofisina-copeptin purificado a partir de pituitaria de salmón. 33 Figura 6.- Expresión de PRL en pituitaria de peces adultos y alevines sobrevivientes al desafío con patógenos (R. salmoninarum y P. salmonis). 35 Figura 7.-Análisis semi-cuantitativo de PRL en pituitarias de salmón, adultos y alevines sobrevivientes al desafío con patógenos, R. salmoninarum y P. salmonis. 37 Figura 8.- Inmunodetección de Cp en RPD de pituitaria de peces adultos y alevines sobrevivientes al desafío con patógenos (R. salmoninarum y P. salmonis). 38 Figura 9.- Análisis semi-cuantitativo de copeptin en pituitarias de salmón, adultos y alevines sobrevivientes al desafío con patógenos, R. salmoninarum y P. salmonis. 41 Figura 10.- Medición del anión superoxido en macrófagos renales de cabeza de riñón. 43
8 VIII Figura 11.- Efecto in vivo de prolactina y copeptin en salmones desafiados con P. salmonis, sobre los niveles plasmáticos de IgM. 47 Figura 12.- Efecto en in vivo de prolactina y el copeptido en los niveles plasmáticos de lisozimas. 48 Figura 13: Grafico de correlaciones. 51
9 IX LISTA DE ABREBIATURAS AVP BKD Cp DAB GnRH IgD IgM MHC NBT Np NPO PAP PBS PMA PRL RPD SDS-PAGE SRS Arginina vasopresina Enfermedad bacteriana del Riñón copeptin diaminobencidina hormona liberadora de gonadotropina inmunoglobulina D inmunoglobulina M complejo mayor de histocompatibilidad Nitro Blue Tetrazolium neurofisina núcleo preóptico complejo peroxidasa anti peroxidasa tampón fosfato salino Phorbol myristate acetate Prolactina rostral pars distalis Electroforesis en geles desnaturantes Sindrome Rickettsial del salmón
10 X TRH Hormona liberadora de tirotropina
11 1 1. RESUMEN Prolactina (PRL), es una hormona polipeptídica de 25 kda sintetizada y secretada principalmente por las células especializadas de la hipófisis anterior denominada lactotropicas. A esta hormona se le atribuyen una serie de funciones, entre ellas se encuentra la modulación del sistema inmune, tanto en mamíferos como peces. Con respecto al mecanismo de liberación de la hormona desde la hipófisis, se ha descrito que el motivo polipeptídico copeptin, que se encuentra presente en los precursores de isotocina/vasotocina y vasopresina, posee una actividad liberadora de PRL. En el presente trabajo fue desarrollado un protocolo de purificación de copeptin a partir de pituitarias de S. salar, mediante el uso de extracciones con acetona ácida y cromatografías de filtración molecular e intercambio aniónico. Análisis de SDS-PAGE y Western-blot permiten establecer un buen grado de pureza de este polipeptido. Luego se utilizó este polipéptido y prolactina para evaluar la respuesta inmune in vivo de salmones desafiados con Piscirickettsia salmonis, midiendo ciertos parámetros inmunes, como niveles de IgM plasmática, la producción de anión superoxido y los niveles de lisozimas, evidenciando una posible acción moduladora de prolactina. Adicionalmente, se cuantificó por inmunohistoquímica cromogénica la presencia del copeptin en la región de la rostral pars distalis (RPD) de pituitarias, lugar donde ocurre la síntesis de prolactina. Esta evaluación se efectuó en peces sanos (adultos) y desafiados con patógenos bacterianos, observándose una diferencia significativa entre ambos grupos de peces.
12 2 SUMMARY Prolactin (PRL) is a 25 kda polypeptide hormone synthesized and secreted primarily by lactotrophs which are specialized cells located in the anterior pituitary gland. This hormone has a number of functions, one of them being the modulation of immune system in both animal and fish. The mechanism by which this hormone is released from hypofisis involves a copeptin motif. This motif is also found in precursors of isotocin/vasotocin and vasopressin which also show a prolactin releasing activity. In the present work, we developed a copeptin purification protocol from Salmon salar pituitary cells. The extraction was made using acid acetone and molecular filtration or anion exchange chromatography. Analysis, by SDS-page and western blot showed high purity of the polypeptide. The purified polypeptide and prolactine were used to evaluate the immune response in vivo of salmons which were defied with Piscirickettsia salmonis. Measure of the serum levels of IgM, superoxide anion and lysozyme suggested a possible modulatory role of prolactine. Additionally, chromogenic immunohistochemestry was used to quantify the presence of copeptin in the rostral pars distalis (RPD) region of pituitary glands, where prolactine is syntetized. Experiments conducted with healthy fish (adults) and fish infected by bacterial pathogens, showed statistically significant differences.
13 3 2. INTRODUCCIÓN Prolactina (PRL), es una hormona polipeptídica de 25 kda sintetizada y secretada principalmente por las células especializadas de la hipófisis anterior, denominadas lactotrópicas. Fue descrita por primera vez en 1928 y su nombre se debe a las observaciones de que un extracto de la glándula hipofisaria puede promover la lactancia en conejos. Posteriormente, se identificó que prolactina participa en el desarrollo de la glándula mamaria y en la producción de las proteínas de la leche en el embarazo y post-parto en mamíferos (Freeman et al., 2000). En la actualidad se sabe que ella está relacionada en más de 300 funciones biológicas, que no poseen relación con la lactancia o el área reproductiva, como son regular el equilibrio de agua y electrolitos en el riñón, intestino y placenta, estimular el desarrollo y proliferación celular de una serie de órganos, como el hígado, piel y páncreas entre otros (Bole-Feysot et al., 1998; Freeman et al., 2000). En la actualidad en la literatura existe evidencia consistente de que prolactina estaría influenciando el sistema inmune. Este sistema se encuentra formado por distintos tipos de células que provienen de una célula progenitora común o célula madre, éstas son producidas en la medula ósea para luego pasar por procesos de diferenciación en la misma medula ósea o en el timo dando origen a distintos tipos celulares que poseen características y funciones específicas, como son los linfocitos T, los linfocitos B y los monocitos entre otras. El sistema inmune tiene como función desarrollar mecanismos de protección del organismo frente al ataque de agentes ambientales extraños; estos pueden ser microorganismos o sus productos, alimentos, químicos, polen etc. Este sistema actúa frente al ataque con complejas adaptaciones que involucran al sistema inmune y neuroendocrino respectivamente, en especial componentes del eje hipotálamo-hipófisis-adrenal, actuando de forma conjunta. La idea de la comunicación intercelular entre ambos sistemas, hoy en día se encuentra aceptada
14 4 completamente. Existen estudios que avalan dicha interacción y que establecen que podría ser una comunicación tanto dentro como entre el sistema inmune y neuroendocrino, utilizando para este fin receptores y moléculas de señalización (citoquinas) que se comparten en ambos sistemas. Se ha demostrado, que en mamíferos diferentes células inmunológicas producen péptidos sintetizados por órganos del sistema neuroendocrino entre ellos el hipotálamo y la hipófisis. Tanto la estructura como el patrón de síntesis de estos péptidos por leucocitos son casi igual que los producidos por este sistema (Weigent & Blalock, 1995; Davis, 1998; Buckley, 2001). Como primera evidencia de esta síntesis en 1980 se encontró que linfocitos infectados con un virus producían una proteína que compartía antigenicidad y bioactividad con ACTH (Weigent & Blalock, 1995). Poco tiempo después se identificó que también eran fuente de TSH, PRL, GH, beta-endorfinas, entre otras hormonas. De la misma forma se ha visto que células del timo igual producen hormonas hipotalámicas como vasopresina, oxitocina y la producción inversa de péptidos inmunitarios, como citoquinas e interleuquinas por células de la hipófisis (Dan & Lall, 1998). Al ser prolactina una hormona de origen hipofisiario, realiza sus efectos biológicos a través de su interacción con su receptor, el cual se encuentra distribuido en diferentes células del organismo como células blancos son las de la gandula mamaria, ovarios, células del sistema nervioso central, las células del bazo, hígado, páncreas, riñón, útero, glándula adrenal (Freeman et al., 2000) y células T, B y macrófagos (Clevenger et al., 1998, Clevenger & Kline, 2001). La síntesis de prolactina no se encuentra limitada a la hipófisis sino que está demostrado que varias células del sistema inmunológico sintetizan esta hormona, entre ella se puede contar las células del estroma de la medula ósea, las células mononucleares de sangre periférica (linfocitos y monocitos) y los timocitos (Montgomery, 2001). Se identificó también su
15 5 producción en varias líneas celulares, provenientes de cáncer y tumores. La línea celular T Jurkat, derivada de leucemia aguda de células T, expresa el mrna de prolactina y libera la proteína de 23,5 kda junto a varias de sus isoformas. Un número igual de estudios detectaron el mrna de PRL en tejidos inmunes humanos, semejantes al timo, bazo, nódulos linfáticos, amígdalas. De esta forma, se demostró que el transcripto de prolactina se expresa constitutivamente in vivo (Montgomery, 2001; Welniak et al., 2001). El efecto biológico de prolactina sobre el sistema inmunológico fue demostrado por primera vez cuando linfocitos de sangre periférica humana, requerían prolactina para su proliferación in vitro. Así mismo se observó que anticuerpos antiprolactina inhibían profundamente la proliferación de células linfoides en presencia de mitogénos específicos de células B y T, tales como IL-2 e IL-4; la adición de PRL revertía esta situación en cultivos de linfocitos, no así hormona del crecimiento. Esta capacidad de PRL pone en manifiesto su especificidad (Hartmann et al., 1989; Clevenger et al., 1990). También se observó la presencia de una molécula en el medio de cultivo de esplenocitos murinos (linfocitos obtenidos de bazo) que inducían la proliferación de la línea celular derivada de linfoma de rata Nb2 que es dependiente de prolactina para proliferar (Ali et al., 1991). Prolactina actúa igualmente en el sistema inmune como un factor de diferenciación para las células natural killer. (Buckley, 2001; Sun et al., 2004). Todas estas evidencias ponen en manifiesto la participación de prolactina en el sistema inmune jugando un importante rol como citoquina en una posible comunicación entre ambos sistemas. En la actualidad el estudio de las funciones de prolactina no solamente se encuentra enfocado hacia los mamíferos sino también se está evaluando sus efectos en otras especies. En teleósteos, existe una variedad de artículos que demuestran que prolactina juega un papel fundamental en su fisiología, en procesos relacionados con la osmorregulación, principalmente
16 6 durante la adaptación a agua dulce (Kelly et al., 1999 Hirano, 1986; Sandra et al., 2000; Yada et al., 1991; Davis, 1998; McCormick, 2001; Manzon, 2002). En salmónidos como el salmón coho (Oncorhynchus kisutch) se observó un aumento en los niveles plasmático de prolactina cuando se traslada peces adultos desde agua salada a agua dulce (Sakamoto et al., 1991). En cambio cuando se transfieren desde agua dulce a agua salada especímenes de salmón amago (Oncorhynchus rhodurus), se produce una disminución de los niveles plasmáticos de la hormona. Esto apoya la acción de prolactina para mantener la homeostasis en peces. También está descrito que es la hormona hipofisiaria mayormente afectada por los cambios en el medio ambiente, observándose que en el pez C. carpio un aumento significativo de su síntesis y expresión de mrna durante la estación cálida (Figueroa et al., 1994, 1997). En peces, el sistema inmunológico puede ser dividido en innato o inespecífico y adquirido o específico, donde el innato se encuentra altamente desarrollado, existiendo macromoléculas elementales que aumentan la función defensiva de esta barrera primaria. Diversos autores han descrito la presencia y actividad de lizosimas en el mucus y la piel de varios peces, tanto así que se ha observado que el mucus de la trucha arco iris es capaz de lisar células de V. anguillarum (Hjelmeland et al., 1983) y recientemente se ha identificado también la presencia de calicreína, una serina proteasa en la piel de carpa y en el mucus del salmón (Figueroa et al., 2002). Por otro lado, se ha verificado la presencia de factores inducibles durante la respuesta inmune en peces, como mediadores inflamatorios, de los cuales los que se encuentran especialmente caracterizados son citoquinas, particularmente interleuquina 1, interleuquina 6 y el factor de necrosis tumoral alfa (Engelsma et al., 2002). Factores de coagulación (fibrinogeno), proteínas de unión a hemoglobina, (haptoglobina), antioxidantes (ceruloplasmina) y antiproteasas (α 1 antitripsina, α 2 macroglobulina), también se han identificado en teleósteos y recientemente se ha descrito la
17 7 presencia de proteínas de fase aguda, como la proteína C y la proteína ameloide A (Watts, et al., 2001). La evidencia de un sistema inmune adquirido en peces es la presencia de inmunoglobulinas, receptores de células T. En trucha arco-iris se ha clonado y secuenciado los genes que codifican para los polipéptidos alfa y beta del receptor de las células T. En peces, a través de estudios funcionales o reacciones con anticuerpos monoclonales, han sido identificadas las células que participan en la respuesta inmune adquirida, células B (B1 y B2) y T (helper y citotóxicas). Además la función de macrófagos, como células presentadoras de antígenos está bien documentada. Con respecto a la producción de inmunoglobulinas en peces, solamente se han descrito dos formas, la IgM e IgD; esta última en el salmón del Atlántico y trucha arco iris (Watts, et al., 2001; Ohta & Flajnik, 2006). En teleósteos el conocimiento respecto al efecto del sistema neuroendocrino en relación al sistema inmune es muy escaso y la función específica de prolactina sobre el sistema inmune de los peces se ha comenzado a estudiar recientemente. Estudios relacionados a este tema han demostrado que cuando se administra prolactina en peces se observa una estimulación en la actividad fagocitaría de los leucocitos (Harris & Bird, 2000). También se observó que aumenta la actividad mitótica de los leucocitos en el salmón (Oncorhynchus keta)) y es necesaria para mantener los niveles de la inmunoglobulina M (IgM) en la trucha arco iris (Oncorhynchus mykiss). De igual forma, se describió que en macrófagos tratados con prolactina aumentaba la producción intra y extracelular del anión superoxido (Sakai et al., 1996a, 1996b; Yada et al., 1999). La expresión extrapituitaria del gen de prolactina en peces se ha observado en diversos tejidos, como, ovario, hígado, testículos, agallas y bazo (Imaoka et al., 2000).
18 8 En común como en otras hormonas la acción de prolactina es a través de la unión a un receptor específico (RPRL). Los receptores de prolactina fueron identificados en diferentes órganos de tilapia como riñón, agallas, hígado gónadas e intestino (Power, 2005). El receptor fue clonado y aislado por primera vez en tilapia del Nilo (Sandra et al., 1995), posteriormente se ha clonado en varias otras especies de peces, pez dorado, trucha arcoíris entre algunos (Power, 2005). En tejidos hematopoyéticos está descrita su presencia en carpa común (San Martín et al., 2004). Se mencionó anteriormente que prolactina es sintetizada y secretada por diferentes tipos de células, entre ellas, células del sistema inmunológico. También se mencionó que su receptor se encuentra distribuido en varios tejidos. Esto nos indica la versatilidad con lo cual prolactina actúa sobre el organismo, pero en relación a su sistema de liberación, es conocido que la células lactotropicas de la pituitaria anterior producen prolactina de forma constitutiva, pero la secreción de la hormona por dichas células se encuentra regulada por factores hipotalámicos, dentro de los cuales el neurotransmisor dopamina es el más importante, tanto en la secreción, como en la liberación de prolactina por la hipófisis (Freeman et al., 2000). En peces no se conoce mucho sobre los factores reguladores de su liberación, solo se han identificado la hormona liberadora de gonadotropina (GnRH) y la hormona liberadora de tirotropina (TRH) (Barry & Grau. 1986). En 1998, Himura et al. identificaron un nuevo péptido de un extracto de hipotálamo bovino, el que mostraba una específica actividad liberadora de prolactina. Este péptido constaba de dos formas moleculares, un péptido de 31 amino ácidos y otro de 20 residuos (PrPR20). Ese mismo año Fujimoto et al. (1998), aisló un péptido del cerebro de la carpa cruciana y la comparación de su secuencia evidenció que la secuencia aminoacidica era marcadamente homologa a la de bovino (PrPR 20). Posteriormente, se identificó su presencia en extractos de
19 9 cerebro de tilapia y de salmón chum (Moriyama et al., 2002). Conjuntamente a los factores liberadores señalados anteriormente, el motivo C-terminal del precursor de vasopresina en mamíferos, el copeptin, se ha postulado como un posible factor liberador de prolactina, (Nagy et al., 1988). La superfamilia de hormonas vasopresina/oxitocina se encuentra ampliamente distribuida en el reino animal y son sintetizadas en el hipotálamo. Su núcleo está compuesto de un péptido de 9 aminoácidos con varios residuos altamente conservados como son las cisteinas en la posición 1 y 6. Ambas hormonas juegan papeles fundamentales en la fisiología de los seres vivos. Vasopresina actúa principalmente a nivel renal, reabsorbiendo el agua en los riñones y con esto ayudando a mantener los niveles normales de osmolaridad sanguínea. A su vez oxitocina interviene en procesos relacionados con la reproducción, produciendo la contracción uterina durante el parto y participando en la secreción de la leche en la lactancia (Gainer & Wray, 1994). En peces teleósteos, vasopresina/isotocina son respectivamente la contraparte de vasopresina/oxitocina en mamíferos (Heierhorst et al., 1989). También son producidas en el hipotálamo en el núcleo preóptico (NPO) y transportadas a través de los axones neuronales hacia la neurohipófisis. Estas hormonas son sintetizadas como una pre-pro-hormona de 150 residuos aminoacídicos, formada por un péptido señal, la hormona (9 aminoácidos), neurofisina (Np) y un segmento rico en lisinas en el C-terminal denominado copeptin (Cp). A Este motivo copeptin, se le han indicado funciones como liberador de prolactina en mamíferos (Nagy et al., 1988). En mamíferos, el copeptin (figura 1) se encuentra presente sólo en el precursor de vasopresina, ya que el de oxitocina carece de él. También posee una señal de N-glicosilación (por eso se suele denominar glicopéptido) y se encuentra separado de Np, por un sitio de corte para proteasas, representado por una arginina, entre Np y Cp. En cambio en peces ambos precursores
20 10 poseen el motivo copeptin, se encuentra ausente la señal de glicosilación y posiblemente no se encuentre separado de Np por la ausencia del residuo de arginina, conocida señal de corte para el procesamiento proteolítico. Los precursores de las hormonas han sido clonados en varios peces (Heierhorst et al., 1989; Figueroa et al., 1989; Hyodo et al., 1991; Flores et al., 2007). El papel del motivo copeptin, todavía no se encuentra dilucidado completamente, diversos investigaciones han postulado una posible función liberadora de prolactina. Estudios en la carpa común han demostrado que el motivo Cp, no es proteolizado de Np, sino que está unido a ella. También se observó que la incubación de explantes de pituitaria con Cp purificado, resultaba en una estimulación potente de la liberación de prolactina en el medio de cultivo. Adicionalmente con técnicas de inmunohistoquimica se ha observado en pituitaria de carpa una relación morfológica entre Cp y las células productoras de prolactina (Flores et al., 2007). Las investigaciones relacionadas con dilucidar las interacciones entre el sistema neuroendocrino y el sistema inmune en teleósteos, son de suma importancia para la industria del salmón la cual utiliza en su producción el salmón del Atlántico (Salmo salar). Chile se encuentra entre los mayores productores de salmón en el mundo pero, hoy en día esta industria es atacada por una serie de agentes infecciosos que generan cuantiosas pérdidas, provocando una alta mortalidad entre los peces. La manera de controlarlos es a través del uso de altas concentraciones de antibióticos. Esto representa un mecanismo no muy eficaz del control de las infecciones, que también conlleva un riesgo para la salud, como la aparición de nuevas resistencias y la ingesta de estos antibióticos en el consumo humano.
21 11 NH2 * * ± COOH Peptido de señal Isotocina Neurofisina Copeptin Figura 1: Esquema de la composición del precursor de Isotocina, mostrando sus sitios de procesamiento proteolítico. (*) Indica los dos sitios de corte para la formación de la hormona (Vasotocina, oxitocin/isotocina), estos se encuentran en todos los precursores conocidos. (±) El último sitio de corte para la liberación del copeptin sólo se encuentra en los precursores AVP en mamíferos.
22 12 Por esta razón es de vital importancia seguir desarrollando diversas investigaciones con el fin de obtener conocimientos sobre la fisiología a nivel del sistema inmune, de su regulación y potenciales moduladores de sus funciones. Prolactina y su posible rol como una hormona inmuno-moduladora, abre un campo de posibilidades para su uso como una forma de potenciar el sistema inmune de los peces. Además se puede señalar la posible participación del motivo copeptin del precursor de isotocina como un posible factor liberador de prolactina en teleósteos (Flores et al., 2007). Bajo estos antecedentes anteriormente planteados, se formula la hipótesis: El motivo proteico copeptín es capaz de potenciar el efecto inmunomodulador de prolactina sobre el sistema inmune de Salmo salar, frente a patógenos bacterianos, debido a que posee una actividad ligada a la liberación de prolactina. Para probar esta hipótesis, proponemos como objetivo general estudiar el efecto in vivo de PRL y del copéptido liberador de PRL, como moduladores de la respuesta inmune de Salmo salar frente a patógenos bacterianos. Por ello en esta Tesis planteamos desarrollar los siguientes objetivos específicos: (1) Purificar el copeptin asociado a la poliproteína Isotocina. (2) Analizar in vivo la respuesta inmune de los peces tratados con prolactina, copeptin y PBS 1X para lo cual se evaluará una serie de parámetros como niveles de IgM, Actividad de lisozima y generación de anión superoxido en peces desafiados con la bacteria P. salmonis.
23 13 3. MATERIALES Y MÉTODOS 3.1 Materiales Reactivos Acetona, Merck, Darmstadt, Alemania. Ácido acético Equilab. Ácido clorhídrico Caledon. Ácido fosfórico Winkler Ltda. Acrilamida- bisacrilamida 29:1 Winkler Ltda. Albúmina de suero bovino, BSA, Winkler Ltda. Alcohol etílico, Winkler Ltda. Alcohol isopropílico, Baker Chemical Co. Alcohol metílico, Winkler Ltda. Anticuerpo anti IgG conejo: Dako. Anticuerpo anti IgG conejo conjugado a peroxidasa: Dako. Complejo peroxidasa-antiperoxidasa (PAP) hecho en conejo, Rockland Azul de coomassie Sigma Chemical Co. Azul de bromofenol, Sigma Chemical Co. Azul de dextrano, Sigma Chemical Co. Bálsamo de Canadá, Scharlau
24 14 Cloruro de potasio, Winkler Ltda Cloruro de sodio Winkler Ltda DEAE - Celulosa Diaminobenzidina, DAB Sigma Chemical Co DMSO, Winkler Ltda. Dodecil sulfato de sodio, SDS, Winkler Ltda. Etanol, Winkler Ltda. Glicerol, Merck (Darmstadt, Alemania) Glicina, Winkler Ltda. Hidróxido de sodio, Merck (Darmstadt, Alemania). Isopropanol, Winkler Ltda. Leche descremada, CALO Metanol, Winkler Ltda. Marcador de peso molecular rango amplio, preteñido, Winkler Ltda Marcador de peso molecular rango amplio, preteñido, BioLabs NBT, Sigma Chemical Co Percoll, Amersham Pharmacia Biotech AB Perhidrol 30%, H2O2, Merck (Darmstadt, Alemania). Persulfato de amonio, Winkler Ltda
25 15 Sephadex G-25 Temed Merck, Darmstadt, Alemania Tris base, Winkler Ltda. TEMED B-mercapto etanol, Merck, Darmstadt, Alemania Triton X- 100, Sigma Chemical Co Tween- 20, Merck, Darmstadt, Alemania Xilol, Arquimed Soluciones. Bouin acuoso: Cada 100 ml contiene 75 ml de ácido pícrico saturado en agua, 25 ml de buffer de corrida y formalina 40% y 5 ml de ácido acético. PBS: NaCl 8 g/l; KCl 0,2 g/l; Na 2 HPO 4 0,24 g/l. ph 7,4. 0 Tampón de carga geles nativos: 62.5 mm Tris-HCl, ph 6.8, Glicerol 10%, azul de bromofenol % Tampón de carga SDS-PAGE 4X,: 62,5 mm Tris: HCl ph 6,8; 20% glicerol, 2 % SDS, 5% b-mercapto etanol, 0,5% Azul de bromo fenol. Tampón de corrida geles nativos: 25 mm Tris, 192 mm glicina. Tampón de corrida para SDS-PAGE 1X: 25mM Tris; 192 mm glicina; 0,1 %SDS ph 8,3. Tampón de transferencia geles nativos: Tris 25 mm, Glicina 193 mm, metanol 20%. Tampón de transferencia para SDS-PAGE 1X: 25 mm Tris; 193 mm glicina; 0,1% SDS; 20% metanol.
26 16 Medio de Hank: Solución balanceada de sales Medio RPMI: Medio diseñado para el crecimiento de linfoblastos y líneas celulares leucémicas en suspensión. Contiene sales inorgánicas, aminoácidos, vitaminas y otros componentes como glucosa y rojo fenol. Reactivo de Bradford: Azul de Coomassie G-250 0,01%; etanol 4,75%; ácido fosfórico 8,5%. Solución de bloqueo (inmunohistoquímica): Albúmina de suero bovino1%; tritón X-100 0,3%; leche descremada 5% en PBS 1X. Solución de bloqueo para Wester blot: Albúmina de suero bovino1%; tween-20 0,3% y leche descremada 5% en PBS 1X. Solución de fijación para SDS-PAGE: metanol 50%, ácido acético 12%. Solución de desteñido para SDS-PAGE: ácido acético 7%; metanol 30%. Solución de tinción para SDS-PAGE: Azul de Coomassie 0,3%; metanol 50%; ácido acético 10%. Solución de revelado: 20 ml PBS; 30 µl perhidrol 30%; H2O2; 1 ml DAB 10 mg/ml. Solución de acetona ácida fría: Ácido clorhídrico: acetona 1:28 v/v. Solución de ácido acético: ácido acético 0.1 M TNT: Tris: HCl 0,1 M; NaCl 0,15 M; tween-20 0,05%; ph: 7,5. Tampón Tris: HCl: Tris: HCl 20 mm, ph 7,4. Tampón espaciador para SDS-PAGE: Tris: HCl 0,5 M ph 6,8; SDS 0,4%.
27 17 Tampón espaciador geles nativos: Tris-HCl 0,5 M ph 6.8. Tampón separador para SDS-PAGE: Tris: HCl 1,5 M ph 8,8; SDS 0,4%. Tampón separador geles nativos: Tris-HCl 1,5 M ph Softwares Un-Scan-It, Silk scientific Inc (USA) Image-Pro-Plus 3.0 (Media Cybernetics, USA) Anticuerpos Anticuerpo anti-igm de Salmón/Trucha Este es un anticuerpo monoclonal anti-igm de Salmón del Atlántico (Salmo salar)/trucha Arcoíris (Oncorhynchus mykiss), adquirido en Aquatic Diagnostics Ltd, donado por el Dr. Alex Romero Anti copeptin de carpa (Cyprinus Carpio) hecho en conejo, LabBMP Este es un anticuerpo policlonal anti-copeptin de carpa hecho en conejo, en contra del motivo copeptin (C-terminal) del precursor de Isotocina de carpa, fabricado en nuestro laboratorio Anticuerpo anti-prl. Es un suero anti-prl recombinante de tilapia (tiprl-i y tiprl-ii) (Swennen et al 1991), donado por la Dra. F. Rentier-Delrue (Bélgica). 3.2 Métodos Purificación de copeptin de Salmo salar Obtención de las hipófisis de Salmo salar (para purificar copeptin).
28 18 Las pituitarias de salmón se obtuvieron de las cabezas de salmones adultos en las cuales se le realizó un corte, se limpió cuidadosamente del tejido extra, quedando al descubierto la hipófisis, la cual se extrajo rápidamente, guardándolas a -80ºC hasta su utilización. Los individuos adultos de Salmo salar se consiguieron en el centro de faenamiento primario de la empresa salmonera Marine Harvest, Cai-Caen, Calbuco, Puerto Montt Extracción Ácida. Para la extracción ácida nos basamos en el protocolo descrito por Andersen et al. (1988), con ciertas modificaciones. Un gramo de tejido se homogeneizó y extrajo en 3 ml de acetona ácida fría: Acetona; 1:28 v/v HCl/acetona, por 2 horas a -20ºC. Posteriormente la solución se centrifugó a 5700 rpm, por 30 minutos a 4ºC, (centrífuga Wifug), el sobrenadante se reservo y el sedimento se utilizó para la purificación de prolactina. El sobrenadante se re-precipitó con el doble de volumen de acetona fría por 24 horas a -20ºC. En seguida se centrifugó nuevamente a 5700 rpm por 30 minutos a -4ºC el sobrenadante se descartó y el sedimento se guardó refrigerado Cromatografía de filtración en gel. El sedimento obtenido en el paso anterior ( ) fue resuspendido en 2 ml de ácido acético 0,1 M y sometidos a cromatografía de filtración en gel en una columna de 1,5 x 30 cm con Sephadex G-25 equilibrada con ácido acético 0,1 M. Con el uso de azul de dextrano 0,1 %, se midió el V 0. Se aplicó a la columna aproximadamente 2 ml de muestra y la elución fue realizada con ácido acético 0,1 M como fase soluble de forma manual, recolectando fracciones de 1 ml aproximadamente. Las fracciones obtenidas en el V 0 fueron concentradas por ultra centrifugación, (Millipore) y analizada por Western blot para asegurar la presencia de la proteína.
29 Cromatografía de intercambio iónico. A la solución concentrada, previa al paso de la cromatografía de intercambio iónico, se ajustó el ph a 7,4 con Tris-HCl 20 mm. Al ajustarse el ph se generó precipitación de proteínas. La fracción precipitada fue resuspendida en tampón Tris-HCl 20 mm y ambas fracciones fueron cargadas sobre una columna de intercambio aniónico, DEAE-Celulosa equilibrada con Tris-HCl 20 mm. Para la elución de las fracciones retenidas, se utilizó un gradiente continuo de NaCl entre 0 y 0,3M obteniéndose fracciones de 0,6 ml Cuantificación de proteínas mediante el método de Bradford. Utilizando el método de Bradford (Bradford et al., 1976), se procedió a realizar una curva de calibración entre las concentraciones de 5-30 µg de proteína por ml de reactivo. Se uso como estándar BSA en agua luego de 10 min se realizó la lectura de absorbancia en un espectrofotómetro a una longitud de onda de 595 nm. Con el fin de determinar la concentración de proteínas en las muestras, se tomaron alícuotas diluidas de ellas y se le adicionó la cantidad de reactivo de Bradford. Luego de 10 min se midió su absorbancia en un espectrofotómetro a la misma longitud de onda de 595 nm y el valor obtenido se interpoló en la curva de calibración. Las muestras fueron medidas contra un blanco, en este caso se uso agua destilada para el blanco y las diluciones realizadas, con el reactivo de Bradford Electroforesis en geles de poliacrilamida. Se elaboraron los geles con el sistema de tampón discontinuo en condiciones denaturantes descrito originalmente por Laemmli (1970). Las dimensiones del gel fueron 95 x 100 x 0,75 mm con surcos de 5 mm de ancho por 10 mm de longitud, organizados entre dos placas de vidrio y
30 20 espaciadores de teflón. El gel separador se confeccionó con acrilamida-bisacrilamida 30% (p/v) y 0,8% respectivamente, a una concentración final de 15% (p/v, tamponado en Tris- HCl 1,5 M, ph 8,8 y SDS 0,4%. El gel espaciador se preparó a una concentración final de 4% (p/v) tamponado con Tris-HCl 0,5 M, ph 6,8 y SDS 0,4%. Ambos fueron polimerizados con persulfato de amonio 0,05% (p/v) y TEMED 0,15% (p/v) como concentración final. A las muestras se le adicionó tampón de muestra y fueron denaturadas calentándolas por 5 minutos a 95ºC, para posteriormente ser cargadas cuidadosamente en los surcos del gel. Luego el sistema fue montado y sumergido en tampón de corrida, se le aplicó una corriente de 10 ma hasta que el indicador del frente iónico llegó al borde del gel inferior. Al terminar la electroforesis, el gel se fijó en una solución de fijación (metanol 50 %; ácido acético 12%) por 30 minutos, entonces se sacó de la solución de fijación y se dejó tiñendo toda la noche en una solución de teñido (Azul de Coomassie R-250 0,3%, metanol 50%, ácido acético 10%). Posteriormente el gel fue desteñido mediante repetidos lavados con solución de desteñido (30 % metanol, 7 % ácido acético) hasta que el gel quedara completamente claro y sólo se pudieran apreciar las bandas teñidas. Las etapas de fijado hasta desteñido, se realizaron en una plataforma rotatoria con una agitación suave y constante. Inmunodetección de proteínas inmovilizadas en nitrocelulosa Análisis por Western Blot Los productos de purificación de copeptin a partir de hipófisis de Salmo salar se corrieron en dos al 15 % en condiciones denaturantes (SDS-PAGE). Un gel se tiño y el otro se electrotransfirió a una membrana de nitrocelulosa en tampón de transferencia durante toda la noche a 50 ma. Posteriormente la membrana de nitrocelulosa se incubó por 30 min en solución de bloqueo, para eliminar los sitios de unión inespecífica de las proteínas. Con la finalidad de inmunodetectar a la proteína, la membrana se incubó por un periodo mínimo de 5 horas con el
31 21 anticuerpo primario anti-copeptin de carpa diluido 1:1000 en solución de bloqueo, luego se hicieron 3 lavados de 10 minutos cada uno con TNT con agitación suave, luego de a este paso se incubó la membrana por 1 hora con el segundo anticuerpo anti-igg de conejo conjugado a peroxidasa diluido también en solución de bloqueo, con un titulo 1:1000. Nuevamente se lavó la membrana con TNT 3 veces, para eliminar el excedente de anticuerpo. Se reveló la membrana incubando con una solución de revelado por 15 minutos y deteniendo la reacción realizando repetidos lavados con agua destilada Evaluación in vivo de PRL, copéptido de Isotocina y PBS sobre la respuesta de Salmo salar frente a Piscirickettsia salmonis Animales de experimentación. Se utilizaron peces Salmo salar de 150 gramos, los cuales fueron divididos en tres grupos experimentales e inyectados intraperitonialmente con PRL, copeptido y PBS respectivamente, con una dosis de 0,1 µg por gramo de peso. Luego de la inyección, fueron desafiados con un patógeno bacteriano (Piscirickettsia salmonis). La dosis de patógenos corresponde a la que permite obtener una mortalidad 60%. La duración del desafío fue de 15 días con una temperatura de 12ºC. Al término de los experimentos los peces fueron sacrificados por decapitación y se cortaron en forma sagital para abrirlos con el propósito de ubicar y extraer los diferentes órganos. Los ensayos se realizaron en la dependencia de la empresa Aquagestión en Puerto Montt.
32 Extracción de macrófagos renales. El riñón del pez se colocó sobre una malla de nylon con aberturas de 80 µm, la cual se encontraba previamente dispuesta en un vaso precipitado de 80 ml, conteniendo 700 µl de medio RPMI 1640 tamponado con NaHCO 3, ph 7,4. La disgregación de las células se realizó colocando el tejido en medio de la malla y disponiéndolo como un sándwich, luego utilizando pinzas de punta roma se presiono suavemente tamizando el tejido. Se obtuvo 500 µl de suspensión celular y se mantuvieron a 4ºC hasta su utilización Elaboración del gradiente discontinuo de Percoll. Con la intención de poder separar los macrófagos renales, se elaboró un gradiente discontinuo de Percoll utilizándose para ello, percoll 51% de medio de Hank-Percoll 34% en tubos de vidrio de 5 ml. A cada tubo se agregó 1 ml de percoll 51 % y posteriormente se adicionó cuidadosamente con una pipeta Pasteur 1 ml de percoll 34% Separación de las fracciones celulares. Para la purificación de los macrófagos renales. Se cargó cuidadosamente con una pipeta Pasteur 500 µl de la suspensión celular, sobre el gradiente de Percoll, evitando dañar la gradiente en el proceso. Los tubos fueron centrifugados a 800 xg por 40 min. a 20ºC. Posterior a la centrifugación, se recuperó de la interfase el anillo de leucocitos, el cual se aspiró cuidadosamente con una pipeta Pasteur, evitando la contaminación excesiva con Percoll. Se obtuvieron aproximadamente 300 µl de una mezcla de Percoll/leucocitos, a la que se le adicionó 700 µl de medio de Hank en tubos de 1,5 ml y se volvió a centrifugar a 800 xg por 10 min a 4 ºC. El sobrenadante se desechó y las células fueron resuspendidas en 500 µl de medio de Hank. En seguida se centrifugaron a 500 xg por 5 min. Este lavado se repitió una vez más. Por último las
33 23 células se resuspendieron en 300 µl de medio RPMI 1640 tamponado con NaHCO 3, ph 7,4 y se conservaron a 4ºC hasta su utilización Conteo y evaluación de la viabilidad de los leucocitos. El conteo y viabilidad de las células, se realizó en una cámara de Neubahuer a través de la técnica de exclusión por azul tripan. Para esto, se prepararon diluciones (1:10 v/v) de las suspensiones celulares y se mezclaron con azul tripan en medio de Hank a una concentración final de 0,1%. Se cargó la cámara con 20 µl de la suspensión celular y se contabilizó el número de las células viables y no viables. Para ello se utilizó el criterio de 90% de viabilidad para la utilización posterior de las células en los ensayos de actividad inmune. Las suspensiones celulares fueron ajustadas a 10 7 células/ml para su utilización Evaluación de la producción del anión superoxido. Con el fin de medir la actividad citotóxica de las células, se utilizaron las suspensiones celulares obtenidas en las etapas anteriores ( ) de los diferente grupos experimentales. Para cada suspensión celular se sembró 25 µl en placas de microcultivo de 96 pocillos y por duplicado ajustada a 10 7 células/ml. En seguida a cada pocillo se le adiciono 175 µl RPMI 1640 tamponado NaHCO 3, ph 7,4 suplementado con plasma de S. salar (2%) y se lavó dos veces la monocapa con medio de Hank. Luego de los lavados se le adicionó, 100 ul de medio de Hank conteniendo 1 mg/ml de nitroblue tetrazolium (NBT) y acetato de forbol miristato (PMA) 1ug/ml. La placa se incubó por 90 minutos a 20ºC, en este proceso el NBT es reducido por el anión superoxido a un formazan azul insoluble. Posteriormente el medio es eliminado y se agregan 100 ml de metanol a cada pocillo con el fin de fijar las células, dejándose 10 minutos a
34 24 temperatura ambiente. Luego se retiró el metanol y se dejó secar a temperatura ambiente por unos minutos. Finalmente para disolver el formazan se adiciono 120 µl de KOH 2M y 140 µl de dimetil sulfoxido (DMSO) y se dejó a temperatura ambiente. Luego se midió la densidad óptica a 620 nm con un lector de microplacas. Evaluación de los niveles de IgM plasmática de peces (S. salar) inyectados con PRL, copeptin, PBS y desafiados con Piscirickettsia salmones Extracción de plasma. La sangre de los tres grupos de peces experimentales se obtuvo de la vena caudal utilizándo jeringas heparinizadas de 1 ml, recolectando aproximadamente 500 µl de sangre por pez. Para la obtención del plasma la sangre fue centrifugada a 2000 xg por 5 minutos, separándose en sobrenadante (plasma) y sedimento (elementos figurados), el sobrenadante se guardó rápidamente a -20ºC para los ensayos de Western-blot, con el fin de determinar IgM plasmática Electroforesis en geles de poliacrilamida en condiciones nativas. Se elaboraron geles con el sistema de tampón discontinuo en condiciones nativas (Laemmli, 1970; modificado). Las dimensiones de los geles fueron 95 x 100 x 0,75 mm y 16 x 20 x 0,5 cm organizados entre dos placas de vidrio y espaciadores de teflón. El gel separador se preparó con acrilamida-bisacrilamida 30% (p/v) 0,8% (p/v) respectivamente, a una concentración final de 7,5 % (p/v), tamponado con Tris-HCl 1,5 M, ph 8,8. El gel espaciador, se preparó a una concentración final de 4% (p/v) tamponado con Tris-HCl 0,5 M, ph 6.8. Ambos fueron polimerizados con persulfato de amonio 0,05% (p/v) y TEMED 0,15% (p/v) de concentración final. Las muestras con tampón de muestra de muestra se incubaron por 1 hora a temperatura ambiente para luego ser cargadas cuidadosamente en los surcos del gel.
35 25 Luego el sistema fue montado y sumergido en tampón de corrida, se aplicó una corriente de 50 Volts por aproximadamente 6 horas. Finalizada la electroforesis, el gel se fijó con solución de fijación (Metanol 50 %, ácido acético 12%) durante 1 h, luego se tiñó en solución de teñido (Azul de Coomassie R-250 0,3%, metanol 50%, ácido acético 10%) por mínimo 4 h y finalmente el gel se destiñó mediante repetidos lavados con una solución de desteñido (30 % metanol, 7 % ácido acético) hasta que el gel quedara completamente claro y sólo se apreciaran las bandas teñidas. Todas estas etapas se llevaron a cabo con agitación suave y constante en una plataforma rotatoria Análisis de electrotransferencia para geles de poliacrilamida en condiciones nativas. Luego de la electroforesis en geles nativos al 7 %, de las diferentes muestras de plasma. Se electrotransfirió y bloqueo como se describe en el paso , con la diferencia que el primer anticuerpo fue anti IgM de salmón/trucha. Finalmente se reveló la membrana con el sistema DAB-peroxidasa Cuantificación de inmunorreactividad. Para la cuantificación de la inmunorreactividad de los Western-blot realizados para la detección de IgM plasmática, se efectuó un análisis semicuantitativo de la intensidad de reacción, utilizando el programa UN-SCAN-IT, donde n = 3 y el análisis estadístico de los valores de t. test. P< 0,05, lo que es estadísticamente significativo Ensayo de actividad de lisozimas. Se mezcló en placa de cultivo de 96 pocillos 200 µl de una suspensión de Micrococus lisodeikticus 0,2 mg/ml en buffer fosfato sodio (NaH 2 PO 4 / NaHPO 4 ) 50 mm con 5, 10, 20, y 40 µl de plasma en pocillos diferentes y luego se registro la absorbancia a 530 nm a los 1, 5 y 10 min. Una unidad de actividad se definió como la cantidad de muestra que causa una disminución de la absorbancia de 0,001/min. (Lie et al., 1989).
36 Inmunohistoquímica Material biológico. Para realizar la inmuhistoquímica se utilizaron pituitarias de peces entre cm (20-30 gramos) que fueron sometidos a desafíos con patógenos bacterianos en la empresa Novartis S. A., Pto. Varas; en este caso fue con R. salmoninarum y P. salmonis. La dosis de patógenos corresponde a la que permite obtener una mortalidad 60%. El desafío se realizó durante 35 días a una temperatura del agua de 12ºC Fijación de los cortes histológicos. Las pituitarias de salmón de peces sobrevivientes al desafío fueron incubadas en Bouin acuoso por 48 horas y posteriormente deshidratadas mediante una batería de etanol en concentraciones crecientes, terminando con un tratamiento con xilol, posteriormente se incluyeron en Histoplast (parafina sólida) y finalmente, se confeccionaron cortes (5 µm de grosor) con un micrótomo y fueron colocados sobre porta objetos Inmunohistoquímica cromogénica. Los cortes para ser utilizados, primero se desparafinaron con xilol y luego se rehidrataron con diluciones de etanol, desde el 100 % de etanol hasta el 50 %. Después del último tratamiento con etanol, estos fueron secados al aire. Posteriormente son enjuagados con PBS e incubados por 10 minutos en una solución de perhidrol 3% en metanol, con el fin de inactivar las peroxidasas endógenas del tejido. Se lavaron los cortes con PBS por 5 minutos y se incubaron por 30 minutos en la solución de bloqueo. A continuación se eliminó la solución de bloqueo y se incubó por toda la noche (mínimo 12 horas) con el anticuerpo primario diluido en la solución de bloqueo con una dilución de anticuerpo 1:500 para anticuerpo anti-prl de tilapia y anti-copeptin de carpa
37 27 respectivamente a 20ºC en una cámara húmeda. Transcurrido dicho tiempo, se realizaron 3 lavados con PBS por 5 minutos cada uno, para luego ser incubados con el método de PAP, luego fueron lavados nuevamente. Para evidenciar las marcas se incubó con la solución de revelado y 10 minutos más tarde se agregaron 15 µl de perhidrol 30% y se dejó otros 5 minutos. Posteriormente, los cortes fueron lavados nuevamente tres veces con PBS y se procedió al montaje de los cortes. Para lo cual fueron tratados con una batería de etanol en concentraciones ascendentes de 50% hasta 100%, con un último tratamiento en xilol. Luego se le adicionó bálsamo de Canadá y se los cubrió con un cubre objeto Cuantificación de la inmunorreacción. Con el fin de cuantificar las reacciones inmunocitoquímicas, se efectuó un análisis semicuantitativo de las distintas muestras. Las cuantificaciones fueron efectuadas utilizando un sistema de digitalización automática por medio del programa Image-Pro-Plus 3.0 (Media Cybernetics, USA), por el cual se determinó la densidad óptica integrada (IOD) sobre el área reactiva (reacciones positivas). En el análisis estadístico de los valores, el t-test fue P < 0,05 lo que se consideró estadísticamente significativo.
38 28 4. RESULTADOS 4.1 Purificación del copeptin de Salmo salar. Se realizó la purificación del copeptin, a través de la precipitación con solventes orgánicos a ph ácido. Posterior a la recolección de las muestras en la empresa Marine Harvest (Cai-Caen, Calbuco), las pituitarias de salmón fueron guardadas a -80ºC y se utilizaron para la extracción de proteínas con acetona ácida 100%, quedando el copeptin disuelto en el sobrenadante de la solución. Seguidamente se reprecipitó el sobrenadante con acetona fría al 100%. La figura 2 muestra un esquema explicativo de las diferentes etapas de la extracción ácida. Al finalizar el proceso de extracción, entonces se verificó la presencia de la proteína en el precipitado final resuspendido en ácido acético 0,1 M, a través del análisis de western blot usando un anticuerpo anti-copeptin de carpa. Despues la fracción de proteínas extraídas se cargó en una columna de cromatografía en gel (Sephadex G-25). Debido al tamaño del precursor de isotocina y las características estructurales del Sephadex G-25 (diámetro del poro), la proteína eluyó en la fracción cero (V 0 ) de la cromatografía, junto a una serie de proteínas de similar tamaño, obteniéndose un único pico de absorbancia que mostraba una lectura máxima entre 0,8 y 0,9 a partir de 1 gramo de pituitaria de salmón (figura 3). Su presencia fue corroborada a través del análisis de dot blot de las diferentes fracciones, mostrando señal positiva para el copeptin. Estas fracciones fueron concentradas por ultrafiltración a un volumen de 2,5ml y cargadas a una cromatografía de intercambio iónico, DEAE celulosa, equilibrada con Tris-HCl 20 mm ph 7.4, donde fue eluida a través de una gradiente de sal de 0 0,3 M (figura 4). Posteriormente se confeccionó un pool de cada uno de los diferentes picos obtenidos en la última cromatografía.
39 29 Homogenizado de pituitaria en acetona acida fría 100% El precipitado se guardó Guardar a -20ºC 2 h. Centrifugar a 5000rpm. Sobrenadante se adicionan 1/3 de volumen de acetona fría 100% -20ºC por 4h. Resuspender el precipitado en acido acético 0.1 M guardar a -20ºC Figura 2: Esquema explicativo de la precipitación del copeptin con solventes orgánicos y medio acido.
40 30 Perfil de elución cromatografía en gel Sephadex G-25 l 0,9 0,8 0,7 absorbancia a 260 nm 0,6 0,5 0,4 0,3 0,2 0,1 0, Numero de fracción Figura 3: Cromatografía de filtración en gel Sephadex G-25. En una columna de 1,5 x 30 cm equilibrada con acido acético 0,1 M. Se cargó la fracción final obtenida de la precipitaciones con solventes orgánicos y resuspendidas en acido acético 0,1 M, como fase liquida de la cromatografía se usó ácido acético. Se recolecto el volumen de vacío de la columna midiendo la absorbancia a 260 nm de las diferentes fracciones.
41 31 Perfil de elución cromatografía DEAE-celulosa Figura 4: Cromatografía de intercambio aniónico en DEAE-Celulosa equilibrada con Tris- HCl 20 mm ph 7,4 con un flujo de 1 ml/min recolectando fracciones de 1,5 ml. Se cargó la fracción V 0 de la filtración en gel (Sephadex G-25). Los números 3, 4, 5, 6 corresponden a los diferentes picos obtenidos en la cromatografía. Los círculos azules marcan el inicio y termino de la cromatografía, los círculos verdes indican el tiempo en segundos durante la cromatografía. La línea azul corresponde a absorbancia medida de las fracciones recolectadas. La elución de las proteínas retenidas se efectuó con una gradiente continua de NaCl entre 0-0,3 M. Se confeccionó un pool individual para cada uno de los distintos picos (números 3, 4, 5 y 6) y se concentraron por ultrafiltración.
42 32 La presencia del copeptin-glicopeptido en las fracciones concentradas fue confirmada mediante electroforesis en poliacrilamida en condiciones denaturantes, electrotransferencia y análisis de western blot (figura 5). Con esta metodología se evidenció claramente una reacción positiva en la región de peso molecular correspondiente al tamaño de la proteína (14 kda) en los geles electrotransferidos. La integridad de las bandas fue verificada a través de la tinción en paralelo del gel con azul de Coomassie. Con las técnicas de electroforesis en SDS-PAGE, electrotransferencia y western blot se demostró una purificación casi a homogeneidad del copeptin (Cp) de Salmo salar asociado a neurofisina de los precursores de las poli-proteínas isotocina y vasotocina. 4.2 Expresión diferencial del copeptin asociado a Isotocina en hipófisis de Salmo salar desafiados con patógenos bacterianos. Antecedentes en la literatura mostraban que el copeptin se ubicaba en axones hipotalámicos en directo contacto con células lactotropas de la rostral pars distalis en la carpa común, (Flores et al., 2007). Esto, sumado a otros antecedentes del laboratorio, nos permitió plantearnos como interrogante, cómo sería la expresión diferencial del copeptin en la hipófisis de S. salar desafiados con patógenos bacterianos? y al mismo tiempo comparar la expresión de prolactina en los mismos grupos de peces. Con este propósito se utilizó un anticuerpo policlonal anti-copeptin de carpa y anti-prolactina de tilapia, para poder visualizar la inmunorreacción e identificar su localización, en cortes de glándula hipofisiaria de peces adultos y alevines expuestos a los patógenos R. salmoninarum y P. salmonis, mediante el análisis de inmunohistoquímica cromogénica.
43 33 A B ,5 Figura 5: Electroforesis en gel de poliacrilamida en condiciones denaturantes de neurofisina-copeptin purificado a partir de pituitaria de salmón. A: Las proteínas de las distintas fracciones de las etapas de purificación, se separaron en un gel de poliacrilamida al 15% y se tiñeron con azul de Coomassie. Carril 1: carga de la cromatografía de intercambio iónico (DEAE-celulosa), Carril 2: estándar de PM preteñido, Carril 3: V 0 de la DEAE-celulosa, Carriles 4 al 6: corresponden a los números de los picos que están detallados en el perfil cromatográfico. B: Western-blot con el anticuerpo anti-cp de las proteínas fraccionadas en A y evidenciado por el sistema peroxidasa-dab-perhidrol. Tanto la tinción del gel como el Western-blot permiten demostrar que se ha logrado purificar significativamente el copeptin de Salmo salar asociado a los precursores de las poli-proteínas isotocina y vasotocina.
44 Expresión de prolactina en hipófisis de salmones sanos y desafiados con patógenos. La incubación con el anticuerpo anti-prolactina en las secciones de la glándula de la pituitaria de peces adultos evidenció una fuerte reacción positiva de color café en el citoplasma de las células de la rostral pars distalis (RPD) (figura 6, A), donde se encuentran ubicadas las células lactotropas sintetizadoras de prolactina en la pituitaria. La misma reacción inmune se observa en los cortes de la glándula hipofisiaria de alevines desafiados (figura 6). Se muestra una clara y nítida diferencia en la inmunotinción en ambos grupos de peces experimentales, esto nos revela que entre ambos grupos de peces existe una diferencia en el contenido de prolactina en la pituitaria. Posteriormente, se procedió a realizar el análisis semi-cuantitativo de las inmunohistoquímicas para prolactina de ambos grupos de peces experimentales, en el cual utilizando un sistema de digitalización automática, se determinó la densidad óptica integrada sobre el área reactiva (reacción positiva) figura 7. Resultando un aumento en la producción de prolactina en el grupo de peces desafiados con R. salmoninarum con respecto a los peces adultos, lo contrario sucedió con el grupo de peces expuestos al patógeno P. salmonis donde se observó una disminución de los niveles de prolactina con respecto a los adultos Expresión del copeptin en hipófisis de salmones sanos y desafiados con patógenos. Los cortes de la pituitaria de peces adultos se incubaron con el suero inmune anti-copeptin a una dilución 1:500 figura 8, la unión del anticuerpo se reveló con sistema peroxidasa-dabperhidrol. Se aprecia una única reacción positiva de color café en las células de la región apical de la rostra pars distalis, donde las células lactotropas se encuentran localizadas.
45 35 Control sin 1º anticuerpo A RPD B RPD Desafiados R. salmoninarum P. salmonis C D C* D* Figura 6: Inmunohistoquímica de la expresión de PRL en pituitaria de peces adultos (peces sanos) y alevines sobrevivientes al desafío con patógenos (R. salmoninarum y P. salmonis). Panel A inmunohistoquímica de prolactina en hipófisis de peces adultos de salmón, panel B inmunohistoquímica de PRL en hipófisis de peces adultos de salmón control sin 1 anticuerpo. Panel C, C* inmunohistoquímica de prolactina en hipófisis de alevines de salmón desafiados con el patógeno R. salmoninarum, panel D, D* inmunohistoquímica de prolactina en hipófisis de
46 36 alevines de salmón desafiados con P. salmonis. La dilución del anticuerpo fue 1:500 y las fotografías fueron capturadas con objetivo de 4 x (A y B) 20 x (C y D). Se destaca claramente la reacción positiva de color café en el citoplasma de las células de la RPD. Como tinción de contraste se uso hematoxilina.
47 Densidad Optica Integrada (X 10000) PRL n = BKD SRS Adulto Figura 7: Expresión diferencial de prolactina en pituitaria de salmones adultos (peces sanos) y alevines sobrevivientes al desafío con patógenos, R. salmoninarum (BKD) y P. Salmonis (SRS). Se analizó semicuantitativamente por el programa Image-Pro-Plus 3.0, la inmunorreacción de prolactina en la hipófisis de los tres grupos de grupos de peces (BKD, SRS y adulto). La inmunorreacción fue cuantificada como densidad óptica integrada Las diferencias encontradas en la inmunohistoquímica son estadísticamente significativas para ambos grupos de peces (n = 4). Obteniéndose un valor de t-test. P < 0,05.
48 38 A A* RPD RPD Desafiados R. salmoninarum P. salmonis B C B* C* Figura 8: Inmunodetección de Cp en RPD de pituitaria de peces adultos (sanos) y alevines sobrevivientes al desafío con patógenos (R. salmoninarum y P. salmonis). En el panel A y A* inmunohistoquímica de copeptin en hipófisis de salmón adulto. En el panel B, B* inmunohistoquímica de copeptin en hipófisis de alevines de salmón desafiados al patógeno R. salmoninarum, en el panel C, C* inmunohistoquímica de copeptin en hipófisis de alevines de salmón desafiados al patógeno P. salmonis. Se destaca claramente en todos los paneles la reacción positiva de color café en la región de las células de la RPD. La dilución del anticuerpo
49 39 fue 1:500 y las imágenes fueron capturadas con objetivo de 20 x. Como tinción de contraste se uso hematoxilina.
50 40 Estos resultados confirman lo descrito anteriormente para la distribución histológica del copeptin en hipófisis de salmón. Para visualizar la expresión del copeptin en alevines de salmones expuestos a patógenos bacterianos, las secciones de la hipófisis de ambos grupos de peces se fijaron en Bouin acuoso se procesaron como fue descrito, con el fin de realizar cortes de 5 μm para inmunohistoquímica. Luego se incubó con el anticuerpo anti-copeptin a una dilución 1:500 utilizándose hematoxilina como tinción de contraste para resaltar los núcleos. De esta forma, respecto a los peces desafiados se observa una clara diferencia de la inmunotinción, que es inversamente proporcional al contenido de prolactina (figura 6). También para los grupos de peces evaluados con copeptin se realizó el análisis semicuantitativo de las imágenes, en el cual utilizando un sistema de digitalización automática, se determinó la densidad óptica integrada sobre el área reactiva (reacción positiva) figura 9. Este análisis evidencio una disminución en la producción de copeptin en ambos grupos de peces desafiados a patógenos con respecto al grupo de peces adulto y también una producción de copeptin inversamente proporcional al contenido de prolactina. 4.3 Evaluación in vivo de la acción de PRL, copéptido de isotocina y PBS sobre la respuesta de Salmo salar frente a Piscirickettsia salmonis. Cuando se obtuvo el copeptin purificado casi a homogeneidad, se realizó el ensayo de desafío de los salmones con el patógeno bacteriano Piscirickettsia salmonis. Se utilizaron tres grupos de peces experimentales de 150 gramos, los cuales fueron inyectados intraperitonialmente con copeptin, PBS y prolactina a una concentración de 0,1 µg por gramo de peso. La prolactina utilizada fue purificada por el método de Andersen et al. (1988) en el laboratorio de biología molecular de peces.
51 Densidad Optica Integrada (x 1000) 41 1,6 1,4 1,2 1,0 8,0 6,0 4,0 2,0 0,0 Copeptin BKD SRS Adulto n = 4 Figura 9: Expresión diferencial de copeptin en pituitaria de salmones adultos (peces sanos) y alevines sobrevivientes al desafío con patógenos, R. salmoninarum (BKD) y P. salmonis (SRS). Se analizo semi-cuantitativamente por el programa Image-Pro-Plus 3.0, la inmunorreacción de copeptin en la hipófisis de los tres grupos de peces (BKD, SRS y adulto). La inmunorreacción fue cuantificada como densidad óptica integrada. Las diferencias encontradas en la inmunohistoquímica son estadísticamente significativas para ambos grupos de peces (n = 4), obteniéndose un valor de t-test. P < 0,05.
52 42 La dosis utilizada del patógeno permitía obtener una mortalidad 60% (Dosis letal 50). Los protocolos y por ende las dosis de patógeno utilizadas en este ensayo, corresponden a protocolos estándar de la Empresa Novartis donde se desarrollaron estos experimentos. Estos protocolos y dosis son de carácter reservado y no pueden ser difundidos en esta tesis. El desafió duró 15 días con una temperatura de 12ºC. Al termino del ensayo los peces fueron sacrificados y sus órganos recolectados para realizar los diferentes ensayos Efecto in vivo de PRL en macrófagos de cabeza de riñón. Datos en la literatura aportan una clara evidencia que prolactina y otras hormonas hipofisiarias aumentan la producción del anión súper oxido en leucocitos de cabeza de riñón de tilapia in vitro (Yada et al., 2002). Por lo tanto, uno de los parámetros inmunes que se quiso evaluar fue la producción del anión superoxido por macrófagos de cabeza de riñón Salmo salar. La obtención y preparación de los macrófagos renales está descrita en Materiales y Métodos. El nivel de células fue normalizado a una concentración de 10 7 células/ml. Se sembraron en microplacas, se le adicionó NBT y se mezclaron con o sin PMA como estimulante de la producción de O - 2, transcurrido el tiempo de incubación, las células fueron fijadas y el NBT reducido fue disuelto en DSMO, para evaluar la absorbancia una longitud de onda de 620 nm. Los resultados fueron cuantificados, normalizados a la razón de estimulación siendo el grupo de los peces control los inyectados con PBS 1X figura 10. Se aprecia que respecto a los peces inyectados con prolactina y copeptin un aumento en la - producción del O 2 con respecto a los peces inyectados con PBS 1X.
53 43 Figura 10: Efecto de prolactina, copeptido y PBS 1x (sin estimular) sobre la producción del anión superoxido en macrófagos de cabeza de riñón de peces desafiados con Piscirickettsia salmonis. Los niveles de anión superoxido se expresan como una razón de estimulación donde 1 es el de nivel de anión superoxido producido por los macrófagos de cabeza de riñón, obtenidos de los peces inyectados con PBS 1X (control). Las barras celestes son los niveles de anión superoxido producidos por los macrófagos de cabeza de riñón sin estimular con PMA, obtenidos de peces inyectados con PBS 1X, prolactina y copeptido posterior al desafío con la Piscirickettsia salmonis respectivamente, expresados como razón de estimulación. Las barras azules son los niveles de anión superoxido producidos por los macrófagos de cabeza de riñón estimulados con PMA, obtenidos de peces inyectados con PBS 1X, prolactina y
54 44 copeptido posterior al desafío con la Piscirickettsia salmonis respectivamente, expresados como razón de estimulación. Los peces se inyectaron con PBS, PRL y copeptin respectivamente, desafiados con Piscirickettsia salmonis y analizados 15 días post desafío. Después del tratamiento, células magrofágicas de riñón estimulada y no estimulas con PMA se les midió la producción de anión superoxido con el método de la reducción del NBT.
55 Evaluación de los niveles plasmáticos de IgM de peces inyectados con PRL, copeptin y PBS desafiados con P. salmonis. Otro parámetro inmune que se evaluó, fueron los niveles plasmáticos de IgM, debido a que esta inmunoglobulina se encuentra asociada a la respuesta inmune humoral mediada por linfocitos B ya que existen evidencias preliminares en la literatura de que PRL aumenta los niveles de IgM en el plasma de la trucha arco iris (Yada et al., 1999). Se obtuvo sangre de los peces experimentales expuestos al patógeno de los tres grupos, la cual fue tratada para la obtención del plasma (Materiales y Métodos ). Los niveles de IgM se midieron con el uso de técnicas electroforéticas en geles nativos, con el propósito de no afectar su estructura cuaternaria, ya que está descrito que en la mayoría de los teleósteos IgM existe como una molécula de alto peso molecular y formando un tetrámero (Watts et al., 2001). A través del análisis de western blot con el uso del anticuerpo anti IgM de Salmón/Trucha, se identificó la presencia en el plasma de esta inmunoglobulina. La figura 11 muestra los resultados obtenidos de la cuantificación de los niveles de IgM en los distintos grupos experimentales, evidenciando una diferencia significativa entre los salmones inyectados con PRL y copeptin con respecto a los peces tratados con PBS Evaluación de los niveles plasmáticos de lizosima en peces inyectados con PRL, copeptido y PBS desafiados con Piscirickettsia salmonis. Las lisozimas son uno de los componentes del sistema de defensa no humoral en los peces. Por ello se consideró evaluar los niveles plasmáticos de lisozima. Para ello se extrajo el plasma de los diferentes grupos de peces experimentales y se midió la actividad de esta enzima por una técnica de turbidimetría los resultados se muestran en la figura 12. Se observa un aumento de los niveles de esta enzima en los peces inyectados con prolactina y una pequeña
56 46 disminución en los peces inyectados con copeptin con respecto a los peces inyectados con PBS 1 X.
57 47 Figura 11: Efecto in vivo de prolactina y copeptin en salmones desafiados con Piscirickettsia salmonis, sobre los niveles plasmáticos de IgM. Los niveles plasmáticos de IgM se presentan como razón de estimulación siendo 1 los niveles de IgM, obtenidos de peces inyectados con PBS 1X (control). Los niveles plasmáticos de IgM total aumentan (estadísticamente) significativamente en los peces inyectados con prolactina y copeptido con respecto a los peces inyectados con PBS 1X Los peces de 150 g se inyectaron con PBS, PRL (0,1 μg/g peso de pez) y copeptin (0,1μg/g peso de pez) respectivamente, desafiados con Piscirickettsia salmonis y analizados 15 días post desafío. Posterior al tratamiento, se midió el nivel de IgM en el plasma cargando 5 ug de proteínas total de plasma a un gel nativo, para luego realizar un análisis semi-cuantitativo del Western blot, con el programa UN-SCAN-IT.
58 48 Figura 12: Efecto en in vivo de prolactina y el copeptido en los niveles plasmáticos de lisozimas de peces desafiados con Piscirickettsia salmonis. No se observan diferencias significativas entre los tres grupos de peces desafiados; PBS 1X, prolactina y copeptido. Posterior al desafío con el patógenos Piscirickettsia salmonis, se midió los niveles plasmáticos de lisozima por absorbancia a 530 nm. Una unidad de actividad se definió como la cantidad de muestra que causa una disminución de la absorbancia de 0,001/min. (Lie et al., 1989).
59 49 5. DISCUSIÓN En la actualidad a nivel global la industria del salmón ha evolucionado extraordinariamente, siendo Chile uno de los mayores productores de salmón del mundo. Los avances en el conocimiento permiten que esta industria se renueve continuamente y esta renovación debe estar a la par de las nuevas tecnologías y necesidades del mercado tanto nacional como internacional, promoviendo salmones de mejor calidad y potenciando las formas de cultivo y crianza de los peces. Estos eventos llevaron a la industria del salmón a aumentar la demanda tanto nacional como internacional de nuevas ovas y salmones, lo que originó el ingreso y diseminación de patógenos infecciosos a las diferentes áreas de cultivo. Entre ellos se destacan la Piscirickettsia salmonis una bacteria intracelular causante del Síndrome Ricketsial del Salmón (SRS) (McCarthy et al., 2008) y que fue observada por primera vez en Chile en También, Flavobacterium psychrophilum, un bacilo Gram negativo que origina diversas patologías en peces salmónidos, desde necrosis ulcerativa de la piel hasta una infección sistémica. Es el agente infeccioso causal de la enfermedad o Síndrome del alevín de la trucha arco iris (Crump et al., 2001). Otro ejemplo es Renibacterium salmoninarum agente etiológico de la denominada enfermedad bacteriana del riñón (BKD) que produce sintomatologías graves en los salmones, como aumento de tamaño del riñón, generalmente fluido en la cavidad abdominal y tanto en el riñón como en el bazo y el hígado aparecen nódulos grisáceos o masas difusa (Varpu Hirvelä- Kosk, 2007). Finalmente podemos mencionar Vibrio sp., patógeno que afecta a los salmones chilenos desde hace bastante tiempo. El virus IPN, virus de la necrosis pancreática infecciosa, produce una infección sistémica aguda en alevines de 1 a 6 meses de edad, pudiendo provocar incluso, mortalidades acumulativas del orden del 100% de la población afectada (Soliman et al., 2009). Los peces sobrevivientes permanecen en estado portador de por vida, diseminando el virus
60 50 por largo tiempo, manteniendo así el virus en el agua (Wolf, 1988). La figura 13 muestra la correlación entre las principales especies de salmón con la aparición en el tiempo de los importantes agentes causales de las patologías más dañinas. Cabe subrayar que los patógenos entre los que se generan mayores pérdidas actualmente destacan, P. salmonis, Vibrio y los virus IPN e ISA. El principal agente infeccioso bacteriano causal de la mortalidad de las tres especies de mayor cultivo en Chile (Atlántico, Coho y trucha) es la Piscirickettsia salmonis, con un 64,2% en el año 2004, seguida de Aeromona salmonicida 11,1% y la vibriosis 12,2 %. La Piscirickettsia salmonis, como se mencionó anteriormente es una bacteria intracelular facultativa que origina una alta mortalidad, puede producir disminución del apetito, dispersión, prolongación de ciclo por falta de crecimiento, etc. Los antibióticos mayormente usados en la industria de los salmones son ácido oxolínico, enrofloxacino inyectable, u oxitetracilina oral o inyectable. No obstante al ser la P. salmonis una bacteria intracelular la mayoría de los tratamientos con antibióticos solo alivian, pero no solucionan el problema. Esto es preocupante, debido a que el uso indiscriminado de antibióticos por la industria salmonera puede originar altos riesgos en la salud humana, como la aparición de nuevas cepas resistente, potenciando la resistencia de estas bacterias a los fármacos y producir la diseminación a otros componentes de la biosfera, incluido el hombre. Esta nueva problemática de la propagación masiva de los agentes patógenos y el uso de altas dosis de antibióticos para su tratamiento, han llevado al estudio y la innovación de nuevas técnicas para atacar los agentes infecciosos causantes de las diferentes enfermedades. Por este motivo el conocimiento obtenido del estudio de la regulación del sistema inmune por el sistema endocrino, proyecta una nueva herramienta de ataque y control de los agentes infecciosos.
61 51 Figura 13: Grafico de correlaciones de la producción nacional de las tres principales especies de salmón, salmón del Atlántico, Salmón coho y trucha con la aparición en el tiempo de los primordiales agentes causales de las patologías más dañinas.
RESULTADOS Y DISCUSIÓN. Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv
 RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a
 Introducción Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a los investigadores verificar la expresión de una proteína, determinar la cantidad relativa
Introducción Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a los investigadores verificar la expresión de una proteína, determinar la cantidad relativa
AMINOÁCIDOS SE PUEDEN UNIR POR ENLACES PEPTÍDICOS
 Tema 4. Proteínas: funciones biológicas y estructura primaria. Enlace peptídico. Péptidos y proteínas. Diversidad de funciones biológicas. Niveles de organización estructural de las proteínas. Separación
Tema 4. Proteínas: funciones biológicas y estructura primaria. Enlace peptídico. Péptidos y proteínas. Diversidad de funciones biológicas. Niveles de organización estructural de las proteínas. Separación
CUANTIFICACIÓN DE ADENOSIN DESAMINASA (ADA)
 CUANTIFICACIÓN DE ADENOSIN DESAMINASA (ADA) PROTOCOLO ADA FUNDAMENTO DEL METODO: La adenosindesaminasa (ADA) es una enzima del catabolismo de las purinas que cataliza la conversión de la adenosina en inosina
CUANTIFICACIÓN DE ADENOSIN DESAMINASA (ADA) PROTOCOLO ADA FUNDAMENTO DEL METODO: La adenosindesaminasa (ADA) es una enzima del catabolismo de las purinas que cataliza la conversión de la adenosina en inosina
DANAGENE RNA PURIFICATION KIT
 DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
C A P Í T U L O 3 M A T E R I A L E S Y M É T O D O. Se ejecutaron varias pruebas para la inactivación de Escherichia Coli ATCC 25922 en agua
 C A P Í T U L O 3 M A T E R I A L E S Y M É T O D O Se ejecutaron varias pruebas para la inactivación de Escherichia Coli ATCC 25922 en agua destilada utilizando Dióxido de Titanio dopado con Nitrógeno,
C A P Í T U L O 3 M A T E R I A L E S Y M É T O D O Se ejecutaron varias pruebas para la inactivación de Escherichia Coli ATCC 25922 en agua destilada utilizando Dióxido de Titanio dopado con Nitrógeno,
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDS-PAGE. Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE)
 ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
UNIDAD 15: EL SISTEMA IMNUNITARIO
 UNIDAD 15: EL SISTEMA IMNUNITARIO Lee atentamente. 1. EL ORGANISMO RECONOCE A LOS ELEMENTOS EXTRAÑOS Las células de una persona introducidas en otra son reconocidas por el organismo como algo extraño no
UNIDAD 15: EL SISTEMA IMNUNITARIO Lee atentamente. 1. EL ORGANISMO RECONOCE A LOS ELEMENTOS EXTRAÑOS Las células de una persona introducidas en otra son reconocidas por el organismo como algo extraño no
PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN DE LAS COMPETENCIAS PROFESIONALES CUESTIONARIO DE AUTOEVALUACIÓN PARA LAS TRABAJADORAS Y TRABAJADORES
 MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
Biología Celular y Molecular. Guía de TP Nro. 3. Ensayos de proliferación, adhesión y migración celular in vitro.
 Biología Celular y Molecular. Guía de TP Nro. 3 Ensayos de proliferación, adhesión y migración celular in vitro. Introducción La valoración de la proliferación celular y la citotoxicidad in vitro es, muchas
Biología Celular y Molecular. Guía de TP Nro. 3 Ensayos de proliferación, adhesión y migración celular in vitro. Introducción La valoración de la proliferación celular y la citotoxicidad in vitro es, muchas
Programa donde se inscribe la beca y/o la tesis: Interacciones biológicas: de las
 Titulo: Potencial uso simultáneo de micopatógenos biocontroladores de hormigas cortadoras de hojas. Autores: Natalia G. Armando, Jorge A. Marfetán, Patricia J. Folgarait Correo: ng.armando14@gmail.com
Titulo: Potencial uso simultáneo de micopatógenos biocontroladores de hormigas cortadoras de hojas. Autores: Natalia G. Armando, Jorge A. Marfetán, Patricia J. Folgarait Correo: ng.armando14@gmail.com
Tipos de células madre
 Biología Bachillerato IES Fuentesnuevas 1 CÉLULAS MADRE O TRONCALES (STEM CELLS) Las células madre son células que tienen capacidad de renovarse continuamente por sucesivas divisiones por mitosis y de
Biología Bachillerato IES Fuentesnuevas 1 CÉLULAS MADRE O TRONCALES (STEM CELLS) Las células madre son células que tienen capacidad de renovarse continuamente por sucesivas divisiones por mitosis y de
Informe del trabajo práctico nº7
 Informe del trabajo práctico nº7 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Mostrar las propiedades que presentan
Informe del trabajo práctico nº7 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Mostrar las propiedades que presentan
CROMATOGRAFÍA DE FILTRACIÓN EN GEL
 1.- FUNDAMENTO TEÓRICO CROMATOGRAFÍA DE FILTRACIÓN EN GEL Filtración en gel - 1 (Farmacia) La cromatografía de exclusión o filtración en gel es una clase de cromatografía sólido-líquido que permite la
1.- FUNDAMENTO TEÓRICO CROMATOGRAFÍA DE FILTRACIÓN EN GEL Filtración en gel - 1 (Farmacia) La cromatografía de exclusión o filtración en gel es una clase de cromatografía sólido-líquido que permite la
Módulo 1 Biología Molecular Genética Molecular II 2009. Módulo 1. Amplificación de un fragmento de ADN genómico por PCR
 Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
Normalización de soluciones de NaOH 0,1N y HCl 0,1N.
 Laboratorio N 1: Normalización de soluciones de NaOH 0,1N y HCl 0,1N. Objetivos: - Determinar la normalidad exacta de una solución de hidróxido de sodio aproximadamente 0,1 N, utilizando biftalato de potasio
Laboratorio N 1: Normalización de soluciones de NaOH 0,1N y HCl 0,1N. Objetivos: - Determinar la normalidad exacta de una solución de hidróxido de sodio aproximadamente 0,1 N, utilizando biftalato de potasio
TRABAJO PRACTICO Nº 3 ENZIMOINMUNOANALISIS ELISA
 TRABAJO PRACTICO Nº 3 ENZIMOINMUNOANALISIS ELISA Docentes encargados: Bioq. Natalia Guiñazú Bioq. Maria Sol Renna Biol. Virginia Andreani Bioq. Mauricio Figueredo Bioq. Vanina Garrido Bioq. Laura Dulgerian
TRABAJO PRACTICO Nº 3 ENZIMOINMUNOANALISIS ELISA Docentes encargados: Bioq. Natalia Guiñazú Bioq. Maria Sol Renna Biol. Virginia Andreani Bioq. Mauricio Figueredo Bioq. Vanina Garrido Bioq. Laura Dulgerian
7.012 Serie de ejercicios 5
 Nombre Grupo 7.012 Serie de ejercicios 5 Pregunta 1 Al estudiar los problemas de esterilidad, usted intenta aislar un hipotético gen de conejo que explique la prolífica reproducción de estos animales.
Nombre Grupo 7.012 Serie de ejercicios 5 Pregunta 1 Al estudiar los problemas de esterilidad, usted intenta aislar un hipotético gen de conejo que explique la prolífica reproducción de estos animales.
Tipificación de Grupos Sanguineos e Isohemaglutininas
 Tipificación de Grupos Sanguineos e Isohemaglutininas Introducción Los eritrocitos expresan antígenos de membrana. Dichos antígenos se encuentran determinados genéticamente y pueden ser identificados mediante
Tipificación de Grupos Sanguineos e Isohemaglutininas Introducción Los eritrocitos expresan antígenos de membrana. Dichos antígenos se encuentran determinados genéticamente y pueden ser identificados mediante
ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA
 VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO
 Actividad Experimental SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO Investigación previa 1.- Investigar las medidas de seguridad que hay que mantener al manipular KOH y H SO, incluyendo que acciones
Actividad Experimental SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO Investigación previa 1.- Investigar las medidas de seguridad que hay que mantener al manipular KOH y H SO, incluyendo que acciones
Identificación y caracterización de células madres cancerígenas (CMCs) en Sarcoma de Ewing
 Identificación y caracterización de células madres cancerígenas (CMCs) en Sarcoma de Ewing Introducción Una célula madre o célula troncal es una célula que tiene capacidad de autorrenovarse mediante divisiones
Identificación y caracterización de células madres cancerígenas (CMCs) en Sarcoma de Ewing Introducción Una célula madre o célula troncal es una célula que tiene capacidad de autorrenovarse mediante divisiones
CONTRATO DE SUMINISTROS PLIEGO DE PRESCRIPCIONES TÉCNICAS IÓNICO. OBJETO DEL CONTRATO: SUMINISTRO E INSTALACIÓN DE UN CROMATÓGRAFO
 UNIVERSIDAD DE JAÉN CONTRATO DE SUMINISTROS PLIEGO DE PRESCRIPCIONES TÉCNICAS OBJETO DEL CONTRATO: SUMINISTRO E INSTALACIÓN DE UN CROMATÓGRAFO IÓNICO. NÚMERO DE EXPEDIENTE 2013/06 PROCEDIMIENTO DE ADJUDICACIÓN
UNIVERSIDAD DE JAÉN CONTRATO DE SUMINISTROS PLIEGO DE PRESCRIPCIONES TÉCNICAS OBJETO DEL CONTRATO: SUMINISTRO E INSTALACIÓN DE UN CROMATÓGRAFO IÓNICO. NÚMERO DE EXPEDIENTE 2013/06 PROCEDIMIENTO DE ADJUDICACIÓN
turbidez en los medios de cultivo. La duración de la prueba de esterilidad es de 14 días. Las pruebas de toxicidad (específica y general), llamadas
 Para que una prueba se considere validada deberá cumplir los requisitos siguientes: Precisión: es la variación de los resultados de acuerdo a la desviación estándar o al coeficiente de variación. Exactitud:
Para que una prueba se considere validada deberá cumplir los requisitos siguientes: Precisión: es la variación de los resultados de acuerdo a la desviación estándar o al coeficiente de variación. Exactitud:
MÉTODOS CROMATOGRÁFICOS: 1. Exclusión molecular 2. Intercambio iónico 3. Afinidad SSN
 MÉTODOS CROMATOGRÁFICOS: 1. Exclusión molecular 2. Intercambio iónico 3. Afinidad SSN Propiedades de una proteína que son útiles para su purificación por cromatografía Peso molecular Carga iónica Hidrofobicidad
MÉTODOS CROMATOGRÁFICOS: 1. Exclusión molecular 2. Intercambio iónico 3. Afinidad SSN Propiedades de una proteína que son útiles para su purificación por cromatografía Peso molecular Carga iónica Hidrofobicidad
Prácticas de Análisis Instrumental
 Prácticas de Análisis Instrumental Asignatura: Análisis Instrumental Alumno: Daniel González Mancebo Practica 1. DETERMINACIÓN DE CONSTANTES DE EQUILIBRIO MEDIANTE ESPECTROFOTOMETRÍA UV- VISIBLE. Lo primero
Prácticas de Análisis Instrumental Asignatura: Análisis Instrumental Alumno: Daniel González Mancebo Practica 1. DETERMINACIÓN DE CONSTANTES DE EQUILIBRIO MEDIANTE ESPECTROFOTOMETRÍA UV- VISIBLE. Lo primero
NMX-F-070-1964. MÉTODO DE PRUEBA PARA LA DETERMINACIÓN DE TIAMINA. THIAMINE DETERMINATION. TEST METHOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS.
 NMX-F-070-1964. MÉTODO DE PRUEBA PARA LA DETERMINACIÓN DE TIAMINA. THIAMINE DETERMINATION. TEST METHOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. ASUNTO Con fundamento en lo dispuesto en los Artículos
NMX-F-070-1964. MÉTODO DE PRUEBA PARA LA DETERMINACIÓN DE TIAMINA. THIAMINE DETERMINATION. TEST METHOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. ASUNTO Con fundamento en lo dispuesto en los Artículos
PRÁCTICA 5. CALORIMETRÍA
 PRÁCTICA 5. CALORIMETRÍA INTRODUCCIÓN Al mezclar dos cantidades de líquidos a distinta temperatura se genera una transferencia de energía en forma de calor desde el más caliente al más frío. Dicho tránsito
PRÁCTICA 5. CALORIMETRÍA INTRODUCCIÓN Al mezclar dos cantidades de líquidos a distinta temperatura se genera una transferencia de energía en forma de calor desde el más caliente al más frío. Dicho tránsito
PRACTICA No. 9 PREPARACION DE DISOLUCIONES
 1 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II PRACTICA No. 9 PREPARACION DE DISOLUCIONES INTRODUCCION:
1 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II PRACTICA No. 9 PREPARACION DE DISOLUCIONES INTRODUCCION:
SERVICIO DE ANTICUERPOS POLICLONALES A PEDIDO
 SERVICIO DE ANTICUERPOS POLICLONALES A PEDIDO GrupoBios S.A. Avda.Zañartu 1482 Ñuñoa Santiago-Chile Teléfono: (56-2) 473 6100 Fax: (56-2) 239 4250 e-mail: ventas@grupobios.cl www.grupobios.cl 2011 CONTENIDO
SERVICIO DE ANTICUERPOS POLICLONALES A PEDIDO GrupoBios S.A. Avda.Zañartu 1482 Ñuñoa Santiago-Chile Teléfono: (56-2) 473 6100 Fax: (56-2) 239 4250 e-mail: ventas@grupobios.cl www.grupobios.cl 2011 CONTENIDO
6. Reacciones de precipitación
 6. Reacciones de precipitación Las reacciones de precipitación son aquellas en las que el producto es un sólido; se utilizan en los métodos gravimétricos de análisis y en las titulaciones por precipitación.
6. Reacciones de precipitación Las reacciones de precipitación son aquellas en las que el producto es un sólido; se utilizan en los métodos gravimétricos de análisis y en las titulaciones por precipitación.
BENTLEY BactoCount IBC
 BENTLEY BactoCount IBC Características del equipo El BactoCount IBC es un equipo automático para contar rápido e individualmente las bacterias de la leche cruda. Capacidad: de 50 hasta 150 muestras / hora.
BENTLEY BactoCount IBC Características del equipo El BactoCount IBC es un equipo automático para contar rápido e individualmente las bacterias de la leche cruda. Capacidad: de 50 hasta 150 muestras / hora.
CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL
 LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
Practica la genética Ficha didáctica del profesorado Bachillerato
 Ficha didáctica del profesorado Bachillerato www.eurekamuseoa.es Extracción de ADN Cuál es la función de cada uno de los ingredientes utilizados para realizar la disolución tampón para la visualización
Ficha didáctica del profesorado Bachillerato www.eurekamuseoa.es Extracción de ADN Cuál es la función de cada uno de los ingredientes utilizados para realizar la disolución tampón para la visualización
CAPÍTULO III RESULTADOS Y ANÁLISIS DE RESULTADOS
 CAPÍTULO III RESULTADOS Y ANÁLISIS DE RESULTADOS Para el proceso de purificación del aceite, se pudo observar, en el momento del filtrado algunas partículas sólidas retenidas en los diferentes filtros
CAPÍTULO III RESULTADOS Y ANÁLISIS DE RESULTADOS Para el proceso de purificación del aceite, se pudo observar, en el momento del filtrado algunas partículas sólidas retenidas en los diferentes filtros
FICHA PÚBLICA DEL PROYECTO
 FICHA PÚBLICA DEL PROYECTO PROGRAMA DE ESTÍMULOS A LA INNOVACIÓN NUMERO DE PROYECTO: 214028 EMPRESA BENEFICIADA: PHARMACOS EXAKTA S.A. DE C.V. TÍTULO DEL PROYECTO: DESARROLLO DE UN MINI-ARREGLO DE ANTIGENOS
FICHA PÚBLICA DEL PROYECTO PROGRAMA DE ESTÍMULOS A LA INNOVACIÓN NUMERO DE PROYECTO: 214028 EMPRESA BENEFICIADA: PHARMACOS EXAKTA S.A. DE C.V. TÍTULO DEL PROYECTO: DESARROLLO DE UN MINI-ARREGLO DE ANTIGENOS
23. Hidrólisis ácida y enzimática del glucógeno
 23. Hidrólisis ácida y enzimática del glucógeno Emilia Martínez Galisteo, Carmen Alicia Padilla Peña, Concepción García Alfonso, José Antonio Bárcena Ruiz, Jesús Diez Dapena. Departamento de Bioquímica
23. Hidrólisis ácida y enzimática del glucógeno Emilia Martínez Galisteo, Carmen Alicia Padilla Peña, Concepción García Alfonso, José Antonio Bárcena Ruiz, Jesús Diez Dapena. Departamento de Bioquímica
LIMPIEZA Y DESINFECCIÓN EN LA INDUSTRIA LÁCTEA
 LIMPIEZA Y EN LA INDUSTRIA LÁCTEA LD EN LAS INDUSTRIAS DE ALIMENTOS La sanitización/higienización es un concepto general que comprende la creación y mantenimiento de las condiciones óptimas de higiene
LIMPIEZA Y EN LA INDUSTRIA LÁCTEA LD EN LAS INDUSTRIAS DE ALIMENTOS La sanitización/higienización es un concepto general que comprende la creación y mantenimiento de las condiciones óptimas de higiene
Práctica 5 CINÉTICA ENZIMÁTICA: DETERMINACIÓN ESPECTOFOTOMÉTRICA DE LA CONSTANTE DE MICHAELIS-MENTEN DE LA PAPAÍNA
 Práctica 5 CINÉTICA ENZIMÁTICA: DETERMINACIÓN ESPECTOFOTOMÉTRICA DE LA CONSTANTE DE MICHAELIS-MENTEN DE LA PAPAÍNA 1. Objetivo Se pretende calcular la constante de Michaelis-Menten (K M ), la constante
Práctica 5 CINÉTICA ENZIMÁTICA: DETERMINACIÓN ESPECTOFOTOMÉTRICA DE LA CONSTANTE DE MICHAELIS-MENTEN DE LA PAPAÍNA 1. Objetivo Se pretende calcular la constante de Michaelis-Menten (K M ), la constante
4. Materiales y Métodos. Los equipos que a continuación se mencionan se encuentran en el laboratorio de
 39 4. Materiales y Métodos 4.1 Equipos Los equipos que a continuación se mencionan se encuentran en el laboratorio de Ingeniería Ambiental de la Universidad de las Américas Puebla y en el Laboratorio de
39 4. Materiales y Métodos 4.1 Equipos Los equipos que a continuación se mencionan se encuentran en el laboratorio de Ingeniería Ambiental de la Universidad de las Américas Puebla y en el Laboratorio de
Instituto de Innovación en Biotecnología e Industria
 Instituto de Innovación en Biotecnología e Industria Centro de Biotecnología Vegetal (CEBIVE) Marcadores moleculares para caracterizar cultivares de aguacates criollos (Persea americana) del tipo antillano,
Instituto de Innovación en Biotecnología e Industria Centro de Biotecnología Vegetal (CEBIVE) Marcadores moleculares para caracterizar cultivares de aguacates criollos (Persea americana) del tipo antillano,
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN
 5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
MINISTERIO DE SANIDAD SERVICIOS SOCIALES E IGUALDAD. Qué es la sangre del cordón umbilical y para qué sirve?
 RESPUESTAS A LAS PREGUNTAS MÁS COMUNES SOBRE SANGRE DE CORDÓN UMBILICAL, PLANTEADAS TRAS LA APROBACIÓN DEL REAL DECRETO 1301/2006 SOBRE CALIDAD Y SEGURIDAD DE CÉLULAS Y TEJIDOS. Qué es la sangre del cordón
RESPUESTAS A LAS PREGUNTAS MÁS COMUNES SOBRE SANGRE DE CORDÓN UMBILICAL, PLANTEADAS TRAS LA APROBACIÓN DEL REAL DECRETO 1301/2006 SOBRE CALIDAD Y SEGURIDAD DE CÉLULAS Y TEJIDOS. Qué es la sangre del cordón
Int. Cl. 7 : C12N 9/02. 72 Inventor/es: Kajiyama, Naoki. 74 Agente: Carvajal y Urquijo, Isabel
 19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 249 794 1 Int. Cl. 7 : C12N 9/02 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 9766.6 86 Fecha de presentación
19 OFICINA ESPAÑOLA DE PATENTES Y MARCAS ESPAÑA 11 Número de publicación: 2 249 794 1 Int. Cl. 7 : C12N 9/02 12 TRADUCCIÓN DE PATENTE EUROPEA T3 86 Número de solicitud europea: 9766.6 86 Fecha de presentación
Dr. David Cano González Hospital Virgen del Rocío. Sevilla
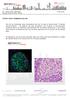 INTRA-ISLET COMMUNICATION Uno de los simposios más interesantes de hoy ha sido el denominado intraislet communication. El objetivo de este simposium era mostrar la comunicación existente entre los distintos
INTRA-ISLET COMMUNICATION Uno de los simposios más interesantes de hoy ha sido el denominado intraislet communication. El objetivo de este simposium era mostrar la comunicación existente entre los distintos
ANEXO I. Inmunofenotipificación Celular por Citometría de Flujo
 ANEXO I Inmunofenotipificación Celular por Citometría de Flujo Reactivos Anticuerpos monoclonales fluoromarcados (BD Bioscience Pharmingen) Medio DMEM con 0.02% de azida de sodio Paraformaldehido (PFA)
ANEXO I Inmunofenotipificación Celular por Citometría de Flujo Reactivos Anticuerpos monoclonales fluoromarcados (BD Bioscience Pharmingen) Medio DMEM con 0.02% de azida de sodio Paraformaldehido (PFA)
MATERIALES Y MÉTODOS
 MATERIALES Y MÉTODOS Para la obtención, aislamiento y caracterización de la proteína de superficie HSPB66 de H. pylori ATCC 43504 se realizó un cultivo de esta cepa, seguido de la extracción de proteínas
MATERIALES Y MÉTODOS Para la obtención, aislamiento y caracterización de la proteína de superficie HSPB66 de H. pylori ATCC 43504 se realizó un cultivo de esta cepa, seguido de la extracción de proteínas
ALERGENOS-DETERMINACIÓN DE LISOZIMA
 ALERGENOS-DETERMINACIÓN DE LISOZIMA Disertante: Brom. Carolina Chiconofri Departamento de Normas Analíticas Especiales Sub. De Investigación para la Fiscalización Instituto Nacional de Vitivinicultura
ALERGENOS-DETERMINACIÓN DE LISOZIMA Disertante: Brom. Carolina Chiconofri Departamento de Normas Analíticas Especiales Sub. De Investigación para la Fiscalización Instituto Nacional de Vitivinicultura
LABORATORIO DE QUÍMICA ANALÍTICA E INSTRUMENTAL 502503. GUÍA No 2.3- METODOS DE SEPARACIÓN POR DESTILACIÓN
 LABORATORIO DE QUÍMICA ANALÍTICA E INSTRUMENTAL 502503 GUÍA No 2.3- METODOS DE SEPARACIÓN POR DESTILACIÓN I. EL PROBLEMA Dos líquidos completamente miscibles se pueden separar por métodos físicos llamados
LABORATORIO DE QUÍMICA ANALÍTICA E INSTRUMENTAL 502503 GUÍA No 2.3- METODOS DE SEPARACIÓN POR DESTILACIÓN I. EL PROBLEMA Dos líquidos completamente miscibles se pueden separar por métodos físicos llamados
PRÁCTICA 4 DETERMINACIÓN DE LA CONCENTRACIÓN IÓNICA TOTAL DEL AGUA POTABLE, USANDO LA CROMATOGRAFÍA DE INTERCAMBIO IÓNICO
 PRÁCTICA 4 DETERMINACIÓN DE LA CONCENTRACIÓN IÓNICA TOTAL DEL AGUA POTABLE, USANDO LA CROMATOGRAFÍA DE INTERCAMBIO IÓNICO 1.- FUNDAMENTO TEÓRICO. 1.1.- Materiales de intercambio iónico. El intercambio
PRÁCTICA 4 DETERMINACIÓN DE LA CONCENTRACIÓN IÓNICA TOTAL DEL AGUA POTABLE, USANDO LA CROMATOGRAFÍA DE INTERCAMBIO IÓNICO 1.- FUNDAMENTO TEÓRICO. 1.1.- Materiales de intercambio iónico. El intercambio
PRUEBA RAPIDA EN EMBARAZADAS (n=62,214 2009-Junio 2010) NO REACTIVO n=218 REACTIVO INDETERMINADO. Tabla 9: Resultados Prueba rápida
 11-RESULTADOS 11.1-Interpretación y análisis de resultados Un total de de 62,214 mujeres embarazadas se realizaron la prueba rápida de VIH durante años 2009 hasta junio 2010 (Tabla 9). De ellas, 61,808
11-RESULTADOS 11.1-Interpretación y análisis de resultados Un total de de 62,214 mujeres embarazadas se realizaron la prueba rápida de VIH durante años 2009 hasta junio 2010 (Tabla 9). De ellas, 61,808
Actualizaciones. Eritropoyetina
 Actualizaciones Eritropoyetina Acciones de la eritropoyetina. La eritropoyetina es una glicoproteína plasmática que estimula la eritropoyesis y actúa además sobre otras células de la sangre como los granulocitos,
Actualizaciones Eritropoyetina Acciones de la eritropoyetina. La eritropoyetina es una glicoproteína plasmática que estimula la eritropoyesis y actúa además sobre otras células de la sangre como los granulocitos,
Dar a conocer la capacidad de disolución del agua frente a otras sustancias.
 MINISTERIO DE EDUCACION Actividad 1: Agua en la vida II. Laboratorio: Solubilidad del agua 1. Tema: AGUA DISOLVENTE UNIVERSAL 2. Objetivo: Dar a conocer la capacidad de disolución del agua frente a otras
MINISTERIO DE EDUCACION Actividad 1: Agua en la vida II. Laboratorio: Solubilidad del agua 1. Tema: AGUA DISOLVENTE UNIVERSAL 2. Objetivo: Dar a conocer la capacidad de disolución del agua frente a otras
V MATERIALES Y MÉTODOS
 V MATERIALES Y MÉTODOS 5.1 Aislamiento de bacterias e identificación 5.1.1 Cepas tomadas del cepario de la Universidad de las Américas-Puebla En el cepario del Departamento de Química y Biología hay algunas
V MATERIALES Y MÉTODOS 5.1 Aislamiento de bacterias e identificación 5.1.1 Cepas tomadas del cepario de la Universidad de las Américas-Puebla En el cepario del Departamento de Química y Biología hay algunas
IMPACTO DE LOS ESTUDIOS CON NOPAL
 RESUMEN Existe evidencia desde 1552 de los efectos medicinales del nopal. Sin embargo, hasta la fecha no se ha establecido el mecanismo por el cual el nopal ejerce su efecto sobre las concentraciones de
RESUMEN Existe evidencia desde 1552 de los efectos medicinales del nopal. Sin embargo, hasta la fecha no se ha establecido el mecanismo por el cual el nopal ejerce su efecto sobre las concentraciones de
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA
 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA PROGRAMA DE INGENIERIA DE ALIMENTOS 211612 TRANSFERENCIA DE MASA ACTIVIDAD 11 RECONOCIMIENTO UNIDAD 3 BOGOTA D.C. Extracción líquido - líquido La extracción líquido-líquido,
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA PROGRAMA DE INGENIERIA DE ALIMENTOS 211612 TRANSFERENCIA DE MASA ACTIVIDAD 11 RECONOCIMIENTO UNIDAD 3 BOGOTA D.C. Extracción líquido - líquido La extracción líquido-líquido,
INFORME PROYECTO DE INVESTIGACION
 INFORME PROYECTO DE INVESTIGACION EFECTO DE LOS EXTRACTOS DIALIZABLES EN LA RESPUESTA INMUNE HUMORAL EN UN MODELO DE INFECCIÓN IN VIVO CON HERPES SIMPLEXI CLAVE: 20070367 DR. SERGIO ANTONIO ESTRADA PARRA.
INFORME PROYECTO DE INVESTIGACION EFECTO DE LOS EXTRACTOS DIALIZABLES EN LA RESPUESTA INMUNE HUMORAL EN UN MODELO DE INFECCIÓN IN VIVO CON HERPES SIMPLEXI CLAVE: 20070367 DR. SERGIO ANTONIO ESTRADA PARRA.
Glándula Adrenal y Hormonas Adrenales EJE HIIPOTÁLAMO-HIPÓFISIS-GLÁNDULA
 Glándula Adrenal y Hormonas Adrenales EJE HIIPOTÁLAMO-HIPÓFISIS-GLÁNDULA Glándula Adrenal - Las glándulas adrenales están localizadas en la parte superior de los riñones -Cada glándula consiste de una
Glándula Adrenal y Hormonas Adrenales EJE HIIPOTÁLAMO-HIPÓFISIS-GLÁNDULA Glándula Adrenal - Las glándulas adrenales están localizadas en la parte superior de los riñones -Cada glándula consiste de una
Calculadora de Tamaño muestral GRANMO
 Calculadora de Tamaño muestral GRANMO Versión 7.12 Abril 2012 http://www.imim.es/ofertadeserveis/software-public/granmo/ Entre las distintas ofertas que existen para el cálculo del tamaño muestral, ofrecemos
Calculadora de Tamaño muestral GRANMO Versión 7.12 Abril 2012 http://www.imim.es/ofertadeserveis/software-public/granmo/ Entre las distintas ofertas que existen para el cálculo del tamaño muestral, ofrecemos
Extracción sólido-líquido
 Extracción sólido-líquido Objetivos de la práctica! Determinar la concentración de saturación del soluto en el disolvente en un sistema ternario arena-azúcar-agua, estableciendo la zona operativa del diagrama
Extracción sólido-líquido Objetivos de la práctica! Determinar la concentración de saturación del soluto en el disolvente en un sistema ternario arena-azúcar-agua, estableciendo la zona operativa del diagrama
AISLAMIENTO DE ÁCIDO DESOXIRRIBONUCLEICO (DNA) GENÓMICO Y PLASMÍDICO
 AISLAMIENTO DE ÁCIDO DESOXIRRIBONUCLEICO (DNA) GENÓMICO Y PLASMÍDICO E l estudio del genoma de los seres vivos a sido uno d los principales objetivos de la Biología. Desde los trabajos de Mendel (1866),
AISLAMIENTO DE ÁCIDO DESOXIRRIBONUCLEICO (DNA) GENÓMICO Y PLASMÍDICO E l estudio del genoma de los seres vivos a sido uno d los principales objetivos de la Biología. Desde los trabajos de Mendel (1866),
Materiales para la secuenciación de ADN
 Introduccion La Secuenciación Sanger es un método de secuenciación de ADN en el que el ADN diana se desnaturaliza y se hibrida con un cebador de oligonucleótidos, que se extiende entonces gracias a la
Introduccion La Secuenciación Sanger es un método de secuenciación de ADN en el que el ADN diana se desnaturaliza y se hibrida con un cebador de oligonucleótidos, que se extiende entonces gracias a la
Universidad Tecnológica de Panamá Centro de Investigaciones Hidráulicas e Hidrotécnicas Laboratorio de Sistemas Ambientales
 Página: 1 de 5 1. Introducción: La medición de nitratos en aguas residuales se hace en mg/l. El método es conocido usualmente con el nombre de Reducción de Cadmio, que es donde los iones de nitrito reaccionan
Página: 1 de 5 1. Introducción: La medición de nitratos en aguas residuales se hace en mg/l. El método es conocido usualmente con el nombre de Reducción de Cadmio, que es donde los iones de nitrito reaccionan
LABORATORIO: MICROBIOLOGÍA BIOQUÍMICA Y HEMATOLOGÍA.
 LABORATORIO: MICROBIOLOGÍA BIOQUÍMICA Y HEMATOLOGÍA. CS Illes Columbretes Página 1 En el laboratorio de microbiología se realizan investigaciones microbiológicas (diagnóstico bacteriológico, micológico,
LABORATORIO: MICROBIOLOGÍA BIOQUÍMICA Y HEMATOLOGÍA. CS Illes Columbretes Página 1 En el laboratorio de microbiología se realizan investigaciones microbiológicas (diagnóstico bacteriológico, micológico,
5 Materiales y Métodos
 5 Materiales y Métodos Los tejidos de Cenchurs ciliaris utilizados en esta investigación fueron obtenidos por pretratamiento con H 2 SO 4 al 0.15 M, a 135ºC, para eliminar la hemicelulosa. Con los tejidos
5 Materiales y Métodos Los tejidos de Cenchurs ciliaris utilizados en esta investigación fueron obtenidos por pretratamiento con H 2 SO 4 al 0.15 M, a 135ºC, para eliminar la hemicelulosa. Con los tejidos
SEMINARIO 2 Parámetros del grado de perecibilidad de un alimento
 UNIVERSIDAD NACIONAL DEL CENTRO DE LA PROVINCIA DE BUENOS AIRES Facultad de Ingeniería Carrera: Licenciatura en Tecnología de los Alimentos Asignatura: Bioquímica de los Alimentos I. HUMEDAD SEMINARIO
UNIVERSIDAD NACIONAL DEL CENTRO DE LA PROVINCIA DE BUENOS AIRES Facultad de Ingeniería Carrera: Licenciatura en Tecnología de los Alimentos Asignatura: Bioquímica de los Alimentos I. HUMEDAD SEMINARIO
II. METODOLOGÍA. El proceso de elaboración del biodiesel se constituye de siete pasos fundamentales: 6.1. DETERMINACIÓN DE LOS GRAMOS DE CATALIZADOR
 II. METODOLOGÍA 6. PROCESO DE ELABORACIÓN El proceso de elaboración del biodiesel se constituye de siete pasos fundamentales: 1. Determinación de los gramos de catalizador 2. Preparación del Metóxido de
II. METODOLOGÍA 6. PROCESO DE ELABORACIÓN El proceso de elaboración del biodiesel se constituye de siete pasos fundamentales: 1. Determinación de los gramos de catalizador 2. Preparación del Metóxido de
CélluVîtas Omega 3 Natural
 CélluVîtas Omega 3 Natural Descripción del producto El Omega 3 Natural extraído en frío elaborado por CélluVîtas es un complemento alimenticio que presenta una elevada concentración de ácidos grasos Omega
CélluVîtas Omega 3 Natural Descripción del producto El Omega 3 Natural extraído en frío elaborado por CélluVîtas es un complemento alimenticio que presenta una elevada concentración de ácidos grasos Omega
Tiene especial importancia la entrega ininterrumpida de oxígeno al cerebro y al corazón.
 1) Qu Qué es la SANGRE? La sangre es un tejido liquido vital, formado en la médula ósea. Está compuesta por células (Glóbulos rojos, Glóbulos blan - cos y Plaquetas) suspendidas en un líquido denominado
1) Qu Qué es la SANGRE? La sangre es un tejido liquido vital, formado en la médula ósea. Está compuesta por células (Glóbulos rojos, Glóbulos blan - cos y Plaquetas) suspendidas en un líquido denominado
El Banco Nacional de ADN oferta un control de calidad de muestras de ADN y ARN.
 PROGRAMA CONTROL DE CALIDAD DE MUESTRAS El Banco Nacional de ADN oferta un control de calidad de muestras de ADN y ARN. El programa completo de control de calidad de muestras de ADN y ARN engloba diferentes
PROGRAMA CONTROL DE CALIDAD DE MUESTRAS El Banco Nacional de ADN oferta un control de calidad de muestras de ADN y ARN. El programa completo de control de calidad de muestras de ADN y ARN engloba diferentes
PRÁCTICA Nº 5 REACCIONES DE POLIMERIZACIÓN. Objetivos
 PRÁCTICA Nº 5 REACCINES DE PLIMERIZACIÓN bjetivos - Realizar un ejemplo práctico de reacción de polimerización por condensación: Preparación de un poliéster. Preparación de una poliamida. - Resaltar la
PRÁCTICA Nº 5 REACCINES DE PLIMERIZACIÓN bjetivos - Realizar un ejemplo práctico de reacción de polimerización por condensación: Preparación de un poliéster. Preparación de una poliamida. - Resaltar la
Capítulo 6. Valoración respiratoria
 498 Capítulo 6. Valoración respiratoria 6.19. La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 6.19 La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 499
498 Capítulo 6. Valoración respiratoria 6.19. La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 6.19 La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 499
A continuación se presenta los resultados obtenidos en las pruebas realizadas en
 6.0 RESULTADOS, COMPARACIÓN Y ANALISIS. 6.1 PERMEABILIDAD. A continuación se presenta los resultados obtenidos en las pruebas realizadas en el laboratorio para la determinación del coeficiente de permeabilidad
6.0 RESULTADOS, COMPARACIÓN Y ANALISIS. 6.1 PERMEABILIDAD. A continuación se presenta los resultados obtenidos en las pruebas realizadas en el laboratorio para la determinación del coeficiente de permeabilidad
Actividad de Biología: Cromatografía de Pigmentos Vegetales Guía del Estudiante
 Actividad de Biología: Cromatografía de Pigmentos Vegetales Guía del Estudiante Objetivos: Los estudiantes serán capaces de Explicar cuáles moléculas hacen que muchas de las plantas tengan hojas verdes
Actividad de Biología: Cromatografía de Pigmentos Vegetales Guía del Estudiante Objetivos: Los estudiantes serán capaces de Explicar cuáles moléculas hacen que muchas de las plantas tengan hojas verdes
Trabajo Práctico N o 1
 1 Trabajo Práctico N o 1 Soluciones y diluciones OBJETIVOS - Conocer todas las formas de indicar la concentración química de una solución. - Ser capaz de calcular la concentración de una solución a partir
1 Trabajo Práctico N o 1 Soluciones y diluciones OBJETIVOS - Conocer todas las formas de indicar la concentración química de una solución. - Ser capaz de calcular la concentración de una solución a partir
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE QUIMICA GENERAL
 UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE QUIMICA GENERAL ESTUDIO DE LA SOLUBILIDAD Y LOS FACTORES QUE LA AFECTAN OBJETIVOS 1. Interpretar
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE QUIMICA GENERAL ESTUDIO DE LA SOLUBILIDAD Y LOS FACTORES QUE LA AFECTAN OBJETIVOS 1. Interpretar
pk A DE UN INDICADOR ÁCIDO-BASE
 pk A DE UN INDICADOR ÁCIDO-BASE OBJETIVO Determinar el pk a de un indicador ácido-base por espectroscopia visible. Descripción del Experimento Primero deben verificar la λ max de la forma con mayor absorbencia
pk A DE UN INDICADOR ÁCIDO-BASE OBJETIVO Determinar el pk a de un indicador ácido-base por espectroscopia visible. Descripción del Experimento Primero deben verificar la λ max de la forma con mayor absorbencia
REACCIONES DE IONES METÁLICOS
 Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
Dr. José Vicente García Pérez. Resumen
 Estudio de la Aplicación de Ultrasonidos de Alta Intensidad en Sistemas Sólido-Líquido y Sólido-Gas. Influencia en la Cinética de Transporte de Materia y en la Estructura de los Productos Autor César Ozuna
Estudio de la Aplicación de Ultrasonidos de Alta Intensidad en Sistemas Sólido-Líquido y Sólido-Gas. Influencia en la Cinética de Transporte de Materia y en la Estructura de los Productos Autor César Ozuna
Preparación de medios de cultivo
 Objetivos Preparación de medios de cultivo Curso: Métodos en fitopatología 24 de abril de 2009 Dr. Pedro Mondino Conocer a que denominamos medio de cultivo en el laboratorio de Fitopatología. Reconocer
Objetivos Preparación de medios de cultivo Curso: Métodos en fitopatología 24 de abril de 2009 Dr. Pedro Mondino Conocer a que denominamos medio de cultivo en el laboratorio de Fitopatología. Reconocer
.- En qué tipo de enfermos está indicado el trasplante de células de sangre de cordón umbilical?
 RESPUESTAS A LAS PREGUNTAS MÁS COMUNES SOBRE SANGRE DE CORDÓN UMBILICAL PLANTEADAS TRAS LA APROBACIÓN DEL REAL DECRETO 1301/2006 SOBRE CALIDAD Y SEGURIDAD DE CÉLULAS Y TEJIDOS Qué es la sangre del cordón
RESPUESTAS A LAS PREGUNTAS MÁS COMUNES SOBRE SANGRE DE CORDÓN UMBILICAL PLANTEADAS TRAS LA APROBACIÓN DEL REAL DECRETO 1301/2006 SOBRE CALIDAD Y SEGURIDAD DE CÉLULAS Y TEJIDOS Qué es la sangre del cordón
EQUILIBRIO QUÍMICO: REACCIONES ÁCIDO-BASE
 Página: 1/7 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 8: EQUILIBRIO QUÍMICO: REACCIONES ÁCIDO-BASE Bibliografía: Química, La Ciencia Central, T.L. Brown, H. E. LeMay, Jr., B. Bursten; Ed. Prentice-Hall, Hispanoamérica,
Página: 1/7 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 8: EQUILIBRIO QUÍMICO: REACCIONES ÁCIDO-BASE Bibliografía: Química, La Ciencia Central, T.L. Brown, H. E. LeMay, Jr., B. Bursten; Ed. Prentice-Hall, Hispanoamérica,
11.2-DISCUSIÓN Prueba rápida
 11.2-DISCUSIÓN Prueba rápida Como se observa en la tabla 9 del total de las embarazadas (62,214) a las que se les realizo la prueba rápida un 99.3%(61,808) de ellas dio como resultado no reactivo, tan
11.2-DISCUSIÓN Prueba rápida Como se observa en la tabla 9 del total de las embarazadas (62,214) a las que se les realizo la prueba rápida un 99.3%(61,808) de ellas dio como resultado no reactivo, tan
La separación de mezclas de las cuales existen dos tipos como son las homogéneas y heterogéneas
 Introducción En el tema operaciones fundamentales de laboratorio se dan una serie e pasos muy importantes para el desarrollo del programa de laboratorio por ejemplo podemos citar varios procedimientos
Introducción En el tema operaciones fundamentales de laboratorio se dan una serie e pasos muy importantes para el desarrollo del programa de laboratorio por ejemplo podemos citar varios procedimientos
(Estudios in vivo y estudios in vitro)
 (Estudios in vivo y estudios in vitro) IN VIVO: es la experimentación con un todo, que viven organismos en comparación. Ensayos con animales y ensayos clínicos son dos formas de investigación in vivo.
(Estudios in vivo y estudios in vitro) IN VIVO: es la experimentación con un todo, que viven organismos en comparación. Ensayos con animales y ensayos clínicos son dos formas de investigación in vivo.
Práctica 1A Ensayo de Granulometría Prácticas de Laboratorio
 1A ENSAYO DE GRANULOMETRÍA 1. TIPOS DE SUELO. RECONOCIMIENTO VISUAL Desde un punto de vista geotécnico, existen cuatro grandes tipos de suelos: gravas, arenas, limos y arcillas, caracterizados principalmente
1A ENSAYO DE GRANULOMETRÍA 1. TIPOS DE SUELO. RECONOCIMIENTO VISUAL Desde un punto de vista geotécnico, existen cuatro grandes tipos de suelos: gravas, arenas, limos y arcillas, caracterizados principalmente
CARDIOCHEK y CARDIOCHEK P.A
 CARDIOCHEK y CARDIOCHEK P.A NUEVA GENERACIÓN DE ANALIZADORES PORTÁTILES Introducción El Cardiochek y Cardiochek P.A son instrumentos portátiles que proporcionan medidas rápidas y precisas de múltiples
CARDIOCHEK y CARDIOCHEK P.A NUEVA GENERACIÓN DE ANALIZADORES PORTÁTILES Introducción El Cardiochek y Cardiochek P.A son instrumentos portátiles que proporcionan medidas rápidas y precisas de múltiples
HEMOGLOBINA GLICOSILADA QUE DEBE SABER EL PACIENTE?
 LA HEMOGLOBINA GLICOSILADA QUE DEBE SABER EL PACIENTE? 1 QUE ES LA HEMOGLOBINA GLICOSILADA? a hemoglobina es una proteína que se encuentra L en los glóbulos rojos de nuestra sangre y es la encargada de
LA HEMOGLOBINA GLICOSILADA QUE DEBE SABER EL PACIENTE? 1 QUE ES LA HEMOGLOBINA GLICOSILADA? a hemoglobina es una proteína que se encuentra L en los glóbulos rojos de nuestra sangre y es la encargada de
constituye aproximadamente el 60% de la reserva de aminoácidos del músculo esquelético.
 Qué es la glutamina? La glutamina es el más abundante aminoácido libre en el cuerpo humano, y constituye aproximadamente el 60% de la reserva de aminoácidos del músculo esquelético. La glutamina es un
Qué es la glutamina? La glutamina es el más abundante aminoácido libre en el cuerpo humano, y constituye aproximadamente el 60% de la reserva de aminoácidos del músculo esquelético. La glutamina es un
EQUILIBRIO QUÍMICO: EQUILIBRIO ÁCIDO-BASE
 EQUILIBRIO QUÍMICO: EQUILIBRIO ÁCIDO-BASE Cynthia Fernandez - cyntuche@hotmail.com Algunos indicadores entre los cuales se encuentran la fenolftaleína y el azul de bromotimol (fucsia y azul respectivamente).
EQUILIBRIO QUÍMICO: EQUILIBRIO ÁCIDO-BASE Cynthia Fernandez - cyntuche@hotmail.com Algunos indicadores entre los cuales se encuentran la fenolftaleína y el azul de bromotimol (fucsia y azul respectivamente).
UNIDAD 3: SOLUCIONES
 UNIDAD 3: SOLUCIONES 1 Las soluciones son mezclas homogéneas. Estas constan de dos o más componentes en una única fase, por ejemplo agua con sal de cocina, o azúcar en agua Para estudiar o trabajar con
UNIDAD 3: SOLUCIONES 1 Las soluciones son mezclas homogéneas. Estas constan de dos o más componentes en una única fase, por ejemplo agua con sal de cocina, o azúcar en agua Para estudiar o trabajar con
Biotecnología. Historia y aplicaciones Su utilización en el INTA Alto Valle. investigación
 Alejandro Giayetto Técnico INTA agiayetto@correo.inta.gov.ar Mirta Rossini Técnico INTA mrossini@correo.inta.gov.ar Diana Vera Biotecnóloga labfitopatologia@correo.inta.gov.ar investigación 10 Biotecnología
Alejandro Giayetto Técnico INTA agiayetto@correo.inta.gov.ar Mirta Rossini Técnico INTA mrossini@correo.inta.gov.ar Diana Vera Biotecnóloga labfitopatologia@correo.inta.gov.ar investigación 10 Biotecnología
Determinación del equivalente eléctrico del calor
 Determinación del equivalente eléctrico del calor Julieta Romani Paula Quiroga María G. Larreguy y María Paz Frigerio julietaromani@hotmail.com comquir@ciudad.com.ar merigl@yahoo.com.ar mapaz@vlb.com.ar
Determinación del equivalente eléctrico del calor Julieta Romani Paula Quiroga María G. Larreguy y María Paz Frigerio julietaromani@hotmail.com comquir@ciudad.com.ar merigl@yahoo.com.ar mapaz@vlb.com.ar
LABORATORIO DE QUÍMICA FACULTAD DE FARMACIA CRISTALIZACIÓN.
 CRISTALIZACIÓN. Un compuesto orgánico cristalino está constituido por un empaquetamiento tridimensional de moléculas unidas principalmente por fuerzas de Van der Waals, que originan atracciones intermoleculares
CRISTALIZACIÓN. Un compuesto orgánico cristalino está constituido por un empaquetamiento tridimensional de moléculas unidas principalmente por fuerzas de Van der Waals, que originan atracciones intermoleculares
Estudio de la evaporación
 Estudio de la evaporación Volumen del líquido Tipo de líquido Superficie del recipiente Altura del recipiente Forma del recipiente Presencia de una sal disuelta Introducción Todos hemos observado que una
Estudio de la evaporación Volumen del líquido Tipo de líquido Superficie del recipiente Altura del recipiente Forma del recipiente Presencia de una sal disuelta Introducción Todos hemos observado que una
Calf Notes.com. Notas Acerca de Terneros #39 - Usando el refractómetro
 Calf Notes.com Notas Acerca de Terneros #39 - Usando el refractómetro Introducción. El medir el grado de transferencia de inmunidad pasiva a los terneros recién nacidos puede decirle mucho acerca del nivel
Calf Notes.com Notas Acerca de Terneros #39 - Usando el refractómetro Introducción. El medir el grado de transferencia de inmunidad pasiva a los terneros recién nacidos puede decirle mucho acerca del nivel
Liceo Chachagua. Cómo se ve afectado el porcentaje de Oxígeno Disuelto en el agua, al comparar dos sectores del Río Chachagüita separados por la Zona
 Liceo Chachagua Cómo se ve afectado el porcentaje de Oxígeno Disuelto en el agua, al comparar dos sectores del Río Chachagüita separados por la Zona central de la Comunidad de Chachagua, durante los meses
Liceo Chachagua Cómo se ve afectado el porcentaje de Oxígeno Disuelto en el agua, al comparar dos sectores del Río Chachagüita separados por la Zona central de la Comunidad de Chachagua, durante los meses
Código: IDK-010 Ver: 1. Proteína G C825T. Sistema para la detección de la mutación C825T en el gene de la proteína G.
 C825T Sistema para la detección de la mutación C825T en el gene de la proteína G. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy www.atgen.com.uy
C825T Sistema para la detección de la mutación C825T en el gene de la proteína G. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy www.atgen.com.uy
Cómo llevar a cabo una reacción química desde el punto de vista experimental
 Cómo llevar a cabo una reacción química desde el punto de vista experimental Para obtener un compuesto se pueden utilizar varias técnicas, que incluyen el aislamiento y la purificación del mismo. Pero
Cómo llevar a cabo una reacción química desde el punto de vista experimental Para obtener un compuesto se pueden utilizar varias técnicas, que incluyen el aislamiento y la purificación del mismo. Pero
I. DATOS DE IDENTIFICACIÓN
 UNIVERSIDAD AUTÓNOMA DE BAJA CALIFORNIA COORDINACION DE FORMACION BASICA COORDINACION DE FORMACION PROFESIONAL Y VINCULACIÓN PROGRAMA DE UNIDAD DE APRENDIZAJE 1. Unidad Académica: FACULTAD DE CIENCIAS
UNIVERSIDAD AUTÓNOMA DE BAJA CALIFORNIA COORDINACION DE FORMACION BASICA COORDINACION DE FORMACION PROFESIONAL Y VINCULACIÓN PROGRAMA DE UNIDAD DE APRENDIZAJE 1. Unidad Académica: FACULTAD DE CIENCIAS
