UNIVERSIDAD AUSTRAL DE CHILE INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 1
|
|
|
- Margarita Núñez Ríos
- hace 7 años
- Vistas:
Transcripción
1 INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 1 EQUILIBRIO ACIDO-BASE La función celular es óptima cuando el ph del LEC es 7.4 ([H+] de 40 nmoles/litro). Sin embargo hay muchas situaciones, especialmente enfermedades, donde el ph plasmático varía de lo normal, produciendo un cambio en el estado de ionización de grupos químicos, alterando la actividad de enzimas y la integridad de las membranas celulares. Cambios que son peligrosos para la vida y por lo tanto requieren inmediata corrección. Un estado en que el ph del LEC es bajo es conocido como acidosis y la situación opuesta en que el ph aumenta como alcalosis; ambos estados reflejan una alteración en la regulación de la [H+] del LEC. La actividad metabólica normal, contínuamente genera una carga de ácido que es regulada dentro del organismo por : - Buffers químicos intracelulares y extracelulares. - Regulación respiratoria de la [CO2] - Excreción de ácido y regeneración de los sistemas buffer del organismo por el riñón. Estos mecanismos regulatorios son complementarios y el riñón y el pulmón tienen considerable capacidad compensatoria, el riñón por regulación de excreción de ácidos o bases y el pulmón por variación de la tasa de CO2 ventilado. Las alteraciones ácido-base pueden ser clasificadas según su origen en respiratorias o metabólicas. La acidosis o alcalosis respiratoria derivan de una disfunción respiratoria primaria y la acidosis y alcalosis metabólica pueden ser de origen renal o alimentario. La acidosis metabólica también puede ser producida por el aumento de la producción de ácido, ej. ácido láctico despues de un ejercicio intenso o no acostumbrado. En algunas situaciones las alteraciones ácido base son complejas y a pesar de la significativa pérdida de ácido o base corporal, el ph plasmático se mantiene dentro del rango normal por ejemplo un paciente con vómito severo y diarrea, donde se pierden grandes cantidades de ácido y base corporal. MECANISMOS DE REGULACION I. AMORTIGUACION Sistema Buffer El fundamento de la regulación ácido-base es la ecuación de Henderson-Hasselbalch, que deriva de las características de un sistema buffer simple que consiste en un ácido débil y una base conjugada, y se representa: HA ===== H+ + A- (1) Dentro de ciertos límites, un buffer puede mantener una [H+]p constante cuando aumenta el ácido o la base. Si aumentan los H+ en solución el equilibrio se desplaza hacia la izquierda y el aumento de base o disminución de H+ desplaza el equilibrio hacia la derecha. Cuando la reacción expresada por esta ecuación está en equilibrio, la [H+] y [A-] son una fracción constante de [HA]. Este equilibrio puede ser expresado por: K= [H+][A-] (2) donde K es la constante de disociación [HA] A partir de la ecuación (2) se obtiene una expresión de la [H+]: [H+] = K[HA] (3) [A-] luego: -log[h+]= -logk + log [A-] (4) [HA] puede ser escrita como la ecuación de Henderson-Hasselbalch: ph = pk + log [A-] (5) [HA] Un sistema buffer es más efectivo cuando el ph y pk son iguales y la relación [A-] / [HA] es uno. Hay varios sistemas buffer en el organismo, los cuales estan localizados en el plasma, eritrocitos, fluido intersticial, fluido intracelular y los minerales de la matriz osea. 1
2 INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 2 Buffer bicarbonato El sistema buffer bicarbonato constituye alrededor del 75% de la capacidad buffer del plasma y alrededor del 40% de la capacidad buffer total del eritrocito, la mayor parte de la capacidad del fluido intersticial y un una proporción de la capacidad intracelular. El sistema se fundamenta en la siguiente ecuación: CO2 + H2O ==== H2CO3 ==== H+ + HCO3- (6) que traspasado a la ecuación de Henderson-Hasselbalch queda de la siguiente manera: ph = pk + log [HCO3-] (7) [H2CO3] a temperatura corporal de 36-37ºC el pk de este sistema es 6.1 y el coeficiente de solubilidad del CO2 es de 0.03 mmoles/mmhg. ph = log [HCO3-] Donde HCO3 es concentración normal en plasma: 24 mmoles/l 0.03xPCO2 y PCO2 es presión parcial de CO2 en el plasma: 40 mmhg Cuando el ph es 7.4, la relación: [HCO3-] / 0.03 x PCO2 = 20 : 1 24 / 0.03 x / 1.2 = 20 : 1 Considerando que las condiciones para que un sistema buffer sea óptimo es que la relación de la base y el ácido sea 1 : 1, éste sistema no parece ser el mejor. Sin embargo este sistema buffer es muy eficiente, porque actúa como un sistema abierto, donde la PaCO2 es mantenida constante en 40 mmhg, por el sistema respiratorio y la [HCO3-]p por el riñón. Bajo estas condiciones la adición de ácido fijo puede disminuir la [HCO3-]p, pero el cambio en el ph es mínimo porque se mantiene constante la PaCO2. El sistema bicarbonato es incapaz de tamponear por si mismo el H2CO3. Este es tamponeado dentro de los eritrocitos por la hemoglobina (Hb), proteínas y fosfatos. La enzima anhidrasa carbónica cataliza la formación de H2CO3 a partir de CO2 y H2O, el ácido se ioniza en H+ y HCO3- (6) y el H+ es tamponeado principalmente por Hb, el HCO3-abandona el eritrocito hacia el plasma y se intercambia con un Cl-. El riñón juega un importante rol en la conservación de las reservas de NaHCO3 del organismo a través de un proceso de reabsorción y regeneración de buffer. El sistema respiratorio controla la [CO2] corporal, este componente respiratorio se representa por PCO2. El HCO3-representa el componente metabólico o renal. Buffer fosfato: Bajo condiciones fisiológicas, la función del sistema buffer fosfato es optimizada en la ecuación: H2PO4- === HPO4= + H+ que tiene un pk de 6.8. Este sistema es muy importante en el LIC y también dentro del lumen tubular renal, donde juega un rol muy importante como buffer urinario. Proteinas: (S. Anfoteras) Los grupos ácidos y bases de la molécula de proteina poseen un gran potencial amortiguador y son capaces de tamponear H2CO3 (Hb) y ácido de origen metabólico. Las proteinas son importantes en la amortiguación intracelular y en el plasma, con Hb predominando en los eritrocitos. La mayor capacidad de tampón de la Hb es proporcionada por el grupo imidazol de la histidina y las regiones N-terminal de la valina. La Hb es más efectiva como amortiguador en su forma desoxigenada, debido al efecto del O2 sobre el valor del pk. 2
3 INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 3 II. ELIMINACION RESPUESTA RESPIRATORIA. El sistema respiratorio es vital en la mantención del estado ácido-base a través de la regulación de la PaCO2. Cuando se acumula CO2 en el plasma se genera ácido, cuando el CO2 disminuye también lo hace el ácido. La alta solubilidad del CO2 en lipidos, permite que éste cruce la barrera hematoencefálica fácilmente, de tal manera que si el CO2 aumenta en el plasma, rapidamente se produce disminución del ph del fluido cerebro espinal. En respuesta a este cambio de ph, los quimio-receptores centrales estimulan la hiperventilación dentro de pocos minutos en un esfuerzo por eliminar el excedente de CO2. Una PCO2 baja puede producir hipoventilación, pero este mecanismo puede ser anulado si concomitantemente hay una severa hipoxia. Un aumento en la [H+]p o una disminución del O2, estimulan los quimiorreceptores aórtico y carotídeos y se produce hiperventilación. Significado de la medición de CO2 y O2. La eliminación de CO2 por el pulmón depende de su capacidad funcional, sin embargo la interrogante del intercambio de O2 no puede ser ignorada. La PO2 es un importante indicador de la función pulmonar y aunque este no tiene influencia directa sobre el equilibrio ácido-base, a menudo indica el origen de una alteración ácidobase. Dióxido de carbono La PaCO2 es una medida del CO2 disuelto en el plasma. La PaCO2 depende del equilibrio entre su producción metabólica y su remoción por el pulmón. El rango normal para la PaCO2 es desde 35 a 40 mmhg. Valores más altos indican hipercapnia, y valores más bajos hipocapnia. Hipercapnia es frecuentemente el resultado de hipoventilación, pero puede ocurrir en pacientes sometidos a anestesia, uso de un circuito de anestesia con un gran espacio muerto, o cuando las maquinas de anestesia poseen una reducida unidad de soda, aumenta la PaCO2. Hipocapnia es invariablemente el resultado de hiperventilación. Oxigeno La PO2 es usualmente determinada en la sangre arterial, pero es solamente una medida del O2 disuelto en el plasma y no de la cantidad total presente en la sangre. PaO2 es un reflejo de la función de intercambio gaseoso pulmonar, y el rango normal es mmhg. Cuando baja de este rango se produce hipoxemia y puede bajar hasta 60 mmhg o menos, la hipoxemia severa es un fuerte estimulante respiratorio. La PaO2 mayor de 100 mmhg produce Hiperoxia; como la Hb esta saturada un 97% cuando la PaO2 es 100 mmhg, la hiperoxia tiene un pequeño efecto sobre la saturación de la Hb. Hiperoxia nunca ocurre como un estado natural en una enfermedad, pero es algunas veces el resultado de la administración de una mezcla de gas anestésico rico en O2. Algunas causas conocidas de hipoxemia son: baja concentración de O2 en el aire inspirado, hipoventilación, alteración en la difusión de gases, alteración en la relación ventilación perfusión y shunt vascular pulmonar. RESPUESTA RENAL. La producción de ácido fijo en el organismo es consecuencia principalmente del catabolismo proteico, con una pequeña contribución de la degradación de fosfolípidos y ácidos nucleicos. El H+ es amortiguado inicialmente por los sistemas buffer intra y extracelular, pero el la celula tubular renal genera H+ y los secreta hacia la orina. La excreción renal de hidrógeno se hace por los mecanismo de: reabsorción de bicarbonato, titulación de fosfatos y excreción de amonio. 3
4 INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 4 Reabsorción de Bicarbonato: Este mecanismo se realiza en el túbulo contorneado proximal, a partir del NaHCO3 filtrado por el glomerulo, el Na+ filtrado es intercambiado por H+ que se combina con el HCO3-filtrado en el lumen tubular formando H2CO3 el cual se disocia en CO2 y H2O. El CO2 rápidamente difunde hacia la célula tubular, donde puede unirse a H2O formando H2CO3 bajo influencia de anhidrasa carbónica. La disociación del H2CO3 de H+ y HCO3; el H+ se intercambia por Na+ y el bicarbonato se mueve hacia el plasma, este HCO3- no es el inicialmente filtrado. El CO2 que difunde desde el filtrado al plasma es eliminado por el pulmón. TUBULO RENAL CELULA TUBULAR PLASMA HCO3- + Na+- Na+ Na+ H+ H+ + HCO3- HCO3- H2CO3 H2O +CO2 H2CO3 CO2 + H2O CO2 CO2 Titulación de Fosfato: Este mecanismo se basa en la cantidad de Na2HPO4 filtrado el cual se disocia a Na+ y NaHPO4-. El Na+ se intercambia por H+ producido por la célula tubular a partir de la ionización de H2CO3 que fue formado de la unión de CO2 y H2O. El H+ es eliminado en el NaH2PO4. Excreción del amonio: Este mecanismo depende de la generación de amoniaco por el metabolismo de la célula tubular, a partir de glutamina y otros amino ácidos. El NH3 difunde rápidamente al lumen tubular donde se une al H+ para formar NH4+ que es no difusible. Los mecanismos del fosfato y del amonio regeneran HCO3- y determinan la acidez neta de la orina en que una gran cantidad de H+ puede ser concentrado en la orina sin disminuir el ph. En acidosis, cuando aumenta la [H+] estos mecanismos renales pueden responder eliminando más ácidos en la orina, pero pueden demorar entre 4 a 5 días en alcanzar su máxima efectividad en el caso de amonio. Algunos factores pueden influenciar la actividad de estos mecanismos renales. Si disminuye la reabsorción de Na+ disminuye la excreción de H+ en la orina y predispone a la acidosis; ésto puede ocurrir si hay expansión del LEC, debido a que en estos casos la reabsorción de Na+ está disminuída. La secreción de H+ también disminuye cuando se inhibe la anhidrasa carbónica por drogas como la acetozolamida. En cambio, cuando se aumenta la reabsorción de Na+, ej. cuando aumenta aldosterona, cantidades importantes de H+ y K+ pueden perderse por la orina, y al mismo tiempo se aumenta la reabsorción de HCO3-. En alcalosis, cuando la [HCO3-]p excede los 28 mmoles/litro, el HCO3- filtrado aumenta y el intercambio de Na+ por H+ es reducido y se elimina HCO3- por la orina. Medición del estado acido-base Se realiza usando un equipo analizador de gases sanguíneos, se utiliza una muestra de sangre arterial heparinizada y obtenida y mantenida en condiciones anaerobicas, esta muestra puede mantenerse congelada, el equipo permite medir ph, PCO2 y PO2. Interpretación de las alteraciones ácido-base Es importante que los resultados de los gases sanguíneos sean interpretados con el conocimiento de la historia y detalles del examen clínico del paciente. 4
5 INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 5 Los resultados de los gases sanguíneos pueden ser interpretados de la siguinte manera: el ph plasmático indica si el pacientel está con acidosis o alcalosis. La PCO2 es el componente respiratorio, depende de una adecuada función ventilatoria y está relacionada con la tasa metabólica. FISIOPATOLOGIA DE LAS ALTERACIONES ACIDO-BASE. Acidosis Respiratoria Se presenta cuando el pulmón no es capaz de eliminar el CO2 a una tasa suficientemente rápida, y esto es causado por una hopoventilación. Condiciones precipitante de acidosis respiratoria: - Depresión centro respiratorio bulbar (CRB): Ej.anestesia, sedantes, traumas SNC, aumento de la presión del LCR. - Disminución de la función pulmonar: obstrucción de las vias aéreas, neumonía, edema pulmonar, neumotorax, hemotorax, hidrotorax, atelectasia, distensión abdominal, inadecuada mecánica de ventilación. Bajo estas condiciones la PCO2 aumenta y como es un gas fácilmente difusible ingresa a los eritrocitos, donde la anhidrasa carbónica cataliza la formación de H2CO3 que se ioniza en H+ y HCO3-. El HCO3-abandona el eritrocito en intercambio por Cl-, proceso conocido como desviación del cloruro, y el H+ es amortiguado por la Hb. En otras células el H+ formado en el LEC puede ingresar a las células en intercambio por K+, aumentando la [K+]p hipercalemia o hiperpotasemia. De acuerdo a la ley de acción de masas cuando se ioniza el H2CO3 produce H+ y HCO3 en forma proporcional hasta un límite de alrededor de 32 mmoles/l [HCO3-]p cuando la PCO2 aumenta hasta aprox. 80 mmhg. Sobre este límite por cada 10 mmhg que aumente la PCO2 la [HCO3-]p podría aumentar 1 mmol/l en acidosis respiratoria aguda, y 3-4 mmoles/l en enfermedad crónica. El riñon responde a la acidosis respiratoria con la excreción de H+ y reabsorción y regeneración de HCO3-. Acidosis Metabólica: Se produce cuando el riñón es incapaz de eliminar el H+ generado por la actividad metabólica o también cuando hay una perdida excesiva de HCO3-corporal. Causas comunes de acidosis metabolica: a) disminución de la excreción renal de H+: - insuficiencia renal - inhibición de la anhidrasa carbónica b) pérdida del HCO3- corporal: - diarrea - daño del túbulo proximal del riñon c) aumento en la producción de H+: - cetoacidosis diabética - acidosis láctica - intoxicación (etilen glicol, salicilatos, metanol). Durante la Acidosis metabólica la mayor cantidad de H+ son amortiguados por buffer intracelular y extracelular. El H+ ingresa a la célula en intercambio por K+ predisponiendo a una hipercalemia, esta tendencia no se da en pacientes que presentan enfermedades que cursan con una gran pérdida de K+ como son diarreas severas y necrosis tubular aguda del riñón. Si la alteración es prolongada, algunos H+ pueden intercambiarse con Ca++ de los huesos para amortiguarse. El ph plasmático disminuye y la PCO2 aumenta, los quimio-receptores estimulan un incremento compensatorio de la ventilación pulmonar. La hiperventilación es un signo usado para el diagnóstico. Esta respuesta respiratoria es iniciada rápidamente y puede ser máxima en algunas horas, cuando la compensación respiratoria es máxima. Si el riñón está sano, los mecanismos renales ajustan al máximo la conservación de HCO3- y la excreción de H+, acidificando la orina. Daño renal extensivo puede limitar la eficacia de la respuesta renal, pero el ph de la orina puede ser menor que 6 en desórdenes como cetoacidosis diabética. 5
6 INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 6 La terapeutica de la acidosis metabólica esta basada en la rápida remoción, si es posible, de la causa básica, la corrección de los desbalances del volumen y de la concentración de los electrolitos del LEC y la mantención de una adecuada función renal. Si todo esto se realiza los mecanismos normales del organismo pueden corregir la acidosis. Sin embargo, si la causa básica de la acidosis es díficil de remover y la acidosis es severa, la administración de solución de bicarbonato es recomendada. Esto debe hacerse cautelosamente, pués la administración excesivamente rápida puede producir serios problemas. Los precursores del bicarbonato, como son lactato, acetato, gluconato, o citrato pueden ser usados en algunas circunstancias, pero también ellos tienen sus inconvenientes; lactato por ej: requiere metabolismo hepático para ser convertido y es contraindicado en pacientes con enfermedad hepática. Alcalosis respiratoria Es el resultado de hiperventilación y la PCO2 es anormalmente baja. Algunas de las causas precipitantes comunes son: Hiperventilación por dolor, excitación y enfermedad del SNC: meningitis, encefalitis y hemorragia. Además de presión de ventilación muy positiva, hipoxia arterial severa (enfermedad respiratoria severa y anemia), hipertermia y fiebre. La excesiva eliminación de CO2 disminuye la concentración de H+ y de HCO3- como lo muestra la siguiente ecuación: H+ + HCO3- ===== H2CO3 ==== CO2 + H2O El desplazamiento hacia la derecha de esta reacción produce la liberación de H+ por los buffer intracelulares en intercambio por K+, lo cual produce tendencia a Hipocalemia, que es exacerbada por la respuesta renal que retiene H+ e elimina K+. En adición los mecanismos renales promueven la eliminación de HCO3- y la retención de cloro. La alcalosis respiratoria es severa cuando la PCO2 disminuye a alrededor de 20 mmhg y ph aumenta a alrededor de 7.6. En este punto algunos mecanismos entran en juego tales como: a) vasocontricción periférica, b) disminuye la habilidad de la hemoglobina de liberar O2. c) se estimula la producción de ácido láctico por los eritrocitos via la enzima fosfofructoquinasa. En alcalosis respiratoria aguda la [HCO3-]p disminuye en aprox. 1 a 3 mmoles/l por cada 10 mmhg que disminuye la PCO2, en alcalosis respiratoria crónica la reducción de la [HCO3-]p es aprox. 5 mmoles/l. Alcalosis Metabólica Puede ser el resultado de excesiva pérdida de H+ o un desvío de H+ desde el LEC al LIC, o excesiva infusión de solución alcalinizante como es NaHCO3. Causas de alcalosis metabólica: vómito, terapia con diureticos y obstrucción pilorica o duodenal. Consideraciones fisiopatológicas de la alcalosis metabólica. La relación entre la excreción renal de H+ y regeneración de HCO3- es muy importante, pero también es importante en este punto la secreción gástrica de H+ que también genera HCO3- que entra al plasma. Normalmente los H+ secretados en el lumen gástrico son recuperados en el intestino delgado, pero podrían ser perdidos por vómito o secuestro gástrico y ocurre alcalosis. Ademas, el vómito severo puede causar hipovolemia, y esto puede producir la reabsorción de Na+, excreción de H+ (aciduria paradojal) y regeneración de HCO3-. Esto puede exacerbar la alcalosis inducida por el vómito. Hipocalemia predispone a alcalosis metabólica por la salida de K+ y el ingreso de H+ a la célula. Es por esta via que el hiperaldosteronismo produce alcalosis metabólica. 6
7 INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 7 La respuesta respiratoria a la alcalosis metabólica es hipoventilación. La ventilación alveolar es reducida y la PCO2 aumenta entre 0.5 a 1.0 mmhg por cada 1 mmol/l que aumenta la [HCO3-]p. La hipoventilación disminuye la PO2, lo que limita la respuesta respiratoria. La respuesta renal es excretar una orina alcalina. En ocasiones, sin embargo, hay una aciduria paradojal, cuando en el túbulo contorneado distal el Na+ es intercambiado por H+ más que por K+ y el ph de la orina se mantiene ácido. Los principios terapéuticos involucrados en el tratamiento de una alcalosis metabólica son la corrección del volumen, y los déficit de Na+, Cl+ y K+. La restitución de Na+ y Cl+ sin K+, puede exacerbar el problema en presencia de hipocalemia severa, por posterior promoción del intercambio renal de Na+ por H+ y ademas de la regeneración de HCO3-. La restitución del K+ es particularmente importante en el hiperaldosteronismo. Si los mecanismos regulatorios no son capaces de corregir el problema, se puede infundir soluciones acidificantes, pero su administración debe ser cuidadosamente monitoreada. Soluciones isotónicas de cloruro de arginina y lisina, cloruro de amonio y ácido clorhídrico pueden ser infundidos. Todos los compuestos con la excepción de ácido clorhídrico requieren inicialmente metabolismo hepático y están contraindicado cuando existe una alteración hepática o renal. Efecto de la alteración del equilibrio ácido base sobre otros organos. Junto con la estimulación de la función respiratoria y renal para tratar de corregir la alteración del equilibrio ácido base, la función de otros sistemas orgánicos incluyendo al sistema nervioso y cardiovascular son alterados por la alteracion ácido base. Un aumento o disminución de los niveles de CO2 y un aumento de la [H+] tienen efecto narcotizante sobre el cerebro. Consecuentemente pacientes con estos cambios pueden parecer deprimidos. El aumento de los niveles de CO2 y de la [H+] tienen diferentes efectos sobre el sistema cardiovascular. Cuando los cambios son pequeños, la función circulatoria es usualmente mantenida a través de la estimulación del sistema simpático adrenal. Esta respuesta prevalece sobre la acción depresiva directa de CO2 e H+ sobre miocardio y vasos. Si la acidosis es severa se produce marcada depresión del miocardio y vasodilatación periférica, lo cual reduce drásticamente la eficiencia del sistema circulatorio. Alcalosis respiratoria y metabólica tienen un efecto estimulatorio moderado sobre el miocardio. Acidosis y alcalosis metabólica severa pueden inducir arritmias cardíacas severas. El ph, influye en la K de ionización de los fármacos y en la unión a proteinas plasmáticas. Las formas no ionizadas difunden facilmente a través de la membrana celular. APUNTES FISIOPATOLOGIA: FARM 212 7
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS
 EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
SOLUCIONES BUFFERS. pk = valor de ph en el cual las concentraciones del ácido y la sal son iguales
 SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
1. Líquidos corporales. 2. Anatomía y función renal. 3. Hormonas ADH y aldosterona
 1. Líquidos corporales 2. Anatomía y función renal 3. Hormonas ADH y aldosterona Propiedades de la Homeostasis 1. Importancia tanto del sistema nervioso como del endocrino. 2. Controles antagónicos. 3.
1. Líquidos corporales 2. Anatomía y función renal 3. Hormonas ADH y aldosterona Propiedades de la Homeostasis 1. Importancia tanto del sistema nervioso como del endocrino. 2. Controles antagónicos. 3.
Ventilación Pulmonar. -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón
 Ventilación Pulmonar -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón Funciones básicas de la ventilación pulmonar Intercambio gaseoso con el ambiente. Regular el acidez en sangre. Comunicación
Ventilación Pulmonar -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón Funciones básicas de la ventilación pulmonar Intercambio gaseoso con el ambiente. Regular el acidez en sangre. Comunicación
Organización Funcional y el Medio Interno
 Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Programa 3º Curso. Curso (Prof. M García-Caballero)
 Programa 3º Curso Departamento de Cirugía Curso 2008-09 Equilibrio i hidroelectrolítico lí i y ácido-base (Prof. M García-Caballero) http://www.cirugiadelaobesidad.net/ CAMBIOS DE FLUIDOS Y ELECTROLITOS
Programa 3º Curso Departamento de Cirugía Curso 2008-09 Equilibrio i hidroelectrolítico lí i y ácido-base (Prof. M García-Caballero) http://www.cirugiadelaobesidad.net/ CAMBIOS DE FLUIDOS Y ELECTROLITOS
ESTADO ACIDO BASE ACIDOSIS METABOLICA. ETIOLOGÍA DE LA ACIDOSIS METABÓLICA Inhabilidad Para Secretar La Carga Acida De La Dieta +
 ESTADO ACIDO BASE Los siguientes pasos son usados para evaluar los desordenes acidobase: 1.Determinar la anormalidad de base acidosis metabólica y/o alcalosis metabólica. 2.Determinar los factores contribuyentes
ESTADO ACIDO BASE Los siguientes pasos son usados para evaluar los desordenes acidobase: 1.Determinar la anormalidad de base acidosis metabólica y/o alcalosis metabólica. 2.Determinar los factores contribuyentes
capnografia volumetrica NICO Claudia Eyzaguirre G. Enfermera clínica.
 capnografia volumetrica NICO Claudia Eyzaguirre G. Enfermera clínica. El CO2 es un producto final del O2 utilizado por las células después del metabolismo celular. Una vez que el CO2 alcanza los pulmones
capnografia volumetrica NICO Claudia Eyzaguirre G. Enfermera clínica. El CO2 es un producto final del O2 utilizado por las células después del metabolismo celular. Una vez que el CO2 alcanza los pulmones
ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO
 Toxicología alimentaria Diplomatura de Nutrición humana y dietética Curso 2010-2011 ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO Dr. Jesús Miguel Hernández-Guijo Dpto. Farmacología
Toxicología alimentaria Diplomatura de Nutrición humana y dietética Curso 2010-2011 ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO Dr. Jesús Miguel Hernández-Guijo Dpto. Farmacología
Cátedra de Fisiología Humana CAPÍTULO I CAPITULO III. Equilibrio Acido Base PH. Carrera de Enfermería. Universidad Nacional del Nordeste
 CAPÍTULO I Cátedra de Fisiología Humana CAPITULO III Equilibrio Acido Base PH Carrera de Enfermería. Universidad Nacional del Nordeste 37 CAPITULO 3: Cada soluto del organismo, el sodio, el potasio, el
CAPÍTULO I Cátedra de Fisiología Humana CAPITULO III Equilibrio Acido Base PH Carrera de Enfermería. Universidad Nacional del Nordeste 37 CAPITULO 3: Cada soluto del organismo, el sodio, el potasio, el
Alteraciones de los Fluidos Corporales, Electrolitos
 Alteraciones de los Fluidos Corporales, Electrolitos Introducción Abner J. Gutiérrez Chávez, MVZ, MC. Facultad de Medicina Veterinaria y Zootecnia, UNAM. Dpto. Producción Animal: Rumiantes Existen diversas
Alteraciones de los Fluidos Corporales, Electrolitos Introducción Abner J. Gutiérrez Chávez, MVZ, MC. Facultad de Medicina Veterinaria y Zootecnia, UNAM. Dpto. Producción Animal: Rumiantes Existen diversas
Pauta de corrección guía IV medio Homeostasis
 Pauta de corrección guía IV medio Homeostasis Actividad 1.- Registra la temperatura ambiental en un día cada una hora. Así mismo registra la temperatura corporal que tu cuerpo tiene en cada hora. Grafica
Pauta de corrección guía IV medio Homeostasis Actividad 1.- Registra la temperatura ambiental en un día cada una hora. Así mismo registra la temperatura corporal que tu cuerpo tiene en cada hora. Grafica
Trastornos respiratorios. Acidosis y alcalosis
 Trastornos respiratorios Acidosis y alcalosis Acidosis Respiratoria Trastorno que se caracteriza por aumento primario de la paco2 con elevación de la concentración de H+ en sangre, disminución del ph y
Trastornos respiratorios Acidosis y alcalosis Acidosis Respiratoria Trastorno que se caracteriza por aumento primario de la paco2 con elevación de la concentración de H+ en sangre, disminución del ph y
Tema 2. El agua, el ph y los equilibrios iónicos
 Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
Un adulto sano, suele ser capaz de mantener los equilibrios hidroelectrolíticos y ácido-base.
 BALANCE HIDRICO BALANCE HIDRICO Para conservar la salud y mantener las funcíones corporales, es necesario un EQUILIBRIO líquido, electrolítico y ácido báse. El requerimiento es: aporte y eliminación armónico
BALANCE HIDRICO BALANCE HIDRICO Para conservar la salud y mantener las funcíones corporales, es necesario un EQUILIBRIO líquido, electrolítico y ácido báse. El requerimiento es: aporte y eliminación armónico
8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE A continuación se presentan una serie de casos prácticos resueltos,
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE A continuación se presentan una serie de casos prácticos resueltos,
DESORDEN ACIDO BASICO
 DESORDEN ACIDO BASICO Cuando se habla de regulacion del equilibrio acido base, se habla en realidad de la Regulacion de la concentracion de iones hidrogenos en los liquidos corporales 1 Como la concentracion
DESORDEN ACIDO BASICO Cuando se habla de regulacion del equilibrio acido base, se habla en realidad de la Regulacion de la concentracion de iones hidrogenos en los liquidos corporales 1 Como la concentracion
El Sistema Nervioso Autónomo en el Nativo de Altura
 El Sistema Nervioso Autónomo en el Nativo de Altura María Rivera-Ch 1, Marc J. Drinkhill 2, Roger Hainsworth 2 1 UPCH, 2 Universidad de Leeds Esquema de la presentación I. Poblaciones que viven en la altura
El Sistema Nervioso Autónomo en el Nativo de Altura María Rivera-Ch 1, Marc J. Drinkhill 2, Roger Hainsworth 2 1 UPCH, 2 Universidad de Leeds Esquema de la presentación I. Poblaciones que viven en la altura
Fisiología y envejecimiento Aparato urinario. Tema 11
 Tema 11 Funciones generales. Anatomía Nefrona Filtración glomerular Reabsorción tubular Secreción tubular Micción Envejecimiento Funciones generales * Mantenimiento de la homeostasis hídrica y electrolítica.
Tema 11 Funciones generales. Anatomía Nefrona Filtración glomerular Reabsorción tubular Secreción tubular Micción Envejecimiento Funciones generales * Mantenimiento de la homeostasis hídrica y electrolítica.
Transporte de oxígeno y de dióxido de carbono (CO 2 ) en la sangre. La hemoglobina aumenta la capacidad de la sangre para transportar oxígeno.
 Transporte de oxígeno y de dióxido de carbono (CO 2 ) en la sangre La sangre transporta los gases respiratorios por todo el organismo. El O2 se transporta desde los pulmones hasta todos los tejidos del
Transporte de oxígeno y de dióxido de carbono (CO 2 ) en la sangre La sangre transporta los gases respiratorios por todo el organismo. El O2 se transporta desde los pulmones hasta todos los tejidos del
Trastornos del equilibrio ácido-base
 NOTA DELS COMISSIONARIS: hi ha aclaracions i correccions importants al document Fe d errades, és important que us el mireu de cara a l examen!! Trastornos del equilibrio ácidobase INTRODUCCIÓN CONCEPTOS
NOTA DELS COMISSIONARIS: hi ha aclaracions i correccions importants al document Fe d errades, és important que us el mireu de cara a l examen!! Trastornos del equilibrio ácidobase INTRODUCCIÓN CONCEPTOS
Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ
 ALTERACIONES DEL EQUILIBRIO ÁCIDO-BASE Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ El ph refleja la concentración de cationes de hidrógeno presentes en una determinada
ALTERACIONES DEL EQUILIBRIO ÁCIDO-BASE Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ El ph refleja la concentración de cationes de hidrógeno presentes en una determinada
FISIOPATOLOGIA. Concentración normal H+: 40 nmoles/l. -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3
 FISIOPATOLOGIA Concentración normal H+: 40 nmoles/l -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3 FISIOPATOLOGIA ACIDO-BASE ACIDO: sustancia capaz de ceder protones BASE: sustancia
FISIOPATOLOGIA Concentración normal H+: 40 nmoles/l -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3 FISIOPATOLOGIA ACIDO-BASE ACIDO: sustancia capaz de ceder protones BASE: sustancia
Tema 1. Introducción
 Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Ventilación Mecánica en el RN Cardiópata con Hiperflujo Pulmonar
 Ventilación Mecánica en el RN Cardiópata con Hiperflujo Pulmonar Dra. Ximena Alegría Palazón Profesor Adjunto Universidad de Valparaíso Unidad de Neonatología Hospital Carlos Van Buren VM Cardiopatías
Ventilación Mecánica en el RN Cardiópata con Hiperflujo Pulmonar Dra. Ximena Alegría Palazón Profesor Adjunto Universidad de Valparaíso Unidad de Neonatología Hospital Carlos Van Buren VM Cardiopatías
7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
DIARREA o SÍNDROME DIARREICO. Prof. MARCOS MOREIRA ESPINOZA INSTITUTO DE FARMACOLOGIA y MORFOFISIOLOGIA UNIVERSIDAD AUSTRAL DE CHILE
 DIARREA o SÍNDROME DIARREICO Prof. MARCOS MOREIRA ESPINOZA INSTITUTO DE FARMACOLOGIA y MORFOFISIOLOGIA UNIVERSIDAD AUSTRAL DE CHILE DIARREA O SINDROME DIARREICO DEFINICIÓN: EVACUACIÓN DE HECES LÍQUIDAS,
DIARREA o SÍNDROME DIARREICO Prof. MARCOS MOREIRA ESPINOZA INSTITUTO DE FARMACOLOGIA y MORFOFISIOLOGIA UNIVERSIDAD AUSTRAL DE CHILE DIARREA O SINDROME DIARREICO DEFINICIÓN: EVACUACIÓN DE HECES LÍQUIDAS,
TALLER DE ANALISIS DE GASES ARTERIALES
 TALLER DE ANALISIS DE GASES ARTERIALES Dr. Menfil A Orellana-Barrios Medicina Interna Cursos Precongreso Congreso de Residentes 2012 HGSJDD www.drmenfilorellana.wordpress.com Para qué se utilizan los Gases
TALLER DE ANALISIS DE GASES ARTERIALES Dr. Menfil A Orellana-Barrios Medicina Interna Cursos Precongreso Congreso de Residentes 2012 HGSJDD www.drmenfilorellana.wordpress.com Para qué se utilizan los Gases
TEST APARATO RESPIRATORIO BIR 2015-2016
 1.- Cuál de los siguientes es el estímulo directo para las neuronas del área quimiosensible de la zona bulbar reguladora de la respiración?: 1. po 2. 2. pco 2. 3. CO 3 H 2. 4. CO 3 H -. 5. Concentración
1.- Cuál de los siguientes es el estímulo directo para las neuronas del área quimiosensible de la zona bulbar reguladora de la respiración?: 1. po 2. 2. pco 2. 3. CO 3 H 2. 4. CO 3 H -. 5. Concentración
ENFERMERÍA CLÍNICA I Felicitas Merino de la Hoz TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS
 TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS ÍNDICE 1. Introducción. 2. Análisis e interpretación de los gases arteriales. 3. Alteraciones del equilibrio ácido- base. 3.1. Acidosis respiratoria. 3.2. Alcalosis
TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS ÍNDICE 1. Introducción. 2. Análisis e interpretación de los gases arteriales. 3. Alteraciones del equilibrio ácido- base. 3.1. Acidosis respiratoria. 3.2. Alcalosis
Proceso de liberación de energía, requiere aporte continuo de oxigeno(o2) y eliminación de bióxido de carbono(co2) principal función del aparato
 Proceso de liberación de energía, requiere aporte continuo de oxigeno(o2) y eliminación de bióxido de carbono(co2) principal función del aparato respiratorio. En condiciones normales la respiración es
Proceso de liberación de energía, requiere aporte continuo de oxigeno(o2) y eliminación de bióxido de carbono(co2) principal función del aparato respiratorio. En condiciones normales la respiración es
SALES MINERALES , CO 3. Aniones: Cl -, PO 4. , NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K +
 SALES MINERALES Aniones: Cl -, PO 4 3-, CO 3 2-, NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K + SALES PRECIPITADAS Vieira SALES PRECIPITADAS: CaCO 3 Exoesqueleto de Ca Sales de Ca: caparazones
SALES MINERALES Aniones: Cl -, PO 4 3-, CO 3 2-, NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K + SALES PRECIPITADAS Vieira SALES PRECIPITADAS: CaCO 3 Exoesqueleto de Ca Sales de Ca: caparazones
Proteínas plasmáticas. Proteínas plasmáticas. Sales de litio 0% Ampicilina 18% Morfina 35% Aspirina 50% Fenitoína 90% Diazepam 98% Warfarina 99%
 Distribución Distribución y fijación de fármacos Paso del fármaco desde la sangre a los diversos tejidos La capacidad de los fármacos para distribuirse en el organismo va a depender de: a) Características
Distribución Distribución y fijación de fármacos Paso del fármaco desde la sangre a los diversos tejidos La capacidad de los fármacos para distribuirse en el organismo va a depender de: a) Características
VOMITO o EMESIS. Prof. MARCOS MOREIRA ESPINOZA INSTITUTO DE FARMACOLOGIA Y MORFOFISIOLOGIA UNIVERSIDAD AUSTRAL DE CHILE
 VOMITO o EMESIS Prof. MARCOS MOREIRA ESPINOZA INSTITUTO DE FARMACOLOGIA Y MORFOFISIOLOGIA UNIVERSIDAD AUSTRAL DE CHILE VOMITO o EMESIS 1. DEFINICIÓN: VOMITO, ACTO REFLEJO QUE CONSISTE EN LA EVACUACIÓN
VOMITO o EMESIS Prof. MARCOS MOREIRA ESPINOZA INSTITUTO DE FARMACOLOGIA Y MORFOFISIOLOGIA UNIVERSIDAD AUSTRAL DE CHILE VOMITO o EMESIS 1. DEFINICIÓN: VOMITO, ACTO REFLEJO QUE CONSISTE EN LA EVACUACIÓN
Lección 24. Fármacos Diuréticos UNIDAD VII: PROBLEMAS CARDIOVASCULARES Y SANGUÍNEOS. Ricardo Brage e Isabel Trapero - Farmacología Lección 24
 Ricardo Brage e Isabel Trapero - Lección 24 UNIDAD VII: PROBLEMAS CARDIOVASCULARES Y SANGUÍNEOS Lección 24 Fármacos Diuréticos Guión Ricardo Brage e Isabel Trapero - Lección 24 1. BASES CONCEPTUALES. 2.
Ricardo Brage e Isabel Trapero - Lección 24 UNIDAD VII: PROBLEMAS CARDIOVASCULARES Y SANGUÍNEOS Lección 24 Fármacos Diuréticos Guión Ricardo Brage e Isabel Trapero - Lección 24 1. BASES CONCEPTUALES. 2.
Lic. Jürgen Freer B.
 Lic. Jürgen Freer B. Distintos estudios han demostrado una relación entre la desestabilización del control fisiológico de la hemostasia y la incidencia de enfermedades cardiovasculares. Así la angina de
Lic. Jürgen Freer B. Distintos estudios han demostrado una relación entre la desestabilización del control fisiológico de la hemostasia y la incidencia de enfermedades cardiovasculares. Así la angina de
El sistema respiratorio
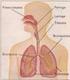 El sistema respiratorio Así como es indispensable incorporar materia del medio, también es importante liberar la energía química que se encuentra almacenada en las distintas moléculas orgánicas incorporadas.
El sistema respiratorio Así como es indispensable incorporar materia del medio, también es importante liberar la energía química que se encuentra almacenada en las distintas moléculas orgánicas incorporadas.
MEDIO INTERNO HOMEOSTASIS. Estructura del medio interno. Se denomina asi al medio extracelular, el medio que rodea a las celulas
 MEDIO INTERNO Se denomina asi al medio extracelular, el medio que rodea a las celulas HOMEOSTASIS Estructura del medio interno El agua representa el 40-60% del peso corporal del organismo. 1 Distribución
MEDIO INTERNO Se denomina asi al medio extracelular, el medio que rodea a las celulas HOMEOSTASIS Estructura del medio interno El agua representa el 40-60% del peso corporal del organismo. 1 Distribución
FISIOLOGIA MEDICINA FISIOLOGÍA DEL APARATO DIGESTIVO
 FISIOLOGIA MEDICINA FISIOLOGÍA DEL APARATO DIGESTIVO 2006 Ximena Páez TEMA 11 I. ABSORCIÓN AGUA Y ELECTROLITOS II. SECRECIÓN ELECTROLITOS III. ABSORCIÓN MINERALES, VIT HIDROSOLUBLES IV. MALABSORCIÓN I.
FISIOLOGIA MEDICINA FISIOLOGÍA DEL APARATO DIGESTIVO 2006 Ximena Páez TEMA 11 I. ABSORCIÓN AGUA Y ELECTROLITOS II. SECRECIÓN ELECTROLITOS III. ABSORCIÓN MINERALES, VIT HIDROSOLUBLES IV. MALABSORCIÓN I.
Volemia y Glóbulos Rojos
 UNIVERSIDAD CENTROCCIDENTAL LISANDRO ALVARADO DECANATO DE CIENCIAS DE LA SALUD DEPARTAMENTO DE FISIOLOGIA ENFERMERIA Volemia y Glóbulos Rojos Lic. Ana López-Fonseca ana.lopez@.ucla.edu.ve CONTENIDO.-Sangre
UNIVERSIDAD CENTROCCIDENTAL LISANDRO ALVARADO DECANATO DE CIENCIAS DE LA SALUD DEPARTAMENTO DE FISIOLOGIA ENFERMERIA Volemia y Glóbulos Rojos Lic. Ana López-Fonseca ana.lopez@.ucla.edu.ve CONTENIDO.-Sangre
OBJETIVOS DEL TEMA: Objetivos de la 2da actividad: 1.- Interpretar los signos y síntomas de la encefalopatía-hepática.
 TEMA: Metabolismo de Aminoácidos. TÍTULO: Encefalopatía hepática CONTENIDOS. 1.- La Encefalopatía hepática. a) Toxicidad del amoníaco. b) Causas de la encefalopatía hepática (coma hepático). c) Mecanismo
TEMA: Metabolismo de Aminoácidos. TÍTULO: Encefalopatía hepática CONTENIDOS. 1.- La Encefalopatía hepática. a) Toxicidad del amoníaco. b) Causas de la encefalopatía hepática (coma hepático). c) Mecanismo
Efecto de la inhibición de los receptores dopaminérgicos D2 centrales en la atenuación ventilatoria durante la exposición prolongada a la hipoxia
 Efecto de la inhibición de los receptores dopaminérgicos D2 centrales en la atenuación ventilatoria durante la exposición prolongada a la hipoxia José Luis Macarlupú, Rosa Cardenas, Francisco Villafuerte,
Efecto de la inhibición de los receptores dopaminérgicos D2 centrales en la atenuación ventilatoria durante la exposición prolongada a la hipoxia José Luis Macarlupú, Rosa Cardenas, Francisco Villafuerte,
Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales. Verónica Pantoja. Lic. MSP.
 Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales Professor: Kinesiologia Verónica Pantoja. Lic. MSP. 1.Precipitadas Formando estructuras sólidas, insolubles, con función esquelética.
Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales Professor: Kinesiologia Verónica Pantoja. Lic. MSP. 1.Precipitadas Formando estructuras sólidas, insolubles, con función esquelética.
Alteraciones ácido-base Simples y Mixtos: Una Aproximación Práctica Robert C Narins, M.D. y Michael Emmett, M.D. Modificado por Mauricio Durán, M.D.
 1 Alteraciones ácido-base Simples y Mixtos: Una Aproximación Práctica Robert C Narins, M.D. y Michael Emmett, M.D. Modificado por Mauricio Durán, M.D. Revisiones recientes del metabolismo ácido-base se
1 Alteraciones ácido-base Simples y Mixtos: Una Aproximación Práctica Robert C Narins, M.D. y Michael Emmett, M.D. Modificado por Mauricio Durán, M.D. Revisiones recientes del metabolismo ácido-base se
TEMA 7: REACCIONES DE TRANSFERENCIA DE PROTONES
 TEMA 7: REACCIONES DE TRANSFERENCIA DE PROTONES 1. Concepto de ácido y de base De las distintas teorías que existen de ácidos y bases, sólo vamos a exponer dos de las más utilizadas, la teoría de Arrhenius
TEMA 7: REACCIONES DE TRANSFERENCIA DE PROTONES 1. Concepto de ácido y de base De las distintas teorías que existen de ácidos y bases, sólo vamos a exponer dos de las más utilizadas, la teoría de Arrhenius
Verónica Mate García Isabel Moreno Moraleda Gracia Guajardo-Fajardo Adriana Serrano Olave
 Verónica Mate García Isabel Moreno Moraleda Gracia Guajardo-Fajardo Adriana Serrano Olave Introducción Efectos del tabaco fumado Afectaciones por polución aérea Intoxicación por CO Intoxicación por oxígeno
Verónica Mate García Isabel Moreno Moraleda Gracia Guajardo-Fajardo Adriana Serrano Olave Introducción Efectos del tabaco fumado Afectaciones por polución aérea Intoxicación por CO Intoxicación por oxígeno
INTOXICACION CON ASPIRINA
 INTOXICACION CON ASPIRINA La intoxicación con aspirina es un hecho sumamente común en la práctica médica. La misma responde entre otras cosas, a que es un medicamento que puede adquirirse sin receta en
INTOXICACION CON ASPIRINA La intoxicación con aspirina es un hecho sumamente común en la práctica médica. La misma responde entre otras cosas, a que es un medicamento que puede adquirirse sin receta en
Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D.
 Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D. Vallejos Javier Serial Marcos Sebastián Rausch Ricardo Simón Laura Solé Juan
Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D. Vallejos Javier Serial Marcos Sebastián Rausch Ricardo Simón Laura Solé Juan
INSUFICIENCIA RESPIRATORIA AGUDA GIOVANNY CAMPOMANES ESPINOZA MEDICO INTERNISTA
 INSUFICIENCIA RESPIRATORIA AGUDA GIOVANNY CAMPOMANES ESPINOZA MEDICO INTERNISTA Zona de Conducción TRAQUEA BRONQUIOS BRONQUIOLOS BRONQUIOLOS TERMINALES Z O 1 2 3 4 5 16 Zona de Transición Y Respiratoria
INSUFICIENCIA RESPIRATORIA AGUDA GIOVANNY CAMPOMANES ESPINOZA MEDICO INTERNISTA Zona de Conducción TRAQUEA BRONQUIOS BRONQUIOLOS BRONQUIOLOS TERMINALES Z O 1 2 3 4 5 16 Zona de Transición Y Respiratoria
Profesor(a): C.D. María Isabel Pérez Aguilar
 Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
Concepto de ph. Bases
 Concepto de ph El concepto de ph nace de dos tipos de especies químicas llamadas ácidos y bases, las que se pueden clasificar como tal y predecir su potencia o fuerza de acuerdo al valor de su ph. Características
Concepto de ph El concepto de ph nace de dos tipos de especies químicas llamadas ácidos y bases, las que se pueden clasificar como tal y predecir su potencia o fuerza de acuerdo al valor de su ph. Características
PROCEDIMIENTO DE OXIGENOTERAPIA PARA EL SERVICIO DE URGENCIAS
 PROCEDIMIENTO DE OXIGENOTERAPIA PARA EL SERVICIO DE URGENCIAS PO-URG-OTU-48 : 2 18/01/2013 PROCEDIMIENTO DE OXIGENOTERAPIA CONTROL DE CAMBIOS Fecha Descripción del Cambio 1 30/03/2012 Se actualiza documentación
PROCEDIMIENTO DE OXIGENOTERAPIA PARA EL SERVICIO DE URGENCIAS PO-URG-OTU-48 : 2 18/01/2013 PROCEDIMIENTO DE OXIGENOTERAPIA CONTROL DE CAMBIOS Fecha Descripción del Cambio 1 30/03/2012 Se actualiza documentación
TEMA 11 I. ABSORCIÓN DE AGUA Y ELECTROLITOS
 1 TEMA 11 I. ABSORCIÓN DE AGUA Y ELECTROLITOS 1. Introducción 2. Conceptos 2.1 ósmosis, molaridad y osmolaridad de soluciones, 2.2 presión osmótica, presión hidrostática. 2.3 soluciones isotónicas, hipotónicas,
1 TEMA 11 I. ABSORCIÓN DE AGUA Y ELECTROLITOS 1. Introducción 2. Conceptos 2.1 ósmosis, molaridad y osmolaridad de soluciones, 2.2 presión osmótica, presión hidrostática. 2.3 soluciones isotónicas, hipotónicas,
Neumologí a Iº SECCIÓN : CIENCIAS BÁSICAS (RESUMEN) ANATOMÍA DEL APARATO RESPIRATORIO. www. PLUS -medica.com
 Neumologí a Iº SECCIÓN : CIENCIAS BÁSICAS (RESUMEN) ANATOMÍA DEL APARATO RESPIRATORIO VIAS AÉREAS 4 Las células de Kultchitsky Se encuentran en el epitelio de la mucosa de tráquea y bronquios. Es una célula
Neumologí a Iº SECCIÓN : CIENCIAS BÁSICAS (RESUMEN) ANATOMÍA DEL APARATO RESPIRATORIO VIAS AÉREAS 4 Las células de Kultchitsky Se encuentran en el epitelio de la mucosa de tráquea y bronquios. Es una célula
METABOLISMO DE LIPIDOS
 METABOLISMO DE LIPIDOS Al igual que en el metabolismo de los carbohidratos, el metabolismo de lípidos consiste en: Digestión Transporte Almacenamiento Degradación Biosíntesis DIGESTIÓN DE LIPIDOS Los lípidos
METABOLISMO DE LIPIDOS Al igual que en el metabolismo de los carbohidratos, el metabolismo de lípidos consiste en: Digestión Transporte Almacenamiento Degradación Biosíntesis DIGESTIÓN DE LIPIDOS Los lípidos
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 6, Opción A Junio, Ejercicio 4, Opción B Reserva 1, Ejercicio 4, Opción A Reserva, Ejercicio 5, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 6, Opción A Junio, Ejercicio 4, Opción B Reserva 1, Ejercicio 4, Opción A Reserva, Ejercicio 5, Opción
Sistemas de ingreso, intercambio y transporte de sustancias en el organismo. Sistema Circulatorio
 Sistema circulatorio Observe y explore comprensivamente esta presentación Sistemas de ingreso, intercambio y transporte de sustancias en el organismo: Sistema circulatorio. Esta le permitirá avanzar y
Sistema circulatorio Observe y explore comprensivamente esta presentación Sistemas de ingreso, intercambio y transporte de sustancias en el organismo: Sistema circulatorio. Esta le permitirá avanzar y
MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ
 MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ 1-Historia clínica G D Varón de 1 año y 5 meses MOTIVO DE CONSULTA retraso del crecimiento ANTECEDENTES RNTPAEG
MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ 1-Historia clínica G D Varón de 1 año y 5 meses MOTIVO DE CONSULTA retraso del crecimiento ANTECEDENTES RNTPAEG
EL AGUA Y LAS SALES MINERALES
 EL AGUA Y LAS SALES MINERALES 1. EL AGUA DE LA MATERIA VIVA El agua es la molécula más abundante de la materia viva La cantidad de agua en los seres vivos es variable Según el tipo de tejido: más agua
EL AGUA Y LAS SALES MINERALES 1. EL AGUA DE LA MATERIA VIVA El agua es la molécula más abundante de la materia viva La cantidad de agua en los seres vivos es variable Según el tipo de tejido: más agua
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 10 ml de solución contiene: Hidrogenocarbonato de sodio
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 10 ml de solución contiene: Hidrogenocarbonato de sodio
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas.
 La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
CISTINURIA. Elisa del Valle
 CISTINURIA Elisa del Valle CISTINURIA La cistinuria es un desorden autosómico recesivo (en el que pocos casos muestran una herencia dominante) Afecta el transporte de membrana de cistina y AA dibásicos
CISTINURIA Elisa del Valle CISTINURIA La cistinuria es un desorden autosómico recesivo (en el que pocos casos muestran una herencia dominante) Afecta el transporte de membrana de cistina y AA dibásicos
DIFUSIÓN - TRANSPORTE DE GASES EN SANGRE. Material de uso interno
 DIFUSIÓN - TRANSPORTE DE GASES EN SANGRE Material de uso interno 2010 Hoy hablaremos de: * Leyes de los gases: aspectos aplicados * Hematosis ó intercambio alvéolo-capilar * Transporte de gases en sangre
DIFUSIÓN - TRANSPORTE DE GASES EN SANGRE Material de uso interno 2010 Hoy hablaremos de: * Leyes de los gases: aspectos aplicados * Hematosis ó intercambio alvéolo-capilar * Transporte de gases en sangre
OXIGENOTERAPIA II JORNADAS INTERNACIONALES DE INVESTIGACIÓN EN EDUCACIÓN Y SALUD:
 OXIGENOTERAPIA II JORNADAS INTERNACIONALES DE INVESTIGACIÓN EN EDUCACIÓN Y SALUD: "Experiencias en educación y salud transcultural" AUTORES: Fernández Sánchez, Pedro. Diplomado en enfermería. Hospital
OXIGENOTERAPIA II JORNADAS INTERNACIONALES DE INVESTIGACIÓN EN EDUCACIÓN Y SALUD: "Experiencias en educación y salud transcultural" AUTORES: Fernández Sánchez, Pedro. Diplomado en enfermería. Hospital
RIÑÓN Y LÍQUIDOS CORPORALES. 29. Regulación del equilibrio ácido-base
 RIÑÓN Y LÍQUIDOS CORPORALES 29. Regulación del equilibrio ácido-base INTRODUCCIÓN La concentración de iones H + libres en sangre se mantiene normalmente entre 40 y 45 nmol/litro, lo cual da un valor de
RIÑÓN Y LÍQUIDOS CORPORALES 29. Regulación del equilibrio ácido-base INTRODUCCIÓN La concentración de iones H + libres en sangre se mantiene normalmente entre 40 y 45 nmol/litro, lo cual da un valor de
GUÍA N 3: Equilibrio Químico y Cinética Química
 1 PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los siguientes términos: a) Reacción irreversible b) Reacción reversible c) Equilibrio químico d) Constante de equilibrio e) Principio de Le Chatelier
1 PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los siguientes términos: a) Reacción irreversible b) Reacción reversible c) Equilibrio químico d) Constante de equilibrio e) Principio de Le Chatelier
Estrés térmico y ejercicio físico
 Estrés térmico y ejercicio físico Elaborado por Lic. Manuel Salazar Leitón Temperatura Central o de núcleo: Cabeza, cavidad torácica y abdominal. (37 C) Superficial: Piel, tejido subcutáneo y muscular.
Estrés térmico y ejercicio físico Elaborado por Lic. Manuel Salazar Leitón Temperatura Central o de núcleo: Cabeza, cavidad torácica y abdominal. (37 C) Superficial: Piel, tejido subcutáneo y muscular.
Pruebas de función pulmonar. Diana Carolina Góngora
 Pruebas de función pulmonar Diana Carolina Góngora Definición Grupo de exámenes para medir la eficiencia de los pulmones para tomar y liberar aire, para movilizar gases, como el oxígeno, desde la atmósfera
Pruebas de función pulmonar Diana Carolina Góngora Definición Grupo de exámenes para medir la eficiencia de los pulmones para tomar y liberar aire, para movilizar gases, como el oxígeno, desde la atmósfera
Clase 6 Minerales. Temas: Funciones. Alimentos fuente. Recomendaciones de ingesta. María Fernanda Garat. Lic. en Nutrición.
 Clase 6 Minerales Temas: Funciones. Alimentos fuente. Recomendaciones de ingesta. 1 MINERALES Son elementos inorgánicos que desempeñan importantes funciones en nuestro organismo como facilitar la acción
Clase 6 Minerales Temas: Funciones. Alimentos fuente. Recomendaciones de ingesta. 1 MINERALES Son elementos inorgánicos que desempeñan importantes funciones en nuestro organismo como facilitar la acción
TÍTULO: VENTILACIÓN Y TEMPERATURA INSTITUTO SUPERIOR PEDAGOGICO ENRIQUE JOSE VARONA, LA HABANA
 TÍTULO: VENTILACIÓN Y TEMPERATURA AUTOR: PROFESOR TITULAR INSTITUTO SUPERIOR PEDAGOGICO ENRIQUE JOSE VARONA, LA HABANA Ambiente Térmico Cambios Fisiológicos y Psicomotores (Cambios ambientales extremos)
TÍTULO: VENTILACIÓN Y TEMPERATURA AUTOR: PROFESOR TITULAR INSTITUTO SUPERIOR PEDAGOGICO ENRIQUE JOSE VARONA, LA HABANA Ambiente Térmico Cambios Fisiológicos y Psicomotores (Cambios ambientales extremos)
Terapia Líquida en Pediatría
 PROGRAMA DE EDUCACIÓN MEDICA CONTINUADA TERCER CURSO DE 1974-1975 LÍQUIDOS Y ELECTROLITOS EN LA PRACTICA MEDICA Terapia Líquida en Pediatría Dr. Francisco Cleaves T. La administración de líquidos parenterales
PROGRAMA DE EDUCACIÓN MEDICA CONTINUADA TERCER CURSO DE 1974-1975 LÍQUIDOS Y ELECTROLITOS EN LA PRACTICA MEDICA Terapia Líquida en Pediatría Dr. Francisco Cleaves T. La administración de líquidos parenterales
Concepto de ph. ph = - log [H + ]
![Concepto de ph. ph = - log [H + ] Concepto de ph. ph = - log [H + ]](/thumbs/39/19109627.jpg) Fuerza de Ácidos y Bases Concepto de ph Ácidos Los ácidos se diferencian de acuerdo a su capacidad para ceder protones al medio, o químicamente dicho, por su capacidad de disociación, esa también es la
Fuerza de Ácidos y Bases Concepto de ph Ácidos Los ácidos se diferencian de acuerdo a su capacidad para ceder protones al medio, o químicamente dicho, por su capacidad de disociación, esa también es la
Fisiología del evento ISQUEMIA / ANOXIA. Rodolfo A. Cabrales Vega MD Docente Programa de Medicina Universidad Tecnológica de Pereira
 Fisiología del evento ISQUEMIA / ANOXIA Rodolfo A. Cabrales Vega MD Docente Programa de Medicina Universidad Tecnológica de Pereira Porque cualquier miembro suelto, ya esté recubierto por piel o por carne,
Fisiología del evento ISQUEMIA / ANOXIA Rodolfo A. Cabrales Vega MD Docente Programa de Medicina Universidad Tecnológica de Pereira Porque cualquier miembro suelto, ya esté recubierto por piel o por carne,
Nutrición n Mineral. Parte I
 Nutrición n Mineral Parte I Por qué usamos minerales en producción animal Funciones del organismo 1. Mantenimiento 2. Actividad 3. Crecimiento 4. Reproducción 5. Producción de leche Funciones de los Minerales
Nutrición n Mineral Parte I Por qué usamos minerales en producción animal Funciones del organismo 1. Mantenimiento 2. Actividad 3. Crecimiento 4. Reproducción 5. Producción de leche Funciones de los Minerales
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
PROSPECTO: INFORMACIÓN PARA EL USUARIO Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
Prospecto: información para el usuario. Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio
 Prospecto: información para el usuario Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve
Prospecto: información para el usuario Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve
Aparatos que intervienen en la nutrición
 Aparatos que intervienen en la nutrición El ser humano necesita ingerir alimentos y agua diariamente, para el mantenimiento de sus constantes vitales. De los alimentos se utilizan distintos nutrientes,
Aparatos que intervienen en la nutrición El ser humano necesita ingerir alimentos y agua diariamente, para el mantenimiento de sus constantes vitales. De los alimentos se utilizan distintos nutrientes,
SEMINARIO: ESTUDIO DEL PH FETAL INTRAPARTO
 Fecha: 1 de Diciembre de 2010 Nombre: Dra. Ana Fuentes Rozalén R2 Tipo de Sesión: Seminario SEMINARIO: ESTUDIO DEL PH FETAL INTRAPARTO El objetivo de este seminario es que entendamos la fisiopatología
Fecha: 1 de Diciembre de 2010 Nombre: Dra. Ana Fuentes Rozalén R2 Tipo de Sesión: Seminario SEMINARIO: ESTUDIO DEL PH FETAL INTRAPARTO El objetivo de este seminario es que entendamos la fisiopatología
FISIOLOGIA RESPIRATORIA
 FISIOLOGIA RESPIRATORIA LA RESPIRACION TIENE COMO FUNCION PROPORCIONAR O 2 A LAS CELULAS Y EXTRAER EL EXCESO DE CO 2 PRODUCIDO POR ELLAS Componentes de las vías aéreas TRÁQUEA BRONQUIOS BRONQUÍOLOS ZONA
FISIOLOGIA RESPIRATORIA LA RESPIRACION TIENE COMO FUNCION PROPORCIONAR O 2 A LAS CELULAS Y EXTRAER EL EXCESO DE CO 2 PRODUCIDO POR ELLAS Componentes de las vías aéreas TRÁQUEA BRONQUIOS BRONQUÍOLOS ZONA
1º CURSO FISIOLOGÍA HUMANA
 UNIVERSIDAD AUTÓNOMA DE MADRID CURSO 2012-2013 1º CURSO FISIOLOGÍA HUMANA Coordinación: Profesores: Esther Martínez Miguel UNIVERSIDAD AUTÓNOMA DE MADRID PLAN DE ESTUDIOS 1999 2 UNIVERSIDAD AUTÓNOMA DE
UNIVERSIDAD AUTÓNOMA DE MADRID CURSO 2012-2013 1º CURSO FISIOLOGÍA HUMANA Coordinación: Profesores: Esther Martínez Miguel UNIVERSIDAD AUTÓNOMA DE MADRID PLAN DE ESTUDIOS 1999 2 UNIVERSIDAD AUTÓNOMA DE
Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp
 Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp Enf. María Guadalupe Vega Jefe de Piso Unidad de Terapia Intensiva Hospital General Las Américas, Ecatepec
Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp Enf. María Guadalupe Vega Jefe de Piso Unidad de Terapia Intensiva Hospital General Las Américas, Ecatepec
Ciclo Cardiaco -Guía de Estudio PARTE II - Presión arterial.
 Area de Fisiología Cardiovascular, Renal y Respiratoria. - 2016 - TRABAJO PRACTICO Nº 3 - CICLO CARDIACO II Ciclo Cardiaco -Guía de Estudio PARTE II - Presión arterial. I. Defina 1) Presión Sistólica 2)
Area de Fisiología Cardiovascular, Renal y Respiratoria. - 2016 - TRABAJO PRACTICO Nº 3 - CICLO CARDIACO II Ciclo Cardiaco -Guía de Estudio PARTE II - Presión arterial. I. Defina 1) Presión Sistólica 2)
Clase 8. Funciones principales y estructura de los riñones
 Clase 8 Funciones principales y estructura de los riñones Funciones principales de los riñones La principal misión de los riñones es la excreción diferencial de diversas sustancias, de forma que la composición
Clase 8 Funciones principales y estructura de los riñones Funciones principales de los riñones La principal misión de los riñones es la excreción diferencial de diversas sustancias, de forma que la composición
REGULACIÓN DEL ph. Teoría Acido-Base - Anfolitos. Por lo común lo vemos representado como ph = - log [H + ]
![REGULACIÓN DEL ph. Teoría Acido-Base - Anfolitos. Por lo común lo vemos representado como ph = - log [H + ] REGULACIÓN DEL ph. Teoría Acido-Base - Anfolitos. Por lo común lo vemos representado como ph = - log [H + ]](/thumbs/40/20899659.jpg) REGULACIÓN DEL ph Teoría Acido-Base - Anfolitos Que es el ph??? Por lo común lo vemos representado como ph = - log [H ] Estrictamente, ph = - log a H En soluciones diluídas expresarlo en concentración
REGULACIÓN DEL ph Teoría Acido-Base - Anfolitos Que es el ph??? Por lo común lo vemos representado como ph = - log [H ] Estrictamente, ph = - log a H En soluciones diluídas expresarlo en concentración
6. Equilibrio ácido-base I
 6. Equilibrios ácido-base I Química (1S, Grado Biología) UAM 6. Equilibrio ácido-base I Contenidos Equilibrios ácido-base I Ácidos y bases Producto iónico del agua. Disoluciones neutras, ácidas y básicas.
6. Equilibrios ácido-base I Química (1S, Grado Biología) UAM 6. Equilibrio ácido-base I Contenidos Equilibrios ácido-base I Ácidos y bases Producto iónico del agua. Disoluciones neutras, ácidas y básicas.
Composición Líquido Elementos formes
 Composición Líquido Elementos formes Plasma Glóbulos blancos Glóbulos rojos Plaquetas Transporte de sustancias Homeostasis de los líquidos l corporales Protección TRANSPORTE O 2 desde los pulmones a los
Composición Líquido Elementos formes Plasma Glóbulos blancos Glóbulos rojos Plaquetas Transporte de sustancias Homeostasis de los líquidos l corporales Protección TRANSPORTE O 2 desde los pulmones a los
PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS.
 PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS. OBJETIVOS En esta práctica se tratarán aspectos de interés relacionados con los equilibrios
PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS. OBJETIVOS En esta práctica se tratarán aspectos de interés relacionados con los equilibrios
Compartimentos cerebrales
 Compartimentos cerebrales 1 Metabolismo cerebral El encéfalo requiere oxígeno y nutrientes para cubrir necesidades metabólicas. En reposo el metabolismo cerebral es 7.5 veces el met. promedio del resto
Compartimentos cerebrales 1 Metabolismo cerebral El encéfalo requiere oxígeno y nutrientes para cubrir necesidades metabólicas. En reposo el metabolismo cerebral es 7.5 veces el met. promedio del resto
ASFIXIA Y PARADA CARDIACA POR INMERSIÓN. Ángel Aguado Vidal Julio César Ramírez Nava CBA
 ASFIXIA Y PARADA CARDIACA POR INMERSIÓN Ángel Aguado Vidal Julio César Ramírez Nava CBA INTRODUCCIÓN El Ahogamiento y Casi-ahogamiento ahogamiento son una causa frecuente de muerte o daño neurológico severo
ASFIXIA Y PARADA CARDIACA POR INMERSIÓN Ángel Aguado Vidal Julio César Ramírez Nava CBA INTRODUCCIÓN El Ahogamiento y Casi-ahogamiento ahogamiento son una causa frecuente de muerte o daño neurológico severo
Oliguria. Tema 25: Alteraciones de la cantidad y el ritmo urinario
 Tema 25: Alteraciones de la cantidad y el ritmo urinario Oliguria Poliuria Polaquiuria, disuria, tenesmo, estranguria Nicturia Síndromes de las vías urinarias Síndrome prostático Síndrome de infección
Tema 25: Alteraciones de la cantidad y el ritmo urinario Oliguria Poliuria Polaquiuria, disuria, tenesmo, estranguria Nicturia Síndromes de las vías urinarias Síndrome prostático Síndrome de infección
Sistema renal. Odontología 2008
 Sistema renal Odontología 2008 Sistema renal Los riñones Si están bien perfundidos Mediante los mecanismos básicos: Filtración Reabsorción Secreción Regulan el medio interno Eliminan sustancias de deshecho
Sistema renal Odontología 2008 Sistema renal Los riñones Si están bien perfundidos Mediante los mecanismos básicos: Filtración Reabsorción Secreción Regulan el medio interno Eliminan sustancias de deshecho
Aspectos destacados del sistema cardiocirculatorio y respiratorio, ligados al entrenamiento deportivo. Dr. Juan Carlos Mazza (Argentina)
 Aspectos destacados del sistema cardiocirculatorio y respiratorio, ligados al entrenamiento deportivo Dr. Juan Carlos Mazza (Argentina) SISTEMA CARDIOVASCULAR Cualquier sistema de circulación requiere
Aspectos destacados del sistema cardiocirculatorio y respiratorio, ligados al entrenamiento deportivo Dr. Juan Carlos Mazza (Argentina) SISTEMA CARDIOVASCULAR Cualquier sistema de circulación requiere
1. Concepto de sistema tampón. Cita algunos ejemplos biológicos de tampones inorgánicos.
 VALENCIA (COMUNIDAD VALENCIANA) / JUNIO 00. COU / BIOLOGIA / BIOMOLECULAS / OPCION A / EJERCICIO 1 OPCION A 1. Concepto de sistema tampón. Cita algunos ejemplos biológicos de tampones inorgánicos. La actividad
VALENCIA (COMUNIDAD VALENCIANA) / JUNIO 00. COU / BIOLOGIA / BIOMOLECULAS / OPCION A / EJERCICIO 1 OPCION A 1. Concepto de sistema tampón. Cita algunos ejemplos biológicos de tampones inorgánicos. La actividad
Curso Superior de Medicina Intensiva y Cuidados Críticos Necochea, 2007-2009
 Trastornos del equilibrio ácido-base Introducción Las primeras definiciones contemporáneas de ácido y base pueden atribuirse a Arrhenius, quien en 1887 definió ácido como un donante de ion hidrógeno y
Trastornos del equilibrio ácido-base Introducción Las primeras definiciones contemporáneas de ácido y base pueden atribuirse a Arrhenius, quien en 1887 definió ácido como un donante de ion hidrógeno y
COLEGIO SAN FRANCISCO JAVIER GUIAS
 COLEGIO SAN FRANCISCO JAVIER GUIAS Código PGF 03 R07 2009 08 V03 Estudiante: Guía Nº: 2 Profesor: Andrés Fernando Rosero Ortiz Grado: 11 Asignatura: Química Sección: ABCD Tema: Equilibrio químico Equilibrio
COLEGIO SAN FRANCISCO JAVIER GUIAS Código PGF 03 R07 2009 08 V03 Estudiante: Guía Nº: 2 Profesor: Andrés Fernando Rosero Ortiz Grado: 11 Asignatura: Química Sección: ABCD Tema: Equilibrio químico Equilibrio
INSUFICIENCIA RENAL AGUDA
 INSUFICIENCIA RENAL AGUDA La insuficiencia renal aguda es un síndrome clínico que se produce por una reducción brusca de la filtración glomerular con retención progresiva de productos nitrogenados en sangre
INSUFICIENCIA RENAL AGUDA La insuficiencia renal aguda es un síndrome clínico que se produce por una reducción brusca de la filtración glomerular con retención progresiva de productos nitrogenados en sangre
PUNTO 1º - LA FUNCIÓN DE NUTRICIÓN
 PUNTO 1º - LA FUNCIÓN DE NUTRICIÓN Definición Nutrición: Conjunto de procesos mediante los cuales los seres vivos toman materia y energía del exterior y la transforman en materia propia y en energía. Definición
PUNTO 1º - LA FUNCIÓN DE NUTRICIÓN Definición Nutrición: Conjunto de procesos mediante los cuales los seres vivos toman materia y energía del exterior y la transforman en materia propia y en energía. Definición
Formas de energía en el cuerpo humano. Química Eléctrica Calorífica Mecánica
 Formas de energía en el cuerpo humano Química Eléctrica Calorífica Mecánica CONCEPTOS BÁSICOS Unidad de medida de energía más utilizada: Kilocaloría Caloría = cantidad de energía en forma de calor necesaria
Formas de energía en el cuerpo humano Química Eléctrica Calorífica Mecánica CONCEPTOS BÁSICOS Unidad de medida de energía más utilizada: Kilocaloría Caloría = cantidad de energía en forma de calor necesaria
