PROCEDIMIENTO TÉCNICO PARA EL DIAGNÓSTICO SEROLÓGICO DE SÍFILIS
|
|
|
- Lucas Páez Carmona
- hace 7 años
- Vistas:
Transcripción
1 Instituto de Salud Pública Ministerio de Salud DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO PROCEDIMIENTO TÉCNICO PARA EL DEPARTAMENTO LABORATORIO BIOMÉDICO NACIONAL Y DE REFERENCIA NOVIEMBRE, 2015
2 AUTORES ISP: T.M. Rodrigo Colina Morales Encargado de Laboratorio de Agentes de Infecciones de Transmisión Sexual ITS Sección Bacteriología, Subdepto. Enfermedades Infecciosas Departamento Laboratorio Biomédico Nacional y de Referencia Instituto de Salud Pública de Chile T.M. Alejandra Manríquez Cortez Laboratorio de Agentes de Infecciones de Transmisión Sexual ITS Sección Bacteriología, Subdepto. Enfermedades Infecciosas Departamento Laboratorio Biomédico Nacional y de Referencia Instituto de Salud Pública de Chile REVISORES INTERNOS Dra. Paola Pidal Méndez Jefe Departamento Laboratorio Biomédico Nacional y de Referencia. Dr. Juan Carlos Hormazabal Jefe de Subdepartamento de Enfermedades Infecciosas Laboratorio Biomédico Nacional y de Referencia Instituto de Salud Pública de Chile BQ. Pamela Araya Rodríguez Jefe Sección Bacteriología, Subdepto. Enfermedades Infecciosas, Departamento Laboratorio Biomédico Nacional y de Referencia Dra. Verónica Ramírez Muñoz Jefe Subdepto. Coordinación Externa, Departamento Laboratorio Biomédico Nacional y de Referencia Instituto de Salud Pública de Chile
3 DIAGNÓSTICO SEROLÓGICO DE SÍFILIS I.- ALCANCE Este documento de recomendaciones técnicas está dirigido a los laboratorios clínicos de la red asistencial que realizan el diagnóstico serológico de Sífilis para las técnicas de VDRL, RPR y MHA-Tp. II.- INTRODUCCION La Sífilis es una enfermedad infecciosa sistémica causada por Treponema pallidum (T. pallidum) de reservorio humano exclusivo, y que cursa clínicamente en etapas. Se transmite preferentemente por contacto sexual, por contacto directo con las lesiones, contacto directo con sangre y de la madre al hijo durante el embarazo. La Sífilis primaria corresponde a la primera etapa de la infección. El período de incubación es de 4 semanas (rango entre 1 y 90 días). La primera manifestación clínica, denominada chancro primario, aparece en el punto de inoculación (puerta de entrada) del treponema, como una pequeña erosión que posteriormente se ulcera, es habitualmente única, indolora, con bordes bien definidos y que desaparece espontáneamente en un período de 3 a 8 semanas. La Sífilis secundaria corresponde a la etapa de diseminación hematógena. Se manifiesta dentro de los 6 primeros meses después de la infección, habitualmente 6 a 8 semanas. El comienzo del período secundario se acompaña a menudo de síntomas similares a un estado gripal tales como fiebre, cefalea, acompañado de un rash cutáneo y linfadenopatía generalizada. Las lesiones cutáneas más frecuentes pueden ser máculas, pápulas o lesiones pápulo escamosas, no pruriginosas, distribuidas simétricamente principalmente en tronco y extremidades, es frecuente la localización palmo-plantar. En esta etapa las lesiones son altamente infectantes por contener gran cantidad de treponemas en su superficie. Sin tratamiento estas manifestaciones cutáneas y mucosas desaparecen espontáneamente. Se presentan en episodios de tres a cuatro semanas de duración y en forma recurrente. Cuando las manifestaciones visibles de la enfermedad desaparecen gradualmente se pasa al estado de Sífilis latente precoz, que se caracteriza por la ausencia de signos clínicos, cuando la infección ha ocurrido en los 12 meses previos al diagnóstico. La Sífilis latente tardía es una etapa que se caracteriza por ausencia de signos clínicos, cuando la infección inicial ha ocurrido en un tiempo mayor a los 12 meses previos. Esta etapa puede prolongarse por décadas. En esta etapa la enfermedad no es transmisible por vía sexual. La Sífilis terciaria corresponde a la etapa destructiva de la enfermedad, por lo general se desarrolla muchos años después de la infección primaria en pacientes no tratados o tratados inadecuadamente. En las lesiones de Sífilis Terciaria la presencia de treponemas es rara y las lesiones destructivas son producto de una reacción de hipersensibilidad. Clínicamente puede presentar compromiso cardiovascular, de grandes vasos y válvulas cardíacas, y la presencia de gomas sifilíticos que corresponden a lesiones granulomatosas 3
4 características de la sífilis tardía que se presentan en la piel, en las mucosas y los huesos. La neurosífilis se puede manifestar en cualquiera de las etapas clínicas de la enfermedad y consiste en el compromiso del Sistema Nervioso Central (SNC) por T. pallidum. Esta puede ser asintomática, pero con alteraciones en el líquido cefalorraquídeo. Clínicamente se puede presentar como meningitis sifilítica, compromiso de los pares craneanos, sífilis meningovascular, tabes dorsal y parálisis general progresiva. La identificación del T. pallidum mediante el examen directo del exudado de la lesión (microscopía de campo oscuro y/o fluorescencia directa) es una prueba definitiva para asegurar el diagnóstico, aunque un resultado negativo del mismo no descarta la posibilidad de la enfermedad, ya que la presencia de treponemas puede ser escasa dependiendo de los días de evolución y de tratamientos previos. Debido a las dificultades que puede presentar la realización del diagnóstico directo, la experiencia indica que el diagnóstico indirecto (serológico) se ha convertido en el procedimiento de uso más frecuente. Actualmente existen diferentes técnicas de laboratorio para el diagnóstico serológico de sífilis: PRUEBAS NO TREPONÉMICAS (Reagínicas) No determinan anticuerpos específicos frente a T. pallidum, y se basan en la detección de reaginas o anticuerpos anti lipídicos (inespecíficos) en respuesta al material lipoidal liberado por los tejidos dañados por el T. pallidum. Se utiliza una solución alcohólica con presencia de cardiolipina, colesterol y lecitina. Estas pruebas son: VDRL (Venereal Research Disease Laboratory) RPR (Rapid Plasma Reagin) USR (Unheated Serum Reagin) Son técnicas de bajo costo, fáciles de efectuar, se utilizan como pruebas de inicio en la detección serológica de sífilis y para evaluar la respuesta al tratamiento. La desventaja que presentan es que, debido a su inespecificidad, pueden arrojar falsos resultados positivos. PRUEBAS TREPONÉMICAS: detectan específicamente los anticuerpos contra T. pallidum y su utilidad en el laboratorio está orientada a confirmar serológicamente los resultados obtenidos por las pruebas no treponémicas. Las pruebas treponémicas más conocidas son: FTA-Abs (Inmunofluorescencia indirecta con absorción del suero) MHA-Tp (Microhemaglutinación) ELISA (Inmunoensayo) Quimioluminiscencia Estas técnicas carecen de utilidad para monitorear los tratamientos, ya que suelen permanecer positivas en el 85 a 90% de los pacientes tratados adecuadamente. Es importante recordar que un resultado de examen no treponémico reactivo indica sospecha de infección activa (en curso) o serología residual. En el diagnóstico de la Sífilis es fundamental el análisis del examen clínico, los antecedentes epidemiológicos y los resultados de exámenes de laboratorio. Ninguno de estos aspectos por si solo entrega un diagnóstico definitivo. El uso de las técnicas treponémicas para confirmación de serología, está reservado para aquellos casos en que el equipo clínico tratante lo considere pertinente y en todos los casos de gestantes sin antecedentes 4
5 de Sífilis previa con serología no treponémica reactiva. El diagnóstico de Sífilis en el recién nacido hijo de madre con sífilis requiere de la comparación de la curva serológica de la mujer durante la gestación, con el resultado de la técnica no treponémica del recién nacido, por tanto ambos deben ser evaluados con la misma técnica de laboratorio (no treponémica). III.- PRUEBA NO TREPONÉMICA VDRL 1.- GENERALIDADES Este procedimiento corresponde a la técnica de VDRL, la cual es una reacción antígeno-anticuerpo de floculación en lámina que está estandarizada para su realización en suero calentado y en líquido cefalorraquídeo (LCR) sin calentar. Emplea una suspensión de antígeno VDRL que se prepara con antígeno VDRL y solución salina amortiguada VDRL. El antígeno es una solución alcohólica incolora que contiene cardiolipina al 0,03%, colesterol al 0,9% y suficiente lecitina purificada para producir una reactividad estándar. La solución salina amortiguada VDRL contiene formaldehido neutro, fosfato disódico, fosfato monopotásico y cloruro de sodio. El examen VDRL mide anticuerpos inespecíficos contra material lipoidal liberado de las células huésped dañadas, así como material de estructura proteica y posiblemente cardiolipina, liberados desde los treponemas. Los anticuerpos antilipoidales son anticuerpos que se producen no sólo como consecuencia de la sífilis y de otras enfermedades treponémicas, sino también en respuesta a enfermedades de naturaleza aguda y crónica en las cuales se produce daño de los tejidos. La técnica VDRL permite el análisis cualitativo y cuantitativo de las muestras de suero y LCR. Es de elección para seguimiento del tratamiento, por ser el primer examen serológico que disminuye sus títulos de reactividad después de un tratamiento adecuado. Un examen No treponémico Reactivo sin otra evidencia clínica o epidemiológica de sífilis, no confirma una infección por T. pallidum. 2. MATERIALES, REACTIVOS Y EQUIPOS MATERIALES Láminas de vidrio con anillos de parafina u otro similar de 14 mm de diámetro Micropipeta de 200 µl Tubos khan Soporte de madera para las láminas. Vaso precipitado de 50 ml Jeringa de vidrio de 1 ó 2 ml Aguja calibre 18G calibrada con 60 +/- 2 gotas /ml (Suero). Aguja calibre 21G calibrada con 100 +/- 2 gotas/ml (LCR). Frasco de vidrio de 30 ml con tapa esmerilada y de fondo plano, para preparación de antígeno Pipetas de vidrio 1 y 5 ml Propipetas 5
6 REACTIVOS Suspensión antigénica Solución salina amortiguada Suero fisiológico al 0.9% Suero fisiológico al 10% Sueros controles: Reactivo, Reactivo débil, No Reactivo EQUIPOS Rotador orbital adaptable a 180 +/- 2 rpm, que describa un circulo de ¾ de pulgada de diámetro en un plano horizontal. Baño termorregulado a 56ºC Centrífuga Microscopio óptico, equipado con ocular 10x y un objetivo de 10x Termómetro ambiental Vitrina refrigerada (2-8ºC) Freezer para -20ºC 3.- TÉCNICA VDRL EN MUESTRAS DE SUERO Antes de empezar a trabajar, el personal del laboratorio debe disponer y utilizar todos los elementos de protección personal requeridos para la manipulación de sangre y fluidos biológicos: guantes, delantal de bioseguridad, antiparras PREPARACIÓN DE MUESTRAS DE SUERO Verificar que las muestras tengan un volumen adecuado, estén libres de hemólisis, lipemia y/o contaminación, condiciones que constituyen causal de rechazo Si la muestra es sangre total, se centrifuga a rpm por 5 minutos para separar el suero Rotular el tubo primario y secundario con el número asignado por el laboratorio Del tubo primario se traspasa el suero a otro tubo khan (secundario), ambos previamente rotulados con el mismo número entregado por el laboratorio Inactivar los sueros tapados a 56ºC durante 30 minutos en el baño termorregulado Dejar enfriar a temperatura ambiente durante 10 minutos hasta su procesamiento y no más allá de 4 horas. Si excede dicho tiempo deberá inactivar nuevamente por 10 minutos adicionales Completar el registro de lecturas de VDRL donde se consignan las muestras a procesar en la corrida Si las muestras no se procesan dentro de las siguientes 4 horas, estas se deben conservar refrigeradas a 2-8 C por un máximo de 48 horas Si las muestras no se procesan dentro de las 48 horas se deben congelar a -20 C, pudiendo conservarse de esta forma hasta 2 años. 6
7 3.2.- PREPARACIÓN DEL ANTÍGENO PARA VDRL EN SUERO Temperar el laboratorio entre 23 y 29 C (óptimo 25 C) Agregar con pipeta de vidrio a un frasco con tapa esmerilada y fondo plano, 0.4 ml de solución salina amortiguada incluida en el kit Agregar 0.5 ml de solución de antígeno gota a gota, por 6 segundos a la solución salina, haciendo rotar el frasco suave y continuamente. La punta de la pipeta debe quedar a nivel del tercio superior del frasco para evitar que tome contacto con la solución salina. Se obtiene la velocidad de rotación adecuada cuando el centro del frasco describe un círculo de dos pulgadas (5 cms.) de diámetro 3 veces por segundo (18 veces en 6 segundos). Continuar con la rotación del frasco durante 10 segundos. Ver figura N Añadir 4.1 ml de solución salina amortiguada con pipeta de 5 ml dejándola escurrir suavemente Tapar el frasco y agitar por inversión vigorosa aproximadamente 30 veces en 10 segundos La solución debe ser usada dentro de las siguientes 8 a 12 horas. Este volumen de 5 ml de suspensión de antígeno alcanza para 180 determinaciones aproximadamente Controlar la suspensión de antígeno cada vez que se prepare, con sueros patrones o sueros control de reactividad conocida (Reactivo, Reactivo débil y No Reactivo). Se recomienda la utilización de sueros controles comerciales, ya que están estabilizados, por lo que no es necesario congelarlos. Los controles preparados en los Laboratorios, deben ser sueros de pacientes, caracterizados por un profesional con experiencia. En este caso, se debe alicuotar los sueros y congelarlos a -20 ºC. Los controles in-house deben ser calentados a 56ºC antes de utilizarlos Las reacciones con los sueros controles deben reproducir la pauta de reactividad establecida. Un suero No Reactivo debe presentar una dispersión completa de las partículas de antígeno No debe usarse una suspensión de antígeno inadecuada, ni tampoco mezclas de suspensiones de antígeno Los sueros controles deben incluirse en todas las preparaciones de la suspensión de antígeno, para asegurar la concentración adecuada de ésta al momento de realizar las determinaciones. Figura Nº 1 Preparación del antígeno para VDRL. 7
8 3.3.- TÉCNICA CUALITATIVA DE VDRL EN SUERO En el extremo superior izquierdo de cada lámina se anota el número de la primera muestra e inferior izquierdo el número de la última Calibrar la aguja despuntada calibre 18G con una jeringa de vidrio de 2 ml aspirando 1 ml de suspensión la cual debe rendir 60 +/-2 gotas, es decir entre 58 y 62. Una gota de aguja calibre 18G corresponde a 17 µl Ubicar las láminas de vidrio en el soporte de madera según el número de muestras a procesar. Agitar los tubos en vortex y con micropipeta dispensar 50 µl de cada una de las muestras preparadas en el punto anterior dentro de cada pocillo y extender el contenido por toda la superficie. Ver figura N Homogenizar la suspensión de antígeno con suaves movimientos circulares. Aspirar un volumen suficiente y en forma vertical, agregar una gota a cada pocillo. Se puede utilizar cualquier dispositivo que rinda el volumen exacto requerido de antígeno. En el caso del uso de una pipeta automática, se recomienda el uso de una pipeta a repetición para minimizar posibles inconvenientes en la cantidad de alícuota dispensada Agitar las láminas durante 4 minutos a 180 rpm en rotador orbital. Figura Nº 2. Láminas para VDRL con 12 pocillos y ejemplo de dispensado de muestras. 3.4 LECTURA E INTERPRETACIÓN DE RESULTADOS TÉCNICA CUALITATIVA DE VDRL EN SUERO Inmediatamente después de la agitación leer las reacciones al microscopio con aumento de 100 x (10x ocular y 10x objetivo) Leer los controles No Reactivo (NR), Reactivo débil (Rd) y Reactivo (R) Interpretación de Lecturas (Ver figura Nº 3): Sin grumos o con ligera rugosidad Grumos pequeños Grumos medianos a grandes : No Reactivo (NR) : Reactivo débil (Rd) : Reactivo (R) 8
9 El resultado Reactivo se caracteriza habitualmente por grumos grandes o pequeños, pero el tamaño es uniforme Todo resultado Reactivo, Reactivo débil y No Reactivo rugoso debe ser analizado cuantitativamente. Esporádicamente se puede presentar un fenómeno de prozona, el cual se debe a un exceso de componente reactivo en el suero (anticuerpos reagínicos en muy alto nivel). Este fenómeno no es de fácil reconocimiento, pero se puede sospechar por la presencia de floculación irregular y de grumos débilmente unidos. Una reacción zonal se informa como Reactiva. Figura Nº 3 Interpretación de lecturas de floculación microscópica. No reactivo Reactivo débil Reactivo TÉCNICA CUANTITATIVA DE VDRL EN SUERO Separar las muestras R a cuantificar Dispensar las muestras según figura N Depositar con micropipeta 50 µl de muestra de suero en el pocillo número 1 (dilución 1:1) y 50 µl de suero fisiológico 0.9 % en los pocillos 5 y 9, según figura Nº En el pocillo número 5 agregue 50 µl de muestra de suero (dilución 1:2), mezclar por aspiración ocho veces con la pipeta automática, evitando la formación de burbujas y transferir 50 µl de esta mezcla al pocillo número 9 (dilución 1:4) mezclar ocho veces igual forma como se explicó anteriormente, descartar los últimos 50 µl Proceder de la misma manera con el resto de las muestras paciente Homogenizar suavemente la suspensión del antígeno y añadir 1 gota a cada pocillo, con aguja calibre 18G Agitar la lámina por 4 minutos en rotador a 180 rpm Leer las reacciones al microscopio según se indica en el punto 3.4. e interpretar los resultados según lo indica el ejemplo de la tabla Nº 1. 9
10 Figura N 4: Esquema de diluciones para VDRL cuantificado. Tabla Nº 1: Ejemplo de interpretación de resultados de VDRL cuantificado Si la reactividad continúa, seguir diluyendo la muestra de la siguiente manera: hacer una dilución 1:8 en tubo, colocando 700 µl de suero fisiológico y 100 µl de muestra y mezclar en vórtex Transferir 50 µl de suero fisiológico al pocillo 5 y 6. Agregar 50 µl de la dilución 1:8 al pocillo 4. Tomar otros 50 µl de esta dilución y mezclar 8 veces con los 50 µl de suero fisiológico del pocillo 5, de ahí tomar 50 µl y mezclar con los 50 µl de suero fisiológico del pocillo 6, mezclar 8 veces y eliminar los últimos 50 µl Agregar una gota de antígeno (17 µl) a cada pocillo. 10
11 Agitar la lámina en el rotador orbital, a 180 rpm por 4 minutos Leer al microscopio según el punto 3.4 y seguir el ejemplo de interpretación de resultados. Tabla Nº Si la reactividad continúa (1:32 R o Rd), preparar diluciones adicionales Preparar dilución 1:64 en tubo, tomando 700 µl de suero fisiológico y 100 µl de la dilución 1:8 y se procede según lo descrito anteriormente hasta la obtención de un resultado NR. 4.- TÉCNICA VDRL EN MUESTRAS DE LÍQUIDO CEFALORRAQUÍDEO (LCR) PREPARACIÓN DE LAS MUESTRAS DE LCR Si las muestras no se procesan dentro de las 4 horas, se conservan refrigeradas entre 2-8 C por un máximo de 48 horas Si las muestras no se procesan dentro de las 48 horas, pueden ser conservadas congeladas a -20 C hasta ser procesadas Las muestras de LCR no necesitan ser inactivadas PREPARACIÓN DEL ANTÍGENO PARA VDRL EN LCR Coloque una parte de solución salina al 10 % y una parte de suspensión de antígeno preparada para usar en muestras de suero Homogenizar suavemente y dejar en reposo por al menos 5 minutos a temperatura ambiente Esta suspensión se puede utilizar solo hasta 2 horas después de preparada EJECUCIÓN TÉCNICA CUALITATIVA Y CUANTITATIVA DE VDRL EN MUESTRAS DE LCR Calibrar la aguja despuntada calibre 21G con una jeringa de vidrio de 2 ml aspirando 1 ml de suspensión la cual debe rendir 100 +/- 2 gotas, es decir entre 98 y 102, correspondiente a 10 µl Las muestras de LCR se procesan de manera cualitativa y cuantitativa, desde la dilución 1:1 a 1: Utilizar una fila horizontal de 4 pocillos de la lámina para cada muestra de LCR Colocar 50 µl de solución salina al 0.9 % en las posiciones 2, 3 y 4 de la lámina Agregar 50 µl LCR al pocillo Tomar otros 50 µl de LCR y mezclar 8 veces con la solución salina del pocillo 2 (dilución 1:2). Traspasar 50 µl al pocillo 3 (dilución 1:4) mezclar 8 veces. Traspasar 50 µl al pocillo 4 (dilución 1:8) mezclar 8 veces y eliminar los 50 µl restantes Homogenizar suavemente la suspensión de antígeno para VDRL en LCR Aspirar el antígeno y en posición vertical agregar una gota a cada muestra (10 µl) Simultáneamente para evaluar reactividad y concentración del antígeno se debe realizar un análisis cuantitativo del control reactivo Agitar las láminas durante 8 minutos en agitador de placas a 180 rpm. 11
12 4.4.- LECTURA E INTERPRETACIÓN DE RESULTADOS TÉCNICA VDRL EN LCR Inmediatamente después de la agitación leer las reacciones según el punto Informar los resultados en término de la mayor dilución de LCR que se observe reactividad. En el estudio de LCR no existe el criterio Rd, siendo toda reactividad categorizada como reactiva (R). 5.- CONTROL DE CALIDAD EN TÉCNICAS DE VDRL CONTROL DE CALIDAD INTERNO Se deben utilizar sueros controles de reactividad R, Rd y NR. Se recomienda la utilización de sueros controles comerciales, ya que son estabilizados, por lo que no es necesario congelarlos. Los controles preparados en los Laboratorios, deben ser sueros de pacientes caracterizados por un profesional con experiencia Estos sueros se deben alicuotar y mantener congelados a -20 ºC. Los controles in-house deben ser calentados a 56ºC antes de utilizarlos Para cada nuevo lote de antígeno se tiene que verificar con los controles R, Rd y NR CRITERIOS DE ACEPTABILIDAD Con el antígeno preparado para la técnica de VDRL, los controles R, Rd y NR presentan una reacción como se observa en la figura Nº El control reactivo es titulado en cada preparación, y éste debe dar un título esperado y reproducible en cada procedimiento CRITERIOS DE RECHAZO Si los controles NR, Rd y R no se comportan de la manera esperada se interrumpe el proceso y se siguen los siguientes pasos: a) Repetir la lectura de los controles utilizando el mismo antígeno. Si la discordancia persiste, Preparar nuevamente el antígeno, idealmente por otro profesional competente. b) Verificar que la fecha de vencimiento del kit esté vigente. Si el problema continúa, utilizar un kit nuevo y repetir los controles. Cambiar de N de Lote si persiste la no conformidad. c) Verificar la temperatura ambiental, esta influye en la reactividad del antígeno. Verificar que esté entre 23 y 29 C. Bajo 23 C pueden obtenerse falsos negativos y sobre 29 C falsos positivos. 12
13 IV.- PRUEBA NO TREPONÉMICA RPR 1.- GENERALIDADES Este procedimiento corresponde a la técnica de RPR, la cual es una reacción antígeno-anticuerpo de floculación en tarjeta (círculo de 18 mm de diámetro) que se realiza en suero o plasma sin calentar o calentado, empleándose una suspensión de antígeno VDRL modificado con fosfato de sodio y potasio, mertiolato, cloruro de colina, EDTA y partículas de carbón. El cloruro de colina elimina la necesidad de calentar las muestras; el EDTA le da mayor estabilidad a la suspensión de antígeno y las partículas de carbón permiten que la lectura se realice a ojo desnudo. El examen RPR mide anticuerpos inespecíficos producidos en respuesta al material lipoidal liberado desde las células dañadas del huésped, así como en respuesta a material de estructura proteica, liberado desde los treponemas. Los anticuerpos antilipoidales son anticuerpos producidos, no solo a consecuencia de una sífilis u otras enfermedades treponémicas sino también en respuesta a enfermedades no treponémicas, agudas o crónicas, en las cuales hay daño de los tejidos. Si hay presencia de anticuerpos, estos se combinan con las partículas lipídicas del antígeno produciendo aglutinación. Las partículas de carbón coaglutinan con los anticuerpos dando como resultado la formación de grumos negros sobre el fondo blanco de la tarjeta de lectura. Si no hay anticuerpos presentes se observa en la muestra un color gris uniforme, un punto negro o una cola de humo. La técnica de RPR se emplea generalmente como técnica de screening (tamizaje). Un examen no treponémico reactivo, sin otra evidencia clínica y/o epidemiológica de sífilis, no confirma la infección. La prueba de RPR en tarjeta no puede utilizarse para analizar líquido cefalorraquídeo, la única prueba estandarizada y recomendada internacionalmente es el VDRL. 2.- MATERIAL, REACTIVO Y EQUIPO MATERIALES Aguja calibre 20G sin bisel, que rinde un volumen de 60 ± 2 gotas por ml de antígeno Micropipeta automática REACTIVOS E INSUMOS Tarjetas recubiertas de plástico, cada una con 10 círculos de 18 mm de diámetro. Pipetas plásticas desechables, que rinden un volumen de 50 µl por gota. Antígeno RPR, en ampollas de 1 o 3 ml. Frasco plástico para distribuir el antígeno. Aguja calibre 20G sin bisel, que rinde un volumen de 60 ± 2 gotas por ml de antígeno. Sueros Controles NR, R, Rd o Mínimo. EQUIPOS Rotador orbital adaptable a 180 +/- 2 rpm, que describa un circulo de ¾ de pulgada de diámetro en un plano horizontal. Refrigerador (2-8ºC) Freezer para -20ºC Cubierta humedecedora 13
14 3.- DESARROLLO Antes de empezar a trabajar, el personal del laboratorio debe disponer y utilizar todos los elementos de protección personal requeridos para la manipulación de sangre y fluidos biológicos: guantes, delantal de bioseguridad, antiparras PREPARACIÓN DE MUESTRAS DE SUERO Verificar que las muestras tengan un volumen adecuado, estén libres de hemólisis, lipemia y/o contaminación, condiciones que constituyen causal de rechazo Si la muestra es sangre total, se centrifuga a rpm por 5 minutos para separar el suero Si el análisis se realiza de inmediato, los sueros se pueden retener en el tubo de recolección original. Vaciar a tubos limpios y secos si se va a postergar el análisis Completar el registro de lecturas de RPR donde se consignan las muestras a procesar en la corrida Si las muestras no se procesan dentro de las siguientes 4 horas, estas se deben conservar refrigeradas a 2-8 C por un máximo de 48 horas Si las muestras no se procesan dentro de las 48 horas se deben congelar a -20 C SUSPENSIÓN DE ANTÍGENO DE RPR Seguir las instrucciones del fabricante Colocar la aguja en el frasco plástico Agitar suavemente la ampolla de antígeno para resuspender las partículas de carbón Abrir cuidadosamente la ampolla protegiendo los dedos con guantes o toalla de papel Por succión, trasladar toda la suspensión del antígeno desde la ampolla al frasco plástico, colocando la aguja en el fondo de la ampolla y comprimiendo el frasco plástico para usarlo como una perilla de succión Rotular el frasco plástico con el número de lote, fecha de expiración de la suspensión de antígeno y fecha en que se vació el antígeno de la ampolla al frasco plástico La ampolla con antígeno, sin abrir y de manera refrigerada a 2º- 8 ºC se mantiene estable durante 12 meses después de la fecha de manufactura. No congelar La suspensión de antígeno depositada en el frasco plástico es estable hasta 3 meses, de manera refrigerada entre 2º - 8ºC La suspensión de antígeno debe protegerse de la luz y de temperaturas superiores a 30ºC. Nunca debe utilizarse más allá de la fecha de expiración El uso inmediato de un antígeno refrigerado puede producir una disminución de la sensibilidad de la prueba. Por esta razón después de retirar del refrigerador, permitir que el antígeno alcance la temperatura ambiente (entre 23º y 29ºC) antes de usarlo Usar sólo las suspensiones de antígeno que reproduzcan el patrón de reacción con los sueros controles Agitar suavemente el frasco cada vez que se distribuya el antígeno. 14
15 3.3.- PRUEBA CUALITATIVA DE RPR EN SUERO (EN TARJETA) Depositar 50 µl de muestra sin calentar o calentada, en un anillo de 18 mm de la tarjeta, usando una pipeta automática. Figura N Guardar las tarjetas a temperatura ambiente, no tocar con los dedos el área dentro de los anillo para no engrasarlos. Cada anillo debe usarse una sola vez Extienda el suero completamente dentro del anillo con la punta plástica, evitando que el suero se salga de este Agitar suavemente el frasco plástico que contiene el antígeno para resuspender las partículas Sosteniendo el frasco plástico con la aguja en posición vertical dejar caer varias gotas para eliminar el aire de la aguja y agregar una gota de la suspensión de antígeno RPR a cada anillo que contenga suero. No mezclar. El antígeno y la muestra se mezclarán durante la rotación Colocar la tarjeta en un rotador orbital y agitar 8 minutos a 100 (+/- 2) rpm De manera opcional se recomienda usar una cámara húmeda para cubrir las tarjetas durante el período de rotación, para evitar la evaporación. Puede colocarse una bandeja recubierta con papel absorbente humedecido con agua destilada Leer las reacciones a ojo desnudo, inmediatamente después de terminada la rotación, sobre un fondo negro y con luz blanca potente. No emplear luz fluorescente porque las reacciones mínimas pueden omitirse. Para distinguir mejor los resultados No Reactivos de los Reactivos mínimos, girar e inclinar ligeramente la tarjeta. Figura Nº 5: Ejemplo de tarjeta plástica RPR con 10 anillos 15
16 3.4.- LECTURA E INTERPRETACIÓN DE RESULTADOS TÉCNICA CUALITATIVA DE RPR Informar los resultados de la siguiente manera: Grumos pequeños a grandes: Sin grumos o rugosidad muy leve: Reactivo (R) No Reactivo (NR) En el examen RPR los resultados se informan como Reactivo o No Reactivo. La reacción Reactiva mínima (o débil) se informa Reactiva. Figura Nº 6: Interpretación de lectura de floculación macroscópica PRUEBA CUANTITATIVA DE RPR EN SUERO (EN TARJETA) Para cada muestra a ser analizada, deposite 50 ul de solución salina al 0.9% en los anillos Nº 2 al Nº5 de la tarjeta. No se debe extender la solución salina Coloque 50 µl de muestra en el anillo Nº Deposite 50 µl de muestra en el anillo Nº 2 mezclando el contenido 5 a 6 veces, evitando la formación de burbujas. Extienda la mezcla en todo el diámetro del anillo Transferir 50 µl del anillo 2, al 3, al 4, al 5 mezclando después de cada transferencia. Deseche 50 µl después de mezclar el contenido en el anillo Nº Sosteniendo el frasco plástico con la aguja en posición vertical dejar caer varias gotas para eliminar el aire de la aguja, posteriormente agregar una gota de la suspensión de antígeno RPR a cada anillo que contenga suero. No mezclar Colocar la tarjeta en el rotador orbital y agitar 8 minutos a 100 (+/- 2) r.p.m Opcionalmente es recomendable usar una cámara húmeda para cubrir las tarjetas durante el período de rotación Leer las reacciones, a ojo desnudo, inmediatamente después de terminada la rotación, sobre un 16
17 fondo negro y con luz potente. No emplear luz fluorescente porque las reacciones mínimas pueden omitirse. Para distinguir mejor los resultados No Reactivos de los Reactivos mínimos, girar e inclinar ligeramente la tarjeta Si la solución más diluida analizada (1:16) resulta reactiva, se prepara una dilución 1:16 de la muestra de prueba, agregando 100 µl de suero a 1.5 ml de solución salina al 0.9%. Mezclar bien. Deposite 50 µl de dilución 1:16 en el anillo Nº 1 y complete el procedimiento en la forma descrita anteriormente hasta obtener un resultado No Reactivo. 4.- CONTROL DE CALIDAD RPR CONTROL DE CALIDAD INTERNO Se deben utilizar sueros controles R y NR, es recomendable además la inclusión de un control de reactividad mínima Se recomienda la utilización de sueros controles comerciales, ya que son estabilizados, por lo que no es necesario congelarlos. Los controles preparados en los Laboratorios, deben ser sueros de pacientes caracterizados por un profesional con experiencia. Estos sueros se deben alicuotar y mantener congelados a -20 ºC Para cada nuevo lote de un kit se debe realizar una verificación con los sueros controles CRITERIOS DE ACEPTABILIDAD Los sueros controles reproducen el patrón de reactividad correspondiente CRITERIOS DE RECHAZO Si los controles no se comportan de la manera esperada se interrumpe el proceso y se siguen estos pasos: Repetir la lectura de los controles utilizando el mismo antígeno. Si la discordancia persiste, repetir el procedimiento con un nuevo frasco de antígeno Verificar la vigencia del kit con la fecha de vencimiento. Si el problema continúa, utilizar un kit nuevo y repetir los controles. Cambiar a otro lote de kit si persiste la no conformidad. 17
18 V.- PRUEBA TREPONEMICA MHA-Tp 1.- GENERALIDADES Test de hemaglutinación pasiva para la detección de anticuerpos específicos anti-t. pallidum. Este método utiliza eritrocitos de pollo como fase sólida, los cuales están sensibilizados con un extracto antigénico de T. pallidum, que se encuentra adherido a la membrana del eritrocito. Estos eritrocitos sensibilizados aglutinarán con los anticuerpos específicos presentes en el suero de pacientes sifilíticos. Esta técnica tiene la ventaja de su alta especificidad, la cual es comparable con FTA-ABS. Las reacciones falso-positivas son extremadamente infrecuentes, por estas razones esta técnica se utiliza como prueba de confirmación serológica. 2.- MATERIALES, REACTIVOS Y EQUIPOS Materiales Tubos de vidrio khan Placas de microtitulación con fondo en U Soporte con espejo de aumento para lectura del fondo de los pocillos. Reactivos Kit de MHA-Tp: Reactivo antígeno: Suspensión de eritrocitos de pollo sensibilizados. Reactivo Control: Suspensión de eritrocitos de pollo no sensibilizados. Solución diluyente: Tampón fosfato salino que contiene componentes solubles de Treponema Reiter y agentes estabilizadores. Control positivo: Suero de conejo inmune. Control negativo: Suero de conejo no inmune. Equipos Centrífuga Micropipetas automáticas Refrigerador (2-8ºC) Freezer para -20ºC 3.- DESARROLLO DE LA TECNICA Antes de empezar a trabajar, el personal del laboratorio debe disponer y utilizar todos los elementos de protección personal requeridos para la manipulación de sangre y fluidos biológicos: guantes, delantal de bioseguridad, antiparras PREPARACIÓN DE LAS MUESTRAS Y ALMACENAJE Verificar que las muestras tengan un volumen adecuado, estén libres de hemólisis, lipemia y/o contaminación, condiciones que constituyen causal de rechazo. 18
19 Si la muestra es sangre total se centrifuga a rpm por 5 minutos para separar el suero, rotular el tubo primario y secundario con el examen solicitado, número asignado y la fecha, utilizando una etiqueta autoadhesiva impresa Si las muestras no se procesan dentro de las 4 horas, se conservan refrigerados entre 2-8 C por un máximo de 72 horas Si las muestras no se procesan dentro de las 72 horas, se conservan congeladas a -20 C PROCEDIMIENTO TÉCNICO Permitir que los reactivos alcancen la temperatura ambiente Para cada test se necesitan 4 pocillos de la microplaca, 2 de los cuales se utilizarán para la preparación de la dilución de la muestra. Ver Tabla Nº Verificar que los eritrocitos del reactivo antígeno y el reactivo control estén resuspendidos adecuadamente (debe realizarse suavemente) Distribuir 25 µl de solución diluyente en el pocillo 1, 100 µl en el pocillo 2 y 25 µl en cada uno de los pocillos 3 y Añadir 25 µl de la muestra en el pocillo 1. Mezclar el contenido del pocillo 1 y transferir 25 µl al pocillo 2. Mezclar y transferir 25 µl del pocillo 2 al pocillo 3, mezclar y desechar 25 µl del pocillo 3. Transferir otros 25 µl del pocillo 2 al pocillo 4, mezclar y desechar 25 µl del pocillo Añadir 75 µl de reactivo control al pocillo 3 y 75 µl de reactivo antígeno al pocillo Mezclar el contenido de los pocillos dando ligeros golpes en los lados de la placa Cubrir la placa e incubar durante minutos a temperatura ambiente y en lugar libre de vibraciones. Mantener lejos de cualquier fuente de calor Leer los resultados en el soporte con espejo de aumento. Tabla Nº 2. Esquema de realización de las diluciones en prueba de MHA-Tp Pocillo N control Solución diluyente µl Muestra µl 25 4 prueba Mezclar y transferir Dilución de la muestra 1:2 1:10 1:20 1:20 Reactivo control µl Reactivo antígeno Dilución final 1:
20 3.3.- LECTURA E INTERPRETACIÓN DE RESULTADOS La lectura e interpretación es realizada de acuerdo a la tabla N 3. Las lecturas correspondientes a +/- y 1+ ocurren ocasionalmente, debido al título bajo de anticuerpos o a errores técnicos. A estos sueros se les debe repetir el examen. Si el resultado es el mismo, se deben informar cómo no reactivo o reactivo mínimo respectivamente. Tabla Nº3. Lectura e Interpretación de resultados de prueba de hemaglutinación. 4+ Tapiz homogéneo de células aglutinadas que cubre el fondo del pocillo, a veces con bordes irregulares 3+ Tapiz homogéneo de células aglutinadas que cubre parcialmente el fondo del pocillo 2+ Tapiz homogéneo de células aglutinadas rodeado por un anillo de eritrocitos 1+ Tapiz homogéneo de células aglutinadas rodeado por un anillo de eritrocitos. Repetir, si da igual informar R. Si da +/- o informar NR. +/- Botón de eritrocitos con una pequeña abertura central. Repetir, si da igual o informar NR. - Botón de eritrocitos con una muy pequeña abertura central o botón totalmente compacto Interpretación: Positivo o Reactivo: desde 4+ a 1+ Negativo o No Reactivo: - Los resultados deben ser informados como Reactivo o No Reactivo, de acuerdo a la interpretación realizada. 20
21 4.- CONTROL DE CALIDAD MHA-Tp Incluir el control positivo y el control negativo en cada serie de muestras teniendo en cuenta que estos controles ya están pre diluidos 1:20. Añadir 25 µl de cada control directamente en los pocillos 3 y 4. No añadir solución diluyente. Enfrentar ambos controles con el Reactivo control y el Reactivo antígeno. Criterios de aceptabilidad: Cuando los controles positivo y negativo se comportan de acuerdo a lo esperado. Criterios de rechazo: Si los controles positivo y negativo no se comportan como en la tabla de lectura se rechaza la corrida. Si no se acepta la corrida, se repite al análisis. Si persiste el rechazo se cambia de lote de kit. Los sueros positivos que además que presenten reacción positiva con el reactivo control, se deben informar no concluyente. En esta situación se recomienda el envío de la muestra al laboratorio de referencia. BIBLIOGRAFÍA 1.- Instituto Nacional de Enfermedades Infecciosas ANLIS Dr. Carlos G. Malbrán. Manual de Técnicas y Procedimientos para el Diagnóstico de Sífilis. Abril S. A. Larsen, B. M. Steiner, A. H. Rudolph. Laboratory Diagnosis and Interpretation of Test for Syphilis. Clin Microbiol Rev Jan; 8(1): Manual de técnicas para Sífilis. Liliana Urra Centers for Disease Control and Prevention. Manual of Tests for Syphilis. 9th Edition. Disponible en: 21
Diagnóstico Serológico de Sífilis Técnicas no treponémicas
 Diagnóstico Serológico de Sífilis Técnicas no treponémicas T.M. Rodrigo Colina Morales Laboratorio de Infecciones de Transmisión Sexual Sección Bacteriología Mayo 2014 Diagnóstico Serológico de Sífilis
Diagnóstico Serológico de Sífilis Técnicas no treponémicas T.M. Rodrigo Colina Morales Laboratorio de Infecciones de Transmisión Sexual Sección Bacteriología Mayo 2014 Diagnóstico Serológico de Sífilis
Parámetros Clínicos y Serológicos en el Diagnóstico de la Sífilis
 Curso Teorico-Práctico en Técnicas de Diagnóstico de Serología de Sífilis Instituto de Salud Pública Parámetros Clínicos y Serológicos en el Diagnóstico de la Sífilis 2014 Dra. M Soledad Bertolo P. Jefe
Curso Teorico-Práctico en Técnicas de Diagnóstico de Serología de Sífilis Instituto de Salud Pública Parámetros Clínicos y Serológicos en el Diagnóstico de la Sífilis 2014 Dra. M Soledad Bertolo P. Jefe
WITNESS RELAXIN (plasma, serum) RLX RLX u d 9 n n ersio V X RLX L R -W IO B S
 WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS
 HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Diagnóstico Serológico de Sífilis Técnicas treponémicas
 Diagnóstico Serológico de Sífilis Técnicas treponémicas T.M. Rodrigo Colina Morales Laboratorio de Infecciones de Transmisión Sexual Sección Bacteriología Mayo 2014 FTA-ABS (Fluorescent Treponemal Antibody
Diagnóstico Serológico de Sífilis Técnicas treponémicas T.M. Rodrigo Colina Morales Laboratorio de Infecciones de Transmisión Sexual Sección Bacteriología Mayo 2014 FTA-ABS (Fluorescent Treponemal Antibody
Caso clínico Sífilis Secundaria. Dra. Macarena Vidal Abril de 2013
 Caso clínico Sífilis Secundaria Dra. Macarena Vidal Abril de 2013 Historia clínica Sexo femenino, 47 años. Procedente de Montevideo. Casada, ama de casa, 2 hijos. Motivo de consulta en Departamento de
Caso clínico Sífilis Secundaria Dra. Macarena Vidal Abril de 2013 Historia clínica Sexo femenino, 47 años. Procedente de Montevideo. Casada, ama de casa, 2 hijos. Motivo de consulta en Departamento de
Identificación y medición de la respuesta inmune PRUEBAS SECUNDARIAS
 Identificación y medición de la respuesta inmune PRUEBAS SECUNDARIAS La prueba a realizar depende de las características del Ag SOLUBLE PRECIPITACIÓN PARTICULADO AGLUTINACIÓN SUPERFICIE + COMPLEMENTO FIJACIÓN
Identificación y medición de la respuesta inmune PRUEBAS SECUNDARIAS La prueba a realizar depende de las características del Ag SOLUBLE PRECIPITACIÓN PARTICULADO AGLUTINACIÓN SUPERFICIE + COMPLEMENTO FIJACIÓN
SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA
 SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA Aplicación El análisis de sangre ImmuView Legionella de Statens Serum Institute se ha creado para el diagnóstico de una infección
SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA Aplicación El análisis de sangre ImmuView Legionella de Statens Serum Institute se ha creado para el diagnóstico de una infección
LIMPIEZA Y DESINFECCION
 PAGINA: 1 de 7 1. DEFINICION: Es el procedimiento, mediante el cual son eliminados los diferentes desechos generados en los procesos de recolección y procesamiento de muestras; y además se describe el
PAGINA: 1 de 7 1. DEFINICION: Es el procedimiento, mediante el cual son eliminados los diferentes desechos generados en los procesos de recolección y procesamiento de muestras; y además se describe el
VDRL PERSISTENTEMENTE POSITIVO UN PROBLEMA CLÍNICO FRECUENTE
 VDRL PERSISTENTEMENTE POSITIVO UN PROBLEMA CLÍNICO FRECUENTE Dr. Martín Lopez Corregido por Prof. Adj. Zaida Arteta Ateneo 30 de Agosto 2013 SF 31 años. EA: Enviada a policlínica de Infectología por VDRL
VDRL PERSISTENTEMENTE POSITIVO UN PROBLEMA CLÍNICO FRECUENTE Dr. Martín Lopez Corregido por Prof. Adj. Zaida Arteta Ateneo 30 de Agosto 2013 SF 31 años. EA: Enviada a policlínica de Infectología por VDRL
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL
 UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO
 SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
Olanzapina en polvo y disolvente para suspensión inyectable de liberación prolongada
 ZYPADHERA Olanzapina en polvo y disolvente para suspensión inyectable de liberación prolongada Instrucciones para la reconstitución y administración dirigido a Profesionales Sanitarios Información sobre
ZYPADHERA Olanzapina en polvo y disolvente para suspensión inyectable de liberación prolongada Instrucciones para la reconstitución y administración dirigido a Profesionales Sanitarios Información sobre
Fortel PROSTATE (PSA)
 Fortel PROSTATE (PSA) Test para Screening Simple, realizable y confidencial [Seleccione la fecha] Un test visual fácil, para detectar niveles anormales del Antígeno Prostático Específico (PSA), sobre rango
Fortel PROSTATE (PSA) Test para Screening Simple, realizable y confidencial [Seleccione la fecha] Un test visual fácil, para detectar niveles anormales del Antígeno Prostático Específico (PSA), sobre rango
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt
 Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
Práctica Nº 5 Prueba de Diagnóstico Serológico para Infección por Treponema pallidum (V.D.R.L.) y evaluación microscópica de Treponemas orales
 Universidad de Los Andes Facultad de Odontología Departamento de Biopatología Cátedra de Microbiología 2º Año, U-2011 Práctica Nº 5 Prueba de Diagnóstico Serológico para Infección por Treponema pallidum
Universidad de Los Andes Facultad de Odontología Departamento de Biopatología Cátedra de Microbiología 2º Año, U-2011 Práctica Nº 5 Prueba de Diagnóstico Serológico para Infección por Treponema pallidum
Inmunohematología. Dra. Ana Cecilia Haro
 Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
ORDEN SPIROCHAETALES FAMILIA TREPONEMATACEAE GÉNERO TREPONEMA. QF L. Urra 12-08-13
 ORDEN SPIROCHAETALES FAMILIA TREPONEMATACEAE GÉNERO TREPONEMA QF L. Urra 12-08-13 Infección por T. pallidum subespecie pallidum Huésped produce anticuerpos: 1. contra material lipoidal liberado por las
ORDEN SPIROCHAETALES FAMILIA TREPONEMATACEAE GÉNERO TREPONEMA QF L. Urra 12-08-13 Infección por T. pallidum subespecie pallidum Huésped produce anticuerpos: 1. contra material lipoidal liberado por las
DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4
 Universidad Tecnológica Nacional Facultad Regional La Plata DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4 Descenso crioscópico Objeto de la experiencia:
Universidad Tecnológica Nacional Facultad Regional La Plata DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4 Descenso crioscópico Objeto de la experiencia:
GenPE: estudio Internacional de Genética en Preeclampsia
 GenPE: estudio Internacional de Genética en Preeclampsia INSTRUCTIVO Toma de muestra proyecto GenPE PAQUETE PARA CAPTACIÓN DE PACIENTE Y TOMA DE MUESTRA. Cuando llegue a su institución la caja del proyecto
GenPE: estudio Internacional de Genética en Preeclampsia INSTRUCTIVO Toma de muestra proyecto GenPE PAQUETE PARA CAPTACIÓN DE PACIENTE Y TOMA DE MUESTRA. Cuando llegue a su institución la caja del proyecto
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA
 PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
Métodos para la determinación de grasas
 Practica 4 Métodos para la determinación de grasas Antecedentes Los lípidos se encuentran ampliamente distribuidos en animales y vegetales, formado parte fundamental de membranas celulares. En los alimentos
Practica 4 Métodos para la determinación de grasas Antecedentes Los lípidos se encuentran ampliamente distribuidos en animales y vegetales, formado parte fundamental de membranas celulares. En los alimentos
Determinación de Alcalinidad en aguas naturales y residuales
 QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Alcalinidad en aguas naturales y residuales Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 29/09/2013 Método Titulométrico
QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Alcalinidad en aguas naturales y residuales Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 29/09/2013 Método Titulométrico
Trabajo Práctico N 3. Reconocimiento de sustancias ácidas, básicas y neutras. mediante el empleo de indicadores químicos.
 Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
INSTRUCCIÓN TÉCNICA DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Determinación del antígeno D Débil Du Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de
Determinación del antígeno D Débil Du Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de
D E L I A R O S A H E R R E R A H E R N Á N D E Z B a c t e r i ó l o g a
 D E L I A R O S A H E R R E R A H E R N Á N D E Z B a c t e r i ó l o g a B L A N C A L U Z S A L D A R R I A G A G A V I R I A B a c t e r i ó l o g a REVISADO POR APROBADO POR NOMBRE Delia Rosa Herrera
D E L I A R O S A H E R R E R A H E R N Á N D E Z B a c t e r i ó l o g a B L A N C A L U Z S A L D A R R I A G A G A V I R I A B a c t e r i ó l o g a REVISADO POR APROBADO POR NOMBRE Delia Rosa Herrera
PRUEBAS DE DIAGNOSTICO. Hospital Roosevelt Laboratorio Clínica de Enfermedades Infecciosas Septiembre 2013
 PRUEBAS DE DIAGNOSTICO Hospital Roosevelt Laboratorio Clínica de Enfermedades Infecciosas Septiembre 2013 DIAGNÓSTICO DE LA INFECCIÓN POR EL VIH El diagnóstico definitivo de la infección por el VIH sólo
PRUEBAS DE DIAGNOSTICO Hospital Roosevelt Laboratorio Clínica de Enfermedades Infecciosas Septiembre 2013 DIAGNÓSTICO DE LA INFECCIÓN POR EL VIH El diagnóstico definitivo de la infección por el VIH sólo
INSTRUCCIONES PARA LA PROFICIENCIA DE JUNIO
 15 de agosto de 2016 Laboratorios Participantes Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia
15 de agosto de 2016 Laboratorios Participantes Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia
Sífilis. Epidemiologia, diagnóstico y tratamiento. Dr. Samuel Navarro Alvarez, MSP Medico Internista e Infectólogo
 Sífilis. Epidemiologia, diagnóstico y tratamiento Dr. Samuel Navarro Alvarez, MSP Medico Internista e Infectólogo Generalidades de Sífilis Enfermedad descrita hace mas 500 de años Treponema padillum, esquiroqueta
Sífilis. Epidemiologia, diagnóstico y tratamiento Dr. Samuel Navarro Alvarez, MSP Medico Internista e Infectólogo Generalidades de Sífilis Enfermedad descrita hace mas 500 de años Treponema padillum, esquiroqueta
MEDICIÓN DEL VOLUMEN
 MEDICIÓN DEL VOLUMEN CONCEPTOS BÁSICOS Volumen: porción de espacio que ocupa un cuerpo ya sea sólido, líquido o gaseoso. Capacidad: es el volumen de un fluido que puede contener o suministrar un instrumento
MEDICIÓN DEL VOLUMEN CONCEPTOS BÁSICOS Volumen: porción de espacio que ocupa un cuerpo ya sea sólido, líquido o gaseoso. Capacidad: es el volumen de un fluido que puede contener o suministrar un instrumento
COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS
 DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
Tenga en cuenta el espacio pequeño. Me pareció que el espacio aéreo más, un CDS más débiles se produjo. Tanto como el 50% menos!
 Cómo preparo CDS a través del "Shot Glass" Método Cómo preparar un litro o cuarto de galón de solución de 25 ppm de dióxido de cloro - 26 de septiembre 212 Descargo de responsabilidad: Este procedimiento
Cómo preparo CDS a través del "Shot Glass" Método Cómo preparar un litro o cuarto de galón de solución de 25 ppm de dióxido de cloro - 26 de septiembre 212 Descargo de responsabilidad: Este procedimiento
Protocolo de toma de muestra arterial MANUAL DE CALIDAD LABORATORIO CLÍNICO. PRO 08 D Ed 01 Protocolo extracción arterial
 MANUAL DE CALIDAD LABORATORIO CLÍNICO Protocolo de toma de muestra arterial Código Fecha emisión/última revisión Revisado Aprobado PRO 08 D Ed 01 18/11/09 Spsor. Rafael Infantes Viano Dr. Vidal Pérez Valero.
MANUAL DE CALIDAD LABORATORIO CLÍNICO Protocolo de toma de muestra arterial Código Fecha emisión/última revisión Revisado Aprobado PRO 08 D Ed 01 18/11/09 Spsor. Rafael Infantes Viano Dr. Vidal Pérez Valero.
INSTITUTO DE EDUCACIÓN SUPERIOR TECNOLÓGICO PRIVADO SANTA ROSA DE LIMA ENFERMERÍA Y VÍAS DE ADMINISTRACIÓN DE LAS VACUNAS
 INSTITUTO DE EDUCACIÓN SUPERIOR TECNOLÓGICO PRIVADO SANTA ROSA DE LIMA ENFERMERÍA Y VÍAS DE ADMINISTRACIÓN DE LAS VACUNAS LIC. JUDITH ISABEL POLO NICHO 1. PUNTOS CLAVE: Las vacunas deben administrarse
INSTITUTO DE EDUCACIÓN SUPERIOR TECNOLÓGICO PRIVADO SANTA ROSA DE LIMA ENFERMERÍA Y VÍAS DE ADMINISTRACIÓN DE LAS VACUNAS LIC. JUDITH ISABEL POLO NICHO 1. PUNTOS CLAVE: Las vacunas deben administrarse
CÓMO... Tomar Muestras de Tejido para Histopatología
 para Histopatología Por qué se deben tomar muestras de tejido para histopatología? El tomar muestras de tejido para histopatología es una manera barata y rápida de obtener información adicional importante
para Histopatología Por qué se deben tomar muestras de tejido para histopatología? El tomar muestras de tejido para histopatología es una manera barata y rápida de obtener información adicional importante
Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención
 Guía de Referencia Rápida Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención Guía de Referencia Rápida
Guía de Referencia Rápida Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención Guía de Referencia Rápida
Treponema pallidum. y la sífilis
 Treponema pallidum y la sífilis Treponema pallidum Generalidades No desarrolla in vitro; en el laboratorio se le cultiva en testículos de conejo Es Gram y anaerobia Es liofilizable (Nichol) y presenta
Treponema pallidum y la sífilis Treponema pallidum Generalidades No desarrolla in vitro; en el laboratorio se le cultiva en testículos de conejo Es Gram y anaerobia Es liofilizable (Nichol) y presenta
INSTRUCTIVO PARA LA BÚSQUEDA ACTIVA INSTITUCIONAL DE SÍFILIS GESTACIONAL Y CONGÉNITA INSTITUTO NACIONAL DE SALUD DICIEMBRE DE 2011
 INSTRUCTIVO PARA LA BÚSQUEDA ACTIVA INSTITUCIONAL DE SÍFILIS GESTACIONAL Y CONGÉNITA INSTITUTO NACIONAL DE DICIEMBRE DE 2011 SUBDIRECCIÓN DE VIGILANCIA Y CONTROL EN PÚBLICA GRUPO DE INFECCIONES DE TRANSMISIÓN
INSTRUCTIVO PARA LA BÚSQUEDA ACTIVA INSTITUCIONAL DE SÍFILIS GESTACIONAL Y CONGÉNITA INSTITUTO NACIONAL DE DICIEMBRE DE 2011 SUBDIRECCIÓN DE VIGILANCIA Y CONTROL EN PÚBLICA GRUPO DE INFECCIONES DE TRANSMISIÓN
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico.
 FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
FUNDAMENTO MATERIAL Y EQUIPOS. Entre otros materiales es necesario disponer de:
 González,E.yAlloza,A.M. Ensayos para determinar las propiedades mecánicas y físicas de los áridos: métodos para la determinación de la resistencia a la fragmentación. Determinación de la resistencia a
González,E.yAlloza,A.M. Ensayos para determinar las propiedades mecánicas y físicas de los áridos: métodos para la determinación de la resistencia a la fragmentación. Determinación de la resistencia a
J. Muestras Proficiencia para Contaje de Espermatozoides.
 22 de febrero de 2016 Laboratorios Participantes Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de
22 de febrero de 2016 Laboratorios Participantes Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de
Pruebas de Compatibilidad de Materiales Constituyentes del Shotcrete
 Anexo A: Pruebas de Compatibilidad de Materiales Constituyentes del Shotcrete A ANEXOS Pruebas de Compatibilidad de Materiales Constituyentes del Shotcrete Este anexo presenta una forma estandarizada en
Anexo A: Pruebas de Compatibilidad de Materiales Constituyentes del Shotcrete A ANEXOS Pruebas de Compatibilidad de Materiales Constituyentes del Shotcrete Este anexo presenta una forma estandarizada en
CONTROL DE CALIDAD EN EL LABORATORIO DE SEROLOGIA DE SIFILIS
 CONTROL DE CALIDAD EN EL LABORATORIO DE SEROLOGIA DE SIFILIS TM. Alejandra Manríquez C. Laboratorio de Infecciones de Transmisión Sexual Instituto de Salud Pública Mayo 2013 Definiciones Qué es Calidad?
CONTROL DE CALIDAD EN EL LABORATORIO DE SEROLOGIA DE SIFILIS TM. Alejandra Manríquez C. Laboratorio de Infecciones de Transmisión Sexual Instituto de Salud Pública Mayo 2013 Definiciones Qué es Calidad?
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente
 Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO FACULTAD DE MEDICINA Y NUTRICIÓN Unidad Médica de Simulación Clínica "Dr. José Jorge Talamas Márquez"
 LICENCIATURA EN NUTRICIÓN Practica #10 TOMA DE MUESTRA DE GLUCOSA CAPILAR OBJETIVOS: Al concluir la práctica el alumno será capaz de: 1. Definir y conocer la técnica de toma de muestra de glucosa capilar
LICENCIATURA EN NUTRICIÓN Practica #10 TOMA DE MUESTRA DE GLUCOSA CAPILAR OBJETIVOS: Al concluir la práctica el alumno será capaz de: 1. Definir y conocer la técnica de toma de muestra de glucosa capilar
Infección por T. pallidum subespecie pallidum
 Infección por T. pallidum subespecie pallidum Huésped produce anticuerpos: 1. contra material lipoidal liberado por las células dañadas (reaginas) 2. contra material lipoproteico y cardiolipina liberada
Infección por T. pallidum subespecie pallidum Huésped produce anticuerpos: 1. contra material lipoidal liberado por las células dañadas (reaginas) 2. contra material lipoproteico y cardiolipina liberada
Sistema Integrado de Gestión. Titulación ácido-base. Determinación del contenido de ácido acético en el vinagre
 Sistema Integrado de Gestión Titulación ácido-base. Determinación del contenido de ácido acético en el vinagre Versión 3 Proceso: Investigación IV Febrero de 2016 Página 2 de 9 1. OBJETIVOS Ilustrar los
Sistema Integrado de Gestión Titulación ácido-base. Determinación del contenido de ácido acético en el vinagre Versión 3 Proceso: Investigación IV Febrero de 2016 Página 2 de 9 1. OBJETIVOS Ilustrar los
Manejo de la Sífilis en Atención Primaria
 Manejo de la Sífilis en Atención Primaria O L I V E R T O S T E - B E L L O D O R T A R 1 M F Y C T U T O R A : M A R I A J O S E M O N E D E R O M I R A C. S. R A F A L A F E N A E N E R O 2 0 1 5 Qué
Manejo de la Sífilis en Atención Primaria O L I V E R T O S T E - B E L L O D O R T A R 1 M F Y C T U T O R A : M A R I A J O S E M O N E D E R O M I R A C. S. R A F A L A F E N A E N E R O 2 0 1 5 Qué
SOLICITUD DE COTIZACIÓN REACTIVOS PARA LABORATORIO CLINICO Proceso de Compra Menor
 CAJA DE SALUD DE LA BANCA PRIVADA www.csbp.com.bo REGIONAL Cochabamba SOLICITUD DE COTIZACIÓN REACTIVOS PARA LABORATORIO CLINICO Proceso de Compra Menor N RL-06/13 N RL-06/13 Cochabamba 5 de Agosto de
CAJA DE SALUD DE LA BANCA PRIVADA www.csbp.com.bo REGIONAL Cochabamba SOLICITUD DE COTIZACIÓN REACTIVOS PARA LABORATORIO CLINICO Proceso de Compra Menor N RL-06/13 N RL-06/13 Cochabamba 5 de Agosto de
Métodos para la cuantificación de nitrógeno y proteína
 Practica 5 Métodos para la cuantificación de nitrógeno y proteína Antecedentes Para la determinación de proteínas en muestras de alimentos se cuenta con una gran variedad de métodos, basados en diferentes
Practica 5 Métodos para la cuantificación de nitrógeno y proteína Antecedentes Para la determinación de proteínas en muestras de alimentos se cuenta con una gran variedad de métodos, basados en diferentes
MANEJO DE INSTRUMENTAL DE LABORATORIO. ESCUELA DE TECNOLOGIA MEDICA CURSO Bioquímica aplicada T.M Alejandra Espinosa
 MANEJO DE INSTRUMENTAL DE LABORATORIO ESCUELA DE TECNOLOGIA MEDICA CURSO Bioquímica aplicada T.M Alejandra Espinosa BALANZAS ANALITICAS Instrumento para pesar cuya capacidad va desde 1 gr hasta algunos
MANEJO DE INSTRUMENTAL DE LABORATORIO ESCUELA DE TECNOLOGIA MEDICA CURSO Bioquímica aplicada T.M Alejandra Espinosa BALANZAS ANALITICAS Instrumento para pesar cuya capacidad va desde 1 gr hasta algunos
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO
 PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
TRABAJO PRÁCTICO N 0 3 TERMOQUÍMICA
 TRABAJO PRÁCTICO N 0 3 TERMOQUÍMICA OBJETIVOS Determinación de la variación de entalpía asociada a procesos químicos. Aplicación de conceptos termodinámicos: temperatura, calor, entalpía. Verificación
TRABAJO PRÁCTICO N 0 3 TERMOQUÍMICA OBJETIVOS Determinación de la variación de entalpía asociada a procesos químicos. Aplicación de conceptos termodinámicos: temperatura, calor, entalpía. Verificación
Método de ensayo de cementos. Determinación del tiempo de fraguado y de la estabilidad de volumen
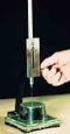 González,E.yAlloza,A.M. Método de ensayo de cementos. Determinación del tiempo de fraguado y de la estabilidad de volumen FUNDAMENTO La pasta de cemento de consistencia normal tiene una resistencia especificada
González,E.yAlloza,A.M. Método de ensayo de cementos. Determinación del tiempo de fraguado y de la estabilidad de volumen FUNDAMENTO La pasta de cemento de consistencia normal tiene una resistencia especificada
Bowie & Dick. Paquetes de prueba de
 Paquetes de prueba de Bowie & Dick Bowie & Dick Test Pack BD125X BD125X/2 BD125X/3 BD125X16 BD125X16/2 BD125X16/3 El Paquete de Prueba de Bowie & Dick fue diseñado para controlar la remoción de aire y
Paquetes de prueba de Bowie & Dick Bowie & Dick Test Pack BD125X BD125X/2 BD125X/3 BD125X16 BD125X16/2 BD125X16/3 El Paquete de Prueba de Bowie & Dick fue diseñado para controlar la remoción de aire y
Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia
 Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia LABORATORIO NACIONAL DE BACTERIOLOGIA DIAGNOSTICO DE LABORATORIO EN LA VIGILANCIA DE LEPTOSPIROSIS EN LA RED NACIONAL DE LABORATORIOS
Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia LABORATORIO NACIONAL DE BACTERIOLOGIA DIAGNOSTICO DE LABORATORIO EN LA VIGILANCIA DE LEPTOSPIROSIS EN LA RED NACIONAL DE LABORATORIOS
Diploma la Química desde la perspectiva de la Química Verde. Guía. de Laboratorio XI Cinética y Química Verde
 Diploma Enseñanza de la Química desde la perspectiva de la Química Verde Guía de Laboratorio XI Cinética y Química Verde Santiago, 2016 Tabla de contenidos Parte I. Trabajo Práctico 1. Objetivos de la
Diploma Enseñanza de la Química desde la perspectiva de la Química Verde Guía de Laboratorio XI Cinética y Química Verde Santiago, 2016 Tabla de contenidos Parte I. Trabajo Práctico 1. Objetivos de la
Indice. PN/L/E/004/00 Página 1 de 7 Rev.: 0 Fecha de Edición: FARMACIA FUNCIONAMIENTO Y MANTENIMIENTO DEL BAÑO TERMOSTÁTICO (BAÑO MARÍA)
 FARMACIA EQUIPOS FUNCIONAMIENTO Y MANTENIMIENTO DEL BAÑO TERMOSTÁTICO (BAÑO MARÍA) Página 1 de 7 Rev.: 0 Fecha de Edición: Procedimientos relacionados: FUNCIONAMIENTO Y MANTENIMIENTO DEL BAÑO TERMOSTÁTICO
FARMACIA EQUIPOS FUNCIONAMIENTO Y MANTENIMIENTO DEL BAÑO TERMOSTÁTICO (BAÑO MARÍA) Página 1 de 7 Rev.: 0 Fecha de Edición: Procedimientos relacionados: FUNCIONAMIENTO Y MANTENIMIENTO DEL BAÑO TERMOSTÁTICO
Procedimiento específico: PEC01 REALIZACIÓN DEL BAÑO DEL "PUNTO DEL HIELO" Copia No Controlada. Instituto Nacional de Tecnología Industrial
 Instituto Nacional de Tecnología Industrial Centro de Desarrollo e Investigación en Física y Metrología Procedimiento específico: PEC01 REALIZACIÓN DEL BAÑO DEL "PUNTO DEL HIELO" Revisión: Abril 2015 Este
Instituto Nacional de Tecnología Industrial Centro de Desarrollo e Investigación en Física y Metrología Procedimiento específico: PEC01 REALIZACIÓN DEL BAÑO DEL "PUNTO DEL HIELO" Revisión: Abril 2015 Este
Sistema Integrado de Gestión RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS PROGRAMAS DE DEPORTE Y FISIOTERAPIA GUIA PRÁCTICA N 6
 Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
PRÁCTICA 1 HERRAMIENTAS Y OPERACIONES BÁSICAS EN EL LABORATORIO BIOANALÍTICO
 PRÁCTICA 1 HERRAMIENTAS Y OPERACIONES BÁSICAS EN EL LABORATORIO BIOANALÍTICO INTRODUCCIÓN Todos los instrumentos de medida que se utilizan en el laboratorio tienen algún tipo de escala para medir una magnitud,
PRÁCTICA 1 HERRAMIENTAS Y OPERACIONES BÁSICAS EN EL LABORATORIO BIOANALÍTICO INTRODUCCIÓN Todos los instrumentos de medida que se utilizan en el laboratorio tienen algún tipo de escala para medir una magnitud,
Test para partículas subvisibles en soluciones inyectables y parenterales USP<788> EP2.9.19
 Comunicación Técnica Test para partículas subvisibles en soluciones inyectables y parenterales USP EP2.9.19 La contaminación de partículas presente en soluciones inyectables y parenterales consiste
Comunicación Técnica Test para partículas subvisibles en soluciones inyectables y parenterales USP EP2.9.19 La contaminación de partículas presente en soluciones inyectables y parenterales consiste
TÍTULO: Determinación colorimétrica de fenoles en agua por el método de la 4- aminoantipirina
 Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
El impacto de las pruebas rápidas en la promoción, prevención y diagnóstico de la sífilis
 El impacto de las pruebas rápidas en la promoción, prevención y diagnóstico de la sífilis XIII CURSO INTERNACIONAL DE ENFERMEDADES INFECCIOSAS XIV SEMINARIO INTEGRAL DEL SIDA Santiago de Cali Marzo 12
El impacto de las pruebas rápidas en la promoción, prevención y diagnóstico de la sífilis XIII CURSO INTERNACIONAL DE ENFERMEDADES INFECCIOSAS XIV SEMINARIO INTEGRAL DEL SIDA Santiago de Cali Marzo 12
CANTIDAD DE PARTICULAS LIVIANAS EN LOS AGREGADOS PETREOS I.N.V. E
 CANTIDAD DE PARTICULAS LIVIANAS EN LOS AGREGADOS PETREOS I.N.V. E 221 07 1. OBJETO 1.1 Esta norma tiene por objeto establecer el método para determinar el porcentaje de partículas livianas en los agregados
CANTIDAD DE PARTICULAS LIVIANAS EN LOS AGREGADOS PETREOS I.N.V. E 221 07 1. OBJETO 1.1 Esta norma tiene por objeto establecer el método para determinar el porcentaje de partículas livianas en los agregados
INSTRUCTIVO TRANSPORTE DE MATERIAL SUCIO O CONTAMINADO
 1. OBJETIVO: Establecer las orientaciones metodológicas para el manejo correcto del material contaminado en los servicios clínicos con el objetivo de evitar la diseminación de microrganismos en el Hospital
1. OBJETIVO: Establecer las orientaciones metodológicas para el manejo correcto del material contaminado en los servicios clínicos con el objetivo de evitar la diseminación de microrganismos en el Hospital
DETERMINACION DE CAFEÍNA EN TE, CAFÉ Y YERBA MATE Basado en Método AOAC Modificado
 ME-711.02-008 Página 1 de 5 1. OBJETIVO Determinar el contenido de cafeína en fruitivos como té, café o yerba mate por método Bailey y Andrews. 2. CAMPO DE APLICACIÓN Y ALCANCE El método es aplicable a
ME-711.02-008 Página 1 de 5 1. OBJETIVO Determinar el contenido de cafeína en fruitivos como té, café o yerba mate por método Bailey y Andrews. 2. CAMPO DE APLICACIÓN Y ALCANCE El método es aplicable a
Módulo 4. Cadena de frío y gestión segura de residuos en el marco del cambio/switch. Fase Final. para la. Erradicación de.
 Fase Final para la Erradicación de la Poliomielitis -Argentina- Módulo 4 Cadena de frío y gestión segura de residuos en el marco del cambio/switch Curso Auto administrado En los anteriores módulos conocimos
Fase Final para la Erradicación de la Poliomielitis -Argentina- Módulo 4 Cadena de frío y gestión segura de residuos en el marco del cambio/switch Curso Auto administrado En los anteriores módulos conocimos
Termoquímica Calor de Neutralización
 LABORATORIO DE FISICOQUÍMICA QMC-313 Termoquímica Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 23/05/2014 Página 2 de 6 Termoquímica Tabla de contenido 1. FUNDAMENTO... 3 2. INSTRUMENTOS
LABORATORIO DE FISICOQUÍMICA QMC-313 Termoquímica Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 23/05/2014 Página 2 de 6 Termoquímica Tabla de contenido 1. FUNDAMENTO... 3 2. INSTRUMENTOS
Patología Médica Facultad de Medicina de Granada. Prof. Juan Jiménez Alonso Curso académico
 TOXOPLASMOSIS Patología Médica Facultad de Medicina de Granada. Prof. Juan Jiménez Alonso Curso académico 2002-2003 TOXOPLASMOSIS * Infección producida por T. Gondii, que es un protozoo intracelular que
TOXOPLASMOSIS Patología Médica Facultad de Medicina de Granada. Prof. Juan Jiménez Alonso Curso académico 2002-2003 TOXOPLASMOSIS * Infección producida por T. Gondii, que es un protozoo intracelular que
ELISA IgM PARA DIAGNOSTICO DE LEPTOSPIRA
 Página 1 de 9 ELISA IgM PARA DIAGNOSTICO DE LEPTOSPIRA Elaborado por: CNSP Blgo. Manuel Céspedes Zambrano Revisado por: CNSP TM. Julia I. Espinoza Soto CNSP MV Gladys Malásquez Mendoza Aprobado por: RD
Página 1 de 9 ELISA IgM PARA DIAGNOSTICO DE LEPTOSPIRA Elaborado por: CNSP Blgo. Manuel Céspedes Zambrano Revisado por: CNSP TM. Julia I. Espinoza Soto CNSP MV Gladys Malásquez Mendoza Aprobado por: RD
6.6. Precauciones especiales de eliminación y otras manipulaciones Instrucciones para el Sistema de Tres Agujas
 6.6. Precauciones especiales de eliminación y otras manipulaciones Instrucciones para el Sistema de Tres Agujas RISPERDAL CONSTA microesferas de liberación prolongada contenido en el vial sólo se debe
6.6. Precauciones especiales de eliminación y otras manipulaciones Instrucciones para el Sistema de Tres Agujas RISPERDAL CONSTA microesferas de liberación prolongada contenido en el vial sólo se debe
MMP. MÉTODOS DE MUESTREO Y PRUEBA DE MATERIALES
 LIBRO: PARTE: TÍTULO: CAPÍTULO: MMP. MÉTODOS DE MUESTREO Y PRUEBA DE MATERIALES 4. MATERIALES PARA PAVIMENTOS 04. Materiales Pétreos para Mezclas Asfálticas 014. Azul de Metileno de Materiales Pétreos
LIBRO: PARTE: TÍTULO: CAPÍTULO: MMP. MÉTODOS DE MUESTREO Y PRUEBA DE MATERIALES 4. MATERIALES PARA PAVIMENTOS 04. Materiales Pétreos para Mezclas Asfálticas 014. Azul de Metileno de Materiales Pétreos
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS
 PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
Servicio de calibraciones en planta
 Testo Argentina S.A. Servicio de calibraciones en planta Estimado Cliente: Testo Argentina S.A. se ha propuesto ser no solo un proveedor de instrumentos de primera calidad, sino también su socio en la
Testo Argentina S.A. Servicio de calibraciones en planta Estimado Cliente: Testo Argentina S.A. se ha propuesto ser no solo un proveedor de instrumentos de primera calidad, sino también su socio en la
El Laboratorio en la Vigilancia de Influenza
 El Laboratorio en la Vigilancia de Influenza QBP MANUEL ARROYO ROJAS Laboratorio de Virus Respiratorios del TIPOS DE MUESTRAS Exudado Faríngeo Exudado Nasofaríngeo Aspirado Bronqueoalveolar Suero (pareados)
El Laboratorio en la Vigilancia de Influenza QBP MANUEL ARROYO ROJAS Laboratorio de Virus Respiratorios del TIPOS DE MUESTRAS Exudado Faríngeo Exudado Nasofaríngeo Aspirado Bronqueoalveolar Suero (pareados)
NycoCard CRP Single Test
 NycoCard CRP Single Test ES DESCRIPCION DEL PRODUCTO Aplicaciones NycoCard CRP Single Test es un test de diagnóstico in vitro para medir de una forma rápida la proteína C reactiva (CRP) en la sangre humana.
NycoCard CRP Single Test ES DESCRIPCION DEL PRODUCTO Aplicaciones NycoCard CRP Single Test es un test de diagnóstico in vitro para medir de una forma rápida la proteína C reactiva (CRP) en la sangre humana.
FICHA TÉCNICA RESINA ACRÍLICA AUTOPOLIMERIZABLE VERACRIL, OPTI-CRYL DPFTPT-020
 RSINA ACRÍLICA AUTOPOLIMRIZABL VRACRIL, OPTI-CRYL 1 GNRALIDADS DL PRODUCTO Los polímeros de metacrilato han tenido gran popularidad en la odontología porque se procesan con facilidad utilizando técnicas
RSINA ACRÍLICA AUTOPOLIMRIZABL VRACRIL, OPTI-CRYL 1 GNRALIDADS DL PRODUCTO Los polímeros de metacrilato han tenido gran popularidad en la odontología porque se procesan con facilidad utilizando técnicas
Práctica 3. Solubilidad
 PREGUNTS RESPONDER L FINL DE L PRÁTI Práctica 3. Solubilidad Revisaron: M. en. Martha Magdalena Flores Leonar Dr. Víctor Manuel Ugalde Saldívar QF. Fabiola González Olguín La concentración es una propiedad
PREGUNTS RESPONDER L FINL DE L PRÁTI Práctica 3. Solubilidad Revisaron: M. en. Martha Magdalena Flores Leonar Dr. Víctor Manuel Ugalde Saldívar QF. Fabiola González Olguín La concentración es una propiedad
UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE ARECIBO DEPARTAMENTO DE CIENCIAS Y TECNOLOGÍA BIOL 3405: LABORATORIO DE INMUNOLOGÍA
 UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE ARECIBO DEPARTAMENTO DE CIENCIAS Y TECNOLOGÍA BIOL 3405: LABORATORIO DE INMUNOLOGÍA I. TÍTULO Dilución II. OBJETIVOS Repasar el concepto de dilución
UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE ARECIBO DEPARTAMENTO DE CIENCIAS Y TECNOLOGÍA BIOL 3405: LABORATORIO DE INMUNOLOGÍA I. TÍTULO Dilución II. OBJETIVOS Repasar el concepto de dilución
PRECAUCIONES ESTANDARES DE BIOSEGURIDAD, ALMACENAMIENTO Y ELIMINACIÓN DE SUSTANCIAS PELIGROSAS
 ELABORADO POR ULTIMA REVISÓN APROBADO POR NOMBRE DRA PAULINA PEÑALOZA TM FABIOLA NUÑEZ DRA. FANCY GAETE TM JANNETTE AMARO TM ANGIE CALFUMAN TM RAÚL JARA TM FABIOLA NUÑEZ DR JULIO MONTT VIDAL CARGO SUBJEFE
ELABORADO POR ULTIMA REVISÓN APROBADO POR NOMBRE DRA PAULINA PEÑALOZA TM FABIOLA NUÑEZ DRA. FANCY GAETE TM JANNETTE AMARO TM ANGIE CALFUMAN TM RAÚL JARA TM FABIOLA NUÑEZ DR JULIO MONTT VIDAL CARGO SUBJEFE
CALIBRACION DEL MATERIAL VOLUMÊTRICO
 MATERIAL VOLUMÉTRICO CALIBRACION DEL MATERIAL VOLUMÊTRICO El material volumétrico tiene por finalidad la medición exacta de volúmenes y debe ser controlado antes de utilizarlo. Para ello se requiere pesar
MATERIAL VOLUMÉTRICO CALIBRACION DEL MATERIAL VOLUMÊTRICO El material volumétrico tiene por finalidad la medición exacta de volúmenes y debe ser controlado antes de utilizarlo. Para ello se requiere pesar
1- MATERIAL NECESARIO:
 1- MATERIAL NECESARIO: - Calador sonda con celdas. - Calador para bolsones - Caladores de bolsas - Bolsas plásticas para muestras con cierre hermético o bolsas de cartón con interior parafinado. - Catre.
1- MATERIAL NECESARIO: - Calador sonda con celdas. - Calador para bolsones - Caladores de bolsas - Bolsas plásticas para muestras con cierre hermético o bolsas de cartón con interior parafinado. - Catre.
Reglamento sobre RTE
 Directiva 10.240.4 del FSIS Anexo 5 Reglamento sobre RTE 9 CFR 430.1, Definiciones. Agente antimicrobiano. Una sustancia incluida o añadida a un producto RTE que tiene el efecto de reducir o eliminar un
Directiva 10.240.4 del FSIS Anexo 5 Reglamento sobre RTE 9 CFR 430.1, Definiciones. Agente antimicrobiano. Una sustancia incluida o añadida a un producto RTE que tiene el efecto de reducir o eliminar un
MANUAL DE PRÁCTICAS DE LABORATORIO
 MANUAL DE PRÁCTICAS DE LABORATORIO IBT QUÍMICA ORGÁNICA FICHA TECNICA FICHA TÉCNICA QUIMICA ORGÁNICA Fecha: 12 Abril 2012 Nombre del catedrático: Edith Ponce Recinos Nombre de la práctica: Identificación
MANUAL DE PRÁCTICAS DE LABORATORIO IBT QUÍMICA ORGÁNICA FICHA TECNICA FICHA TÉCNICA QUIMICA ORGÁNICA Fecha: 12 Abril 2012 Nombre del catedrático: Edith Ponce Recinos Nombre de la práctica: Identificación
GUÍA PARA EL MANEJO DE CENTRIFUGAS DE PIE
 GUÍA PARA EL MANEJO DE CENTRIFUGAS DE PIE GICUV Guía para el Manejo de Centrifugas de Pie 1 Oficina de Planeación y Desarrollo Institucional Prof. Carlos Hernán González Campo, Representante de la Dirección
GUÍA PARA EL MANEJO DE CENTRIFUGAS DE PIE GICUV Guía para el Manejo de Centrifugas de Pie 1 Oficina de Planeación y Desarrollo Institucional Prof. Carlos Hernán González Campo, Representante de la Dirección
ILUSTRE CONSEJO GENERAL DE COLEGIOS DE DENTISTAS DE ESPAÑA
 2010 ILUSTRE CONSEJO GENERAL DE COLEGIOS DE DENTISTAS DE ESPAÑA Qué es un accidente biológico (AB) Cuales son los riesgos de transmisión? Para el VHB (hepatitis B) Para el VHC (hepatitis C) Para el VIH
2010 ILUSTRE CONSEJO GENERAL DE COLEGIOS DE DENTISTAS DE ESPAÑA Qué es un accidente biológico (AB) Cuales son los riesgos de transmisión? Para el VHB (hepatitis B) Para el VHC (hepatitis C) Para el VIH
(7) Las medidas previstas en el presente Reglamento se ajustan al dictamen del Comité del Código Aduanero. Artículo 1
 L 274/6 REGLAMENTO DE EJECUCIÓN (UE) N o 974/2014 DE LA COMISIÓN de 11 de septiembre de 2014 por el que se establece el método refractométrico para la determinación del residuo seco soluble en los productos
L 274/6 REGLAMENTO DE EJECUCIÓN (UE) N o 974/2014 DE LA COMISIÓN de 11 de septiembre de 2014 por el que se establece el método refractométrico para la determinación del residuo seco soluble en los productos
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-312-1978. DETERMINACIÓN DE REDUCTORES DIRECTOS Y TOTALES EN ALIMENTOS. METHOD OF TEST FOR TOTAL AND DIRECT REDUCING SUBSTANCES IN FOOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En
NMX-F-312-1978. DETERMINACIÓN DE REDUCTORES DIRECTOS Y TOTALES EN ALIMENTOS. METHOD OF TEST FOR TOTAL AND DIRECT REDUCING SUBSTANCES IN FOOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
Normas para la Toma de Muestras. Mediante una torunda estéril se procederá de la siguiente forma:
 Anexo 1: Normas para la Toma de Muestras a) Toma de Frotis Faríngeo: - Se realizará un escobillado (frotado) con hisopo preferiblemente de materia sintético (Ej: tipo Dacron), de la faringe, pilares y
Anexo 1: Normas para la Toma de Muestras a) Toma de Frotis Faríngeo: - Se realizará un escobillado (frotado) con hisopo preferiblemente de materia sintético (Ej: tipo Dacron), de la faringe, pilares y
PRÁCTICA 2: CONDUCTIVIDAD TÉRMICA DE LOS METALES
 PRÁCTICA 2: CONDUCTIVIDAD TÉRMICA DE LOS METALES 1. OBJETIVO En esta práctica se determina la conductividad térmica del cobre y del aluminio midiendo el flujo de calor que atraviesa una barra de cada uno
PRÁCTICA 2: CONDUCTIVIDAD TÉRMICA DE LOS METALES 1. OBJETIVO En esta práctica se determina la conductividad térmica del cobre y del aluminio midiendo el flujo de calor que atraviesa una barra de cada uno
Capítulo II: Aspectos clínicos y Organización de los servicios para la atención del dengue
 Capítulo II: Aspectos clínicos y Organización de los servicios para la atención del dengue Tema 3 : Organización de los servicios para la atención del dengue Contenido: La Organización de los servicios
Capítulo II: Aspectos clínicos y Organización de los servicios para la atención del dengue Tema 3 : Organización de los servicios para la atención del dengue Contenido: La Organización de los servicios
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
ScanGel NEUTRAL 86429 48 Tarjetas 86430 1080 Tarjetas
 ScanGel NEUTRAL 86429 48 Tarjetas 86430 1080 Tarjetas GEL NEUTRO Grupo sérico, screening de Ac irregulares, pruebas cruzadas IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad
ScanGel NEUTRAL 86429 48 Tarjetas 86430 1080 Tarjetas GEL NEUTRO Grupo sérico, screening de Ac irregulares, pruebas cruzadas IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad
Universidad de Buenos Aires, Facultad de Medicina. Departamento de Microbiología, Parasitología e Inmunología. Cátedra 1 Microbiología II
 Universidad de Buenos Aires, Facultad de Medicina Departamento de Microbiología, Parasitología e Inmunología Cátedra 1 Microbiología II Teórico 1 Diagnóstico Bacteriológico Cristina Cerquetti ccerquetti@yahoo.com.ar
Universidad de Buenos Aires, Facultad de Medicina Departamento de Microbiología, Parasitología e Inmunología Cátedra 1 Microbiología II Teórico 1 Diagnóstico Bacteriológico Cristina Cerquetti ccerquetti@yahoo.com.ar
