PROBLEMAS Y CUESTIONES Tema 6
|
|
|
- Cristóbal Robles Martin
- hace 7 años
- Vistas:
Transcripción
1 PROBLEMAS Y CUESTIONES Tema 6 *6. Las funciones de espín α y β forman un conjunto completo de funciones de espín, de modo que cualquier función de espín monoelectrónica puede escribirse como una combinación lineal de ellas. Se pide: a) Teniendo en cuenta las expresiones ˆ S xα = hβ y S ˆ xβ = hα, obtener dos funciones propias normalizadas del operador Ŝ x con valores propios h / y h /. b) Teniendo en cuenta que S ˆ α = y hβ i y β h α y = i, obtener dos funciones propias normalizadas del operador Ŝ y con valores propios h / y h /. c) Supóngase que una medida de S z para el electrón da el valor h / ; si inmediatamente después se realiza una medida de S x, Cuáles son las probabilidades de que se obtenga h / y h /? Solución.- a) ϕ = ( α + β ) y ϕ = ( α β ). c) / y /. 6. Sean ψ y ψ las funciones para la partícula en la caja monodimensional de longitud unidad, correspondientes a n = y n =, respectivamente. Si hay un electrón en cada uno de estos orbitales, la parte espacial del triplete y del singlete son, respectivamente, ψ A = ( / ) ( ψψ ψ ψ) y ψ S = ( / ) ( ψψ + ψ ψ). Imagínese que la partícula está dentro de un intervalo dx alrededor de x = 0.5 y la partícula está dentro de un intervalo dx alrededor de x = Mostrar que la función de onda ψ A( x = 0.5, x = 0.55) es muy pequeña, mientras que ψ S ( x = 0.5, x = 0.55) es grande. Justificar el resultado en base al principio de exclusión de Pauli. 6.3 Calcular las integrales: a) Σ ˆ S Σ, b) Σ S ˆ Σ y c) Σ S ˆ Σ Σ = ( α + β ) / Comprueba que Σ es función propia de Dato.- ˆ S xα = hβ y S ˆ xβ = hα Solución.- a) 3h / 4, b) h / y c) 0. Ŝ y de x Ŝ x, pero no lo es de z Ŝ z.. Siendo *6.4 Muestra que si los orbitales espaciales φ y φ son ortogonales, las seis funciones de onda determinantales, φ φ, φ φ, φ φ + φ φ, φ φ φ φ, φ φ y φ φ, son mutuamente ortogonales. 6.5 Hallar los valores propios de Ŝ z para las funciones φ φ y φ φ. Solución.- h y, 0 respectivamente. 6.6 Demuestra que las tres funciones de espín diferentes del estado triplete, αα, ββ y αβ+βα, son linealmente independientes. *6.7 Son ortogonales las funciones s s y s s s s si se cumpliera s s 0? Repite para el caso s s y s s + s s. Solución.- a) No, b) Si.
2 6.8 En unidades atómicas ( h = ) se tiene = + z + z. Para un sistema de N partículas: N ˆ z = z ( i), S = x S i= ˆ N x( i) y N y = i= i= ( i). Comprueba que la función de espín para un sistema de 3 electrones, ψ = ααβ αβα βαα, es función propia de los operadores Ŝ y Ŝ z con valores propios S = / y M S = /. Dato.- S ˆ ˆ + α = S β = 0 y en u.a. Ŝ +β = α, Ŝ α = β. *6.9 Si para un sistema de dos electrones tenemos en cuenta que = + z h + z, donde S ˆ ˆ () ˆ z = Sz + Sz () y S ˆ ˆ () ˆ ± = S± + S± (), comprobar que las funciones de espín simétricas/antisimétricas son funciones propias de Ŝ con valores propios h / 0, respectivamente. 6.0 Demuestra que a pesar de que α y β no son funciones propias de Ŝ x (ni de cambio sí que lo son de S ˆx (y de S ˆy ). y Ŝ y ), en 6. Demuestra que la función de onda, representada por el determinante s s c s + c, para un átomo de tres electrones, es idénticamente nula. s 6. La parte de espín de las funciones de onda para el primer estado excitado del átomo de helio puede ser ψ a = α( ) α(), ψ b = α( ) β () + β () α() y ψ c = β ( ) β (). Puesto que S ˆ z ψ = M S hψ, Cuáles son los valores de M S para las tres funciones de espín anteriores? Solución.-, 0, - (respectivamente). 6.3 Dados las funciones de onda determinantales D = φ φ y D = φ φ, se pide: a) Evaluar la integral D D si los orbitales de base están normalizados pero no son ortogonales (es decir, φ φ = φ φ = Δ 0 ) b) Comprueba que D D D + D 0. Solución.- a) D = D = Δ 6.4 Para un estado excitado del átomo de Litio, se propone la siguiente función de onda: s () s () s (3) ψ = s() s() s(3) 6 3s() 3s() 3s(3) Donde s, s y 3s son funciones propias del hamiltoniano monoelectrónico Li. Se pide: a) Satisface ψ el principio de exclusión de Pauli? b) Escribe el hamiltoniano exacto Ĥ, en unidades atómicas, para el átomo de Litio. c) Es ψ una función propia del hamiltoniano exacto del Litio? d) Si despreciamos los términos de repulsión electrónica en Ĥ (hamiltoniano exacto del átomo de Litio), qué energía, en unidades atómicas, se asocia a la función ψ? e) Qué componente z del espín y del momento angular orbital (en u.a.) debe esperarse para el átomo de Litio en este estado? Solución.- a) Si, c) No, d) -6,5 u.a., e) -3/ u.a. y 0 (respectivamente). +
3 *6.5 Un estado atómico al que corresponde el término 3 D 3 está descrito por la función de onda ψ. Cuál es el valor de a en cada una de las expresiones A ˆ ψ = aψ, cuando el operador  viene dado por cada una de las posibilidades: a) ˆL, b) Ŝ, c) Ĵ d) Lˆ z, e) Ŝ z y f) Ĵ z? Nota.- Asume que es válido el acoplamiento L S. Si hay más de una posibilidad indícalas todas. Solución.- a) 6h, b) h, c) h, d) (,, 0,, ) h, e) (, 0,) h, f) ( 3,,, 0,,, 3) h *6.6 Cuántos estados existen para cada uno de los siguientes términos multipletes: a) 3 D, b) 5 F? Solución.- a) 5, b) 35 *6.7 Para una configuración electrónica determinada, son posibles todos los términos siguientes: P 3/, P / y S 0? Razona la respuesta. *6.8 Qué valores de J pueden surgir en los términos siguientes: S, P, 3 P, 3 D, D, D y 4 D? Cuántos estados (distinguidos por los posibles valores de M J ) pueden darse en cada uno de los casos? 3
4
5
6
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica
 Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Ultima actualización 3 de febrero de 205 Índice. Aproximación
Estados cuánticos para átomos polielectrónicos y espectroscopía atómica Antonio M. Márquez Departamento de Química Física Universidad de Sevilla Ultima actualización 3 de febrero de 205 Índice. Aproximación
MODELOS ATOMICOS. Solución Å; Ultravioleta; 1106 m/s
 MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
El átomo: sus partículas elementales
 El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
Tema 2_3. Átomos Polielectronicos y Sistema Periódico
 Tema 2_3. Átomos Polielectronicos y Sistema Periódico Caso más sencillo: átomo de helio (2 electrones) ĤΨ = EΨ ^ ^ Ĥ = T + V z r 12 x atracción del núcleo (+2e) sobre el electrón 1, a una distancia r 1
Tema 2_3. Átomos Polielectronicos y Sistema Periódico Caso más sencillo: átomo de helio (2 electrones) ĤΨ = EΨ ^ ^ Ĥ = T + V z r 12 x atracción del núcleo (+2e) sobre el electrón 1, a una distancia r 1
Sistemas de Ecuaciones Lineales y Determinantes. Sistemas de Ecuaciones Lineales y Determinantes. Molecular BásicaB. Fisicoquímica. Clase en Titulares
 Sistemas de Ecuaciones Lineales Fisicoquímica Molecular BásicaB Tercer Semestre Carrera de Químico Tema 8 Si tenemos un sistema de n ecuaciones lineales con n incógnitas, podemos resolverlo recurriendo
Sistemas de Ecuaciones Lineales Fisicoquímica Molecular BásicaB Tercer Semestre Carrera de Químico Tema 8 Si tenemos un sistema de n ecuaciones lineales con n incógnitas, podemos resolverlo recurriendo
TEMA 3: ESTRUCTURA MOLECULAR
 TEMA 3: ESTRUCTURA MOLECULAR 3.1 Introducción a la Teoría de Orbitales Moleculares. 3.2 Orbitales Moleculares. Molécula de dihidrógeno. 3.3 Estructura y simetría de los orbitales moleculares. 3.4 Diagrama
TEMA 3: ESTRUCTURA MOLECULAR 3.1 Introducción a la Teoría de Orbitales Moleculares. 3.2 Orbitales Moleculares. Molécula de dihidrógeno. 3.3 Estructura y simetría de los orbitales moleculares. 3.4 Diagrama
Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos
 Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos INTEGRANTES: * Nazate Amuy Ana * Veloz Hidalgo Polet TEMA: Combinación Lineal de Orbitales Atómicos ORBITAL ATÓMICO
Universidad Central del Ecuador Facultad de Ciencias Químicas Fundamentos Espectroscópicos INTEGRANTES: * Nazate Amuy Ana * Veloz Hidalgo Polet TEMA: Combinación Lineal de Orbitales Atómicos ORBITAL ATÓMICO
Guía de Problemas N 0 1 Teoría cinética de los gases y mecánica estadística.
 Guías de Problemas Guía de Problemas N 0 1 Teoría cinética de los gases y mecánica estadística 1 a) Calcular la energía cinética media de traslación de una molécula de gas a 300 o K b)calcular la velocidad
Guías de Problemas Guía de Problemas N 0 1 Teoría cinética de los gases y mecánica estadística 1 a) Calcular la energía cinética media de traslación de una molécula de gas a 300 o K b)calcular la velocidad
PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS.
 PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS. 1. Explique que indica el número cuántico magnético y el número cuántico de espín. Número cuántico magnético:
PROBLEMAS RESUELTOS DE DISTRIBUCIÓN ELECTRONICA EN NIVELES, SUBNIVELES Y ORBITALES ATÓMICOS. 1. Explique que indica el número cuántico magnético y el número cuántico de espín. Número cuántico magnético:
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica. Ing. Sol de María Jiménez González
 Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Introducción al Estado Sólido: El amarre fuerte (tight-binding, en inglés)
 Introducción al Estado Sólido: El amarre fuerte (tight-binding, en inglés) R. Baquero Departamento de Física Cinvestav setiembre 2008 amarre fuerte 1 Por qué estudiamos el método de amarre fuerte? Uno
Introducción al Estado Sólido: El amarre fuerte (tight-binding, en inglés) R. Baquero Departamento de Física Cinvestav setiembre 2008 amarre fuerte 1 Por qué estudiamos el método de amarre fuerte? Uno
Física cuántica I - Colección de ejercicios cortos
 Física cuántica I - Colección de ejercicios cortos http://teorica.fis.ucm.es En las siguientes cuestiones una y sólo una de las cuatro respuestas ofrecidas es correcta. Dígase cuál. Es conveniente hacer
Física cuántica I - Colección de ejercicios cortos http://teorica.fis.ucm.es En las siguientes cuestiones una y sólo una de las cuatro respuestas ofrecidas es correcta. Dígase cuál. Es conveniente hacer
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León.
 Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
Universidad de San Carlos de Guatemala. Facultad de Ingeniería. Escuela de Ciencias. Departamento de Química. Catedrática: Tania de León. Química General. Código: 0348. Primer semestre. Hoja de trabajo.
ESTRUCTURA DEL ÁTOMO - RESUMEN
 TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
3.1. Estructura atómica
 3.1. Estructura atómica Átomo Protones (+) Núcleo Neutrones (sin carga) Corteza Electrones (-) *Z Número atómico = Número de protones. Cuando el átomo está en estado neutro, Z también es equivalente al
3.1. Estructura atómica Átomo Protones (+) Núcleo Neutrones (sin carga) Corteza Electrones (-) *Z Número atómico = Número de protones. Cuando el átomo está en estado neutro, Z también es equivalente al
Ordenando Electrones. De qué forma? 2do Medio > Química Configuración Electrónica. Analiza la siguiente situación:
 do Medio > Química Ordenando Electrones Analiza la siguiente situación: Uno de los mayores logros de la ciencia de la primera mitad del siglo XX se dio en el área de la física, y fue el desarrollo de la
do Medio > Química Ordenando Electrones Analiza la siguiente situación: Uno de los mayores logros de la ciencia de la primera mitad del siglo XX se dio en el área de la física, y fue el desarrollo de la
QUÍMICA LICENCIATURA DE INGENIERÍA EN ENERGÍAS RENOVABLES
 QUÍMICA LICENCIATURA DE INGENIERÍA EN ENERGÍAS RENOVABLES 2013-1 Teoría: Dra. Karina Cuentas Gallegos Martes y jueves 10-12 hrs. Laboratorio: M.C. Mirna Guevara García Jueves 12-14 hrs. Curso de Química
QUÍMICA LICENCIATURA DE INGENIERÍA EN ENERGÍAS RENOVABLES 2013-1 Teoría: Dra. Karina Cuentas Gallegos Martes y jueves 10-12 hrs. Laboratorio: M.C. Mirna Guevara García Jueves 12-14 hrs. Curso de Química
4. Complementos sobre Problemas de Contorno para S.D.O. Lineales. 4. Complementos sobre Problemas de Contorno
 para S.D.O. Lineales 4.1. Problemas de contorno para s.d.o. lineales. Teorema de alternativa 4.1. Problemas de contorno. Teorema de alternativa Fijemos A C 0 ([α, β]; L(R N )) y b C 0 ([α, β]; R N ), dos
para S.D.O. Lineales 4.1. Problemas de contorno para s.d.o. lineales. Teorema de alternativa 4.1. Problemas de contorno. Teorema de alternativa Fijemos A C 0 ([α, β]; L(R N )) y b C 0 ([α, β]; R N ), dos
INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3.
 El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
Capítulo I: Comportamiento Cuántico
 ENUNCIADOS Capítulo I: Comportamiento Cuántico Problema. Hallar la ecuación del movimiento x x(t), de una partícula de masa m, sometida a un potencial Hamilton: V(x) kx, aplicando las ecuaciones de H pi
ENUNCIADOS Capítulo I: Comportamiento Cuántico Problema. Hallar la ecuación del movimiento x x(t), de una partícula de masa m, sometida a un potencial Hamilton: V(x) kx, aplicando las ecuaciones de H pi
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
Apuntes de la asignatura Química Física II (Licenciatura en Química) Tema 7: El átomo de hidrógeno
 Apuntes de la asignatura Química Física II (Licenciatura en Química) Tema 7: El átomo de hidrógeno Ángel José Pérez Jiménez Dept. de Química Física (Univ. Alicante) Índice 1. Partícula sometida a un potencial
Apuntes de la asignatura Química Física II (Licenciatura en Química) Tema 7: El átomo de hidrógeno Ángel José Pérez Jiménez Dept. de Química Física (Univ. Alicante) Índice 1. Partícula sometida a un potencial
Guía de Estudio para 1er Parcial Temas Selectos de Química
 Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
Qué estudiamos en Química Orgánica? ÁTOMOS Y ELECTRONES! ENLACE QUÍMICO
 Química Orgánica I Qué estudiamos en Química Orgánica? Cómo los compuestos orgánicos reaccionan: Rompimiento y formación de enlaces. Enlaces que se forman cuando átomos comparten electrones, enlaces que
Química Orgánica I Qué estudiamos en Química Orgánica? Cómo los compuestos orgánicos reaccionan: Rompimiento y formación de enlaces. Enlaces que se forman cuando átomos comparten electrones, enlaces que
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica
 Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
6 DINAMICA DEL CUERPO RIGIDO
 6 DINAMICA DEL CUERPO RIGIDO 6. CINEMATICA 6.. Configuracion de un Cuerpo Rígido: Angulos de Euler Un cuerpo rígido se puede entender como una distribución continua de materia que se subdivide en pequeños
6 DINAMICA DEL CUERPO RIGIDO 6. CINEMATICA 6.. Configuracion de un Cuerpo Rígido: Angulos de Euler Un cuerpo rígido se puede entender como una distribución continua de materia que se subdivide en pequeños
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio 2, Opción B Reserva 2, Ejercicio 2, Opción A Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2015 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio 2, Opción B Reserva 2, Ejercicio 2, Opción A Reserva 3, Ejercicio
Enlace químico II: geometría molecular e hibridación de orbitales atómicos
 Enlace químico II: geometría e hibridación de orbitales atómicos Capítulo 10 Modelo de la repulsión de los pares de electrones de la capa de valencia (): Predice la geometría de la molécula a partir de
Enlace químico II: geometría e hibridación de orbitales atómicos Capítulo 10 Modelo de la repulsión de los pares de electrones de la capa de valencia (): Predice la geometría de la molécula a partir de
TEMA 3 EL ENLACE COVALENTE
 TEMA 3 EL ENLACE COVALENTE 1. Orbitales atómicos. 2. Teoría de orbitales moleculares (OM). 3. El enlace en la molécula de metano. 4. La molécula de etano. 5. La molécula de etileno. 6. La molécula de acetileno.
TEMA 3 EL ENLACE COVALENTE 1. Orbitales atómicos. 2. Teoría de orbitales moleculares (OM). 3. El enlace en la molécula de metano. 4. La molécula de etano. 5. La molécula de etileno. 6. La molécula de acetileno.
Configuración Electrónica
 Los subniveles se ordenan según el valor de n + l Distribución de los electrones en el átomo Número Orbitales que ocupan relativa A menor valor de n + l, menor energía (más estable) Válido sólo si l 3
Los subniveles se ordenan según el valor de n + l Distribución de los electrones en el átomo Número Orbitales que ocupan relativa A menor valor de n + l, menor energía (más estable) Válido sólo si l 3
Capítulo 2. Fundamentos de la Química Cuántica.
 Capítulo.. Objetivos: Introducción de la naturaleza dual (onda-partícula) de la materia Introducción del concepto de función de onda Familiarizar al alumno con los conceptos más básicos de la mecánica
Capítulo.. Objetivos: Introducción de la naturaleza dual (onda-partícula) de la materia Introducción del concepto de función de onda Familiarizar al alumno con los conceptos más básicos de la mecánica
6.- Cuál es la velocidad de una onda transversal en una cuerda de 2 m de longitud y masa 0,06 kg sometida a una tensión de 500 N?
 FÍSICA 2º DE BACHILLERATO PROBLEMAS DE ONDAS 1.- De las funciones que se presentan a continuación (en las que todas las magnitudes están expresadas en el S.I.), sólo dos pueden representar ecuaciones de
FÍSICA 2º DE BACHILLERATO PROBLEMAS DE ONDAS 1.- De las funciones que se presentan a continuación (en las que todas las magnitudes están expresadas en el S.I.), sólo dos pueden representar ecuaciones de
Estructura de la materia y Sistema Periódico
 Estructura de la materia y Sistema Periódico 1 - Respecto el número cuántico «n» que aparece en el modelo atómico de Bohr indicar de manera razonada cuáles de las siguientes frases son correctas y cuáles
Estructura de la materia y Sistema Periódico 1 - Respecto el número cuántico «n» que aparece en el modelo atómico de Bohr indicar de manera razonada cuáles de las siguientes frases son correctas y cuáles
UNIVERSIDADES DE ANDALUCÍA PRUEBA DE ACCESO A LA UNIVERSIDAD
 Opción A Ejercicio 1.- Sea f : R R definida por f(x) = x 3 +ax 2 +bx+c. a) [1 75 puntos] Halla a,b y c para que la gráfica de f tenga un punto de inflexión de abscisa x = 1 2 y que la recta tangente en
Opción A Ejercicio 1.- Sea f : R R definida por f(x) = x 3 +ax 2 +bx+c. a) [1 75 puntos] Halla a,b y c para que la gráfica de f tenga un punto de inflexión de abscisa x = 1 2 y que la recta tangente en
EXTRUCTURA ATOMICA ACTUAL
 ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
Resolución PRÁCTICO 9
 Resolución PRÁCTICO 9 1- Complete las siguientes ecuaciones nucleares, remplazando las X por los símbolos o números correspondientes (Nota: X toma diferentes números y símbolos en cada una de las situaciones):
Resolución PRÁCTICO 9 1- Complete las siguientes ecuaciones nucleares, remplazando las X por los símbolos o números correspondientes (Nota: X toma diferentes números y símbolos en cada una de las situaciones):
ies menéndez tolosa 1 Escribe la combinación o combinaciones de números cuánticos correspondientes a: a) un electrón 1s y b) un electrón 4f.
 ies menéndez tolosa Escribe la combinación o combinaciones de números cuánticos correspondientes a: a) un electrón s y un electrón 4f. a) Un electrón s Situado en el er nivel n =, como es un orbital s
ies menéndez tolosa Escribe la combinación o combinaciones de números cuánticos correspondientes a: a) un electrón s y un electrón 4f. a) Un electrón s Situado en el er nivel n =, como es un orbital s
Thompson (1898) Rutherford (1911) Bohr (1913) Schrödinger (1926) NUMEROS CUANTICOS
 Thompson (1898) Modelo Atómico Rutherford (1911) Bohr (1913) Propiedad corpuscular de las onda (PLANCK) Propiedad ondulatoria de las partículas (De Broglie) Schrödinger (1926) Números cuánticos 1 NUMEROS
Thompson (1898) Modelo Atómico Rutherford (1911) Bohr (1913) Propiedad corpuscular de las onda (PLANCK) Propiedad ondulatoria de las partículas (De Broglie) Schrödinger (1926) Números cuánticos 1 NUMEROS
Problemas de Química (1ero Grado de Química). Tema 2. ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS
 Problemas de Química (1ero Grado de Química). Tema 2. ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1. Para el isótopo del elemento con Z = 36 y número másico 84 indique: (a) su número de protones; (b) su
Problemas de Química (1ero Grado de Química). Tema 2. ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1. Para el isótopo del elemento con Z = 36 y número másico 84 indique: (a) su número de protones; (b) su
Lección 10 Química Física (Curso )
 LECCIÓN 10. MOLÉCULAS DIATÓMICAS. Objetivos de la lección Diagramas de correlación y configuración electrónica de moléculas diatómicas homonucleares. Términos espectroscópicos moleculares. Estados electrónicos
LECCIÓN 10. MOLÉCULAS DIATÓMICAS. Objetivos de la lección Diagramas de correlación y configuración electrónica de moléculas diatómicas homonucleares. Términos espectroscópicos moleculares. Estados electrónicos
ANALISIS DE FRECUENCIA EN HIDROLOGIA JULIAN DAVID ROJO HERNANDEZ
 ANALISIS DE FRECUENCIA EN HIDROLOGIA JULIAN DAVID ROJO HERNANDEZ Probabilidad - Período de retorno y riesgo La probabilidad de ocurrencia de un fenómeno en hidrología puede citarse de varias Formas: El
ANALISIS DE FRECUENCIA EN HIDROLOGIA JULIAN DAVID ROJO HERNANDEZ Probabilidad - Período de retorno y riesgo La probabilidad de ocurrencia de un fenómeno en hidrología puede citarse de varias Formas: El
LISTA DE SÍMBOLOS. Capítulo 2 EJEMPLOS Y TEORIA DE LAS VIBRACIONES PARAMÉTRICAS 2.1 Introducción T - Periodo Ω - Frecuencia a- parámetro b- parámetro
 LISTA DE SÍMBOLOS Capítulo 2 EJEMPLOS Y TEORIA DE LAS VIBRACIONES PARAMÉTRICAS 2.1 Introducción T - Periodo Ω - Frecuencia a- parámetro b- parámetro 2.1.1 Rigidez Flexiva que Difiere en dos Ejes x- Desplazamiento
LISTA DE SÍMBOLOS Capítulo 2 EJEMPLOS Y TEORIA DE LAS VIBRACIONES PARAMÉTRICAS 2.1 Introducción T - Periodo Ω - Frecuencia a- parámetro b- parámetro 2.1.1 Rigidez Flexiva que Difiere en dos Ejes x- Desplazamiento
Ejercicios de Física cuántica y nuclear. PAU (PAEG)
 1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
Configuración electrónica y Tabla Periódica
 Configuración electrónica y Tabla Periódica El modelo mecánico-cuántico de los átomos permite responder una de la preguntas centrales de la química: por qué los elementos se comportan como lo hacen? O
Configuración electrónica y Tabla Periódica El modelo mecánico-cuántico de los átomos permite responder una de la preguntas centrales de la química: por qué los elementos se comportan como lo hacen? O
La Ecuación de Schrödinger
 La Ecuación de Schrödinger Dr. Héctor René VEGA CARRILLO Notas del curso de Física Moderna Unidad Académica de Ingeniería Eléctrica Universidad Autónoma de Zacatecas Buzón electrónico: fermineutron@yahoo.com
La Ecuación de Schrödinger Dr. Héctor René VEGA CARRILLO Notas del curso de Física Moderna Unidad Académica de Ingeniería Eléctrica Universidad Autónoma de Zacatecas Buzón electrónico: fermineutron@yahoo.com
Modelo Pregunta 1A a) b) Septiembre Pregunta A1.- a) b) c) d) Junio Pregunta 1A a) b) c) d) Solución. Modelo Pregunta 1B.
 Modelo 2014. Pregunta 1A.- Cuando una muestra de átomos del elemento con Z = 19 se irradia con luz ultravioleta, se produce la emisión de electrones, formándose iones con carga +1. a) Escriba la configuración
Modelo 2014. Pregunta 1A.- Cuando una muestra de átomos del elemento con Z = 19 se irradia con luz ultravioleta, se produce la emisión de electrones, formándose iones con carga +1. a) Escriba la configuración
como el número real que resulta del producto matricial y se nota por:
 Espacio euclídeo 2 2. ESPACIO EUCLÍDEO 2.. PRODUCTO ESCALAR En el espacio vectorial se define el producto escalar de dos vectores y como el número real que resulta del producto matricial y se nota por:,
Espacio euclídeo 2 2. ESPACIO EUCLÍDEO 2.. PRODUCTO ESCALAR En el espacio vectorial se define el producto escalar de dos vectores y como el número real que resulta del producto matricial y se nota por:,
Ejercicios de Ondas Mecánicas y Ondas Electromagnéticas.
 Ejercicios de Ondas Mecánicas y Ondas Electromagnéticas. 1.- Determine la velocidad con que se propagación de una onda a través de una cuerda sometida ala tensión F, como muestra la figura. Para ello considere
Ejercicios de Ondas Mecánicas y Ondas Electromagnéticas. 1.- Determine la velocidad con que se propagación de una onda a través de una cuerda sometida ala tensión F, como muestra la figura. Para ello considere
Ejercicio 3.1. Sea el campo de velocidades de un escurrimiento definido por : v = x 2 yē x + x 2 tē y (3.1)
 Ejercicio 3.1. Sea el campo de velocidades de un escurrimiento definido por : Se pide: v = x yē x + x tē y (3.1) a. A qué tipo de formalismo corresponde este análisis del escurrimiento, lagrangeano o eulereano?
Ejercicio 3.1. Sea el campo de velocidades de un escurrimiento definido por : Se pide: v = x yē x + x tē y (3.1) a. A qué tipo de formalismo corresponde este análisis del escurrimiento, lagrangeano o eulereano?
DIVISIÓN DE CIENCIAS BÁSICAS DEPARTAMENTO DE FÍSICA PROGRAMA DE ASIGNATURA
 CENTRO UNIVERSITARIO DE CIENCIAS EXACTAS E INGENIERÍAS DIVISIÓN DE CIENCIAS BÁSICAS DEPARTAMENTO DE FÍSICA PROGRAMA DE ASIGNATURA NOMBRE DE LA MATERIA FÍSICA MODERNA CLAVE DE MATERIA FS 301 DEPARTAMENTO
CENTRO UNIVERSITARIO DE CIENCIAS EXACTAS E INGENIERÍAS DIVISIÓN DE CIENCIAS BÁSICAS DEPARTAMENTO DE FÍSICA PROGRAMA DE ASIGNATURA NOMBRE DE LA MATERIA FÍSICA MODERNA CLAVE DE MATERIA FS 301 DEPARTAMENTO
CONCEPTOS BÁSICOS DE ESPACIOS VECTORIALES Alumno. Cristina Mª Méndez Suero
 Fundamento Científico del Currículum de Matemáticas en Enseñanza Secundaria CONCEPTOS BÁSICOS DE ESPACIOS VECTORIALES Alumno. Cristina Mª Méndez Suero ESPACIOS VECTORIALES DEFINICIÓN... 1 PROPIEDADES DE
Fundamento Científico del Currículum de Matemáticas en Enseñanza Secundaria CONCEPTOS BÁSICOS DE ESPACIOS VECTORIALES Alumno. Cristina Mª Méndez Suero ESPACIOS VECTORIALES DEFINICIÓN... 1 PROPIEDADES DE
Sistema Periódico de los elementos. 2º Bachillerato
 Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 2, Opción B Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 2, Opción B Reserva 3, Ejercicio
Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro:
 RESPUESTAS BLOQUE III Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro: Tipo de raciación Partículas Carga eléctrica Masa(uma) Alfa α +2 4
RESPUESTAS BLOQUE III Ponte en forma 1.- Realiza las actividades que se te solicitan a continuación: a) Completa el siguiente cuadro: Tipo de raciación Partículas Carga eléctrica Masa(uma) Alfa α +2 4
Modelado de Disolvente
 Seminario Fuerzas Intermoleculares Modelado de Disolvente Presentado por: David Ignacio Ramírez Palma Instituto de Química, Universidad Nacional Autónoma de México Noviembre 2014. 1 Contenido - Concepto
Seminario Fuerzas Intermoleculares Modelado de Disolvente Presentado por: David Ignacio Ramírez Palma Instituto de Química, Universidad Nacional Autónoma de México Noviembre 2014. 1 Contenido - Concepto
Actividad: Cómo son las configuraciones electrónicas?
 Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
Configuración Electrónica
 Configuración Electrónica La configuración electrónica de un átomo indica la forma como están distribuidos los electrones entre los distintos orbitales atómicos. Según el Principio de Exclusión de Pauli,
Configuración Electrónica La configuración electrónica de un átomo indica la forma como están distribuidos los electrones entre los distintos orbitales atómicos. Según el Principio de Exclusión de Pauli,
Enlace químico II: geometría molecular e hibridación de orbitales atómicos
 Enlace químico II: geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Teorías de cómo ocurren
Enlace químico II: geometría molecular e hibridación de orbitales atómicos Capítulo 10 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Teorías de cómo ocurren
PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS.
 PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS. PARTÍCULAS FUNDAMENTALES. CONCEPTOS PREVIOS De acuerdo con lo anterior, en un átomo hay tres partículas fundamentales: protones y neutrones,
PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS. PARTÍCULAS FUNDAMENTALES. CONCEPTOS PREVIOS De acuerdo con lo anterior, en un átomo hay tres partículas fundamentales: protones y neutrones,
Tema 7 CO 2. PCl 5. Los enlaces múltiples se tratan como los sencillos en RPECV 1 enlace doble 1 enlace simple 109,5º.
 Tema 7: El Enlace Químico (III): moléculas poliatómicas 7.1 Geometría molecular: teoría RPEV (AJ3.1-3, P12, W8, 10) 7.2 Orbitales híbridos (AJ3.5-7) 7.3 Orbitales moleculares deslocalizados: compuestos
Tema 7: El Enlace Químico (III): moléculas poliatómicas 7.1 Geometría molecular: teoría RPEV (AJ3.1-3, P12, W8, 10) 7.2 Orbitales híbridos (AJ3.5-7) 7.3 Orbitales moleculares deslocalizados: compuestos
Forman base cuando p 0 y 1.
 1 VECTORES: cuestiones y problemas Preguntas de tipo test 1. (E11). Los vectores u = (p, 0, p), v = (p, p, 1) y w = (0, p, ) forman una base de R : a) Sólo si p = 1 b) Si p 1 c) Ninguna de las anteriores,
1 VECTORES: cuestiones y problemas Preguntas de tipo test 1. (E11). Los vectores u = (p, 0, p), v = (p, p, 1) y w = (0, p, ) forman una base de R : a) Sólo si p = 1 b) Si p 1 c) Ninguna de las anteriores,
Construcción de bases en la suma y la intersección de subespacios (ejemplo)
 Construcción de bases en la suma y la intersección de subespacios (ejemplo) Objetivos Aprender a construir bases en S + S y S S, donde S y S están dados como subespacios generados por ciertos vectores
Construcción de bases en la suma y la intersección de subespacios (ejemplo) Objetivos Aprender a construir bases en S + S y S S, donde S y S están dados como subespacios generados por ciertos vectores
Colegio Internacional Torrequebrada. Departamento de Matemáticas
 Geometría. Problema 1: Calcula la distancia del punto P(1, 1, 1) a la recta Problema 2: Dadas las rectas, se pide: a) Analiza su posición relativa. b) Halla la ecuación general del plano π que contiene
Geometría. Problema 1: Calcula la distancia del punto P(1, 1, 1) a la recta Problema 2: Dadas las rectas, se pide: a) Analiza su posición relativa. b) Halla la ecuación general del plano π que contiene
El método de súper y sub soluciones en el espacio de funciones casi periódicas.
 El método de súper y sub soluciones en el espacio de funciones casi periódicas. Universidad de Buenos Aires - IMAS (CONICET) UMA - Bahía Blanca - 2016 Super y sub soluciones Problema periódico asociado
El método de súper y sub soluciones en el espacio de funciones casi periódicas. Universidad de Buenos Aires - IMAS (CONICET) UMA - Bahía Blanca - 2016 Super y sub soluciones Problema periódico asociado
Guía. Álgebra II. Examen parcial III. Transformaciones lineales. Teoremas los más importantes cuyas demostraciones se pueden incluir en el examen
 Guía. Álgebra II. Examen parcial III. Transformaciones lineales. Teoremas los más importantes cuyas demostraciones se pueden incluir en el examen 1. Teorema de la representación matricial de una transformación
Guía. Álgebra II. Examen parcial III. Transformaciones lineales. Teoremas los más importantes cuyas demostraciones se pueden incluir en el examen 1. Teorema de la representación matricial de una transformación
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio, Opción A Reserva 3, Ejercicio, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 3, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio, Opción A Reserva 3, Ejercicio, Opción
Espacios Vectoriales Asturias: Red de Universidades Virtuales Iberoamericanas 1
 Espacios Vectoriales 201 6Asturias: Red de Universidades Virtuales Iberoamericanas 1 Índice 1 Espacios Vectoriales... 4 1.1 Definición de espacio vectorial... 4 1.2 Definición de subespacio vectorial...
Espacios Vectoriales 201 6Asturias: Red de Universidades Virtuales Iberoamericanas 1 Índice 1 Espacios Vectoriales... 4 1.1 Definición de espacio vectorial... 4 1.2 Definición de subespacio vectorial...
Modelos Colectivos. Introducción.
 Modelos Colectivos. Introducción. El modelo de capas predice que todos los núcleos par -par tienen J P =0 en su estado fundamental. En el caso del 130 Sn sus 50 protones saturan la capa 1g 9/ mientras
Modelos Colectivos. Introducción. El modelo de capas predice que todos los núcleos par -par tienen J P =0 en su estado fundamental. En el caso del 130 Sn sus 50 protones saturan la capa 1g 9/ mientras
Capítulo 1 Vectores. 26 Problemas de selección - página 13 (soluciones en la página 99)
 Capítulo 1 Vectores 26 Problemas de selección - página 13 (soluciones en la página 99) 21 Problemas de desarrollo - página 22 (soluciones en la página 100) 11 1.A PROBLEMAS DE SELECCIÓN Sección 1.A Problemas
Capítulo 1 Vectores 26 Problemas de selección - página 13 (soluciones en la página 99) 21 Problemas de desarrollo - página 22 (soluciones en la página 100) 11 1.A PROBLEMAS DE SELECCIÓN Sección 1.A Problemas
Lección 4 Química Física (Curso )
 Lección 4 Química Física (Curso -) LECCIÓN 4. OSCILADOR ARMÓNICO Y ABSORCIÓN DE RADIACIÓN Objetivos de la Lección El oscilador armónico simple. Osciladores acoplados: Energía de London. Absorción de radiación
Lección 4 Química Física (Curso -) LECCIÓN 4. OSCILADOR ARMÓNICO Y ABSORCIÓN DE RADIACIÓN Objetivos de la Lección El oscilador armónico simple. Osciladores acoplados: Energía de London. Absorción de radiación
Con posterioridad el físico alemán Sommerfeld introdujo en el modelo la posibilidad de órbitas elípticas. Köningsberg, Munich, 1951
 4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
Ejercicios de Matrices, determinantes y sistemas de ecuaciones lineales. Álgebra 2008
 Ejercicios de Matrices, determinantes sistemas de ecuaciones lineales. Álgebra 8 - Dado el sistema de ecuaciones lineales 5 (a) ['5 puntos] Clasifícalo según los valores del parámetro λ. (b) [ punto] Resuélvelo
Ejercicios de Matrices, determinantes sistemas de ecuaciones lineales. Álgebra 8 - Dado el sistema de ecuaciones lineales 5 (a) ['5 puntos] Clasifícalo según los valores del parámetro λ. (b) [ punto] Resuélvelo
Apéndice sobre ecuaciones diferenciales lineales
 Apéndice sobre ecuaciones diferenciales lineales Juan-Miguel Gracia 10 de febrero de 2008 Índice 2 Determinante wronskiano. Wronskiano de f 1 (t), f 2 (t),..., f n (t). Derivada de un determinante de funciones.
Apéndice sobre ecuaciones diferenciales lineales Juan-Miguel Gracia 10 de febrero de 2008 Índice 2 Determinante wronskiano. Wronskiano de f 1 (t), f 2 (t),..., f n (t). Derivada de un determinante de funciones.
Enlaces químicos I: conceptos básicos. Capítulo 9
 Enlaces químicos I: conceptos básicos Capítulo 9 Los electrones de valencia son los últimos electrones de un orbital en un átomo, que son los causantes de los enlaces químicos. Grupo e - configuración
Enlaces químicos I: conceptos básicos Capítulo 9 Los electrones de valencia son los últimos electrones de un orbital en un átomo, que son los causantes de los enlaces químicos. Grupo e - configuración
Física General IV: Óptica
 Facultad de Matemática, Astronomía y Física Universidad Nacional de Córdoba Física General IV: Óptica Práctico de Laboratorio N 1: Ondas en una Cuerda Elástica 1 Objetivo: Estudiar el movimiento oscilatorio
Facultad de Matemática, Astronomía y Física Universidad Nacional de Córdoba Física General IV: Óptica Práctico de Laboratorio N 1: Ondas en una Cuerda Elástica 1 Objetivo: Estudiar el movimiento oscilatorio
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. LA TABLA PERIÓDICA.
 PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. LA TABLA PERIÓDICA. A partir de la posición de los elementos en la tabla periódica formando grupos y períodos podemos deducir la evolución de algunas propiedades
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. LA TABLA PERIÓDICA. A partir de la posición de los elementos en la tabla periódica formando grupos y períodos podemos deducir la evolución de algunas propiedades
ESTRUCTURA DE LA MATERIA QCA 05 ANDALUCÍA
 1.- a) Escriba la configuración electrónica de los elementos A, B y C, cuyos números atómicos son 33, 35 y 37, respectivamente. b) Indique el grupo y el periodo al que pertenecen. c) Razone que elemento
1.- a) Escriba la configuración electrónica de los elementos A, B y C, cuyos números atómicos son 33, 35 y 37, respectivamente. b) Indique el grupo y el periodo al que pertenecen. c) Razone que elemento
Magnetismo. Rubén Pérez. Departamento de Física Teórica de la Materia Condensada, Universidad Autónoma de Madrid, Spain ruben.perez@uam.
 Magnetismo Rubén Pérez Departamento de Física Teórica de la Materia Condensada, Universidad Autónoma de Madrid, Spain ruben.perez@uam.es Física del Estado Sólido II, Tema 3, Curso 2010/2011 Orden magnético:
Magnetismo Rubén Pérez Departamento de Física Teórica de la Materia Condensada, Universidad Autónoma de Madrid, Spain ruben.perez@uam.es Física del Estado Sólido II, Tema 3, Curso 2010/2011 Orden magnético:
MODELOS MOLECULARES Y SUPERFICIES DE ENERGÍA POTENCIAL
 MODELOS MOLECULARES Y SUPERFICIES DE ENERGÍA POTENCIAL 1 La modelación molecular El propósito fundamental de la modelación molecular es elaborar modelos virtuales perceptibles y confiables de las estructuras
MODELOS MOLECULARES Y SUPERFICIES DE ENERGÍA POTENCIAL 1 La modelación molecular El propósito fundamental de la modelación molecular es elaborar modelos virtuales perceptibles y confiables de las estructuras
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS
 PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS MATERIA: Química General I CARRERA: Química Analítica NIVEL: Primero
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS MATERIA: Química General I CARRERA: Química Analítica NIVEL: Primero
Transformaciones lineales
 Semana 8 [1/62] 8 de septiembre de 27 Definiciones básicas Semana 8 [2/62] Definición Transformación lineal U, V dos espacios vectoriales sobre el mismo cuerpo Ã. T : U V es una transformación (o función)
Semana 8 [1/62] 8 de septiembre de 27 Definiciones básicas Semana 8 [2/62] Definición Transformación lineal U, V dos espacios vectoriales sobre el mismo cuerpo Ã. T : U V es una transformación (o función)
4 ; 3. d) 2 y 5 3. a) 2,2 b) c) 2,24 d) 2,236 e) 2,23607
 EL NÚMERO REAL.- LOS NÚMEROS IRRACIONALES. NÚMEROS REALES - Indicar a qué conjuntos ( Ν, Ζ, Q, R ) pertenecen los siguientes números: -2 ; ; -4/ 5; 6/ 4; 4 ; 25 ; Ν ; 6/ 4 Ζ -2 ; 25 Q -4/ 5 ; 6 ; 4 ; 8
EL NÚMERO REAL.- LOS NÚMEROS IRRACIONALES. NÚMEROS REALES - Indicar a qué conjuntos ( Ν, Ζ, Q, R ) pertenecen los siguientes números: -2 ; ; -4/ 5; 6/ 4; 4 ; 25 ; Ν ; 6/ 4 Ζ -2 ; 25 Q -4/ 5 ; 6 ; 4 ; 8
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014 QUÍMICA TEMA 2: LA ESTRUCTURA DEL ÁTOMO Junio, Ejercicio 2, Opción A Reserva 1, Ejercicio 2, Opción A Reserva 2, Ejercicio 3, Opción B Reserva 3, Ejercicio
Incidencia de Anestesia General en Operación Cesárea: Registro de Tres Años. Castillo Alvarado, Frencisco Miguel. CAPÍTULO III
 CAPÍTULO III ESTADÍSTICA DE LOS PORTADORES DE CARGA DEL SEMICONDUCTOR 1. Introducción. Cada material suele presentar varias bandas, tanto de conducción (BC) como de valencia (BV), pero las más importantes
CAPÍTULO III ESTADÍSTICA DE LOS PORTADORES DE CARGA DEL SEMICONDUCTOR 1. Introducción. Cada material suele presentar varias bandas, tanto de conducción (BC) como de valencia (BV), pero las más importantes
Espacios Vectoriales www.math.com.mx
 Espacios Vectoriales Definiciones básicas de Espacios Vectoriales www.math.com.mx José de Jesús Angel Angel jjaa@math.com.mx MathCon c 007-009 Contenido. Espacios Vectoriales.. Idea Básica de Espacio Vectorial.................................
Espacios Vectoriales Definiciones básicas de Espacios Vectoriales www.math.com.mx José de Jesús Angel Angel jjaa@math.com.mx MathCon c 007-009 Contenido. Espacios Vectoriales.. Idea Básica de Espacio Vectorial.................................
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS. Partícula Masa (g) Carga (Coulombs) Carga unitaria. Electrón
 MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
Corteza atómica: Estructura electrónica
 Corteza atómica: Estructura electrónica Aunque los conocimientos actuales sobre la estructura electrónica de los átomos son bastante complejos, las ideas básicas son las siguientes: 1. Existen 7 niveles
Corteza atómica: Estructura electrónica Aunque los conocimientos actuales sobre la estructura electrónica de los átomos son bastante complejos, las ideas básicas son las siguientes: 1. Existen 7 niveles
Metal Cu Al Peso específico 8,9 g/cm 3 2,7 g/cm 3 Peso atómico 64 g/mol 27 g/mol Número de electrones libres 1 e - /átomo 3 e - /átomo
 1. La densidad específica del tungsteno es de 18,8 g/cm 3 y su peso atómico es 184. La concentración de electrones libres es 1,23 x 10 23 /cm 3.Calcular el número de electrones libres por átomo. 2. Dadas
1. La densidad específica del tungsteno es de 18,8 g/cm 3 y su peso atómico es 184. La concentración de electrones libres es 1,23 x 10 23 /cm 3.Calcular el número de electrones libres por átomo. 2. Dadas
ESTADÍSTICA. Población Individuo Muestra Muestreo Valor Dato Variable Cualitativa ordinal nominal. continua
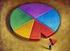 ESTADÍSTICA Población Individuo Muestra Muestreo Valor Dato Variable Cualitativa ordinal nominal Cuantitativa discreta continua DISTRIBUCIÓN DE FRECUENCIAS Frecuencia absoluta: fi Frecuencia relativa:
ESTADÍSTICA Población Individuo Muestra Muestreo Valor Dato Variable Cualitativa ordinal nominal Cuantitativa discreta continua DISTRIBUCIÓN DE FRECUENCIAS Frecuencia absoluta: fi Frecuencia relativa:
EXAMEN FÍSICA 2º BACHILLERATO TEMA 3: ONDAS
 INSTRUCCIONES GENERALES Y VALORACIÓN La prueba consiste de dos opciones, A y B, y el alumno deberá optar por una de las opciones y resolver las tres cuestiones y los dos problemas planteados en ella, sin
INSTRUCCIONES GENERALES Y VALORACIÓN La prueba consiste de dos opciones, A y B, y el alumno deberá optar por una de las opciones y resolver las tres cuestiones y los dos problemas planteados en ella, sin
Conjunto R 3 y operaciones lineales en R 3
 Conjunto R 3 y operaciones lineales en R 3 Objetivos. Definir el conjunto R 3 y operaciones lineales en R 3. Requisitos. Conjunto de los números reales R, propiedades de las operaciones aritméticas en
Conjunto R 3 y operaciones lineales en R 3 Objetivos. Definir el conjunto R 3 y operaciones lineales en R 3. Requisitos. Conjunto de los números reales R, propiedades de las operaciones aritméticas en
Teoría estructural de Kekulé: fórmulas estructurales
 TEMA 1.- Enlaces en las moléculas orgánicas. Enlaces C-, metano. Enlaces C-C, etano. Enlaces C=C, etileno. Enlaces C C, acetileno. Enlaces sencillos carbono heteroátomo. Enlaces múltiles carbono heteroátomo.
TEMA 1.- Enlaces en las moléculas orgánicas. Enlaces C-, metano. Enlaces C-C, etano. Enlaces C=C, etileno. Enlaces C C, acetileno. Enlaces sencillos carbono heteroátomo. Enlaces múltiles carbono heteroátomo.
4.1. Polinomios y teoría de ecuaciones
 CAPÍTULO 4 Polinomios y teoría de ecuaciones 4.1. Polinomios y teoría de ecuaciones Un polinomio real en x, o simplemente polinomio en x es una expresión algebraica de la forma a n x n + a n 1 x n 1 +
CAPÍTULO 4 Polinomios y teoría de ecuaciones 4.1. Polinomios y teoría de ecuaciones Un polinomio real en x, o simplemente polinomio en x es una expresión algebraica de la forma a n x n + a n 1 x n 1 +
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre Fase específica OPCIÓN A
 1 PAU Química. Septiembre 2010. Fase específica OPCIÓN A Cuestión 1A. Considere las sustancias: cloruro de potasio, agua, cloro y sodio. a) Indique el tipo de enlace que presenta cada una de ellas. b)
1 PAU Química. Septiembre 2010. Fase específica OPCIÓN A Cuestión 1A. Considere las sustancias: cloruro de potasio, agua, cloro y sodio. a) Indique el tipo de enlace que presenta cada una de ellas. b)
Comportamiento Electrónico de los Materiales. Tema 1. Fundamentos Físicos de la Estructura Electrónica del Átomo
 Comportamiento Electrónico de los Materiales Tema 1. Fundamentos Físicos de la Estructura Electrónica del Átomo 1.1 Fundamentos de la Estructura Atómica de la Materia1. 1.1.1 Historia: Se tiene conocimiento
Comportamiento Electrónico de los Materiales Tema 1. Fundamentos Físicos de la Estructura Electrónica del Átomo 1.1 Fundamentos de la Estructura Atómica de la Materia1. 1.1.1 Historia: Se tiene conocimiento
GUIA DE APRENDIZAJE QUIMICA 1º MEDIO TEMA : CONFIGURACIÓN ELECTRÓNICA
 Liceo Juan Antonio Ríos Quinta Normal GUIA DE APRENDIZAJE QUIMICA 1º MEDIO TEMA : CONFIGURACIÓN ELECTRÓNICA Unidad temática: Estructura atómica Objetivo General:Comprender el comportamiento de los electrones
Liceo Juan Antonio Ríos Quinta Normal GUIA DE APRENDIZAJE QUIMICA 1º MEDIO TEMA : CONFIGURACIÓN ELECTRÓNICA Unidad temática: Estructura atómica Objetivo General:Comprender el comportamiento de los electrones
FÍSICA y QUÍMICA. Número cuántico Secundario (SUBNIVEL) l. Número cuántico Magnético (ORBITAL, como si fuera una caja) m.
 TEMA 1: ESTRUCTURA DE LA MATERIA. MODELOS ATÓMICOS 1. Modelo Atómico de RUTHERFORD a. Modelo predecesor de Thomson. b. Modelo atómico de Rutherford. c. Virtudes y defectos del Modelo de Rutherford. 2.
TEMA 1: ESTRUCTURA DE LA MATERIA. MODELOS ATÓMICOS 1. Modelo Atómico de RUTHERFORD a. Modelo predecesor de Thomson. b. Modelo atómico de Rutherford. c. Virtudes y defectos del Modelo de Rutherford. 2.


