RECOMENDACIONES PARA LA DETECCIÓN E IDENTIFICACIÓN DE ANTICUERPOS IRREGULARES ERITROCITARIOS
|
|
|
- Lucía Castilla Bustamante
- hace 6 años
- Vistas:
Transcripción
1 Instituto de Salud Pública Ministerio de Salud DOCUMENTOS TÉCNICOS RA EL LABORATORIO CLÍNICO RECOMENDACIONES RA LA DETECCIÓN E IDENTIFICACIÓN DE ANTICUERPOS IRREGULARES ERITROCITARIOS DERTAMENTO LABORATORIO BIOMÉDICO NACIONAL Y DE REFERENCIA DICIEMBRE, 2014
2 AUTOR: TM. Mg. Cs. Andrés Aburto Almonacid. Encargado Área de Inmunohematología. Sección de Hematología e Inmunohematología. Departamento Laboratorio Biomédico Nacional y de Referencia. REVISORES INSTITUTO DE SALUD PÚBLICA DE CHILE: TM. Mg. Mitzy Celis Morales. Jefe Sección Coordinación de Redes de Laboratorios. Subdepartamento Coordinación Externa. Departamento Laboratorio Biomédico Nacional y de Referencia. Dra. Verónica Ramírez Muñoz. Jefe Subdepartamento Coordinación Externa. Departamento Laboratorio Biomédico Nacional y de Referencia. Instituto de Salud Pública de Chile. REVISORES EXTERNOS: TM. Mg. Cs. Leonor Armanet Bernales. Directora Escuela de Tecnología Médica. Universidad de Chile. TM. Mg. Ped. Univ. Hugo Henríquez Bello. Director Docente Escuela de Tecnología Médica. Universidad Mayor. TM. Guillermo Herrera Calderon. TM. Banco de Sangre Hospital Clínico de la Universidad Católica de Chile. Dr. Federico Liendo Palma. Jefe UMT/Banco de Sangre. Complejo Asistencial Barros Luco Trudeau. Dra. María Cristina Martínez Valenzuela. Directora Centro de Sangre Concepción. TM. Ramón Schifferli Salazar. TM. Encargado de Calificación Microbiológica e Inmunohematológica. Centro de Sangre y Tejidos de Valparaíso. TM. Carolina Villalobos Urbina. Jefe de Centro y Encargada de Calidad UMT/Banco de Sangre. Complejo Asistencial Barros Luco Trudeau.
3 RECOMENDACIONES RA LA DETECCIÓN E IDENTIFICACIÓN DE ANTICUERPOS IRREGULARES ERITROCITARIOS RESUMEN Este documento presenta recomendaciones para el procedimiento de detección e identificación de anticuerpos irregulares, y está dirigido a los Centros de Sangre, Unidades de Medicina Transfusional, Bancos de Sangre y Laboratorios Clínicos. Para su elaboración se recogieron las opiniones y sugerencias de los participantes del X Taller Nacional para Centros de Sangre y Unidades de Medicina Transfusional, realizado en mayo de 2013 en el Instituto de Salud Pública de Chile, y ha sido consensuado con el Comité de Expertos PEEC del área de Inmunohematología. Este documento entrega las directrices para la realización de una correcta detección e identificación de anticuerpos irregulares, a fin de contribuir en asegurar la calidad de estos estudios inmunohematológicos en cada institución. OBJETIVO El objetivo de estas recomendaciones es disponer de una metodología para la detección e identificación de anticuerpos irregulares contra antígenos eritrocitarios que contribuya a la obtención de resultados confiables y reproducibles. ALCANCE Estas recomendaciones aplican a los Centros de Sangre, Unidades de Medicina Transfusional, Bancos de Sangre y Laboratorios Clínicos que realizan detección con o sin identificación de anticuerpos irregulares eritrocitarios en la sangre de donantes, pacientes y embarazadas. INTRODUCCIÓN Los anticuerpos irregulares corresponden a aquellos anticuerpos distintos a los anticuerpos naturales del sistema ABO, que pueden aparecer en respuesta a la exposición a un antígeno eritrocitario extraño (transfusión o trasplante), por incompatibilidad materno-fetal o sin un estímulo identificable. En algunos casos, su presencia se asocia a la exposición a antígenos ambientales, bacterianos o virales de características bioquímicas similares a los antígenos eritrocitarios. En nuestro país, los anticuerpos irregulares más frecuentemente encontrados en donantes de sangre son: anti-le a, anti-k y anti-e, mientras que en pacientes son: anti-d, anti-e y anti-k. Todos estos anticuerpos son capaces de provocar hemólisis in vivo y acortamiento en la sobrevida normal de los glóbulos rojos (Anexo 1). La heterogeneidad de los anticuerpos, en cuanto a su tipo, clase de inmunoglobulina, temperatura de reacción, tipo de hemólisis asociada, su capacidad de activar complemento, entre otras características, hacen que la pesquisa e identificación de ellos, deba hacerse de una manera estandarizada y controlada. La detección e identificación de anticuerpos irregulares habitualmente se realiza mediante técnicas de aglutinación en tubo, en columna o en microplaca, con etapas a temperatura ambiente, 37 C y antiglobulina humana. En algunas ocasiones y de acuerdo a condiciones observadas en cada laboratorio, se puede realizar análisis a 4 C frente a la 3
4 sospecha de crioaglutininas. Cuando se detecta la presencia de un aloanticuerpo, se debe determinar su especificidad mediante la identificación y la consiguiente deducción de su significado clínico, empleando un enfoque sistemático descrito en el algoritmo (Anexo 2). DEFINICIONES Y ABREVIACIONES a) Abreviaciones: ACD: Ácido cítrico, citrato, dextrosa. CE: Comunidad Europea CI: Centrifugación Inmediata EDTA: Ácido Etilendiaminotetraacético. FDA: Food and Drug Administration GR: Glóbulos Rojos LISS: Solución de Baja Fuerza Iónica NISS: Solución Salina de fuerza iónica normal : Prueba Autóloga PBS: buffer fosfato salino ph 6.9 a 7.2 SAGH: Suero Antiglobulina Humana TAD: Test Antiglobulina Humana Directa TAI: Test Antiglobulina Humana Indirecta b) Definición de conceptos - Aloanticuerpo: anticuerpo producido en un individuo que está dirigido contra antígenos eritrocitarios que él carece, presentes en otro individuo de su misma especie. - Autoanticuerpo: anticuerpo producido en un individuo que está dirigido contra antígenos que expresan sus propios eritrocitos. - Identificación básica de anticuerpos irregulares: procedimiento del laboratorio de inmunohematología que permite identificar la especificidad de la mayoría de los anticuerpos eritrocitarios de importancia clínica, detectados en el TAI. Involucra el uso de células panel de identificación básico y técnicas con potenciadores de reacción (suero antiglobulina humana poliespecífico y solución LISS), que permiten determinar la especificidad de anticuerpos únicos o algunas mezclas de anticuerpos. DESARROLLO I. DETECCIÓN DE ANTICUERPOS IRREGULARES a) Muestras Suero o plasma obtenido a partir de sangre total sin o con anticoagulante (EDTA, ACD), respectivamente, de acuerdo a las especificaciones del fabricante del método o reactivo que utiliza. El uso de plasma podría impedir la detección de anticuerpos irregulares que se revelan solamente por la presencia de complemento adherido a los eritrocitos. Para estudios automatizados se requiere plasma y en tests manuales es deseable el uso de suero. Las muestras para estudio deben ser almacenadas a 4 C y las pruebas deben ser realizadas en el menor tiempo posible, no excediendo las 72 horas desde su obtención. b) Reactivos - Células Panel para detección de anticuerpos irregulares: sets comerciales de 2 o 3 frascos y en concentración adecuada para cada tipo de técnica. Ej. Tubo: 2-4%, Columna: 0,8-1%. Estás células deben tener certificación de fabricación ISO o estar aprobadas por organismos (FDA, CE), sobre su capacidad de detectar anticuerpos clínicamente significativos, debiendo expresar al menos los siguientes antígenos: D, C, E, c, e, M, N, S, s, P1, Le a, Le b, K, k, Fy a, Fy b, Jk a y Jk b. El laboratorio debiese disponer de reactivos con expresiones homocigotas para los antígenos D, C, E, S, s, Fy a, Fy b, Jk a y Jk c. - En los sets de dos células, uno de los frascos debe ser R 1 /R 1 y el otro R 2 /R 2, en los sets de tres células, el tercero debe ser r/r. - Suero Antiglobulina Humana: tipo poliespecífico, apropiado para cada tipo de técnica (incorporado en los sistemas de aglutinación en columna o en presentaciones para su utilización en tubos). 4
5 - LISS: de acuerdo a la estandarización del reactivo o a las recomendaciones del fabricante (incorporado en los sistemas de aglutinación en columna o en presentaciones para su utilización en tubos). - Suero AB inerte: plasma convertido en suero y calentado a 56 C por 1 hora. - Suero fisiológico tamponado, PBS o solución diluyente recomendada para la técnica utilizada. c) Técnicas Los métodos de detección disponible son: hemaglutinación en tubo, adhesión de eritrocitos en fase sólida (microplaca) y hemaglutinación en columnas. En los dos últimos métodos se dispone de sistemas semiautomatizados y automatizados, a diferencia del método en tubo que corresponde a una técnica manual. d) Procedimiento 1.- Identificar las muestras a estudiar y centrifugarlas de acuerdo al tiempo estandarizado en la centrífuga, para obtener suero o plasma. 2.- Verificar que los reactivos estén vigentes y que tanto reactivos como equipos cumplan con los parámetros definidos en el control de calidad del laboratorio de inmunohematología. Las células panel deben utilizarse a la concentración definida por el fabricante para realizar la técnica. 3.- Para cada muestra a procesar se deben realizar en forma independiente las siguientes reacciones, utilizando volúmenes de suero o plasma y suspensión de glóbulos rojos de acuerdo a la técnica empleada: ver tabla 1. Tabla 1 TUBO, COLUMNA O MICROPLACA SUERO O PLASMA GLÓBULOS ROJOS UTILIDAD Reacción I Muestra en estudio Panel I (R 1 /R 1 ), en concentración adecuada a la técnica usada Detección de anticuerpos irregulares dirigidos hacia antígenos presentes en el Panel I Reacción II Muestra en estudio Panel II (R 2 /R 2 ) en concentración adecuada a la técnica usada Detección de anticuerpos irregulares dirigidos hacia antígenos presentes en el Panel II Reacción III Muestra en estudio Panel III (r/r) en concentración adecuada a la técnica usada Detección de anticuerpos irregulares dirigidos hacia antígenos presentes en el Panel III (opcional) Muestra en estudio Muestra en estudio en concentración adecuada a la técnica usada Determinación de presencia de alo y/o autoanticuerpo 5
6 4.- Mezclar y centrifugar de acuerdo a la calibración para lectura de aglutinación de la centrífuga, o a los tiempos y revoluciones establecidas por el inserto de la técnica utilizada. 5.- Observar en busca de aglutinación y/o hemólisis, de acuerdo a la técnica de lectura automatizada que recomiende el fabricante o tecnica estandarizada en el laboratorio. 6.- Registrar los resultados obtenidos en intensidad de cruces, de acuerdo a la tabla de reacción del Anexo Dependiendo de la técnica utilizada, el procedimiento debe asegurar que se cumplan las distintas etapas de lectura propias de la técnica: - Tubo: Se recomienda realizar en medio de LISS-Coombs por su mayor sensibilidad que el medio NISS. La lectura se puede realizar en tres etapas, permitiendo diferenciar anticuerpos que actúan en salino a temperatura ambiente, en salino a 37 C y con SAGH, permitiendo inferir la clase de inmunoglobulina (IgM y/o IgG) y la temperatura óptima a la cual son activas. - Aglutinación en columna: la lectura se realiza en una etapa, permitiendo detectar principalmente los anticuerpos clínicamente significativos, pero no estableciendo la clase de inmunoglobulina y la temperatura óptima a la cual son activas. También es posible detectar anticuerpos de clase IgM que presentan amplio rango térmico. - Adhesión de eritrocitos en fase sólida: uno de los componentes de la reacción antígeno-anticuerpo es inmovilizado en pocillo (fase sólida) a la que se adiciona antígeno/anticuerpo libre (muestra) y el punto final de la reacción se evidencia por la adición de eritrocitos que pueden ser parte de la reacción antígeno-anticuerpo o se pueden usar como células indicadoras. e) Interpretación Ejemplos de reacciones que pueden observarse en detección de anticuerpos irregulares y su complemento con otras metodologías se muestran en la siguiente tabla: ver tabla 2. Tabla 2 REACCIÓN NEL I REACCIÓN NEL II TAD RESULTADO DE DETECCIÓN DE ANTICUERPOS INTERPRETACIÓN Positivo Aloanticuerpo Positivo Aloanticuerpo Positivo Aloanticuerpo Negativo Ausencia de Anticuerpos /0 Positivo Autoanticuerpo + Aloanticuerpo /0 Positivo Autoanticuerpo/Crioaglutinina 0 = hay reacción de aglutinación + = Aglutinación de cualquier intensidad (4+, 3+, 2+, 1+) 6
7 f) Informe de resultados La denominación recomendada para el informe del resultado de este estudio es: DETECCIÓN DE ANTICUERPOS IRREGULARES: POSITIVO; NEGATIVO (según corresponda al paciente o donante estudiado). En caso de ser positivo, se recomienda registrar las alternativas posibles de especificidades de los anticuerpos detectados de acuerdo al panel utilizado. Se adjunta en Anexo 4, propuesta de registro de resultados. II. IDENTIFICACIÓN BÁSICA DE ANTICUER- POS IRREGULARES a) Muestras La identificación de anticuerpos irregulares debe realizarse con muestras sanguíneas con las mismas características definidas en este documento para la Detección de Anticuerpos Irregulares, en su punto I.a). Para el estudio de mezclas de anticuerpos complejos o múltiples, es fundamental disponer necesariamente de los glóbulos rojos de la muestra para realizar estudios de fenotipificación, autocontrol o TAD. La solicitud de examen que acompaña a la muestra debe incluir al menos la identificación completa del paciente (nombre con dos apellidos), fecha, procedencia, edad, sexo, pertenencia a alguna etnia, historial médico con especial énfasis en historia transfusional reciente, embarazos, patologías asociadas, consumo de algún medicamento, etc., lo que será de utilidad en el proceso de identificación de anticuerpos e interpretación de resultados. b) Reactivos - Células Panel para identificación de anticuerpos irregulares: El panel básico de identificación generalmente presenta entre 8 a 11 frascos de células con diferentes especificidades antigénicas. Existen estos paneles de células en presentaciones de hasta 16 tipos de glóbulos rojos de distintos donantes. La elección del tipo de panel debe ser realizada en base a las características del laboratorio, el tipo de pacientes que atiende y las estadísticas de los casos estudiados en el curso de un año, es deseable que el laboratorio construya tablas con la prevalencia de las especificidades identificadas durante el año. El panel debe permitir que se identifiquen claramente las especificidades de los aloanticuerpos más prevalentes en la población y de mayor importancia clínica (Anexo 1). Debe verificarse y considerarse las siguientes características básicas del panel de identificación: a) Presentar especificidades para los siguientes antígenos: D, C, E, c, e, M, N, S, s, P1, Le a, Le b, K, k, Fy a, Fy b, Jk a y Jk b. b) Poseer al menos dos células panel que presenten y dos células panel que carezcan de los antígenos señalados en el punto anterior. En la tabla de trabajo (Anexo 5) se puede observar que los antígenos e y k no cumplen esta regla, por lo que se debe incorporar al análisis, las células del panel de detección de anticuerpos irregulares, logrando así cumplir esta regla. c) Disponer de células con doble dosis (homocigotas) especialmente de los antígenos Jk a, Jk b, S, s, Fy a, y Fy b, ya que estos antígenos se expresan más débilmente cuando los genes involucrados están en forma heterocigota. d) Poseer células rr (cde/cde) en el panel y que entre ellas expresen los antígenos K, Fy a, Fy b, Jk a, Jk b, M, S, s, de preferencia al estado homocigoto, de manera de poder evidenciar la presencia de ellos junto al anti-d, dada la frecuencia de este anticuerpo. e) Verificar que el inserto de especificación del reactivo y la tabla de trabajo que vienen con el panel, coincidan con el número de lote del reactivo. Este punto es muy importante al momento de querer interpretar los resultados. 7
8 f) Las células panel no deben utilizarse más allá de la fecha de expiración indicada por el fabricante. g) Cada laboratorio de acuerdo a su realidad (frecuencia de anticuerpos irregulares, características étnicas de la población que atiende, entre otras), debe definir al momento de su compra, características especiales del panel a utilizar. - Suero Antiglobulina Humana: Ver punto Ib) de Detección de anticuerpos irregulares. - LISS: de acuerdo a la estandarización del reactivo o a las recomendaciones del fabricante, en caso de ser usado para esta metodología (incorporado en los sistemas de aglutinación en columna o en presentaciones para su utilización en tubos). - Suero fisiológico tamponado, PBS o solución diluyente recomendada para la técnica utilizada. c) Técnicas Existen técnicas manuales, semiautomatizadas y automatizadas, en tubo, columna y microplaca. Tabla 3 d) Procedimiento 1.- Rotular la muestra a investigar y centrifugarla de acuerdo al tiempo estandarizado en la centrífuga para obtener suero o plasma. 2.- Verificar que los reactivos estén vigentes y que tanto reactivos como equipos cumplan con los parámetros definidos en el control de calidad del laboratorio de inmunohematología. Las células panel deben utilizarse a la concentración definida para la técnica a realizar en el inserto del fabricante. 3.- Verificar que la hoja de trabajo del panel de identificación está disponible y su número de lote corresponde al del reactivo que se utilizará. 4.- Para cada muestra a procesar, se deben efectuar tantas reacciones de acuerdo al número de células panel básico utilizado en el laboratorio: ver tabla Mezclar y centrifugar de acuerdo a la calibración de la centrífuga para lectura, o a los tiempos y revoluciones establecidas por el fabricante. 6.- Observar en busca de aglutinación y/o hemólisis, de acuerdo a la técnica de lectura automatizada o manual que recomiende el fabricante. 7.- Registrar los resultados obtenidos en intensidad de cruces, de acuerdo a la tabla de reacción del Anexo 3. TUBO, COLUMNA O MICROPLACA SUERO O PLASMA GLÓBULOS ROJOS UTILIDAD Reacción 1 Muestra en estudio Panel 1 en concentración adecuada a la técnica usada Detectar reacción de acuerdo al fenotipo del Panel 1 Reacción 2 Muestra en estudio Panel 2 en concentración adecuada a la técnica usada Detectar reacción de acuerdo al fenotipo del Panel 2 Reacción 3 Muestra en estudio Panel 3 en concentración adecuada a la técnica usada Detectar reacción de acuerdo al fenotipo del Panel 3 Reacción n* Muestra en estudio Panel n en concentración adecuada a la técnica usada Detectar reacción de acuerdo al fenotipo del Panel n Muestra en estudio Muestra en estudio en concentración adecuada a la técnica usada Determinación de presencia de alo y/o autoanticuerpo *n: número de células del panel utilizadas en la identificación. 8
9 8.- Dependiendo de la técnica definida en sus protocolos, debe asegurarse de cumplir con las distintas etapas de lectura que se requieren: - Tubo: la lectura realizada en las tres etapas, puede permitir diferenciar la detección de anticuerpos que actúan a temperatura ambiente, a 37 C y con SAGH. Además, la lectura y el registro de las intensidades en cruces puede orientar a la especificidad de un solo anticuerpo o a una mezcla de ellos. - Aglutinación en columna: la lectura se puede realizar en una etapa, permitiendo detectar los anticuerpos clínicamente significativos, pero no permite establecer la clase y la temperatura a la cual ellos son activos. El análisis de las intensidades en cruces puede orientar a la especificidad de un solo anticuerpo o a una mezcla de ellos. e.- Interpretación La asignación de la identificación de anticuerpos irregulares, debe realizarse a través de la interpretación del registro de los resultados de las reacciones señaladas en la tabla de trabajo (Anexo 5). Es importante verificar que ella corresponda al lote de panel celular que se haya utilizado. A continuación se señala un ejemplo de identificación básica de anticuerpos irregulares con especificidad anti-s: 1.- Identificar y registrar adecuadamente la intensidad de cruces para cada célula panel, lo cual puede orientar a la especificidad del o los anticuerpos en la muestra. 2.- Proceda a descartar aquellas especificidades de anticuerpos para las cuales el estudio muestra un resultado negativo (descarte por reacciones negativas) con células de expresión homocigota. En la figura se deben analizar las células 1, 3, 8, 10 y 11. La célula 1 permite descartar las especificidades D, C, e, M, s, k, P1, Le b y Jk b (tachado azul); la célula 3 permite descartar las especificidades E, c, N, Le a, Fy b (tachado rojo); la célula 8 no descarta especificidades adicionales; la célula 10 descarta la especificidad Jk a (tachado verde); la célula 11 descarta la especificidad Fy a (tachado negro). Este análisis no permitió excluir las especificidades S y K. Cel Rh MNS Kell P Lewis Duffy Kidd Cel Resultado D C E c e M N S s K k P1 Le a Le b Fy a Fy b Jk a Jk b TA 37C AHG CC 1 R 1 R ü 2 R 1 R R 2 R ü 4 r r r r rr rr R 0 r ü 9 rr rr ü 11 R 1 R ü 9
10 Cel Rh MNS Kell P Lewis Duffy Kidd Cel Resultado D C E c e M N S s K k P1 Le a Le b Fy a Fy b Jk a Jk b TA 37C AHG CC 1 R 1 R ü 2 R 1 R R 2 R ü 4 r r r r rr rr R 0 r ü 9 rr rr ü 11 R 1 R ü 3.- Proceda a comparar el patrón de reacciones (positivas y negativas) de su columna de resultados con las columnas para la especificidad S y K. El patrón de reacción en esta etapa permite descartar la especificidad K, ya que la célula 10 positiva para Kell presenta reacción negativa. 4.- La especificidad probable del anticuerpo es anti-s, lo cual se debe demostrar por la ausencia del antígeno S en el fenotipo de los globulos rojos. 5.- Cuando no es posible identificar los anticuerpos en una muestra a través del panel básico, se deben utilizar técnicas adicionales (fenotipo eritrocitario, panel enzimático, elución-adsorción) o derivar a laboratorio de Referencia para completar estudio. f.- Informe de resultados La denominación recomendada es: IDENTIFICACIÓN DE ANTICUERPOS IRRE- GULARES: anti-d, anti-k, anti-fy b (según corresponda al paciente o donante estudiado). Aspectos a considerar en la identificación de anticuerpos El suero o plasma del paciente debe ser analizado por la misma técnica que se usó en la detección del anticuerpo. La inclusión de glóbulos rojos del paciente puede ser útil en el reconocimiento de anticuerpos dirigidos contra antígenos de alta frecuencia o la presencia de autoanticuerpos. La especificidad del anticuerpo sólo se debe asignar cuando es reactivo con al menos dos células panel que tienen el antígeno y no reactivo con al menos dos células panel que carecen del antígeno. Siempre que sea posible, la presencia de anti-jk a, -Jk b,-s, -s, -Fy a, y Fy b debe excluirse usando células que tengan expresiones homocigotas del antígeno relevante. Se debe utilizar un suero control anti-d débil ( 0,1 UI / ml) para asegurar la eficacia del procedimiento, incluyendo la expresión antigénica sobre células panel. Cuando una especificidad de anticuerpos ha sido identificada, es esencial que la presencia de otros anticuerpos clínicamente significativos 10
11 no sean omitidos. Anticuerpos múltiples sólo se pueden confirmar por la elección de las células panel negativas para la especificidad reconocida, pero positivas para otros antígenos capaces de producir anticuerpos clínicamente significativos. El conocimiento de los fenotipos del paciente puede ayudar en la selección de células para el proceso de identificación y exclusión. Cuando se ha identificado un anticuerpo, los glóbulos rojos del paciente deben ser fenotipados para establecer la ausencia del antígeno (s) correspondiente a la especificidad de los anticuerpos identificados. Se deben utilizar controles apropiados, es decir, antígeno positivo (heterocigoto) y antígeno negativo. III. CONTROL DE CALIDAD a) Control de Calidad Interno: Seguir los procedimientos de control de calidad recomendados por los fabricantes de reactivos y equipos. Cada laboratorio debe realizar control de calidad. Control negativo: utilizar un suero AB inerte estandarizado, como muestra en estudio. Debe dar un resultado negativo. Control positivo: utilizar un suero con anticuerpos irregulares de clase IgG, como muestra en estudio. Debe presentar una intensidad de reacción de 2+ (anti-d débil ( 0,1 UI / ml)) con alguno de los glóbulos rojos utilizados en el test. Este reactivo control debe ser de origen humano y estandarizado por el encargado de calidad del laboratorio. Control de lavado o Células Control Coombs (se usa sólo en técnicas en tubo y cuando el resultado de la detección en la etapa AGH es negativa): corresponde a GR sensibilizados con cantidades bajas de IgG, de manera que ellos son capaces de revelar el suero AGH que queda libre, en aquellos test que muestran un resultado negativo. Este reactivo control debe dar un resultado positivo. b) Control de calidad de cada nuevo lote de reactivos: corresponde a la verificación para asegurar la conformidad con los criterios utilizados. Cualquier reactivo que no cumpla con las especificación requeridas para los test, no se debe utilizar. Tomar al azar uno o dos frascos de reactivos a verificar del nuevo lote como mínimo y examinarlos por inspección visual, en cuanto a corroborar que el volumen y la etiqueta señalan aspectos específicos del reactivo, Nº de lote y fecha de vencimiento con un plazo adecuado a las necesidades del servicio. Además verificar presencia del inserto que especifica características, modo de uso y control de calidad. Evaluar en el laboratorio de Inmunohematología sus características en cuanto a actividad, especificidad, sensibilidad y potencia, según corresponda. Si estos reactivos han sido evaluados por una entidad de referencia, deben solicitarse los resultados y verificar la coherencia con el Nº de lote, marca y fecha de vencimiento del reactivo en uso. Los paneles de identificación deben presentar para los anticuerpos simples por lo menos dos tipos de células positivas y tres negativas, o una positiva y siete negativas para permitir identificar con un valor de p de 0,05. Se recomienda controlar al azar una o dos expresiones antigénicas heterocigotas (fenotipar) de las células de detección e identificación. c) Con cada nueva técnica o tecnología: además de probar los reactivos como se describen anteriormente, es conveniente realizar junto a este nuevo método, si es posible, en paralelo con el método que se estaba usando, de acuerdo al protocolo de verificación implementado en el laboratorio. Incluyendo al menos 10 muestra de sueros con anticuerpos irregulares positivos (almacenadas en serotecas), para evaluar reproducibilidad y concordancia de los resultados. 11
12 Esa semana de prueba puede utilizarse también como etapa de inducción y capacitación del personal que utilizará la nueva técnica o tecnología. En esta etapa es imprescindible la participación del proveedor para la entrega de información, asesoría y capacitación. Esto deberá asegurar que el método es apto para su uso rutinario. Especificaciones de los reactivos Suero Antiglobulina humana - poliespecífico (SAGH) a.- Inspección visual - Etiqueta con el nombre del producto, el número de lote (serie), la fecha de vencimiento, las condiciones de almacenamiento y el nombre del fabricante o su logo. - Inserto del producto debe aportar los mismos detalles que los señalados en la etiqueta, pero explicitando el método recomendado para su uso, los controles de calidad a aplicar, los diluyentes recomendados etc., que pueden ser necesarios, además de cualquier limitación o advertencias en el uso de ese reactivo. Debe incluir también detalles de la composición del reactivo, entregar las advertencias de bioseguridad, y aportar detalles para su uso seguro. Todos los reactivos no-celulares deben estar libres de hemólisis, precipitados, partículas o formación de gel. b.- Sensibilidad: debe presentar hemólisis o aglutinación después de una incubación con suero fresco inerte y compatible, como en una prueba de compatibilidad, usando las siguientes células no sensibilizadas: 2 células A, 2 células B, 2 células O. Se deben obtener reacciones positivas con: Glóbulos rojos RhD positivos (preferiblemente R 1 r) sensibilizadas con un débil anti-d (0,1 UI/ ml o 20 nanogramos/ml) Glóbulos rojos recubiertos con C3b y C3d. Reacciones negativas se deben obtener Con las mismas células, pero no sensibilizadas con anti-d ni complemento. c.- Potencia: Obtener el mismo título o más alto, sin prozona, que el obtenido con una solución de potencia mínima o un AHG con licencia al día (FDA o CE), usando glóbulos rojos RhD positivos recubiertos con un anti-d de 0,1 UI/ml o 20 nanogramos/ml (reacción de 2+ en SAGH). Es útil tener un pequeño panel de anticuerpos débiles (1+ a 2+) de especificidad conocida por ej. anti-fy a además de un anti-d, para utilizar tanto en estudios de especificidad como potencia. Salino LISS ph Conductividad ms/cm Osmolaridad mosmol/kg
13 Solución salina de baja fuerza iónica (LISS) Aspecto; sin turbidez, ni partículas. hemolizar, ni causar aglutinación de las células. El LISS se puede utilizar de dos maneras: suspendiendo los glóbulos rojos de prueba en LISS (1,5-2%) o agregando un volumen igual de la solución de LISS al suero y utilizando glóbulos rojos suspendidos en salino (3%). Las células suspendidas en LISS no se deben conservar más de 24 horas para ser usadas. b) Control de Calidad Externo: Los Centros de Sangre, Unidades de Medicina Transfusional, Bancos de Sangre y Laboratorios Clínicos del país que realizan esta determinación deben participar en algún programa de evaluación externa de la calidad, para que en conjunto con el control de calidad interno, se asegure la calidad de la detección e identificación de anticuerpos irregulares eritrocitarios. REFERENCIAS BIBLIOGRÁFICAS American Association of Blood Banks. AABB Standards for Blood Bank and Transfusion Services, 25th ed., Bethesda, Maryland, Guidelines for the blood transfusion services in the United Kingdom, 7th edition Harmening DM, Modern Blood Banking and Transfusion Practices, 6th ed., Ministerio de Salud de Chile. Orientaciones para Centros de Sangre y Unidades de Medicina Transfusional, MINSAL, Roback JD, editor. AABB Technical Manual, 17th ed., Bethesda, Maryland,
14 ANEXO 1 Características de los anticuerpos irregulares de significancia clínica y sus frecuencias en donantes y pacientes en dos Servicios de Sangre chilenos durante los años Reactividad Asociado a Frecuencias Sistema Sanguíneo Anticuerpo 4 C 22 C 37 C AGH EHRN RHT Donantes 1 n % Pacientes 2 n % MNS Anti-M Anti-N Anti-S Anti-s Anti-U Raro Raro Raro Raro Raro P1PK Anti-P1 Raro Rh Anti-D Anti-C Anti-E Anti-c Anti-e Lutheran Anti-Lu a Anti-Lu b Raro Leve Kell Anti-K Anti-k Anti-Kp a Anti-Kp b Anti-Js a Anti-Js b Lewis Anti-Le a Anti-Le b Raro Duffy Anti-Fy a Anti-Fy b Kidd Anti-Jk a Anti-Jk b Diego Anti-Di a Anti-Di, Yt Anti-Yt a Anti-Yt b Xg Anti-Xg a Scianna Anti-Sc1 Anti-Sc2 Dombrock Anti-Do a Anti-Do b Colton Anti-Co a Anti-Co b TOTAL Fuente: Manual Técnico AABB, 2011 (adaptado) 1 Datos obtenidos sobre un total de donantes del Centro Metropolitano de Sangre y Tejidos, Santiago. 2 Datos obtenidos sobre un total de pacientes del Hospital Guillermo Grant Benavente, Concepción. 14
15 ANEXO 2 Algoritmo para la detección e identificación de anticuerpos irregulares eritrocitarios. 15
16 ANEXO 3 Intensidades de Reacción de acuerdo a las distintas técnicas de aglutinación. INTENSIDAD DE REACCIÓN AGLUTINACIÓN TUBO/MICROPLACA AGLUTINACIÓN EN COLUMNA (GEL Y ESFERAS DE VIDRIO) AGLUTINACIÓN MICROPLACA (FASE SÓLIDA) 4+ Botón único. Fondo claro. Sin células libres. Banda homogénea de aglutinados en la parte superior de la columna. La adherencia es fuerte, cubriendo por completo la monocapa. 3+ Varios aglutinados de gran tamaño. Fondo claro. Sin células libres. Banda superior de aglutinado y desplazamiento en la parte superior de la columna. El grado de adherencia es moderado a fuerte, ligera formación de células en el centro del pocillo. 2+ Muchos aglutinados de mediano tamaño. Fondo claro. Sin células libres. Aglutinados pequeños en la columna y a lo largo de la columna. El grado de adherencia es moderado, botón celular irregular con agujero. 1+ Numerosos aglutinados pequeños. Fondo turbio por GR libres. aglutinados pequeños en la columna. El grado de adherencia es ligero a pequeño, botón celular difuso. +/- Apenas la aglutinación es visible. Fondo turbio por GR libres. Escasos aglutinados de pequeño tamaño en la columna. aplica. 0 Ausencia de aglutinación Banda de GR al fondo de la columna, resto de la columna sin aglutinados. hay adherencia, botón celular central bien definido. 16
17 ANEXO 4 Elementos básicos de un registro recomendado para anotar los resultados de la detección de anticuerpos irregulares eritrocitarios Fecha: Tecnólogo Médico responsable: Identificación paciente/ donante Reacción Panel I (intensidad de cruces) Reacción Panel II (intensidad de cruces) (intensidad de cruces) CI 37ºC AGH CI 37ºC AGH CI 37ºC AGH Resultado Detección de Anticuerpos Interpretación (Características del o los Anticuerpos) Posibles especificidades involucradas Ejemplos de reacciones - Paciente XXXX Negativo Ausencia de anticuerpos Paciente XXXX Positivo Aloanticuerpo Anti-c; Anti-E; anti-k.. Paciente XXXX Positivo Aloanticuerpo Anti-D;.. Paciente XXXX Positivo Autoanticuerpo frío Paciente n. Reactivo Lote N de serie Marca Fecha vencimiento Panel celular Columna (soporte) AGH LISS Otro reactivo 17
18 ANEXO 5 Ejemplo de tabla de trabajo para la identificación de anticuerpos irregulares. Cel Rh MNS Kell P Lewis Duffy Kidd Cel Resultado D C E c e M N S s K k P1 Le a Le b Fy a Fy b Jk a Jk b TA 37C AHG CC 1 R 1 R R 1 R R 2 R r r r r rr rr R 0 r rr rr R 1 R
RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA ABO
 DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA ABO 14 de enero de 2013 AUTOR TM. Andrés Aburto Almonacid. Encargado de Inmunohematología. Sección de Hematología
DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA ABO 14 de enero de 2013 AUTOR TM. Andrés Aburto Almonacid. Encargado de Inmunohematología. Sección de Hematología
RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA ABO
 DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA ABO Enero 2013 AUTOR TM. Andrés Aburto Almonacid. Encargado Área de Inmunohematología. Sección de Hematología
DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA ABO Enero 2013 AUTOR TM. Andrés Aburto Almonacid. Encargado Área de Inmunohematología. Sección de Hematología
RECOMENDACIONES PARA LA REALIZACIÓN DE LAS PRUEBAS CRUZADAS EN MEDICINA TRANSFUSIONAL
 Instituto de Salud Pública Ministerio de Salud DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO RECOMENDACIONES PARA LA REALIZACIÓN DE DEPARTAMENTO LABORATORIO BIOMÉDICO NACIONAL Y DE REFERENCIA 1 DE ABRIL,
Instituto de Salud Pública Ministerio de Salud DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO RECOMENDACIONES PARA LA REALIZACIÓN DE DEPARTAMENTO LABORATORIO BIOMÉDICO NACIONAL Y DE REFERENCIA 1 DE ABRIL,
RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA RhD
 DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA RhD 14 de enero de 2013 AUTOR TM. Andrés Aburto Almonacid. Encargado Área de Inmunohematología. Sección de
DOCUMENTOS TÉCNICOS PARA EL LABORATORIO CLÍNICO RECOMENDACIONES PARA LA CLASIFICACIÓN SANGUÍNEA RhD 14 de enero de 2013 AUTOR TM. Andrés Aburto Almonacid. Encargado Área de Inmunohematología. Sección de
INSTRUCCIÓN TÉCNICA DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Identificación de anticuerpos Página 1 de 7 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería
Identificación de anticuerpos Página 1 de 7 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería
Inmunohematología 2017
 Inmunohematología 2017 REACCIONES DE HEMAGLUTINACIÓN 1-Sensibilización 2-Aglutinación Ag + Ac Ag-Ac FACTORES QUE AFECTAN LA HEMAGLUTINACIÓN Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo
Inmunohematología 2017 REACCIONES DE HEMAGLUTINACIÓN 1-Sensibilización 2-Aglutinación Ag + Ac Ag-Ac FACTORES QUE AFECTAN LA HEMAGLUTINACIÓN Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo
Inmunohematología. Dra. Ana Cecilia Haro
 Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
INSTRUCCIÓN TÉCNICA. Escrutinio de anticuerpos Irregulares o Coombs Indirecto DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Página 1 de 6 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería REVISIÓN FECHA DESCRIPCIÓN
Página 1 de 6 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería REVISIÓN FECHA DESCRIPCIÓN
Sistema de Evaluación:
 Universidad Central Del Este UCE Facultad de Ciencias de la Salud Escuela de Bioanálisis Programa de la asignatura: (BIA-061) Inmunohematología Total de Créditos: 3 Teoría: 2 Practica: 3. Prerrequisitos:
Universidad Central Del Este UCE Facultad de Ciencias de la Salud Escuela de Bioanálisis Programa de la asignatura: (BIA-061) Inmunohematología Total de Créditos: 3 Teoría: 2 Practica: 3. Prerrequisitos:
Albúmina 22 % I.- Introducción. II.- Características. III.- Presentación
 Albúmina 22 % I.- Introducción En 1945 Cameron y Diamond establecieron que ciertos sueros anti-d(anti-rh) podían aglutinar glóbulos rojos Rho positivos en presencia de albúmina de bovino pero no aglutinaban
Albúmina 22 % I.- Introducción En 1945 Cameron y Diamond establecieron que ciertos sueros anti-d(anti-rh) podían aglutinar glóbulos rojos Rho positivos en presencia de albúmina de bovino pero no aglutinaban
INSTRUCTIVO DETERMINACIÓN DE GRUPOS A,B,O Y RH-D
 1. OBJETIVO: Desarrollar la clasificación de Grupo y Rh a los usuarios del Hospital Regional de Arica Dr. Juan Noé Crevani, de acuerdo con los antígenos y anticuerpos presentes en la sangre, esto con el
1. OBJETIVO: Desarrollar la clasificación de Grupo y Rh a los usuarios del Hospital Regional de Arica Dr. Juan Noé Crevani, de acuerdo con los antígenos y anticuerpos presentes en la sangre, esto con el
Cuáles son los resultados del ABO, Rh y detección de anticuerpos? Son los resultados del Coombs Indirecto significativo? Por qué?
 CASO CLINICO NRO.1 Paciente femenina de 32 años ingresada al servicio de obstetricia en trabajo de parto. Antecedentes de 2 partos normales previos en otra ciudad. El servicio de obstetricia solicita estudio
CASO CLINICO NRO.1 Paciente femenina de 32 años ingresada al servicio de obstetricia en trabajo de parto. Antecedentes de 2 partos normales previos en otra ciudad. El servicio de obstetricia solicita estudio
PROGRAMA DE PROFICIENCIA EN INMUNOHEMATOLOGIA INFORME 2013
 PROGRAMA DE PROFICIENCIA EN INMUNOHEMATOLOGIA INFORME 2013 Este programa de control externo permite verificar el desempeño de los procesos en el área de Inmunohematología, evalúa los reactivos utilizados
PROGRAMA DE PROFICIENCIA EN INMUNOHEMATOLOGIA INFORME 2013 Este programa de control externo permite verificar el desempeño de los procesos en el área de Inmunohematología, evalúa los reactivos utilizados
Pontificia Universidad Católica del Ecuador
 Apartado postal 17-01-218 1. DATOS INFORMATIVOS: MATERIA O MÓDULO: CÓDIGO: 1098 BANCO DE SANGRE T-L CARRERA: Licenciatura en Bioanálisis Clínico NIVEL: Sexto No. CRÉDITOS: 3 CRÉDITOS TEORÍA: 2 CRÉDITOS
Apartado postal 17-01-218 1. DATOS INFORMATIVOS: MATERIA O MÓDULO: CÓDIGO: 1098 BANCO DE SANGRE T-L CARRERA: Licenciatura en Bioanálisis Clínico NIVEL: Sexto No. CRÉDITOS: 3 CRÉDITOS TEORÍA: 2 CRÉDITOS
Prueba de Antiglobulina Indirecta
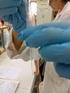 Procedimiento 1 Prueba de Antiglobulina Indirecta Principio La técnica de inmunoglobulina indirecta fue descrita por primera vez en 1945 por Coombs y colaboradores y permite observar aglutinaciones de
Procedimiento 1 Prueba de Antiglobulina Indirecta Principio La técnica de inmunoglobulina indirecta fue descrita por primera vez en 1945 por Coombs y colaboradores y permite observar aglutinaciones de
CONTROL DE CALIDAD INTERNO EN INMUNOHEMATOLOGIA
 CONTROL DE CALIDAD INTERNO EN INMUNOHEMATOLOGIA DEFINICION: LAS TECNICAS OPERACIONALES Y ACTIVIDADES QUE SE USAN PARA CUMPLIR CON LOS REQUISITOS DE CALIDAD (ISO 8402:1996) REACTIVOS EQUIPOS MATERIAL CONTROL
CONTROL DE CALIDAD INTERNO EN INMUNOHEMATOLOGIA DEFINICION: LAS TECNICAS OPERACIONALES Y ACTIVIDADES QUE SE USAN PARA CUMPLIR CON LOS REQUISITOS DE CALIDAD (ISO 8402:1996) REACTIVOS EQUIPOS MATERIAL CONTROL
D VI ce ccd VI.Ee Raro 600 Ag/GR Caucásicos. D VI Ce BARC CcD VI.ee Más frecuente Ag/GR Caucásicos y Japoneses D VI
 D VI tipo 1 D VI tipo 2 D VI tipo 3 D VI tipo 4 D VI tipo 1 D VI tipo 2 D VI tipo 3 D VI tipo 4 D VI tipo 1 D VI ce ccd VI.Ee Raro 600 Ag/GR Caucásicos D VI tipo 2 D VI Ce BARC CcD VI.ee Más frecuente
D VI tipo 1 D VI tipo 2 D VI tipo 3 D VI tipo 4 D VI tipo 1 D VI tipo 2 D VI tipo 3 D VI tipo 4 D VI tipo 1 D VI ce ccd VI.Ee Raro 600 Ag/GR Caucásicos D VI tipo 2 D VI Ce BARC CcD VI.ee Más frecuente
INSTRUCCIÓN TÉCNICA DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Investigación de crioaglutininas Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería
Investigación de crioaglutininas Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de Enfermería
Jueves 13 de septiembre de 2012 DIARIO OFICIAL (Segunda Sección) 91
 Jueves 13 de septiembre de 2012 DIARIO OFICIAL (Segunda Sección) 91 NOTA Aclaratoria a la Primera Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico, publicada el
Jueves 13 de septiembre de 2012 DIARIO OFICIAL (Segunda Sección) 91 NOTA Aclaratoria a la Primera Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico, publicada el
Pruebas de compatibilidad, qué técnica emplear?
 Pruebas de compatibilidad, qué técnica emplear? XIV Jornadas de Medicina Transfusional Dra. Carmen Buesa García Sº Hematología y Hemoterapia Hospital Universitario Central de Asturias Pruebas pretransfusionales
Pruebas de compatibilidad, qué técnica emplear? XIV Jornadas de Medicina Transfusional Dra. Carmen Buesa García Sº Hematología y Hemoterapia Hospital Universitario Central de Asturias Pruebas pretransfusionales
Manual de Inmunohematología
 Calidad y Seguridad Del Paciente Hospital Regional Rancagua HRR Código: SGC-MIH Página: 1 de 59 INDICE / CONTENIDO Contenidos: Página Clasificación ABO y Rh D en tubo 02 Clasificación ABO y Rh D en lámina
Calidad y Seguridad Del Paciente Hospital Regional Rancagua HRR Código: SGC-MIH Página: 1 de 59 INDICE / CONTENIDO Contenidos: Página Clasificación ABO y Rh D en tubo 02 Clasificación ABO y Rh D en lámina
Detección e Identificación anticuerpos irregulares clínicamente significativos. Roxana Regalado R. Médico Asistente Banco de Sangre - INEN
 Detección e Identificación anticuerpos irregulares clínicamente significativos Roxana Regalado R. Médico Asistente Banco de Sangre - INEN Hemoterapia La transfusión de hemocomponentes se considera como
Detección e Identificación anticuerpos irregulares clínicamente significativos Roxana Regalado R. Médico Asistente Banco de Sangre - INEN Hemoterapia La transfusión de hemocomponentes se considera como
EL COMPLEMENTO ideal
 Hematíes reactivo 3% y 5% EL COMPLEMENTO ideal NOT VALID FOR PRINTING! Low resolution PDF file. For high resolution files, please contact Corporate Communications corporatecomms@grifols.com Hematíes reactivo
Hematíes reactivo 3% y 5% EL COMPLEMENTO ideal NOT VALID FOR PRINTING! Low resolution PDF file. For high resolution files, please contact Corporate Communications corporatecomms@grifols.com Hematíes reactivo
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
ScanGel ScanCell P x 10 ml
 ScanGel ScanCell P 86596 3 x 10 ml GLÓBULOS ROJOS TEST DE ORIGEN HUMANO PRETRATADOS CON PAPAÍNA PARA LA DETECCIÓN DE LOS ANTICUERPOS IRREGULARES ANTIERITROCITARIOS IVD Todos los productos fabricados y
ScanGel ScanCell P 86596 3 x 10 ml GLÓBULOS ROJOS TEST DE ORIGEN HUMANO PRETRATADOS CON PAPAÍNA PARA LA DETECCIÓN DE LOS ANTICUERPOS IRREGULARES ANTIERITROCITARIOS IVD Todos los productos fabricados y
NTE AS Centro Producción de Componentes Sanguíneos NORMAS TECNICAS ESPECÍFICAS AUTORIZACION SANITARIA UNIDADES DE PRODUCCION COMPONENTES SANGUÍNEOS
 NORMAS TECNICAS ESPECÍFICAS AUTORIZACION SANITARIA UNIDADES DE PRODUCCION COMPONENTES SANGUÍNEOS I. INTRODUCCIÓN Definición: La Unidad de Procesamiento de Componentes Sanguíneos está constituida por las
NORMAS TECNICAS ESPECÍFICAS AUTORIZACION SANITARIA UNIDADES DE PRODUCCION COMPONENTES SANGUÍNEOS I. INTRODUCCIÓN Definición: La Unidad de Procesamiento de Componentes Sanguíneos está constituida por las
TARJETA ABD/GRUPO INVERSO, MONOCLONAL
 TARJETA ABD/GRUPO INVERSO, MONOCLONAL DiaClon ABO/D + Grupo Inverso NOMBRE DiaClon ABO/D + Grupo Inverso DESCRIPCION La tarjeta DiaClon ABO/D + Reverse Grouping contiene anticuerpos monoclonales anti-a,
TARJETA ABD/GRUPO INVERSO, MONOCLONAL DiaClon ABO/D + Grupo Inverso NOMBRE DiaClon ABO/D + Grupo Inverso DESCRIPCION La tarjeta DiaClon ABO/D + Reverse Grouping contiene anticuerpos monoclonales anti-a,
Avances en Inmunohematología: Normativa y nuevas metodologías
 Avances en Inmunohematología: Normativa y nuevas metodologías XLIII CONGRESO MEXICANO DE PATOLOGIA CLINICA Asociación Mexicana de Medicina Transfusional, A.C. 30 de Octubre a 2 de Noviembre, 2013 Centro
Avances en Inmunohematología: Normativa y nuevas metodologías XLIII CONGRESO MEXICANO DE PATOLOGIA CLINICA Asociación Mexicana de Medicina Transfusional, A.C. 30 de Octubre a 2 de Noviembre, 2013 Centro
Técnicas de aglutinación En estas técnicas se hacen visibles los complejos Ag-Ac por la aglutinación que producen los anticuerpos cuando el Ag forma
 Técnicas de aglutinación En estas técnicas se hacen visibles los complejos Ag-Ac por la aglutinación que producen los anticuerpos cuando el Ag forma parte, o se ha unido artificialmente, a la superficie
Técnicas de aglutinación En estas técnicas se hacen visibles los complejos Ag-Ac por la aglutinación que producen los anticuerpos cuando el Ag forma parte, o se ha unido artificialmente, a la superficie
ScanGel ScanBrom ml
 ScanGel ScanBrom 86445 12 ml BROMELINA PARA PRUEBAS CRUZADAS IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad se hallan bajo un sistema de garantía de calidad desde la recepción
ScanGel ScanBrom 86445 12 ml BROMELINA PARA PRUEBAS CRUZADAS IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad se hallan bajo un sistema de garantía de calidad desde la recepción
PROCEDIMIENTO DE CONDICIONES DE ALMACENAMIENTO Y TRANSPORTE DE COMPONENTES SANGUÍNEOS
 Páginas: 1 de 8 PROCEDIMIENTO DE CONDICIONES DE ALMACENAMIENTO Y TRANSPORTE DE COMPONENTES SANGUÍNEOS Elaborado por: Revisado por: Aprobado por: T.M. Mauricio Gutiérrez Cea Encargado TM. Carlos Figueroa
Páginas: 1 de 8 PROCEDIMIENTO DE CONDICIONES DE ALMACENAMIENTO Y TRANSPORTE DE COMPONENTES SANGUÍNEOS Elaborado por: Revisado por: Aprobado por: T.M. Mauricio Gutiérrez Cea Encargado TM. Carlos Figueroa
11. MÉTODOS PARA LA DETECCIÓN DEL ROTAVIRUS. Actualmente existen diversos métodos en el mercado que pueden utilizarse
 11. MÉTODOS PARA LA DETECCIÓN DEL ROTAVIRUS Actualmente existen diversos métodos en el mercado que pueden utilizarse para el diagnóstico de rotavirus, las cuales pueden realizarse directamente a partir
11. MÉTODOS PARA LA DETECCIÓN DEL ROTAVIRUS Actualmente existen diversos métodos en el mercado que pueden utilizarse para el diagnóstico de rotavirus, las cuales pueden realizarse directamente a partir
Demanda de fenotipos eritrocitarios específicos en paciente politransfundidos: Dificultades y soluciones
 Curso de actualización en Inmunoh. Pediatrica Fundación Hemocentro Bs.As. 16 de octubre de 214 Demanda de fenotipos eritrocitarios específicos en paciente politransfundidos: Dificultades y soluciones Dra.
Curso de actualización en Inmunoh. Pediatrica Fundación Hemocentro Bs.As. 16 de octubre de 214 Demanda de fenotipos eritrocitarios específicos en paciente politransfundidos: Dificultades y soluciones Dra.
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE BIOANÀLISIS
 PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE BIOANÀLISIS 1. DATOS INFORMATIVOS: MATRIA: BANCO DE SANGRE T-L CÓDIGO: 10498 CARRERA: Bioanálisis Clínico NIVEL: Sexto No. CRÉDITOS: 3 CRÉDITOS TEORÍA:
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE BIOANÀLISIS 1. DATOS INFORMATIVOS: MATRIA: BANCO DE SANGRE T-L CÓDIGO: 10498 CARRERA: Bioanálisis Clínico NIVEL: Sexto No. CRÉDITOS: 3 CRÉDITOS TEORÍA:
Antígenos Anticuerpo Aglutinógeno Aglutinina Es la clasificación de la sangre de acuerdo a los antígenos presentes en la membrana de los glóbulos rojo
 Grupos Sanguíneos neos Antígenos Anticuerpo Aglutinógeno Aglutinina Es la clasificación de la sangre de acuerdo a los antígenos presentes en la membrana de los glóbulos rojos y a los anticuerpos presentes
Grupos Sanguíneos neos Antígenos Anticuerpo Aglutinógeno Aglutinina Es la clasificación de la sangre de acuerdo a los antígenos presentes en la membrana de los glóbulos rojos y a los anticuerpos presentes
P08.- DETERMINACIÓN DE LOS GRUPOS SANGUÍNEOS
 P08.- DETERMINACIÓN DE LOS GRUPOS SANGUÍNEOS Objetivos de la práctica Comprender el concepto de grupo sanguíneo y conocer los tipos sanguíneos más importantes. Conocer la importancia de determinar el grupo
P08.- DETERMINACIÓN DE LOS GRUPOS SANGUÍNEOS Objetivos de la práctica Comprender el concepto de grupo sanguíneo y conocer los tipos sanguíneos más importantes. Conocer la importancia de determinar el grupo
Revista Salud Pública y Nutrición Edición Especial 3-2012 23 y 24 de Agosto 2011; Monterrey, N.L., México
 RESPYN Revista Salud Pública y Nutrición Edición Especial 3-2012 23 y 24 de Agosto 2011; Monterrey, N.L., México PRUEBAS Questions?! PRETRANSFUSIONALES Y SU CONTROL DE CALIDAD Pruebas Pre-transfusionales?
RESPYN Revista Salud Pública y Nutrición Edición Especial 3-2012 23 y 24 de Agosto 2011; Monterrey, N.L., México PRUEBAS Questions?! PRETRANSFUSIONALES Y SU CONTROL DE CALIDAD Pruebas Pre-transfusionales?
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE BIOANÀLISIS
 PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE BIOANÀLISIS 1. DATOS INFORMATIVOS: MATRIA: BANCO DE SANGRE T-L CÓDIGO: 10498 CARRERA: Bioanálisis Clínico NIVEL: Sexto No. CRÉDITOS: 3 CRÉDITOS TEORÍA:
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE BIOANÀLISIS 1. DATOS INFORMATIVOS: MATRIA: BANCO DE SANGRE T-L CÓDIGO: 10498 CARRERA: Bioanálisis Clínico NIVEL: Sexto No. CRÉDITOS: 3 CRÉDITOS TEORÍA:
BUENAS PRACTICAS DE LABORATORIO EN EL ANÁLISIS DE NIVELES DE FÁRMACOS Y SUS METABOLITOS EN ESPECÍMENES BIOLÓGICOS
 MINISTERIO DE SANIDAD Y CONSUMO BUENAS PRACTICAS DE LABORATORIO EN EL ANÁLISIS DE NIVELES DE FÁRMACOS Y SUS METABOLITOS EN ESPECÍMENES BIOLÓGICOS DOCUMENTO Nº 5 1ª Versión Noviembre 2001 AGENCIA ESPAÑOLA
MINISTERIO DE SANIDAD Y CONSUMO BUENAS PRACTICAS DE LABORATORIO EN EL ANÁLISIS DE NIVELES DE FÁRMACOS Y SUS METABOLITOS EN ESPECÍMENES BIOLÓGICOS DOCUMENTO Nº 5 1ª Versión Noviembre 2001 AGENCIA ESPAÑOLA
Programa Formativo. Objetivos. Código: Curso: Hematología y Hemoterapia. Duración: 70h.
 Código: 40657 Curso: Hematología y Hemoterapia Modalidad: ONLINE Duración: 70h. Objetivos La sangre es un tejido líquido que circula permanentemente por el sistema vascular y está formado por vasos sanguíneos
Código: 40657 Curso: Hematología y Hemoterapia Modalidad: ONLINE Duración: 70h. Objetivos La sangre es un tejido líquido que circula permanentemente por el sistema vascular y está formado por vasos sanguíneos
PROGRAMA CURSO INMUNOHEMATOLOGIA Y BANCO DE SANGRE 2011
 PROGRAMA CURSO INMUNOHEMATOLOGIA Y BANCO DE SANGRE 2011 DATOS GENERALES: Asignatura: Inmunohematología y Banco de Sangre Carrera : Tecnología Médica Nivel Curricular: 8 semestre (4 año) Escuela, programa
PROGRAMA CURSO INMUNOHEMATOLOGIA Y BANCO DE SANGRE 2011 DATOS GENERALES: Asignatura: Inmunohematología y Banco de Sangre Carrera : Tecnología Médica Nivel Curricular: 8 semestre (4 año) Escuela, programa
La importancia de la historia clínica
 La importancia de la historia clínica Aloinmunización frente al antígeno Lutheran b en una anciana Mariana Ferraro Rosset Servicio de Hematología Hospital del Mar / Barcelona 31 de mayo 2012 SISTEMA LUTHERAN
La importancia de la historia clínica Aloinmunización frente al antígeno Lutheran b en una anciana Mariana Ferraro Rosset Servicio de Hematología Hospital del Mar / Barcelona 31 de mayo 2012 SISTEMA LUTHERAN
Dra. GIOVANA GARCIA Dra. Giovana García
 FUNDAMENTOS DE INMUNOHEMATOLOGÍA Dra. GIOVANA GARCIA Dra. Giovana García INMUNOHEMATOLOGIA Parte de la hematología que estudia los inmunes procesos inmunes relacionados don las células sanguíneas. Los
FUNDAMENTOS DE INMUNOHEMATOLOGÍA Dra. GIOVANA GARCIA Dra. Giovana García INMUNOHEMATOLOGIA Parte de la hematología que estudia los inmunes procesos inmunes relacionados don las células sanguíneas. Los
Antisueros EL COMPLEMENTO ideal
 Antisueros EL COMPLEMENTO ideal NOT VALID FOR PRINTING! Low resolution PDF file. For high resolution files, please contact Corporate Communications corporatecomms@grifols.com Antisueros CUANDO SE NECESITA
Antisueros EL COMPLEMENTO ideal NOT VALID FOR PRINTING! Low resolution PDF file. For high resolution files, please contact Corporate Communications corporatecomms@grifols.com Antisueros CUANDO SE NECESITA
PROCEDIMIENTO DE TRAZABILIDAD UNIDAD DE MEDICINA TRANSFUSIONAL
 UNIDAD DE MEDICINA TRANSFUSIONAL Página: 1 de 19 Introducción y definiciones La trazabilidad es un sistema organizado de registros, que permite ubicar e identificar la sangre y sus componentes en forma
UNIDAD DE MEDICINA TRANSFUSIONAL Página: 1 de 19 Introducción y definiciones La trazabilidad es un sistema organizado de registros, que permite ubicar e identificar la sangre y sus componentes en forma
SISTEMA Rh Q.F.B. LUIS ISMAEL RIOS MONTOYA DIRECTOR
 SISTEMA Rh Q.F.B. LUIS ISMAEL RIOS MONTOYA DIRECTOR HOLA, BUENAS NOCHES SISTEMA Rh Sistema complejo Fué descubierto en 1939 por Levine y Stetson. Son proteínas. SISTEMA Rh En 1940 Landsteiner y Wiener,
SISTEMA Rh Q.F.B. LUIS ISMAEL RIOS MONTOYA DIRECTOR HOLA, BUENAS NOCHES SISTEMA Rh Sistema complejo Fué descubierto en 1939 por Levine y Stetson. Son proteínas. SISTEMA Rh En 1940 Landsteiner y Wiener,
Técnico en Hematología y Hemoterapia. Sanidad, Dietética y Nutrición
 Técnico en Hematología y Hemoterapia Sanidad, Dietética y Nutrición Ficha Técnica Categoría Sanidad, Dietética y Nutrición Referencia 166762-1501 Precio 50.36 Euros Sinopsis La sangre es la especialidad
Técnico en Hematología y Hemoterapia Sanidad, Dietética y Nutrición Ficha Técnica Categoría Sanidad, Dietética y Nutrición Referencia 166762-1501 Precio 50.36 Euros Sinopsis La sangre es la especialidad
José Antonio Paredes Arrascue
 José Antonio Paredes Arrascue Dr. (c), Mg., Lic. en Tecnología Médica Profesor Asociado de la Facultad de Medicina U.N.M.S.M. Tecnólogo Médico del Servicio de Medicina Transfusional H.N.E.R.M. - EsSalud
José Antonio Paredes Arrascue Dr. (c), Mg., Lic. en Tecnología Médica Profesor Asociado de la Facultad de Medicina U.N.M.S.M. Tecnólogo Médico del Servicio de Medicina Transfusional H.N.E.R.M. - EsSalud
PLIEGO DE BASES TÉCNICAS
 PLIEGO DE BASES TÉCNICAS EXPEDIENTE Nº: G/112/20/1/1091/O491/0000/102013 OBJETO: Provisión de reactivos para Tipaje Inmunohematológico en donaciones de sangre en el Centro Vasco de Transfusión y Tejidos
PLIEGO DE BASES TÉCNICAS EXPEDIENTE Nº: G/112/20/1/1091/O491/0000/102013 OBJETO: Provisión de reactivos para Tipaje Inmunohematológico en donaciones de sangre en el Centro Vasco de Transfusión y Tejidos
Anemia Hemolítica Autoinmune Diagnóstico inmunohematológico
 Anemia Hemolítica Autoinmune inmunohematológico Dr. Arturo Pereira S. de Hemoterapia y Hemostasia Introducción Anemia Hemolítica Autoinmune (AHAI) Es la causa más frecuente de anemia hemolítica en el adulto.
Anemia Hemolítica Autoinmune inmunohematológico Dr. Arturo Pereira S. de Hemoterapia y Hemostasia Introducción Anemia Hemolítica Autoinmune (AHAI) Es la causa más frecuente de anemia hemolítica en el adulto.
INSTRUCCIÓN TÉCNICA DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Determinación del antígeno D Débil Du Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de
Determinación del antígeno D Débil Du Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de
CAPACITACIÓN BÁSICA EN HEMOTERAPIA Curso Universitario de pos grado
 CAPACITACIÓN BÁSICA EN HEMOTERAPIA Curso Universitario de pos grado Justificación: La Hemoterapia, en tanto especialidad medica, esta constituida por diferentes procesos articulados entre si. Dichos procesos
CAPACITACIÓN BÁSICA EN HEMOTERAPIA Curso Universitario de pos grado Justificación: La Hemoterapia, en tanto especialidad medica, esta constituida por diferentes procesos articulados entre si. Dichos procesos
Martes 21 de agosto de 2012 DIARIO OFICIAL (Primera Sección) 92
 Martes 21 de agosto de 2012 DIARIO OFICIAL (Primera Sección) 92 PRIMERA Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico. Al margen un sello con el Escudo Nacional,
Martes 21 de agosto de 2012 DIARIO OFICIAL (Primera Sección) 92 PRIMERA Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico. Al margen un sello con el Escudo Nacional,
PRIMERA Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico.
 DOF: 21/08/2012 PRIMERA Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico. Al margen un sello con el Escudo Nacional, que dice: Estados Unidos Mexicanos.- Consejo
DOF: 21/08/2012 PRIMERA Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico. Al margen un sello con el Escudo Nacional, que dice: Estados Unidos Mexicanos.- Consejo
GELES FORMULADOS CON REACTIVOS MONOCLONALES DE ORIGEN MURINO O HUMANO O GEL NEUTRO
 ScanGel ABO Complete/RH/K Duo 86719 2 x 24 tarjetas 86709 2 x 144 tarjetas ScanGel ABO Complete/RH1 Duo y ScanGel Monoclonal RH/K Phenotypes Duo tarjetas GELES FORMULADOS CON REACTIVOS MONOCLONALES DE
ScanGel ABO Complete/RH/K Duo 86719 2 x 24 tarjetas 86709 2 x 144 tarjetas ScanGel ABO Complete/RH1 Duo y ScanGel Monoclonal RH/K Phenotypes Duo tarjetas GELES FORMULADOS CON REACTIVOS MONOCLONALES DE
PROTOCOLO PROGRAMA EVALUACION EXTERNA DEL DESEMPEÑO DIRECTA EN INMUNOHEMATOLOGÍA PARA BANCOS DE SANGRE Y SERVICIOS DE TRANSFUSIÓN PEEDD- IH- 2016
 PROTOCOLO PROGRAMA EVALUACION EXTERNA DEL DESEMPEÑO DIRECTA EN INMUNOHEMATOLOGÍA PARA BANCOS DE SANGRE Y SERVICIOS DE TRANSFUSIÓN PEEDD- IH- 2016 GRUPO RED NACIONAL BANCOS DE SANGRE Y SERVICIOS DE TRANSFUSIÓN
PROTOCOLO PROGRAMA EVALUACION EXTERNA DEL DESEMPEÑO DIRECTA EN INMUNOHEMATOLOGÍA PARA BANCOS DE SANGRE Y SERVICIOS DE TRANSFUSIÓN PEEDD- IH- 2016 GRUPO RED NACIONAL BANCOS DE SANGRE Y SERVICIOS DE TRANSFUSIÓN
Pruebas diagnósticas basadas en la respuesta inmunitaria
 Pruebas diagnósticas basadas en la respuesta inmunitaria 1 Por qué utilizamos el diagnóstico inmunológico? El diagnóstico clínico no suele ser definitivo. Las lesiones histológicas pueden ser indicativas
Pruebas diagnósticas basadas en la respuesta inmunitaria 1 Por qué utilizamos el diagnóstico inmunológico? El diagnóstico clínico no suele ser definitivo. Las lesiones histológicas pueden ser indicativas
Grupos Sanguineos Y Factor Rh
 Grupos Sanguineos Y Factor Rh Tomás Cristobal Silva Gálvez 3ro Medio San Andrés Fecha: 24-08-12 Asignatura: Biología Porfesor: José Rojas Grupos Sanguineos: Los Grupos sanguíneos es la clasificación de
Grupos Sanguineos Y Factor Rh Tomás Cristobal Silva Gálvez 3ro Medio San Andrés Fecha: 24-08-12 Asignatura: Biología Porfesor: José Rojas Grupos Sanguineos: Los Grupos sanguíneos es la clasificación de
Se define la compatibilidad en transfusión como la falta
 Capítulo 4 PRUEBAS PRETRANSFUSIONALES: COMPATIBILIDAD EN TRANSFUSIÓN L. Barbolla. Hospital de Móstoles, Madrid. E. Contreras. Centre de Transfusió i Banc de Teixits, Tarragona. Se define la compatibilidad
Capítulo 4 PRUEBAS PRETRANSFUSIONALES: COMPATIBILIDAD EN TRANSFUSIÓN L. Barbolla. Hospital de Móstoles, Madrid. E. Contreras. Centre de Transfusió i Banc de Teixits, Tarragona. Se define la compatibilidad
PROGRAMA CURSO INMUNOHEMATOLOGIA Y BANCO DE SANGRE 2013
 PROGRAMA CURSO INMUNOHEMATOLOGIA Y BANCO DE SANGRE 2013 DATOS GENERALES: Asignatura: Inmunohematología y Banco de Sangre Carrera : Tecnología Médica Nivel Curricular: 8 semestre (4 año) Escuela, programa
PROGRAMA CURSO INMUNOHEMATOLOGIA Y BANCO DE SANGRE 2013 DATOS GENERALES: Asignatura: Inmunohematología y Banco de Sangre Carrera : Tecnología Médica Nivel Curricular: 8 semestre (4 año) Escuela, programa
QUANTA Chek ANA Panel
 QUANTA Chek ANA Panel 708111 Uso previsto El QUANTA Chek TM ANA Panel se utiliza como control de calidad de los procedimientos IFA y ELISA para anticuerpos antinucleares. Cada suero sirve como control
QUANTA Chek ANA Panel 708111 Uso previsto El QUANTA Chek TM ANA Panel se utiliza como control de calidad de los procedimientos IFA y ELISA para anticuerpos antinucleares. Cada suero sirve como control
ScanGel ReverScan A1, B x 5 ml ReverScan A1, A2, B, O x 5 ml
 ScanGel ReverScan A1, B 86790 2 x 5 ml ReverScan A1, A2, B, O 86795 4 x 5 ml GLÓBULOS ROJOS TEST DE ORIGEN HUMANO PARA LA PRUEBA SÉRICA DEL TIPAJE ABO IVD Todos los productos fabricados y comercializados
ScanGel ReverScan A1, B 86790 2 x 5 ml ReverScan A1, A2, B, O 86795 4 x 5 ml GLÓBULOS ROJOS TEST DE ORIGEN HUMANO PARA LA PRUEBA SÉRICA DEL TIPAJE ABO IVD Todos los productos fabricados y comercializados
Calificación de Equipos. Bact: Ana Lucia Aguirre Mejía
 Calificación de Equipos Bact: Ana Lucia Aguirre Mejía Agenda Introducción Normas Calificación de Equipos Calificación de Diseño (CD) Calificación de Instalación (CI ) Calificación de Operación (CO) Calificación
Calificación de Equipos Bact: Ana Lucia Aguirre Mejía Agenda Introducción Normas Calificación de Equipos Calificación de Diseño (CD) Calificación de Instalación (CI ) Calificación de Operación (CO) Calificación
PROCEDIMIENTO PARA EL ANÁLISIS INMUNOHEMATOLÓGICO DE LA SANGRE Y SUS COMPONENTES SANGUÍNEOS
 PROCEDIMIENTO PARA EL ANÁLISIS INMUNOHEMATOLÓGICO DE LA SANGRE Y SUS COMPONENTES SANGUÍNEOS DOM-P210-HR6_001 NOVIEMBRE DEL 2003 NOVIEMBRE DEL 2003 001 Este documento es vigente y está actualizado porque
PROCEDIMIENTO PARA EL ANÁLISIS INMUNOHEMATOLÓGICO DE LA SANGRE Y SUS COMPONENTES SANGUÍNEOS DOM-P210-HR6_001 NOVIEMBRE DEL 2003 NOVIEMBRE DEL 2003 001 Este documento es vigente y está actualizado porque
Sistemas Antigénicos eritrocitarios ABO, Lewis y P. Lourdes Torres Ribas 14 de Enero 2015 FBSTIB
 Sistemas Antigénicos eritrocitarios ABO, Lewis y P Lourdes Torres Ribas 14 de Enero 2015 FBSTIB Descubrimiento de los Antígenos -La administración intravenosa de medicamentos se hizo por vez primera en
Sistemas Antigénicos eritrocitarios ABO, Lewis y P Lourdes Torres Ribas 14 de Enero 2015 FBSTIB Descubrimiento de los Antígenos -La administración intravenosa de medicamentos se hizo por vez primera en
NORMA Oficial Mexicana NOM-019-SSA1-1993, Que establece las especificaciones sanitarias del reactivo antiglobulina humana para la prueba de coombs.
 DOF: 07/11/1994 NORMA Oficial Mexicana NOM-019-SSA1-1993, Que establece las especificaciones sanitarias del reactivo antiglobulina humana para la prueba de coombs. AUGUSTO BONDANI GUASTI, Director General
DOF: 07/11/1994 NORMA Oficial Mexicana NOM-019-SSA1-1993, Que establece las especificaciones sanitarias del reactivo antiglobulina humana para la prueba de coombs. AUGUSTO BONDANI GUASTI, Director General
SISTEMA Rh. Bioquìmica: Ma. Eugenia Morales
 SISTEMA Rh Bioquìmica: Ma. Eugenia Morales El sistema Rh RH es el sistema más polimórfico Presenta mas de 45 antigenos Descubierto por Landsteiner y Wiener en 194 por un trabajo en monos Rhesus Genes RH
SISTEMA Rh Bioquìmica: Ma. Eugenia Morales El sistema Rh RH es el sistema más polimórfico Presenta mas de 45 antigenos Descubierto por Landsteiner y Wiener en 194 por un trabajo en monos Rhesus Genes RH
Métodos para Inmunidad Viral
 Métodos para Inmunidad Viral Radioinmunoensayo (RIA) Técnica muy sensible basada en la competencia de unión al anticuerpo específico entre el antígeno a cuantificar y cantidades conocidas del antígeno
Métodos para Inmunidad Viral Radioinmunoensayo (RIA) Técnica muy sensible basada en la competencia de unión al anticuerpo específico entre el antígeno a cuantificar y cantidades conocidas del antígeno
LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH CONTROL DE CALIDAD EXTERNO
 TALLER ANALISIS RESULTADOS PEEC BACTERIOLOGIA PROGRAMA: IDENTIFICACIÓN BACTERIANA Y SUSCEPTIBILIDAD ANTIMICROBIANA LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH ACTIVIDADES ABRIL 2011 TM M. Soledad Prat.
TALLER ANALISIS RESULTADOS PEEC BACTERIOLOGIA PROGRAMA: IDENTIFICACIÓN BACTERIANA Y SUSCEPTIBILIDAD ANTIMICROBIANA LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH ACTIVIDADES ABRIL 2011 TM M. Soledad Prat.
LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH
 TALLER ANALISIS RESULTADOS PEEC BACTERIOLOGIA PROGRAMA: IDENTIFICACIÓN BACTERIANA Y SUSCEPTIBILIDAD ANTIMICROBIANA LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH ACTIVIDADES ABRIL 2011 TM M. Soledad Prat.
TALLER ANALISIS RESULTADOS PEEC BACTERIOLOGIA PROGRAMA: IDENTIFICACIÓN BACTERIANA Y SUSCEPTIBILIDAD ANTIMICROBIANA LABORATORIO INFECCIONES INTRAHOSPITALARIAS- IIH ACTIVIDADES ABRIL 2011 TM M. Soledad Prat.
Examen de laboratorio: Chagas. Obtención de sangre Cantidad Características Conservación Procesa miento En capilares Heparinizados.
 Examen de laboratorio: Chagas Examen de laboratorio Microconcentra ción en Micrométodo en tubo centración Strout ELISA IFI HAI Tipo de muestra venosa o Venosa Suero o plasma sanguíneo Obtención de sangre
Examen de laboratorio: Chagas Examen de laboratorio Microconcentra ción en Micrométodo en tubo centración Strout ELISA IFI HAI Tipo de muestra venosa o Venosa Suero o plasma sanguíneo Obtención de sangre
PROGRAMA CURSO INMUNOHEMATOLOGIA Y BANCO DE SANGRE 2015
 PROGRAMA CURSO INMUNOHEMATOLOGIA Y BANCO DE SANGRE 2015 DATOS GENERALES: Asignatura: Inmunohematología y Banco de Sangre Carrera : Tecnología Médica Nivel Curricular: 8 semestre (4 año) Escuela, programa
PROGRAMA CURSO INMUNOHEMATOLOGIA Y BANCO DE SANGRE 2015 DATOS GENERALES: Asignatura: Inmunohematología y Banco de Sangre Carrera : Tecnología Médica Nivel Curricular: 8 semestre (4 año) Escuela, programa
CARTERA DE SERVICIOS
 CARTERA DE SERVICIOS 1.- Denominación: SERVICIO DE HEMATOLOGÍA Y HEMOTERAPIA Se trata de un servicio que debe incluirse en el Área de Servicios Médicos por lo que corresponde a Hematología Clínica (consultas,
CARTERA DE SERVICIOS 1.- Denominación: SERVICIO DE HEMATOLOGÍA Y HEMOTERAPIA Se trata de un servicio que debe incluirse en el Área de Servicios Médicos por lo que corresponde a Hematología Clínica (consultas,
Discrepancias. Fuente: Manual Téfnico de la AABB (17º edición) 1
 Discrepancias ABO Tec. Graciela Deutsch - Noviembre 2015 Fuente: Manual Téfnico de la AABB (17º edición) 1 2 Antisueros conocidos GRs. de fenotipo ABO conocidos A B O Anti-A A Anti-B B Anti-AB AB 3 DETERMINACIÓN
Discrepancias ABO Tec. Graciela Deutsch - Noviembre 2015 Fuente: Manual Téfnico de la AABB (17º edición) 1 2 Antisueros conocidos GRs. de fenotipo ABO conocidos A B O Anti-A A Anti-B B Anti-AB AB 3 DETERMINACIÓN
PROCEDIMIENTO DE CONTROL A, B, O Y RH-D PRE-TRANFUSIONAL
 Código : Páginas: 1 de 6 PROCEDIMIENTO DE CONTROL A, B, O Y RH-D PRE-TRANFUSIONAL Elaborado por: Revisado por: Aprobado por: T.M. Mauricio Gutiérrez Cea Encargado TM. Carlos Figueroa Zaror Jefe de Laboratorio
Código : Páginas: 1 de 6 PROCEDIMIENTO DE CONTROL A, B, O Y RH-D PRE-TRANFUSIONAL Elaborado por: Revisado por: Aprobado por: T.M. Mauricio Gutiérrez Cea Encargado TM. Carlos Figueroa Zaror Jefe de Laboratorio
PROPUESTAS DE MODIFICACIÓN (DEFINICIONES APROBADAS EN LA REUNIÓN DEL 27 DE OCTUBRE) Dice Debe decir Justificación/Comentario
 PROPUESTAS DE MODIFICACIÓN (DEFINICIONES APROBADAS EN LA REUNIÓN DEL 27 DE OCTUBRE) Agentes de diagnóstico: Todos los insumos incluyendo antígenos, anticuerpos, calibradores, verificadores, reactivos,
PROPUESTAS DE MODIFICACIÓN (DEFINICIONES APROBADAS EN LA REUNIÓN DEL 27 DE OCTUBRE) Agentes de diagnóstico: Todos los insumos incluyendo antígenos, anticuerpos, calibradores, verificadores, reactivos,
ELEMENTOS DE UN SISTEMA BASADO EN LA ADMINISTRACIÓN DE LA CALIDAD
 ELEMENTOS DE UN SISTEMA BASADO EN LA ADMINISTRACIÓN DE LA CALIDAD Por Jorge Everardo Aguilar -Morales 2017 ELEMENTOS DE UN SISTEMA DE ADMINISTRACIÓN BASADO EN LA CALIDAD La definición del concepto de calidad
ELEMENTOS DE UN SISTEMA BASADO EN LA ADMINISTRACIÓN DE LA CALIDAD Por Jorge Everardo Aguilar -Morales 2017 ELEMENTOS DE UN SISTEMA DE ADMINISTRACIÓN BASADO EN LA CALIDAD La definición del concepto de calidad
CRITERIOS ESPECIFICOS DE ACREDITACIÓN. ENTIDADES DE CERTIFICACIÓN DE ETIQUETADO DE VACUNO
 Página 1 de 7 CRITERIOS ESPECIFICOS DE ACREDITACIÓN. ENTIDADES DE CERTIFICACIÓN DE ETIQUETADO DE VACUNO REVISIÓN Nº FECHA MODIFICACIONES 01 2001/12/18 Nueva elaboración 02 Mayo 2002 Apartados 3, 7 y 8.3
Página 1 de 7 CRITERIOS ESPECIFICOS DE ACREDITACIÓN. ENTIDADES DE CERTIFICACIÓN DE ETIQUETADO DE VACUNO REVISIÓN Nº FECHA MODIFICACIONES 01 2001/12/18 Nueva elaboración 02 Mayo 2002 Apartados 3, 7 y 8.3
Recolección y uso de datos en la Producción de Alimentos
 Recolección y uso de datos en la Producción de Alimentos www.axonas.com.ar Durante mucho tiempo, la industria alimentaria se basó en las quejas de los consumidores, los reportes de enfermedades y el sentido
Recolección y uso de datos en la Producción de Alimentos www.axonas.com.ar Durante mucho tiempo, la industria alimentaria se basó en las quejas de los consumidores, los reportes de enfermedades y el sentido
ACTIVIDAD PRÁCTICA No. 6 REACCIONES DE HIPERSENSIBILIDAD
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA CENTRO UNIVERSITARIO METROPOLITANO FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDACTICA DE INMUNOLOGÍA Y MICROBIOLOGÍA MÉDICA TERCER AÑO ACTIVIDAD PRÁCTICA No. 6 REACCIONES
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA CENTRO UNIVERSITARIO METROPOLITANO FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDACTICA DE INMUNOLOGÍA Y MICROBIOLOGÍA MÉDICA TERCER AÑO ACTIVIDAD PRÁCTICA No. 6 REACCIONES
INMUNOHEMATOLOGÍA EN EL EMBARAZO. Isoinmunización Rh. Sergio Jiménez López R4 de Bioquímica Clínica
 INMUNOHEMATOLOGÍA EN EL EMBARAZO Isoinmunización Rh Sergio Jiménez López R4 de Bioquímica Clínica GENERALIDADES En la membrana celular de los hematíes existen diferentes proteínas, las cuales son las responsables
INMUNOHEMATOLOGÍA EN EL EMBARAZO Isoinmunización Rh Sergio Jiménez López R4 de Bioquímica Clínica GENERALIDADES En la membrana celular de los hematíes existen diferentes proteínas, las cuales son las responsables
IMPORTANCIA DE LAS PRUEBAS CRUZADAS PRETRANSFUSIONALES EN LA DETECCION DE ESTADOS DE INCOMPATIBILIDAD SEROLOGICA
 IMPORTANCIA DE LAS PRUEBAS CRUZADAS PRETRANSFUSIONALES EN LA DETECCION DE ESTADOS DE INCOMPATIBILIDAD SEROLOGICA L. Carboni*, A. Solórzano*, C. Montero** Key Word Index: Pretransfusional crossmatch RESUMEN
IMPORTANCIA DE LAS PRUEBAS CRUZADAS PRETRANSFUSIONALES EN LA DETECCION DE ESTADOS DE INCOMPATIBILIDAD SEROLOGICA L. Carboni*, A. Solórzano*, C. Montero** Key Word Index: Pretransfusional crossmatch RESUMEN
Universidad Central Del Este UCE Facultad de Ciencias de la Salud Escuela de Bioanálisis
 Universidad Central Del Este UCE Facultad de Ciencias de la Salud Escuela de Bioanálisis Programa de la Asignatura: (BIA-101) Serología Clínica Total de Créditos: 1 Teoría: 0 Practica: 2 Prerrequisitos:
Universidad Central Del Este UCE Facultad de Ciencias de la Salud Escuela de Bioanálisis Programa de la Asignatura: (BIA-101) Serología Clínica Total de Créditos: 1 Teoría: 0 Practica: 2 Prerrequisitos:
Sistema de Grupo Sanguíneo Kidd
 Uy esto sigue! Sistema de Grupo Sanguíneo Kidd Grupos Sanguíneos mas allá del ABO y Rh Objetivos 1. Reconocer la nomenclatura de los antígenos y anticuerpos 2. Bioquímica y genética 2. Los alelos principales
Uy esto sigue! Sistema de Grupo Sanguíneo Kidd Grupos Sanguíneos mas allá del ABO y Rh Objetivos 1. Reconocer la nomenclatura de los antígenos y anticuerpos 2. Bioquímica y genética 2. Los alelos principales
 CURRICULUM VITAE ANTECEDENTES PERSONALES Nombre Correo Electrónico FERNANDO NICOLAS VALDES ABARZA fdovaldesabarza@hotmail.com fernando.valdes@intraumatologico.cl laboratorio.trauma@hotmail.com ANTECEDENTES
CURRICULUM VITAE ANTECEDENTES PERSONALES Nombre Correo Electrónico FERNANDO NICOLAS VALDES ABARZA fdovaldesabarza@hotmail.com fernando.valdes@intraumatologico.cl laboratorio.trauma@hotmail.com ANTECEDENTES
complejo polisacárido membrana plasmática palmitato
 Gen RHD Proteina RhD Gen RHCE Proteina RhCcEe RHCED (RH30) y RHAG (RH50) RH30 y RH50 son proteínas integrales de membrana que muestran una topología similar al atravesar 12 veces la membrana. RH30 contiene
Gen RHD Proteina RhD Gen RHCE Proteina RhCcEe RHCED (RH30) y RHAG (RH50) RH30 y RH50 son proteínas integrales de membrana que muestran una topología similar al atravesar 12 veces la membrana. RH30 contiene
Validación de métodos analíticos:
 Métodos analíticos adecuados a su propósito Validación de métodos analíticos: Conceptos y elementos Prof. Dr. Bertram Nagel Consultor PTB Leipzig, Alemania 1 Los buenos resultados analíticos se basan en
Métodos analíticos adecuados a su propósito Validación de métodos analíticos: Conceptos y elementos Prof. Dr. Bertram Nagel Consultor PTB Leipzig, Alemania 1 Los buenos resultados analíticos se basan en
Guía para el docente
 Guía para el docente Descripción curricular: - Nivel: 4.º Medio - Subsector: Biología - Unidad temática: Biología humana y salud Rechazo inmune - Palabras clave: grupos sanguíneos ABO, factor Rh, transfusión
Guía para el docente Descripción curricular: - Nivel: 4.º Medio - Subsector: Biología - Unidad temática: Biología humana y salud Rechazo inmune - Palabras clave: grupos sanguíneos ABO, factor Rh, transfusión
Inmunohematología basada en la evidencia. Dra Graciela León de González Banco Municipal de Sangre del DC Caracas Venezuela gonzaleo@cantv.
 Inmunohematología basada en la evidencia Dra Graciela León de González Banco Municipal de Sangre del DC Caracas Venezuela gonzaleo@cantv.net Problema: Embarazada sensibilizada Paciente femenino de 34 años
Inmunohematología basada en la evidencia Dra Graciela León de González Banco Municipal de Sangre del DC Caracas Venezuela gonzaleo@cantv.net Problema: Embarazada sensibilizada Paciente femenino de 34 años
Tecnicas rápidas Alergenos Alimentarios: ELISA convencional Tests Inmunocromatográficos. Alejandro Castanera Vitaltech Ibérica s.l.
 Tecnicas rápidas para detección de Alergenos Alimentarios: ELISA convencional Tests Inmunocromatográficos Alejandro Castanera Vitaltech Ibérica s.l. Antecedentes Los alergenos alimentarios son proteínas
Tecnicas rápidas para detección de Alergenos Alimentarios: ELISA convencional Tests Inmunocromatográficos Alejandro Castanera Vitaltech Ibérica s.l. Antecedentes Los alergenos alimentarios son proteínas
WITNESS RELAXIN (plasma, serum) RLX RLX u d 9 n n ersio V X RLX L R -W IO B S
 WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
RESULTADOS Y DISCUSIÓN
 RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
TEMA 14. Métodos inmunológicos para la identificación microbiana
 TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
AGENCIA NACIONAL DE MEDICAMENTOS INSTRUCTIVO SOBRE CONTENIDO DEL RÓTULO DE LOS PRODUCTOS FARMACÉUTICOS
 INSTRUCTIVO SOBRE CONTENIDO DEL RÓTULO DE LOS PRODUCTOS FARMACÉUTICOS 1.- ASPECTOS LEGALES El rotulado de los productos farmacéuticos debe cumplir con lo señalado en el título II (De Los Envases y El Rotulado)
INSTRUCTIVO SOBRE CONTENIDO DEL RÓTULO DE LOS PRODUCTOS FARMACÉUTICOS 1.- ASPECTOS LEGALES El rotulado de los productos farmacéuticos debe cumplir con lo señalado en el título II (De Los Envases y El Rotulado)
MANUAL DE NORMAS Y PROCEDIMIENTOS PROCEDIMIENTO: OPERATIVOS DE ORINAS
 SERVICIO DE LABORATORIO 1 DE 5 1. OBJETIVO El objetivo del presente documento es describir el procedimiento para determinar las características físicas, química y microscópicas de muestras de orinas. 2.
SERVICIO DE LABORATORIO 1 DE 5 1. OBJETIVO El objetivo del presente documento es describir el procedimiento para determinar las características físicas, química y microscópicas de muestras de orinas. 2.
MDmulticard CENTÍMETROS CAPAZ DE SALVAR UN LABORATORIO DE CINCO UNA VIDA EN CINCO MINUTOS
 MDmulticard UN LABORATORIO DE CINCO CENTÍMETROS CAPAZ DE SALVAR UNA VIDA EN CINCO MINUTOS NOT VALID FOR PRINTING! Low resolution PDF file. For high resolution files, please contact Corporate Communications
MDmulticard UN LABORATORIO DE CINCO CENTÍMETROS CAPAZ DE SALVAR UNA VIDA EN CINCO MINUTOS NOT VALID FOR PRINTING! Low resolution PDF file. For high resolution files, please contact Corporate Communications
PRUEBA CRUZADA Detecciòn de Anticuerpos irregulares. Dr. Julio A. Vidal Escudero
 PRUEBA CRUZADA Detecciòn de Anticuerpos irregulares Dr. Julio A. Vidal Escudero Reacciòn adversa transfusional: Reacciòn Febril Hemolìtica IV Francia:(1668). Giovanni Battista Denis, médico de Luis XVI.-Transf.de
PRUEBA CRUZADA Detecciòn de Anticuerpos irregulares Dr. Julio A. Vidal Escudero Reacciòn adversa transfusional: Reacciòn Febril Hemolìtica IV Francia:(1668). Giovanni Battista Denis, médico de Luis XVI.-Transf.de
