Miguel Ángel Gómez López, 2º Farmacia UCLM
|
|
|
- Catalina Ponce Lara
- hace 6 años
- Vistas:
Transcripción
1 Bioquímica I. Proteínas 1. Proteínas Biomoléculas orgánicas a base de C,H,O,N. Son macromoléculas/polímeros formados por la repetición de aminoácidos unidos por enlace peptídico. Los seres humanos no tenemos nitrogenasas para fijar y aprovechar el nitrógeno atmosférico (N2). Por esto, son nuestra principal fuente de nitrógeno. Representan más del 50% del peso seco de la célula y tienen una gran diversidad de funciones: protectora, vitaminas, anticuerpos, aunque sobretodo estructural. 1) Clasificación Holoproteínas: formadas únicamente por aminoácidos. Heteroproteínas: formadas por una parte proteica y una parte no proteica (grupo prostético). Son las cromoproteínas, glucoproteínas, lipoproteínas, nucleoproteínas y fosfoproteínas. 2. Aminoácidos Son los monómeros de las proteínas. Todos están compuestos por un carbono con 4 sustituyentes: -H, - COO -, -NH3 y grupo R. Se designan con los nombres vulgares o abreviaturas de 3 letras o 1. Existen 20 aminoácidos proteicos, 10 de ellos esenciales (Arg, Phe, His, Ile, Leu, Lys, Met, Thr, Trp,Val). Sus propiedades son estas: Sólidos/cristalinos. Elevado punto de fusión. Solubles en agua. Tienen actividad óptica (=isomería). Son sustancias anfóteras (ácido-base). Podemos atender a distintas clasificaciones de aminoácidos. Según criterio biológico: 1) AAs proteicos codificables o universales 2) AAs proteicos modificacos o particulares: colágeno (4-hidroxiprolina, 5-hidroxilisina), tiroides (T3). 3) AAs no proteicos: más de 100, abundantes en plantas superiores. Participan en el metabolismo del nitrógeno (L-ornitina y L-citrulina) o coenzimas (beta-alanina). Almacenan energía: creatina. Según criterio químico: 1) Según carga de la cadena R: según la polaridad del radical a ph fisiológico = 7,2: a. Apolares/hidrófobos El radical es un grupo metilo (CH2, CH3). Suelen ser compuestos aromáticos (leucina). b. Polares sin carga El radical es un grupo OH o NH2. Destacamos la serina, cisteína. c. Polares con carga negativa (-): AAs ácidos El radical es un grupo ácido (COOH). A ph fisiológico, cede un protón y se queda en forma de COO -. Destacamos el ácido glutámico (glutamato). d. Polares con carga positiva (+): AAs básicos Destacamos la lisina o la arginina. BIOQUÍMICA I 1
2 2) Según la estructura de la cadena R: alifáticos, aromáticos y heterocíclicos 3) Con carbono asimétrico (excepto Gly): L (plantas) y D-aminoácidos (microorganismos). De los 20 aminoácidos proteicos, todos presentan un carbono asimétrico, excepto la glicina, cuyo radical es un H y por tanto el carbono alfa no es asimétrico. Por esto, los 19 restantes si presentarán isomería. Se clasifican en D o L, según el grupo amino esté a la derecha o la izquierda, respectivamente. Son los aminoácidos L los que abundan en los seres vivos y la naturaleza Comportamiento anfótero La estructura de los AAs corresponde a una sal interna, ion doble o forma zwitterion. Cada AA tiene al menos 2 grupos ionizables. La forma cargada o no cargada depende del ph. La curva de titulación de un aminoácido representa las variaciones de ph de una solución al ir añadiendo concentraciones conocida de un ácido o una base. El pk representa la capacidad de captar o ceder protones por parte de un grupo funcional de un aminoácido en un ph determinado. Además, es el punto de mayor capacidad tamponadora de ese grupo funcional. El pi es el ph al cual la carga neta de las moléculas en solución es nula. Ahí, el poder tamponador del aminoácido es mínimo. El único AA capaz de actuar como tampón a ph fisiológico es la His (pkr=6.0). Actúan como base cuando ph < pi. El grupo amina ha cogido protones (NH3 + ). Siempre que el pi esté por encima del ph, actuará como una base. Actúan como ácido cuando ph > pi. El grupo ácido ha cedido protones (COO - ). Siempre que el ph se mayor que el pi actuará como un ácido. Actúan como ácido-base cuando ph = pi. El grupo ácido ha cedido protones (COO - ) y el grupo amino ha cogido (NH3 + ). pk1: 50% base y 50% zwitterion (ácido-base). pk2: 50% ácido y 50% zwitterion. pi: valor del ph del medio donde todo el AA está en forma zwitterion o dipolar 2.2. Implicaciones clínicas pi = pk1 + pk2 2 Fenilcetonuria: defecto genético en fenilalanina hidroxilasa. Se da la acumulación de Phe, fenilpiruvato y fenil-lactato. Cistinuria: defecto en el transporte por las células epiteliales de cistina y AAs básicos. Aparece cistina, Lys, Arg y ornitina en orina. Enfermedad de Hartnup Síndrome de Fanconi 3. Enlace peptídico Es un enlace covalente de tipo amida, entre el COOH del primer aminoácido y el NH2 del segundo aminoácido, con pérdida de una molécula de agua. El primero queda con el NH2 libre = amino terminal, y el segundo queda con el COOH libre = carboxilo terminal. Su formación requiere aporte de energía, mientras la hidrólisis del ATP esté termodinámicamente favorecida. Tiene carácter parcial de doble enlace, a medio camino entre enlace sencillo y enlace doble, porque no puede rotar no girar. La estructura nativa es la más estable de todas las posibles y es funcional. BIOQUÍMICA I 2
3 4. Estructura primaria Secuencia de aminoácidos, que según si número, tipo y orden dan lugar a diversas estructuras. Es una estructura plana, no funcional. La estructura nativa depende de la estructura primaria, ya que depende de cómos sea esta se plegará de una u otra forma y será estable de una u otra, con una misión concreta. 5. Estructura secundaria Resulta del plegamiento de la primaria. Hay muchas, pero destacamos las tres más importantes: 1) α-hélice Forma una hélice dextrógira muy estable. La presentan las α-queratinas. La estructura está estabilizada por puentes de hidrógeno intracatenarios, entre el O de un aminoácido y el H unido a un N de 4 más (n+4). Al calor se estiran, y al frío recuperan su forma original. 1 giro de hélice contiene 3,6 residuos. Abundante en proteínas globulares, con cooperatividad en el plegamiento. Las prolinas introducen curvaturas que rompen la hélice, esto permite el plegamiento sobre sí misma = estructuras supersecundarias. Los radicales están hacia fuera, permitiendo aminoácidos voluminosos y con carga. La estructura forma cordones de 3 a 7 cabos, unidos por puentes disulfuro entre cadenas polipeptídicas paralelas. 2) β-lámina plegada Forma de acordeón abierta, más extendida que la α-hélice. Destaca la fibroína de la seda. Está estabilizada por puentes de hidrógeno intercatenarios (sin codos) e intracatenarios (con giros beta), entre cadenas antiparalelas. Al calor no se estiran. Permite la asociación de varias cadenas polipeptídicas una al lado de la otra, pudiendo ser paralelas o antiparalelas. Abundante en proteínas fibrilares y un 15% en la estructura terciaria de globulares. Los acordamientos beta son giros de 180º mediante la conexión de los extremos de 2 segmentos de hojas beta antiparalelas. Involucra 4 AAs por puentes de hidrógeno entre n y n+3. Los hay de tipo I (más frecuentes) y II (Gly en posición 3). Los radicales están hacia dentro, permitiendo aminoácidos pequeños y sin carga, para que no haya repulsiones e inestabilidad. No tiene enlaces disulfuro. 3) Hélice de colágeno Más abierto que el acordeón de la hoja plegada, dificultando la formación de puentes de hidrógeno. La forman la prolina, lisina, hidroxiprolina e hidroxilisina. El colágeno está formado por la repetición del tropocolágeno (3 hélices). Entre esas 3 cadenas se dan puentes de hidrógeno intercatenarios; y entre tropocolágenos, enlaces covalentes entre radicales adyacentes. Funciones del colágeno: a. Principal proteína de tejidos conectivos. b. Bajo valor biológico, faltan AAs esenciales. c. Su ebullición da lugar a gelatina. d. Su mala formación produce escorbuto, por falta de vitamina C, que aporta OH a los AAs. Otras estructuras secundarias son giros beta, barrilete de láminas beta o meandros beta. BIOQUÍMICA I 3
4 6. Estructura terciaria Resulta del plegamiento de la secundaria. Si es poco, da lugar a proteínas fibrosas; si es mucho, proteína globulares. Las fibrosas son insolubles, con función estructural, en forma de fibra y con un solo tipo de estructura secundaria. Destacamos los colágenos, queratinas, elastinas y fibroínas. Las globulares son solubles, con función dinámica, en forma de esfera y con varios tipos de estructura secundaria. Llevan radicales polares al exterior, para su disolución en agua (ptes. de H), y apolares al interior (hidrófobos). Destaca la mioglobulina (transporte O2 en músculo) y ribonucleasa pancreática. Además, destacamos prolaminas, gluteninas, albúminas, hormonas y enzimas. Hay unas fuerzas que estabilizan la estructura terciaria: 1) Interacciones hidrofóbicas entre no polares. 2) Puentes de hidrógeno. 3) Interacciones iónicas. 4) Fuerzas de Van der Walls. 5) Puentes disulfuro. Los dominios estructurales son pequeños grupos de AAs específicos de cada proteína que funcionan independientemente del resto y anclan a los ligandos, para actuar sobre la proteína. Sus funciones son: 1) Anclar ligandos. 2) Atravesar la membrana plasmática. 3) Constituir centro activo de enzimas. 4) Enlazar al ADN en la transcripción. 7. Estructura cuaternaria Se denominan proteínas oligoméricas, formadas por varias cadenas polipeptídicas (protómeros), entre las cuales hay enlaces débiles, aunque a veces hay disulfuros. Se dan por asociación de monómeros con distinta conformación, mediante los cuales se establecen interacciones débiles: fuerzas de Van de Waals, puentes de hidrógeno y fuerzas electrostáticas. Destacamos la hemoglobina, con cuatro cadenas (2 alfa, 2 beta) y 4 grupos hemo (anillo tetrapirrólico); y los anticuerpos, con 4 cadenas (2 H, 2 L). 8. Propiedades de las proteínas 1) Capacidad amortiguadora Mantienen constante el ph del medio a pesar de que se añadan pequeñas cantidades de ácido o base. Su carbonos y nitrógenos no pueden ionizarse, solo tienen un extremo amino y carboxilo terminal, que no es suficiente. La capacidad reside en los radicales de los AAs de los grupos 3 (COOH) y 4 (NH3). 2) Solubilidad Las globulares son solubles porque tienen los radicales hacia fuera y están rodeadas de agua, que establecen puentes de hidrógeno con ellos y las disuelve. Las fibrilares son insolubles porque tienen radicales muy grandes (CH3) y no deja a la proteína ser globosa. La solubilidad depende de: a. Concentración iónica: a más sales (+/-) se establecen más puentes de hidrógeno con el agua y aumenta la solubilidad. Pero si se añaden muchas, las cargas se disponen alrededor de la proteína y quitan moléculas de agua = - solubilidad. BIOQUÍMICA I 4
5 b. Temperatura: al calentar, la proteína pierde agua y se precipita = -solubilidad. c. ph: si ph < pi, el COOH no estará ionizado; si ph > pi, el NH2 no estará ionizado, perdiéndose cargas = -solubilidad. 3) Especificidad En la de especie, las proteína son específicas en cada estructura, cambian el número, tipo u orden de los aminoácidos, aunque la mayoría coincide, porque realizan la misma función. Las diferencias son grandes en especies alejadas evolutivamente y pequeñas en las emparentadas. En la de función, cada proteína tiene una función específica, según la estructura primaria y la conformación nativa (ligando concreto). Un cambio en la secuencia de AAs cambia el tipo de plegamiento y puede tener ya otra función = especificidad. 4) Desnaturalización Es la pérdida de las estructuras espaciales y la vuelta a la primaria, dejando de ser soluble y funcional. Las cadenas se pliegan y adoptan configuraciones al azar. Las causas de desnaturalización son temperaturas superiores a 50 ºC o ph extremos. Si estas causas duran poco tiempo, puede producirse la renaturalización = vuelta a estructura espacial. Hay dos casos principales de desnaturalización: a. Cortado de la leche: desnaturalización de la caseína por ph ácido. b. Precipitación de la clara de huevo: desnaturalización de la ovoalbúmina por calor. 9. Heteroproteínas 1) Cromoproteínas: g.prostético = pigmento. Hay porfirínicas (con grupo hemo) como hemoglobina y mioglobina; y no porfirínicas (con otro grupo) como la hemocianina. 2) Glucoproteínas: g.prostético = glúcido. Destacamos los anticuerpos. 3) Lipoproteínas: g.prostético = lípido. LDL/HDL, seroalbúmina con ácidos grasos. 4) Fosfoproteínas: g.prostético = H3PO4. Destaca la caseína o la vitelina. 5) Nucleoproteínas: g.prostético = ácido nucleico. Destaca la cromatina (ADN + histonas). 10. Funciones proteínas 1) Estructural: colágeno, elastina, queratina. 2) Enzimática: el 99,9% son globulares. 3) Hormonal: insulina, glucagón, calcitonina. 4) Defensiva: anticuerpos, trombina. 5) Transporte: seroalbúmina, hemoglobina, mioglobina. 6) Reserva: ovoalbúmina, caseína. 7) Homeostática: todas las proteínas. 8) Contráctil: actina, miosina, dineína (cilios y flagelos). BIOQUÍMICA I 5
Proteínas. Características generales
 Proteínas Características generales Son las macromoléculas más abundantes en las células. Constituyen hasta el 50% del peso. Forman moléculas específicas en cada especie, incluso entre individuos. Además,
Proteínas Características generales Son las macromoléculas más abundantes en las células. Constituyen hasta el 50% del peso. Forman moléculas específicas en cada especie, incluso entre individuos. Además,
EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS
 EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS 1) Qué es un tetrapéptido?. Construye uno, formado por los siguientes aminoácidos: Ala, Cys, Ser y Tyr. 2) Haz corresponder los elementos de las dos columnas: -Cys -Hormona
EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS 1) Qué es un tetrapéptido?. Construye uno, formado por los siguientes aminoácidos: Ala, Cys, Ser y Tyr. 2) Haz corresponder los elementos de las dos columnas: -Cys -Hormona
Tema 5: aminoácidos y proteínas
 1. Los aminoácidos 2. Propiedades de los aminoácidos 3. El enlace peptídico 4. Estructuras 1 aria y 2 aria de las proteínas 5. Estructuras 3 aria y 4 aria de las proteínas 6. Propiedades de las proteínas
1. Los aminoácidos 2. Propiedades de los aminoácidos 3. El enlace peptídico 4. Estructuras 1 aria y 2 aria de las proteínas 5. Estructuras 3 aria y 4 aria de las proteínas 6. Propiedades de las proteínas
TEMA 2.- PROTEÍNAS. AMINOÁCIDOS
 TEMA 2.- PROTEÍNAS. AMINOÁCIDOS Diversidad estructural y funcional de las proteínas. Aminoácidos: características estructurales y clasificación. Aminoácidos estándares y derivados. Aminoácidos esenciales
TEMA 2.- PROTEÍNAS. AMINOÁCIDOS Diversidad estructural y funcional de las proteínas. Aminoácidos: características estructurales y clasificación. Aminoácidos estándares y derivados. Aminoácidos esenciales
Holoproteínas (sólo contienen aa)
 TEMA 4: P ROTEÍNAS 1. Concepto y clasificación Las proteínas son biomoléculas orgánicas formadas por C, H, O, N y en menor medida P y S y otros elementos (Fe,Cu, Mg, ). Son polímeros no ramificados de
TEMA 4: P ROTEÍNAS 1. Concepto y clasificación Las proteínas son biomoléculas orgánicas formadas por C, H, O, N y en menor medida P y S y otros elementos (Fe,Cu, Mg, ). Son polímeros no ramificados de
 Aminoácidos I Br. Cecilia López Área Bioquímica Departamento de Biología Molecular y Celular Marzo 2012 Aminoácidos Proteínas Neurotransmisores (GABA, dopamina) Mediadores de la inflamación (Histamina)
Aminoácidos I Br. Cecilia López Área Bioquímica Departamento de Biología Molecular y Celular Marzo 2012 Aminoácidos Proteínas Neurotransmisores (GABA, dopamina) Mediadores de la inflamación (Histamina)
Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de
 Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
Aminoácidos. Los aminoácidos se agrupan en la figura según las propiedades de sus cadenas
 Aminoácidos Es esencial tener un conocimiento básico acerca de la química de las proteínas, para entender la nutrición y otros conceptos del metabolismo. Las proteínas se componen de carbono, hidrógeno,
Aminoácidos Es esencial tener un conocimiento básico acerca de la química de las proteínas, para entender la nutrición y otros conceptos del metabolismo. Las proteínas se componen de carbono, hidrógeno,
Estructura y propiedades de las proteínas
 Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
Aminoácidos y péptidos
 Aminoácidos y péptidos AMINOÁCIDOS: Moléculas orgánicas con un grupo amino (NH 2) y un grupo carboxilo (COOH). Los aminoácidos proteicos son α aminoácidos, que portan las dos funciones sobre el carbono
Aminoácidos y péptidos AMINOÁCIDOS: Moléculas orgánicas con un grupo amino (NH 2) y un grupo carboxilo (COOH). Los aminoácidos proteicos son α aminoácidos, que portan las dos funciones sobre el carbono
Unidad 3: Organización molecular de la célula Proteínas
 Proteínas Las proteínas son las biomoléculas más abundantes de las células, constituyendo el 50% de su peso seco aproximadamente. Estructuralmente, son polímeros de aminoácidos. Existe una enorme variedad
Proteínas Las proteínas son las biomoléculas más abundantes de las células, constituyendo el 50% de su peso seco aproximadamente. Estructuralmente, son polímeros de aminoácidos. Existe una enorme variedad
Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno
 Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno Tema 3 Proteínas Fibrosas y Proteínas Globulares Fibrosas Globulares Forma alargada Unidades repetidas de un solo tipo de estructura secundaria
Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno Tema 3 Proteínas Fibrosas y Proteínas Globulares Fibrosas Globulares Forma alargada Unidades repetidas de un solo tipo de estructura secundaria
PROTEÍNAS. Las proteínas están constituidas por la unión de numerosas moléculas sencillas (monómeros) denominados aminoácidos.
 PROTEÍNAS 1. INTRODUCCIÓN Las proteínas son los constituyentes químicos fundamentales de la materia viva. Constituyen alrededor del 50% en peso seco del cuerpo. Los glúcidos y lípidos se encuentran en
PROTEÍNAS 1. INTRODUCCIÓN Las proteínas son los constituyentes químicos fundamentales de la materia viva. Constituyen alrededor del 50% en peso seco del cuerpo. Los glúcidos y lípidos se encuentran en
Tema 4c Estructura tridimensional de las proteínas. Proteínas fibrosas. Proteínas globulares.
 Tema 4c Estructura tridimensional de las proteínas. Proteínas fibrosas. Proteínas globulares. Proteínas fibrosas Estructura y función de las queratinas Estructura y función del colágeno Triple hélice de
Tema 4c Estructura tridimensional de las proteínas. Proteínas fibrosas. Proteínas globulares. Proteínas fibrosas Estructura y función de las queratinas Estructura y función del colágeno Triple hélice de
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
Estructura tridimensional de proteínas
 Estructura tridimensional de proteínas 1. En solución acuosa, la conformación proteica esta determinada por dos factores prioritarios. Uno es la formación de un número máximo de enlaces de hidrógeno. El
Estructura tridimensional de proteínas 1. En solución acuosa, la conformación proteica esta determinada por dos factores prioritarios. Uno es la formación de un número máximo de enlaces de hidrógeno. El
Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas.
 Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Guía de Biología I Medio Departamento de Ciencias Profesora NATALIA URQUIETA M.
 COLEGIO SAN CRISTOBAL Av. Diego Portales N 1.520. La Florida Guía de Biología I Medio Departamento de Ciencias Profesora NATALIA URQUIETA M. MOLÉCULAS ORGANICAS. Los componentes orgánicos de la materia
COLEGIO SAN CRISTOBAL Av. Diego Portales N 1.520. La Florida Guía de Biología I Medio Departamento de Ciencias Profesora NATALIA URQUIETA M. MOLÉCULAS ORGANICAS. Los componentes orgánicos de la materia
Material elaborado por F. Agius, O. Borsani, P.Díaz, S. Gonnet, P. Irisarri, F. Milnitsky y J. Monza. Bioquímica. Facultad de Agronomía.
 AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
FISIOLOGÍA GENERAL Jesús Merino Pérez y María José Noriega Borge
 BIOMOLÉCULAS. PROTEÍNAS BIOMOLÉCULAS Los bioelementos se unen para formar biomoléculas, también denominadas principios inmediatos. En los seres vivos las moléculas se caracterizan por presentar una gran
BIOMOLÉCULAS. PROTEÍNAS BIOMOLÉCULAS Los bioelementos se unen para formar biomoléculas, también denominadas principios inmediatos. En los seres vivos las moléculas se caracterizan por presentar una gran
Composición química de los seres vivos
 Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas.
 Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Estructura 3D de proteínas
 Estructura 3D de proteínas Aportaciones de la Bioinformática Structural Bioinformatics Laboratory Research Group on Biomedical Informatics (GRIB) Universitat Pompeu Fabra Sumario Conceptos básicos (I):
Estructura 3D de proteínas Aportaciones de la Bioinformática Structural Bioinformatics Laboratory Research Group on Biomedical Informatics (GRIB) Universitat Pompeu Fabra Sumario Conceptos básicos (I):
Proteínas fibrosas. α-queratinas
 Hélices α entrecruzadas por puentes disulfuro Proteínas fibrosas α-queratinas Estructura Características Localización Estructuras resistentes e insolubles de dureza y flexibilidad variables Estructura
Hélices α entrecruzadas por puentes disulfuro Proteínas fibrosas α-queratinas Estructura Características Localización Estructuras resistentes e insolubles de dureza y flexibilidad variables Estructura
BIOQUIMICA Y FISIOLOGÍA MICROBIANA. Dra. Yenizey Merit Alvarez Cisneros
 BIOQUIMICA Y FISIOLOGÍA MICROBIANA Dra. Yenizey Merit Alvarez Cisneros Moléculas importantes para la vida Compuestos Orgánicos (contienen carbono e hidrógeno) y forma enlaces covalentes Azucares Aminoácidos
BIOQUIMICA Y FISIOLOGÍA MICROBIANA Dra. Yenizey Merit Alvarez Cisneros Moléculas importantes para la vida Compuestos Orgánicos (contienen carbono e hidrógeno) y forma enlaces covalentes Azucares Aminoácidos
OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo.
 1 OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo. 2 3 4 Son las moléculas que forman a los organismos o participan de su metabolismo. Orgánicas
1 OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo. 2 3 4 Son las moléculas que forman a los organismos o participan de su metabolismo. Orgánicas
Tema 4b Estructura tridimensional de las proteínas. Estructura supersecundaria y terciaria.
 Tema 4b Estructura tridimensional de las proteínas. Estructura supersecundaria y terciaria. Estructura supersecundaria Motivos Dominios Estructura terciaria Fuerzas que la estabilizan Plegamiento de proteínas
Tema 4b Estructura tridimensional de las proteínas. Estructura supersecundaria y terciaria. Estructura supersecundaria Motivos Dominios Estructura terciaria Fuerzas que la estabilizan Plegamiento de proteínas
Tema 1: Los seres vivos: composición y función
 Tema 1: Los seres vivos: composición y función https://www.youtube.com/watch?v=-s28cydwauo El nivel atómico El nivel atómico Bioelementos: elementos que constituyen la materia viva Fundamentales: C, H,
Tema 1: Los seres vivos: composición y función https://www.youtube.com/watch?v=-s28cydwauo El nivel atómico El nivel atómico Bioelementos: elementos que constituyen la materia viva Fundamentales: C, H,
3. AMINOACIDOS. PROPIEDADES ACIDO-BASE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 3. AMINOACIDOS. PROPIEDADES ACIDO-BASE ESQUEMA - Aminoácidos. Definición, funciones y clasificación - Tipos de aminoácidos: aminoácidos
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 3. AMINOACIDOS. PROPIEDADES ACIDO-BASE ESQUEMA - Aminoácidos. Definición, funciones y clasificación - Tipos de aminoácidos: aminoácidos
SEGUNDA PARTE DE BIOMOLÉCULAS: PROTEÍNAS Y ÁCIDOS NUCLEICOS.
 EXAMEN DE BIOLOGÍA Y GEOLOGÍA DE 1 º BACHILLERATO GRUPO A SEGUNDA PARTE DE BIOMOLÉCULAS: PROTEÍNAS Y ÁCIDOS NUCLEICOS. NOMBRE Y APELLIDOS: 1º. Cómo afectaría a la función de la hemoglobina y la mioglobina
EXAMEN DE BIOLOGÍA Y GEOLOGÍA DE 1 º BACHILLERATO GRUPO A SEGUNDA PARTE DE BIOMOLÉCULAS: PROTEÍNAS Y ÁCIDOS NUCLEICOS. NOMBRE Y APELLIDOS: 1º. Cómo afectaría a la función de la hemoglobina y la mioglobina
Lehninger Principles of Biochemistry Fourth Edition
 David L. Nelson and Michael M. Cox Lehninger Principles of Biochemistry Fourth Edition Capítulo 3: Amino Acidos, Péptidos, y Proteínas Copyright 2004 by W. H. Freeman & Company Estereoquímica de Aminoácidos
David L. Nelson and Michael M. Cox Lehninger Principles of Biochemistry Fourth Edition Capítulo 3: Amino Acidos, Péptidos, y Proteínas Copyright 2004 by W. H. Freeman & Company Estereoquímica de Aminoácidos
ESTRUCTURA 4ª. áá ESENCIAL
 PROTEINAS COMPOSICIÓN AMINOÁCIDOS ENLACE PEPTÍDICO ESTRUCTURA CLASIFICACIÓN áá ESENCIAL PROPIEDADES NO POLARES POLARES S/CARGA POLARES C/CARGA OPTICAS ACIDO-BASE (Anfóteras) SOLUBILIDAD PUNTO DE FUSIÓN
PROTEINAS COMPOSICIÓN AMINOÁCIDOS ENLACE PEPTÍDICO ESTRUCTURA CLASIFICACIÓN áá ESENCIAL PROPIEDADES NO POLARES POLARES S/CARGA POLARES C/CARGA OPTICAS ACIDO-BASE (Anfóteras) SOLUBILIDAD PUNTO DE FUSIÓN
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR
 INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - Componentes químicos de la célula - Un poco de química 1 Un poco de química El 99% del peso de una célula corresponde a C, H, N y O. La sustancia más abundante
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - Componentes químicos de la célula - Un poco de química 1 Un poco de química El 99% del peso de una célula corresponde a C, H, N y O. La sustancia más abundante
H N CH COOH. dipéptido
 CLASE : PROTEINAS Fuerzas que influyen en estructura Proteica Papel de secuencia de aminoácidos en estructura de la proteína Estructura Secundaria de las Proteínas Plegamiento (Folding) de proteínas y
CLASE : PROTEINAS Fuerzas que influyen en estructura Proteica Papel de secuencia de aminoácidos en estructura de la proteína Estructura Secundaria de las Proteínas Plegamiento (Folding) de proteínas y
Las moléculas que forman los seres vivos, o las sustancias que provienen de ellos, la madera o los alimentos. Son muy grandes, ya que están formadas
 Las moléculas que forman los seres vivos, o las sustancias que provienen de ellos, la madera o los alimentos. Son muy grandes, ya que están formadas por miles, o millones de átomos. MACROMOLÉCULAS Son
Las moléculas que forman los seres vivos, o las sustancias que provienen de ellos, la madera o los alimentos. Son muy grandes, ya que están formadas por miles, o millones de átomos. MACROMOLÉCULAS Son
I) Biomoléculas 6) Proteínas I-6 PROTEÍNAS
 I-6 PROTEÍNAS CONCEPTO Y CARACTERÍSTICAS Concepto: Se pueden definir como polímeros formados por la unión, mediante enlaces peptídicos, de unidades de menor masa molecular llamadas aminoácidos. Son moléculas
I-6 PROTEÍNAS CONCEPTO Y CARACTERÍSTICAS Concepto: Se pueden definir como polímeros formados por la unión, mediante enlaces peptídicos, de unidades de menor masa molecular llamadas aminoácidos. Son moléculas
Funciones biológicas de las proteínas. 1.- Enzimas. Las proteínas más variadas y de mayor especialización son aquéllas con actividad catalítica.
 Funciones biológicas de las proteínas 1.- Enzimas. Las proteínas más variadas y de mayor especialización son aquéllas con actividad catalítica. 2.- Proteínas de transporte. Proteínas de transporte en el
Funciones biológicas de las proteínas 1.- Enzimas. Las proteínas más variadas y de mayor especialización son aquéllas con actividad catalítica. 2.- Proteínas de transporte. Proteínas de transporte en el
BIOMOLÉCULAS. Son moléculas fundamentales para la constitución y funcionamiento de todo ser vivo. Se clasifican en dos grupos:
 FICHA N 2 UNIDAD III: CÉLULAS A ORGANISMOS Profesora Verónica Abasto Córdova Ciencias Naturales 8 Básico Nombre : Curso : Fecha : Revisión BIOMOLÉCULAS Son moléculas fundamentales para la constitución
FICHA N 2 UNIDAD III: CÉLULAS A ORGANISMOS Profesora Verónica Abasto Córdova Ciencias Naturales 8 Básico Nombre : Curso : Fecha : Revisión BIOMOLÉCULAS Son moléculas fundamentales para la constitución
Proteínas. José Seijo Ramil
 P.1. Aminoácidos: P.1.1. Concepto y fórmula general. P.1.2. Estereoisomería y actividad óptica P.1.3. Propiedades de los aminoácidos: Comportamiento anfótero. Punto isoeléctrico P.1.4 Clasificación P.2.
P.1. Aminoácidos: P.1.1. Concepto y fórmula general. P.1.2. Estereoisomería y actividad óptica P.1.3. Propiedades de los aminoácidos: Comportamiento anfótero. Punto isoeléctrico P.1.4 Clasificación P.2.
APRENDIZAJES ESPERADOS:
 APRENDIZAJES ESPERADOS: Identifican la composición y función biológica de los carbohidratos. Identifican la estructura, composición y organización de las proteínas. Comprenden el rol biológico de ciertas
APRENDIZAJES ESPERADOS: Identifican la composición y función biológica de los carbohidratos. Identifican la estructura, composición y organización de las proteínas. Comprenden el rol biológico de ciertas
ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS AMINOÁCIDOS
 ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS Fabián Rodríguez Julio 2011 AMINOÁCIDOS Un aminoácido es una molécula orgánica que en su estructura contiene un grupo amino (NH 2 ) y un grupo carboxilo
ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS Fabián Rodríguez Julio 2011 AMINOÁCIDOS Un aminoácido es una molécula orgánica que en su estructura contiene un grupo amino (NH 2 ) y un grupo carboxilo
TEORIA CELULAR. En el mundo vivo, la unidad fundamental es la célula. DECUBRIMIENTO DE LAS CELULAS
 TEORIA CELULAR En el mundo vivo, la unidad fundamental es la célula. DECUBRIMIENTO DE LAS CELULAS El nombre de célula significa celda, así las llamo Robert Hooke. En 1839 el zoólogo alemán Theodore Schwann
TEORIA CELULAR En el mundo vivo, la unidad fundamental es la célula. DECUBRIMIENTO DE LAS CELULAS El nombre de célula significa celda, así las llamo Robert Hooke. En 1839 el zoólogo alemán Theodore Schwann
AMINOÁCIDOS, PÉPTIDOS Y PROTEINAS. M.Sc. GABY MÓNICA FELIPE BRAVO
 AMINÁCIDS, PÉPTIDS Y PRTEINAS M.Sc. GABY MÓNICA FELIPE BRAV AMINÁCIDS C H 2 N C H R TDS LS AMINÁCIDS QUE FRMAN PARTE DE LAS PRTEÍNAS SN L-AMINÁCIDS CLASIFICACIÓN DE LS AMINÁCIDS ALIFÁTICS N PLARES ARMÁTICS
AMINÁCIDS, PÉPTIDS Y PRTEINAS M.Sc. GABY MÓNICA FELIPE BRAV AMINÁCIDS C H 2 N C H R TDS LS AMINÁCIDS QUE FRMAN PARTE DE LAS PRTEÍNAS SN L-AMINÁCIDS CLASIFICACIÓN DE LS AMINÁCIDS ALIFÁTICS N PLARES ARMÁTICS
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA
 BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
Aminoácidos y Proteínas. Bioquímica Kinesiología UNLAM 2014
 Aminoácidos y Proteínas Bioquímica Kinesiología UNLAM 2014 Proteínas Constituyen las moléculas orgánicas más abundantes de las células (50% del peso seco). Son macromoléculas, formadas por aminoácidos
Aminoácidos y Proteínas Bioquímica Kinesiología UNLAM 2014 Proteínas Constituyen las moléculas orgánicas más abundantes de las células (50% del peso seco). Son macromoléculas, formadas por aminoácidos
Metabolismo y uso de Proteínas. Jorge Ml. Sánchez Centro de Inv. en Nutrición Animal Escuela de Zootecnia Universidad de Costa Rica
 Metabolismo y uso de Proteínas Jorge Ml. Sánchez Centro de Inv. en Nutrición Animal Escuela de Zootecnia Universidad de Costa Rica Metabolismo de las Proteínas Funciones en el organismo 1. Constituyen
Metabolismo y uso de Proteínas Jorge Ml. Sánchez Centro de Inv. en Nutrición Animal Escuela de Zootecnia Universidad de Costa Rica Metabolismo de las Proteínas Funciones en el organismo 1. Constituyen
REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS.
 REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS. PRESENTACIÓN Los animales incluyendo al hombre, recibimos pocas moléculas sencillas y una gran cantidad de macromoléculas, como almidones, proteínas
REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS. PRESENTACIÓN Los animales incluyendo al hombre, recibimos pocas moléculas sencillas y una gran cantidad de macromoléculas, como almidones, proteínas
Polímero corto Monómero. síntesis. degradación
 Polímero corto Monómero síntesis degradación Hidratos de carbono. Glúcidos o azúcares. Monómeros Glúcidos. Dímeros. Glu+Glu= Maltosa (azúcar presente en la malta, un grano) Glu+Frc= Sacarosa (azúcar de
Polímero corto Monómero síntesis degradación Hidratos de carbono. Glúcidos o azúcares. Monómeros Glúcidos. Dímeros. Glu+Glu= Maltosa (azúcar presente en la malta, un grano) Glu+Frc= Sacarosa (azúcar de
Carbohidratos. CLASIFICACIÓN DE LOS CARBOHIDRATOS ALIMENTICIOS y ejemplos
 Carbohidratos También llamados hidratos de carbono, son uno de los tres tipos de macronutrientes presentes en nuestra alimentación (los otros dos son las grasas y las proteínas). Existen en multitud de
Carbohidratos También llamados hidratos de carbono, son uno de los tres tipos de macronutrientes presentes en nuestra alimentación (los otros dos son las grasas y las proteínas). Existen en multitud de
Niveles de organización biológica. La composición de los seres vivos
 Niveles de organización biológica. La composición de los seres vivos Imagen de Fondo bajo licencia Creative Commons, autor: René Ehrtardt. Animación ADN de dominio público, fuente:wikipedia Con este tema
Niveles de organización biológica. La composición de los seres vivos Imagen de Fondo bajo licencia Creative Commons, autor: René Ehrtardt. Animación ADN de dominio público, fuente:wikipedia Con este tema
Proteínas fibrosas. Alfa Queratinas Beta-Queratinas Fibroína Colágeno Elastina
 Proteínas Fibrosas La mayor parte o casi toda la proteína está organizada de manera paralela a un sólo eje Las proteínas fibrosas son generalmente fuertes mecánicamente Son generalmente insolubles Generalmente
Proteínas Fibrosas La mayor parte o casi toda la proteína está organizada de manera paralela a un sólo eje Las proteínas fibrosas son generalmente fuertes mecánicamente Son generalmente insolubles Generalmente
INTRODUCCIÓN A LA BIOQUÍMICA. La bioquímica se puede definir como el estudio de las bases moleculares de la vida.
 INTRODUCCIÓN A LA BIOQUÍMICA La bioquímica se puede definir como el estudio de las bases moleculares de la vida. BIOMOLECULAS + Los seres vivos están formados por miles de clases diferentes de moléculas
INTRODUCCIÓN A LA BIOQUÍMICA La bioquímica se puede definir como el estudio de las bases moleculares de la vida. BIOMOLECULAS + Los seres vivos están formados por miles de clases diferentes de moléculas
ESTRUCTURA Y PROPIEDADES DE LAS PROTEÍNAS
 ESTRUCTURA Y PROPIEDADES DE LAS PROTEÍNAS Máster Ingeniería Biomédica M. Victoria Luque Guillén Índice Índice 1. Introducción... 1 2. Aminoácidos... 1 2.1. Los aminoácidos... 1 2.2. Los aminoácidos esenciales...
ESTRUCTURA Y PROPIEDADES DE LAS PROTEÍNAS Máster Ingeniería Biomédica M. Victoria Luque Guillén Índice Índice 1. Introducción... 1 2. Aminoácidos... 1 2.1. Los aminoácidos... 1 2.2. Los aminoácidos esenciales...
Departamento de Química Física Facultad de Ciencias
 Interacciones electrostáticas. Interacciones electrostáticas. Los fenómenos de interacción con el disolvente y cosolventes. Interacciones electrostáticas. El origen de las cargas en proteínas. Fuentes
Interacciones electrostáticas. Interacciones electrostáticas. Los fenómenos de interacción con el disolvente y cosolventes. Interacciones electrostáticas. El origen de las cargas en proteínas. Fuentes
Tema 3: Las moléculas de la vida
 Tema 3: Las moléculas de la vida Principios inmediatos compuestos: - Agua. - Hidratos de carbono. - Lípidos. - Proteínas. - Acidos Nucleicos. Elemento. La materia, incluso la que constituye los organismos
Tema 3: Las moléculas de la vida Principios inmediatos compuestos: - Agua. - Hidratos de carbono. - Lípidos. - Proteínas. - Acidos Nucleicos. Elemento. La materia, incluso la que constituye los organismos
Biología General y Metodología de las Ciencias 2016 BIOMOLÉCULAS
 BIOMOLÉCULAS Objetivos: Reconocer los distintos niveles de organización de la materia. Diferenciar las propiedades constreñimiento, emergentes y colectivas. Identificar las principales Biomoléculas según
BIOMOLÉCULAS Objetivos: Reconocer los distintos niveles de organización de la materia. Diferenciar las propiedades constreñimiento, emergentes y colectivas. Identificar las principales Biomoléculas según
Repaso Opción múltiple Macromoléculas Biológicas
 Repaso Opción múltiple Macromoléculas Biológicas 1. Por qué esta información sobre el carbono es tan importante para entender las moléculas de la vida? a. Es el esqueleto de las moléculas biológicas requeridas
Repaso Opción múltiple Macromoléculas Biológicas 1. Por qué esta información sobre el carbono es tan importante para entender las moléculas de la vida? a. Es el esqueleto de las moléculas biológicas requeridas
4. CURVAS DE TITULACION DE AMINOACIDOS
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 4. CURVAS DE TITULACION DE AMINOACIDOS ESQUEMA - Curvas de titulación de los aminoácidos Curva de titulación de un aminoácido
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 4. CURVAS DE TITULACION DE AMINOACIDOS ESQUEMA - Curvas de titulación de los aminoácidos Curva de titulación de un aminoácido
PREUNIVERSITARIO POPULAR FRAGMENTOS COMUNES. Sábado 24 abril 2012 Ciencias - Biología. Aldo Gárate Soto BIOMOLÉCULAS. Aminoácidos y Proteínas.
 Sábado 24 abril 2012 Ciencias - Biología. Aldo Gárate Soto BIOMOLÉCULAS Aminoácidos y Proteínas. Los aminoácidos son compuestos orgánicos que poseen un grupo amino (NH 2 ), un grupo carboxilo (COOH), un
Sábado 24 abril 2012 Ciencias - Biología. Aldo Gárate Soto BIOMOLÉCULAS Aminoácidos y Proteínas. Los aminoácidos son compuestos orgánicos que poseen un grupo amino (NH 2 ), un grupo carboxilo (COOH), un
Componentes químicos de
 Componentes químicos de las célulasc Componentes químicos Las células están compuestas por una enorme cantidad y variedad de moléculas que pueden clasificarse en: Componentes inorgánicos Componentes orgánicos
Componentes químicos de las célulasc Componentes químicos Las células están compuestas por una enorme cantidad y variedad de moléculas que pueden clasificarse en: Componentes inorgánicos Componentes orgánicos
INTRODUCCION A LA ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS
 INTRODUCCION A LA ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS Lic. Claudio Vidos Departamento de investigación de DEMIK Electromedicina Director del INSTITUTO CAV Rehabilitación Departamento de investigación
INTRODUCCION A LA ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS Lic. Claudio Vidos Departamento de investigación de DEMIK Electromedicina Director del INSTITUTO CAV Rehabilitación Departamento de investigación
4. El esquema adjunto representa la estructura de una molécula denominada lisozima.
 BLOQUE I : La base físico-química de la materia 1. a. Nombre y formule un monosacárido que contenga seis átomos de carbono. b. Indica esquemáticamente una diferencia estructural existente entre el almidón
BLOQUE I : La base físico-química de la materia 1. a. Nombre y formule un monosacárido que contenga seis átomos de carbono. b. Indica esquemáticamente una diferencia estructural existente entre el almidón
Agua, carbohidratos y Lípidos
 Agua, carbohidratos y Lípidos Biomoléculas Inorgánicas Características del agua El agua es el principal e imprescindible componente del cuerpo humano. Aproximadamente el 60 % de este agua se encuentra
Agua, carbohidratos y Lípidos Biomoléculas Inorgánicas Características del agua El agua es el principal e imprescindible componente del cuerpo humano. Aproximadamente el 60 % de este agua se encuentra
Procesamiento de proteínas y modificaciones post-traduccionales
 Procesamiento de proteínas y modificaciones post-traduccionales Las proteínas después de sintetizadas en los ribosomas, deben ser procesadas para que logren tener su conformación nativa y ser activas Eventos
Procesamiento de proteínas y modificaciones post-traduccionales Las proteínas después de sintetizadas en los ribosomas, deben ser procesadas para que logren tener su conformación nativa y ser activas Eventos
01. INTRODUCCION. Conceptos previos. Verónica González Núñez Universidad de Salamanca
 01. INTRODUCCION. Conceptos previos Verónica González Núñez Universidad de Salamanca ESQUEMA. Introducción. Conceptos previos I. Principales grupos funcionales en Bioquímica II. Formación de compuestos
01. INTRODUCCION. Conceptos previos Verónica González Núñez Universidad de Salamanca ESQUEMA. Introducción. Conceptos previos I. Principales grupos funcionales en Bioquímica II. Formación de compuestos
Metabolismo de AMINOÁCIDOS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
Proteínas y enzimas. Biología. Niveles de organización I. Nivel molecular: Composición química de los seres vivos (II) Proteínas y Enzimas.
 Proteínas y enzimas Biología Niveles de organización I. Nivel molecular: Composición química de los seres vivos (II) Proteínas y Enzimas. 1. Proteínas: concepto e importancia biológica Importante Las proteínas
Proteínas y enzimas Biología Niveles de organización I. Nivel molecular: Composición química de los seres vivos (II) Proteínas y Enzimas. 1. Proteínas: concepto e importancia biológica Importante Las proteínas
MOMENTO DIPOLAR DE ENLACE. La polaridad de un enlace se mide con el momento dipolar de enlace, µ.
 didactalia.net En la mayoría de los compuestos orgánicos el átomo de carbono se enlaza a átomos más electronegativos, lo que promueve que los electrones del enlace covalente sean atraídos con mayor intensidad
didactalia.net En la mayoría de los compuestos orgánicos el átomo de carbono se enlaza a átomos más electronegativos, lo que promueve que los electrones del enlace covalente sean atraídos con mayor intensidad
Biomoléculas Orgánicas II
 Biomoléculas Orgánicas II INTRODUCCIÓN Tal como se vio en la clase anterior, los elementos químicos se organizan de tal forma que aumentan su complejidad y desarrollan funciones que son específicas. En
Biomoléculas Orgánicas II INTRODUCCIÓN Tal como se vio en la clase anterior, los elementos químicos se organizan de tal forma que aumentan su complejidad y desarrollan funciones que son específicas. En
Pagina casos de estudios:
 Libros para consulta de alumnos en el Área de Biología La Célula. De Coopers Biología Celular y Molecular G. Karp Becker.El mundo de la Célula 6Ed. Editorial Pearson Education. Alberts/Bray/Hopkin/Johnson/Lewis/Raff/Roberts/Walter.
Libros para consulta de alumnos en el Área de Biología La Célula. De Coopers Biología Celular y Molecular G. Karp Becker.El mundo de la Célula 6Ed. Editorial Pearson Education. Alberts/Bray/Hopkin/Johnson/Lewis/Raff/Roberts/Walter.
ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO
 ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO Todos los aminoácidos tienen, como mínimo, dos grupos titulables o ionizables, cada uno con un pka característico y, por tanto, con dos zonas tampón
ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO Todos los aminoácidos tienen, como mínimo, dos grupos titulables o ionizables, cada uno con un pka característico y, por tanto, con dos zonas tampón
PREGUNTAS PAU PROTEÍNAS
 PREGUNTAS PAU PROTEÍNAS EJERCICIO 1 a) Cuáles son las unidades estructurales de las proteínas? [0 2] b) Escriba su fórmula general [0 2]. c) Atendiendo a la variedad de radicales cite cuatro tipos de dichas
PREGUNTAS PAU PROTEÍNAS EJERCICIO 1 a) Cuáles son las unidades estructurales de las proteínas? [0 2] b) Escriba su fórmula general [0 2]. c) Atendiendo a la variedad de radicales cite cuatro tipos de dichas
QUÍMICA DE PROTEÍNAS
 QUÍMICA DE PROTEÍNAS COMPOSICIÓN ALIMENTO VOLATIL POR SECADO (AGUA o HUMEDAD) MATERIA SECA ORGANICA INORGANICA (CENIZAS) SOLUBLE EN DISOLVENTES ORGANICOS (GRASA O LIPIDOS) CON NITROGENO (PROTEINAS) NO
QUÍMICA DE PROTEÍNAS COMPOSICIÓN ALIMENTO VOLATIL POR SECADO (AGUA o HUMEDAD) MATERIA SECA ORGANICA INORGANICA (CENIZAS) SOLUBLE EN DISOLVENTES ORGANICOS (GRASA O LIPIDOS) CON NITROGENO (PROTEINAS) NO
CLASIFICACIÓN SEGÚN SU POLARIDAD NO POLARES POLARES NEUTROS ACIDOS BASICOS
 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2015 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2015 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
Proteínas. Tabla 1: Funciones de las proteínas
 Colegio Lectura Hispano Complementaria Americano Depto. de Ciencias - Biología Nivel: 4to medio Unidad I Proteínas 1 En las células, son las proteínas las macromoléculas más abundantes y las que constituyen
Colegio Lectura Hispano Complementaria Americano Depto. de Ciencias - Biología Nivel: 4to medio Unidad I Proteínas 1 En las células, son las proteínas las macromoléculas más abundantes y las que constituyen
XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA
 Rol de los Aminoácidos en el Cultivo de Vid XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA 2011 La Molina, 06 y 07 de Julio, 2011 Ing. M.Sc. Federico Ramírez D. Gerente Técnico Aminoácidos Las plantas
Rol de los Aminoácidos en el Cultivo de Vid XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA 2011 La Molina, 06 y 07 de Julio, 2011 Ing. M.Sc. Federico Ramírez D. Gerente Técnico Aminoácidos Las plantas
Tema 2. Biomoléculas compuestas orgánicas: Proteínas y biocatalizadores. PAU Biología. CEA García Alix
 PROTEÍNAS Y BIOCATALIZADORES (2011-12) 15.- Aminoácidos proteicos: Estructura general. Carácter anfótero. Clasificación según la cadena lateral: apolar, polar sin carga y polar con carga (ácida o básica).
PROTEÍNAS Y BIOCATALIZADORES (2011-12) 15.- Aminoácidos proteicos: Estructura general. Carácter anfótero. Clasificación según la cadena lateral: apolar, polar sin carga y polar con carga (ácida o básica).
Fuerzas Intermoleculares. Materia Condensada.
 Fuerzas Intermoleculares. Materia Condensada. Contenidos Introducción. Tipos de fuerzas intermoleculares. Fuerzas ion-dipolo Fuerzas ion-dipolo inducido Fuerzas de van der Waals Enlace de hidrógeno Tipos
Fuerzas Intermoleculares. Materia Condensada. Contenidos Introducción. Tipos de fuerzas intermoleculares. Fuerzas ion-dipolo Fuerzas ion-dipolo inducido Fuerzas de van der Waals Enlace de hidrógeno Tipos
Figura III.1: Estructura de aminoácidos
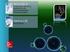 Características generales Las proteínas son compuestos orgánicos complejos, cuya estructura básica es una cadena de aminoácidos. Los aminoácidos son sustancias compuestas por carbono, oxígeno, hidrógeno
Características generales Las proteínas son compuestos orgánicos complejos, cuya estructura básica es una cadena de aminoácidos. Los aminoácidos son sustancias compuestas por carbono, oxígeno, hidrógeno
Proteínas. Fabrizio Marcillo Morla MBA. (593-9)
 Proteínas Fabrizio Marcillo Morla MBA barcillo@gmail.com (593-9) 4194239 Otras Publicaciones del mismo autor en Repositorio ESPOL Fabrizio Marcillo Morla Guayaquil, 1966. BSc. Acuicultura. (ESPOL 1991).
Proteínas Fabrizio Marcillo Morla MBA barcillo@gmail.com (593-9) 4194239 Otras Publicaciones del mismo autor en Repositorio ESPOL Fabrizio Marcillo Morla Guayaquil, 1966. BSc. Acuicultura. (ESPOL 1991).
PROTEÍNAS Y ÁCIDOS NUCLEICOS
 DESAFÍO Nº 10 Profesor Mauricio Hernández Fonseca Biología 1 Medio Nombre del Estudiante : Curso : PROTEÍNAS Y ÁCIDOS NUCLEICOS TIMBRE PROTEÍNAS Las proteínas son macromoléculas de elevada masa molecular.
DESAFÍO Nº 10 Profesor Mauricio Hernández Fonseca Biología 1 Medio Nombre del Estudiante : Curso : PROTEÍNAS Y ÁCIDOS NUCLEICOS TIMBRE PROTEÍNAS Las proteínas son macromoléculas de elevada masa molecular.
ANATOMIA. La vida es química. Los principios básicos de anatomía y fisiología se basan en principios dela química: la bioquímica.
 T 2. Química de la vida ANATOMIA 1. Niveles de organización química. Átomos Elementos, moléculas y compuestos 2. Enlaces químicos Enlaces iónicos Enlaces covalentes Puentes de hidrógeno 3. Química inorgánica
T 2. Química de la vida ANATOMIA 1. Niveles de organización química. Átomos Elementos, moléculas y compuestos 2. Enlaces químicos Enlaces iónicos Enlaces covalentes Puentes de hidrógeno 3. Química inorgánica
Universidad Nacional Autónoma de México
 Universidad Nacional Autónoma de México Facultad de Química Curso Genética y Biología Molecular (1630) Licenciatura Químico Farmacéutico Biológico Dra. Herminia Loza Tavera Profesora Titular de Carrera
Universidad Nacional Autónoma de México Facultad de Química Curso Genética y Biología Molecular (1630) Licenciatura Químico Farmacéutico Biológico Dra. Herminia Loza Tavera Profesora Titular de Carrera
Aminoácidos, Péptidos y Proteínas
 OBJETIVOS. Definir el concepto de aminoácidos sobre la base de su estructura. Enunciar la fórmula general de un aminoácido. Nombrar y formular los diferentes tipos de aminoácidos. Clasificación de los
OBJETIVOS. Definir el concepto de aminoácidos sobre la base de su estructura. Enunciar la fórmula general de un aminoácido. Nombrar y formular los diferentes tipos de aminoácidos. Clasificación de los
AMINOÁCIDOS Y PROTEÍNAS
 TEMA 2 AMINOÁCIDOS Y PROTEÍNAS Antes de realizar la guía deberá revisar: 1. Concepto de ph y poder amortiguador de una solución. 2. Características químicas de los aminoácidos. Evaluación: 1. Formule la
TEMA 2 AMINOÁCIDOS Y PROTEÍNAS Antes de realizar la guía deberá revisar: 1. Concepto de ph y poder amortiguador de una solución. 2. Características químicas de los aminoácidos. Evaluación: 1. Formule la
Tema 7 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD
 Tema 7 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD 1 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD 1. Concepto y naturaleza química de la biofase 2. Lípidos: acciones inespecíficas 3. Proteínas: enzimas
Tema 7 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD 1 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD 1. Concepto y naturaleza química de la biofase 2. Lípidos: acciones inespecíficas 3. Proteínas: enzimas
Profesor(a): C.D. María Isabel Pérez Aguilar
 Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
TEMA 8: PROTEÍNAS. 1.-INTRODUCCIÓN. 2.-COMPOSICIÓN DE LAS PROTEÍNAS. 3.-CLASIFICACIÓN DE LAS PROTEÍNAS.
 TEMA 8: PROTEÍNAS. 1 1.-INTRODUCCIÓN. El término proteína deriva del griego "proteos" (lo primero, lo principal) y habla de su gran importancia para los seres vivos. La importancia de las proteínas es,
TEMA 8: PROTEÍNAS. 1 1.-INTRODUCCIÓN. El término proteína deriva del griego "proteos" (lo primero, lo principal) y habla de su gran importancia para los seres vivos. La importancia de las proteínas es,
QUIMICA BIOLOGICA INTRODUCCION GENERAL
 QUIMICA BIOLOGICA INTRODUCCION GENERAL 1 BIOQUIMICA: La química de los seres vivos. La palabra "Bioquímica" fué utilizada por primera vez por Félix Hoppe-Seyler en 1877, en el prólogo al primer número
QUIMICA BIOLOGICA INTRODUCCION GENERAL 1 BIOQUIMICA: La química de los seres vivos. La palabra "Bioquímica" fué utilizada por primera vez por Félix Hoppe-Seyler en 1877, en el prólogo al primer número
La palabra "Bioquímica" fué utilizada por primera vez. número de "Hoppe-Seylers Zeitschrift für Physiologische Chemie" (la primera revista de
 BIOQUIMICA: La química de los seres vivos. La palabra "Bioquímica" fué utilizada por primera vez por Félix Hoppe-Seyler en 1877, en el prólogo al primer número de "Hoppe-Seylers Zeitschrift für Physiologische
BIOQUIMICA: La química de los seres vivos. La palabra "Bioquímica" fué utilizada por primera vez por Félix Hoppe-Seyler en 1877, en el prólogo al primer número de "Hoppe-Seylers Zeitschrift für Physiologische
Tema 2. El agua, el ph y los equilibrios iónicos
 Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
Repaso: Química celular (biomoléculas)
 Repaso: Química celular (biomoléculas) Hay 4 tipos principales de biomoléculas: 1) glúcidos o hidratos de carbono, 2) lípidos o grasas, 3) proteínas y 4) ácidos nucleicos. Las biomoléculas más grandes,
Repaso: Química celular (biomoléculas) Hay 4 tipos principales de biomoléculas: 1) glúcidos o hidratos de carbono, 2) lípidos o grasas, 3) proteínas y 4) ácidos nucleicos. Las biomoléculas más grandes,
AMINOACIDOS Y PROTEÍNAS
 AMINOACIDOS Y PROTEÍNAS I. OBJETIVO. Reconocer aminoácidos y proteínas a nivel de laboratorio. Analizar el tipo de estructura de los aminoácidos. II. FUNDAMENTO TEORICO. AMINOACIDOS: Cualquiera de los
AMINOACIDOS Y PROTEÍNAS I. OBJETIVO. Reconocer aminoácidos y proteínas a nivel de laboratorio. Analizar el tipo de estructura de los aminoácidos. II. FUNDAMENTO TEORICO. AMINOACIDOS: Cualquiera de los
AMINOÁCIDOS Y PÉPTIDOS
 TEMA 4 AMINOÁCIDOS Y PÉPTIDOS 1. Estructura y clasificación de los aminoácidos. 2. Propiedades ácido-base de los aminoácidos y péptidos 3. El enlace peptídico 4. Péptidos: hidrólisis y secuenciación 1.
TEMA 4 AMINOÁCIDOS Y PÉPTIDOS 1. Estructura y clasificación de los aminoácidos. 2. Propiedades ácido-base de los aminoácidos y péptidos 3. El enlace peptídico 4. Péptidos: hidrólisis y secuenciación 1.
Digestión y absorción de PROTEÍNAS. Marijose Artolozaga Sustacha, MSc
 Digestión y absorción de PROTEÍNAS Marijose Artolozaga Sustacha, MSc Digestión de proteínas de la dieta La mayor fuente de N de la dieta son las proteínas Unos 100g de proteína al día No se pueden absorber
Digestión y absorción de PROTEÍNAS Marijose Artolozaga Sustacha, MSc Digestión de proteínas de la dieta La mayor fuente de N de la dieta son las proteínas Unos 100g de proteína al día No se pueden absorber
SUSANA SERRADILLA IES LAS VIÑAS. MANILVA. ORGANIZACIÓN BÁSICA DEL CUERPO HUMANO
 SUSANA SERRADILLA IES LAS VIÑAS. MANILVA. ORGANIZACIÓN BÁSICA DEL CUERPO HUMANO ORGANIZACIÓN BÁSICA DEL CUERPO HUMANO Características diferenciales de los seres vivos Los niveles de organización biológica
SUSANA SERRADILLA IES LAS VIÑAS. MANILVA. ORGANIZACIÓN BÁSICA DEL CUERPO HUMANO ORGANIZACIÓN BÁSICA DEL CUERPO HUMANO Características diferenciales de los seres vivos Los niveles de organización biológica
Actividades de los lípidos Tema 1
 Actividades de los lípidos Tema 1 parte 3 BLOQUE 1: TEST 1. Qué tipo de lípidos son los más abundantes en la membrana plasmática de la mayoría de las células? a) Fosfolípidos b) Acidos grasos esenciales
Actividades de los lípidos Tema 1 parte 3 BLOQUE 1: TEST 1. Qué tipo de lípidos son los más abundantes en la membrana plasmática de la mayoría de las células? a) Fosfolípidos b) Acidos grasos esenciales
Iniciativa de Ciencia Progresiva
 Slide 1 / 42 New Jersey enter for Teaching and Learning Iniciativa de iencia Progresiva Este material está disponible gratuitamente en www.njctl.org y está pensado para el uso no comercial de estudiantes
Slide 1 / 42 New Jersey enter for Teaching and Learning Iniciativa de iencia Progresiva Este material está disponible gratuitamente en www.njctl.org y está pensado para el uso no comercial de estudiantes
- Las proteínas son esenciales para la formación y el mantenimiento de los tejidos corporales.
 TEMA 6. PROTEÍNAS - Las proteínas son esenciales para la formación y el mantenimiento de los tejidos corporales. - Los aa son los elementos estructurales de las proteínas. Las proteínas de plantas y animales
TEMA 6. PROTEÍNAS - Las proteínas son esenciales para la formación y el mantenimiento de los tejidos corporales. - Los aa son los elementos estructurales de las proteínas. Las proteínas de plantas y animales
Actividad introductoria: Aplicación en la industria de las fuerzas intermoleculares.
 Grado 10 Ciencias - Unidad 3 Cómo se relacionan los componentes del mundo? Tema Cómo afectan las fuerzas intermoleculares las propiedades de los compuestos? Curso: Nombre: Actividad introductoria: Aplicación
Grado 10 Ciencias - Unidad 3 Cómo se relacionan los componentes del mundo? Tema Cómo afectan las fuerzas intermoleculares las propiedades de los compuestos? Curso: Nombre: Actividad introductoria: Aplicación
