Revista de Actualización Clínica Volumen
|
|
|
- María Jesús Segura Giménez
- hace 6 años
- Vistas:
Transcripción
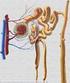
1 AMORTIGUADORES ( BUFFERS) Mg.Sc. Dra. Bustamante Cabrera Gladys 1 Cordon Patiño Catherine 2 RESUMEN La capacidad de regulación del medio ácido o alcalino a través de sustancias denominadas amortiguadoras, es una propiedad bien definida del cuerpo humano, mediante la cual, se establecen relaciones de equilibrio entre elementos ácidos y básicos. Es de esta forma que la homeostasis corporal, logra mantener las funciones vitales, ante cualquier cambio en el ph del medio, produciendo, excretando o reabsorbiendo sustancias, que se organizarán de dentro hacia fuera de la célula y en forma inversa, cuando los cambios sucedan en cualquier lado de la membrana. De esta manera, las sustancias que se convierten en reguladoras del ph, reciben el nombre de sustancias buffer o tampones fisiológicos, siendo el más importante, el sistema bicarbonato, al cual se unen con menor intensidad el sistema fosfato y la hemoglobina, así como los sistemas regulatorios pulmonares y renales a partir de la concentración de H +, de esta forma, la regulación sanguínea, intersticial y proteica, se entrelazan en una acción compleja, controlando y reponiendo el ph de la sangre, ante cualquier modificación que ponga en riesgo su estabilidad. La necesidad del conocimiento sobre el tema, permite al clínico orientar su 1 Médico Especialista en Medicina Interna. Docente Emérito UMSA. Mg.Sc. Psicopedagogía y Educación Superior. MBL. Dirección de desarrollo Local. Mg.Sc. Gestión, planificación y evaluación de proyectos. Miembro CNB. 2 Univ. Tercer Año Facultad de Odontología UMSA manejo ante circunstancias que condicionan acidosis o alcalosis. PALABRAS CLAVE Sustancias buffer. Tampón fisiológico. Bicarbonato. Fosfato. Acido Carbónico. ph INTRODUCCION Todo organismo vivo produce en forma constante ácidos orgánicos resultantes de reacciones metabólicas, catabolismo proteico y otras moléculas activas, lo que genera un grado de acidez a los fluidos intra y extracelulares, que puede ser medido por el ph, el cual puede a su vez ser regulado a partir de los llamados tampones fisiológicos o sustancias buffer, así como por la eliminación de ácidos o bases a través de los pulmones o riñones. 1,2 Los fluidos orgánicos, así como las sustancias que se encuentran disueltas en ellos, pueden tener cambios en el ph, en función al tipo de ingesta alimenticia y las reacciones metabólicas existentes, por lo que la falta de esta regulación, puede llevar a reacciones indeseables en el organismo. De esta manera la respuesta inmediata producida por las sustancias tampón o buffer (fosfato, bicarbonato y hemoglobina), ante variaciones del ph se constituyen en la primera barrera de defensa para la estabilización de dichos cambios. 1,3,-5 Los amortiguadores están formados por un ácido débil y su base conjugada o una base débil con su ácido conjugado, de manera que en caso de existir exceso de ácidos, sea la base que reacciona ante tal situación y visceversa. 2,5 Es así que la formación de aniones GAP (8-16 meq/l) hacen que se mantenga la electroneutralidad de las soluciones, considerándose a este grupo de Página2087
2 elementos como la diferencia entre aniones plasmáticos que normalmente no se encuentran (catión más abundante) y los aniones medidos más abundantes. El valor esperado debe oscilar entre Meq/L, valor que deberá ser corregido ante la presencia de bajos niveles de albumina. 6 Tomando en cuenta que el plasma sanguíneo y el fluido intersticial e intracelular tienen composición diferente en la concentración de electrolitos, se comprenderá que cada célula del organismo tiene un sistema propio de regulación de estas concentraciones, donde los aniones bicarbonato, fosfato mono y dibásico y proteínas, se constituirán el sistema regulador más importante, estableciendo ph de 7.35 a 7,45 como valor normal. Es así que los sistemas amortiguadores pueden ser: a) Sanguíneos: donde interviene proteínas como la hemoglobina (Hb), oxihemoglobina (HbO 2 ), sistema bicarbonato (HCO3 /H 2 CO 3 ), sistema fosfato (H 2 PO - 4/HPO 2-4). b) Plasmáticos e intersticiales: donde intervienen el sistema bicarbonato (HCO3 /H 2 CO 3 ). c) Intracelulares: donde intervienen predominantemente el sistema fosfato (H 2 PO - 4/HPO 2-4) y las proteínas (Hb/HbO 2 ). 3 TEORIA DE ARRENHIUS El físico químico Svante August. Arrhenius en 1884 planteó en su tesis doctoral que los iones, formados por carga eléctrica positiva, tenían movilidad en el agua, por lo que eran considerados como elementos conductores de electricidad, y que estos iones aumentan su disociación mientras mayor sea la dilución de la disolución. Según este científico las bases son sustancias que producen hidroxilo (OH - ) cuando se disocian al disolverse en agua. Esta teoría ha sido criticada por muchos estudiosos quienes aseguran que el concepto de ácido ha sido limitado a especies químicas que contienen hidrógeno, mientras que el concepto de bases, limitan a todas las especies que contienen hidroxilo, además que su referencia sobre la disociación de estas sustancias, se refiere a aquellas donde hay base acuosa, excluyendo a las reacciones que suceden en lugares donde hay ausencia de agua. 6-7 BICARBONATO El bicarbonato es una sal ácida derivada del acido carbónico, de sabor ácido y de color blanco amarillento y constituye el principal amortiguador ácido-básico del organismo. Este elemento químico se origina del metabolismo del ácido carbónico cuando este pierde uno o dos protones y tiene la capacidad de alcalinizar el medio donde se encuentra disuelto. FOSFATOS La vía de las pentosas fosfato, es una vía secundaria del metabolismo de la glucosa, con el fin de generar reducción de NADPH + H +, producir pentosas como la ribosas-5-p, para la formación de ácidos nucleicos y la formación de monosacárido fosfato, para la producción de CO2. - El HCO 3 producido al interior de la célula, luego del proceso tampón de la hemoglobina difunde por la membrana del glóbulo rojo e intercambia con iones Página2088
3 cloro (Cl - ) del plasma, mediante el mecanismo denominado desplazamiento del cloruro HEMOGLOBINA Es una proteína globular que se encuentra en gran cantidad en los glóbulos rojos, siendo el transportador de O 2 desde los pulmones hacia todos los tejidos del cuerpo, así como del CO 2 y de H + de los tejidos hacia los pulmones. Su anillo imidazolico, fijado con una histidina proximal, le permite tener el efecto tampón, Es decir que la oxigenación de la Hb aumenta la acidez del medio, al intervenir el H + en dicha fijación, mientras que la desoxigenación aumenta su capacidad de base. El momento en el que el CO 2 llega al eritrocito reacciona con el H 2 O, por acción de la anhidrasa carbónica, produciendo (90%) y carbamino Hb (7%). El H 2 CO 3 pasa directamente a HCO - 3, liberando un H +, que se une a la desoxi Hb, produciendo desoxi Hb +, reteniendo dos hidrogeniones por cada O 2 que pierde. De esta forma la mayor cantidad de CO 2 es transportado, produciéndose un proceso inverso a nivel pulmonar. MECANISMO DE REGULACION DE LOS AMORTIGUADORES BICARBONATO Normalmente, el producto del metabolismo de las células, es la producción de protones, que son sustancias ácidas, que de no ser eliminadas, aumentarían la acidez del espacio intersticial y del plasma. Así producidos los ácidos, el primer sistema en intervenir es el del bicarbonato que usa su base conjugada logrando la formación de ácido carbónico, el que circula por el torrente circulatorio, llegando a los pulmones, donde se descompone por acción de la anhidrasa carbónica, en agua y dióxido de carbono (H 2 O + CO 2 ), siendo este último eliminado por los pulmones. Se comprende entonces que el CO 2 formado en los tejidos corporales, es arrastrado por el sistema bicarbonato en forma de ácido carbónico, y que la reacción enzimática en la que interviene la anhidrasa carbónica en el glóbulo rojo, cuenta además con la participación de la hemoglobina en su forma básica y ácida, facilitando la conversión del CO 2, expelido en la respiración. Este sistema amortiguador bicarbonato, básico e importante, puede en algún momento, ser superado por la producción de ácidos, y el consumo de toda la fuente de bicarbonato, activando de esta manera la reposición de dicho anión a nivel renal, sistema fisiológico que empieza a extraer del cuerpo el bicarbonato en forma de H 2 CO 3, el que por acción de la misma anhidrasa carbónica, disocia a esta molécula, convirtiéndola en HCO 3 más hidrogeniones (H + ), esta última sustancia se intercambia por sodio (Na), de forma tal, que por cada molécula de Na filtrada, se elimina un hidrogenión por la orina, acidificando de esta forma, este fluido orgánico, el cual deberá de igual forma que todos los fluidos del cuerpo, mantener un ph óptimo, que en su caso es de aproximadamente 6, el que puede sin embargo, ser modificado en caso de excreciones exageradas o insuficientes de hidrogeniones, lo que producirá cambios en la fisiología renal. Como se ha visto hasta el momento, la regulación del ph en los sistemas orgánicos es importante, de tal forma que se debe mantener un ph sanguíneo de 7,4 y una proporción de HCO - 3 /H 2 CO 3 de 20:1. 2 Página2089
4 MECANISMO DE REGULACION DE LOS AMORTIGUADORES FOSFATO Si bien el ph corporal, permite la vida mientras se encuentre entre 7,00 y 7,80, los procesos relacionados a acidosis se encuentran con un ph menor a 7,35, mientras que la alcalosis se presenta cuando el ph supera los 7,45, con las consiguientes alteraciones respiratorias y metabólicas. El sistema de amortiguación de los fosfatos, permite de igual forma, pero con menor participación, la regulación del ph sanguíneo, a través de la formación del fosfato monoácido (HPO 4 2 ) en fosfato diácido (HPO 4 - ) que será excretado por la orina, el protón eliminado será intercambiado de la misma manera como se explicó anteriormente, por un ión Na MECANISMO DE ACCION DEL SISTEMA REGULADOR DE LAS PROTEINAS Las proteínas involucradas en la formación y transporte del ácido carbónico, se orientan principalmente a la hemoglobina, elemento que participa en forma importante en la amortiguación de las sustancias. Es de esta forma, que la desoxihemoglobina se convierte en un regulador de mejor calidad que la oxihemoglobina, en el sentido que la capacidad de captación de oxígeno por los tejidos mejora la capacidad de regulación de la Hb, constituyéndose en la proteína de mejor y mayor capacidad de tampón, en relación a otras proteínas plasmáticas. La capacidad de amortiguación de las proteínas se debe a la presencia de : a) Grupos ionizables de las cadenas laterales de los aminoácidos (AA): aspartato (Asp), glucosa (Glu), lisina (Lys), arginina (Arg), histamina (His), tirosina (Tyr), cisteína (Cys). b) Grupos COOH y NH2 terminales. El grupo imidazólico de la histidina será el principal responsable del poder de amortiguación de las proteínas ante cambios del ph, debido a que su pk está cerca a 7. Es así que cuando se encuentra un ph bajo, los grupos ionizables se protonan y su carga es positiva, mientras que si el ph es alto, los grupos se desprotonan y su carga se hace negativa La hemoglobina al ser una proteína globular, que tiene la capacidad de transportar oxígeno, regula La producción de H+, de dos formas: a) mediante un efecto amortiguador, combinándose con H+, en este caso su capacidad procede de los grupos ionizables, con un pk cercano al ph dentro del eritrocito, pero no puede amortiguar la cantidad total de H+ que fue generado por el transporte de CO 2 y eso explica la pequeña diferencia del que existe entre la sangre arterial y venosa. b) mediante un mecanismo izohídrico, denominado efecto de Bohr, el que consiste en la disminución de la afinidad de la hemoglobina por el O 2, cuando el ph disminuye. BIBLIOGRAFIA 1. Túnez Fiñana I., Galván Cejudo A., Fernández Reyes E. ph y amortiguadores: Tampones fisiológicos. URL en : DORES.pdf Fecha de acceso: 26 de Página2090
5 2. Vega Avila E., Konigsberg Fainstein M., La importancia biológica de los sistemas amortiguadores. URL actos/anterior/n42ne/sistam.pdf Martin A. M. Soluciones reguladoras de ph. URL ad/soluciones%20regulador AS%20DE%20pH.pdf Fecha de acceso: 26 de. 4. Hidrólisis y soluciones buffer. URL Acidos_y_Bases_III_Hidrolisis_y_Sol uciones_buffer.pdf Fecha de acceso: 26 de. 5. Ruiz Márquez M.J., Ortiz García C., Sánchez Luque J.J. Trastornos del equilibrio ácido base. 6. Medicina Interna División Clínica. Hospital General de Agudos Dr. Cosme Argerich. Acidosis metabólica. URL rtual/pdf/41.pdf Fecha de acceso: 26 de 7. Reacciones Acido base. Cap 3. URL /apuntes/problemas/cap3_1.pdf Lehninger, Mathews, Stryer,Voet. Tema 22 Ruta de las pentosas fosfato. URL imica_farmacia/r-t22-pentosas- 11.pdf Fecha de acceso: 26 de 9. Curso de biomoléculas. Universidad del país Vasco. URL x.htm Fecha de acceso: 26 de 10. Capítulo 8. Los amortiguadores fisiológicos. URL : e/cap82.pdf Fecha de acceso: 26 de. 11. Brandan N., Aguirre M.V. Cátedra de Bioquímica Hemoglobina 2008: URL /bioquimica/pdf/hemoglobina.pdf Página2091
1.-EQUILIBRIOS IÓNICOS EN DISOLUCIONES ACUOSAS.
 TEMA 5 EQUILIBRIOS IÓNICOS y SISTEMAS TAMPÓN. GUIÓN. ( 2 sesiones). 1.- EQUILIBRIOS IÓNICOS EN DISOLUCIÓN ACUOSA 2.- CONCEPTO DE SISTEMA TAMPÓN. 3.- IMPORTANCIA DE LA REGULACIÓN DEL PH FISIOLÓGICO. 4.-
TEMA 5 EQUILIBRIOS IÓNICOS y SISTEMAS TAMPÓN. GUIÓN. ( 2 sesiones). 1.- EQUILIBRIOS IÓNICOS EN DISOLUCIÓN ACUOSA 2.- CONCEPTO DE SISTEMA TAMPÓN. 3.- IMPORTANCIA DE LA REGULACIÓN DEL PH FISIOLÓGICO. 4.-
Actualización en Medio Interno Conceptos básicos
 Actualización en Medio Interno Conceptos básicos Bioquímica Lucrecia Drago Bioquímica M. Fernanda Pontoriero Ácidos Moléculas capaces de liberar H + HCl H + + Cl H 2 CO 3 H + + HCO 3 Bases Moléculas capaces
Actualización en Medio Interno Conceptos básicos Bioquímica Lucrecia Drago Bioquímica M. Fernanda Pontoriero Ácidos Moléculas capaces de liberar H + HCl H + + Cl H 2 CO 3 H + + HCO 3 Bases Moléculas capaces
Equilibrio Ácido - Base
 Equilibrio Ácido - Base OBJETIVOS Comprender la importancia de mantener los valores de ph dentro del rango normal Analizar los diferentes mecanismos de regulación que permiten mantener el equilibrio ácido-base
Equilibrio Ácido - Base OBJETIVOS Comprender la importancia de mantener los valores de ph dentro del rango normal Analizar los diferentes mecanismos de regulación que permiten mantener el equilibrio ácido-base
Fundación H.A. Barceló Facultad de Medicina
 Fundación H.A. Barceló Facultad de Medicina LICENCIATURA EN NUTRICION PRIMER AÑO FISIOLOGIA MODULO 16 LECCIONES 1 Y 2 1 MODULO 16: Equilibrio Electrolítico y Control de ph OBJETIVOS - Conocer las vías
Fundación H.A. Barceló Facultad de Medicina LICENCIATURA EN NUTRICION PRIMER AÑO FISIOLOGIA MODULO 16 LECCIONES 1 Y 2 1 MODULO 16: Equilibrio Electrolítico y Control de ph OBJETIVOS - Conocer las vías
REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE. Bqca. Sofía Langton Fisiología Humana Junio 2014
 REGULACIÓN DEL EQUILIBRIO ÁCIDOBASE Bqca. Sofía Langton Fisiología Humana Junio 2014 Objetivos 1. Estudiar la importancia del balance ácidobase en el organismo. 2. Comprender los tres sistemas (amortiguadores,
REGULACIÓN DEL EQUILIBRIO ÁCIDOBASE Bqca. Sofía Langton Fisiología Humana Junio 2014 Objetivos 1. Estudiar la importancia del balance ácidobase en el organismo. 2. Comprender los tres sistemas (amortiguadores,
b. Base es la sustancia que en disolución acuosa se disocia, liberando aniones de hidroxilo (OH ) según la ecuación general:
 ACIDOS y BASES Teorías ácido - base Los ácidos y las bases fueron definidos por primera vez por el científico sueco Svante Arrhenius en 1887 en su teoría disociación iónica, en la que establecía que hay
ACIDOS y BASES Teorías ácido - base Los ácidos y las bases fueron definidos por primera vez por el científico sueco Svante Arrhenius en 1887 en su teoría disociación iónica, en la que establecía que hay
Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires
 ÁCIDOS Y BASES Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires OBJETIVOS: - Reconocer ácidos, bases y sales, determinar sus disociaciones en agua, según sean electrolitos fuertes
ÁCIDOS Y BASES Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires OBJETIVOS: - Reconocer ácidos, bases y sales, determinar sus disociaciones en agua, según sean electrolitos fuertes
SOLUCIONES BUFFERS. pk = valor de ph en el cual las concentraciones del ácido y la sal son iguales
 SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
PH y SISTEMAS TAMPÓN
 PH y SISTEMAS TAMPÓN DISOCIACIÓN DEL AGUA.- El agua se disocia de la manera siguiente: HOH H+ OH- El valor de Kéq. a 25ºC es muy pequeña, siendo del orden de 1 8 x 10(-16). Esto significa
PH y SISTEMAS TAMPÓN DISOCIACIÓN DEL AGUA.- El agua se disocia de la manera siguiente: HOH H+ OH- El valor de Kéq. a 25ºC es muy pequeña, siendo del orden de 1 8 x 10(-16). Esto significa
6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
BALANCE ÁCIDO-BASE Y REGULACIÓN DEL ph
 BALANCE ÁCIDO-BASE Y REGULACIÓN DEL ph INTRODUCCION Importancia del mantenimiento del ph [H + ] afecta: Conformación de proteínas Reacciones donde el H + es producto o reactivo Liberación de O 2 de la
BALANCE ÁCIDO-BASE Y REGULACIÓN DEL ph INTRODUCCION Importancia del mantenimiento del ph [H + ] afecta: Conformación de proteínas Reacciones donde el H + es producto o reactivo Liberación de O 2 de la
Equilibrio Acido-Base
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Conceptos
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Conceptos
ARTICULOS DE INTERES
 ARTICULOS DE INTERES TEORIA DE BRÖNSTED Y LOWRY Dra. Zeballos López Lourdes 1 RESUMEN Johannes Brönsted y Thomas Lowry fueron científicos que desarrollaron una teoría sobre los ácidos y las bases, sustancias
ARTICULOS DE INTERES TEORIA DE BRÖNSTED Y LOWRY Dra. Zeballos López Lourdes 1 RESUMEN Johannes Brönsted y Thomas Lowry fueron científicos que desarrollaron una teoría sobre los ácidos y las bases, sustancias
Equilibrio Acido-Base
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,008 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,008 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
EQUILIBRIO ÁCIDO-BASE
 EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
HCl H + + Cl Ácido Hidrogenión Base Conjugada. Revista de Actualización Clínica Volumen POTENCIAL DE HIDROGENIONES- ph
 POTENCIAL DE HIDROGENIONES- ph Dr. Mansilla Canela Gonzalo 1 RESUMEN En todo organismo vivo, se producen sustancias ácidas y álcalis a partir del metabolismo de hidratos de carbono, lípidos y proteínas.
POTENCIAL DE HIDROGENIONES- ph Dr. Mansilla Canela Gonzalo 1 RESUMEN En todo organismo vivo, se producen sustancias ácidas y álcalis a partir del metabolismo de hidratos de carbono, lípidos y proteínas.
Tema: Soluciones Buffer-Amortiguadoras
 ESCUELA DE CIENCIAS AGRICOLA, PECUARIAS Y DEL MEDIO AMBIENTE ECAPMA Nombre l Curso: 334001-Sistema Metabólico Nutricional Tema: Soluciones Buffer-Amortiguadoras JAIRO ENRIQUE GRANADOS MORENO.,MSc (Director
ESCUELA DE CIENCIAS AGRICOLA, PECUARIAS Y DEL MEDIO AMBIENTE ECAPMA Nombre l Curso: 334001-Sistema Metabólico Nutricional Tema: Soluciones Buffer-Amortiguadoras JAIRO ENRIQUE GRANADOS MORENO.,MSc (Director
Amortiguadores o Buffer. SEMANA 13 Licda. Lilian Judith Guzman melgar
 Amortiguadores o Buffer SEMANA 13 Licda. Lilian Judith Guzman melgar Soluciones amortiguadoras También llamadas soluciones: Buffer Reguladoras Tampón Solución Buffer Es una solución de un ácido débil y
Amortiguadores o Buffer SEMANA 13 Licda. Lilian Judith Guzman melgar Soluciones amortiguadoras También llamadas soluciones: Buffer Reguladoras Tampón Solución Buffer Es una solución de un ácido débil y
Química de la Vida. Br. Ángel E. Hernández C.
 Química de la Vida Br. Ángel E. Hernández C. Conceptos básicos Bioquímica Biología Molecular Átomo Partículas subatómicas Molécula Polaridad Solubilidad Compuesto Orgánico Inorgánico Solución Mezcla Carga
Química de la Vida Br. Ángel E. Hernández C. Conceptos básicos Bioquímica Biología Molecular Átomo Partículas subatómicas Molécula Polaridad Solubilidad Compuesto Orgánico Inorgánico Solución Mezcla Carga
Amortiguadores o Buffer. SEMANA 13 Licda. Lilian Judith Guzman Melgar
 Amortiguadores o Buffer SEMANA 13 Licda. Lilian Judith Guzman Melgar Soluciones amortiguadoras También llamadas soluciones: Buffer Reguladoras Tampón Solución Buffer Es una solución de un ácido débil y
Amortiguadores o Buffer SEMANA 13 Licda. Lilian Judith Guzman Melgar Soluciones amortiguadoras También llamadas soluciones: Buffer Reguladoras Tampón Solución Buffer Es una solución de un ácido débil y
Amortiguadores o Buffer. SEMANA 13 Licda. Lilian Judith Guzman Melgar
 Amortiguadores o Buffer SEMANA 13 Licda. Lilian Judith Guzman Melgar Soluciones amortiguadoras También llamadas soluciones: Buffer Reguladoras Tampón Solución Buffer Es una solución de un ácido débil y
Amortiguadores o Buffer SEMANA 13 Licda. Lilian Judith Guzman Melgar Soluciones amortiguadoras También llamadas soluciones: Buffer Reguladoras Tampón Solución Buffer Es una solución de un ácido débil y
Equilibrio Acido-Base. Dr Jorge Brenes Dittel. Nefrología.
 Equilibrio Acido-Base Dr Jorge Brenes Dittel. Nefrología. Equilibrio Acido-base. Fisiología ph es el logaritmo de la concentracíon del ión hidrogenion expresada en milimoles por litro. [H+] en sangre es
Equilibrio Acido-Base Dr Jorge Brenes Dittel. Nefrología. Equilibrio Acido-base. Fisiología ph es el logaritmo de la concentracíon del ión hidrogenion expresada en milimoles por litro. [H+] en sangre es
1.- FOSFATO MONOSUSTITUIDO/FOSFATO DISUSTITUIDO (H2PO4 - /HPO4 = )
 1. FOSFATO MONOSUSTITUIDO/FOSFATO DISUSTITUIDO (H2PO4 /HPO4 = ) El ácido fosfórico (H 3 PO 4 ), además de formar parte de numerosos compuestos orgánicos (ácidos nucleicos, fosfolípidos, azúcares, etc.)
1. FOSFATO MONOSUSTITUIDO/FOSFATO DISUSTITUIDO (H2PO4 /HPO4 = ) El ácido fosfórico (H 3 PO 4 ), además de formar parte de numerosos compuestos orgánicos (ácidos nucleicos, fosfolípidos, azúcares, etc.)
LA MATERIA VIVA Y EL AGUA
 Página 1 de 11 LA MATERIA VIVA Y EL AGUA Haga clic en la respuesta correcta. Mostrar las preguntas individualmente 1. Tipo C. Siempre se produce una variación en el ph de una disolución reguladora si simultáneamente
Página 1 de 11 LA MATERIA VIVA Y EL AGUA Haga clic en la respuesta correcta. Mostrar las preguntas individualmente 1. Tipo C. Siempre se produce una variación en el ph de una disolución reguladora si simultáneamente
METABOLISMO ACIDO / BASE
 METABOLISMO ACIDO / BASE Dr Sergio Octavio GRANADOS TINAJERO Hospital Angeles de Villahermosa, Villahermosa, Tabasco, México. Course : 3 Year : 2003 Language : Spanish Country : Mexico City : Baja California
METABOLISMO ACIDO / BASE Dr Sergio Octavio GRANADOS TINAJERO Hospital Angeles de Villahermosa, Villahermosa, Tabasco, México. Course : 3 Year : 2003 Language : Spanish Country : Mexico City : Baja California
Líquidos corporales Compartimiento Equilibrio de líquidos. Q.F. Adriana Cordero
 Líquidos corporales Compartimiento Equilibrio de líquidos Q.F. Adriana Cordero INTRODUCCIÒN El agua y los solutos disueltos en cada uno de los compartimentos corporales de fluidos constituyen los líquidos
Líquidos corporales Compartimiento Equilibrio de líquidos Q.F. Adriana Cordero INTRODUCCIÒN El agua y los solutos disueltos en cada uno de los compartimentos corporales de fluidos constituyen los líquidos
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM. ACIDOS Y BASES, ph, BUFFERS
 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM ACIDOS Y BASES, ph, BUFFERS Ionización del agua y producto iónico del agua (K w ) H 2 O H + + OH - K eq = [H + ][OH - ] [H 2 O] K eq = [H + ][OH - ] [H 2 O] K eq
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM ACIDOS Y BASES, ph, BUFFERS Ionización del agua y producto iónico del agua (K w ) H 2 O H + + OH - K eq = [H + ][OH - ] [H 2 O] K eq = [H + ][OH - ] [H 2 O] K eq
Agua, electrolitos, balance acido-base. Dra. Luz E. Cuevas-Molina NURS 1231
 Agua, electrolitos, balance acido-base Dra. Luz E. Cuevas-Molina NURS 1231 1 Introducción Para mantener la homoestasis debe haber un balance entre las cantidades de fluido y electrolitos Los electrolitos
Agua, electrolitos, balance acido-base Dra. Luz E. Cuevas-Molina NURS 1231 1 Introducción Para mantener la homoestasis debe haber un balance entre las cantidades de fluido y electrolitos Los electrolitos
Dra. Carmen Aída Martínez
 Dra. Carmen Aída Martínez Hemoproteínas Más abundantes en el ser humano. Función de almacenamiento y transporte de oxigeno. Valores normales: Hombres: 13 18 gr/dl Mujeres: 12-16 gr/dl Globina ESTRUCTURA
Dra. Carmen Aída Martínez Hemoproteínas Más abundantes en el ser humano. Función de almacenamiento y transporte de oxigeno. Valores normales: Hombres: 13 18 gr/dl Mujeres: 12-16 gr/dl Globina ESTRUCTURA
BIOQUIMICA CLINICA II
 Universidad Autónoma de Chiapas Facultad de Ciencias Químicas Campus IV BIOQUIMICA CLINICA II UNIDAD 5 EQUILIBRIO ACIDO-BASE TITULAR DEL CURSO : M.C. CONSUELO CHANG RUEDA CICLO ENERO - DICIEMBRE - 2015
Universidad Autónoma de Chiapas Facultad de Ciencias Químicas Campus IV BIOQUIMICA CLINICA II UNIDAD 5 EQUILIBRIO ACIDO-BASE TITULAR DEL CURSO : M.C. CONSUELO CHANG RUEDA CICLO ENERO - DICIEMBRE - 2015
El CO2, en presencia de anhidrasa carbónica (AC), se hidrata de la siguiente forma: CO2 + H2O <------> CO3H2 < > H+ + HCO3-
 Equilibro Acido Base El equilibrio ácido-base requiere la integración de tres sistemas orgánicos, el hígado, los pulmones y el riñón. En resumen, el hígado metaboliza las proteínas produciendo iones hidrógeno
Equilibro Acido Base El equilibrio ácido-base requiere la integración de tres sistemas orgánicos, el hígado, los pulmones y el riñón. En resumen, el hígado metaboliza las proteínas produciendo iones hidrógeno
FISICA QUIMICA
 FISICA QUIMICA 2018-1 DESARROLLO DE LA TEORIA DE LA DISOCIACION ELECTROLITICA. CONDUCCION DE LA ELECTRICIDAD. CONDUCCION ELECTROLITICA. ELECTROLISIS SOLUCIONES Se trata de un caso particular de dispersiones.
FISICA QUIMICA 2018-1 DESARROLLO DE LA TEORIA DE LA DISOCIACION ELECTROLITICA. CONDUCCION DE LA ELECTRICIDAD. CONDUCCION ELECTROLITICA. ELECTROLISIS SOLUCIONES Se trata de un caso particular de dispersiones.
SESION DE APRENDIZAJE N 1 GENERALIDADES
 SESION DE APRENDIZAJE N 1 GENERALIDADES El término Fisiología proviene etimológicamente de dos voces griegas: Physis=naturaleza y logos= estudio. Es la ciencia que estudia las funciones de los seres vivos.
SESION DE APRENDIZAJE N 1 GENERALIDADES El término Fisiología proviene etimológicamente de dos voces griegas: Physis=naturaleza y logos= estudio. Es la ciencia que estudia las funciones de los seres vivos.
PROPÓSITO DE MEDIR LOS GASES ARTERIALES
 FISIOLOGÍA DE GASES ARTERIALES La primera parte de este módulo comprende elementos básicos sobre la fisiología de los gases arteriales. Este módulo ayudará a los profesionales de la enfermería y cardiorrespiratorios
FISIOLOGÍA DE GASES ARTERIALES La primera parte de este módulo comprende elementos básicos sobre la fisiología de los gases arteriales. Este módulo ayudará a los profesionales de la enfermería y cardiorrespiratorios
SOLUCIONES AMORTIGUADORAS ELABORADO POR: LIC. RAUL HERNANDEZ MAZARIEGOS. 3. Cuál es la función de un ácido débil en una solución reguladora:
 GUIA DE ESTUDIO SOLUCIONES AMORTIGUADORAS ELABORADO POR: LIC. RAUL HERNANDEZ MAZARIEGOS 1. Defina solución tampón o solución reguladora: 2. De qué componentes está formada una solución tampón:. Cuál es
GUIA DE ESTUDIO SOLUCIONES AMORTIGUADORAS ELABORADO POR: LIC. RAUL HERNANDEZ MAZARIEGOS 1. Defina solución tampón o solución reguladora: 2. De qué componentes está formada una solución tampón:. Cuál es
Trabajo Práctico N o 2 BUFFERS BIOLÓGICOS
 1 Trabajo Práctico N o 2 BUFFERS BIOLÓGICOS OBJETIVOS A partir de la ecuación de HendersonHasselbach calcular la concentración de (H + ),(Aceptor de H + ) o (Dador de H + ). Conocer cómo se mantiene el
1 Trabajo Práctico N o 2 BUFFERS BIOLÓGICOS OBJETIVOS A partir de la ecuación de HendersonHasselbach calcular la concentración de (H + ),(Aceptor de H + ) o (Dador de H + ). Conocer cómo se mantiene el
EDUCATIVO. Alteraciones del. - Departamento de Fisiopatología - Facultad de Medicina 2011MATERIAL. Dr MSc José Boggia
 - Departamento de Fisiopatología - Facultad de Medicina Alteraciones del equilibrio i ácido-base 2011 Dr MSc José Boggia PANORAMICA GLOBAL I. Recordatorio de la fisiología ácido-base II. Diagnóstico de
- Departamento de Fisiopatología - Facultad de Medicina Alteraciones del equilibrio i ácido-base 2011 Dr MSc José Boggia PANORAMICA GLOBAL I. Recordatorio de la fisiología ácido-base II. Diagnóstico de
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA CICLO ACADÉMICO 2,009
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Equilibrio AcidoAcido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Equilibrio AcidoAcido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO:
 REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO: - FISIOLOGÍA DE ÁCIDOS Y BASES - EXCRECIÓN RENAL DE H + Miryam Romero R. MSc. PhD. Profesora de Fisiología Departamento de Ciencias Fisiológicas Universidad del Valle
REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO: - FISIOLOGÍA DE ÁCIDOS Y BASES - EXCRECIÓN RENAL DE H + Miryam Romero R. MSc. PhD. Profesora de Fisiología Departamento de Ciencias Fisiológicas Universidad del Valle
Reconociendo al Sistema Respiratorio como un eliminador de desechos
 Reconociendo al Sistema Respiratorio como un eliminador de desechos INTRODUCCIÓN Como sabemos el cuerpo humano produce muchos desechos, por esto nuestros sistemas están encargados de eliminarlos, pero
Reconociendo al Sistema Respiratorio como un eliminador de desechos INTRODUCCIÓN Como sabemos el cuerpo humano produce muchos desechos, por esto nuestros sistemas están encargados de eliminarlos, pero
Agua en el cuerpo: líquido intracelular y extracelular
 KILO POR KILO, EL CUERPO contiene más agua que cualquier otro componente. Después del oxígeno, el agua es el ingrediente más importante para la vida; sin ella, los procesos biológicos, y la vida, cesan
KILO POR KILO, EL CUERPO contiene más agua que cualquier otro componente. Después del oxígeno, el agua es el ingrediente más importante para la vida; sin ella, los procesos biológicos, y la vida, cesan
Reacciones ácido-base
 Reacciones ácido-base 1 Brønsted-Lowry (1923) Ácido: Especie que tiene tendencia a ceder un H + Base: Especie que tiene tendencia a aceptar un H + CH 3 COOH (aq) + H 2 O (l) H 3 O + (aq) + CH 3 COO (aq)
Reacciones ácido-base 1 Brønsted-Lowry (1923) Ácido: Especie que tiene tendencia a ceder un H + Base: Especie que tiene tendencia a aceptar un H + CH 3 COOH (aq) + H 2 O (l) H 3 O + (aq) + CH 3 COO (aq)
GUIA DE ESTUDIO SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por: Licda. Edda García
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2015 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2015 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
Control del Equilibrio ácido-base
 Control del Equilibrio ácido-base Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia
Control del Equilibrio ácido-base Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia
GUIAS DE LABORATORIO DE BIOQUIMICA BASICA FACULTAD DE SALUD PROGRAMA DE ENFERMERIA Docente: MANUEL ANDRES GIRALDO JACOBO
 LABORATORIO N 5 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO Tiempo de práctica: 2 horas MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Objetivos 1. Al finalizar la práctica,
LABORATORIO N 5 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO Tiempo de práctica: 2 horas MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Objetivos 1. Al finalizar la práctica,
Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales. Verónica Pantoja. Lic. MSP.
 Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales Professor: Kinesiologia Verónica Pantoja. Lic. MSP. 1.Precipitadas Formando estructuras sólidas, insolubles, con función esquelética.
Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales Professor: Kinesiologia Verónica Pantoja. Lic. MSP. 1.Precipitadas Formando estructuras sólidas, insolubles, con función esquelética.
1.1. BIOLEMENTOS: Concepto: Son los elementos químicos que constituyen los seres vivos. Clasificación: * Primarios (~ 96%): C, H, O, N, P, S.
 1.1. BIOLEMENTOS: Concepto: Son los elementos químicos que constituyen los seres vivos. Clasificación: Biogénicos * Primarios (~ 96%): C, H, O, N, P, S. * Secundarios (~ 3,9%) :Na +, K +, Ca ++, Mg ++,
1.1. BIOLEMENTOS: Concepto: Son los elementos químicos que constituyen los seres vivos. Clasificación: Biogénicos * Primarios (~ 96%): C, H, O, N, P, S. * Secundarios (~ 3,9%) :Na +, K +, Ca ++, Mg ++,
Fisiopatología del Equilibrio Ácido-Base ACIDOSIS
 Fisiopatología del Equilibrio Ácido-Base ACIDOSIS Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: I. ACIDOSIS:
Fisiopatología del Equilibrio Ácido-Base ACIDOSIS Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: I. ACIDOSIS:
La Bioquímica y los Bioelementos. 1.Los elementos de la vida 2.Las biomoléculas 3.El agua 4.Las sales minerales
 La Bioquímica y los Bioelementos 1.Los elementos de la vida 2.Las biomoléculas 3.El agua 4.Las sales minerales LOS ELEMENTOS DE LA VIDA Los ss.vv. (seres vivos) están constituidos por materia y, por
La Bioquímica y los Bioelementos 1.Los elementos de la vida 2.Las biomoléculas 3.El agua 4.Las sales minerales LOS ELEMENTOS DE LA VIDA Los ss.vv. (seres vivos) están constituidos por materia y, por
TEMA 1: LA NATURALEZA BÁSICA DE LA MATERIA QUÉ ELEMENTOS INTEGRAN LA MATERIA VIVA?
 TEMA 1: LA NATURALEZA BÁSICA DE LA MATERIA QUÉ ELEMENTOS INTEGRAN LA MATERIA VIVA? Concepto de Bioquímica Concepto de Bioelemento Los bioelementos, también conocidos como elementos biogénicos, son los
TEMA 1: LA NATURALEZA BÁSICA DE LA MATERIA QUÉ ELEMENTOS INTEGRAN LA MATERIA VIVA? Concepto de Bioquímica Concepto de Bioelemento Los bioelementos, también conocidos como elementos biogénicos, son los
GUIAS DE LABORATORIO DE BIOQUIMICA BASICA FACULTAD DE SALUD PROGRAMA DE ENFERMERIA Docente: MANUEL ANDRES GIRALDO JACOBO LABORATORIO N 7
 LABORATORIO N 7 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Tiempo de práctica: 2 horas Integrantes: INTRODUCCIÓN Dentro de los
LABORATORIO N 7 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Tiempo de práctica: 2 horas Integrantes: INTRODUCCIÓN Dentro de los
Escala de ph. Concentración de H + en Eq/L
 Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia capaz de aceptar un H + ÁCIDO: sustancia
Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia capaz de aceptar un H + ÁCIDO: sustancia
LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER
 LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER 1.- INTRODUCCIÓN Soluciones Ácido-Base Los solutos disueltos en agua pueden clasificarse como electrolitos y no electrolitos en función de su capacidad de
LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER 1.- INTRODUCCIÓN Soluciones Ácido-Base Los solutos disueltos en agua pueden clasificarse como electrolitos y no electrolitos en función de su capacidad de
Como transportamos el Oxigeno a los tejidos. A través de proteínas asociadas a metales de transición como el hierro y el cobre.
 Como transportamos el Oxigeno a los tejidos A través de proteínas asociadas a metales de transición como el hierro y el cobre. Grupo Hemo Los anillos pirrol tiene puentes a-metileno y grupos M, V, M,
Como transportamos el Oxigeno a los tejidos A través de proteínas asociadas a metales de transición como el hierro y el cobre. Grupo Hemo Los anillos pirrol tiene puentes a-metileno y grupos M, V, M,
Guía soluciones acuosas
 UNIVERSIDAD N LA REPUBLICA Nombre del Estudiante: Guía soluciones acuosas Carrera Asignatura Nivel Enfermería Bioquímica Segundo Nivel Semestre 2 semestre Año 2016 Docente Dr. Patricio Muñoz Torres Puntaje
UNIVERSIDAD N LA REPUBLICA Nombre del Estudiante: Guía soluciones acuosas Carrera Asignatura Nivel Enfermería Bioquímica Segundo Nivel Semestre 2 semestre Año 2016 Docente Dr. Patricio Muñoz Torres Puntaje
5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS Para realizar estos problemas se aconseja consultar una tabla con las
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS Para realizar estos problemas se aconseja consultar una tabla con las
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS
 UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. LABORATORIO DE BIOQUÍMICA CLÍNICA (CLAVE 1807) Licenciatura de QFB
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA LABORATORIO DE BIOQUÍMICA CLÍNICA (CLAVE 1807) Licenciatura de QFB Laura Carmona Salazar Rosalinda Velázquez Salgado 2017-II Este material es exclusivamente
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA LABORATORIO DE BIOQUÍMICA CLÍNICA (CLAVE 1807) Licenciatura de QFB Laura Carmona Salazar Rosalinda Velázquez Salgado 2017-II Este material es exclusivamente
Tema 5 Estructura cuaternaria de proteínas
 Tema 5 Estructura cuaternaria de proteínas Estructura y función de la Hemoglobina Unión de la Hemoglobina a ligandos Curva unión O 2 a la Hemoglobina Efectores alostéricos Efecto del ph sobre la saturación
Tema 5 Estructura cuaternaria de proteínas Estructura y función de la Hemoglobina Unión de la Hemoglobina a ligandos Curva unión O 2 a la Hemoglobina Efectores alostéricos Efecto del ph sobre la saturación
Concepto de ph. Bases
 Concepto de ph El concepto de ph nace de dos tipos de especies químicas llamadas ácidos y bases, las que se pueden clasificar como tal y predecir su potencia o fuerza de acuerdo al valor de su ph. Características
Concepto de ph El concepto de ph nace de dos tipos de especies químicas llamadas ácidos y bases, las que se pueden clasificar como tal y predecir su potencia o fuerza de acuerdo al valor de su ph. Características
Fisiopatología Del Equilibrio Ácido-Base Alcalosis
 Fisiopatología Del Equilibrio Ácido-Base Alcalosis Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: II. ALCALOSIS
Fisiopatología Del Equilibrio Ácido-Base Alcalosis Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: II. ALCALOSIS
Sistema Integrado de Gestión
 Sistema Integrado de Gestión GUÍA PRÁCTICA N 52 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Versión 1 Proceso: Investigación -
Sistema Integrado de Gestión GUÍA PRÁCTICA N 52 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Versión 1 Proceso: Investigación -
GUIAS DE ESTUDIO PARA QUINTO PARCIAL DE TEORIA
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS 2017 CIENCIAS BASICAS Y BIOLOGICAS U.D. BIOQUIMICA SEGUNDO AÑO GUIAS DE ESTUDIO PARA QUINTO PARCIAL DE TEORIA GUIA DE ESTUDIO No. 27:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS 2017 CIENCIAS BASICAS Y BIOLOGICAS U.D. BIOQUIMICA SEGUNDO AÑO GUIAS DE ESTUDIO PARA QUINTO PARCIAL DE TEORIA GUIA DE ESTUDIO No. 27:
Entendiéndose como ph, el grado de acides o alcalinidad relativa de una solución.
 Fisiolología normal Medio interno medio líquido donde vive y se desarrolla la célula líquido extracelular (E.C). Composición química más o menos permanente. Las substancias que lo componen están en concentraciones
Fisiolología normal Medio interno medio líquido donde vive y se desarrolla la célula líquido extracelular (E.C). Composición química más o menos permanente. Las substancias que lo componen están en concentraciones
Química III Soluciones reguladoras. Ing. Esp. Fanny E. Molina S.
 Química III Soluciones reguladoras Ing. Esp. Fanny E. Molina S. 1 Soluciones Reguladoras 1. Definición de soluciones reguladoras 2. Importancia de las soluciones reguladoras 3. Cuidados 4. Preparación
Química III Soluciones reguladoras Ing. Esp. Fanny E. Molina S. 1 Soluciones Reguladoras 1. Definición de soluciones reguladoras 2. Importancia de las soluciones reguladoras 3. Cuidados 4. Preparación
TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE
 TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE ALTERACIONES ACIDO-BASE Los ácidos son producidos en forma continua, durante el metabolismo normal La concentración de hidrógeno en el LEC se mantiene en un
TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE ALTERACIONES ACIDO-BASE Los ácidos son producidos en forma continua, durante el metabolismo normal La concentración de hidrógeno en el LEC se mantiene en un
UD 8. Aplicaciones de los equilibrios ácido-base
 UD 8. Aplicaciones de los equilibrios ácido-base 8.1 Efecto del ion común. 8.2 Disoluciones reguladoras del ph. 8.3 Sistemas reguladores biológicos. 8.4 Valoraciones ácido-base. 8.5 Indicadores ácido-base.
UD 8. Aplicaciones de los equilibrios ácido-base 8.1 Efecto del ion común. 8.2 Disoluciones reguladoras del ph. 8.3 Sistemas reguladores biológicos. 8.4 Valoraciones ácido-base. 8.5 Indicadores ácido-base.
Tema 2. El agua, el ph y los equilibrios iónicos
 Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
TEMA 3. FUNCIÓN TUBULAR (II). EQUILIBRIO DEL AGUA. EQUILIBRIO ÁCIDO- BÁSICO
 TEMA 3. FUNCIÓN TUBULAR (II). EQUILIBRIO DEL AGUA. EQUILIBRIO ÁCIDO- BÁSICO Equilibrio del agua. Resorción de agua en túbulo proximal y en asa de Henle. Mecanismos de concentración y de dilución de la
TEMA 3. FUNCIÓN TUBULAR (II). EQUILIBRIO DEL AGUA. EQUILIBRIO ÁCIDO- BÁSICO Equilibrio del agua. Resorción de agua en túbulo proximal y en asa de Henle. Mecanismos de concentración y de dilución de la
Consecuencias estructurales del descenso del Fe(II): Curvas de saturación y Efectos modificadores.
 Consecuencias estructurales del descenso del Fe(II): Curvas de saturación y Efectos modificadores. Vamos a estudiar las curvas de afinidad de la mioglobina y de la hemoglobina frente al oxígeno, así como
Consecuencias estructurales del descenso del Fe(II): Curvas de saturación y Efectos modificadores. Vamos a estudiar las curvas de afinidad de la mioglobina y de la hemoglobina frente al oxígeno, así como
INSTITUTO POLITÉCNICO NACIONAL ESCUELA NACIONAL DE MEDICINA Y HOMEOPATÍA REGULACION DEL EQUILIBRIO ACIDO- BASICO
 INSTITUTO POLITÉCNICO NACIONAL ESCUELA NACIONAL DE MEDICINA Y HOMEOPATÍA Medicina y Homeopatía Bioquímica Practica 4 REGULACION DEL EQUILIBRIO ACIDO- BASICO Profesor: Candelas Villagómez Daniel Integrantes:
INSTITUTO POLITÉCNICO NACIONAL ESCUELA NACIONAL DE MEDICINA Y HOMEOPATÍA Medicina y Homeopatía Bioquímica Practica 4 REGULACION DEL EQUILIBRIO ACIDO- BASICO Profesor: Candelas Villagómez Daniel Integrantes:
Regulación de (H+) Equilibrio ácido-básico
 Regulación de (H+) Equilibrio ácido-básico Introducción v CO2 es generado dentro de las células à Forma H2CO3 (ácido carbónico) al disolverse en agua Introducción ácidos no volátiles v Ácidos no volátiles:
Regulación de (H+) Equilibrio ácido-básico Introducción v CO2 es generado dentro de las células à Forma H2CO3 (ácido carbónico) al disolverse en agua Introducción ácidos no volátiles v Ácidos no volátiles:
La Composición del medio que rodea a las células debe permanecer constante: (HOMEOSTASIS) y entre límites compatibles con las reacciones vitales
 pulmones Tracto Gastrointestinal FLUIDOS INTRA- Y EXTRA-CELULARES Al pasar por los pulmones el CO2 sale y entra O2 a la sangre nutrientes Nutrientes y O2 entran a cls Deshechos y CO2 salen de las cls Los
pulmones Tracto Gastrointestinal FLUIDOS INTRA- Y EXTRA-CELULARES Al pasar por los pulmones el CO2 sale y entra O2 a la sangre nutrientes Nutrientes y O2 entran a cls Deshechos y CO2 salen de las cls Los
INTRODUCCIÓN A LA BIOQUÍMICA
 INTRODUCCIÓN A LA BIOQUÍMICA HISTORIA Y ACTUALIDAD DE LA BIOQUÍMICA HISTORIA Y ACTUALIDAD DE LA BIOQUÍMICA HISTORIA Y ACTUALIDAD DE LA BIOQUÍMICA CONCEPTO DE BIOQUÍMICA DIVISIÓN DE LA BIOQUÍMICA COMPOSICIÓN
INTRODUCCIÓN A LA BIOQUÍMICA HISTORIA Y ACTUALIDAD DE LA BIOQUÍMICA HISTORIA Y ACTUALIDAD DE LA BIOQUÍMICA HISTORIA Y ACTUALIDAD DE LA BIOQUÍMICA CONCEPTO DE BIOQUÍMICA DIVISIÓN DE LA BIOQUÍMICA COMPOSICIÓN
CARRERA DE MEDICINA GUÍA DE PRÁCTICA DE LABORATORIO
 ASIGNATURA: BIOQUÍMICA CICLO: SEGUNDO SEMESTRE: A 2014 ÁREA: CIENCIAS MORFOFUNCIONALES MALLA: 6 NÚMERO HORAS SEMANALES DE LA PRÁCTICA: 4 NIVEL CURRICULAR: BÁSICO (CIENCIAS BÁSICAS) LABORATORIO: BIOQUÍMICA
ASIGNATURA: BIOQUÍMICA CICLO: SEGUNDO SEMESTRE: A 2014 ÁREA: CIENCIAS MORFOFUNCIONALES MALLA: 6 NÚMERO HORAS SEMANALES DE LA PRÁCTICA: 4 NIVEL CURRICULAR: BÁSICO (CIENCIAS BÁSICAS) LABORATORIO: BIOQUÍMICA
[A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x
![[A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x [A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x](/thumbs/55/35730009.jpg) Una reacción enzimática transcurre en 10 ml de una disolución cuya concentración total de citrato es 120 mm y su ph inicial es de 7. Durante la reacción se producen 0.2 miliequivalentes de un ácido. Calcular
Una reacción enzimática transcurre en 10 ml de una disolución cuya concentración total de citrato es 120 mm y su ph inicial es de 7. Durante la reacción se producen 0.2 miliequivalentes de un ácido. Calcular
INDICE Parte 2. Pág 8.4 LOS AMORTIGUADORES FISIOLOGICOS
 Capítulo 8 Parte 2/4 8.4 LOS AMORTIGUADORES FISIOLOGICOS Los sistemas buffers que hay en la sangre y en el extracelular ya fueron señalados en la Tabla 8.III. Los analizaremos uno por uno: a) Bicarbonato
Capítulo 8 Parte 2/4 8.4 LOS AMORTIGUADORES FISIOLOGICOS Los sistemas buffers que hay en la sangre y en el extracelular ya fueron señalados en la Tabla 8.III. Los analizaremos uno por uno: a) Bicarbonato
Equipo 5 Sistemas amortiguadores
 Equipo 5 Sistemas amortiguadores Anaya Gutiérrez Erick Jesús García García Esmira Jazmin García Montesinos Ana Paola Gonzales Galindo Jesús Antonio Jóse Ruíz Diego Mendez Silva Clara Anaid Yépez Cancino
Equipo 5 Sistemas amortiguadores Anaya Gutiérrez Erick Jesús García García Esmira Jazmin García Montesinos Ana Paola Gonzales Galindo Jesús Antonio Jóse Ruíz Diego Mendez Silva Clara Anaid Yépez Cancino
FUNCIÓN CIRCULATORIA Y EXCRETORA TEMA 4
 FUNCIÓN CIRCULATORIA Y EXCRETORA TEMA 4 EL MEDIO INTERNO Los organismos unicelulares toman los nutrientes del medio y eliminan los productos de desecho a través de su membrana. Los organismos pluricelulares
FUNCIÓN CIRCULATORIA Y EXCRETORA TEMA 4 EL MEDIO INTERNO Los organismos unicelulares toman los nutrientes del medio y eliminan los productos de desecho a través de su membrana. Los organismos pluricelulares
Para resolver ésta guía deberá leer el tema en el Capítulo 10 del libro de texto.
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2016 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2016 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
UNIDAD 2_2 BIOELEMENTOS Y BIOMOLÉCULAS INORGÁNICAS: SALES MINERALES
 UNIDAD 2_2 BIOELEMENTOS Y BIOMOLÉCULAS INORGÁNICAS: SALES MINERALES Bloque 1. La base molecular y fisicoquímica de la vida. Contenidos Contenidos y criterios de evaluación Biología. 2.º Bachillerato 1.
UNIDAD 2_2 BIOELEMENTOS Y BIOMOLÉCULAS INORGÁNICAS: SALES MINERALES Bloque 1. La base molecular y fisicoquímica de la vida. Contenidos Contenidos y criterios de evaluación Biología. 2.º Bachillerato 1.
DISOLUCIONES Y AMINOÁCIDOS
 DISOLUCIONES Y AMINOÁCIDOS EQUILIBRIO QUIMICO Las reacciones reversibles son aquellas en las que los reactivos no se transforman totalmente en productos, ya que éstos vuelven a formar los reactivos, dando
DISOLUCIONES Y AMINOÁCIDOS EQUILIBRIO QUIMICO Las reacciones reversibles son aquellas en las que los reactivos no se transforman totalmente en productos, ya que éstos vuelven a formar los reactivos, dando
Sangre: Composición celular y plasmática Principales electrolitos Macro y microelementos. Proteínas, glúcidos, lípidos y lipoproteínas.
 Sangre: Composición celular y plasmática Principales electrolitos Macro y microelementos. Proteínas, glúcidos, lípidos y lipoproteínas. Nitrógeno no proteico, cetonas, enzimas plasmáticas. Respuestas fisiológicas
Sangre: Composición celular y plasmática Principales electrolitos Macro y microelementos. Proteínas, glúcidos, lípidos y lipoproteínas. Nitrógeno no proteico, cetonas, enzimas plasmáticas. Respuestas fisiológicas
SGUICEL009QM11-A16V1. Ácido base I: conceptos y teorías
 SGUICEL009QM11-A16V1 Ácido base I: conceptos y teorías Ítem Alternativa Habilidad 1 B Reconocimiento 2 A Comprensión 3 E Reconocimiento 4 E Comprensión 5 E ASE 6 E Comprensión 7 D Comprensión 8 E Comprensión
SGUICEL009QM11-A16V1 Ácido base I: conceptos y teorías Ítem Alternativa Habilidad 1 B Reconocimiento 2 A Comprensión 3 E Reconocimiento 4 E Comprensión 5 E ASE 6 E Comprensión 7 D Comprensión 8 E Comprensión
Organización Funcional y el Medio Interno
 Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
MATERIA DE HEMATOLOGIA UNIDAD 1: COMPOSICION DE LA SANGRE
 MATERIA DE HEMATOLOGIA UNIDAD 1: COMPOSICION DE LA SANGRE TITULAR DE LA MATERIA: DRA. CONSUELO CHANG RUEDA CICLO: ENERO - DICIEMBRE 2016 DRA EN C. CONSUELO CHANG RUEDA 1 UNIDADES I.- COMPOSICION DE LA
MATERIA DE HEMATOLOGIA UNIDAD 1: COMPOSICION DE LA SANGRE TITULAR DE LA MATERIA: DRA. CONSUELO CHANG RUEDA CICLO: ENERO - DICIEMBRE 2016 DRA EN C. CONSUELO CHANG RUEDA 1 UNIDADES I.- COMPOSICION DE LA
REACCIONES DE TRANSFERENCIA DE PROTONES ELECTROLITOS
 REACCIONES DE TRANSFERENCIA DE PROTONES CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA ELECTROLITOS Un electrolito es una sustancia que al disolverse en agua experimenta una disociación (o ionización) total
REACCIONES DE TRANSFERENCIA DE PROTONES CURSO: 2º DE BACHILLERATO ASIGNATURA: QUÍMICA ELECTROLITOS Un electrolito es una sustancia que al disolverse en agua experimenta una disociación (o ionización) total
Bases Científicas 1 Autor: Marta Adonis
 ACIDO-BASE En los organismos vivos la concentración de protones debe mantenerse dentro de límites muy estrechos, como requisito indispensable para el desarrollo normal de los procesos metabólicos intracelulares.
ACIDO-BASE En los organismos vivos la concentración de protones debe mantenerse dentro de límites muy estrechos, como requisito indispensable para el desarrollo normal de los procesos metabólicos intracelulares.
Profesor(a): C.D. María Isabel Pérez Aguilar
 Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
GENERALIDADES DEL SISTEMA RESPIRATORIO
 GENERALIDADES DEL SISTEMA RESPIRATORIO MCs. Gonzalo Tiznado M. Instituto de Anatomía, Histología y Patología Facultad de Medicina Los pulmones están diseñado para el intercambio gaseoso entre el medio
GENERALIDADES DEL SISTEMA RESPIRATORIO MCs. Gonzalo Tiznado M. Instituto de Anatomía, Histología y Patología Facultad de Medicina Los pulmones están diseñado para el intercambio gaseoso entre el medio
BIOQUÍMICA DE LA CÉLULA BIOL 4545
 BIOQUÍMICA DE LA CÉLULA BIOL 4545 EXPECTATIVAS: Que usted espera aprender en esta clase? BIOQUÍMICA DE LA CÉLULA BIOL 4545 AGUA Y ph 11.08.2014 OBJETIVOS DE APRENDIZAJE: Apreciar la importancia del agua
BIOQUÍMICA DE LA CÉLULA BIOL 4545 EXPECTATIVAS: Que usted espera aprender en esta clase? BIOQUÍMICA DE LA CÉLULA BIOL 4545 AGUA Y ph 11.08.2014 OBJETIVOS DE APRENDIZAJE: Apreciar la importancia del agua
Tema 1. Introducción
 Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Introducción histórica
 Introducción histórica Ácidos y bases se conocen desde la antigüedad. Robert Boyle (s. XVII) propiedades de los ácidos. Primera descripción sistemática de las Lavoisier (1743 1794) Primera teoría sobre
Introducción histórica Ácidos y bases se conocen desde la antigüedad. Robert Boyle (s. XVII) propiedades de los ácidos. Primera descripción sistemática de las Lavoisier (1743 1794) Primera teoría sobre
Soluciones acuosas. Importancia del agua. Patricio Muñoz Torres n Lugar donde se inició y ocurre la vida.
 Soluciones acuosas Patricio Muñoz Torres patricio.munozt@gmail.com Importancia del agua n Lugar donde se inició y ocurre la vida. n Diversas propiedades como disolvente, debido a su cohesión interna. n
Soluciones acuosas Patricio Muñoz Torres patricio.munozt@gmail.com Importancia del agua n Lugar donde se inició y ocurre la vida. n Diversas propiedades como disolvente, debido a su cohesión interna. n
TALLER DE ANALISIS DE GASES ARTERIALES
 TALLER DE ANALISIS DE GASES ARTERIALES Dr. Menfil A Orellana-Barrios Medicina Interna Cursos Precongreso Congreso de Residentes 2012 HGSJDD www.drmenfilorellana.wordpress.com Para qué se utilizan los Gases
TALLER DE ANALISIS DE GASES ARTERIALES Dr. Menfil A Orellana-Barrios Medicina Interna Cursos Precongreso Congreso de Residentes 2012 HGSJDD www.drmenfilorellana.wordpress.com Para qué se utilizan los Gases
Pauta de corrección guía IV medio Homeostasis
 Pauta de corrección guía IV medio Homeostasis Actividad 1.- Registra la temperatura ambiental en un día cada una hora. Así mismo registra la temperatura corporal que tu cuerpo tiene en cada hora. Grafica
Pauta de corrección guía IV medio Homeostasis Actividad 1.- Registra la temperatura ambiental en un día cada una hora. Así mismo registra la temperatura corporal que tu cuerpo tiene en cada hora. Grafica
