UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA CICLO ACADÉMICO 2,009
|
|
|
- Rafael Acosta Navarro
- hace 7 años
- Vistas:
Transcripción
1 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Equilibrio AcidoAcido-Base Dr. Mynor A. Leiva Enríquez
2 Las moléculas de agua forman Dipolos. Forman puentes De hidrógeno. Tienen forma de tetraedro con acción nucleofílica hacia otras moléculas. H2O + H2O H3+ + OH-
3 Conceptos Generales Un Mol = Peso molecular (o atómico) de la sustancia, expresado en gramos. 23 Un Mol = 6.02 x 10 moléculas o átomos. 1 Mol de Hidrógeno = 1 gramo (porque su peso molecular es 1) 1 Mol de Oxígeno = 16 gramos (porque su peso molecular es 16) 1 Mol de agua (H2O) = 18 gramos (la suma de 16 del Oxígeno + 2 del Hidrógeno)
4 Conceptos Generales Se puede calcular el número de moléculas de agua que hay en un litro de volumen (la concentración), con la siguiente fórmula: [H2O]] = peso de la misma / peso molecular [H2O]] = 1 litro = 1000 gramos / 18 = 55.5 Moles / L. Para averiguar el número de moléculas de agua por litro, multiplicamos 55.5 x (6.02 x 10 ) 23
5
6 Formas ionizadas predominantes Ejemplo No disociada Disociada Ácido fuerte: ácido clorhídrico HCL H + + Cl - Base fuerte: hidróxido de sodio NaOH Na + + OH - Sales: Cloruro de Sodio NaCl Na + + Cl - Ácido débil: ácido carbónico H 2 CO 3 H + + HCO 3 - AGUA H 2 O Muy poco H + + OH -
7 Según el concepto de Bronsted-Lowry: Acido: sustancia capaz de donar un H+ Base: sustancia capaz de aceptar un H+ Plasma [H+] = 40 mmol/l ph = bicarbonato/acac carbónico Se reemplaza el ac carbónico por CO2 cuya [ ] es proporcional Relación HCO3/CO = 20/1 CO2
8 MECANISMOS DE REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE. 1) Los sistemas buffer de la sangre, líquidos orgánicos, células y las sales minerales de los huesos. 2) La excreción y retención de dióxido de carbono por los pulmones. 3) La excreción de una orina ácida o alcalina,, y 4) La formación y excreción de amoníaco o ácidos orgánicos.
9 Otros sistemas de amortiguación Na-proteína + HCL Na 2 HPO 4 + HCL 2KHbO 2 + H 2 SO 4 Na 2 CO 3 + H 2 CO 3 H Hb + KOH H-proteína + NaCl NaH 2 PO 4 2H HbO 2 2 (NaHCO 3) K Hb + H 2 O + NaCl + K 2 SO 4
10 Buffer de los líquidos orgánicos. Amortiguación estimada (%) de ácidos o álcalis fijos invasores Principales Buffers presentes Ubicación de depósitos de Buffers 40% En parte BHCO 3 En parte no determinados Células tisulares 30% BHCO 3 Líquidos extracelulares excepto sangre 13% 17% BHb y BhbO 2 BHCO 3 Sangre
11 Mecanismos de defensa 1) Sist buffer: Amortiguar compartimento e.c: - Bicarbonato/CO2 de sangre 75% de cap buffer 2) Sist. Respiratorio: regular eliminación o retención de CO2: pco2 40mmHg. Si la pco2 la ventilación alveolar
12 Función de los pulmones
13 Regulación respiratoria del ph sanguíneo Músculos respiratorios Centro Respiratorio Ventilación alveolar pco 2 Quimiorreceptores pco 2 ph po 2 Señales de la sangre
14
15 pco2 REGULACIÓN RENAL DEL EQUILIBRIO ACIDO-BASE CO 2 + H 2 O H 2 CO 3 a.c. ph H + + HCO 3 - Acidez Excreción Reabsorción titulable de amonio de HCO3-
16 3) Sist. Renal: Regula excreción de H+ - por reabsorción tubular de HCO3 filtrado en el glomérulo - por regeneración de bicarbonato gastado en la neutralización del ácido fijo, mediante la eliminación de H+. Para eliminar el exceso de H+ por la orina, se combina con tampones intratubulares: acidez titulable o como amonio
17 Ecuación de Henderson - Hasselbalch
18 Ecuación de Henderson - Hasselbalch
19 Ecuación de Henderson - Hasselbalch ph = log HCO x pco 2
20 Acidosis y Alcalosis Acidosis Metabólica: Cuando la alteración reduce la cifra de bicarbonato (el numerador). 2. Acidosis Respiratoria: Cuando la alteración eleva la cifra del CO2 disuelto (el denominador) Alcalosis Metabólica: Cuando la alteración eleva la cifra de bicarbonato. 2. Alcalosis Respiratoria: Cuando la alteración disminuye la cifra del CO2 disuelto. Bicarbonato ph = pk + log Ác. Carbónico
21 Acidosis Respiratoria Existe una hipoventilacion alveolar primaria pco2 >40 mmhg ph < 7.35 Alcalosis Respiratoria Existe una hiperventilacion alveolar primaria pco2 <40 mmhg ph > 7.45
22 Acidosis: Descompensada: cuando la cifra de ph es baja. Compensada: cuando la cifra de ph es normal, pero la cifra del CO2 total es aún anormal Alcalosis: Descompensada: cuando la cifra del ph es alta. Compensada: cuando la cifra de ph es normal, pero la cifra del CO2 total es aún anormal
23 Hallazgos de Laboratorio Estado ácido-base ph Urinario HCO 3 - plasmático H 2 CO 3 plasmático N O R M A L 6 a 7 24 a 28 meq/l 1.20 a 1.40 meq/l Acidosis Respiratoria Disminuye Aumenta Aumenta Alcalosis Respiratoria Aumenta Disminuye Disminuye Acidosis Metabólica Alcalosis Metabólica Disminuye Disminuye Disminuye Aumenta Aumenta Aumenta
24 Reserva Alcalina Total
25 La Anhidrasa carbónica cataliza la siguiente ecuación: CO2 + H2O H2CO3 H+ + HCO3 1-Producción contínua de ácidos fijos: meq / día de ácidos fijos metabolismo de aminoácidos meq / día de ácido volátil en forma de CO2
26 ACIDOSIS METABOLICA MECANISMOS DE PRODUCCIÓN: ingreso de ácidos fijos egreso de ácidos fijos Pérdidas de bicarbonato Mezcla de los factores anteriores
27 Anion Gap o Brecha Aniónica = (Na+) - (Cl-) + (HCO3-) VALOR NORMAL: 8-12 meq/l Causas de Acidosis Metabólica con BRECHA ANIÓNICA AUMENTADA Insuficiencia Renal Acidosis Láctica Cetoacidosis (diabética, alcohólica o de ayuno prolongado) Ingestión excesiva de salicilatos metanol o formaldehído etilenglicol paraldehído tolueno bebidas alcohólicas Citrato en Transfusiones Masivas
28 Trastornos del equilibrio ácido-base A c i d o s i s m e t a b ó l i c a Anión GAP: Na + - [Cl HCO 3 ] Cationes = Aniones K+ Mg++ Ca++ Globulinas Na + Otros aniones - HCO 3 Cl - GAP = 12 2 Sulfatos Fosfatos Lactatos Cetoácidos Otros ácidos orgánicos
29 Causas de Acidosis con Brecha Aniónica NORMAL Administración de ácidos Pérdidas de Bicarbonato Alteración de la Excresión renal de ácido. Hiperalimentación Administración de HCL Gastrointestinal Renal Con hipopotasemia Con hiperpotasemia Por HCL y/o Colestiramina En Alcalosis metabólica severa Diarrea Drenaje pancreático o biliar Ureterosigmoidostomía Acidosis tubular renal proximal Cetoacidosis (en el tx) Post hipocapnia crónica Acidosis tubular renal distal Acidosis tub. Renal distal hiperkaliémica Hipoaldosteronismo Perfusión renal reducida
30 ALCALOSIS METABOLICA MECANISMOS DE PRODUCCION: MECANISMOS: EJEMPLOS: 1. Contracción del espacio extracelular: vómitos diuréticos 2. Aumento del ingreso de bases: bicarbonato lactato citrato 3. Aumento de pérdidas de ácidos fijos: digestivas renales
31 D I A G N Ó S T I C O PARAMETROS EQ. AC-BASE: (medidos en sangre arterial) ph: pco 2 : 37 a 43 mm de Hg Bicarbonato: 23 a 25 meq/l CO 2 total: 26 a 28 mmoles/l Buffer Base: 45 a 50 meq/l Base Excess: 0 ± 3.0 meq/l Anion gap: 8 a 12 meq/l
32 PARÁMETROS SANGUÍNEOS DE UNA ACIDOSIS METABÓLICA Estado A-B ph pco2 HCO3 - real HCO3 - standard BE Trastorno puro Normal Negativo Trastorno compensado Negativo
33 PARÁMETROS SANGUÍNEOS DE UNA ALCALOSIS METABÓLICA Estado A-B ph pco2 HCO3 - HCO3 - BE real standard Trastorno puro Normal +++ Trastorno compensado ++
34 Manifestaciones Clínicas MANIFESTACIONES CLINICAS DE LA ALCALOSIS: La mayoría no presentan manifestaciones clínicas Musculares: Tetania Desplazamiento curva saturación de la Hb Metabólicas: activación de la glicólisis e inhibición del C. de Krebs, C. Pentosas y de la gluconeogénesis Depleción de potasio Hipercapnia
35 MANIFESTACIONES CLINICAS DE LA ACIDOSIS: No existe ningún signo clínico ni síntoma específico de la acidosis metabólica Estos dependen de la causa que la haya provocado
36 Manifestaciones clínicas: acidosis Signos sugerentes: Respiración de Kussmaul náuseas y vómitos alteraciones del estado mental, incluyendo coma En acidosis severa (ph< ) 7.15) hipotensión, por depresión de contractilidad cardiaca y vaso dilatación arterial suele existir hiperpotasemia
37 LLUVIOSO
38 H1N1 no se ha ido
Equilibrio Acido-Base
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,008 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,008 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
Equilibrio Acido-Base
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Conceptos
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Conceptos
Control del Equilibrio ácido-base
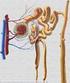 Control del Equilibrio ácido-base Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia
Control del Equilibrio ácido-base Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia
Escala de ph. Concentración de H + en Eq/L
 Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia capaz de aceptar un H + ÁCIDO: sustancia
Escala de ph ph Concentración de H + en Eq/L 1 0.1 2 0.01 3 0.001 4 0.0001 5 0.00001 6 0.000001 7 0.0000001 7.4 0.0000004 8 0.00000001 9 0.000000001 ÁLCALI: sustancia capaz de aceptar un H + ÁCIDO: sustancia
Equilibrio Ácido - Base
 Equilibrio Ácido - Base OBJETIVOS Comprender la importancia de mantener los valores de ph dentro del rango normal Analizar los diferentes mecanismos de regulación que permiten mantener el equilibrio ácido-base
Equilibrio Ácido - Base OBJETIVOS Comprender la importancia de mantener los valores de ph dentro del rango normal Analizar los diferentes mecanismos de regulación que permiten mantener el equilibrio ácido-base
EQUILIBRIO ÁCIDO-BASE
 EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
Actualización en Medio Interno Conceptos básicos
 Actualización en Medio Interno Conceptos básicos Bioquímica Lucrecia Drago Bioquímica M. Fernanda Pontoriero Ácidos Moléculas capaces de liberar H + HCl H + + Cl H 2 CO 3 H + + HCO 3 Bases Moléculas capaces
Actualización en Medio Interno Conceptos básicos Bioquímica Lucrecia Drago Bioquímica M. Fernanda Pontoriero Ácidos Moléculas capaces de liberar H + HCl H + + Cl H 2 CO 3 H + + HCO 3 Bases Moléculas capaces
EDUCATIVO. Alteraciones del. - Departamento de Fisiopatología - Facultad de Medicina 2011MATERIAL. Dr MSc José Boggia
 - Departamento de Fisiopatología - Facultad de Medicina Alteraciones del equilibrio i ácido-base 2011 Dr MSc José Boggia PANORAMICA GLOBAL I. Recordatorio de la fisiología ácido-base II. Diagnóstico de
- Departamento de Fisiopatología - Facultad de Medicina Alteraciones del equilibrio i ácido-base 2011 Dr MSc José Boggia PANORAMICA GLOBAL I. Recordatorio de la fisiología ácido-base II. Diagnóstico de
Equilibrio Acido-Base. Dr Jorge Brenes Dittel. Nefrología.
 Equilibrio Acido-Base Dr Jorge Brenes Dittel. Nefrología. Equilibrio Acido-base. Fisiología ph es el logaritmo de la concentracíon del ión hidrogenion expresada en milimoles por litro. [H+] en sangre es
Equilibrio Acido-Base Dr Jorge Brenes Dittel. Nefrología. Equilibrio Acido-base. Fisiología ph es el logaritmo de la concentracíon del ión hidrogenion expresada en milimoles por litro. [H+] en sangre es
Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires
 ÁCIDOS Y BASES Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires OBJETIVOS: - Reconocer ácidos, bases y sales, determinar sus disociaciones en agua, según sean electrolitos fuertes
ÁCIDOS Y BASES Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires OBJETIVOS: - Reconocer ácidos, bases y sales, determinar sus disociaciones en agua, según sean electrolitos fuertes
BALANCE ÁCIDO-BASE Y REGULACIÓN DEL ph
 BALANCE ÁCIDO-BASE Y REGULACIÓN DEL ph INTRODUCCION Importancia del mantenimiento del ph [H + ] afecta: Conformación de proteínas Reacciones donde el H + es producto o reactivo Liberación de O 2 de la
BALANCE ÁCIDO-BASE Y REGULACIÓN DEL ph INTRODUCCION Importancia del mantenimiento del ph [H + ] afecta: Conformación de proteínas Reacciones donde el H + es producto o reactivo Liberación de O 2 de la
Fisiopatología del Equilibrio Ácido-Base ACIDOSIS
 Fisiopatología del Equilibrio Ácido-Base ACIDOSIS Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: I. ACIDOSIS:
Fisiopatología del Equilibrio Ácido-Base ACIDOSIS Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: I. ACIDOSIS:
REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE. Bqca. Sofía Langton Fisiología Humana Junio 2014
 REGULACIÓN DEL EQUILIBRIO ÁCIDOBASE Bqca. Sofía Langton Fisiología Humana Junio 2014 Objetivos 1. Estudiar la importancia del balance ácidobase en el organismo. 2. Comprender los tres sistemas (amortiguadores,
REGULACIÓN DEL EQUILIBRIO ÁCIDOBASE Bqca. Sofía Langton Fisiología Humana Junio 2014 Objetivos 1. Estudiar la importancia del balance ácidobase en el organismo. 2. Comprender los tres sistemas (amortiguadores,
Amortiguadores o Buffer. SEMANA 13 Licda. Lilian Judith Guzman melgar
 Amortiguadores o Buffer SEMANA 13 Licda. Lilian Judith Guzman melgar Soluciones amortiguadoras También llamadas soluciones: Buffer Reguladoras Tampón Solución Buffer Es una solución de un ácido débil y
Amortiguadores o Buffer SEMANA 13 Licda. Lilian Judith Guzman melgar Soluciones amortiguadoras También llamadas soluciones: Buffer Reguladoras Tampón Solución Buffer Es una solución de un ácido débil y
GASES EN SANGRE. modifican el ph sanguineo.
 GASES EN SANGRE ESTADO ACIDO-BASE ESTADO DE OXIGENACION Detectar o confirmar alteraciones metabolicas y/o respiratorias que modifican el ph sanguineo. Determinar si la oxigenacion tisular es la adecuada.
GASES EN SANGRE ESTADO ACIDO-BASE ESTADO DE OXIGENACION Detectar o confirmar alteraciones metabolicas y/o respiratorias que modifican el ph sanguineo. Determinar si la oxigenacion tisular es la adecuada.
REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO:
 REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO: - FISIOLOGÍA DE ÁCIDOS Y BASES - EXCRECIÓN RENAL DE H + Miryam Romero R. MSc. PhD. Profesora de Fisiología Departamento de Ciencias Fisiológicas Universidad del Valle
REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO: - FISIOLOGÍA DE ÁCIDOS Y BASES - EXCRECIÓN RENAL DE H + Miryam Romero R. MSc. PhD. Profesora de Fisiología Departamento de Ciencias Fisiológicas Universidad del Valle
lunes 27 de febrero de 12 Desequilibrio Acido-Base
 Desequilibrio Acido-Base Equilibrio Ácido-Base H + es un anión con muy baja concentración en el cuerpo humano. Na + 3.5 millones de veces mas que H + Escala de ph: mide el grado de acidez de una solución.
Desequilibrio Acido-Base Equilibrio Ácido-Base H + es un anión con muy baja concentración en el cuerpo humano. Na + 3.5 millones de veces mas que H + Escala de ph: mide el grado de acidez de una solución.
Fisiopatología Del Equilibrio Ácido-Base Alcalosis
 Fisiopatología Del Equilibrio Ácido-Base Alcalosis Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: II. ALCALOSIS
Fisiopatología Del Equilibrio Ácido-Base Alcalosis Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: II. ALCALOSIS
TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE
 TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE ALTERACIONES ACIDO-BASE Los ácidos son producidos en forma continua, durante el metabolismo normal La concentración de hidrógeno en el LEC se mantiene en un
TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE ALTERACIONES ACIDO-BASE Los ácidos son producidos en forma continua, durante el metabolismo normal La concentración de hidrógeno en el LEC se mantiene en un
ALTERACIONES DEL EQUILIBRIO ÁCIDO BASE. Prof. Dra. Liliana G. Bianciotti
 ALTERACIONES DEL EQUILIBRIO ÁCIDO BASE Prof. Dra. Liliana G. Bianciotti lbianc@ffyb.uba.ar 2016 ALTERACIONES DEL EQUILIBIO ACIDO-BASE ph 7.35-7.45 Metabolismo de Ca 2+ y K + Solubilidad de sales óseas
ALTERACIONES DEL EQUILIBRIO ÁCIDO BASE Prof. Dra. Liliana G. Bianciotti lbianc@ffyb.uba.ar 2016 ALTERACIONES DEL EQUILIBIO ACIDO-BASE ph 7.35-7.45 Metabolismo de Ca 2+ y K + Solubilidad de sales óseas
HOSPITAL NACIONAL PROF. A. POSADAS SERVICIO DE PEDIATRÍA
 HOSPITAL NACIONAL PROF. A. POSADAS SERVICIO DE PEDIATRÍA EQUILIBRIO ÁCIDO-BASE DESDE LA FISIOLOGÍA SERVICIO DE PEDIATRÍA HOSP. NAC. PROF. A. POSADAS Dept. Pediatría Fac. Medicina - UBA Horacio A. Repetto
HOSPITAL NACIONAL PROF. A. POSADAS SERVICIO DE PEDIATRÍA EQUILIBRIO ÁCIDO-BASE DESDE LA FISIOLOGÍA SERVICIO DE PEDIATRÍA HOSP. NAC. PROF. A. POSADAS Dept. Pediatría Fac. Medicina - UBA Horacio A. Repetto
[A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x
![[A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x [A-] Citrato 3- ph = pka + log. 7 = log [AH] Citrato 2- 7 = log = = x x](/thumbs/55/35730009.jpg) Una reacción enzimática transcurre en 10 ml de una disolución cuya concentración total de citrato es 120 mm y su ph inicial es de 7. Durante la reacción se producen 0.2 miliequivalentes de un ácido. Calcular
Una reacción enzimática transcurre en 10 ml de una disolución cuya concentración total de citrato es 120 mm y su ph inicial es de 7. Durante la reacción se producen 0.2 miliequivalentes de un ácido. Calcular
b. Base es la sustancia que en disolución acuosa se disocia, liberando aniones de hidroxilo (OH ) según la ecuación general:
 ACIDOS y BASES Teorías ácido - base Los ácidos y las bases fueron definidos por primera vez por el científico sueco Svante Arrhenius en 1887 en su teoría disociación iónica, en la que establecía que hay
ACIDOS y BASES Teorías ácido - base Los ácidos y las bases fueron definidos por primera vez por el científico sueco Svante Arrhenius en 1887 en su teoría disociación iónica, en la que establecía que hay
ESTADO ACIDO BASE ACIDOSIS METABOLICA. ETIOLOGÍA DE LA ACIDOSIS METABÓLICA Inhabilidad Para Secretar La Carga Acida De La Dieta +
 ESTADO ACIDO BASE Los siguientes pasos son usados para evaluar los desordenes acidobase: 1.Determinar la anormalidad de base acidosis metabólica y/o alcalosis metabólica. 2.Determinar los factores contribuyentes
ESTADO ACIDO BASE Los siguientes pasos son usados para evaluar los desordenes acidobase: 1.Determinar la anormalidad de base acidosis metabólica y/o alcalosis metabólica. 2.Determinar los factores contribuyentes
PROPÓSITO DE MEDIR LOS GASES ARTERIALES
 FISIOLOGÍA DE GASES ARTERIALES La primera parte de este módulo comprende elementos básicos sobre la fisiología de los gases arteriales. Este módulo ayudará a los profesionales de la enfermería y cardiorrespiratorios
FISIOLOGÍA DE GASES ARTERIALES La primera parte de este módulo comprende elementos básicos sobre la fisiología de los gases arteriales. Este módulo ayudará a los profesionales de la enfermería y cardiorrespiratorios
ESTADO ACIDO-BASE CONCEPTOS TEORICO-PRACTICOS FUNDAMENTALES
 ESTADO ACIDOBASE CONCEPTOS TEORICOPRACTICOS FUNDAMENTALES Estado ácidobase: (EAB) Los trastornos del EAB se observan frecuentemente en la práctica diaria, sobre todo en pacientes agudos, algunos son simples
ESTADO ACIDOBASE CONCEPTOS TEORICOPRACTICOS FUNDAMENTALES Estado ácidobase: (EAB) Los trastornos del EAB se observan frecuentemente en la práctica diaria, sobre todo en pacientes agudos, algunos son simples
 Minino de Cheshire, podrías decirme, por favor, qué camino debo seguir para salir de aquí? Esto depende en gran parte del si>o al que quieras llegar - dijo el Gato. - - No me importa mucho el si>o... -
Minino de Cheshire, podrías decirme, por favor, qué camino debo seguir para salir de aquí? Esto depende en gran parte del si>o al que quieras llegar - dijo el Gato. - - No me importa mucho el si>o... -
El CO2, en presencia de anhidrasa carbónica (AC), se hidrata de la siguiente forma: CO2 + H2O <------> CO3H2 < > H+ + HCO3-
 Equilibro Acido Base El equilibrio ácido-base requiere la integración de tres sistemas orgánicos, el hígado, los pulmones y el riñón. En resumen, el hígado metaboliza las proteínas produciendo iones hidrógeno
Equilibro Acido Base El equilibrio ácido-base requiere la integración de tres sistemas orgánicos, el hígado, los pulmones y el riñón. En resumen, el hígado metaboliza las proteínas produciendo iones hidrógeno
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS
 EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
1.-EQUILIBRIOS IÓNICOS EN DISOLUCIONES ACUOSAS.
 TEMA 5 EQUILIBRIOS IÓNICOS y SISTEMAS TAMPÓN. GUIÓN. ( 2 sesiones). 1.- EQUILIBRIOS IÓNICOS EN DISOLUCIÓN ACUOSA 2.- CONCEPTO DE SISTEMA TAMPÓN. 3.- IMPORTANCIA DE LA REGULACIÓN DEL PH FISIOLÓGICO. 4.-
TEMA 5 EQUILIBRIOS IÓNICOS y SISTEMAS TAMPÓN. GUIÓN. ( 2 sesiones). 1.- EQUILIBRIOS IÓNICOS EN DISOLUCIÓN ACUOSA 2.- CONCEPTO DE SISTEMA TAMPÓN. 3.- IMPORTANCIA DE LA REGULACIÓN DEL PH FISIOLÓGICO. 4.-
METABOLISMO ACIDO / BASE
 METABOLISMO ACIDO / BASE Dr Sergio Octavio GRANADOS TINAJERO Hospital Angeles de Villahermosa, Villahermosa, Tabasco, México. Course : 3 Year : 2003 Language : Spanish Country : Mexico City : Baja California
METABOLISMO ACIDO / BASE Dr Sergio Octavio GRANADOS TINAJERO Hospital Angeles de Villahermosa, Villahermosa, Tabasco, México. Course : 3 Year : 2003 Language : Spanish Country : Mexico City : Baja California
BIOQUIMICA CLINICA II
 Universidad Autónoma de Chiapas Facultad de Ciencias Químicas Campus IV BIOQUIMICA CLINICA II UNIDAD 5 EQUILIBRIO ACIDO-BASE TITULAR DEL CURSO : M.C. CONSUELO CHANG RUEDA CICLO ENERO - DICIEMBRE - 2015
Universidad Autónoma de Chiapas Facultad de Ciencias Químicas Campus IV BIOQUIMICA CLINICA II UNIDAD 5 EQUILIBRIO ACIDO-BASE TITULAR DEL CURSO : M.C. CONSUELO CHANG RUEDA CICLO ENERO - DICIEMBRE - 2015
Índice. Sección I. 1. Química y amortiguamiento acidobásicos Homeostasis acidobásica intracelular... 35
 Índice Prefacio... V Prólogo... VII Indice... IX Colaboradores... XVII Sección I 1. Química y amortiguamiento acidobásicos... 21 - John H. Galla Introducción... 21 Amortiguamiento... 24 El papel de los
Índice Prefacio... V Prólogo... VII Indice... IX Colaboradores... XVII Sección I 1. Química y amortiguamiento acidobásicos... 21 - John H. Galla Introducción... 21 Amortiguamiento... 24 El papel de los
Líquidos corporales Compartimiento Equilibrio de líquidos. Q.F. Adriana Cordero
 Líquidos corporales Compartimiento Equilibrio de líquidos Q.F. Adriana Cordero INTRODUCCIÒN El agua y los solutos disueltos en cada uno de los compartimentos corporales de fluidos constituyen los líquidos
Líquidos corporales Compartimiento Equilibrio de líquidos Q.F. Adriana Cordero INTRODUCCIÒN El agua y los solutos disueltos en cada uno de los compartimentos corporales de fluidos constituyen los líquidos
GUIA DE ESTUDIO SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por: Licda. Edda García
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2015 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2015 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
Revista de Actualización Clínica Volumen
 ACIDOSIS METABOLICA Vargas Flores Tatiana 1 Colaboración: Condori Canaza Claudia 2 RESUMEN El ph responsable del equilibrio ácidobase a nivel del líquido extracelular tiene un valor de 7,35 a 7,40; el
ACIDOSIS METABOLICA Vargas Flores Tatiana 1 Colaboración: Condori Canaza Claudia 2 RESUMEN El ph responsable del equilibrio ácidobase a nivel del líquido extracelular tiene un valor de 7,35 a 7,40; el
SOLUCIONES BUFFERS. pk = valor de ph en el cual las concentraciones del ácido y la sal son iguales
 SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
PH y SISTEMAS TAMPÓN
 PH y SISTEMAS TAMPÓN DISOCIACIÓN DEL AGUA.- El agua se disocia de la manera siguiente: HOH H+ OH- El valor de Kéq. a 25ºC es muy pequeña, siendo del orden de 1 8 x 10(-16). Esto significa
PH y SISTEMAS TAMPÓN DISOCIACIÓN DEL AGUA.- El agua se disocia de la manera siguiente: HOH H+ OH- El valor de Kéq. a 25ºC es muy pequeña, siendo del orden de 1 8 x 10(-16). Esto significa
Bases Científicas 1 Autor: Marta Adonis
 ACIDO-BASE En los organismos vivos la concentración de protones debe mantenerse dentro de límites muy estrechos, como requisito indispensable para el desarrollo normal de los procesos metabólicos intracelulares.
ACIDO-BASE En los organismos vivos la concentración de protones debe mantenerse dentro de límites muy estrechos, como requisito indispensable para el desarrollo normal de los procesos metabólicos intracelulares.
EQUILIBRIO ACIDO - BASE
 EQUILIBRIO ACIDO - BASE Carrera de Médicos Especialistas Universitarios en Medicina Crítica y Terapia Intensiva. Universidad de Buenos Aires CONCEPTOS GENERALES EQUILIBRIO ACIDO-BASE EN FORMA ESTEQUIOMÉTRICA
EQUILIBRIO ACIDO - BASE Carrera de Médicos Especialistas Universitarios en Medicina Crítica y Terapia Intensiva. Universidad de Buenos Aires CONCEPTOS GENERALES EQUILIBRIO ACIDO-BASE EN FORMA ESTEQUIOMÉTRICA
Regulación de (H+) Equilibrio ácido-básico
 Regulación de (H+) Equilibrio ácido-básico Introducción v CO2 es generado dentro de las células à Forma H2CO3 (ácido carbónico) al disolverse en agua Introducción ácidos no volátiles v Ácidos no volátiles:
Regulación de (H+) Equilibrio ácido-básico Introducción v CO2 es generado dentro de las células à Forma H2CO3 (ácido carbónico) al disolverse en agua Introducción ácidos no volátiles v Ácidos no volátiles:
ÁCIDOS Y BASES MPSS GÓMEZ CHANG ERIKA. Todos los derechos reservados. Julio 2007 M. en C. Alicia Cea Bonilla -
 ÁCIDOS Y BASES MPSS GÓMEZ CHANG ERIKA 1 Probablemente no haya otro tipo de equilibrio tan importante como el de ácidos y bases B. M. Mahan y R. J. Myers 2 CASO AMC de 52 años de edad, acostumbraba consumir
ÁCIDOS Y BASES MPSS GÓMEZ CHANG ERIKA 1 Probablemente no haya otro tipo de equilibrio tan importante como el de ácidos y bases B. M. Mahan y R. J. Myers 2 CASO AMC de 52 años de edad, acostumbraba consumir
GUÍA DE EJERCICIOS N 4: Ácido-base, neutralización y buffer. 1.- Defina los ácidos y bases según las teorías ácido-base de Arrhenius y Brönsted-Lowry
 1 GUÍA DE EJERCICIOS N 4: Ácido-base, neutralización y buffer PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los ácidos y bases según las teorías ácido-base de Arrhenius y Brönsted-Lowry 2.- Defina
1 GUÍA DE EJERCICIOS N 4: Ácido-base, neutralización y buffer PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los ácidos y bases según las teorías ácido-base de Arrhenius y Brönsted-Lowry 2.- Defina
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM. ACIDOS Y BASES, ph, BUFFERS
 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM ACIDOS Y BASES, ph, BUFFERS Ionización del agua y producto iónico del agua (K w ) H 2 O H + + OH - K eq = [H + ][OH - ] [H 2 O] K eq = [H + ][OH - ] [H 2 O] K eq
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM ACIDOS Y BASES, ph, BUFFERS Ionización del agua y producto iónico del agua (K w ) H 2 O H + + OH - K eq = [H + ][OH - ] [H 2 O] K eq = [H + ][OH - ] [H 2 O] K eq
TALLER ALTERACIONES DEL EQUILIBRIO ACIDO - BASE
 TALLER ALTERACIONES DEL EQUILIBRIO ACIDO - BASE 1. GENERALIDADES EQUILIBRIO ÁCIDO - BASE 1.1 Valor Normal Gasometría Arterial: PaCO 2 PaO 2 HCO - 3 Sat 35-45 mm Hg > 85 mm Hg 22-26 meq/lt > 95% 1.2 Mecanismos
TALLER ALTERACIONES DEL EQUILIBRIO ACIDO - BASE 1. GENERALIDADES EQUILIBRIO ÁCIDO - BASE 1.1 Valor Normal Gasometría Arterial: PaCO 2 PaO 2 HCO - 3 Sat 35-45 mm Hg > 85 mm Hg 22-26 meq/lt > 95% 1.2 Mecanismos
ALTERACIONES DEL EQUILIBRIO ACIDOBÁSICO
 ALTERACIONES DEL EQUILIBRIO ACIDOBÁSICO RAQUEL YAGÜE ZAPICO R1 MEDICINA INTENSIVA Servicio de Medicina Interna 2012 GENERALIDADES DIARIAMENTE: -Hidrogeniones ( ácidos no volátiles): 70 a 100 mmol en dieta
ALTERACIONES DEL EQUILIBRIO ACIDOBÁSICO RAQUEL YAGÜE ZAPICO R1 MEDICINA INTENSIVA Servicio de Medicina Interna 2012 GENERALIDADES DIARIAMENTE: -Hidrogeniones ( ácidos no volátiles): 70 a 100 mmol en dieta
7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ
 ALTERACIONES DEL EQUILIBRIO ÁCIDO-BASE Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ El ph refleja la concentración de cationes de hidrógeno presentes en una determinada
ALTERACIONES DEL EQUILIBRIO ÁCIDO-BASE Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ El ph refleja la concentración de cationes de hidrógeno presentes en una determinada
Trastornos del equilibrio ácido-base
 NOTA DELS COMISSIONARIS: hi ha aclaracions i correccions importants al document Fe d errades, és important que us el mireu de cara a l examen!! Trastornos del equilibrio ácidobase INTRODUCCIÓN CONCEPTOS
NOTA DELS COMISSIONARIS: hi ha aclaracions i correccions importants al document Fe d errades, és important que us el mireu de cara a l examen!! Trastornos del equilibrio ácidobase INTRODUCCIÓN CONCEPTOS
Interpretación Rápida de los Gases Arteriales
 Artículo de Revisión Concisa Interpretación Rápida de los Gases Arteriales Dr. Juan Ignacio Padilla Cuadra (Decano, Facultad de Medicina, Universidad de Iberoamérica) Introducción: Los gases arteriales
Artículo de Revisión Concisa Interpretación Rápida de los Gases Arteriales Dr. Juan Ignacio Padilla Cuadra (Decano, Facultad de Medicina, Universidad de Iberoamérica) Introducción: Los gases arteriales
Programa 3º Curso. Curso (Prof. M García-Caballero)
 Programa 3º Curso Departamento de Cirugía Curso 2008-09 Equilibrio i hidroelectrolítico lí i y ácido-base (Prof. M García-Caballero) http://www.cirugiadelaobesidad.net/ CAMBIOS DE FLUIDOS Y ELECTROLITOS
Programa 3º Curso Departamento de Cirugía Curso 2008-09 Equilibrio i hidroelectrolítico lí i y ácido-base (Prof. M García-Caballero) http://www.cirugiadelaobesidad.net/ CAMBIOS DE FLUIDOS Y ELECTROLITOS
Trabajo Práctico N o 2 BUFFERS BIOLÓGICOS
 1 Trabajo Práctico N o 2 BUFFERS BIOLÓGICOS OBJETIVOS A partir de la ecuación de HendersonHasselbach calcular la concentración de (H + ),(Aceptor de H + ) o (Dador de H + ). Conocer cómo se mantiene el
1 Trabajo Práctico N o 2 BUFFERS BIOLÓGICOS OBJETIVOS A partir de la ecuación de HendersonHasselbach calcular la concentración de (H + ),(Aceptor de H + ) o (Dador de H + ). Conocer cómo se mantiene el
Fundación H.A. Barceló Facultad de Medicina
 Fundación H.A. Barceló Facultad de Medicina LICENCIATURA EN NUTRICION PRIMER AÑO FISIOLOGIA MODULO 16 LECCIONES 1 Y 2 1 MODULO 16: Equilibrio Electrolítico y Control de ph OBJETIVOS - Conocer las vías
Fundación H.A. Barceló Facultad de Medicina LICENCIATURA EN NUTRICION PRIMER AÑO FISIOLOGIA MODULO 16 LECCIONES 1 Y 2 1 MODULO 16: Equilibrio Electrolítico y Control de ph OBJETIVOS - Conocer las vías
Para resolver ésta guía deberá leer el tema en el Capítulo 10 del libro de texto.
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2016 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2016 SEMANA 13 DISOLUCIONES TAMPON, AMORTIGUADORES O BUFFER Elaborado por:
LA MATERIA VIVA Y EL AGUA
 Página 1 de 11 LA MATERIA VIVA Y EL AGUA Haga clic en la respuesta correcta. Mostrar las preguntas individualmente 1. Tipo C. Siempre se produce una variación en el ph de una disolución reguladora si simultáneamente
Página 1 de 11 LA MATERIA VIVA Y EL AGUA Haga clic en la respuesta correcta. Mostrar las preguntas individualmente 1. Tipo C. Siempre se produce una variación en el ph de una disolución reguladora si simultáneamente
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
Tema: Soluciones Buffer-Amortiguadoras
 ESCUELA DE CIENCIAS AGRICOLA, PECUARIAS Y DEL MEDIO AMBIENTE ECAPMA Nombre l Curso: 334001-Sistema Metabólico Nutricional Tema: Soluciones Buffer-Amortiguadoras JAIRO ENRIQUE GRANADOS MORENO.,MSc (Director
ESCUELA DE CIENCIAS AGRICOLA, PECUARIAS Y DEL MEDIO AMBIENTE ECAPMA Nombre l Curso: 334001-Sistema Metabólico Nutricional Tema: Soluciones Buffer-Amortiguadoras JAIRO ENRIQUE GRANADOS MORENO.,MSc (Director
MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ
 MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ 1-Historia clínica G D Varón de 1 año y 5 meses MOTIVO DE CONSULTA retraso del crecimiento ANTECEDENTES RNTPAEG
MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ 1-Historia clínica G D Varón de 1 año y 5 meses MOTIVO DE CONSULTA retraso del crecimiento ANTECEDENTES RNTPAEG
Cátedra de Fisiología Humana CAPÍTULO I CAPITULO III. Equilibrio Acido Base PH. Carrera de Enfermería. Universidad Nacional del Nordeste
 CAPÍTULO I Cátedra de Fisiología Humana CAPITULO III Equilibrio Acido Base PH Carrera de Enfermería. Universidad Nacional del Nordeste 37 CAPITULO 3: Cada soluto del organismo, el sodio, el potasio, el
CAPÍTULO I Cátedra de Fisiología Humana CAPITULO III Equilibrio Acido Base PH Carrera de Enfermería. Universidad Nacional del Nordeste 37 CAPITULO 3: Cada soluto del organismo, el sodio, el potasio, el
Sistema Integrado de Gestión
 Sistema Integrado de Gestión GUÍA PRÁCTICA N 52 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Versión 1 Proceso: Investigación -
Sistema Integrado de Gestión GUÍA PRÁCTICA N 52 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Versión 1 Proceso: Investigación -
Acidosis y Alcalosis Metabolica.
 Acidosis y Alcalosis Metabolica. Acidosis metabólica Se caracteriza por: ph arterial bajo (concentración alta de hidrogeniones) Reducción en la concentración plasmática de HCO3. Hiperventilación compensatoria.
Acidosis y Alcalosis Metabolica. Acidosis metabólica Se caracteriza por: ph arterial bajo (concentración alta de hidrogeniones) Reducción en la concentración plasmática de HCO3. Hiperventilación compensatoria.
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
Trascripción clase de acidosis
 Trascripción clase de acidosis En las clases hemos visto como se produce el equilibrio ácido base y como el organismo trata de mantener el equilibrio ácido base. Al salirse del equilibrio acido_base se
Trascripción clase de acidosis En las clases hemos visto como se produce el equilibrio ácido base y como el organismo trata de mantener el equilibrio ácido base. Al salirse del equilibrio acido_base se
VARIACIONES SANGUÍNEAS: - pco2 - EL ph ESTIMULO C.R.B., NO COMPENSA DISNEA - po2 - NaHCO3 5 mmol/l
 Fisiopatología Del Equilibrio Ácido-Base: Acidosis PH debe ser menor a 7.35. a) Acidosis Respiratorias b) Acidosis Metabólicas También se habla de acidosis compensadas y no compensadas. Una acidosis puede
Fisiopatología Del Equilibrio Ácido-Base: Acidosis PH debe ser menor a 7.35. a) Acidosis Respiratorias b) Acidosis Metabólicas También se habla de acidosis compensadas y no compensadas. Una acidosis puede
TALLER DE GASES ARTERIALES
 TALLER DE GASES ARTERIALES MOP 24 de Agosto 2010 Objetivos Aprender a reconocer los trastornos del equilibrio ácido-base: Acidosis metabólica y respiratoria, alcalosis metabólica y respiratoria. Familiarizarse
TALLER DE GASES ARTERIALES MOP 24 de Agosto 2010 Objetivos Aprender a reconocer los trastornos del equilibrio ácido-base: Acidosis metabólica y respiratoria, alcalosis metabólica y respiratoria. Familiarizarse
UNIVERSIDAD AUSTRAL DE CHILE INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 1
 INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 1 EQUILIBRIO ACIDO-BASE La función celular es óptima cuando el ph del LEC es 7.4 ([H+] de 40 nmoles/litro). Sin embargo hay muchas situaciones, especialmente
INSTITUTO DE FARMACOLOGIA Prof. Marcos Moreira Espinoza 1 EQUILIBRIO ACIDO-BASE La función celular es óptima cuando el ph del LEC es 7.4 ([H+] de 40 nmoles/litro). Sin embargo hay muchas situaciones, especialmente
1.- FOSFATO MONOSUSTITUIDO/FOSFATO DISUSTITUIDO (H2PO4 - /HPO4 = )
 1. FOSFATO MONOSUSTITUIDO/FOSFATO DISUSTITUIDO (H2PO4 /HPO4 = ) El ácido fosfórico (H 3 PO 4 ), además de formar parte de numerosos compuestos orgánicos (ácidos nucleicos, fosfolípidos, azúcares, etc.)
1. FOSFATO MONOSUSTITUIDO/FOSFATO DISUSTITUIDO (H2PO4 /HPO4 = ) El ácido fosfórico (H 3 PO 4 ), además de formar parte de numerosos compuestos orgánicos (ácidos nucleicos, fosfolípidos, azúcares, etc.)
Guía soluciones acuosas
 UNIVERSIDAD N LA REPUBLICA Nombre del Estudiante: Guía soluciones acuosas Carrera Asignatura Nivel Enfermería Bioquímica Segundo Nivel Semestre 2 semestre Año 2016 Docente Dr. Patricio Muñoz Torres Puntaje
UNIVERSIDAD N LA REPUBLICA Nombre del Estudiante: Guía soluciones acuosas Carrera Asignatura Nivel Enfermería Bioquímica Segundo Nivel Semestre 2 semestre Año 2016 Docente Dr. Patricio Muñoz Torres Puntaje
Fisiopatología Del Equilibrio Ácido-Base: Alcalosis
 Fisiopatología Del Equilibrio Ácido-Base: Alcalosis La alcalosis mucho menos frecuente que la acidosis, pero muy complicada para el organismo. Cuando el organismo sufre alcalosis va a tener problemas bastante
Fisiopatología Del Equilibrio Ácido-Base: Alcalosis La alcalosis mucho menos frecuente que la acidosis, pero muy complicada para el organismo. Cuando el organismo sufre alcalosis va a tener problemas bastante
TEMA 3. EQUILIBRIOS ACIDO BASE
 TEMA 3. EQUILIBRIOS ACIDO BASE 3.1 EQUILIBRIOS IÓNICOS...2 3.2 EQUILIBRIOS ACIDO BASE...3 3.3 PROCEDIMIENTOS GRÁFICOS PARA EL CÁLCULO DE EQUILIBRIOS...5 3.3.1 DIAGRAMA pc-ph...5 3.3.2 DIAGRAMA pc-ph para
TEMA 3. EQUILIBRIOS ACIDO BASE 3.1 EQUILIBRIOS IÓNICOS...2 3.2 EQUILIBRIOS ACIDO BASE...3 3.3 PROCEDIMIENTOS GRÁFICOS PARA EL CÁLCULO DE EQUILIBRIOS...5 3.3.1 DIAGRAMA pc-ph...5 3.3.2 DIAGRAMA pc-ph para
Día 1 ANANMESIS Paciente masculino de 57 años llega a la guardia con fatiga y es internado para su evaluación.
 CASO CLINICO 8 Día 1 ANANMESIS Paciente masculino de 57 años llega a la guardia con fatiga y es internado para su evaluación. ANTECEDENTES Trabajador de la construcción, fumador desde su juventud. Refiere
CASO CLINICO 8 Día 1 ANANMESIS Paciente masculino de 57 años llega a la guardia con fatiga y es internado para su evaluación. ANTECEDENTES Trabajador de la construcción, fumador desde su juventud. Refiere
GUÍA DE EJERCICIOS ADICIONALES N 2 Acido-base, neutralización y buffer
 1 GUÍA DE EJERCICIOS ADICIONALES N 2 Acido-base, neutralización y buffer 1.- Un ácido según la teoría de Arrhenius es aquella sustancia que: a) Libera uno o más iones hidroxilos (OH - ) por cada molécula
1 GUÍA DE EJERCICIOS ADICIONALES N 2 Acido-base, neutralización y buffer 1.- Un ácido según la teoría de Arrhenius es aquella sustancia que: a) Libera uno o más iones hidroxilos (OH - ) por cada molécula
GUIAS DE LABORATORIO DE BIOQUIMICA BASICA FACULTAD DE SALUD PROGRAMA DE ENFERMERIA Docente: MANUEL ANDRES GIRALDO JACOBO
 LABORATORIO N 5 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO Tiempo de práctica: 2 horas MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Objetivos 1. Al finalizar la práctica,
LABORATORIO N 5 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO Tiempo de práctica: 2 horas MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Objetivos 1. Al finalizar la práctica,
SGUICEL009QM11-A16V1. Ácido base I: conceptos y teorías
 SGUICEL009QM11-A16V1 Ácido base I: conceptos y teorías Ítem Alternativa Habilidad 1 B Reconocimiento 2 A Comprensión 3 E Reconocimiento 4 E Comprensión 5 E ASE 6 E Comprensión 7 D Comprensión 8 E Comprensión
SGUICEL009QM11-A16V1 Ácido base I: conceptos y teorías Ítem Alternativa Habilidad 1 B Reconocimiento 2 A Comprensión 3 E Reconocimiento 4 E Comprensión 5 E ASE 6 E Comprensión 7 D Comprensión 8 E Comprensión
QUIMICA GENERAL GUIA DE EJERCICIOS Nº4 Soluciones Ácido-base. 1.- Defina los ácidos y bases según las teorías ácido base que usted conoce.
 1 QUIMICA GENERAL GUIA DE EJERCICIOS Nº4 Soluciones Ácido-base PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los ácidos y bases según las teorías ácido base que usted conoce. 2.- Defina el ph y poh.
1 QUIMICA GENERAL GUIA DE EJERCICIOS Nº4 Soluciones Ácido-base PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los ácidos y bases según las teorías ácido base que usted conoce. 2.- Defina el ph y poh.
LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER
 LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER 1.- INTRODUCCIÓN Soluciones Ácido-Base Los solutos disueltos en agua pueden clasificarse como electrolitos y no electrolitos en función de su capacidad de
LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER 1.- INTRODUCCIÓN Soluciones Ácido-Base Los solutos disueltos en agua pueden clasificarse como electrolitos y no electrolitos en función de su capacidad de
INTERPRETACION DE LOS GASES ARTERIALES
 INTERPRETACION DE LOS GASES ARTERIALES ph PaO2 PaCO2 HCO3 BE Hb SaO2 Bloque 6 Modulo 2 Dr Erick Valencia Anestesiologo Intensivista. Que son los Gases Arteriales? Una muestra de sangre anticoagulada que
INTERPRETACION DE LOS GASES ARTERIALES ph PaO2 PaCO2 HCO3 BE Hb SaO2 Bloque 6 Modulo 2 Dr Erick Valencia Anestesiologo Intensivista. Que son los Gases Arteriales? Una muestra de sangre anticoagulada que
Fisiología y Fisiopatología Del Equilibrio Hidrosalino
 Fisiología y Fisiopatología Del Equilibrio Hidrosalino Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiología Universidad Austral de Chile FISIOLOGÍA DEL EQUILIBRIO HIDROSALINO: 1. IMPORTANCIA
Fisiología y Fisiopatología Del Equilibrio Hidrosalino Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiología Universidad Austral de Chile FISIOLOGÍA DEL EQUILIBRIO HIDROSALINO: 1. IMPORTANCIA
GUIAS DE LABORATORIO DE BIOQUIMICA BASICA FACULTAD DE SALUD PROGRAMA DE ENFERMERIA Docente: MANUEL ANDRES GIRALDO JACOBO LABORATORIO N 7
 LABORATORIO N 7 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Tiempo de práctica: 2 horas Integrantes: INTRODUCCIÓN Dentro de los
LABORATORIO N 7 REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE DESPUÉS DEL EJERCICIO MUSCULAR INTENSO Y DE LA INGESTIÓN DE BICARBONATO DE SODIO Tiempo de práctica: 2 horas Integrantes: INTRODUCCIÓN Dentro de los
medir bicarbonato tbn pero el concepto ph esta directamente asociado a hidrogeniones, por lo tanto lo que - ph COMPATIBLE CON LA VIDA:
 REGULACION DEL EQUILIBRIO ÁCIDO-BASE 1.- ph? Clase 1 - ph NORMAL : 7,35-7,45 - ph COMPATIBLE CON LA VIDA 6,8-7,8 (7,0-7,8) Prof. Marcos Moreira Espinoza Instituto de Farmacología Universidad Austral de
REGULACION DEL EQUILIBRIO ÁCIDO-BASE 1.- ph? Clase 1 - ph NORMAL : 7,35-7,45 - ph COMPATIBLE CON LA VIDA 6,8-7,8 (7,0-7,8) Prof. Marcos Moreira Espinoza Instituto de Farmacología Universidad Austral de
Nombre Grupo. Unidad 6 Ácido-base
 Nombre Grupo OPCIÓN A Unidad 6 Ácido-base 1. (2 p) a) Calcule el ph de una disolución 0.1 M de hidróxido potásico. El hidróxido potásico, como base fuerte que es, está completamente disociada en disolución
Nombre Grupo OPCIÓN A Unidad 6 Ácido-base 1. (2 p) a) Calcule el ph de una disolución 0.1 M de hidróxido potásico. El hidróxido potásico, como base fuerte que es, está completamente disociada en disolución
QUÍMICA 2º Bachillerato Ejercicios: Reacciones Ácido Base
 1(8) Ejercicio nº 1 Completa las siguientes reacciones ácido-base, indicando qué especies químicas son el ácido y la base, y cuáles sus conjugados: a) HA + B b) HCl + NH 3 c) HNO 3 + H 2 O Ejercicio nº
1(8) Ejercicio nº 1 Completa las siguientes reacciones ácido-base, indicando qué especies químicas son el ácido y la base, y cuáles sus conjugados: a) HA + B b) HCl + NH 3 c) HNO 3 + H 2 O Ejercicio nº
UNIDAD RENAL. Anatomía y fisiología del aparato urinario. LEI. JAVIER CESPEDES MATA ME.
 UNIDAD RENAL Anatomía y fisiología del aparato urinario. LEI. JAVIER CESPEDES MATA ME. Funciones de la nefrona Filtración glomerular. Reabsorción glomerular. Secreción tubular. Excresion Tasa de filtración
UNIDAD RENAL Anatomía y fisiología del aparato urinario. LEI. JAVIER CESPEDES MATA ME. Funciones de la nefrona Filtración glomerular. Reabsorción glomerular. Secreción tubular. Excresion Tasa de filtración
Agua, electrolitos, balance acido-base. Dra. Luz E. Cuevas-Molina NURS 1231
 Agua, electrolitos, balance acido-base Dra. Luz E. Cuevas-Molina NURS 1231 1 Introducción Para mantener la homoestasis debe haber un balance entre las cantidades de fluido y electrolitos Los electrolitos
Agua, electrolitos, balance acido-base Dra. Luz E. Cuevas-Molina NURS 1231 1 Introducción Para mantener la homoestasis debe haber un balance entre las cantidades de fluido y electrolitos Los electrolitos
6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
1. Líquidos corporales. 2. Anatomía y función renal. 3. Hormonas ADH y aldosterona
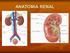 1. Líquidos corporales 2. Anatomía y función renal 3. Hormonas ADH y aldosterona Propiedades de la Homeostasis 1. Importancia tanto del sistema nervioso como del endocrino. 2. Controles antagónicos. 3.
1. Líquidos corporales 2. Anatomía y función renal 3. Hormonas ADH y aldosterona Propiedades de la Homeostasis 1. Importancia tanto del sistema nervioso como del endocrino. 2. Controles antagónicos. 3.
FISIOPATOLOGIA. Concentración normal H+: 40 nmoles/l. -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3
 FISIOPATOLOGIA Concentración normal H+: 40 nmoles/l -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3 FISIOPATOLOGIA ACIDO-BASE ACIDO: sustancia capaz de ceder protones BASE: sustancia
FISIOPATOLOGIA Concentración normal H+: 40 nmoles/l -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3 FISIOPATOLOGIA ACIDO-BASE ACIDO: sustancia capaz de ceder protones BASE: sustancia
Trastornos Acido - Base
 Trastornos Acido - Base Introducción El organismo, en condiciones normales y como consecuencia de su actividad metabólica, produce diariamente de 70 a 100 meq de ácidos fijos (provenientes del metabolismo
Trastornos Acido - Base Introducción El organismo, en condiciones normales y como consecuencia de su actividad metabólica, produce diariamente de 70 a 100 meq de ácidos fijos (provenientes del metabolismo
2ª parte: Equilibrio Acido Base Amortiguación Intracelular De CO 2 : Hemoglobina (Hb)
 2ª parte: Equilibrio Acido Base 15-09-2008 Amortiguación Intracelular De CO 2 : Hemoglobina (Hb) Cómo se va a generar la amortiguación de C0 2 a través de sustancias anfóteras? El C0 2 ingresa a la célula
2ª parte: Equilibrio Acido Base 15-09-2008 Amortiguación Intracelular De CO 2 : Hemoglobina (Hb) Cómo se va a generar la amortiguación de C0 2 a través de sustancias anfóteras? El C0 2 ingresa a la célula
GUÍA DE ESTUDIO SEMANA 12 ACIDOS, BASES Y ELECTROLITOS Licda. Corina Marroquín Orellana
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA DE QUIMICA, PRIMER AÑO GUÍA DE ESTUDIO 2016 SEMANA 12 ACIDOS, BASES Y ELECTROLITOS Licda. Corina Marroquín Orellana
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDACTICA DE QUIMICA, PRIMER AÑO GUÍA DE ESTUDIO 2016 SEMANA 12 ACIDOS, BASES Y ELECTROLITOS Licda. Corina Marroquín Orellana
La Composición del medio que rodea a las células debe permanecer constante: (HOMEOSTASIS) y entre límites compatibles con las reacciones vitales
 pulmones Tracto Gastrointestinal FLUIDOS INTRA- Y EXTRA-CELULARES Al pasar por los pulmones el CO2 sale y entra O2 a la sangre nutrientes Nutrientes y O2 entran a cls Deshechos y CO2 salen de las cls Los
pulmones Tracto Gastrointestinal FLUIDOS INTRA- Y EXTRA-CELULARES Al pasar por los pulmones el CO2 sale y entra O2 a la sangre nutrientes Nutrientes y O2 entran a cls Deshechos y CO2 salen de las cls Los
Fisiopatología Equilibrio Hidrosalino. Potasio
 Fisiopatología Equilibrio Hidrosalino Potasio Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiología Universidad Austral de Chile Valdivia- Chile FISIOPATOLOGIA DEL EQUILIBRIO DEL K+:
Fisiopatología Equilibrio Hidrosalino Potasio Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiología Universidad Austral de Chile Valdivia- Chile FISIOPATOLOGIA DEL EQUILIBRIO DEL K+:
REACCIONES DE TRANSFERENCIA DE PROTONES
 REACCIONES DE TRANSFERENCIA DE PROTONES 1. Un vinagre que contiene un 5 % en masa de ácido acético tiene un ph de 2,4. Calcule: a) La concentración molar inicial de la disolución del ácido. b) La densidad
REACCIONES DE TRANSFERENCIA DE PROTONES 1. Un vinagre que contiene un 5 % en masa de ácido acético tiene un ph de 2,4. Calcule: a) La concentración molar inicial de la disolución del ácido. b) La densidad
La Gasometría MEDICION
 José Miguel La Torre Jiménez La Gasometría MEDICION La gasometría arterial es una de las técnicas más frecuentes realizadas a pacientes en estado crítico. Para realizar una correcta medición de los valores
José Miguel La Torre Jiménez La Gasometría MEDICION La gasometría arterial es una de las técnicas más frecuentes realizadas a pacientes en estado crítico. Para realizar una correcta medición de los valores
Organización Funcional y el Medio Interno
 Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
PROBLEMAS DE SELECTIVIDAD. TEMA 5: ÁCIDOS Y BASES
 PROBLEMAS DE SELECTIVIDAD. TEMA 5: ÁCIDOS Y BASES 2015 1) a) A 25 ºC la constante de basicidad del NH 3 es 1,8 10 5. Si se tiene una disolución 0,1 M, calcula el grado de disociación. b) Calcula la concentración
PROBLEMAS DE SELECTIVIDAD. TEMA 5: ÁCIDOS Y BASES 2015 1) a) A 25 ºC la constante de basicidad del NH 3 es 1,8 10 5. Si se tiene una disolución 0,1 M, calcula el grado de disociación. b) Calcula la concentración
DESORDEN ACIDO BASICO
 DESORDEN ACIDO BASICO Cuando se habla de regulacion del equilibrio acido base, se habla en realidad de la Regulacion de la concentracion de iones hidrogenos en los liquidos corporales 1 Como la concentracion
DESORDEN ACIDO BASICO Cuando se habla de regulacion del equilibrio acido base, se habla en realidad de la Regulacion de la concentracion de iones hidrogenos en los liquidos corporales 1 Como la concentracion
TALLER DE ANALISIS DE GASES ARTERIALES
 TALLER DE ANALISIS DE GASES ARTERIALES Dr. Menfil A Orellana-Barrios Medicina Interna Cursos Precongreso Congreso de Residentes 2012 HGSJDD www.drmenfilorellana.wordpress.com Para qué se utilizan los Gases
TALLER DE ANALISIS DE GASES ARTERIALES Dr. Menfil A Orellana-Barrios Medicina Interna Cursos Precongreso Congreso de Residentes 2012 HGSJDD www.drmenfilorellana.wordpress.com Para qué se utilizan los Gases
CONCENTRACIONES Y SOLUCIONES
 Clase de problemas Nº 2 CONCENTRACIONES Y SOLUCIONES Introducción Las soluciones son mezclas homogéneas de componentes que no reaccionan entre si sino que se disuelven: Solución = Soluto + Solvente El
Clase de problemas Nº 2 CONCENTRACIONES Y SOLUCIONES Introducción Las soluciones son mezclas homogéneas de componentes que no reaccionan entre si sino que se disuelven: Solución = Soluto + Solvente El
