INFORMACION PARA PRESCRIBIR AMPLIA
|
|
|
- Samuel Olivera Fernández
- hace 7 años
- Vistas:
Transcripción
1 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: PAMIGEN 2. Nombre Genérico: GEMCITABINA 3. Forma Farmacéutica y Formulación: Solución Cada frasco ámpula con liofilizado contiene: Clorhidrato de Gemcitabina equivalente a mg y 1000 mg de Gemcitabina. Excipiente c.b.p 1 frasco ámpula 4. Indicación Terapéutica: PAMIGEN (Gemcitabina), está indicado como terapia de primera línea para el tratamiento de pacientes con cáncer pulmonar de células no pequeñas localmente avanzado o metastásico solo o en combinación con cisplatino. PAMIGEN está indicado para el tratamiento de primera línea en pacientes con adenocarcinoma de páncreas localmente avanzado o metastásico. PAMIGEN está indicado para pacientes con cáncer pancreático refractario a 5-FU. PAMIGEN en combinación con cisplatino está indicado en el tratamiento de pacientes con cáncer de vejiga avanzado y/o metastásico y en pacientes con carcinoma de células superficiales de vejiga, en refractariedad a la terapia con BCG. 1
2 PAMIGEN, indicado en combinación con paclitaxel para el tratamiento de pacientes con cáncer de mama no resecable, localmente recurrente o metastásico, que hayan recaído luego de recibir quimioterapia adjuvante o neoadjuvante basada en antraciclinas. PAMIGEN está indicado solo o en en combinación para el tratamiento de pacientes con carcinoma epitelial de ovario recurrente que han recaído como mínimo 6 meses después del tratamiento con platino. PAMIGEN está indicado en el tratamiento de primera línea del cáncer cervicouterino localmente avanzado o metastásico. PAMIGEN, indicado en el tratamiento de los pacientes con cáncer del tracto biliar. 5. Farmacocinética y Farmacodinamia: Farmacocinética: Gemcitabina es rápidamente eliminada del plasma, principalmente por metabolismo de un metabolito inactivo, la 2'-desoxi-2',2'-difluorouridina (dfdu). Menos del 10% de una dosis intravenosa se recupera en la orina como Gemcitabina intacta. La Gemcitabina y dfdu son los únicos compuestos hallados en el plasma y constituyen el 99% del material recuperado en orina. La unión de la Gemcitabina a proteínas plasmáticas es muy baja <10%. Los análisis de los estudios farmacocinéticos poblacionales de dosis simple y múltiple han demostrado que el volumen de distribución de Gemcitabina está significativamente influido por el sexo. El aclaramiento sistémico se encuentra afectado por el sexo y la edad. Estos efectos determinan diferencias en las concentraciones plasmáticas de Gemcitabina y su velocidad de eliminación (vida media) de la circulación sistémica. El aclaramiento sistémico se encuentra dentro de un rango aproximado de 30 L/hr/m 2 a 90 L/hr/m 2. 2
3 A la velocidad de infusión recomendada, su vida media oscila entre 32 a 94 minutos, dependiendo de la edad y el sexo. Farmacodinamia: La Gemcitabina es específica en el ciclo celular actuando en la fase S, eliminando las células que se encuentran en síntesis de ADN (fase S) y bajo ciertas condiciones, bloqueando la progresión de las células a través de la fase de unión G1/S. La Gemcitabina (dfdc) se metaboliza intracelularmente por nucleósidoquinasas a difosfato (dfdcdp) y trifosfato (dfdctp) nucleósidos activos. La acción citotóxica de la Gemcitabina parece ser debida a la inhibición de la síntesis del ADN por dos acciones del dfdcdp y del dfdctp. Primero, el dfdcdp inhibe a la ribonucleótido-reductasa que es la única responsable de catalizar las reacciones que generan los trifosfatos desoxinucleósidos para la síntesis del ADN. La inhibición de esta enzima por el dfdcdp, causa una reducción en las concentraciones de desoxinucleósidos en general, y especialmente en aquella del dctp. Segundo, el dfdctp compite con el dctp por la incorporación al ADN (auto-potenciación). De este modo, la reducción en la concentración intracelular de dctp potencia la incorporación de dfdctp al ADN. El ADN polimerasa epsilon es fundamentalmente incapaz de remover la Gemcitabina y reparar los crecientes filamentos del ADN. Luego que la Gemcitabina es incorporada al ADN, un nucleótido adicional se agrega a los filamentos crecientes de ADN. Después de este agregado, se produce esencialmente una inhibición completa en la síntesis posterior del ADN (terminación encubierta de la cadena). Después de la incorporación al ADN, la Gemcitabina aparece luego para inducir el proceso de muerte celular programada conocido como apoptosis. 6. Contraindicaciones: PAMIGEN está contraindicado en pacientes con hipersensibilidad conocida al medicamento. 3
4 7. Precauciones Generales: Debido a que PAMIGEN puede inducir supresión en la médula ósea, los pacientes que reciban terapia con este fármaco deben ser monitoreados continuamente en el conteo sanguíneo de glóbulos rojos y glóbulos blancos. La prolongación en el tiempo de infusión y aumento en la intensidad de dosis puede incrementar los efectos de toxicidad. Los pacientes comprometidos por toxicidad debida al fármaco pueden requerir tratamiento. 8. Precauciones y restricciones de uso durante el embarazo y la lactancia: El uso de Gemcitabina durante el embarazo debe evitarse por el potencial peligro para el feto. La evaluación de estudios con animales de experimentación ha demostrado toxicidad en la reproducción, por ej. defectos de nacimiento u otros efectos en el desarrollo del embrión o feto, el curso de gestación o desarrollo peri y postnatal. El uso de Gemcitabina debe evitarse en mujeres en período de lactancia por el potencial peligro para el lactante. 9. Reacciones Secundarias y Adversas: HEMATOLOGICAS: Como la Gemcitabina es un supresor medular óseo, puede inducir a anemia, leucopenia y trombocitopenia, como resultado de su administración. También se informa comúnmente neutropenia febril. GASTROINTESTINALES: Las anormalidades en las pruebas de función hepática son muy comunes, pero éstas son habitualmente leves, no progresivas y ocasionalmente se necesita suspender el tratamiento. No obstante, la Gemcitabina deberá ser empleada con precaución en pacientes con función hepática deteriorada. Náusea acompañada de vómito se presentan en forma frecuente. Este efecto adverso raramente resulta limitante de la dosis, y es fácilmente manejable con antieméticos habituales; diarrea y estomatitis también han sido informadas con frecuencia. RENALES: Se ha informado en forma frecuente proteinuria moderada y hematuria. 4
5 PIEL Y TEGUMENTOS: Se ha observado rash, frecuentemente asociado con prurito. El rash es por lo general moderado. También se ha reportado alopecia con frecuencia (usualmente mínima caída del cabello). RESPIRATORIAS: Disnea ha sido reportada con frecuencia. En raras ocasiones se ha reportado broncoespasmo, posterior a la infusión de Gemcitabina. Ocasionalmente se ha reportado neumonitis intersticial. En raras ocasiones se han reportado efectos pulmonares, a veces severos (como edema pulmonar o síndrome de distrés respiratorio del adulto) en asociación a la terapia con Gemcitabina. Si se desarrollaran estos efectos, se debe considerar la discontinuación del tratamiento con Gemcitabina. El uso temprano de medidas de apoyo puede mejorar la condición. GENITO-URINARIAS: Se ha informado raramente de hallazgos clínicos consistentes con Síndrome Urémico Hemolítico en pacientes que reciben Gemcitabina. La Gemcitabina debe discontinuarse a los primeros síntomas de cualquier evidencia microangiopática de anemia hemolítica, tales como la rápida caída de la hemoglobina concomitante a trombocitopenia, elevación de la bilirrubina sérica, creatinina sérica, nitrógeno ureico o LDH. La insuficiencia renal puede no ser reversible aún con la discontinuación de la terapia y puede ser necesaria la diálisis. GENERALES: Se ha informado sobre sintomatología similar a la gripe. Los síntomas más comúnmente informados son: fiebre, dolor de cabeza, dolor de espalda, escalofríos, mialgia, astenia y anorexia; de igual manera: tos, rinitis, malestar, sudoración e insomnio. Se han reportado en muy raras ocasiones reacciones anafilácticas. Se ha reportado toxicidad por radiación (ver sección de interacciones). CARDIOVASCULARES: Se ha informado frecuentemente sobre edema/ edema periférico. Unos pocos casos de hipotensión han sido informados. Se han reportado casos de infarto de miocardio, insuficiencia cardiaca congestiva y arritmia, pero no existe una evidencia clara de que la Gemcitabina cause toxicidad cardiaca. VASCULARES: Muy rara vez se han informado signos clínicos de vasculitis periférica y gangrena. PIEL Y TEGUMENTOS: Muy rara vez se han informado reacciones cutáneas severas, incluidas descamación y erupciones bulosas. 5
6 HEPATOBILIARES: Raramente se han informado pruebas de la función hepática con anormalidades que incluyan aumentos en los niveles de aspartato aminotransferasa (AST), alanina aminotransferasa (ALT), gammaglutamil transferasa (GGT), fosfatasa alcalina y bilirrubina. Se han informado reacciones de hipersensibilización a la radiación. 10. Interacciones medicamentosas y de otro género: Radioterapia concomitante (administrada conjuntamente o con menos de 7 días de diferencia): La toxicidad asociada con esta terapia multimodalidad depende de muchos factores diferentes, que incluyen la dosis de Gemcitabina, la frecuencia de la administración de Gemcitabina, la dosis de radiación, la técnica para la planificación de radioterapia, el tejido blanco y el volumen objetivo. Los estudios preclínicos y clínicos demostraron que la Gemcitabina tiene actividad radiosensibilizante. En un solo estudio, donde se administró dosis de 1000 mg/m 2 de Gemcitabina durante 6 semanas consecutivas como máximo, en forma concomitante con radiación terapéutica torácica a pacientes con cáncer de pulmón de células no pequeñas, se observó toxicidad significativa con posible riesgo de vida en la forma de mucositis severa, en especial esofagitis, y neumonitis, en particular en pacientes que recibían grandes volúmenes de radioterapia [mediana del volumen de tratamiento cm 3 ]. Estudios efectuados con posterioridad sugirieron que es factible administración concomitante de Gemcitabina en dosis más bajas y radioterapia con toxicidad previsible, por ejemplo, en un estudio de fase II en cáncer de pulmón de células no pequeñas, se administraron dosis de radiación torácica de 66Gy con Gemcitabina (600 mg/m 2, cuatro veces) y cisplatino (80 mg/m 2, dos veces) durante 6 semanas. Diversos estudios de fase I y II demostraron que es posible administrar 300 mg/m 2 /semana de Gemcitabina como agente único junto con radioterapia en pacientes con cáncer de pulmón de células no pequeñas y con cáncer de páncreas. Aún no se ha determinado cuál es el régimen óptimo para la administración segura de Gemcitabina con dosis terapéuticas de radiación en todo tipo de tumor. Radioterapia secuencial (administrada con más de 7 días de diferencia): El análisis de datos no indica ningún aumento de la toxicidad cuando la Gemcitabina es administrada con una diferencia mayor de 7 días antes o 6
7 después de la radiación, salvo hipersensibilidad a la radiación. Los datos sugieren que se puede reiniciar la administración de Gemcitabina después de que se hayan resuelto los efectos agudos de la radiación o, por lo menos, una semana después de la radiación. Se han informado lesiones por radiación en tejido blando (por ej. esofagitis, colitis y neumonitis) asociada con el uso tanto simultáneo como no simultáneo de Gemcitabina. 11. Alteraciones de Pruebas de Laboratorio: Deberá monitorearse el recuento de plaquetas, leucocitos y granulocitos en pacientes que reciben Gemcitabina antes de cada dosis. Debe tenerse en cuenta la suspensión o modificación de la terapia cuando se detecte depresión medular inducida por la droga. Se deben realizar pruebas de laboratorio de función renal y hepática en forma periódica. 12. Precaución y relación con efectos de Carcinogénesis, Mutagénesis, Teratogénesis y sobre la Fertilidad: La Gemcitabina produjo daño citogenético en un ensayo in vivo. La Gemcitabina induce mutación precoz en ensayos in vitro en linfoma de ratón (L5178Y). La Gemcitabina ha causado una hipoespermatogénesis dosis reversible y esquema de dosificación dependiente en ratones machos. Aunque los estudios en animales han demostrado un efecto de la Gemcitabina sobre la fertilidad masculina, no se ha observado ningún efecto en la fertilidad femenina. No se han realizado estudios a largo plazo en animales para evaluar el potencial carcinogénico de la Gemcitabina. 13. Dosis y Vía de Administración: Cáncer de Páncreas: Como agente único: PAMIGEN debe ser administrado por infusión intravenosa, una dosis de 1000 mg/m 2 durante 30 minutos, una vez a la semana durante 7 semanas, seguida de una semana de descanso. Las dosis siguientes deberán ser de 1 vez por semana durante 3 semanas y una de descanso. 7
8 Antes de cada dosis deben monitorearse el recuento de plaquetas, leucocitos y granulocitosis y, si fuera necesario, la dosis de PAMIGEN debe ser suspendida o reducida de acuerdo a la toxicidad hematológica observada. Recuento absoluto de granulocitos (x 10 6 /L) Recuento de plaquetas (x 10 6 /L) % de dosis completa >1.000 y > o <500 o < suspender Deberán monitorearse las funciones hepática y renal para detectar toxicidad no hematológica. La dosificación debe ser suspendida hasta que la toxicidad sea resuelta según la opinión del médico tratante. Cáncer del Tracto Biliar: En combinación: La Gemcitabina en combinación con cisplatino se recomienda utilizando cisplatino 70 mg/m 2 administrado en el día 1 como una infusión intravenosa, seguido por Gemcitabina 1250 mg/m 2 administrada en los días 1 y 8, de cada ciclo de 21 días, en una infusión intravenosa de 30 minutos. Este ciclo de 3 semanas es entonces repetido. Como agente único: La dosis recomendada de Gemcitabina es de 1000 mg/m 2, administrada en una infusión intravenosa de 30 minutos. La dosis deber ser repetida cada semana por tres semanas seguidas de un periodo de descanso de una semana. Este ciclo de cuatro semanas debe entonces repetirse. Carcinoma de Mama: Infusión intravenosa (no más de 30 minutos), 1250 mg/m 2 los días 1 y 8 de cada ciclo de 21 días. Paclitaxel debe ser administrado a 175 mg/m 2 el día 1 como una infusión intravenosa de 3 horas antes de la administración de Gemcitabina. Modificación de la dosis por toxicidad hematológica. Los ajustes de la dosis están basados sobre recuentos de leucocitos y plaquetas tomados el día 8 del tratamiento. La dosis de Gemcitabina debe 8
9 ser modificada de acuerdo con las siguientes directivas si se descubre supresión medular. Los pacientes deben tener una cuenta absoluta de granulocitos de cuando menos 1500 (x10 6 /L) antes de iniciar la combinación de Gemcitabina + Paclitaxel. TABLA I Día 8: Guías para la reducción de la dosis de PAMIGEN en combinación con Paclitaxel. Recuento de Granulocitos Absolutos ( x 10 6 /L) Recuento de Plaquetas ( x 10 6 /L) % de dosis completa 1200 y > o o <700 o < Detener Modificación de dosis para toxicidad no hematológica severa (grado 3 ó 4). Gemcitabina debe ser detenida o reducida en un 50% dependiendo del criterio del médico tratante para toxicidad no hematológica severa (grado 3 ó 4), con excepción de alopecia y náusea / vómitos. Para el ajuste de la dosis de paclitaxel, ver la información de ese producto. La dosis recomendada de Gemcitabina como agente único es de 1000 a 1200 mg/m 2 administrada en una infusión durante 30 minutos, en los días 1, 8 y 15 de cada ciclo de 28 días. Este ciclo de cuatro semanas debe entonces repetirse. La dosis en cada ciclo o dentro de un mismo ciclo se puede reducir en función de la toxicidad experimentada por el paciente. Cáncer de Pulmón de células no-pequeñas: Esquema de tres semanas en combinación con platinos: PAMIGEN debe administrarse por vía intravenosa a 1,250 mg/m 2 durante 30 minutos, en los días 1 y 8 de cada ciclo de 21 días. El cisplatino debe administrarse por vía intravenosa a una dosis de 100 mg/m 2 en el día 1, después de la infusión de Gemcitabina. La dosis en cada ciclo o dentro de un mismo ciclo se reduce en función de la toxicidad experimentada por el paciente. 9
10 PAMIGEN en combinación con carboplatino se recomienda utilizando una dosis de Gemcitabina de 1000 ó 1200 mg/m 2, administrada en los días 1 y 8 de cada ciclo de 21 días como una infusión intravenosa en 30 minutos. Después de Gemcitabina se administrará el carboplatino en el día 1 en forma consistente con un objetivo de área bajo la curva (AUC) de 5 mg/ml min. Esquema de cuatro semanas en combinación con platinos: PAMIGEN debe administrarse por vía intravenosa a 1000 mg/m 2 durante 30 minutos, en los días 1, 8 y 15 de cada ciclo de 28 días. El cisplatino debe administrase por vía intravenosa a una dosis de 100 mg/m 2 en el día 1, después de la infusión de Gemcitabina. La dosis en cada ciclo o dentro de un mismo ciclo se reduce en función de la toxicidad experimentada por el paciente. Esquema como agente único: La dosis recomendada de Gemcitabina es de 1000 mg/m 2, administrada en una infusión intravenosa de 30 minutos. Esta debe ser repetida una vez a la semana por tres semanas, seguidas de un período de descanso de una semana. Este ciclo de cuatro semanas deberá ser repetido posteriormente. La dosis en cada ciclo o dentro de un mismo ciclo se reduce en función de la toxicidad experimentada por el paciente. Cáncer de Ovario: En combinación Gemcitabina debe ser administrado de forma intravenosa a una dosis de 1000 mg/m 2 durante 30 minutos en los días 1 y 8 de cada ciclo de 21 días. El carboplatino debe ser administrado por vía intravenosa en el día 1, en forma consistente, con un objetivo de área bajo la curva (AUC) de 4 mg/ml min luego de la administración de Gemcitabina. Los pacientes deben ser monitoreados antes de cada dosis por medio de un recuento de glóbulos rojos y blancos, incluyendo recuentos diferenciales. Los pacientes deben tener un recuento absoluto de granulocitos 1500 x 106 / L y un recuento de plaquetas x 106 /L antes de cada ciclo. Como agente único: La dosis recomendada de Gemcitabina es de 800 a 1250 mg/m 2 administrada en una infusión durante 30 minutos, en los días 1, 8 y 15 de cada ciclo de 28 días. Este ciclo de cuatro semanas debe entonces repetirse. 10
11 Modificaciones en las Dosis: Los ajustes de dosis de Gemcitabina para toxicidad hematológica dentro de un ciclo de tratamiento, están basados en los recuentos de granulocitos y plaquetas tomados el día 8 de la terapia. Si se detecta supresión de la médula, se debe modificar la dosis de acuerdo a las instrucciones de la Tabla II. Tabla II: Instrucciones para la Reducción de Dosis en el Día 8 para PAMIGEN en Combinación con el Carboplatino Recuento absoluto de granulocitos ( x 10 6 /L) Recuento de plaquetas (x 10 6 /L) % de la dosis total 1500 y y <1000 y < Suspender En general, para toxicidad no hematológica severa (Grado 3 ó 4), excepto nausea y vómitos, la terapia con Gemcitabina debe ser detenida o disminuida en un 50%, dependiendo del criterio del médico tratante. Para ajustes en la dosis de carboplatino, se debe ver la información para prescribir. El ajuste de dosis de Gemcitabina en combinación con el carboplatino para ciclos subsiguientes, se basa en la toxicidad observada. La dosis de Gemcitabina en ciclos subsiguientes debe reducirse a 800 mg/m 2 los días 1 y 8, en caso de presentarse cualquiera de las toxicidades hematológicas: Recuentos absolutos de granulocitos < 500 x 10 6 /L por más de 5 días. Recuentos absolutos de granulocitos < 100 x 10 6 /L por más de 3 días. Neutropenia Febril. Plaquetas < x 10 6 /L. Demora del ciclo de más de una semana debido a la toxicidad. Cáncer de Vejiga: La dosis recomendada de Gemcitabina es de 1000 mg/m 2 administrada en una infusión durante 30 minutos, en los días 1, 8 y 15 de cada ciclo de 28 días. El cisplatino debe administrase por vía intravenosa a una dosis de 70 mg/m 2 en el día 1, después de la infusión de Gemcitabina, o en el día 2 de 11
12 cada ciclo de 28 días. Este ciclo de cuatro días debe entonces repetirse. La dosis en cada ciclo o dentro de un mismo ciclo se reduce en función de la toxicidad experimentada por el paciente. Un estudio clínico mostró mayor mielosupresión cuando el cisplatino se utilizó en dosis de 100 mg/m 2. Uso intravesical. La dosis recomendada para el uso intravesical de Gemcitabina en cáncer superficial de vejiga es de 2000 mg, diluidos, ya sea en 100 ó 50 ml de solución salina (concentración de 20 ó 40 mg/ml). El medicamento debe permanecer intravesicalmente por espacio de 60 minutos, una vez a la semana, hasta por 6 semanas consecutivas. Las concentraciones no deben exceder 40 mg/ml y las reducciones de la dosis pueden ser aplicadas con base en la toxicidad experimentada por el paciente. Cáncer de Cérvix: Tratamiento Neoadyuvante y Enfermedad Metastásica. La Gemcitabina en combinación con cisplatino se recomienda utilizando cisplatino 70 mg/m 2 administrado en el día 1, seguido por Gemcitabina 1250 mg/m 2 administrado en los días 1 y 8, cada 21 días. Este ciclo de 3 semanas es entonces repetido. Terapia concomitante con radiación. La Gemcitabina en combinación con cisplatino se recomienda utilizando cisplatino 40 mg/m 2 seguido inmediatamente por Gemcitabina 125 mg/m 2 por infusión intravenosa una vez a la semana por 6 semanas (días 1, 8, 15, 22, 29 y 36), 1 a 2 horas antes de la radioterapia pélvica concomitante. La radioterapia debe consistir de 50.4 Gy mediante radiación externa administrados al campo completo de radiación en 28 fracciones, 1.8 Gy/día, 5 días / semana, durante las 6 semanas de quimioterapia. Control de dosificación: Insuficiencia hepática y renal: La Gemcitabina deberá ser empleada con precaución en pacientes con insuficiencia hepática o con función renal deteriorada. Una insuficiencia renal 12
13 moderada (tasa de filtración glomerular de 30 a 80 ml/min) no ha tenido un efecto consistente y significativo sobre la farmacocinética de la Gemcitabina. Pacientes en edad avanzada: No hay evidencia que sugiera que los ajustes de las dosis son necesarios en pacientes de edad avanzada, aunque la depuración y vida media de la Gemcitabina resultan afectadas por la edad. Niños: La Gemcitabina no ha sido estudiada en niños. 14. Sobredosificación e ingesta accidental: Manifestaciones, manejo y antídoto: No existe un antídoto para la sobredosis de Gemcitabina. Las dosis tan altas como 5,7 g/m 2 han sido administradas mediante infusión IV cerca de 30 minutos, cada dos semanas con toxicidad clínicamente aceptable. En el caso de sospecha de sobredosis, deberá monitorearse al paciente con recuentos de sangre adecuados y deberá recibir terapia de apoyo, en la forma que resulte necesaria. 15. Presentaciones: Caja con 1 frasco ámpula con liofilizado con 200 mg. Caja con 1 frasco ámpula con liofilizado con 1000 mg. 16. Recomendaciones para el Almacenamiento: Consérvese a temperatura ambiente a no más de 30 C. Desechar si no se utiliza en un período de 2 horas después de haberse reconstituido. Si no se administra todo el producto deséchese el sobrante. 17. Leyendas de Protección: Vía de administración: Intravenosa. Dosis: La que el médico señale. Léase instructivo anexo. 13
14 Su venta requiere receta médica. Este medicamento es de alto riesgo. No se deje al alcance de los niños. Este medicamento solo debe ser administrado bajo la supervisión de médicos especialistas en Oncología y con experiencia en quimioterapia antineoplásica. No se administre si el cierre ha sido violado. No se administre si la solución no es transparente, si contiene partículas en suspensión o sedimentos. No se use en el embarazo y lactancia. Literatura exclusiva para médicos. 18. Nombre del Laboratorio y Dirección: Hecho en Paraguay por: FARMACEUTICA PARAGUAYA, S.A. Waldino Lovera esquina Del Carmen, Fernando de la Mora, Paraguay. Distribuido en México por: ASOFARMA DE MEXICO, S.A. DE C.V. Calz. México-Xochimilco N 43, Col. San Lorenzo Huipulco, C.P , Delegación. Tlalpan, D.F. México. 19. Número de Registro del Medicamento, Número de Autorización de la IPP: Reg. N SSA IV IPP N CT050566/ Oct11 14
La citarabina, ARA-C o arabinósido de citocina es un antimetabolito específico de la fase S del ciclo celular; impide la síntesis de ADN.
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: MEDSARA 2. Nombre Genérico: CITARABINA 3. Forma Farmacéutica y Formulación: SOLUCIÓN INYECTABLE Cada frasco ámpula contiene: Citarabina.. 500 mg
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: MEDSARA 2. Nombre Genérico: CITARABINA 3. Forma Farmacéutica y Formulación: SOLUCIÓN INYECTABLE Cada frasco ámpula contiene: Citarabina.. 500 mg
Paracetamol DC 90 equivalente a mg de Paracetamol
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre comercial: TAFIROL 2. Nombre genérico PARACETAMOL 3. Forma farmacéutica y formulación: Cada tableta contiene: Paracetamol DC 90 equivalente a. 1000 mg de Paracetamol
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre comercial: TAFIROL 2. Nombre genérico PARACETAMOL 3. Forma farmacéutica y formulación: Cada tableta contiene: Paracetamol DC 90 equivalente a. 1000 mg de Paracetamol
INFORMACIÓN PARA PRESCRIBIR AMPLIA
 INFORMACIÓN PARA PRESCRIBIR AMPLIA IFADEX MR Ifosfamida Laboratorios Cryopharma, S.A. de C.V INFORMACIÓN PARA PRESCRIBIR AMPLIA 1.- NOMBRE COMERCIAL Y GENÉRICO: 1.1 Nombre comercial: IFADEX MR 1.2 Nombre
INFORMACIÓN PARA PRESCRIBIR AMPLIA IFADEX MR Ifosfamida Laboratorios Cryopharma, S.A. de C.V INFORMACIÓN PARA PRESCRIBIR AMPLIA 1.- NOMBRE COMERCIAL Y GENÉRICO: 1.1 Nombre comercial: IFADEX MR 1.2 Nombre
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
La vida media del salbutamol a nivel plasmático es de 2 a 7 hrs.
 I. DENOMINACIÓN DISTINTIVA. SIBILEX II. DENOMINACIÓN GENÉRICA. Loratadina, Salbutamol, Ambroxol. III. FORMA FARMACEUTICA Y FORMULACION Solución : Cada 100 ml contiene: Clorhidrato de Ambroxol... 150 mg
I. DENOMINACIÓN DISTINTIVA. SIBILEX II. DENOMINACIÓN GENÉRICA. Loratadina, Salbutamol, Ambroxol. III. FORMA FARMACEUTICA Y FORMULACION Solución : Cada 100 ml contiene: Clorhidrato de Ambroxol... 150 mg
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
Estadíos tumor maligno de cuello uterino
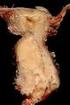 TUMOR MALIGNO DE CUELLO UTERINO Codificación CIE10 C53 tumor maligno del cuello del útero Problema: El cáncer cervical usualmente es un carcinoma de células escamosas (70% de todos los cánceres cervicales),
TUMOR MALIGNO DE CUELLO UTERINO Codificación CIE10 C53 tumor maligno del cuello del útero Problema: El cáncer cervical usualmente es un carcinoma de células escamosas (70% de todos los cánceres cervicales),
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
ETOPOSIDO 100mg/5mL. 1. Identificación del Medicamento. Nombre Comercial. Etoposido 100mg/5mL Solución Inyectable. Nombre Genérico.
 ETOPOSIDO 100mg/5mL 1. Identificación del Medicamento Nombre Comercial Etoposido 100mg/5mL Solución Inyectable Nombre Genérico Etoposido Concentración 100mg/5mL Denominación Común Internacional Etoposido
ETOPOSIDO 100mg/5mL 1. Identificación del Medicamento Nombre Comercial Etoposido 100mg/5mL Solución Inyectable Nombre Genérico Etoposido Concentración 100mg/5mL Denominación Común Internacional Etoposido
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg COMPRIMIDOS RECUBIERTOS ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg COMPRIMIDOS RECUBIERTOS ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Comprimidos
Biotransformación: Se efectúa en el hígado, la cual incluye su activación y posterior
 INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: IFOMIDA 2. Nombre Genérico: IFOSFAMIDA 3. Forma Farmacéutica y Formulación: Solución Inyectable Cada frasco ámpula con liofilizado contiene: Ifosfamida...
INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: IFOMIDA 2. Nombre Genérico: IFOSFAMIDA 3. Forma Farmacéutica y Formulación: Solución Inyectable Cada frasco ámpula con liofilizado contiene: Ifosfamida...
INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. NOMBRE COMERCIAL Y GENÉRICO ADVIL IBUPROFENO. 2. FORMA FARMACÉUTICA Y FORMULACION Tabletas
 INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. NOMBRE COMERCIAL Y GENÉRICO ADVIL IBUPROFENO 2. FORMA FARMACÉUTICA Y FORMULACION Tabletas Fórmula: cada gragea contiene: Ibuprofeno Excipiente c.b.p. 200 mg 1 tableta
INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. NOMBRE COMERCIAL Y GENÉRICO ADVIL IBUPROFENO 2. FORMA FARMACÉUTICA Y FORMULACION Tabletas Fórmula: cada gragea contiene: Ibuprofeno Excipiente c.b.p. 200 mg 1 tableta
FLUCONAZOL. Solución para infusión IV. 200 mg. ALFARMA S.A., PANAMÁ, REPÚBLICA DE PANAMÁ. Fabricante, país:
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: FLUCONAZOL Solución para infusión IV 200 mg Estuche por un frasco de PEBD con 100 ml. Titular
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: FLUCONAZOL Solución para infusión IV 200 mg Estuche por un frasco de PEBD con 100 ml. Titular
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 CLORANFENICOL 250 mg/5 ml SUSPENSION ANTIINFECCIOSO Página 1 CLORANFENICOL 250 mg/5 ml Suspensión Principio Activo
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 CLORANFENICOL 250 mg/5 ml SUSPENSION ANTIINFECCIOSO Página 1 CLORANFENICOL 250 mg/5 ml Suspensión Principio Activo
INFORMACION PARA PRESCRIBIR AMPLIA IPP-A K-ASMAL*
 INFORMACION PARA PRESCRIBIR AMPLIA IPP-A K-ASMAL* FORMA FARMACEUTICA Y FORMULACION Jarabe Cada 100 mi contienen: Fumarato ácido de Ketotifeno equivalente a... 20 mg de Ketotifeno vehículo, c.b.p... 100
INFORMACION PARA PRESCRIBIR AMPLIA IPP-A K-ASMAL* FORMA FARMACEUTICA Y FORMULACION Jarabe Cada 100 mi contienen: Fumarato ácido de Ketotifeno equivalente a... 20 mg de Ketotifeno vehículo, c.b.p... 100
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COTRIMOXAZOL 200/40/5 ml SUSPENSIÓN ANTIINFECCIOSO-ANTIBACTERIANO Página 1 COTRIMOXAZOL 200/40/5 ml Suspensión Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COTRIMOXAZOL 200/40/5 ml SUSPENSIÓN ANTIINFECCIOSO-ANTIBACTERIANO Página 1 COTRIMOXAZOL 200/40/5 ml Suspensión Principio
INFORMACION PARA RESCRIBIR AMPLIA
 INFORMACION PARA RESCRIBIR AMPLIA BEZAFISAL MR BEZAFIBRATO Agente antilipidémico Laboratorios Cryopharma, S.A. de C.V INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. NOMBRE COMERICAL Y GENÉRICO 1.1 Nombre comercial:
INFORMACION PARA RESCRIBIR AMPLIA BEZAFISAL MR BEZAFIBRATO Agente antilipidémico Laboratorios Cryopharma, S.A. de C.V INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. NOMBRE COMERICAL Y GENÉRICO 1.1 Nombre comercial:
LLD Abreviado de Zoloft. Todo medicamento debe conservarse fuera del alcance de los niños.
 LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
Información Para Prescribir Amplia. Aquasol* AD Vitamina A y D2 Cápsulas
 Confidencial Página 1/5 Información Para Prescribir Amplia Aquasol* AD Vitamina A y D2 Cápsulas FORMA FARMACÉUTICA Y FORMULACIÓN: Cada Cápsula contiene: Palmitato de retinol equivalente a 6000UI De retinol
Confidencial Página 1/5 Información Para Prescribir Amplia Aquasol* AD Vitamina A y D2 Cápsulas FORMA FARMACÉUTICA Y FORMULACIÓN: Cada Cápsula contiene: Palmitato de retinol equivalente a 6000UI De retinol
FICHA TECNICA. Tratamiento de la intoxicación por Amanita phalloides.
 FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
Eni* Tabletas e Inyectable. Ciprofloxacino
 Tabletas e Inyectable Ciprofloxacino Descripción Es ciprofloxacino, la fluoroquinolona bactericida potente, con amplio espectro antibacteriano que incluye grampositivos y gramnegativos. Tiene alta eficacia
Tabletas e Inyectable Ciprofloxacino Descripción Es ciprofloxacino, la fluoroquinolona bactericida potente, con amplio espectro antibacteriano que incluye grampositivos y gramnegativos. Tiene alta eficacia
INFORMACION PARA PRESCRIBIR REDUCIDA
 INFORMACION PARA PRESCRIBIR REDUCIDA 1. Nombre Comercial: NABRATIN 2. Nombre Genérico: CLOPIDOGREL 3. Forma Farmacéutica y Formulación: Tabletas. Cada tableta contiene: Bisulfato de Clopidogrel equivalente
INFORMACION PARA PRESCRIBIR REDUCIDA 1. Nombre Comercial: NABRATIN 2. Nombre Genérico: CLOPIDOGREL 3. Forma Farmacéutica y Formulación: Tabletas. Cada tableta contiene: Bisulfato de Clopidogrel equivalente
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 SUPOSITORIO BRONQUIAL LACTANTE SUPOSITORIO ANALGÉSICO, EXPECTORANTE BALSÁMICO Página 1 SUPOSITORIO BRONQUIAL LACTANTE
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 SUPOSITORIO BRONQUIAL LACTANTE SUPOSITORIO ANALGÉSICO, EXPECTORANTE BALSÁMICO Página 1 SUPOSITORIO BRONQUIAL LACTANTE
ENOXPRIM. Solución inyectable. Solución inyectable estéril, libre de pirógenos, contenida en jeringas pre-llenadas listas para usarse.
 ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
ADVIL Ibuprofeno Cápsulas ADVIL. Ibuprofeno
 INFORMACIÓN PARA PRESCRIBIR AMPLIA ADVIL Cápsulas 1. NOMBRE COMERCIAL 2. NOMBRE GENÉRICO ADVIL 3. FORMA FARMACÉUTICA Y FORMULACIÓN Cápsulas Fórmula: cada cápsula contiene: Excipiente c.b.p. 200 mg ó 400
INFORMACIÓN PARA PRESCRIBIR AMPLIA ADVIL Cápsulas 1. NOMBRE COMERCIAL 2. NOMBRE GENÉRICO ADVIL 3. FORMA FARMACÉUTICA Y FORMULACIÓN Cápsulas Fórmula: cada cápsula contiene: Excipiente c.b.p. 200 mg ó 400
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. ACICLOVIR COMBIX 800 mg Comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ACICLOVIR COMBIX 800 mg Comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido de 800 mg contiene: Aciclovir (DCI) 800 mg. 3. FORMA FARMACÉUTICA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ACICLOVIR COMBIX 800 mg Comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido de 800 mg contiene: Aciclovir (DCI) 800 mg. 3. FORMA FARMACÉUTICA
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 BROMHEXINA 4 mg/5 ml JARABE MUCOLÍTICO, EXPECTORANTE Página 1 BROMHEXINA 4 mg/5 ml Jarabe Principio Activo Bromhexina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 BROMHEXINA 4 mg/5 ml JARABE MUCOLÍTICO, EXPECTORANTE Página 1 BROMHEXINA 4 mg/5 ml Jarabe Principio Activo Bromhexina
MEGAPLEX 160mg. Nombre Comercial. Megaplex 160mg. Nombre Genérico. Acetato de Megestrol 160mg. Concentración. 160mg. Denominación Común Internacional
 MEGAPLE 160mg 1. Identificación del Medicamento Nombre Comercial Megaplex 160mg Nombre Genérico Acetato de Megestrol 160mg Concentración 160mg Denominación Común Internacional Acetato de Megestrol N Registro
MEGAPLE 160mg 1. Identificación del Medicamento Nombre Comercial Megaplex 160mg Nombre Genérico Acetato de Megestrol 160mg Concentración 160mg Denominación Común Internacional Acetato de Megestrol N Registro
CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG
 CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG COMPOSICIÓN Por ml: Principio activo: Carboplatino (D.C.I.) 10 mg Excipientes: Agua para inyección c.s. FORMA FARMACÉUTICA Y
CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG COMPOSICIÓN Por ml: Principio activo: Carboplatino (D.C.I.) 10 mg Excipientes: Agua para inyección c.s. FORMA FARMACÉUTICA Y
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
Se recomiendan las siguientes modificaciones en caso de disfunción renal.
 1. NOMBRE DEL MEDICAMENTO ACICLOVIR TEDEC 25 mg/ml solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla contiene: Aciclovir (D.O.E.) 250 mg Para excipientes, ver 6.1. 3. FORMA
1. NOMBRE DEL MEDICAMENTO ACICLOVIR TEDEC 25 mg/ml solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla contiene: Aciclovir (D.O.E.) 250 mg Para excipientes, ver 6.1. 3. FORMA
FICHA TÉCNICA. Por sobre: Acetato de calcio, 2,5 g (equivale a 635 mg de calcio), almidón de maíz, manitol (E421)
 FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO ROYEN 500 mg cápsula dura. ROYEN 2,5 g polvo para suspensión oral. 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ROYEN 500 mg cápsula dura. Por cápsula: Acetato de
FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO ROYEN 500 mg cápsula dura. ROYEN 2,5 g polvo para suspensión oral. 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ROYEN 500 mg cápsula dura. Por cápsula: Acetato de
Cada capsulas contiene: Temozolomina. 20, 100 y 250 mg Excipiente, c.b.p.. 1 cápsula.
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre comercial: RUBRUM ASF 2. Nombre Genérico: ANTINEOPLASICO 3. Forma Farmacéutica y Formulación: Capsulas Cada capsulas contiene: Temozolomina. 20, 100 y 250 mg
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre comercial: RUBRUM ASF 2. Nombre Genérico: ANTINEOPLASICO 3. Forma Farmacéutica y Formulación: Capsulas Cada capsulas contiene: Temozolomina. 20, 100 y 250 mg
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO. 1. NOMBRE DEL MEDICAMENTO Dextrometorfano Hidrobromuro Farmalider 15 mg cápsulas blandas
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Dextrometorfano Hidrobromuro Farmalider 15 mg cápsulas blandas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextrometorfano
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Dextrometorfano Hidrobromuro Farmalider 15 mg cápsulas blandas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextrometorfano
Excipientes con efecto conocido: propilenglicol 200 mg/g
 FELDENE* 0.5% (Piroxicam) Gel 1. NOMBRE DEL PRODUCTO FARMACÉUTICO FELDENE* 0.5% Gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 gramos de FELDENE 0.5% Gel contiene: Piroxicam 0.5 g Excipientes con
FELDENE* 0.5% (Piroxicam) Gel 1. NOMBRE DEL PRODUCTO FARMACÉUTICO FELDENE* 0.5% Gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 gramos de FELDENE 0.5% Gel contiene: Piroxicam 0.5 g Excipientes con
Información Para Prescripción Amplia EFUDIX
 Información Para Prescripción Amplia EFUDIX Crema Fluorouracilo FORMA FARMACÉUTICA Y FORMULACIÓN: Cada 100 g contienen: Fluorouracilo 5 g. Excipiente cbp 100 g. INDICACIONES TERAPÉUTICAS: Dermatológicas:
Información Para Prescripción Amplia EFUDIX Crema Fluorouracilo FORMA FARMACÉUTICA Y FORMULACIÓN: Cada 100 g contienen: Fluorouracilo 5 g. Excipiente cbp 100 g. INDICACIONES TERAPÉUTICAS: Dermatológicas:
Cada TABLETA contiene: Paracetamol DC 90 equivalente a mg de paracetamol Clorzoxazona. 250 mg Excipiente, c.b.p... 1 tableta.
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: TAFIROL FLEX 2. Nombre Genérico: CLORZOXAZONA PARACETAMOL 3. Forma Farmacéutica y Formulación: TABLETA Cada TABLETA contiene: Paracetamol DC 90 equivalente
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: TAFIROL FLEX 2. Nombre Genérico: CLORZOXAZONA PARACETAMOL 3. Forma Farmacéutica y Formulación: TABLETA Cada TABLETA contiene: Paracetamol DC 90 equivalente
Gota! FARMACOS HIPOURICEMIANTES! Y ANTIGOTOSOS! Abordaje farmacológico! Gota!
 Gota FARMACOS HIPOURICEMIANTES Y ANTIGOTOSOS Trastorno caracterizado por: Hiperuricemia Depósito de cristales de urato en la articulación sinovial Inflamación articular aguda Tofos (depósito de urato)
Gota FARMACOS HIPOURICEMIANTES Y ANTIGOTOSOS Trastorno caracterizado por: Hiperuricemia Depósito de cristales de urato en la articulación sinovial Inflamación articular aguda Tofos (depósito de urato)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 64 mg de magnesio (en forma de 550 mg de cloruro de magnesio,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 64 mg de magnesio (en forma de 550 mg de cloruro de magnesio,
DOXORUBIN 200mg/100mL
 DOORUBIN 200mg/100mL 1. IDENTIFICACIÓN DEL PRODUCTO Nombre Comercial Doxorubin Nombre Genérico Doxorubicina Concentración 200mg/100mL Denominación Común Internacional Doxorubicina HCl N Registro Invima
DOORUBIN 200mg/100mL 1. IDENTIFICACIÓN DEL PRODUCTO Nombre Comercial Doxorubin Nombre Genérico Doxorubicina Concentración 200mg/100mL Denominación Común Internacional Doxorubicina HCl N Registro Invima
Topotecán Actavis 1 mg polvo para concentrado para solución para perfusión EFG
 1. NOMBRE DEL MEDICAMENTO Topotecán Actavis 1 mg polvo para concentrado para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene 1 mg de topotecán (como hidrocloruro).
1. NOMBRE DEL MEDICAMENTO Topotecán Actavis 1 mg polvo para concentrado para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial contiene 1 mg de topotecán (como hidrocloruro).
OPCIONES ESTANDAR DE TRATAMIENTO carcinoma basocelular y escamocelular:
 TUMOR MALIGNO DE LA PIEL Codificación CIE10 D04 carcinoma in situ de la piel Problema: El carcinoma basocelular es la forma más común de cáncer de la piel (65%) y el carcinoma escamocelular (21%) es el
TUMOR MALIGNO DE LA PIEL Codificación CIE10 D04 carcinoma in situ de la piel Problema: El carcinoma basocelular es la forma más común de cáncer de la piel (65%) y el carcinoma escamocelular (21%) es el
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO
 ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 25 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN BROMOCRIPTINA 4.2 Posología y forma
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 25 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN BROMOCRIPTINA 4.2 Posología y forma
MACROGOL 3350 BICARBONATO DE SODIO CLORURO DE SODIO CLORURO DE POTASIO
 Autorizada por Secretaría de Salud el 28 septiembre 2011 INFORMACION PARA PRESCRIBIR AMPLIA: 1. Nombre comercial: NULYTELY 2. Nombre genérico: MACROGOL 3350 BICARBONATO DE SODIO CLORURO DE SODIO CLORURO
Autorizada por Secretaría de Salud el 28 septiembre 2011 INFORMACION PARA PRESCRIBIR AMPLIA: 1. Nombre comercial: NULYTELY 2. Nombre genérico: MACROGOL 3350 BICARBONATO DE SODIO CLORURO DE SODIO CLORURO
Repafet. Rupatadina Tabletas. Rupatadina II.- DENOMINACIÓN GENÉRICA: III.- FORMA FARMACÉUTICA Y FORMULACIÓN:
 Repafet Rupatadina Tabletas II.- DENOMINACIÓN GENÉRICA: Rupatadina III.- FORMA FARMACÉUTICA Y FORMULACIÓN: Cada tableta contiene: Fumarato de Rupatadina equivalente a... 10 mg de Rupatadina Excipiente
Repafet Rupatadina Tabletas II.- DENOMINACIÓN GENÉRICA: Rupatadina III.- FORMA FARMACÉUTICA Y FORMULACIÓN: Cada tableta contiene: Fumarato de Rupatadina equivalente a... 10 mg de Rupatadina Excipiente
FICHA TECNICA. Adultos en prediálisis o en diálisis: 1 dosis (40 µg) de 1 ml en cada inyección.
 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 40 mg Vacuna recombinante antihepatitis B. FICHA TECNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 40microgramos/ ml, suspensión inyectable
1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 40 mg Vacuna recombinante antihepatitis B. FICHA TECNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 40microgramos/ ml, suspensión inyectable
Mujeres - De R00 a R99
 R00. Anormalidades del latido cardíaco R01. Soplos y otros sonidos cardíacos R02. Gangrena, no clasificada en otra R03. Lectura de presión sanguínea anormal, sin diagnóstico R04. Hemorragias de las vías
R00. Anormalidades del latido cardíaco R01. Soplos y otros sonidos cardíacos R02. Gangrena, no clasificada en otra R03. Lectura de presión sanguínea anormal, sin diagnóstico R04. Hemorragias de las vías
1. NOMBRE DEL MEDICAMENTO. RANITIDINA 50 mg PREDILUIDA GRIFOLS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. Principio activo
 1. NOMBRE DEL MEDICAMENTO RANITIDINA 50 mg PREDILUIDA GRIFOLS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo Ranitidina (DOE) 50 mg (correspondientes a 55,8 mg de hidrocloruro de ranitidina)
1. NOMBRE DEL MEDICAMENTO RANITIDINA 50 mg PREDILUIDA GRIFOLS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo Ranitidina (DOE) 50 mg (correspondientes a 55,8 mg de hidrocloruro de ranitidina)
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Winthrop20 mg/1 ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Winthrop20 mg/1 ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA DE INFORMACIÓN AL PACIENTE: Simvastatina
 FICHA DE INFORMACIÓN AL PACIENTE: Simvastatina 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Hipolipemiante, inhibidor de la enzima hidroximetil-glutaril-coa-reductasa.. 1.2 Cómo actúa este fármaco: Inhibe
FICHA DE INFORMACIÓN AL PACIENTE: Simvastatina 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Hipolipemiante, inhibidor de la enzima hidroximetil-glutaril-coa-reductasa.. 1.2 Cómo actúa este fármaco: Inhibe
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
INFORMACIÓN PARA PRESCRIBIR AMPLIA
 IPPA-ciclofosfamida INFORMACIÓN PARA PRESCRIBIR AMPLIA C R Y O F A X O L MR Ciclofosfamida LABORATORIOS CRYOPHARMA, S.A DE C.V 1 de 5 1. NOMBRE COMERCIAL Y GENÉRICO INFORMACIÓN PARA PRESCRIBIR AMPLIA 1.1
IPPA-ciclofosfamida INFORMACIÓN PARA PRESCRIBIR AMPLIA C R Y O F A X O L MR Ciclofosfamida LABORATORIOS CRYOPHARMA, S.A DE C.V 1 de 5 1. NOMBRE COMERCIAL Y GENÉRICO INFORMACIÓN PARA PRESCRIBIR AMPLIA 1.1
Información para prescribir amplia FLUANXOL DEPOT Flupentixol Solución inyectable
 Información para prescribir amplia FLUANXOL DEPOT Flupentixol Solución inyectable 1. DENOMINACIÓN DISTINTIVA: Fluanxol Depot 2. DENOMINACIÓN GENÉRICA: Flupentixol 3. FORMA FARMACÉUTICA Y FORMULACIÓN Solución
Información para prescribir amplia FLUANXOL DEPOT Flupentixol Solución inyectable 1. DENOMINACIÓN DISTINTIVA: Fluanxol Depot 2. DENOMINACIÓN GENÉRICA: Flupentixol 3. FORMA FARMACÉUTICA Y FORMULACIÓN Solución
PROSPECTO. CEFTRIAXONA REIG JOFRÉ 1 g IM. Polvo y disolvente para solución inyectable. E.F.G. Ceftriaxona (D.C.I.)
 PROSPECTO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico.
PROSPECTO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico.
- Como disolvente de medicamentos en polvo o liofilizados, previamente a su administración. - Como diluyente de soluciones y/o medicamentos.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables SERRACLINICS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml contienen agua para preparaciones inyectables. ph: 5,0-7,0
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables SERRACLINICS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml contienen agua para preparaciones inyectables. ph: 5,0-7,0
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Teva 20 mg /0,72 ml concentrado y disolvente para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Docetaxel Teva 20 mg /0,72 ml concentrado y disolvente para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA
INSTRUCTIVO REGISTRO PARA LAS ATENCIONES DE QUIMIOTERAPIA
 1. OBJETIVO: Establecer una orientación clara y precisa que permita oficializar el sistema de registro de los tratamientos de quimioterapia en adultos del Hospital Regional de Arica Dr. Juan Noé Crevani,
1. OBJETIVO: Establecer una orientación clara y precisa que permita oficializar el sistema de registro de los tratamientos de quimioterapia en adultos del Hospital Regional de Arica Dr. Juan Noé Crevani,
COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS
 COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS 1. SOLICITUD DEL FÁRMACO Principio activo solicitado: (erbitux
COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS 1. SOLICITUD DEL FÁRMACO Principio activo solicitado: (erbitux
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA. Gotas Óticas. Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g.
 DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
4.2 Indicaciones de uso, especificando las especies a las que va destinado
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Loxicom 5 mg/ml solución inyectable para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Principio activo: Meloxicam Excipientes:
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Loxicom 5 mg/ml solución inyectable para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Principio activo: Meloxicam Excipientes:
FICHA TÉCNICA. Tratamiento de la incontinencia urinaria asociada a la insuficiencia del esfínter uretral en la perra.
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CONTINENZA 40 mg/ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CONTINENZA 40 mg/ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Docetaxel Actavis 20 mg/ml concentrado para solución para perfusión
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Docetaxel Actavis 20 mg/ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Docetaxel Actavis 20 mg/ml concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Potactasol 1 mg polvo para concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Potactasol 1 mg polvo para concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Nombre: Lincomicina Condición de venta: con receta médica Clasificación: antibiotico Disponible en: Nombres de marca:
 Nombre: Lincomicina Condición de venta: con receta médica Clasificación: antibiotico Disponible en: Nombres de marca: Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene
Nombre: Lincomicina Condición de venta: con receta médica Clasificación: antibiotico Disponible en: Nombres de marca: Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA. Azelastina hidrocloruro al 0,05% (0,5 mg/ml). Cada gota contiene 0,015 mg de azelastina hidrocloruro
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Azelastina MABO 0,5 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Azelastina hidrocloruro al 0,05% (0,5
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Azelastina MABO 0,5 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Azelastina hidrocloruro al 0,05% (0,5
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ERGOTAMINA + CAFEÍNA 1/100 mg COMPRIMIDOS RECUBIERTOS ANALGÉSICO, ANTIMIGRAÑOSO Página 1 ERGOTAMINA + CAFEÍNA 1/100
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ERGOTAMINA + CAFEÍNA 1/100 mg COMPRIMIDOS RECUBIERTOS ANALGÉSICO, ANTIMIGRAÑOSO Página 1 ERGOTAMINA + CAFEÍNA 1/100
GO Sildenafil Tabletas
 GO Sildenafil Tabletas FORMA FARMACÉUTICA Y FORMULACIÓN: Cada TABLETA contiene: Citrato de sildenafil equivalente a 25, 50 y 100 mg de sildenafil Excipiente cbp 1 tableta Cada TABLETA (orodispersable)
GO Sildenafil Tabletas FORMA FARMACÉUTICA Y FORMULACIÓN: Cada TABLETA contiene: Citrato de sildenafil equivalente a 25, 50 y 100 mg de sildenafil Excipiente cbp 1 tableta Cada TABLETA (orodispersable)
PROPUESTA DE FICHA TÉCNICA
 PROPUESTA DE FICHA TÉCNICA 1. DENOMINACION DEL MEDICAMENTO EBASTINA COMBIX 10 mg comprimidos recubiertos con película EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película
PROPUESTA DE FICHA TÉCNICA 1. DENOMINACION DEL MEDICAMENTO EBASTINA COMBIX 10 mg comprimidos recubiertos con película EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto con película
Para la lista completa de excipientes, véase la sección Indicaciones de uso, especificando las especies de destino
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 2 mg/ml solución inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam Excipientes: Etanol 2 mg
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 2 mg/ml solución inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam Excipientes: Etanol 2 mg
La osmolaridad calculada de la solución es de 154 mosm/l y el ph de 4,5-7,0. El contenido teórico en sodio y en cloruro es de 77 mmol/l.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Cloruro de Sodio Grifols 0,45% solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml de solución contienen: Cloruro de sodio, 0,45 g La osmolaridad
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Cloruro de Sodio Grifols 0,45% solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml de solución contienen: Cloruro de sodio, 0,45 g La osmolaridad
MARCAR CON UNA X LA RESPUESTA CORRECTA
 Unidad Didáctica 3. Test de evaluación MARCAR CON UNA X LA RESPUESTA CORRECTA 1. Cuál de las siguientes afirmaciones es correcta, en relación con antidepresivos tricíclicos? A. En una persona sana tiene
Unidad Didáctica 3. Test de evaluación MARCAR CON UNA X LA RESPUESTA CORRECTA 1. Cuál de las siguientes afirmaciones es correcta, en relación con antidepresivos tricíclicos? A. En una persona sana tiene
FICHA TECNICA. 1. Denominación del medicamento RHINOSPRAY ANTIALERGICO
 FICHA TECNICA 1. Denominación del medicamento RHINOSPRAY ANTIALERGICO 2. Composición Cada 100 ml contiene: Tramazolina (D.C.I.) clorhidrato Clorfenamina (D.C.I.) maleato 0,118 g 0,505 g 3. Forma farmacéutica
FICHA TECNICA 1. Denominación del medicamento RHINOSPRAY ANTIALERGICO 2. Composición Cada 100 ml contiene: Tramazolina (D.C.I.) clorhidrato Clorfenamina (D.C.I.) maleato 0,118 g 0,505 g 3. Forma farmacéutica
FICHA TECNICA DE URINORM BENZBROMARONA 1. DENOMINACIÓN DEL MEDICAMENTO. URINORM, 100 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TECNICA DE URINORM BENZBROMARONA 1. DENOMINACIÓN DEL MEDICAMENTO URINORM, 100 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Benzbromarona (D.C.I.)...100 mg
FICHA TECNICA DE URINORM BENZBROMARONA 1. DENOMINACIÓN DEL MEDICAMENTO URINORM, 100 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Benzbromarona (D.C.I.)...100 mg
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 SILDENAFIL PARA HOMBRES 50 mg COMPRIMIDOS RECUBIERTOS PARA LA DISFUNCIÓN ERÉCTIL Página 1 SILDENAFIL PARA HOMBRES
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 SILDENAFIL PARA HOMBRES 50 mg COMPRIMIDOS RECUBIERTOS PARA LA DISFUNCIÓN ERÉCTIL Página 1 SILDENAFIL PARA HOMBRES
MINOVAG MR NOVAG. Comprimidos
 MINOVAG MR NOVAG Comprimidos Denominación genérica: Secnidazol.!Forma farmacéutica y formulación: Comprimidos. Cada comprimido contiene: secnidazol 500 mg. Excipiente cbp 1 comprimido.!indicaciones terapéuticas:
MINOVAG MR NOVAG Comprimidos Denominación genérica: Secnidazol.!Forma farmacéutica y formulación: Comprimidos. Cada comprimido contiene: secnidazol 500 mg. Excipiente cbp 1 comprimido.!indicaciones terapéuticas:
Debe utilizarse la dosis eficaz mínima durante el periodo más corto posible a fin de reducir las reacciones adversas.
 ANEXO III 1 ENMIENDAS A INCLUIR EN LAS SECCIONES RELEVANTES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTIENEN NIMESULIDA (FORMULACIONES SISTÉMICAS) El texto añadido aparece
ANEXO III 1 ENMIENDAS A INCLUIR EN LAS SECCIONES RELEVANTES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTIENEN NIMESULIDA (FORMULACIONES SISTÉMICAS) El texto añadido aparece
Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp
 Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp Enf. María Guadalupe Vega Jefe de Piso Unidad de Terapia Intensiva Hospital General Las Américas, Ecatepec
Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp Enf. María Guadalupe Vega Jefe de Piso Unidad de Terapia Intensiva Hospital General Las Américas, Ecatepec
4.2 Indicaciones de uso, especificando las especies a las que va destinado
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 1 mg comprimidos masticables para perros Metacam 2,5 mg comprimidos masticables para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 1 mg comprimidos masticables para perros Metacam 2,5 mg comprimidos masticables para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
Bonadoxina Meclozina/Piridoxina Tableta 25mg / 50mg
 INFORMACIÓN PARA PRESCRIBIR AMPLIA Bonadoxina Meclozina/Piridoxina Tableta 25mg / 50mg 1. DENOMINACIÓN DISTINTIVA BONADOXINA 2. DENOMINACIÓN GENÉRICA Meclozina/Piridoxina 3. FORMA FARMACÉUTICA Y FORMULACIÓN
INFORMACIÓN PARA PRESCRIBIR AMPLIA Bonadoxina Meclozina/Piridoxina Tableta 25mg / 50mg 1. DENOMINACIÓN DISTINTIVA BONADOXINA 2. DENOMINACIÓN GENÉRICA Meclozina/Piridoxina 3. FORMA FARMACÉUTICA Y FORMULACIÓN
2. Centro Nacional de Biopreparados (BioCen), Bejucal, Cuba Planta Productos Parenterales 2 (PPP2) Formulación y llenado Planta de Envase Envase
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre: Hebervital. (Factor Estimulador de Colonias de Granulocitos, GCSF) Forma farmacéutica: Inyección SC e infusión IV. Fortaleza: 0,30 mg/1ml 0,48 mg/1,6
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre: Hebervital. (Factor Estimulador de Colonias de Granulocitos, GCSF) Forma farmacéutica: Inyección SC e infusión IV. Fortaleza: 0,30 mg/1ml 0,48 mg/1,6
INFORMACION PARA PRESCRIBIR AMPLIA
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: TEALEP 2. Nombre Genérico: FINASTERIDA 3. Forma Farmacéutica y Formulación: Comprimidos. Cada comprimido contiene: Finasterida... 5 mg Excipiente
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: TEALEP 2. Nombre Genérico: FINASTERIDA 3. Forma Farmacéutica y Formulación: Comprimidos. Cada comprimido contiene: Finasterida... 5 mg Excipiente
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. VP-gen 100 mg. Etopósido. 100 mg/5ml
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: VP-gen 100 mg (Etopósido) Solución concentrada para infusión IV 100 mg/5ml Estuche por una
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: VP-gen 100 mg (Etopósido) Solución concentrada para infusión IV 100 mg/5ml Estuche por una
INFORMACION PARA PRESCRIBIR AMPLIA
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: ASODOC 2. Nombre Genérico: DOCETAXEL 3. Forma Farmacéutica y Formulación: Solución Inyectable. Cada frasco ámpula contiene: Docetaxel Vehiculo c.b.p.
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: ASODOC 2. Nombre Genérico: DOCETAXEL 3. Forma Farmacéutica y Formulación: Solución Inyectable. Cada frasco ámpula contiene: Docetaxel Vehiculo c.b.p.
FICHA TÉCNICA. La duración estimada del tratamiento será de dos semanas.
 FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD UVALETTE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por comprimido recubierto: - 120,00 mg de extracto seco etanólico al 30%, de planta entera de Taraxacum
FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD UVALETTE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por comprimido recubierto: - 120,00 mg de extracto seco etanólico al 30%, de planta entera de Taraxacum
INFORMACION PARA PRESCRIBIR AMPLIA
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: TAVOR CR 2. Nombre Genérico: OXIBUTININA 3. Forma Farmacéutica y Formulación: Tabletas. Cada tableta contiene: Clorhidrato de Oxibutinina... 5 mg
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: TAVOR CR 2. Nombre Genérico: OXIBUTININA 3. Forma Farmacéutica y Formulación: Tabletas. Cada tableta contiene: Clorhidrato de Oxibutinina... 5 mg
ANEXO I RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Topotecán Hospira 4mg/4 ml concentrado para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de concentrado
ANEXO I RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Topotecán Hospira 4mg/4 ml concentrado para solución para perfusión EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de concentrado
PROYECTO DE MARBETE PARA CAJA VENTA PÚBLICO. ZODOX Doxorrubicina Solución 10 mg/ 5 ml Inyectable
 PROYECTO DE MARBETE PARA CAJA VENTA PÚBLICO Caja con 1 frasco ámpula con 5 ml 10 mg/ 5 ml Fórmula:...10 mg Excipiente c.b.p..5 ml DOSIS: La que el médico señale. VÍA DE ADMINISTRACIÓN: Infusión intravenosa.
PROYECTO DE MARBETE PARA CAJA VENTA PÚBLICO Caja con 1 frasco ámpula con 5 ml 10 mg/ 5 ml Fórmula:...10 mg Excipiente c.b.p..5 ml DOSIS: La que el médico señale. VÍA DE ADMINISTRACIÓN: Infusión intravenosa.
ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO
 Toxicología alimentaria Diplomatura de Nutrición humana y dietética Curso 2010-2011 ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO Dr. Jesús Miguel Hernández-Guijo Dpto. Farmacología
Toxicología alimentaria Diplomatura de Nutrición humana y dietética Curso 2010-2011 ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO Dr. Jesús Miguel Hernández-Guijo Dpto. Farmacología
Información para prescribir amplia CLOPIXOL DEPOT Zuclopentixol Solución inyectable
 Información para prescribir amplia CLOPIXOL DEPOT Zuclopentixol Solución inyectable 1. DENOMINACIÓN DISTINTIVA: Clopixol Depot 2. DENOMINACIÓN GENÉRICA: Zuclopentixol 3. FORMA FARMACÉUTICA Y FORMULACIÓN:
Información para prescribir amplia CLOPIXOL DEPOT Zuclopentixol Solución inyectable 1. DENOMINACIÓN DISTINTIVA: Clopixol Depot 2. DENOMINACIÓN GENÉRICA: Zuclopentixol 3. FORMA FARMACÉUTICA Y FORMULACIÓN:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO: CLARITYNE FLAS 10 mg Liofilizado Oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada liofilizado oral de CLARYTINE FLAS contiene:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO: CLARITYNE FLAS 10 mg Liofilizado Oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada liofilizado oral de CLARYTINE FLAS contiene:
FICHA TÉCNICA. ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
N H S-CCDS-MK4117-MTL
 DESALEX 5 mg Tabletas Recubiertas DESALEX 5 mg Tabletas Orodispersables DESALEX 0,5 mg/ml Jarabe DESALEX 0,25 mg/ 0,5 ml Solución Gotas 1 DESCRIPCIÓN DEL PRODUCTO Desalex 5 mg tabletas recubiertas, Desalex
DESALEX 5 mg Tabletas Recubiertas DESALEX 5 mg Tabletas Orodispersables DESALEX 0,5 mg/ml Jarabe DESALEX 0,25 mg/ 0,5 ml Solución Gotas 1 DESCRIPCIÓN DEL PRODUCTO Desalex 5 mg tabletas recubiertas, Desalex
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Lacovin 20 mg/ml solución cutánea. Lacovin 50 mg/ml solución cutánea.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lacovin 20 mg/ml solución cutánea. Lacovin 50 mg/ml solución cutánea. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de Lacovin 20 mg/ml solución cutánea contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lacovin 20 mg/ml solución cutánea. Lacovin 50 mg/ml solución cutánea. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de Lacovin 20 mg/ml solución cutánea contiene
INFORMACIÓN PARA PRESCRIBIR AMPLIA YUREDOL* Ciclobenzaprina y Clonixinato de Lisina Cápsulas Relajante muscular y Analgésico
 Confidencial Página 1/5 19/01/2011 INFORMACIÓN PARA PRESCRIBIR AMPLIA YUREDOL* Ciclobenzaprina y Clonixinato de Lisina Cápsulas Relajante muscular y Analgésico FORMA FARMACÉUTICA Y FORMULACIÓN: Cada cápsula
Confidencial Página 1/5 19/01/2011 INFORMACIÓN PARA PRESCRIBIR AMPLIA YUREDOL* Ciclobenzaprina y Clonixinato de Lisina Cápsulas Relajante muscular y Analgésico FORMA FARMACÉUTICA Y FORMULACIÓN: Cada cápsula
1. Qué es Actithiol Mucolítico adultos y para qué se utiliza
 Introducción PROSPECTO: INFORMACIÓN PARA EL USUARIO Actithiol Mucolítico adultos 50 mg/ml solución oral Carbocisteína Lea todo el prospecto detenidamente porque contiene información importante para usted.
Introducción PROSPECTO: INFORMACIÓN PARA EL USUARIO Actithiol Mucolítico adultos 50 mg/ml solución oral Carbocisteína Lea todo el prospecto detenidamente porque contiene información importante para usted.
