Ofatumumab en el tratamiento de Leucemia Linfocítica Crónica (LLC) no tratada Eficacia y Seguridad
|
|
|
- Trinidad Roldán Rodríguez
- hace 5 años
- Vistas:
Transcripción
1 Julio 2015 Ofatumumab en el tratamiento de Leucemia Linfocítica Crónica (LLC) no tratada Eficacia y Seguridad
2 Índice 1. Medicamento/ Descripción/ Indicación autorizada Descripción de la enfermedad Tratamiento de referencia de la patología Evaluación de la eficacia y seguridad Puntos clave Referencias Anexos Los informes síntesis de evidencia: medicamentos proporcionan una revisión rápida de la evidencia sobre determinados fármacos que han recibido recientemente la autorización de comercialización en nuestro país. También, sobre fármacos comercializados con anterioridad para los que se aprueban nuevas indicaciones de uso. Se enfocan principalmente a medicamentos de ámbito hospitalario y tienen como objetivo, servir como herramienta de ayuda a profesionales y grupos implicados en la evaluación y posicionamiento terapéuticos de estos fármacos 2
3 1. Medicamento/ Descripción/ Indicación autorizada En enero de 2010, ofatumumab (Arzerra ) recibió la opinión positiva de la EMA para el tratamiento de pacientes con Leucemia Linfocítica Crónica (LLC) refractarios al tratamiento con alemtuzumab y fludarabina. En mayo de 2014 la EMA amplió la indicación del fármaco a pacientes con LLC que no han recibido tratamiento previo y que no son candidatos a un tratamiento basado en fludarabina 1. Tabla 1. Características del medicamento evaluado. Nombre genérico. Nombre comercial. Código ATC Mecanismo de acción Indicación aprobada (Nombre de la agencia reguladora, fecha autorización) Posología recomendada Vía de administración Presentación Titular de la autorización de comercialización Ofatumumab. Arzerra. L01XC10 Anticuerpo monoclonal humano (IgG1k), tipo I, que se une específicamente a la molécula CD20 de las células B. La unión induce la muerte celular, principalmente por citotoxicidad dependiente del complemento y de anticuerpos. Esto resulta en depleción de células B malignas que expresan el epítopo CD20 2. Tratamiento de la LLC en pacientes refractarios a alemtuzumab y fludarabina. Tratamiento de la LLC no tratada previamente en combinación con clorambucil o bendamustina y que no son adecuados para un tratamiento basado en fludarabina 1. (European Medicine Agency (EMA), 22/05/14) Ciclos mensuales, 300 mg en el día 1 del ciclo, seguido de mg en el día 8 (ciclo 1), seguido de mg en el día 1 de los ciclos posteriores durante un mínimo de 3 ciclos hasta obtener la mejor respuesta o un máximo de 12 ciclos (cada 28 días) 2. Perfusión intravenosa. Viales de 100 mg y 1000 mg. Glaxo Group Ltd. 3
4 2. Descripción de la enfermedad La LLC es la forma más frecuente de leucemia en Occidente (25 % del total) con una incidencia a nivel europeo de 3/ pacientes/año. Suele presentar un curso crónico, por tanto si se diagnostica en fases tempranas de la enfermedad la supervivencia puede ser mayor a 10 años, aunque si se detecta en fases avanzadas ésta suele ser de entre 1-3 años. A los 5 años la tasa de supervivencia es del 44 % y el 52 % para hombres y mujeres, respectivamente. La edad media de presentación es de 72 años, aunque un 11 % de los casos ocurre en pacientes menores de 55 años. Más del 90 % de los casos son de linfocitos B 3,4. La heterogeneidad de la enfermedad y la edad avanzada de un buen número de pacientes hacen que existan varias alternativas para el manejo de estos pacientes. Los factores que más influyen en la elección de un tratamiento son la capacidad para tolerar quimioterapia y/o inmunoterapia, mutación del gen TP53, citopenias previas o concomitantes y transformación linfomatosa. No existe una escala estandarizada para valorar el estado de salud en la LLC, aunque la Cumulative Illness Rating Scale (CIRS) puede ser de ayuda. Generalmente son tenidos en cuenta la edad del paciente, Performance Status, presencia de comorbilidades, función renal y susceptibilidad a las infecciones 4. 4
5 3. Tratamiento de referencia de la patología Clorambucil en monoterapia ha sido durante un tiempo la primera opción de tratamiento para los pacientes con LLC previamente no tratados incapaces de tolerar regímenes de quimioterapia basados en fludarabina. De hecho en la guía de la European Society of Medical Oncology de 2011 es el estándar de tratamiento para estos pacientes 5. Sin embargo en los últimos años se han realizado estudios comparativos con clorambucil en los que alternativas como bendamustina en monoterapia 4,6 o combinada con rituximab 6, rituximab combinado con clorambucil 4,6,7 y más recientemente, obinutuzumab combinado con clorambucil 6,8, que está autorizado por la EMA pero aún no ha sido comercializado en España, han mostrado resultados superiores a clorambucil en monoterapia. Se realizó una búsqueda (19 de noviembre de 2014) de guías de práctica clínica (GPCs) de los últimos cinco años en las siguientes bases de datos: National Guideline Clearinghouse Guidelines International Network (GIN), y en las páginas webs de las sociedades científicas correspondientes (sociedades científicas americana, británica y española). Se utilizaron términos libres. A continuación se detalla el tratamiento sistémico de elección para la LLC en los pacientes previamente no tratados no candidatos a recibir un ciclo régimen quimioterápico basado en fludarabina en cada una de las guías localizadas: Guidelines on the diagnosis, investigation and management of chronic lymphocytic leukaemia. British Committee for Standards in Haematology. (2012) 4 : Las opciones de tratamiento propuestas en la guía Británica son clorambucil o bendamustina en monoterapia (Calidad de la evidencia moderada, recomendación fuerte) y la entrada en ensayos clínicos en los que los pacientes sean tratados con clorambucil o bendamustina combinados con un fármaco anti CD20 (Calidad de la evidencia moderada, recomendación fuerte). Chronic lymphocytic leukemia: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. (2011) 5 : La terapia estándar en los pacientes que no pueden recibir regímenes basados en fludarabina es clorambucil (Nivel de evidencia 2, grado de recomendación B), como terapias alternativas se mencionan bendamustina (Nivel de evidencia 2, grado de recomendación B) o regímenes basados en análogos de las purinas a dosis bajas (Nivel de evidencia 3, grado de recomendación B), aunque esta última alternativa no sería adecuada para el tipo de pacientes objeto de este informe. NCCN v.4 (2014) 6 : Las opciones para los pacientes que no pueden recibir fludarabina son clorambucil en monoterapia o combinado con rituximab u obinutuzumab, rituximab en monoterapia, corticoides a altas dosis y bendamustina en monoterapia o combinada con rituximab (Nivel de evidencia 2, grado de consenso A). Alberta Provincial Hematology Tumour Team. Chronic lymphocytic leukemia. (2013) 7 : Clorambucil aparece como la primera opción de tratamiento en pacientes frágiles con comorbilidades. 5
6 4. Evaluación de la eficacia y seguridad Metodología Para identificar la evidencia disponible sobre eficacia y seguridad, se realizó una búsqueda bibliográfica en las siguientes bases de datos para los documentos publicados en los últimos tres años: The Cochrane Library, las bases de datos del Centre for Reviews and Dissemination (CRD) y MEDLINE (a través de Pubmed). Se utilizaron términos libres. Además, se realizó una búsqueda manual en agencias reguladoras como la EMA (para localización del EPAR) en el caso de que ya estuviera publicado y FDA (en su defecto) y de agencias de evaluación de tecnologías sanitarias (ETS) como el National Institute for Health and Care Excellence (NICE), Canadian Agency for Drugs and Technologies in Health (CADTH), y National Horizon Scanning Centre (NHSC). De forma general, los diseños de los estudios a seleccionar fueron los que se indican, en este orden: informes de evaluación de tecnologías sanitarias, metanálisis, revisiones sistemáticas y ensayos clínicos pivotales. Un único evaluador realizó la selección de los artículos, lectura crítica y extracción de datos. Dos evaluadores realizaron el análisis de los resultados. Para evaluar la calidad metodológica de los ECA seleccionados se utilizó la herramienta propuesta por la Colaboración Cochrane 9. En la siguiente tabla se especifican la población, el medicamento a evaluar, el comparador/es óptimos, las variables de resultados y los diseños a considerar. Tabla 2. Pregunta de investigación mediante la utilización del modelo PICO (D) (Population, Intervention, Comparator, Outcomes, Study Design). Población Intervención Comparador (es) más apropiado (s) Resultados de eficacia Resultados de seguridad Pacientes adultos con LLC previamente no tratados y que no son candidatos a un régimen quimioterápico basado en fludarabina. Ofatumumab combinado con clorambucil. Ofatumumab combinado con bendamustina. Clorambucil combinado con rituximab u obinutuzumab. Bendamustina en monoterapia o combinada con rituximab. Supervivencia global Supervivencia libre de progresión Tasa de respuesta global y completa Respuesta tumoral y molecular Duración de la respuesta Tiempo hasta la progresión Tiempo hasta el siguiente tratamiento Supervivencia libre de eventos Calidad de vida. Eventos adversos asociados al tratamiento. Interrupción del tratamiento debido a los eventos adversos. 6
7 Diseño Informes de evaluación de tecnologías sanitarias, metanálisis, revisiones sistemáticas y ensayos clínicos pivotales. Comentarios: Comparadores: Clorambucil combinado con rituximab parece el comparador más adecuado en pacientes que no toleran regímenes quimioterápicos basados en fludarabina. La combinación clorambucil + obinutuzumab ha sido ensayada con buenos resultados aunque la experiencia de uso y el número de pacientes tratados no es excesivamente grande debido a su reciente autorización en Europa. Rituximab en cambio es un fármaco con el que se tiene una amplia experiencia de uso en la práctica clínica habitual. Bendamustina en monoterapia ha mostrado ser superior a clorambucil en monoterapia en pacientes con LLC y es recomendada por varias de las GPCs más actualizadas como una alternativa válida en pacientes frágiles. En cuanto a la combinación bendamustina + rituximab aún no hay resultados en pacientes no candidatos a regímenes de quimioterapia basados en fludarabina, sin embargo actualmente hay en marcha varios ensayos clínicos con esta combinación, como el estudio MaBle (NCT ) en el que se ensaya la combinación en pacientes frágiles. Además guías como por ejemplo la de la ESMO recomiendan la entrada de estos pacientes en ensayos clínicos de bendamustina + un fármaco anti CD20. Por todo esto y porque la combinación ha tenido buenos resultados en pacientes con LLC, bendamustina combinada con rituximab también representa una alternativa válida. Resultados de eficacia y seguridad: Se localizaron (fecha de la búsqueda: 18 de noviembre de 2014) un total de 131 artículos (1 en The Cochrane Library, 0 en CRD y 130 en MEDLINE). Además se localizó un informe de evaluación elaborado por el NICE Ofatumumab for treating previously untreated chronic lymphocytic leukaemia 10 pero no se localizaron, revisiones sistemáticas o metaanálisis que evalúen ofatumumab en la indicación señalada anteriormente. Para el análisis de la eficacia y seguridad se exponen a continuación los datos del ECA pivotal extraídos del informe EPAR 10, ya que aún no han sido publicado. Por otra parte se incluye información del estudio de apoyo OMB también extraída del informe EPAR. Informe del NICE: Ofatumumab for treating previously untreated chronic lymphocytic leukaemia 11 : NICE ha emitido una serie de recomendaciones iniciales sobre el uso de ofatumumab en LLC y un primer borrador de informe de evaluación del fármaco, que se prevé será publicado en abril de 2015, en base a la revisión de la evidencia presentada por el laboratorio fabricante y a la opinión de expertos en la materia. Las recomendaciones preliminares del Comité de Evaluación son: Ofatumumab en combinación con clorambucil es recomendado como una opción costoefectiva en pacientes con LLC previamente no tratada solo si: o o o El paciente no es candidato a un régimen basado en fludarabina y no es capaz de tolerar bendamustina y el fabricante provee el medicamento mediante un esquema de pago basado en resultados. 7
8 Los pacientes que ya estén siendo tratados con el fármaco deben continuar el tratamiento aunque no cumplan los requisitos citados. No es posible realizar una recomendación de la combinación ofatumumab + bendamustina debido a la escasa evidencia disponible y a la falta de datos de eficiencia. Respecto a la evidencia disponible sobre ofatumumab en pacientes con LLC previamente no tratados, NICE destaca los siguientes aspectos: Ofatumumab combinado con clorambucil fue superior a clorambucil en monoterapia en SLP y RG pero no consiguió demostrar superioridad en la SG. Se asume que no existen diferencias en cuanto a SLP, tasa de RG y SG entre ofatumumab + clorambucil y rituximab + clorambucil en base a la comparación indirecta realizada. No es posible la realización de una comparación indirecta entre ofatumumab y bendamustina debido a la diferencia en el estado de salud de los pacientes participantes en los estudios disponibles. A falta de más datos diferencia dos tipos de pacientes, aquellos capaces de tolerar un régimen con bendamustina (en monoterapia o combinada con rituximab) y aquellos que no son capaces. En el primer grupo los comparadores válidos serían clorambucil en monoterapia o combinado con rituximab y en el segundo, además de estos dos regímenes bendamustina en monoterapia o combinada con rituximab. ECA pivotal: OMB Tabla 3. Características del ECA pivotal. Estudio OMB Ofatumumab + clorambucil vs. clorambucil en monoterapia en pacientes previamente no tratados no candidatos a un régimen quimioterápico basado en fludarabina. (COMPLEMENT 1) Diseño Fase III, abierto, multicéntrico, aleatorizado, controlado frente a tratamiento activo. Se estratificó a los pacientes según edad, estadío de Binet y ECOG. Duración Reclutamiento de pacientes: Diciembre marzo Mediana de seguimiento: 30 meses. Hipótesis Superioridad. Los pacientes tratados con ofatumumab + clorambucil obtendrán un aumento del 50 % en la supervivencia libre de progresión con respecto los tratados con clorambucil en monoterapia (27 meses en el grupo de tratamiento vs. 18 meses en el grupo control). Grupo tratamiento (N= 217) Grupo control (N= 227) Variables evaluadas Ciclo 1: Ofatumumab 300 y 1000 mg días 1 y 8 respectivamente + clorambucil 10 mg/m 2 días 1-7. Ciclos posteriores: Ofatumumab 1000 mg día 1 + clorambucil días 1-7 cada 28 días. Clorambucil 10 mg/m 2 días 1-7 cada 28 días. Supervivencia libre de progresión (SLP) (variable principal). Supervivencia Global (SG) Tasa de respuesta global (RG)* Duración de la respuesta Tiempo hasta respuesta Tiempo hasta progresión 8
9 Descripción del análisis Criterios de Inclusión Criterios de Exclusión Características basales (grupo tratamiento vs. grupo control) Tratamiento Tiempo hasta siguiente tratamiento. Supervivencia Libre de eventos (SLE). Respuesta tumoral. Un mínimo de 259 eventos era necesario para, con una potencia del 90 % y un error alfa de 0,05, detectar un aumento en la SLP del 50 % en el grupo de tratamiento con respecto al grupo control. La SLP fue calculada con el método de Kaplan-meier y se compararon los datos usando el test de log-rank estratificado. Análisis según ITT. 18 años, diagnóstico de LLC previamente no tratada, candidato a tratamiento quimioterápico pero no a un régimen basado en fludarabina. Infección crónica o actual que requiera tratamiento sistémico o serología positiva para VHB o VIH, patología cardiaca o cerebrovascular, función renal o hepática deteriorada, toma de corticoides > 100 mg de hidrocortisona o equivalente en los 7 días previos, procesos que puedan influir en la variable principal del estudio, uso de altas dosis de corticoides de forma crónica. Edad (mediana) (años): 69 vs. 70. Sexo (masculino) (%): 64 vs. 62. ECOG PS (%): 0-1: 92 vs. 91 2: 8 vs. 8 Nº comorbilidades (mediana): 3 vs. 3 Puntuación CIRS (mediana): 9 vs. 8 Estadío de Binet (%): A: 35 vs. 31 B: 33 vs. 38 C: 32 vs. 31 Estadío de Rai (%): Riesgo bajo (0): 7 vs. 9 Riesgo intermedio (I, II): 51 vs. 51 Riesgo alto (III, IV): 42 vs pacientes fueron tratados de los cuales 217 recibieron ofatumumab + clorambucil y 227 recibieron clorambucil en monoterapia. La mayoría de los pacientes había suspendido la medicación tras 6 ciclos de tratamiento, el 82 % en el grupo de ofatumumab + clorambucil y el 70 % en el grupo de clorambucil solo. La principal causa de discontinuación fueron los eventos adversos (13,8 % del total de pacientes en el grupo de tratamiento y el 15,8 % en el grupo control) seguida de progresión de la enfermedad (1,8 % en el grupo de tratamiento vs. 8,4 % en el grupo control) *Tasa de respuesta global: Respuesta completa + respuesta parcial. Tabla 4. Resultados de eficacia del ECA pivotal. Variable Ofatumumab + clorambucil (N = 217) Clorambucil (N = 227) RR, OR o HR (IC95 %; p) SLP mediana (meses) 22,4 (19-25,2) 13,1 (10,6-13,8) HR: 0,57 (0,45-0,72; p < 0,001) Tasa de RG (%) 82 (76,7-87,1) 69 (62,1-74,6) OR: 2,16 (1,36-3,42; p = 0,001) SG mediana (meses) NA (46,6 - NA) NA HR: 0,91 (0,57-1,43; p = 0,666) SG a los 2 y 3 años (%) 88 y y 78 ND Tiempo hasta respuesta (meses) 1,9 (1,2-1,9) 2,8 (1,9-3,1) HR: 1,13 (0,91-1,4; p = 0,204) 9
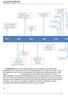
10 Duración de la respuesta (meses) 22,1 (19,1-24,6) 13,2 (10,8-16,4) HR: 0,56 (0,43-0,74; p < 0,001) Tiempo hasta próxima 39,8 (34,7-48,8) 24,7 (22,6-29,1) HR: 0,49 (0,36 - terapia (meses) 0,67; p < 0,001) SLE (meses) 21,9 (17,1-23,8) 10,7 (8,9-12,8) HR: 0,52 (0,42-0,65; p < 0,001) SLP: Supervivencia libre de progresión, RC: Respuesta completa, SG: Supervivencia global, SLE: Supervivencia libre de eventos, RR: riesgo relativo, OR: odds ratio, HR: hazard ratio. IC: intervalo de confianza. NA: No alcanzado. ND: No disponible La superioridad de ofatumumab + clorambucil en la SLP se mantuvo en los distintos subgrupos preespecificados (Figuras 1 y 2) excepto en los pacientes con ECOG 2 probablemente debido al bajo número de participantes y en los pacientes con estadío de Binet B y C, en los que aunque existe una tendencia favorable al grupo de tratamiento, no se alcanzó la significación estadística. Figura 1. SLP según características demográficas y basales. 10
11 Figura 2. SLP según estado de salud y comorbilidades. Fuente: European Medicine Agency (EMA). Scientific discussion. Arzerra (ofatumumab) [Internet]. Londres: EMA; 29 may 2014 [citado 20 Nov 2014]. Procedure number: EMEA/H/C/001131/II/0023. Tabla 5. Resultados de seguridad del ECA pivotal. Parámetro Evento adverso (EA) Evento adverso grado 3 Ofatumumab+ clorambucil (N = 217) Clorambucil (N = 227) Ofatumumab+ clorambucil (N = 217) Clorambucil (N = 227) n % n % n % n % Cualquier evento adverso Neutropenia Nauseas ND ND ND ND Rash <1 Pirexia Trombocitopenia Diarrea ND ND ND ND Astenia Tos ND ND ND ND Vómitos ND ND ND ND Prurito ND ND ND ND Disnea <1 Anemia Urticaria < <1 Leucopenia <1 Neumonía Se incluyen los EA que se han dado en 10 % de los pacientes en alguno de los dos grupos y los EA grado 3 que se han dado en 5 %. ND: No disponible. El 39 % de los pacientes sufrió un EA grave en el grupo de clorambucil + ofatumumab frente al 31 % en el grupo de clorambucil, de ellos fueron fatales en el 6 % de los pacientes en el grupo 11
12 de clorambucil + ofatumumab frente al 11 % en el grupo de clorambucil, sin embargo estos EA fatales solo se relacionaron con la medicación de estudio en el 1 % de los pacientes en el grupo de clorambucil + ofatumumab (3 casos) y en < 1 % en el grupo de clorambucil (1 caso), las causas de los fallecimientos no están disponibles. El 84 % de los pacientes asignados al grupo de clorambucil + ofatumumab sufrieron EA relacionados con la medicación de estudio (15 % EA graves) frente al 65 % (13 % EA graves) de los pacientes tratados con clorambucil. El 13 % de los pacientes tuvieron que suspender la administración del fármaco en el grupo de ofatumumab + clorambucil debido a los EA frente al 14 % de los pacientes tratados con clorambucil en monoterapia. Calidad del ensayo: En base a la herramienta propuesta por la Colaboración Cochrane 10, el ECA pivotal presenta una calidad elevada. Ver Anexo I. EPAR 10 El informe EPAR incluye además los datos del estudio OMB que era un ensayo clínico fase II en el que se incluyó a pacientes con LLC tanto previamente no tratados como en recaída no candidatos a recibir quimioterapia basada en fludarabina. Los pacientes recibieron 6 ciclos de ofatumumab a las mismas dosis del estudio COMPLEMENT 1 más bendamustina 90 mg/m 2 días 1 y 2 en ciclos de 28 días. La variable principal de eficacia fue la tasa de RG, y como variables secundarias se midió la SLP, la SG, el tiempo hasta respuesta, la duración de la respuesta y el tiempo hasta el siguiente tratamiento. Se incluyeron en el estudio 44 pacientes con una mediana de edad de 62,5 años, más jóvenes que en el COMPLEMENT 1, aunque se reclutó a más pacientes con más de 2 comorbilidades. La RG fue alcanzada por el 95 % (IC95 %: 84-99) de los pacientes tras la última dosis de ofatumumab asociado a bendamustina, con un 43 % de respuestas completas. El resto de variables secundarias aún no eran valorables en el momento del análisis. En cuanto a la seguridad, el 98 % de los pacientes sufrió al menos un EA y el 95 % sufrió al menos un EA relacionado con la medicación. Se produjeron EA grado 3 en el 57 % de la población y EA graves en el 34 %, siendo prácticamente todos relacionados con el tratamiento (14 de los 15 EA graves acontecidos). Fortalezas y limitaciones de la evidencia La calidad del estudio COMPLEMENT 1 es elevada, una de las limitaciones que podría tener es que se trataron pacientes que sí eran candidatos a recibir un régimen quimioterápico basado en fludarabina, con lo que se podría haber sobreestimado el efecto del tratamiento, sin embargo estos pacientes se distribuyeron de forma equilibrada entre ambos grupos y su exclusión del análisis principal no produjo cambios significativos en los resultados. Otra limitación que a priori podría restar calidad al estudio, es el carácter abierto del mismo, sin embargo la variable principal de eficacia fue valorada por un comité revisor independiente. En el estudio COMPLEMENT 1 se elige clorambucil como comparador en base a que, al inicio del estudio, año 2008, éste era el estándar de tratamiento para pacientes ancianos con comorbilidades. Sin embargo actualmente existen alternativas, como añadir rituximab a clorambucil o bendamustina en monoterapia o combinada con rituximab, que se han mostrado superiores a clorambucil en monoterapia en este tipo de pacientes, por tanto el comparador podría haber quedado obsoleto y no ser el más adecuado a día de hoy. 12
13 La variable principal de eficacia en el estudio COMPLEMENT 1 fue la SLP en vez de la SG que hubiese sido la variable ideal porque es la que aporta la información más valiosa y con menor probabilidad de sesgos. Sin embargo la LLC es una patología de curso crónico con una supervivencia a largo plazo mayor que otras enfermedades hematológicas, por esto la SLP puede resultar válida como variable principal de eficacia. El análisis de los subgrupos preespecificados en el estudio COMPLEMENT 1 mostró concordancia con el análisis de la población global y no se dieron resultados de subgrupos no preespecificados en el protocolo del estudio. El estudio OMB115911, que sirvió para la autorización de la combinación ofatumumab asociado a bendamustina, es un estudio no comparativo con un bajo número de pacientes, además la variable principal del estudio no es una variable dura y las variables secundarias duras como SG aún no eran valorables. Por todo esto, y aunque los resultados de RG son prometedores, la evidencia que apoya el uso de esta combinación es débil y debería valorarse con cautela. 13
14 5. Puntos clave Ofatumumab combinado con clorambucil es superior a clorambucil en monoterapia en pacientes con leucemia linfocítica crónica previamente no tratados, no candidatos a recibir fludarabina, en supervivencia libre de progresión y en otras variables secundarias relevantes como respuesta global, sin embargo no ha conseguido demostrar superioridad en supervivencia global aunque se aprecia cierta tendencia a favor de la combinación. (Nivel de evidencia 1++) Ofatumumab combinado con bendamustina presenta buenas tasas de RG en pacientes con LLC previamente tratados y no tratados no candidatos a recibir fludarabina, sin la relevancia de los resultados es relativa debido a que no se compara con un grupo control, al bajo número de pacientes tratados y a que los datos de eficacia no están lo suficientemente maduros. (Nivel de evidencia 1-) Ofatumumab combinado con clorambucil produce más eventos adversos que clorambucil en monoterapia, sin embargo el perfil de toxicidad mostrado es aceptable teniendo en cuenta la fragilidad de los pacientes tratados. Los eventos adversos observados son los habituales para un régimen quimioterápico con un agente alquilante y un anti CD20 y no se han detectado eventos adversos graves no esperables (Nivel de evidencia 1++). En cuanto a la combinación ofatumumab asociado a bendamustina parece algo más tóxica que la combinación con clorambucil. A pesar de esto parece tener un perfil de toxicidad aceptable aunque el número de pacientes tratados es bastante escaso y sería recomendable mayor experiencia de uso. (Nivel de evidencia 1-). Se indica tras cada afirmación el nivel de evidencia según la clasificación propuesta por la Scottish Intercollegiate Guidelines Network (SIGN) 12 (Anexo II). 14
15 6. Referencias 1. European Medicine Agency (EMA). Summary of opinion. Arzerra (ofatumumab) [Internet]. Londres: EMA; may 2014 [citado ]. EMA/CHMP/312178/2014. URL: /WC pdf 2. European Medicine Agency (EMA). Ficha técnica de Arzerra (ofatumumab) [Internet]. Londres: EMA; may 2014 [citado ]. URL: _Product_Information/human/001131/WC pdf 3. Asociación española contra el cáncer (AECC). Qué es la leucemia linfática crónica? [Internet]. Madrid: AECC; 2014 [citado 20 oct 2014]. URL: inas/quees.aspx 4. Oscier D, Dearden C, Eren E, Fegan C, Follows G, Hillmen P, et al. Guidelines on the diagnosis, investigation and management of chronic lymphocytic leukaemia. Br J Haematol Dec;159: Eichhorst B, Dreyling M, Robak T, Montserrat E, Hallek M. Chronic lymphocytic leukemia: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol Sep;22 Suppl 6:vi NCCN Clinical Guidelines Practice in Oncology (NCCN Guidelines). Non-Hodgkin s Lymphomas Version [Internet]. Fort Washington: NCCN; 2014 [citado ]. URL: n.org/professionals/physician_gls/pdf/nhl.pdf 7. Alberta Provincial Hematology Tumour Team. Chronic lymphocytic leukemia [Internet]. Edmonton (Alberta): Alberta Health Services, Cancer Care; 2014 [citado 23 oct 2014].24 p. Clinical practice guideline; no. LYHE-007. URL: 8. Goede V, Fischer K, Busch R, Engelke A, Eichhorst B, Wendtner CM Obinutuzumab plus Chlorambucil in Patients with CLL and Coexisting Conditions. N Engl J Med. 2014;370: Higgins JPT, Green S (eds). Cochrane Handbook for Systematic Reviews of Interventions [Internet] Version [actualizado marzo 2011]. The Cochrane Collaboration, [consultado 20/01/2014]. URL: European Medicine Agency (EMA). Scientific discussion. Arzerra (ofatumumab) [Internet]. Londres: EMA; 29 may 2014 [citado 20 Nov 2014]. Procedure number: EMEA/H/C/001131/II/0023. URL: _Variation/human/001131/WC pdf 11. National Institute for Health and Care Excellence (NICE). Ofatumumab for treating 15
16 previously untreated chronic lymphocytic leukaemia [Internet]. Londres: NICE, 2013 [citado ]. NICE Technology appraisal. URL: Scottish Intercollegiate Guidelines Network (SIGN). SIGN 50: a guideline developer s handbook [Internet]. Edinburgh: Healthcare Improvement Scotland; c Section 7: Forming guideline recommendations [Internet] [citado 20 ene 2014]. [2 p.]. URL: 16
17 7. Anexos Anexo I. Evaluación de la calidad metodológica de los estudios. Evaluación del riesgo de sesgo de ensayos controlados aleatorizados, según la herramienta propuesta por la Colaboración Cochrane 9 Dominios Referencia: Estudio COMPLEMENT 1 Generación de la secuencia de aleatorización Riesgo de sesgo bajo Ocultamiento adecuado de la asignación Riesgo de sesgo bajo Cegamiento de los pacientes y del personal Cegamiento de los evaluadores del resultado Datos de resultado incompletos Notificación selectiva de los resultados Otras fuentes de sesgo Riesgo de sesgo bajo Riesgo de sesgo bajo Riesgo de sesgo bajo Riesgo de sesgo bajo Riesgo de sesgo bajo Para cada uno de los dominios evaluados el riesgo de sesgo puede clasificarse como bajo, alto o poco claro. Los criterios a considerar para la categorización del riesgo de sesgo en cada dominio se encuentran claramente descritos en el Manual Cochrane de revisiones sistemáticas de intervenciones 9. Anexo II. Niveles de evidencia científica del SIGN 12 Niveles de evidencia científica Metaanálisis de alta calidad, revisiones sistemáticas de ensayos clínicos o ensayos clínicos de alta calidad con muy poco riesgo de sesgo. Metaanálisis bien realizados, revisiones sistemáticas de ensayos clínicos o ensayos clínicos bien realizados con poco riesgo de sesgos. Metaanálisis, revisiones sistemáticas de ensayos clínicos o ensayos clínicos con alto riesgo de sesgos. Revisiones sistemáticas de alta calidad de estudios de cohortes o de casos y controles. Estudios de cohortes o de casos y controles con riesgo muy bajo de sesgo y con alta probabilidad de establecer una relación causal. Estudios de cohortes o de casos y controles bien realizados con bajo riesgo de sesgo y con una moderada probabilidad de establecer una relación causal. Estudios de cohortes o de casos y controles con alto riesgo de sesgo y riesgo significativo de que la relación no sea causal. 3 Estudios no analíticos, como informes de casos y series de casos. 4 Opinión de expertos. 17
Idelalisib en el tratamiento de Leucemia Linfocítica Crónica Eficacia y Seguridad
 Julio 2015 Idelalisib en el tratamiento de Leucemia Linfocítica Crónica Eficacia y Seguridad Índice 1. Medicamento/ Descripción/ Indicación autorizada... 2 2. Descripción de la enfermedad... 3 3. Tratamiento
Julio 2015 Idelalisib en el tratamiento de Leucemia Linfocítica Crónica Eficacia y Seguridad Índice 1. Medicamento/ Descripción/ Indicación autorizada... 2 2. Descripción de la enfermedad... 3 3. Tratamiento
Combinaciones Quimioterápicas en Leucemia Linfocítica Crónica
 Combinaciones Quimioterápicas en Leucemia Linfocítica Crónica Formación Contínua SEHH-FEHH, Madrid, Oct 2014 Javier Loscertales Pueyo Hospital Universitario La Princesa, Madrid QT en LLC Alquilantes: Clorambucil,
Combinaciones Quimioterápicas en Leucemia Linfocítica Crónica Formación Contínua SEHH-FEHH, Madrid, Oct 2014 Javier Loscertales Pueyo Hospital Universitario La Princesa, Madrid QT en LLC Alquilantes: Clorambucil,
Revista Cubana de Hematología, Inmunología y Hemoterapia. 2017; 36 (Suplemento).
 Seguridad clínica del anticuerpo monoclonal CIMABIOR en pacientes con linfoma no hodgkiniano: revisión integrada de datos 1 García-Vega Y 1, Hernández-Casaña P 1, Saumell-Nápoles Y 1, Fernández-Águila
Seguridad clínica del anticuerpo monoclonal CIMABIOR en pacientes con linfoma no hodgkiniano: revisión integrada de datos 1 García-Vega Y 1, Hernández-Casaña P 1, Saumell-Nápoles Y 1, Fernández-Águila
Tratamiento de rescate de la leucemia linfática crónica. Julio Delgado Hospital Clínic, Barcelona
 Tratamiento de rescate de la leucemia linfática crónica Julio Delgado Hospital Clínic, Barcelona El tratamiento de la LLC en el futuro BCR CD40 CD37 Tru-016 CXCR4 Célula tumoral (LLC) CD52 CD20 Alemtuzumab
Tratamiento de rescate de la leucemia linfática crónica Julio Delgado Hospital Clínic, Barcelona El tratamiento de la LLC en el futuro BCR CD40 CD37 Tru-016 CXCR4 Célula tumoral (LLC) CD52 CD20 Alemtuzumab
Idelalisib en el tratamiento de Linfoma Folicular Eficacia y Seguridad
 Julio 2015 Idelalisib en el tratamiento de Linfoma Folicular Eficacia y Seguridad Índice 1. Medicamento/ Descripción/ Indicación autorizada... 2 2. Descripción de la enfermedad... 3 3. Tratamiento de referencia
Julio 2015 Idelalisib en el tratamiento de Linfoma Folicular Eficacia y Seguridad Índice 1. Medicamento/ Descripción/ Indicación autorizada... 2 2. Descripción de la enfermedad... 3 3. Tratamiento de referencia
EVALUACIÓN DE RESULTADOS DE CRIZOTINIB EN CÁNCER DE PULMÓN NO MICROCÍTICO. Mª José Moreno Fernández
 EVALUACIÓN DE RESULTADOS DE CRIZOTINIB EN CÁNCER DE PULMÓN NO MICROCÍTICO Mª José Moreno Fernández Introducción. Situación actual de Crizotinib. Objetivos. Material y métodos. Resultados. Limitaciones
EVALUACIÓN DE RESULTADOS DE CRIZOTINIB EN CÁNCER DE PULMÓN NO MICROCÍTICO Mª José Moreno Fernández Introducción. Situación actual de Crizotinib. Objetivos. Material y métodos. Resultados. Limitaciones
DIRECCION DE ATENCIÓN Y EVALUACIÓN COMISIÓN DE EVALUACIÓN DE MEDICAMENTOS DE ALTO IMPACTO (CEMAI)
 Página 1 de 5 Introducción El mieloma múltiple (MM) es un tipo de cáncer que se produce por una degeneración maligna de las células plasmáticas, que se encuentran normalmente en la médula ósea. Representa
Página 1 de 5 Introducción El mieloma múltiple (MM) es un tipo de cáncer que se produce por una degeneración maligna de las células plasmáticas, que se encuentran normalmente en la médula ósea. Representa
Eficacia relativa de Palbociclib y Ribociclib en el tratamiento de cáncer de mama localmente avanzado o metastásico. Comparación Indirecta
 Abril 2018 Eficacia relativa de Palbociclib y Ribociclib en el tratamiento de cáncer de mama localmente avanzado o metastásico. Comparación Indirecta Eficacia relativa de Palbociclib y Ribociclib en el
Abril 2018 Eficacia relativa de Palbociclib y Ribociclib en el tratamiento de cáncer de mama localmente avanzado o metastásico. Comparación Indirecta Eficacia relativa de Palbociclib y Ribociclib en el
alotrasplante Quimioterapia de Reinducción en leucemia mieloide aguda recidivante
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
Comunicado de prensa. Basilea, 7 de noviembre de 2013
 Comunicado de prensa Basilea, de noviembre de 2013 Con Gazyva, de Roche, pacientes que padecían uno de los tipos de cáncer hemático más frecuentes vivieron significativamente más tiempo sin empeorar que
Comunicado de prensa Basilea, de noviembre de 2013 Con Gazyva, de Roche, pacientes que padecían uno de los tipos de cáncer hemático más frecuentes vivieron significativamente más tiempo sin empeorar que
LEUCEMIAS EN EL ANCIANO UN DILEMA POR RESOLVER
 LEUCEMIAS EN EL ANCIANO UN DILEMA POR RESOLVER CLASIFICACIÓN DE LAS LEUCEMIAS MIELOIDES LINFOIDES AGUDAS LEUCEMIA AGUDA MIELOBLÁSTICA LEUCEMIA AGUDA LINFOBLÁSTICA CRÓNICAS LEUCEMIA MIELOIDE CRÓNICA LEUCEMIA
LEUCEMIAS EN EL ANCIANO UN DILEMA POR RESOLVER CLASIFICACIÓN DE LAS LEUCEMIAS MIELOIDES LINFOIDES AGUDAS LEUCEMIA AGUDA MIELOBLÁSTICA LEUCEMIA AGUDA LINFOBLÁSTICA CRÓNICAS LEUCEMIA MIELOIDE CRÓNICA LEUCEMIA
Leucemia Linfática Crónica. Dardo Riveros Servicio de Hematología Departamento de Medicina Interna CEMIC
 Leucemia Linfática Crónica Dardo Riveros Servicio de Hematología Departamento de Medicina Interna CEMIC Estadificación de la LLC A Binet Descripción
Leucemia Linfática Crónica Dardo Riveros Servicio de Hematología Departamento de Medicina Interna CEMIC Estadificación de la LLC A Binet Descripción
IDELALISIB en Leucemia Linfocítica Crónica SUPLEMENTO AL INFORME GÉNESIS SEFH DEL 9/6/ /9/2016
 Página: 1 IDELALISIB en Leucemia Linfocítica Crónica SUPLEMENTO AL INFORME GÉNESIS SEFH DEL 9/6/2016 14/9/2016 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME... 1 2.- SOLICITUD Y DATOS DEL PROCESO
Página: 1 IDELALISIB en Leucemia Linfocítica Crónica SUPLEMENTO AL INFORME GÉNESIS SEFH DEL 9/6/2016 14/9/2016 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME... 1 2.- SOLICITUD Y DATOS DEL PROCESO
REUNION BIBLOGRAFICA M
 REUNION BIBLOGRAFICA Ma. Florencia Leguizamón INTRODUCCIÓN Los pacientes con cáncer de pulmón avanzado no células pequeñas con mutación del EGFR pueden experimentar una importante reducción del tumor
REUNION BIBLOGRAFICA Ma. Florencia Leguizamón INTRODUCCIÓN Los pacientes con cáncer de pulmón avanzado no células pequeñas con mutación del EGFR pueden experimentar una importante reducción del tumor
Obinutuzumab en Leucemia Linfática Crónica INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA
 Obinutuzumab en Leucemia Linfática Crónica INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Genérico: Obinutuzumab Nombre Comercial: Gazyvaro Presentaciones: Vial 1000mg/40ml
Obinutuzumab en Leucemia Linfática Crónica INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Genérico: Obinutuzumab Nombre Comercial: Gazyvaro Presentaciones: Vial 1000mg/40ml
BIBLIOGRAFICO ONCOLOGIA ESTUDIO: AVAPERL. Dra. Evelyn S Colombo
 BIBLIOGRAFICO ONCOLOGIA 03.09.13 ESTUDIO: AVAPERL Dra. Evelyn S Colombo Para los pacientes con NSCLC avanzado o metastásico, el pronóstico es pobre, y las tasas de supervivencia a 1 año es de 30 % a 40
BIBLIOGRAFICO ONCOLOGIA 03.09.13 ESTUDIO: AVAPERL Dra. Evelyn S Colombo Para los pacientes con NSCLC avanzado o metastásico, el pronóstico es pobre, y las tasas de supervivencia a 1 año es de 30 % a 40
NOMBRE DEL FÁRMACO e indicación clínica (Informe para la Comisión de Farmacia y Terapéutica del Hospital xxxxxxxxxx) Fecha xx/xx/xx
 NOMBRE DEL FÁRMACO e indicación clínica (Informe para la Comisión de Farmacia y Terapéutica del Hospital xxxxxxxxxx) Fecha xx/xx/xx 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Indicación
NOMBRE DEL FÁRMACO e indicación clínica (Informe para la Comisión de Farmacia y Terapéutica del Hospital xxxxxxxxxx) Fecha xx/xx/xx 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Indicación
Informe de Posicionamiento Terapéutico de Ofatumumab (Arzerra )
 INFORME DE POSICIONAMIENTO TERAPÉUTICO PT/V1/02042014.1 Informe de Posicionamiento Terapéutico de Ofatumumab (Arzerra ) Fecha de publicación: 3 de abril de 2014 La leucemia linfocítica crónica (LLC) es
INFORME DE POSICIONAMIENTO TERAPÉUTICO PT/V1/02042014.1 Informe de Posicionamiento Terapéutico de Ofatumumab (Arzerra ) Fecha de publicación: 3 de abril de 2014 La leucemia linfocítica crónica (LLC) es
Pacientes con cáncer de mama metastásico cuyos tumores sobreexpresen HER2
 1. DENOMINACIÓN DEL ESQUEMA: TRASTUZUMAB 2. INDICACIÓN Pacientes con cáncer de mama metastásico cuyos tumores sobreexpresen HER2 con 3 cruces (determinado por inmunohistoquímica) y que hayan recibido al
1. DENOMINACIÓN DEL ESQUEMA: TRASTUZUMAB 2. INDICACIÓN Pacientes con cáncer de mama metastásico cuyos tumores sobreexpresen HER2 con 3 cruces (determinado por inmunohistoquímica) y que hayan recibido al
Comunicación dirigida a profesionales sanitarios
 Comunicación dirigida a profesionales sanitarios Bendamustina (Levact, Bendamustina Accord, Bendamustina Dr. Reddys, Bendamustina Intas): aumento de la mortalidad observado en estudios clínicos recientes
Comunicación dirigida a profesionales sanitarios Bendamustina (Levact, Bendamustina Accord, Bendamustina Dr. Reddys, Bendamustina Intas): aumento de la mortalidad observado en estudios clínicos recientes
REUNION BIBLIOGRAFICA Martes 26 de Noviembre de 2013
 REUNION BIBLIOGRAFICA Martes 26 de Noviembre de 2013 CENTRO: HOSPITAL NACIONAL DE CLINICAS Mendez Norberto, Médico. PUNTOS CLAVE CANCER GASTRICO La incidencia de cáncer gástrico (CG)se correlaciona con
REUNION BIBLIOGRAFICA Martes 26 de Noviembre de 2013 CENTRO: HOSPITAL NACIONAL DE CLINICAS Mendez Norberto, Médico. PUNTOS CLAVE CANCER GASTRICO La incidencia de cáncer gástrico (CG)se correlaciona con
Fundamentos estadísticos del ensayo clínico, Interpretación de resultados. M José Escudero Barea. Gerente Dpto. Gestión de Datos y Estadística.
 Fundamentos estadísticos del ensayo clínico, Interpretación de resultados. M José Escudero Barea. Gerente Dpto. Gestión de Datos y Estadística. Grupo Español de Investigación en Cáncer de Mama (GEICAM).
Fundamentos estadísticos del ensayo clínico, Interpretación de resultados. M José Escudero Barea. Gerente Dpto. Gestión de Datos y Estadística. Grupo Español de Investigación en Cáncer de Mama (GEICAM).
Vitamina K para evitar la anticoagulación en recién nacidos
 Vitamina K para evitar la anticoagulación en recién nacidos PREGUNTA Es necesaria la administración de para evitar problemas de anticoagulación en recién nacidos? CONTEXTO Anticoagulación en recién nacidos
Vitamina K para evitar la anticoagulación en recién nacidos PREGUNTA Es necesaria la administración de para evitar problemas de anticoagulación en recién nacidos? CONTEXTO Anticoagulación en recién nacidos
Cáncer colorrectal. Actualización y tendencias futuras
 Cáncer. Actualización y tendencias futuras MODALIDAD 100% ONLINE ÁREA MEDICINA DURACIÓN 90 HORAS Programas de Formación y Especialización MEDICINA Y SALUD DESCRIPCIÓN El cáncer es unas de las primeras
Cáncer. Actualización y tendencias futuras MODALIDAD 100% ONLINE ÁREA MEDICINA DURACIÓN 90 HORAS Programas de Formación y Especialización MEDICINA Y SALUD DESCRIPCIÓN El cáncer es unas de las primeras
ESQUEMAS ALTERNATIVOS CON SUNITINIB: MÁS ALLÁ DEL MANEJO DE LOS EFECTOS ADVERSOS
 ESQUEMAS ALTERNATIVOS CON SUNITINIB: MÁS ALLÁ DEL MANEJO DE LOS EFECTOS ADVERSOS María Jose Lecumberri Biurrun CHN León, 20 de mayo de 2016 Estudio fase III de sunitinib vs interferón alfa en primera línea
ESQUEMAS ALTERNATIVOS CON SUNITINIB: MÁS ALLÁ DEL MANEJO DE LOS EFECTOS ADVERSOS María Jose Lecumberri Biurrun CHN León, 20 de mayo de 2016 Estudio fase III de sunitinib vs interferón alfa en primera línea
FACTORES PRONÓSTICOS Y PREDICTIVOS
 GROWING UP IN ONCOLOGY FACTORES PRONÓSTICOS Y PREDICTIVOS Criterios REMARK y niveles de evidencia 18 de Junio de 2013 Lide Larburu Gurrutxaga R4 Oncología Médica Onkologikoa, Donostia REMARK: Reporting
GROWING UP IN ONCOLOGY FACTORES PRONÓSTICOS Y PREDICTIVOS Criterios REMARK y niveles de evidencia 18 de Junio de 2013 Lide Larburu Gurrutxaga R4 Oncología Médica Onkologikoa, Donostia REMARK: Reporting
Revisiones sistemáticas, metaanalisis, MBE (medicina basada en la evidencia) Antonio Guerrero
 Revisiones sistemáticas, metaanalisis, MBE (medicina basada en la evidencia) Antonio Guerrero Revisión científica sanitaria Estudio basado: en la integración estructurada de la información obtenida en
Revisiones sistemáticas, metaanalisis, MBE (medicina basada en la evidencia) Antonio Guerrero Revisión científica sanitaria Estudio basado: en la integración estructurada de la información obtenida en
Obinutuzumab 1ª línea de Leucemia Linfática Crónica
 Informe Base Página: 1 Obinutuzumab 1ª línea de Leucemia Linfática Crónica (Informe para la CURMPS Asturias) Fecha 29/07/2016 ÍNDICE: 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME...2 2.- SOLICITUD
Informe Base Página: 1 Obinutuzumab 1ª línea de Leucemia Linfática Crónica (Informe para la CURMPS Asturias) Fecha 29/07/2016 ÍNDICE: 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME...2 2.- SOLICITUD
MIELOMA MÚLTIPLE: Bortezomib 1/6
 MIELOMA MÚLTIPLE: Bortezomib 1/6 1. DENOMINACIÓN DEL ESQUEMA: BORTEZOMIB 2. USO TERAPÉUTICO (1) : Tratamiento de pacientes con mieloma múltiple que han recibido al menos dos tratamientos previos y que
MIELOMA MÚLTIPLE: Bortezomib 1/6 1. DENOMINACIÓN DEL ESQUEMA: BORTEZOMIB 2. USO TERAPÉUTICO (1) : Tratamiento de pacientes con mieloma múltiple que han recibido al menos dos tratamientos previos y que
Lectura Crítica de Revisiones Sistemáticas. Carlos Canelo Aybar UNAGESP Instituto Nacional De Salud
 Lectura Crítica de Revisiones Sistemáticas Carlos Canelo Aybar UNAGESP Instituto Nacional De Salud Introducción Introducción y definiciones The Cochrane Collaboration, EvipNet, UNAGESP Elementos claves
Lectura Crítica de Revisiones Sistemáticas Carlos Canelo Aybar UNAGESP Instituto Nacional De Salud Introducción Introducción y definiciones The Cochrane Collaboration, EvipNet, UNAGESP Elementos claves
Informe de Posicionamiento Terapéutico de Ofatumumab (Arzerra )
 INFORME DE POSICIONAMIENTO TERAPÉUTICO PT/V1/02042014.1 Informe de Posicionamiento Terapéutico de Ofatumumab (Arzerra ) Fecha de publicación: 3 de abril de 2014 La leucemia linfocítica crónica (LLC) es
INFORME DE POSICIONAMIENTO TERAPÉUTICO PT/V1/02042014.1 Informe de Posicionamiento Terapéutico de Ofatumumab (Arzerra ) Fecha de publicación: 3 de abril de 2014 La leucemia linfocítica crónica (LLC) es
Un análisis bibliográfico (y pragmático) JM. López Vega Universidad de Cantabria
 Un análisis bibliográfico (y pragmático) del ensayo VELVET JM. López Vega Universidad de Cantabria Fundamentos del ensayo VELVET Ensayo HERNATA Andersson, J Clin Oncol 2011 TAXOTERE N = 143 VINORELBINA
Un análisis bibliográfico (y pragmático) del ensayo VELVET JM. López Vega Universidad de Cantabria Fundamentos del ensayo VELVET Ensayo HERNATA Andersson, J Clin Oncol 2011 TAXOTERE N = 143 VINORELBINA
Ultrarresúmenes Oposiciones de Enfermería Comunidad Autónoma de Madrid
 Manual CTO Ultrarresúmenes Oposiciones de Enfermería Comunidad Autónoma de Madrid 15 Tema Fundamentos de la práctica clínica basada en la evidencia. Búsqueda de evidencias científicas: bases de datos bibliográficas,
Manual CTO Ultrarresúmenes Oposiciones de Enfermería Comunidad Autónoma de Madrid 15 Tema Fundamentos de la práctica clínica basada en la evidencia. Búsqueda de evidencias científicas: bases de datos bibliográficas,
CLASIFICACIÓN DE ESTUDIOS CIENTÍFICOS Y LA EVIDENCIA CIENTÍFICA. Sesión de Residentes Societat Catalana de Cirurgia 13 diciembre, 2010
 CLASIFICACIÓN DE ESTUDIOS CIENTÍFICOS Y LA EVIDENCIA CIENTÍFICA Sesión de Residentes Societat Catalana de Cirurgia 13 diciembre, 2010 Criterios de clasificación de los tipos de estudios científicos Finalidad
CLASIFICACIÓN DE ESTUDIOS CIENTÍFICOS Y LA EVIDENCIA CIENTÍFICA Sesión de Residentes Societat Catalana de Cirurgia 13 diciembre, 2010 Criterios de clasificación de los tipos de estudios científicos Finalidad
Guía para la elaboración de informes de síntesis de evidencia: medicamentos Documento Metodológico
 Mayo 2015 Guía para la elaboración de informes de síntesis de evidencia: medicamentos Documento Metodológico Índice 1. Listado de abreviaturas... 2 2. Introducción... 3 3. Objetivos... 4 4. Metodología
Mayo 2015 Guía para la elaboración de informes de síntesis de evidencia: medicamentos Documento Metodológico Índice 1. Listado de abreviaturas... 2 2. Introducción... 3 3. Objetivos... 4 4. Metodología
Fuentes de información y búsqueda bibliográfica: Anexo A del Programa MADRE versión 4.0 (pág. 96 a 112)
 Fuentes de información y búsqueda bibliográfica: Anexo A del Programa MADRE versión 4.0 (pág. 96 a 112) Antonio Monzón Moreno Servicio de Farmacia Hospital Universitario Virgen del Rocío antonio.monzon.sspa@juntadeandalucia.es
Fuentes de información y búsqueda bibliográfica: Anexo A del Programa MADRE versión 4.0 (pág. 96 a 112) Antonio Monzón Moreno Servicio de Farmacia Hospital Universitario Virgen del Rocío antonio.monzon.sspa@juntadeandalucia.es
Comunicado de prensa. Basilea, 5 de diciembre de 2015
 Comunicado de prensa Basilea, 5 de diciembre de 2015 Según los nuevos resultados del estudio CLL-11, Gazyva/Gazyvaro proporcionó casi cuatro años sin tratamiento a pacientes con leucemia linfocítica crónica
Comunicado de prensa Basilea, 5 de diciembre de 2015 Según los nuevos resultados del estudio CLL-11, Gazyva/Gazyvaro proporcionó casi cuatro años sin tratamiento a pacientes con leucemia linfocítica crónica
En esta primera sesión de comunicaciones orales sobre melanoma y otros tumores cutáneos se han presentado las siguientes comunicaciones:
 En esta primera sesión de comunicaciones orales sobre se han presentado las siguientes comunicaciones: 1213O. Characterization of complete responses (CRs) in patients with advanced melanoma (MEL) who received
En esta primera sesión de comunicaciones orales sobre se han presentado las siguientes comunicaciones: 1213O. Characterization of complete responses (CRs) in patients with advanced melanoma (MEL) who received
PAPEL DE CETUXIMAB EN EL TRATAMIENTO DE 1ª LÍNEA DE CECC RECURRENTE Y METASTÁSICO. Pedro Pérez Segura Oncología Médica - HCSC
 PAPEL DE CETUXIMAB EN EL TRATAMIENTO DE 1ª LÍNEA DE CECC RECURRENTE Y METASTÁSICO Pedro Pérez Segura Oncología Médica - HCSC TRAYECTORIA DE CETUXIMAB Aprob CTX 1ªL ESMO/ASCO 1977 1985 2005 2008 2009 2010
PAPEL DE CETUXIMAB EN EL TRATAMIENTO DE 1ª LÍNEA DE CECC RECURRENTE Y METASTÁSICO Pedro Pérez Segura Oncología Médica - HCSC TRAYECTORIA DE CETUXIMAB Aprob CTX 1ªL ESMO/ASCO 1977 1985 2005 2008 2009 2010
XVII Xornadas do Colexio Oficial de Psicoloxía de Galicia
 XVII Xornadas do Colexio Oficial de Psicoloxía de Galicia Guía de Práctica Clínica de Prevención y Tratamiento de la Conducta Suicida: recomendaciones de tratamiento psicoterapéutico e información para
XVII Xornadas do Colexio Oficial de Psicoloxía de Galicia Guía de Práctica Clínica de Prevención y Tratamiento de la Conducta Suicida: recomendaciones de tratamiento psicoterapéutico e información para
Indicaciones clínicas formalmente aprobadas y fecha de aprobación:
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Arzerra 100 mg concentrado para solución para perfusión Arzerra 1.000 mg concentrado para solución para perfusión
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Arzerra 100 mg concentrado para solución para perfusión Arzerra 1.000 mg concentrado para solución para perfusión
[REGULACIÓN] Aprobación acelerada de medicamentos
![[REGULACIÓN] Aprobación acelerada de medicamentos [REGULACIÓN] Aprobación acelerada de medicamentos](/thumbs/93/113723816.jpg) [REGULACIÓN] Aprobación acelerada de medicamentos Emilio Jesús Alegre del Rey Farmacéutico especialista en Farmacia Hospitalaria Hospital Universitario de Puerto Real 2 3 4 Pero qué es antes, la obtención
[REGULACIÓN] Aprobación acelerada de medicamentos Emilio Jesús Alegre del Rey Farmacéutico especialista en Farmacia Hospitalaria Hospital Universitario de Puerto Real 2 3 4 Pero qué es antes, la obtención
Cobimetinib en el tratamiento del melanoma avanzado. Eficacia y Seguridad
 Mayo 216 Cobimetinib en el tratamiento del melanoma avanzado. Eficacia y Seguridad AETSA 216 Cobimetinib en el tratamiento del melanoma avanzado. Eficacia y seguridad. Agencia de Evaluación de Tecnologías
Mayo 216 Cobimetinib en el tratamiento del melanoma avanzado. Eficacia y Seguridad AETSA 216 Cobimetinib en el tratamiento del melanoma avanzado. Eficacia y seguridad. Agencia de Evaluación de Tecnologías
Indicaciones clínicas formalmente aprobadas y fecha de aprobación:
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
Metodología sobre Comparaciones indirectas
 Metodología sobre Comparaciones indirectas Pere Ventayol Servei de Farmàcia Hospital Universitari Son Dureta 1. Qué son las Comparaciones Indirectas? 2. Niveles de complejidad 3. Puntos clave 4. Validez
Metodología sobre Comparaciones indirectas Pere Ventayol Servei de Farmàcia Hospital Universitari Son Dureta 1. Qué son las Comparaciones Indirectas? 2. Niveles de complejidad 3. Puntos clave 4. Validez
Daniel García Belmonte 14 de junio de 2018
 Daniel García Belmonte 14 de junio de 2018 Linfoma difuso de célula grande B Linfomas de células T y NK. QT Linfoma anaplásico. QT Linfoma MALT de la dura. RT Barrera hematoencefálica Linfoma poco frecuente.
Daniel García Belmonte 14 de junio de 2018 Linfoma difuso de célula grande B Linfomas de células T y NK. QT Linfoma anaplásico. QT Linfoma MALT de la dura. RT Barrera hematoencefálica Linfoma poco frecuente.
INFORME PARA LA CURMP SOBRE POSICIONAMIENTO TERAPÉUTICO DE NIVOLUMAB EN CÁNCER DE PULMÓN NO MICROCÍTICO METASTÁSICO EN SEGUNDA LÍNEA DE TRATAMIENTO
 Página 1 de 5 Introducción El Cáncer de Pulmón (CP) es el tumor que más muertes causa en los países desarrollados, representando un problema sanitario de primera magnitud. Globalmente, el CP representa
Página 1 de 5 Introducción El Cáncer de Pulmón (CP) es el tumor que más muertes causa en los países desarrollados, representando un problema sanitario de primera magnitud. Globalmente, el CP representa
CONCEPTO Y EVALUACIÓN DE ALTERNATIVAS TERAPÉUTICAS EQUIVALENTES
 CONCEPTO Y EVALUACIÓN DE ALTERNATIVAS TERAPÉUTICAS EQUIVALENTES Silvia Fénix Caballero H. U. Puerto Real Servicio Andaluz de Salud Fármacos = Indicación Posicionamiento terapéutico y gestión eficiente
CONCEPTO Y EVALUACIÓN DE ALTERNATIVAS TERAPÉUTICAS EQUIVALENTES Silvia Fénix Caballero H. U. Puerto Real Servicio Andaluz de Salud Fármacos = Indicación Posicionamiento terapéutico y gestión eficiente
TEMA 4: DISTINTOS CONTRASTES EN ENSAYOS CLÍNICOS
 TEMA 4: DISTINTOS CONTRASTES EN ENSAYOS CLÍNICOS CONTENIDOS 1 Introducción: contrastes de hipótesis, p-valores e intervalos de confianza, significación estadística y clínicamente relevante 2 Ensayos Clínicos
TEMA 4: DISTINTOS CONTRASTES EN ENSAYOS CLÍNICOS CONTENIDOS 1 Introducción: contrastes de hipótesis, p-valores e intervalos de confianza, significación estadística y clínicamente relevante 2 Ensayos Clínicos
Tipos de Investigación Clínica. Investigación Clínica OBJETIVOS. mejorar la calidad y la expectativa de vida de los ciudadanos. aumentar su bienestar
 Tipos de Investigación Clínica Dra. Belén Sádaba Díaz de Rada Servicio de Farmacología Clínica Clínica Universidad de Navarra Investigación Clínica OBJETIVOS mejorar la calidad y la expectativa de vida
Tipos de Investigación Clínica Dra. Belén Sádaba Díaz de Rada Servicio de Farmacología Clínica Clínica Universidad de Navarra Investigación Clínica OBJETIVOS mejorar la calidad y la expectativa de vida
La revisión de la evidencia para esta guía se basó en dos procesos de análisis
 Material complementario en línea MÉTODOS Y PROCESO La revisión de la evidencia para esta guía se basó en dos procesos de análisis previos detallados. El primero fue de la conferencia de consenso de los
Material complementario en línea MÉTODOS Y PROCESO La revisión de la evidencia para esta guía se basó en dos procesos de análisis previos detallados. El primero fue de la conferencia de consenso de los
Nivolumab en el tratamiento del melanoma avanzado Eficacia y Seguridad
 Diciembre 2015 Nivolumab en el tratamiento del melanoma avanzado Eficacia y Seguridad Índice 1. Medicamento/ Descripción/ Indicación autorizada... 2 2. Descripción de la enfermedad... 3 3. Tratamiento
Diciembre 2015 Nivolumab en el tratamiento del melanoma avanzado Eficacia y Seguridad Índice 1. Medicamento/ Descripción/ Indicación autorizada... 2 2. Descripción de la enfermedad... 3 3. Tratamiento
FARMACOVIGILANCIA PRESCRIPCIÓN RAZONADA DE MEDICAMENTOS. Esther Salgueiro 10, 17 de Marzo de 2015
 FARMACOVIGILANCIA PRESCRIPCIÓN RAZONADA DE MEDICAMENTOS 10, 17 de Marzo de 2015 Esther Salgueiro (salgueiroesther@uniovi.es) FASES DEL DESARROLLO DE MEDICAMENTOS ENSAYO CLÍNICO CONTROLADO/ PRÁCTICA CLÍNICA
FARMACOVIGILANCIA PRESCRIPCIÓN RAZONADA DE MEDICAMENTOS 10, 17 de Marzo de 2015 Esther Salgueiro (salgueiroesther@uniovi.es) FASES DEL DESARROLLO DE MEDICAMENTOS ENSAYO CLÍNICO CONTROLADO/ PRÁCTICA CLÍNICA
Roche alcanza resultados positivos en un estudio de fase III fundamental con el pertuzumab contra el cáncer de mama HER2-positivo metastásico
 Comunicado de prensa Basilea, 8 de diciembre de 2011 Roche alcanza resultados positivos en un estudio de fase III fundamental con el pertuzumab contra el cáncer de mama HER2-positivo metastásico La mediana
Comunicado de prensa Basilea, 8 de diciembre de 2011 Roche alcanza resultados positivos en un estudio de fase III fundamental con el pertuzumab contra el cáncer de mama HER2-positivo metastásico La mediana
Comparaciones indirectas. Roberto Marín Gil FEA Farmacia Hospitalaria
 Comparaciones indirectas Roberto Marín Gil FEA Farmacia Hospitalaria Qué es una comparación indirecta? Comparación de diferentes intervenciones en salud usando datos de distintos estudios Porqué se hacen
Comparaciones indirectas Roberto Marín Gil FEA Farmacia Hospitalaria Qué es una comparación indirecta? Comparación de diferentes intervenciones en salud usando datos de distintos estudios Porqué se hacen
VINORELBINA ORAL. Evaluación para la Guía Farmacoterapéutica de Hospitales del Sistema Sanitario Público de Andalucía, Según el método GINF.
 VINORELBINA ORAL Evaluación para la Guía Farmacoterapéutica de Hospitales del Sistema Sanitario Público de Andalucía, Según el método GINF. Autores: Carmen Martínez Díaz, Jorge Díaz Navarro. Hospital Universitario
VINORELBINA ORAL Evaluación para la Guía Farmacoterapéutica de Hospitales del Sistema Sanitario Público de Andalucía, Según el método GINF. Autores: Carmen Martínez Díaz, Jorge Díaz Navarro. Hospital Universitario
Qué es y cómo deber ser un Ensayo clínico? Metanálisis: aprovechar el esfuerzo de otros
 Ensayo clínico Qué es y cómo deber ser un Ensayo clínico? La calidad de los ensayos clínicos Metanálisis: aprovechar el esfuerzo de otros Registros de ensayos clínicos Ensayo clínico: valoración del efecto
Ensayo clínico Qué es y cómo deber ser un Ensayo clínico? La calidad de los ensayos clínicos Metanálisis: aprovechar el esfuerzo de otros Registros de ensayos clínicos Ensayo clínico: valoración del efecto
: Azacitidina 100mg polvo para inyección. Indicaciones clínicas formalmente aprobadas y fecha de aprobación:
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
LECTURA CRÍTICA DE LA LITERATURA MÉDICA
 OBJETIVO LECTURA CRÍTICA DE LA LITERATURA MÉDICA Capacitar a los participantes en la formulación adecuada de preguntas de investigación, búsqueda de la literatura, análisis crítico de esta información,
OBJETIVO LECTURA CRÍTICA DE LA LITERATURA MÉDICA Capacitar a los participantes en la formulación adecuada de preguntas de investigación, búsqueda de la literatura, análisis crítico de esta información,
A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN
 6 CARMUSTINA EN IMPLANTES A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN 1. Denominación común internacional (DCI), denominación oficial española (DOE) o nombre genérico del principio activo. CARMUSTINA
6 CARMUSTINA EN IMPLANTES A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN 1. Denominación común internacional (DCI), denominación oficial española (DOE) o nombre genérico del principio activo. CARMUSTINA
Pembrolizumab en el tratamiento del melanoma avanzado Eficacia y Seguridad
 Diciembre 215 Pembrolizumab en el tratamiento del melanoma avanzado Eficacia y Seguridad Aetsa 215 Índice 1. Medicamento/ Descripción/ Indicación autorizada... 2 2. Descripción de la enfermedad... 3 3.
Diciembre 215 Pembrolizumab en el tratamiento del melanoma avanzado Eficacia y Seguridad Aetsa 215 Índice 1. Medicamento/ Descripción/ Indicación autorizada... 2 2. Descripción de la enfermedad... 3 3.
CONTROVERSIAS EN EL TRATAMIENTO DEL ASMA. BETA AGONISTAS Y SEGURIDAD
 CONTROVERSIAS EN EL TRATAMIENTO DEL ASMA. BETA AGONISTAS Y SEGURIDAD Desde hace décadas se cuestiona la seguridad del grupo. El Isoproterenol fue el primero en ser asociado a un incremento de muertes relacionadas
CONTROVERSIAS EN EL TRATAMIENTO DEL ASMA. BETA AGONISTAS Y SEGURIDAD Desde hace décadas se cuestiona la seguridad del grupo. El Isoproterenol fue el primero en ser asociado a un incremento de muertes relacionadas
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Arzerra 100 mg concentrado para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Arzerra 100 mg concentrado para solución para perfusión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml
CONTROVERSIA CONTROL ESTRICTO DE CIFRAS DE PRESIÓN ARTERIAL GRUPO 3
 CONTROVERSIA CONTROL ESTRICTO DE CIFRAS DE PRESIÓN ARTERIAL GRUPO 3 INTRODUCCIÓN La hipertensión es altamente prevalente en la población adulta, especialmente entre las personas mayores de 60 años de edad,
CONTROVERSIA CONTROL ESTRICTO DE CIFRAS DE PRESIÓN ARTERIAL GRUPO 3 INTRODUCCIÓN La hipertensión es altamente prevalente en la población adulta, especialmente entre las personas mayores de 60 años de edad,
Toxicidad y tratamiento de la inmunoterapia. Mauro Antonio Valles Cancela. Servicio de Oncología médica. Hospital Ernest Lluch Martín.
 Toxicidad y tratamiento de la inmunoterapia Mauro Antonio Valles Cancela. Servicio de Oncología médica. Hospital Ernest Lluch Martín. Calatayud Introducción Hasta 2010 DTIC, IL-2. Desde 2010 Ipilimumab,
Toxicidad y tratamiento de la inmunoterapia Mauro Antonio Valles Cancela. Servicio de Oncología médica. Hospital Ernest Lluch Martín. Calatayud Introducción Hasta 2010 DTIC, IL-2. Desde 2010 Ipilimumab,
GESIDA 2013: UNA BITERAPIA CON LOPINAVIR/RITONAVIR Y LAMIVUDINA SE MUESTRA NO INFERIOR A UNA PAUTA ESTÁNDAR
 GESIDA 2013: UNA BITERAPIA CON LOPINAVIR/RITONAVIR Y LAMIVUDINA SE MUESTRA NO INFERIOR A UNA PAUTA ESTÁNDAR Los resultados del estudio GARDEL revelan el potencial de este régimen en la terapia de inicio.
GESIDA 2013: UNA BITERAPIA CON LOPINAVIR/RITONAVIR Y LAMIVUDINA SE MUESTRA NO INFERIOR A UNA PAUTA ESTÁNDAR Los resultados del estudio GARDEL revelan el potencial de este régimen en la terapia de inicio.
Interpretación de estudios clínicos fase III para apoyar la toma de decisiones Vaccinology Ciro de Quadros 2016
 Interpretación de estudios clínicos fase III para apoyar la toma de decisiones Vaccinology Ciro de Quadros 2016 Dra. M Teresa Valenzuela B. Vice Decana Investigación y Postgrado Facultad de Medicina Universidad
Interpretación de estudios clínicos fase III para apoyar la toma de decisiones Vaccinology Ciro de Quadros 2016 Dra. M Teresa Valenzuela B. Vice Decana Investigación y Postgrado Facultad de Medicina Universidad
Innovación terapéutica en LLC
 Innovación terapéutica en LLC Javier de la Serna Sº de Hematología Hospital 12 de Octubre Madrid Que caracteriza la LLC Edad mediana al diagnóstico 70-75 años Hallazgo casual en 80% de casos Evolución
Innovación terapéutica en LLC Javier de la Serna Sº de Hematología Hospital 12 de Octubre Madrid Que caracteriza la LLC Edad mediana al diagnóstico 70-75 años Hallazgo casual en 80% de casos Evolución
BIBLIOGRAFICO ( )
 BIBLIOGRAFICO (12-11-2013) Int J Radiation Oncol Biol Phys, Vol. 85, No. 4, pp. 1057e1065, 2013 Elsevier Inc. http://dx.doi.org/10.1016/j.ijrobp.2012.08.041 INTRODUCCIÓN Quimioterapia + Radioterapia es
BIBLIOGRAFICO (12-11-2013) Int J Radiation Oncol Biol Phys, Vol. 85, No. 4, pp. 1057e1065, 2013 Elsevier Inc. http://dx.doi.org/10.1016/j.ijrobp.2012.08.041 INTRODUCCIÓN Quimioterapia + Radioterapia es
OBJETIVOS. GENERAL Introducir el PEG-Heberon a la práctica médica habitual del Sistema Nacional de Salud
 OBJETIVOS GENERAL Introducir el PEG-Heberon a la práctica médica habitual del Sistema Nacional de Salud ESPECÍFICOS Incorporar el uso de PEG-Heberon en combinación con ribavirina al tratamiento de la hepatitis
OBJETIVOS GENERAL Introducir el PEG-Heberon a la práctica médica habitual del Sistema Nacional de Salud ESPECÍFICOS Incorporar el uso de PEG-Heberon en combinación con ribavirina al tratamiento de la hepatitis
Cochrane y las RS. Qué es Cochrane
 Acerca de Cochrane Cochrane y las RS Qué es Cochrane Cochrane (www.cochrane.org) es una organización internacional cuya misión es ayudar a tomar decisiones sanitarias bien fundamentadas preparando, manteniendo
Acerca de Cochrane Cochrane y las RS Qué es Cochrane Cochrane (www.cochrane.org) es una organización internacional cuya misión es ayudar a tomar decisiones sanitarias bien fundamentadas preparando, manteniendo
La investigación en Farmacia Comunitaria al alcance de todos: Programa ADHIÉRETE. Laura Martín Gutiérrez Dpto. Servicios Asistenciales CGCOF
 La investigación en Farmacia Comunitaria al alcance de todos: Programa ADHIÉRETE Laura Martín Gutiérrez Dpto. Servicios Asistenciales CGCOF Índice Introducción El método científico Tipos de estudios Documentación
La investigación en Farmacia Comunitaria al alcance de todos: Programa ADHIÉRETE Laura Martín Gutiérrez Dpto. Servicios Asistenciales CGCOF Índice Introducción El método científico Tipos de estudios Documentación
Equivalentes terapéuticos
 Versión 1 10 Oct 2006 Equivalentes terapéuticos Por qué surge el concepto de equivalentes terapéuticos? El sistema de autorización de medicamentos por parte de las Agencias Reguladoras provoca que en el
Versión 1 10 Oct 2006 Equivalentes terapéuticos Por qué surge el concepto de equivalentes terapéuticos? El sistema de autorización de medicamentos por parte de las Agencias Reguladoras provoca que en el
PROYECTO FINAL. Bioestadística para no estadísticos Principios para interpretar un estudio científico (6ª ed.) GRUPO NP6
 Bioestadística para no estadísticos Principios para interpretar un estudio científico (6ª ed.) PROYECTO FINAL GRUPO NP6 Barcelona, 19 de Septiembre-12 de Diciembre Carlos Barreda Velázquez Raquel Cueto
Bioestadística para no estadísticos Principios para interpretar un estudio científico (6ª ed.) PROYECTO FINAL GRUPO NP6 Barcelona, 19 de Septiembre-12 de Diciembre Carlos Barreda Velázquez Raquel Cueto
Medicamento Dosis Días Administración Vinorelbina mg/m 2 (2,3) 1 Infusión de 50 ml SF administrado en min* (4,5)
 1. DENOMINACIÓN DEL ESQUEMA: VINORELBINA 2. INDICACIÓN Carcinoma de mama avanzado (1) 3. ESQUEMA Medicamento Dosis Días Administración Vinorelbina 25 30 mg/m 2 (2,3) 1 Infusión de 50 ml SF administrado
1. DENOMINACIÓN DEL ESQUEMA: VINORELBINA 2. INDICACIÓN Carcinoma de mama avanzado (1) 3. ESQUEMA Medicamento Dosis Días Administración Vinorelbina 25 30 mg/m 2 (2,3) 1 Infusión de 50 ml SF administrado
Cada CÁPSULA contiene: Temozolomida 5 mg Excipiente c.b.p. 1 cápsula. Temozolomida 20 mg Excipiente c.b.p. 1 cápsula.
 Marca TEMODAL Forma Famacéutica y Formulación Presentación PRESENTACIONES: Cajas de cartón con un frasco de vidrio ámbar con 5, 10 o 20cápsulas de 5, 20, 100, 140, 180 o 250 mg. COMPOSICIÓN FORMA FARMACÉUTICA
Marca TEMODAL Forma Famacéutica y Formulación Presentación PRESENTACIONES: Cajas de cartón con un frasco de vidrio ámbar con 5, 10 o 20cápsulas de 5, 20, 100, 140, 180 o 250 mg. COMPOSICIÓN FORMA FARMACÉUTICA
Los Avances en Melanoma Wednesday, 10 May :20
 El melanoma es uno de los tumores malignos cuya incidencia ha aumentado más rápidamente en los últimos años. En 2015 se diagnosticaron 2.577 casos en varones y 2.313 en mujeres con lo que la última cifra
El melanoma es uno de los tumores malignos cuya incidencia ha aumentado más rápidamente en los últimos años. En 2015 se diagnosticaron 2.577 casos en varones y 2.313 en mujeres con lo que la última cifra
Effectiveness and safety of atomoxetine for ADHD in population between 6 and 19 years: a systematic review
 Anexo 4 Resultados de los estudios ATX versus placebo Revisiones sistemáticas: Estudio Características Nº y tipos de estudios Calidad metodológica de estudios Variable de resultado Síntesis de resultados
Anexo 4 Resultados de los estudios ATX versus placebo Revisiones sistemáticas: Estudio Características Nº y tipos de estudios Calidad metodológica de estudios Variable de resultado Síntesis de resultados
Lucía Teijeira Sánchez Oncología médica Complejo Hospitalario de Navarra
 Terapias dirigidas en el anciano Lucía Teijeira Sánchez Oncología médica Complejo Hospitalario de Navarra Epidemiología Definiciones Qué es paciente anciano? No es lo mismo que paciente frágil No es lo
Terapias dirigidas en el anciano Lucía Teijeira Sánchez Oncología médica Complejo Hospitalario de Navarra Epidemiología Definiciones Qué es paciente anciano? No es lo mismo que paciente frágil No es lo
Comunicado de prensa. supervivencia mediana de los pacientes tratados con TECENTRIQ resultó ser de 13,8 meses, 4,2. Basilea, 9 de octubre de 2016
 Comunicado de prensa Basilea, 9 de octubre de 2016 TECENTRIQ (atezolizumab), de Roche, proporciona en un estudio de fase III una supervivencia significativamente mayor que la quimioterapia en un tipo determinado
Comunicado de prensa Basilea, 9 de octubre de 2016 TECENTRIQ (atezolizumab), de Roche, proporciona en un estudio de fase III una supervivencia significativamente mayor que la quimioterapia en un tipo determinado
Fuentes de Información de Medicamentos Mg. Roselly Robles Hilario
 Fuentes de Información de Medicamentos Mg. Roselly Robles Hilario Centro Nacional de Documentación e Información de Medicamentos CENADIM rrobles@digemid.minsa.gob.pe http://bvcenadim.digemid.minsa.gob.pe
Fuentes de Información de Medicamentos Mg. Roselly Robles Hilario Centro Nacional de Documentación e Información de Medicamentos CENADIM rrobles@digemid.minsa.gob.pe http://bvcenadim.digemid.minsa.gob.pe
EVALUACION Y ANALISIS DEL COMITÉ FARMACOTERAPÈUTICO PARA INCLUSION DE MEDICAMENTOS Al LISTADO OFICIAL
 MINISTERIO DE SALUD Anexo No.2 EVALUACION Y ANALISIS DEL COMITÉ FARMACOTERAPÈUTICO PARA INCLUSION DE MEDICAMENTOS Al LISTADO OFICIAL A. IDENTIFICACIÓN DEL FÁRMACO Denominación común internacional (DCI)
MINISTERIO DE SALUD Anexo No.2 EVALUACION Y ANALISIS DEL COMITÉ FARMACOTERAPÈUTICO PARA INCLUSION DE MEDICAMENTOS Al LISTADO OFICIAL A. IDENTIFICACIÓN DEL FÁRMACO Denominación común internacional (DCI)
Particularidades en la evaluación de fármacos hematológicos
 Particularidades en la evaluación de fármacos hematológicos Pascual Marco Vera. Vicepresidente de la S.E.H.H. Jefe de Servicio de Hematología-Hemoterapia Hospital General Universitario de Alicante Introducción
Particularidades en la evaluación de fármacos hematológicos Pascual Marco Vera. Vicepresidente de la S.E.H.H. Jefe de Servicio de Hematología-Hemoterapia Hospital General Universitario de Alicante Introducción
2. USO TERAPÉUTICO Cáncer colorrectal metastático o localmente avanzado en 2ª línea
 1. DENOMINACIÓN DEL ESQUEMA: IRINOTECÁN (CPT-11) 2. USO TERAPÉUTICO Cáncer colorrectal metastático o localmente avanzado en 2ª línea 3. ESQUEMA (1) Medicamento Dosis Días Administración CPT-11 350 mg/m
1. DENOMINACIÓN DEL ESQUEMA: IRINOTECÁN (CPT-11) 2. USO TERAPÉUTICO Cáncer colorrectal metastático o localmente avanzado en 2ª línea 3. ESQUEMA (1) Medicamento Dosis Días Administración CPT-11 350 mg/m
Comunicado de prensa. Basilea, 16 de mayo de 2013
 Comunicado de prensa a Basilea, 16 de mayo de 2013 Obinutuzumab (GA101), de Roche, redujo significativamente el riesgo de progresión de la enfermedad o muerte en personas con uno de los tipos más frecuentes
Comunicado de prensa a Basilea, 16 de mayo de 2013 Obinutuzumab (GA101), de Roche, redujo significativamente el riesgo de progresión de la enfermedad o muerte en personas con uno de los tipos más frecuentes
Programa MADRE 4.0: DE LA EVALUACIÓN AL POSICIONAMIENTO TERAPÉUTICO
 Programa MADRE 4.0: DE LA EVALUACIÓN AL POSICIONAMIENTO TERAPÉUTICO 97% nuevos medicamentos aprobados por EMA financiados en España INDUSTRIA CREA NUEVOS FÁRMACOS AGENCIAS APRUEBAN HOSPITALES & CCAA MODULAN
Programa MADRE 4.0: DE LA EVALUACIÓN AL POSICIONAMIENTO TERAPÉUTICO 97% nuevos medicamentos aprobados por EMA financiados en España INDUSTRIA CREA NUEVOS FÁRMACOS AGENCIAS APRUEBAN HOSPITALES & CCAA MODULAN
Palbociclib en el tratamiento del cáncer de mama localmente avanzado o metastásico Eficacia y Seguridad
 Mayo 2017 Palbociclib en el tratamiento del cáncer de mama localmente avanzado o metastásico Eficacia y Seguridad Palbociclib en el tratamiento del cáncer de mama localmente avanzado o metastásico. Eficacia
Mayo 2017 Palbociclib en el tratamiento del cáncer de mama localmente avanzado o metastásico Eficacia y Seguridad Palbociclib en el tratamiento del cáncer de mama localmente avanzado o metastásico. Eficacia
Preguntas para responder
 Preguntas para responder DIAGNÓSTICO DEL LUPUS ERITEMATOSO SISTÉMICO Detección precoz 1. La detección precoz y el tratamiento temprano mejoran el pronóstico y la supervivencia de las personas con lupus
Preguntas para responder DIAGNÓSTICO DEL LUPUS ERITEMATOSO SISTÉMICO Detección precoz 1. La detección precoz y el tratamiento temprano mejoran el pronóstico y la supervivencia de las personas con lupus
Nombre del fármaco e indicación clínica (Informe del Servicio de Farmacia Hospitalaria del Hospital xxxxxxxxxx) Fecha xx/xx/xx
 ANEXO II Modelo de Informe Técnico de Evaluación de Nuevos Medicamentos 1 Nombre del fármaco e indicación clínica (Informe del Servicio de Farmacia Hospitalaria del Hospital xxxxxxxxxx) Fecha xx/xx/xx
ANEXO II Modelo de Informe Técnico de Evaluación de Nuevos Medicamentos 1 Nombre del fármaco e indicación clínica (Informe del Servicio de Farmacia Hospitalaria del Hospital xxxxxxxxxx) Fecha xx/xx/xx
Guía de diagnóstico y tratamiento de Leucemia Linfoide Crónica. Sociedad de Hematología del Uruguay
 Guía de diagnóstico y tratamiento de Leucemia Linfoide Crónica Sociedad de Hematología del Uruguay Noviembre 2018 Definición Leucemia linfoide crónica/linfoma linfocítico de células pequeñas (CLL/SLL):
Guía de diagnóstico y tratamiento de Leucemia Linfoide Crónica Sociedad de Hematología del Uruguay Noviembre 2018 Definición Leucemia linfoide crónica/linfoma linfocítico de células pequeñas (CLL/SLL):
Tratamiento antimicrobiano de la bacteriuria en mujeres embarazadas
 antimicrobiano de la bacteriuria en mujeres embarazadas PREGUNTA Se requiere antimicrobiano de la bacteriuria asintomática en mujeres embarazadas? CONTEXTO asintomática en mujeres embarazadas La bacteriuria
antimicrobiano de la bacteriuria en mujeres embarazadas PREGUNTA Se requiere antimicrobiano de la bacteriuria asintomática en mujeres embarazadas? CONTEXTO asintomática en mujeres embarazadas La bacteriuria
Infiltrado Linfocitario Estromal como Factor Predictivo de Respuesta Completa Patológica en Cáncer de Mama HER2 positivo
 Infiltrado Linfocitario Estromal como Factor Predictivo de Respuesta Completa Patológica en Cáncer de Mama HER2 positivo María Asunción Algarra Servicio de Oncología Médica FUNDACIÓN INSTITUTO VALENCIANO
Infiltrado Linfocitario Estromal como Factor Predictivo de Respuesta Completa Patológica en Cáncer de Mama HER2 positivo María Asunción Algarra Servicio de Oncología Médica FUNDACIÓN INSTITUTO VALENCIANO
Aspectos generales de Farmacovigilancia. Métodos para la detección de reacciones adversas a fármacos: Estudios analíticos I.
 Aspectos generales de Farmacovigilancia Tema 3 Métodos para la detección de reacciones adversas a fármacos: Estudios analíticos I. Estudios de cohortes y estudios de casos y controles Miguelez C, Rivero
Aspectos generales de Farmacovigilancia Tema 3 Métodos para la detección de reacciones adversas a fármacos: Estudios analíticos I. Estudios de cohortes y estudios de casos y controles Miguelez C, Rivero
Marco de referencia. Pregunta adecuada, la droga en estudio tiene. -Diferente forma de administración, vía oral (PK)
 Marco de referencia Pregunta adecuada, la droga en estudio tiene -Diferente forma de administración, vía oral (PK) -Diferente mecanismo de acción (PD) Objetivos. Causalidad. Cual es la utilidad de los
Marco de referencia Pregunta adecuada, la droga en estudio tiene -Diferente forma de administración, vía oral (PK) -Diferente mecanismo de acción (PD) Objetivos. Causalidad. Cual es la utilidad de los
PROSPECTO INFORMACIÓN PARA PROFESIONALES (Adaptado a la Disposición ANMAT N 5904/96)
 PROSPECTO INFORMACIÓN PARA PROFESIONALES (Adaptado a la Disposición ANMAT N 5904/96) Gazyva Obinutuzumab Autorizado Bajo condiciones especiales Roche Concentrado para solución para infusión intravenosa
PROSPECTO INFORMACIÓN PARA PROFESIONALES (Adaptado a la Disposición ANMAT N 5904/96) Gazyva Obinutuzumab Autorizado Bajo condiciones especiales Roche Concentrado para solución para infusión intravenosa
FUENTE DE LOS DATOS DE EFECTIVIDAD Los datos de efectividad se obtuvieron de 2 estudios seleccionados tras una revisión bibliográfica.
 AUTOR (ES) Domínguez-Gil A, Rubio C. TITULO Análisis coste efectividad del tratamiento de las infecciones intra-abdominales con piperacilina/tazobactam, en comparación con imipenem/cilastatina. REVISTA
AUTOR (ES) Domínguez-Gil A, Rubio C. TITULO Análisis coste efectividad del tratamiento de las infecciones intra-abdominales con piperacilina/tazobactam, en comparación con imipenem/cilastatina. REVISTA
Niraparib en el tratamiento del cáncer de ovario Eficacia y seguridad relativas de niraparib y olaparib: comparaciones indirectas.
 Abril 2018 Niraparib en el tratamiento del cáncer de ovario Eficacia y seguridad relativas de niraparib y olaparib: comparaciones indirectas. Niraparib en el tratamiento del cáncer de ovario Eficacia y
Abril 2018 Niraparib en el tratamiento del cáncer de ovario Eficacia y seguridad relativas de niraparib y olaparib: comparaciones indirectas. Niraparib en el tratamiento del cáncer de ovario Eficacia y
