Elaborado por: Berta Inés Delgado Fajardo
|
|
|
- David Moreno Ortíz
- hace 7 años
- Vistas:
Transcripción
1 MD 1. Generalidades Los aminoácidos son ácidos orgánicos (con grupo carboxílico, -) que tienen un grupo amino ( ) enlazado a la cadena carbonada. unque el grupo amino puede estar en cualquier carbono de la cadena, los aminoácidos que se encuentran en la naturaleza, todos tienen el grupo amino sobre el carbono alfa,. El carbono es el carbono adyacente al carbono del grupo acido. Este -aminoácido se representa por la siguiente fórmula general: arbono 2 Grupo carboxílico adena radical Debido a la presencia del grupo carboxílico y del grupo amino, los aa tienen carácter ácido y básico por lo que son nfóteros. Este carácter determina las propiedades electrolíticas de las proteinas en solución y de éstas dependen sus propiedades biológicas. En estado sólido existen como iones dipolares, debido a la protonación del grupo amino y a la disociación del grupo carboxílico. El p en el cual predomina la concentración del ión dipolar se denomina punto isoelectrico. La forma dipolar se conoce con el nombre de Zwitterión. Grupo amino protonado 3 Grupo amino protonado - Grupo carboxílico disociado + Grupo carboxílico disociado 2 En soluciones muy ácidas (forma catiónica) eutra (ón dipolar) Zwitterión En soluciones básicas (forma aniónica) p 1 p 2 p 3 Punto isoeléctrico Ejemplo de punto isoeléctrico para la lisina: En un valor bajo de p (alta acidez), los dos grupos amino de la lisina se encuentran protonados y se tiene una forma catiónica, si vamos agregando base para disminuir la acidez y aumentar el p hasta 9,8, encontramos la forma neutra del aminoácido, forma Zwitterión. Este valor de p corresponde al punto isoeléctrico para la lisina. l continuar añadiendo base alcanzamos la forma aniónica a un p de 10,5.
2 argas: (+) (+) (+) (-) (+) (+) (-) (-) forma neutra Forma catiónica forma catiónica Zwitterión forma aniónica p: 2,2 9,0 9,8 10,5 El carbono de los aminoácidos es un carbono quiral, excepto en la glicina, por lo que los aminoácidos son óptimamente activos (rotan el plano de luz polarizada en diferente dirección, dependiendo de el estereoisómero que se analice) es decir pueden ser levógiros y dextrógiros, pero los aminoácidos que forman las proteínas son en general levógiros y se designan por la letra L. Ejemplos: L-leucina (L) L-valina (V) 2. LFÓ DE L MÁD e consideran dos grandes grupos de aminoácidos, los aminoácidos proteicos y aminoácidos no proteicos. (Ver cuadro anexo)
3 eutros o alifáticos Elaborado por: Berta nés Delgado Fajardo Gly, la, Val, Leu, le LF DE L MD romáticos Phe, Trp, Tyr M PTE odificables o Universales: Permanecen como tal en las Proteínas. aturaleza y propiedades de la cadena lateral. idroxiaminos Tioaminoacidos minoaminoacidos Dicarboxilicos er, Thr cisteina, metionina Pro, sp, sn, Glu, Gln Dibasicos Lys, rg, is D Modificados o Particulares Polaridad de la cadena lateral idroxilacion arboxilacion dicion de yodo ondensacion polares nionicos ationicos Polares sin carga la (); Val (V); Leu (L); le (); Phe (F); Trp (W); Met (M); Pro (P) sp (D); Glu (E) Lys (K); rg (); is () Gly (G); Tyr (Y); er (); Thr (T); ys (); sn (); Gln (Q) PTE L-ornitina, L-citrulina, reatina, omoserina D-alanina, D-glutamina, D-fenilalanina -alanina, cido--aminobutirico.
4 2.1. L MÁD PTE se dividen en aminoácidos codificables o universales que permanecen como tales en las proteínas y aminoácidos modificados o particulares que son el resultado de diversas modificaciones químicas que ocurren con posterioridad a la síntesis de proteínas minoácidos codificables se clasifican según la naturaleza de la cadena lateral y según la polaridad de esa cadena. De acuerdo con la naturaleza de la cadena lateral los aminoácidos se clasifican en: eutros o lifáticos: En ellos la cadena lateral es un hidrocarburo alifático. on muy poco reactivos, y fuertemente hidrofóbicos (excepto la Gly, cuya cadena lateral es un átomo de hidrógeno). Estos aa hidrofóbicos tienden a ocupar la parte central de las proteínas globulares, de modo que minimizan su interacción con el disolvente, contribuyendo a la estructura global de la proteina (forman las micelas proteicas). La glycina (G) tiene un importante papel estructural: es invariante en las series filogenéticas. 2 Glicina (Gly) (G) 3 lanina (la) () 3 3 Valina (Val) (V) 3 3 Leucina (Leu) (L) 3 3 soleucina (le) () romáticos: La cadena lateral es un grupo aromático, benceno en el caso de la F, fenol en el caso de la Y e indol en el caso del W. Estos aa, además de formar parte de las proteínas son precursores de otras biomoléculas de interés: ormonas tiroideas, pigmentos o neurotransmisores. La absorción de luz UV por parte de las proteinas, se debe a la presencia de los sistemas aromáticos que absorben luz UV alrededor de los 280 nm. Los aminoácidos fenilalanina y triptofano son hidrofóbicos. Fenialanina (Phe) (F) Triptofano (Trp) (W) Tirosina (Tyr) (Y) idroxiáminoacidos: Poseen un grupo hidroxi en su cadena lateral. on la treonina (T) y la serina (). El grupo - de la er es fundamental en el centro activo de las enzimas denominadas proteinazas. Forma enlaces glicosidicos con oligosacaridos en ciertas proteínas. El grupo es susceptible de fosforilación y
5 es una importante modificación post-traduccional que regula la actividad de muchas proteínas. 3 Treonina (Thr) (T) erina (er) () Tioaminoácidos: ontienen azufre. on y M. La cisteína () tiene gran importancia estructural en las proteínas porque puede reaccionar con el grupo de otra para formar un puente disulfuro (---) permitiendo el plegamiento de la proteína. Por este motivo, en algunos hidrolizados proteicos se obtiene el aa cistina, que está formado por dos cisteínas unidas por un puente disulfuro. Tienen un importante papel estructural, especialmente la isteina por la posibilidad de formar los enlaces disulfuro. Participan en el centro activo de muchas enzimas. La metionina es el aminoácido iniciador de la síntesis de proteínas (odon UG) 3 isteina (ys) () Metionina (Met) (M) minoácidos: Tienen el grupo -amino sustituido por la propia cadena lateral formando un anillo pirrolidínico, es el caso de la prolina que tiene un importante papel estructural, es muy abundante en el colágeno. Prolina (Pro) (P) Dicarboxílicos Y us midas: on el ácido aspártico (D) y el ácido glutámico (E) us amidas correspondientes son la asparragina () y la glutamina (Q) on importantes intermediarios en el metabolismo nitrogenado, sobre todo el Glu y Gln. Forman parte del centro activo de las glicosidasas y de las serin-enzimas. Proveen a la proteína de superficies aniónicas que sirven para fijar cationes como el a cido spartico (sp) (D) sparagina (sn) () cido Glutamico (Glu) (E) Glutamina (Gln) (Q)
6 Dibásicos: La cadena lateral de éstos aa contiene grupos básicos. El grupo básico puede ser un grupo amino como en la lisina (K), un grupo guanidino como en la arginina () o un grupo imidazol como en la histidina () La lisina forma intermediaros covalentes del tipo iminas, en las reacciones catalizadas por enzimas. Este aa (lisina) une determinadas coenzimas a la estructura de la proteína. En el caso de la rg es un importante intermediario en el ciclo de la urea. La is forma parte del sitio activo de muchas enzimas, debido al carácter nucleofilico del midasol. ontribuye al tamponamiento de los medios biológicos para tener un pka cercano al p intracelular. 2 Lisina (Lys) (K) rginina (rg) () istidina (is) () De los 20 aa proteicos, la mitad pueden ser sintetizados por el hombre, pero el resto no y por lo tanto deben ser suministrados en la dieta: son los aa esenciales. on esenciales: Val, Leu, le, Phe, Trp, Tyr, Thr, is, Met y Lys. on estructuras necesarias para el funcionamiento del organismo, pero como no tenemos mecanismos para su síntesis, debemos adquirirlos de fuentes externas, por lo que se conocen con el nombre de esenciales. En los recién nacidos el aa is es esencial porque su organismo todavía no ha madurado lo suficiente como para poder sintetizarlo. Los aminoácidos codificables de acuerdo con la polaridad de la cadena lateral se agrupan en: apolares, polares sin carga, catiónicos y aniónicos. Ver tabla 1.
7 Tabla 1. lasificación de los aminoácidos en función de la polaridad de la cadena lateral lase aracterística ombre imbolos Estructura lanina la () 3 P L E on hidrofóbicos Valina Val (V) 3 3 Leucina Leu (L) 3 3 soleucina leu () 3 3 Fenilalanina Phe (F) Triptofano Trp (W) Metionina Met (M) 3 Prolina Pro (P) P L E in carga Glicina Gly (G) 2 Tyrosina Tyr (Y) erina er () Treonina Thr (T) 3 isteina ys () sparagina sn () 2 Glutamina (Glu) (Q) 2
8 T on Lisina (Lys) (K) 2 aa básicos rginina rg () istidina is () on aa cidos cido aspártico sp (D) cido glutámico Glu (E) minoácidos Modificados o Particulares (Modificaciones postraduccionales). Los aminoácidos codificables presentes en las proteínas pueden experimentar transformaciones que dan lugar a los aminoácidos modificados. Las modificaciones más frecuentes son la hidroxilación, la yodación, la carboxilación y la condensación. La hidroxilación: ocurre generalmente en lisina (K) y prolina (P), que se incorporan a la proteína y después son hidroxilados transformándose en hidroxilisina e hidroxiprolina respectivamente: 2 idroxilisina idroxiprolina
9 La iodación: ocurre por adición de yodo, un ejemplo en la tiroglobulina (una proteina de la tiroides) la tirosina (Y) experimenta iodación del anillo aromático. El yodo entra en las posiciones orto respecto al hidroxilo del anillo aromático: Monoiodotirosina diiodotirosina La carboxilación: en el acido glutámico, la carboxilación después de la síntesis del ácido glutámico (E), lo convierte en ácido -carboxiglutámico cido glutámico (E) cido--carboxiglutámico La condensación: ocurre en la cisteina cuando dos moles se condensan por medio de un puente disulfuro y forman la cistina 2 Dos moles de cisteina istina 2.2. MÁD PTE. e encuentran en plantas superiores y son numerosos. Pertenecen a tres grandes grupos. En la tabla 2 se presenta la clasificación completa.
10 Tabla 2. minoácidos no proteicos lase minoacido aracterística Estructura D-alanina D-aminoacidos e encuentran en general en algunos péptidos y en algunos antibióticos. Por ejemplo estan presentes en péptidos opiodes de anfibios y reptiles. cido D- glutamico D-fenilalanina Forman parte del peptido glicano 1 de la pared celular de las bacterias Presente en el peptido gramisidina-, que tiene acción antibiótica 3 L-ornitina L-citrulina on importantes como intermediarios en el metabolismo de la eliminación del nitrógeno L-homocisteina ntermediario metabólico de la metionina. Puede causar daño arterial 2 2 -aminoacidos no proteicos -aminoacidos L-homoserina L-dopa -alanina ntermediario metabólico en forma de lactona que inhibe la fijación de nitrógeno de las pseudomonas ntermediario metabólico de la tirosina y precursor de catecolaminas, hormonas tiroideas ymelanina Forma parte de algunas coenzimas 2 2 El grupo amino sustituye al carbono y no al carbono cido-aminobutírico (GB) Es un importante neurotransmisor 2 1 Peptido glicano: es una capa resistente que forma la pared celular de la bacteria, constituyendose en un soporte estructural y morfológico. Es un tetrapéptido formado por L-ala, D-ala, D-glu y L-lis, junto con -acetilglucosamina y ácido -acetil murámico.
11 3. BTE DE MD (íntesis de trecker) En ésta síntesis se utiliza un aldehido, ácido cianhídrico y amoniaco. El producto final es una mezcla racémica que puede separarse utilizando enzimas quirales, llamadas decilasas, que reaccionan fácilmente con la forma L. El mecanismo de reacción comprende tres etapas: en la primera etapa se adiciona el amoniaco (mecanismo de adición nucleofílica) para formar la hidroxilamina la cual se deshidrata fácilmente para formar la imina: acetaldehido amoniaco hidroxilamina mina gua + adición nucleofílica deshidratación (eliminación) En el segundo paso, la imina que es el análogo nitrogenado del grupo carbonilo, experimenta una nueva reacción de adición nucleofílica con el ácido cianhídrico y forma un aminonitrilo: mina cido cianhídrico minonitrilo Finalmente el aminonitrilo sufre una hidrólisis en presencia de ácido sulfúrico, agua y calor y produce el -aminoácido correspondiente calor idrólisis del nitrilo -aminoacido (mezcla racémica)
 Aminoácidos I Br. Cecilia López Área Bioquímica Departamento de Biología Molecular y Celular Marzo 2012 Aminoácidos Proteínas Neurotransmisores (GABA, dopamina) Mediadores de la inflamación (Histamina)
Aminoácidos I Br. Cecilia López Área Bioquímica Departamento de Biología Molecular y Celular Marzo 2012 Aminoácidos Proteínas Neurotransmisores (GABA, dopamina) Mediadores de la inflamación (Histamina)
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA
 BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas.
 Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas.
 Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
CLASIFICACIÓN SEGÚN SU POLARIDAD NO POLARES POLARES NEUTROS ACIDOS BASICOS
 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2015 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2015 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
Lehninger Principles of Biochemistry Fourth Edition
 David L. Nelson and Michael M. Cox Lehninger Principles of Biochemistry Fourth Edition Capítulo 3: Amino Acidos, Péptidos, y Proteínas Copyright 2004 by W. H. Freeman & Company Estereoquímica de Aminoácidos
David L. Nelson and Michael M. Cox Lehninger Principles of Biochemistry Fourth Edition Capítulo 3: Amino Acidos, Péptidos, y Proteínas Copyright 2004 by W. H. Freeman & Company Estereoquímica de Aminoácidos
Metabolismo de AMINOÁCIDOS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA
 Rol de los Aminoácidos en el Cultivo de Vid XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA 2011 La Molina, 06 y 07 de Julio, 2011 Ing. M.Sc. Federico Ramírez D. Gerente Técnico Aminoácidos Las plantas
Rol de los Aminoácidos en el Cultivo de Vid XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA 2011 La Molina, 06 y 07 de Julio, 2011 Ing. M.Sc. Federico Ramírez D. Gerente Técnico Aminoácidos Las plantas
3. AMINOACIDOS. PROPIEDADES ACIDO-BASE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 3. AMINOACIDOS. PROPIEDADES ACIDO-BASE ESQUEMA - Aminoácidos. Definición, funciones y clasificación - Tipos de aminoácidos: aminoácidos
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 3. AMINOACIDOS. PROPIEDADES ACIDO-BASE ESQUEMA - Aminoácidos. Definición, funciones y clasificación - Tipos de aminoácidos: aminoácidos
AMINOÁCIDOS Y PÉPTIDOS
 TEMA 4 AMINOÁCIDOS Y PÉPTIDOS 1. Estructura y clasificación de los aminoácidos. 2. Propiedades ácido-base de los aminoácidos y péptidos 3. El enlace peptídico 4. Péptidos: hidrólisis y secuenciación 1.
TEMA 4 AMINOÁCIDOS Y PÉPTIDOS 1. Estructura y clasificación de los aminoácidos. 2. Propiedades ácido-base de los aminoácidos y péptidos 3. El enlace peptídico 4. Péptidos: hidrólisis y secuenciación 1.
AMINOÁCIDOS, PÉPTIDOS Y PROTEINAS. M.Sc. GABY MÓNICA FELIPE BRAVO
 AMINÁCIDS, PÉPTIDS Y PRTEINAS M.Sc. GABY MÓNICA FELIPE BRAV AMINÁCIDS C H 2 N C H R TDS LS AMINÁCIDS QUE FRMAN PARTE DE LAS PRTEÍNAS SN L-AMINÁCIDS CLASIFICACIÓN DE LS AMINÁCIDS ALIFÁTICS N PLARES ARMÁTICS
AMINÁCIDS, PÉPTIDS Y PRTEINAS M.Sc. GABY MÓNICA FELIPE BRAV AMINÁCIDS C H 2 N C H R TDS LS AMINÁCIDS QUE FRMAN PARTE DE LAS PRTEÍNAS SN L-AMINÁCIDS CLASIFICACIÓN DE LS AMINÁCIDS ALIFÁTICS N PLARES ARMÁTICS
Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de
 Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
QUÍMICA DE PROTEÍNAS
 QUÍMICA DE PROTEÍNAS COMPOSICIÓN ALIMENTO VOLATIL POR SECADO (AGUA o HUMEDAD) MATERIA SECA ORGANICA INORGANICA (CENIZAS) SOLUBLE EN DISOLVENTES ORGANICOS (GRASA O LIPIDOS) CON NITROGENO (PROTEINAS) NO
QUÍMICA DE PROTEÍNAS COMPOSICIÓN ALIMENTO VOLATIL POR SECADO (AGUA o HUMEDAD) MATERIA SECA ORGANICA INORGANICA (CENIZAS) SOLUBLE EN DISOLVENTES ORGANICOS (GRASA O LIPIDOS) CON NITROGENO (PROTEINAS) NO
Proteínas. Fabrizio Marcillo Morla MBA. (593-9)
 Proteínas Fabrizio Marcillo Morla MBA barcillo@gmail.com (593-9) 4194239 Otras Publicaciones del mismo autor en Repositorio ESPOL Fabrizio Marcillo Morla Guayaquil, 1966. BSc. Acuicultura. (ESPOL 1991).
Proteínas Fabrizio Marcillo Morla MBA barcillo@gmail.com (593-9) 4194239 Otras Publicaciones del mismo autor en Repositorio ESPOL Fabrizio Marcillo Morla Guayaquil, 1966. BSc. Acuicultura. (ESPOL 1991).
Metabolismo y uso de Proteínas. Jorge Ml. Sánchez Centro de Inv. en Nutrición Animal Escuela de Zootecnia Universidad de Costa Rica
 Metabolismo y uso de Proteínas Jorge Ml. Sánchez Centro de Inv. en Nutrición Animal Escuela de Zootecnia Universidad de Costa Rica Metabolismo de las Proteínas Funciones en el organismo 1. Constituyen
Metabolismo y uso de Proteínas Jorge Ml. Sánchez Centro de Inv. en Nutrición Animal Escuela de Zootecnia Universidad de Costa Rica Metabolismo de las Proteínas Funciones en el organismo 1. Constituyen
ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS AMINOÁCIDOS
 ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS Fabián Rodríguez Julio 2011 AMINOÁCIDOS Un aminoácido es una molécula orgánica que en su estructura contiene un grupo amino (NH 2 ) y un grupo carboxilo
ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS Fabián Rodríguez Julio 2011 AMINOÁCIDOS Un aminoácido es una molécula orgánica que en su estructura contiene un grupo amino (NH 2 ) y un grupo carboxilo
Síntesis de aminoácidos
 Síntesis de aminoácidos 2. Aminoácidos esenciales y no esenciales Los 20 aminoácidos son biológicamente imprescindibles o esenciales! Se llaman aá esenciales los que deben ser suministrados en la dieta
Síntesis de aminoácidos 2. Aminoácidos esenciales y no esenciales Los 20 aminoácidos son biológicamente imprescindibles o esenciales! Se llaman aá esenciales los que deben ser suministrados en la dieta
Composición química de los seres vivos
 Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Se encuentra separado del citoplasma por la envoltura nuclear, que está formada por varias cisternas del retículo endoplasmático, que se mantienen uni
 Se encuentra separado del citoplasma por la envoltura nuclear, que está formada por varias cisternas del retículo endoplasmático, que se mantienen unidas gracias a una red de filamentos intermedios que
Se encuentra separado del citoplasma por la envoltura nuclear, que está formada por varias cisternas del retículo endoplasmático, que se mantienen unidas gracias a una red de filamentos intermedios que
METABOLISMO DE AMINOACIDOS. Kinesiología 2011
 METABOLISMO DE AMINOACIDOS Kinesiología 2011 BALANCE NITROGENADO BN=Nitrógeno total ingerido Nitrógeno total excretado BN=0 existe equilibrio nitrogenado BN es negativo, cuando hay condiciones de síntesis
METABOLISMO DE AMINOACIDOS Kinesiología 2011 BALANCE NITROGENADO BN=Nitrógeno total ingerido Nitrógeno total excretado BN=0 existe equilibrio nitrogenado BN es negativo, cuando hay condiciones de síntesis
Material elaborado por F. Agius, O. Borsani, P.Díaz, S. Gonnet, P. Irisarri, F. Milnitsky y J. Monza. Bioquímica. Facultad de Agronomía.
 AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS
 EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS 1) Qué es un tetrapéptido?. Construye uno, formado por los siguientes aminoácidos: Ala, Cys, Ser y Tyr. 2) Haz corresponder los elementos de las dos columnas: -Cys -Hormona
EJERCICIOS DE BIOQUÍMICA: PRÓTIDOS 1) Qué es un tetrapéptido?. Construye uno, formado por los siguientes aminoácidos: Ala, Cys, Ser y Tyr. 2) Haz corresponder los elementos de las dos columnas: -Cys -Hormona
Aminoácidos y péptidos
 Aminoácidos y péptidos AMINOÁCIDOS: Moléculas orgánicas con un grupo amino (NH 2) y un grupo carboxilo (COOH). Los aminoácidos proteicos son α aminoácidos, que portan las dos funciones sobre el carbono
Aminoácidos y péptidos AMINOÁCIDOS: Moléculas orgánicas con un grupo amino (NH 2) y un grupo carboxilo (COOH). Los aminoácidos proteicos son α aminoácidos, que portan las dos funciones sobre el carbono
Holoproteínas (sólo contienen aa)
 TEMA 4: P ROTEÍNAS 1. Concepto y clasificación Las proteínas son biomoléculas orgánicas formadas por C, H, O, N y en menor medida P y S y otros elementos (Fe,Cu, Mg, ). Son polímeros no ramificados de
TEMA 4: P ROTEÍNAS 1. Concepto y clasificación Las proteínas son biomoléculas orgánicas formadas por C, H, O, N y en menor medida P y S y otros elementos (Fe,Cu, Mg, ). Son polímeros no ramificados de
Metodologías básicas del procesamiento de Proteinas
 Metodologías básicas del procesamiento de Proteinas Alejandra Kun Departamento de Proteínas y Ácidos Nucleicos-IIBCE Unidad Asociada Sección Bioquímica Facultad de Ciencias 13 de octubre 2014 Curso Introducción
Metodologías básicas del procesamiento de Proteinas Alejandra Kun Departamento de Proteínas y Ácidos Nucleicos-IIBCE Unidad Asociada Sección Bioquímica Facultad de Ciencias 13 de octubre 2014 Curso Introducción
BIOMOLÉCULAS. Son moléculas fundamentales para la constitución y funcionamiento de todo ser vivo. Se clasifican en dos grupos:
 FICHA N 2 UNIDAD III: CÉLULAS A ORGANISMOS Profesora Verónica Abasto Córdova Ciencias Naturales 8 Básico Nombre : Curso : Fecha : Revisión BIOMOLÉCULAS Son moléculas fundamentales para la constitución
FICHA N 2 UNIDAD III: CÉLULAS A ORGANISMOS Profesora Verónica Abasto Córdova Ciencias Naturales 8 Básico Nombre : Curso : Fecha : Revisión BIOMOLÉCULAS Son moléculas fundamentales para la constitución
Diferencias entre leche de vaca y de cabra
 Diferencias entre leche de vaca y de cabra Introducción: La leche de cabra tiene propiedades interesantes. El objetivo de este trabajo es poner de relieve algunas de las diferencias entre leche de cabra
Diferencias entre leche de vaca y de cabra Introducción: La leche de cabra tiene propiedades interesantes. El objetivo de este trabajo es poner de relieve algunas de las diferencias entre leche de cabra
A M I N O Á C I D O S
 A M I N O Á C I D O S Qué son? Son componentes básicos, estructurales o funcionales de los pép-dos y las proteínas. Presentan: un grupo carboxilo COOH (ácido) y un grupo amino NH2 (básico) Todos los aminoácidos
A M I N O Á C I D O S Qué son? Son componentes básicos, estructurales o funcionales de los pép-dos y las proteínas. Presentan: un grupo carboxilo COOH (ácido) y un grupo amino NH2 (básico) Todos los aminoácidos
AMINOACIDOS Y PROTEÍNAS
 AMINOACIDOS Y PROTEÍNAS I. OBJETIVO. Reconocer aminoácidos y proteínas a nivel de laboratorio. Analizar el tipo de estructura de los aminoácidos. II. FUNDAMENTO TEORICO. AMINOACIDOS: Cualquiera de los
AMINOACIDOS Y PROTEÍNAS I. OBJETIVO. Reconocer aminoácidos y proteínas a nivel de laboratorio. Analizar el tipo de estructura de los aminoácidos. II. FUNDAMENTO TEORICO. AMINOACIDOS: Cualquiera de los
Estructura del grupo carbonilo
 TEMA 19.- Compuestos carbonílicos. Clasificación y propiedades generales. Reacciones de adición. Características generales y factores con influencia en la velocidad de la adición. Adiciones de Michael.
TEMA 19.- Compuestos carbonílicos. Clasificación y propiedades generales. Reacciones de adición. Características generales y factores con influencia en la velocidad de la adición. Adiciones de Michael.
FISIOLOGÍA GENERAL Jesús Merino Pérez y María José Noriega Borge
 BIOMOLÉCULAS. PROTEÍNAS BIOMOLÉCULAS Los bioelementos se unen para formar biomoléculas, también denominadas principios inmediatos. En los seres vivos las moléculas se caracterizan por presentar una gran
BIOMOLÉCULAS. PROTEÍNAS BIOMOLÉCULAS Los bioelementos se unen para formar biomoléculas, también denominadas principios inmediatos. En los seres vivos las moléculas se caracterizan por presentar una gran
BIOSINTESIS DE AMINOACIDOS
 BISITESIS DE AMIAIDS ARATERISTIAS Y RIEDADES Estructura de los aminoácidos Subunidades monoméricas roteínas Enzimas Anticuerpos rganelos y órganos arbono alfa (quiral) Sustituyentes diferentes R cadena
BISITESIS DE AMIAIDS ARATERISTIAS Y RIEDADES Estructura de los aminoácidos Subunidades monoméricas roteínas Enzimas Anticuerpos rganelos y órganos arbono alfa (quiral) Sustituyentes diferentes R cadena
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA ESCUELA DE CIENCIAS BASICAS TECNOLOGIA E INGENIERIA
 ESCUELA DE CIENCIAS BÁSICAS, TECNOLOGÍA E INGENIERÍA - ECBTI UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA ESCUELA DE CIENCIAS BASICAS TECNOLOGIA E INGENIERIA TEXTO OVA UNIDAD 1 201103 BIOQUÍMICA ALBERTO
ESCUELA DE CIENCIAS BÁSICAS, TECNOLOGÍA E INGENIERÍA - ECBTI UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA ESCUELA DE CIENCIAS BASICAS TECNOLOGIA E INGENIERIA TEXTO OVA UNIDAD 1 201103 BIOQUÍMICA ALBERTO
SÍNTESIS DE AMINOÁCIDOS Y ORIGEN. INTRODUCCIÓN
 SÍNTESIS DE AMINOÁCIDOS Y ORIGEN. INTRODUCCIÓN La mayoría son ingeridos como proteínas en la dieta. Estas proteínas sufren un proceso de digestión para dar lugar a los aminoácidos que las forman. Además,
SÍNTESIS DE AMINOÁCIDOS Y ORIGEN. INTRODUCCIÓN La mayoría son ingeridos como proteínas en la dieta. Estas proteínas sufren un proceso de digestión para dar lugar a los aminoácidos que las forman. Además,
GUIA DE ESTUDIO Nº 9: Aminoácidos, Proteínas y Enzimas
 GUIA DE ESTUDIO Nº 9: Aminoácidos, Proteínas y Enzimas I.- Conceptos básicos: Aminoácidos: Estructura y propiedades ácido base de los aminoácidos. Clasificación según su polaridad. Capacidad buffer. El
GUIA DE ESTUDIO Nº 9: Aminoácidos, Proteínas y Enzimas I.- Conceptos básicos: Aminoácidos: Estructura y propiedades ácido base de los aminoácidos. Clasificación según su polaridad. Capacidad buffer. El
ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO
 ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO Todos los aminoácidos tienen, como mínimo, dos grupos titulables o ionizables, cada uno con un pka característico y, por tanto, con dos zonas tampón
ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO Todos los aminoácidos tienen, como mínimo, dos grupos titulables o ionizables, cada uno con un pka característico y, por tanto, con dos zonas tampón
01. INTRODUCCION. Conceptos previos. Verónica González Núñez Universidad de Salamanca
 01. INTRODUCCION. Conceptos previos Verónica González Núñez Universidad de Salamanca ESQUEMA. Introducción. Conceptos previos I. Principales grupos funcionales en Bioquímica II. Formación de compuestos
01. INTRODUCCION. Conceptos previos Verónica González Núñez Universidad de Salamanca ESQUEMA. Introducción. Conceptos previos I. Principales grupos funcionales en Bioquímica II. Formación de compuestos
OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo.
 1 OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo. 2 3 4 Son las moléculas que forman a los organismos o participan de su metabolismo. Orgánicas
1 OBJETIVO Describir las moléculas orgánicas e inorgánicas en cuanto a su estructura y función nuestro organismo. 2 3 4 Son las moléculas que forman a los organismos o participan de su metabolismo. Orgánicas
Estructura y propiedades de las proteínas
 Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
Digestión y absorción de PROTEÍNAS. Marijose Artolozaga Sustacha, MSc
 Digestión y absorción de PROTEÍNAS Marijose Artolozaga Sustacha, MSc Digestión de proteínas de la dieta La mayor fuente de N de la dieta son las proteínas Unos 100g de proteína al día No se pueden absorber
Digestión y absorción de PROTEÍNAS Marijose Artolozaga Sustacha, MSc Digestión de proteínas de la dieta La mayor fuente de N de la dieta son las proteínas Unos 100g de proteína al día No se pueden absorber
Estereoisomerismo en los alfaaminoácidos.
 Estructura general de un aminoácido. Esta estructura es común a todos los alfaaminoácidos, con una única excepción. (La excepción es la prolina, un aminoácido cíclico). El grupo R o cadenal lateral (en
Estructura general de un aminoácido. Esta estructura es común a todos los alfaaminoácidos, con una única excepción. (La excepción es la prolina, un aminoácido cíclico). El grupo R o cadenal lateral (en
Conocer.. Química Medicinal (FARMACOQUÍMICA) Comprender. Propiedades ADME. Relación estructura-actividad. Propiedades fisicoquímicas
 Química Medicinal (FAMACQUÍMICA) Conocer.. Propiedades fisicoquímicas Influencia de la estructura química sobre la actividad biológica Comprender Mecanismos de acción biológica (farmacológica / toxicológica)
Química Medicinal (FAMACQUÍMICA) Conocer.. Propiedades fisicoquímicas Influencia de la estructura química sobre la actividad biológica Comprender Mecanismos de acción biológica (farmacológica / toxicológica)
Pagina casos de estudios:
 Libros para consulta de alumnos en el Área de Biología La Célula. De Coopers Biología Celular y Molecular G. Karp Becker.El mundo de la Célula 6Ed. Editorial Pearson Education. Alberts/Bray/Hopkin/Johnson/Lewis/Raff/Roberts/Walter.
Libros para consulta de alumnos en el Área de Biología La Célula. De Coopers Biología Celular y Molecular G. Karp Becker.El mundo de la Célula 6Ed. Editorial Pearson Education. Alberts/Bray/Hopkin/Johnson/Lewis/Raff/Roberts/Walter.
ÁCIDOS NUCLEICOS. Aguanten Gregor Mendel y los guisantes!
 ÁCIDOS NUCLEICOS Aguanten Gregor Mendel y los guisantes! ÁCIDOS NUCLEICOS caracts. grales. ADN y ARN son los mensajeros químicos de la información genética de los seres vivos. Son polímeros de nucleótidos,
ÁCIDOS NUCLEICOS Aguanten Gregor Mendel y los guisantes! ÁCIDOS NUCLEICOS caracts. grales. ADN y ARN son los mensajeros químicos de la información genética de los seres vivos. Son polímeros de nucleótidos,
BASE BIOESTIMULANTE DE COMPLEJO AMINOACIDOS DE CADENAS CORTAS y SUS EFECTOS EN LA NUTRICION CITRICOS
 BASE BIOESTIMULANTE DE COMPLEJO AMINOACIDOS DE CADENAS CORTAS y SUS EFECTOS EN LA NUTRICION CITRICOS Efectos PROTIFERT y PEPTIRAM en mezclacon Cocktail Nutrientes en Citricos Variedad Valenciana bajo presión
BASE BIOESTIMULANTE DE COMPLEJO AMINOACIDOS DE CADENAS CORTAS y SUS EFECTOS EN LA NUTRICION CITRICOS Efectos PROTIFERT y PEPTIRAM en mezclacon Cocktail Nutrientes en Citricos Variedad Valenciana bajo presión
METABOLISMO DE PROTEINAS Y AMINOACIDOS
 sección III, metabolismo de proteínas y aminoácidos. Harper, bioquímica, 28a edición. ALFREDO ABADIA G. RESIDENTE III AÑO MD DE LA ACTIVIDAD FISICA Y EL DEPORTE FUCS-HISJ. METABOLISMO DE PROTEINAS Y AMINOACIDOS
sección III, metabolismo de proteínas y aminoácidos. Harper, bioquímica, 28a edición. ALFREDO ABADIA G. RESIDENTE III AÑO MD DE LA ACTIVIDAD FISICA Y EL DEPORTE FUCS-HISJ. METABOLISMO DE PROTEINAS Y AMINOACIDOS
B1 Estructura de los aminoácidos
 SeciÓn B AMINOÁIDOS Y PROTEÍNAS B1 Estructura de los aminoácidos Notas clave Aminoácidos Enantiómeros Los 20 aminoácidos estándar Ácidos, bases y p Amortiguadores Todas las proteínas están formadas por
SeciÓn B AMINOÁIDOS Y PROTEÍNAS B1 Estructura de los aminoácidos Notas clave Aminoácidos Enantiómeros Los 20 aminoácidos estándar Ácidos, bases y p Amortiguadores Todas las proteínas están formadas por
Las proteínas de la dieta tras ser digeridas proporcionan los aminoácidos que utilizaremos para la síntesis de proteínas endógenas, para:
 1 CONCEPTO Las proteínas son moléculas orgánicas formadas por largas cadenas lineales, no ramificadas, de más de 70 aminoácidos (monómeros o unidades que conforman las proteínas) unidos por enlaces peptídicos.
1 CONCEPTO Las proteínas son moléculas orgánicas formadas por largas cadenas lineales, no ramificadas, de más de 70 aminoácidos (monómeros o unidades que conforman las proteínas) unidos por enlaces peptídicos.
METABOLISMO. Metabolismo de las proteínas
 PRODUCTO ANIMAL Cantidad y Características METABOLISMO PARTICIÓN DIGESTIÓN ABSORCIÓN CÉLULAS NUTRIENTES CONSUMO ALIMENTOS METABOLISMO Secuencia de procesos físicos y químicos que tiene lugar en las células,
PRODUCTO ANIMAL Cantidad y Características METABOLISMO PARTICIÓN DIGESTIÓN ABSORCIÓN CÉLULAS NUTRIENTES CONSUMO ALIMENTOS METABOLISMO Secuencia de procesos físicos y químicos que tiene lugar en las células,
Proteínas. Tabla 1: Funciones de las proteínas
 Colegio Lectura Hispano Complementaria Americano Depto. de Ciencias - Biología Nivel: 4to medio Unidad I Proteínas 1 En las células, son las proteínas las macromoléculas más abundantes y las que constituyen
Colegio Lectura Hispano Complementaria Americano Depto. de Ciencias - Biología Nivel: 4to medio Unidad I Proteínas 1 En las células, son las proteínas las macromoléculas más abundantes y las que constituyen
Proteínas María de la Luz Velázquez Monroy & Miguel Ángel Ordorica Vargas
 Introducción Proteínas María de la Luz Velázquez Monroy & Miguel Ángel rdorica Vargas El nombre Proteína fue propuesto en 1838 por el químico sueco Jons Jakob Berzelius (Figura 1) para designar a las substancias
Introducción Proteínas María de la Luz Velázquez Monroy & Miguel Ángel rdorica Vargas El nombre Proteína fue propuesto en 1838 por el químico sueco Jons Jakob Berzelius (Figura 1) para designar a las substancias
QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Agua (o humedad, si se conoce)*
 QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Entregar el 21 de Mayo. Selecciona un alimento, de preferencia de los que consumes con regularidad, que contenga proteínas. 1. De acuerdo
QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Entregar el 21 de Mayo. Selecciona un alimento, de preferencia de los que consumes con regularidad, que contenga proteínas. 1. De acuerdo
ADN, ARN E INFORMACIÓN
 ADN, ARN E INFORMACIÓN LOS ÁCIDOS NUCLEICOS Los ácidos nucleicos fueron descubiertos en 1869 por Miescher, en el pus de los vendajes de heridas, pero su papel en la herencia y control de la actividad celular
ADN, ARN E INFORMACIÓN LOS ÁCIDOS NUCLEICOS Los ácidos nucleicos fueron descubiertos en 1869 por Miescher, en el pus de los vendajes de heridas, pero su papel en la herencia y control de la actividad celular
Proteínas: Leche y caseína
 Proteínas: Leche y caseína El papel de la leche en la naturaleza es para alimentar y proporcionar una protección inmunológica para los mamíferos jóvenes. La leche ha sido una fuente de alimento para los
Proteínas: Leche y caseína El papel de la leche en la naturaleza es para alimentar y proporcionar una protección inmunológica para los mamíferos jóvenes. La leche ha sido una fuente de alimento para los
Aminoácidos. 7. Sobre la actividad óptica de los aminoácidos es cierto que:
 Aminoácidos 1. La valoración de valina con hidróxido sódico, conduce a la obtención de dos pks. La reacción de valoración que se produce al pk2 de 9,62 es: a) COOH + OH- --> -COO- + H2O. b) COOH + -NH2
Aminoácidos 1. La valoración de valina con hidróxido sódico, conduce a la obtención de dos pks. La reacción de valoración que se produce al pk2 de 9,62 es: a) COOH + OH- --> -COO- + H2O. b) COOH + -NH2
Tema 4c Estructura tridimensional de las proteínas. Proteínas fibrosas. Proteínas globulares.
 Tema 4c Estructura tridimensional de las proteínas. Proteínas fibrosas. Proteínas globulares. Proteínas fibrosas Estructura y función de las queratinas Estructura y función del colágeno Triple hélice de
Tema 4c Estructura tridimensional de las proteínas. Proteínas fibrosas. Proteínas globulares. Proteínas fibrosas Estructura y función de las queratinas Estructura y función del colágeno Triple hélice de
AMINOÁCIDOS. Serie AMINOÁCIDOS
 AMINOÁCIDOS Equisalud, de acuerdo con su filosofía de empresa, dedicada a la promoción de la salud, pretende, con la creación de la Línea HoloMega, ayudar a al correcto funcionamiento del organismo mediante
AMINOÁCIDOS Equisalud, de acuerdo con su filosofía de empresa, dedicada a la promoción de la salud, pretende, con la creación de la Línea HoloMega, ayudar a al correcto funcionamiento del organismo mediante
Biología General y Metodología de las Ciencias 2016 BIOMOLÉCULAS
 BIOMOLÉCULAS Objetivos: Reconocer los distintos niveles de organización de la materia. Diferenciar las propiedades constreñimiento, emergentes y colectivas. Identificar las principales Biomoléculas según
BIOMOLÉCULAS Objetivos: Reconocer los distintos niveles de organización de la materia. Diferenciar las propiedades constreñimiento, emergentes y colectivas. Identificar las principales Biomoléculas según
CÓMO SE PUEDE DETERMINAR LA SECUENCIA DEL DNA A PARTIR DE UNA PROTEÍNA? DR. MANUEL E. AQUINO
 Alianza para el Aprendizaje de Ciencias y Matemáticas CÓMO SE PUEDE DETERMINAR LA SECUENCIA DEL DNA A PARTIR DE UNA PROTEÍNA? DR. MANUEL E. AQUINO GUÍA DEL MAESTRO ESTÁNDARES ATENDIDOS: 1. LA NATURALEZA
Alianza para el Aprendizaje de Ciencias y Matemáticas CÓMO SE PUEDE DETERMINAR LA SECUENCIA DEL DNA A PARTIR DE UNA PROTEÍNA? DR. MANUEL E. AQUINO GUÍA DEL MAESTRO ESTÁNDARES ATENDIDOS: 1. LA NATURALEZA
Cuantificación y análisis químico de proteínas
 Cuantificación y análisis químico de proteínas Enlace peptídico R 1 R 2 Secuencia: AlaGluGlyLys o AEGK Puentes disulfuro COO- COO- COO- NH 2 NH 2 NH 2 Modificaciones Post-traduccionales I Análisis químico
Cuantificación y análisis químico de proteínas Enlace peptídico R 1 R 2 Secuencia: AlaGluGlyLys o AEGK Puentes disulfuro COO- COO- COO- NH 2 NH 2 NH 2 Modificaciones Post-traduccionales I Análisis químico
CATABOLISMO DE AMINOÁCIDOS:
 Tema 14: Catabolismo de aminoácidos. Destino del grupo amino: ciclo de la urea. Reacciones y regulación. Destino del esqueleto carbonado. T 14 Ciclo Urea CATABOLISMO DE AMINOÁCIDOS: El amonio procedente
Tema 14: Catabolismo de aminoácidos. Destino del grupo amino: ciclo de la urea. Reacciones y regulación. Destino del esqueleto carbonado. T 14 Ciclo Urea CATABOLISMO DE AMINOÁCIDOS: El amonio procedente
Tema 9. Química Orgánica
 Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Aminoácidos y Proteínas. Bioquímica Kinesiología UNLAM 2014
 Aminoácidos y Proteínas Bioquímica Kinesiología UNLAM 2014 Proteínas Constituyen las moléculas orgánicas más abundantes de las células (50% del peso seco). Son macromoléculas, formadas por aminoácidos
Aminoácidos y Proteínas Bioquímica Kinesiología UNLAM 2014 Proteínas Constituyen las moléculas orgánicas más abundantes de las células (50% del peso seco). Son macromoléculas, formadas por aminoácidos
5,25g CREATINA MONOHIDRAT
 5,25g CREATINA MONOHIDRAT 1g TAURINA La taurina es un agente anticatabólico, y es un imitador de la insulina. Ayuda al crecimiento de las fibras musculares cuando se une a un entrenamiento de alta intensidad.
5,25g CREATINA MONOHIDRAT 1g TAURINA La taurina es un agente anticatabólico, y es un imitador de la insulina. Ayuda al crecimiento de las fibras musculares cuando se une a un entrenamiento de alta intensidad.
QUÍMICA ORGÁNICA BÁSICA
 QUÍMICA ORGÁNICA BÁSICA 1. INTRODUCCIÓN: NATURALEZA DE LA QUÍMICA ORGÁNICA Panorama histórico y situación actual El carácter químico especial del carbono Fuentes y transformaciones de los compuestos orgánicos.
QUÍMICA ORGÁNICA BÁSICA 1. INTRODUCCIÓN: NATURALEZA DE LA QUÍMICA ORGÁNICA Panorama histórico y situación actual El carácter químico especial del carbono Fuentes y transformaciones de los compuestos orgánicos.
Soluciones de la serie de ejercicios 1 (Curso 7.012)
 Soluciones de la serie de ejercicios 1 (urso 7.01) Pregunta 1 a) uáles son los 4 tipos principales de moléculas biológicas mencionadas en clase? ite una función importante de cada tipo de molécula biológica
Soluciones de la serie de ejercicios 1 (urso 7.01) Pregunta 1 a) uáles son los 4 tipos principales de moléculas biológicas mencionadas en clase? ite una función importante de cada tipo de molécula biológica
7.012 Serie de ejercicios 1
 ombre Grupo 7.01 Serie de ejercicios 1 Pregunta 1 a) uáles son los 4 tipos principales de moléculas biológicas mencionadas en clase? ite una función importante de cada tipo de molécula biológica celular.
ombre Grupo 7.01 Serie de ejercicios 1 Pregunta 1 a) uáles son los 4 tipos principales de moléculas biológicas mencionadas en clase? ite una función importante de cada tipo de molécula biológica celular.
AMINOÁCIDOS Descripción de los Aminoácidos y su función en la planta
 AMINOÁCIDOS Descripción de los Aminoácidos y su función en la planta Informe Técnico 1.Introducción.... 3 Aminoácidos proteicos... 5 Aminoácidos en las plantas... 6 2.Función de los aminoácidos... 6 Alifáticos...
AMINOÁCIDOS Descripción de los Aminoácidos y su función en la planta Informe Técnico 1.Introducción.... 3 Aminoácidos proteicos... 5 Aminoácidos en las plantas... 6 2.Función de los aminoácidos... 6 Alifáticos...
INFORME. Análisis nutricional de la tripa de cordero
 Pedido 54 Promotor: Qualillet S.L.U. INFORME Análisis nutricional de la tripa de cordero A petición de Qualillet S.L.U. (Sant Julià de Vilatorta, Barcelona), se han analizado diferentes parámetros de interés
Pedido 54 Promotor: Qualillet S.L.U. INFORME Análisis nutricional de la tripa de cordero A petición de Qualillet S.L.U. (Sant Julià de Vilatorta, Barcelona), se han analizado diferentes parámetros de interés
METABOLISMO DEL NITRÓGENO
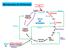 METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS.
 REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS. PRESENTACIÓN Los animales incluyendo al hombre, recibimos pocas moléculas sencillas y una gran cantidad de macromoléculas, como almidones, proteínas
REACCIONES DE POLIMERIZACIÓN DE CARBOHIDRATOS Y AMINOÁCIDOS. PRESENTACIÓN Los animales incluyendo al hombre, recibimos pocas moléculas sencillas y una gran cantidad de macromoléculas, como almidones, proteínas
DOSSIER TECNICO GAMA BIOFERT
 DOSSIER TECNICO GAMA BIOFERT MC Biofert Aminoácidos (Gama) MC Biofert es un bioestimulante natural con un alto porcentaje de aminoácidos libres de rápida asimilación, derivado de la hidrólisis de sustancias
DOSSIER TECNICO GAMA BIOFERT MC Biofert Aminoácidos (Gama) MC Biofert es un bioestimulante natural con un alto porcentaje de aminoácidos libres de rápida asimilación, derivado de la hidrólisis de sustancias
Los nucleótidos están formados por una base nitrogenada, ribosa o desoxirribosa y un grupo fosfato.
 Introducción Los nucleótidos están formados por una base nitrogenada, ribosa o desoxirribosa y un grupo fosfato. Origen de los átomos que componen: Las bases púricas Base Nucleósido Nucleótido monofosfato
Introducción Los nucleótidos están formados por una base nitrogenada, ribosa o desoxirribosa y un grupo fosfato. Origen de los átomos que componen: Las bases púricas Base Nucleósido Nucleótido monofosfato
Aminoácidos. Los aminoácidos se agrupan en la figura según las propiedades de sus cadenas
 Aminoácidos Es esencial tener un conocimiento básico acerca de la química de las proteínas, para entender la nutrición y otros conceptos del metabolismo. Las proteínas se componen de carbono, hidrógeno,
Aminoácidos Es esencial tener un conocimiento básico acerca de la química de las proteínas, para entender la nutrición y otros conceptos del metabolismo. Las proteínas se componen de carbono, hidrógeno,
Por. Harvey Arjona D., I.A., Ph.D.
 Los Aminoácidos en la Agricultura Moderna Por Harvey Arjona D., I.A., Ph.D. CONTENIDO 1. Generalidades 2. Clasificación de a.a. 3. Metabolismo de los a.a. 4. Absorción de a.a. exógenos 5. Obtención industrial
Los Aminoácidos en la Agricultura Moderna Por Harvey Arjona D., I.A., Ph.D. CONTENIDO 1. Generalidades 2. Clasificación de a.a. 3. Metabolismo de los a.a. 4. Absorción de a.a. exógenos 5. Obtención industrial
F FA AC C U ULTAD LTAD D D E
 FACULTAD DE QUÍMICA 4.1 Adición electrofílica a enlaces múltiples C-C 4.2 Adición de radicales libres a enlaces múltiples C-C 4.3 Adición nucleofílica a enlaces múltiples C-C 4.4 Adición nucleofílica a
FACULTAD DE QUÍMICA 4.1 Adición electrofílica a enlaces múltiples C-C 4.2 Adición de radicales libres a enlaces múltiples C-C 4.3 Adición nucleofílica a enlaces múltiples C-C 4.4 Adición nucleofílica a
Proteínas fibrosas. Alfa Queratinas Beta-Queratinas Fibroína Colágeno Elastina
 Proteínas Fibrosas La mayor parte o casi toda la proteína está organizada de manera paralela a un sólo eje Las proteínas fibrosas son generalmente fuertes mecánicamente Son generalmente insolubles Generalmente
Proteínas Fibrosas La mayor parte o casi toda la proteína está organizada de manera paralela a un sólo eje Las proteínas fibrosas son generalmente fuertes mecánicamente Son generalmente insolubles Generalmente
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR
 INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - Componentes químicos de la célula - Un poco de química 1 Un poco de química El 99% del peso de una célula corresponde a C, H, N y O. La sustancia más abundante
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - Componentes químicos de la célula - Un poco de química 1 Un poco de química El 99% del peso de una célula corresponde a C, H, N y O. La sustancia más abundante
Clave Genética y Síntesis de Proteínas
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Clave Genética y Síntesis de Proteínas Dr. Mynor A. Leiva Enríquez
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Clave Genética y Síntesis de Proteínas Dr. Mynor A. Leiva Enríquez
Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno
 Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno Tema 3 Proteínas Fibrosas y Proteínas Globulares Fibrosas Globulares Forma alargada Unidades repetidas de un solo tipo de estructura secundaria
Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno Tema 3 Proteínas Fibrosas y Proteínas Globulares Fibrosas Globulares Forma alargada Unidades repetidas de un solo tipo de estructura secundaria
cadena lateral Un -aminoácido una sección corta de una proteína glicina aminoácidos individuales
 carbono grupo -amino cadena lateral Un -aminoácido enlaces peptídicos una sección corta de una proteína alanina serina glicina aminoácidos individuales cisteína valina AMINÁCIDS Los aminoácidos son cadenas
carbono grupo -amino cadena lateral Un -aminoácido enlaces peptídicos una sección corta de una proteína alanina serina glicina aminoácidos individuales cisteína valina AMINÁCIDS Los aminoácidos son cadenas
Metabolismo de aminoácidos
 Metabolismo de aminoácidos El nitrógeno, presente en la biosfera como nitrato (N 3- ) o dinitrógeno (N 2 ), debe ser reducido a amonio (NH 4+ ) para su incorporación a proteínas. El hombre adquiere el
Metabolismo de aminoácidos El nitrógeno, presente en la biosfera como nitrato (N 3- ) o dinitrógeno (N 2 ), debe ser reducido a amonio (NH 4+ ) para su incorporación a proteínas. El hombre adquiere el
Tema 5: aminoácidos y proteínas
 1. Los aminoácidos 2. Propiedades de los aminoácidos 3. El enlace peptídico 4. Estructuras 1 aria y 2 aria de las proteínas 5. Estructuras 3 aria y 4 aria de las proteínas 6. Propiedades de las proteínas
1. Los aminoácidos 2. Propiedades de los aminoácidos 3. El enlace peptídico 4. Estructuras 1 aria y 2 aria de las proteínas 5. Estructuras 3 aria y 4 aria de las proteínas 6. Propiedades de las proteínas
Biomoléculas orgánicas: Carbohidratos y Lípidos. Propiedad Intelectual Cpech
 Biología Biomoléculas orgánicas: Carbohidratos y Lípidos Repaso Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan
Biología Biomoléculas orgánicas: Carbohidratos y Lípidos Repaso Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan
- Las proteínas son esenciales para la formación y el mantenimiento de los tejidos corporales.
 TEMA 6. PROTEÍNAS - Las proteínas son esenciales para la formación y el mantenimiento de los tejidos corporales. - Los aa son los elementos estructurales de las proteínas. Las proteínas de plantas y animales
TEMA 6. PROTEÍNAS - Las proteínas son esenciales para la formación y el mantenimiento de los tejidos corporales. - Los aa son los elementos estructurales de las proteínas. Las proteínas de plantas y animales
EXPERIMENTO 2 METODOS CUANTITATIVOS PARA LA IDENTIFICACION DE AMINOACIDOS Y PROTEINAS
 EXPEIMENT 2 METDS UANTITATIVS PAA LA IDENTIFIAIN DE AMINAIDS Y PTEINAS EQUISITS epasar las estructuras de los 20 L-α aminoácidos (AA), que forman las proteínas y las características de las proteínas. BJETIVS
EXPEIMENT 2 METDS UANTITATIVS PAA LA IDENTIFIAIN DE AMINAIDS Y PTEINAS EQUISITS epasar las estructuras de los 20 L-α aminoácidos (AA), que forman las proteínas y las características de las proteínas. BJETIVS
Tema 12. Química de los aminoácidos y péptidos
 Tema 12 Química de los aminoácidos y péptidos Estructura Átomo de carbono α Grupo amino α Un α-aminoácido Enlaces peptídicos Cadena lateral Una parte de un péptido Alanina Serina Glicina Cisteina Valina
Tema 12 Química de los aminoácidos y péptidos Estructura Átomo de carbono α Grupo amino α Un α-aminoácido Enlaces peptídicos Cadena lateral Una parte de un péptido Alanina Serina Glicina Cisteina Valina
CONCEPTO MOLECULAR DEL GEN. ESTRUCTURA DE LOS GENES EN EUCARIOTAS
 4) RSRIPIÓN Y RDIÓN DE L INFORMIÓN ENÉI ONEPO MOLELR DEL EN. ESRR DE LOS ENES EN ERIOS oncepto molecular de gen: La mayoría de los genes son fragmentos de la molécula de DN que determinan la síntesis de
4) RSRIPIÓN Y RDIÓN DE L INFORMIÓN ENÉI ONEPO MOLELR DEL EN. ESRR DE LOS ENES EN ERIOS oncepto molecular de gen: La mayoría de los genes son fragmentos de la molécula de DN que determinan la síntesis de
QUÍMICA. 2º Bachilerrato orgánica Estereoisomería:
 TEMA 10: QUÍMICA ORÁNICA. 1.- Isomerías. En química orgánica es usual encontrar compuestos químicos diferentes que poseen igual fórmula molecular. Estos compuestos se denominan isómeros. 1.1. Isómeros
TEMA 10: QUÍMICA ORÁNICA. 1.- Isomerías. En química orgánica es usual encontrar compuestos químicos diferentes que poseen igual fórmula molecular. Estos compuestos se denominan isómeros. 1.1. Isómeros
Proteínas fibrosas. α-queratinas
 Hélices α entrecruzadas por puentes disulfuro Proteínas fibrosas α-queratinas Estructura Características Localización Estructuras resistentes e insolubles de dureza y flexibilidad variables Estructura
Hélices α entrecruzadas por puentes disulfuro Proteínas fibrosas α-queratinas Estructura Características Localización Estructuras resistentes e insolubles de dureza y flexibilidad variables Estructura
Profesor(a): C.D. María Isabel Pérez Aguilar
 Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
Departamento de Química Física Facultad de Ciencias
 Interacciones electrostáticas. Interacciones electrostáticas. Los fenómenos de interacción con el disolvente y cosolventes. Interacciones electrostáticas. El origen de las cargas en proteínas. Fuentes
Interacciones electrostáticas. Interacciones electrostáticas. Los fenómenos de interacción con el disolvente y cosolventes. Interacciones electrostáticas. El origen de las cargas en proteínas. Fuentes
Metabolismo de aminoácidos
 Metabolismo de aminoácidos El nitrógeno, presente en la biosfera como nitrato (NO 3- ) o dinitrógeno (N 2 ), debe ser reducido a amonio (NH 4+ ) para su incorporación a proteínas. El hombre adquiere el
Metabolismo de aminoácidos El nitrógeno, presente en la biosfera como nitrato (NO 3- ) o dinitrógeno (N 2 ), debe ser reducido a amonio (NH 4+ ) para su incorporación a proteínas. El hombre adquiere el
I) Biomoléculas 6) Proteínas I-6 PROTEÍNAS
 I-6 PROTEÍNAS CONCEPTO Y CARACTERÍSTICAS Concepto: Se pueden definir como polímeros formados por la unión, mediante enlaces peptídicos, de unidades de menor masa molecular llamadas aminoácidos. Son moléculas
I-6 PROTEÍNAS CONCEPTO Y CARACTERÍSTICAS Concepto: Se pueden definir como polímeros formados por la unión, mediante enlaces peptídicos, de unidades de menor masa molecular llamadas aminoácidos. Son moléculas
Metabolismo de AMINOÁCIDOS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,012 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,012 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
Estructura tridimensional de proteínas
 Estructura tridimensional de proteínas 1. En solución acuosa, la conformación proteica esta determinada por dos factores prioritarios. Uno es la formación de un número máximo de enlaces de hidrógeno. El
Estructura tridimensional de proteínas 1. En solución acuosa, la conformación proteica esta determinada por dos factores prioritarios. Uno es la formación de un número máximo de enlaces de hidrógeno. El
4. QUÍMICA DEL CARBONO.
 4. QUÍMICA DEL CARBONO. 4.1. FÓRMULA QUÍMICA. El número atómico del carbono es seis, contiene en su núcleo seis protones mientras seis electrones se distribuyen en orbitales a su alrededor. Su configuración
4. QUÍMICA DEL CARBONO. 4.1. FÓRMULA QUÍMICA. El número atómico del carbono es seis, contiene en su núcleo seis protones mientras seis electrones se distribuyen en orbitales a su alrededor. Su configuración
Clasificación de los AA en familias, según su biosíntesis
 Tema 15: : Aspectos generales de la biosíntesis de aminoácidos. Fijación n del nitrógeno a cadenas carbonadas. Algunos ejemplos de interés s biológico. T 15 síntesis AA Los AA se clasifican en esenciales
Tema 15: : Aspectos generales de la biosíntesis de aminoácidos. Fijación n del nitrógeno a cadenas carbonadas. Algunos ejemplos de interés s biológico. T 15 síntesis AA Los AA se clasifican en esenciales
Concepto de Lípido. Es un grupo de sustancias muy heterogéneas que sólo tienen en común estas dos características:
 Lípidos Sesión 01 Concepto de Lípido Los lípidos son biomoléculas orgánicas formadas básicamente por carbono e hidrógeno y generalmente también oxígeno; pero en porcentajes mucho más bajos. Además pueden
Lípidos Sesión 01 Concepto de Lípido Los lípidos son biomoléculas orgánicas formadas básicamente por carbono e hidrógeno y generalmente también oxígeno; pero en porcentajes mucho más bajos. Además pueden
Diferencias en la Respuesta Zootécnica entre lo formulado y lo esperado a Campo??
 Diferencias en la Respuesta Zootécnica entre lo formulado y lo esperado a Campo?? Viernes 13 de Junio 2014 - Grupo de Trabajo Avícola Ing. Agr. Marcelo Cáceres Sumario 1 Modelos de Simulacion 2 Energia
Diferencias en la Respuesta Zootécnica entre lo formulado y lo esperado a Campo?? Viernes 13 de Junio 2014 - Grupo de Trabajo Avícola Ing. Agr. Marcelo Cáceres Sumario 1 Modelos de Simulacion 2 Energia
