Vinflunina Informe de la Comisión de Farmacia y Terapéutica Hospital Universitario Reina Sofía
|
|
|
- Santiago Acosta Torres
- hace 6 años
- Vistas:
Transcripción
1 Vinflunina Informe de la Comisión de Farmacia y Terapéutica Hospital Universitario Reina Sofía 1.- Identificación del fármaco Fármaco: Vinflunina Nombre comercial: Javlor Presentaciones: E/1 vial 25mg/ml, 2 ml y 10 ml Laboratorio: Pierre Fabré Precio adquisición: PVL+IVA= 942,15 (vial 10ml). Grupo Terapéutico: L01CA05: Alcaloides de la vinca y análogos 2.- Solicitud: Dra. María José Méndez Vidal 3.- Resumen de la justificación de la solicitud y del informe de evaluación Resumen de la justificación de la solicitud: Este nuevo fármaco se ha solicitado para constituir una segunda línea de tratamiento en aquellos pacientes que progresen al tratamiento de primera línea basado en platino. Se han estudiado múltiples agentes (tanto tradicionales como nuevos agentes diana) en monoterapia sin que ninguno haya demostrado suficientes datos de actividad para generar un ensayo fase III. Asimismo se han desarrollado varios ensayos (la mayoría en fase II con pequeño número de pacientes) con dobletes de quimioterapia, demostrando una mayor tasa de respuestas con respecto a la monoterapia aunque sin un claro beneficio en la supervivencia. Vinflunina ha mostrado una respuesta significativa aportando un beneficio en supervivencia: aumento de la supervivencia global de 2.6 meses, aumento supervivencia libre de progresión de 1.5 meses, incremento en el control de la enfermedad y en la calidad de vida. Además la toxicidad reportada en todos los estudios es manejable, reversible y no acumulativa. No es nefrotóxica, por lo que se puede administrar de forma segura en pacientes con insuficiencia renal. Otra ventaja, sería la administración cada tres semanas, sin necesidad de una premedicación compleja y en un tiempo rápido (15-20 minutos) hace de la vinflunina un fármaco cómodo de administrar. El abordaje terapéutico para estos pacientes quedaría en: 1ª línea: Gemcitabina + CDDP (con retratamiento si progresa en un tiempo superior a 6 meses.). 2ª línea: -Entrar en ensayo clínico -Tratamiento con taxanos -Vinflunina cuando no se pueda emplear alguno de los anteriores Se estima en alrededor de 6, el número de pacientes al año, que podrían ser candidatos a la terapia con vinflunina siguiendo la propuesta de tratamiento descrita Resumen del informe: El carcinoma de células transicionales del tracto urotelial se trata habitualmente con esquemas que incluyen derivados de platino (Ej: gemcitabina+cddp, paclitaxel+carboplatino), tras progresión a estos esquemas en menos de 6 meses, actualmente se emplean alternativas como gemcitabina, docetaxel, o diversas combinaciones de agentes. Vinflunina es un nuevo fármaco con indicación registrada en segunda línea tras los resultados de un ensayo clínico en fase III llevado a cabo en pacientes con buen estado funcional y comparado con placebo (mejor tratamiento de soporte). Los resultados son considerados como modestos por la sociedad europea de oncología médica y el grupo de asesores científicos de la agencia europea del medicamento modestos, ya que no presenta mejora en supervivencia en el análisis por intención de tratar, que sólo se consigue al aplicar un análisis multivariante de los principales factores pronósticos implicados, y en cualquier caso no alcanza los 3 meses de mejora de supervivencia ni tampoco mejora la
2 calidad de vida. Además se discute que hubiese sido preciso emplear un comparador activo y también que los pacientes incluidos presentaban un estado bastante bueno. Todo esto le resta validez externa e interna al ensayo. El NICE ya ha emitido un informe desfavorable a su empleo en segunda línea. En consecuencia la Comisión de Farmacia acuerda incluir Vinflunina siempre en pacientes con un ECOG 0-1como: - 3ª línea de tratamiento. - También considera favorable su empleo en 2ª línea, donde estaría limitado a: - pacientes con imposibilidad de uso de CDDP+Gemcitabina en primera línea (en este caso la tercera línea quedaría como segunda) - desarrollo de neuropatía periférica a platino que imposibilitaría el uso de taxanos en segunda y donde la alternativa de gemcitabina en monoterapia no sea posible por una progresión a la primera línea rápida (progresión en <6 meses) - Será necesario presentar un informe de los pacientes seleccionados para tratamiento así como un informe de resultados 4.- Farmacología Indicaciones clínicas formalmente aprobadas. EMEA (21/09/09) y AEMyPS (2/12/09): en monoterapia para el tratamiento de pacientes adultos con carcinoma avanzado o metastásico de células transicionales del tracto urotelial en los que haya fracasado un tratamiento previo que incluyera derivados del platino. No se ha estudiado la eficacia y la seguridad de vinflunina en pacientes con estadio funcional 2. FDA: no evaluado Mecanismo de acción. La vinflunina es un análogo de los alcaloides de la vinca, con actividad antitumoral debido a su capacidad para unirse a la tubulina, componente fundamental de los microtúbulos celulares. Impide la formación de microtúbulos y favorece la disolución de los ya existentes, deteniendo la mitosis celular en la metafase, y estimulando la apoptosis. Posología La posología recomendada es de 320 mg/m2 de vinflunina, administrados en forma de perfusión intravenosa de 20 minutos de duración cada 3 semanas. En pacientes con estadio funcional de la OMS/ECOG igual a 1 o PS igual a 0 e irradiación pélvica previa, el tratamiento debe iniciarse a la dosis de 280 mg/m2. En ausencia de cualquier toxicidad hematológica durante el primer ciclo que pueda ocasionar retrasos en el tratamiento o reducción de dosis, se aumentará la dosis hasta un máximo de 320 mg/m2 administrados cada 3 semanas en los ciclos posteriores.
3 En pacientes con RAN < 1.000/mm3 o plaquetas < /mm3 en el día de la administración, el tratamiento deberá retrasarse hasta la recuperación de las cifras (RAN 1.000/mm3 y plaquetas /mm3). Si no se produce la recuperación en el plazo de 2 semanas, deberá interrumpirse el tratamiento definitivamente. En caso de neutropenia de Grado 4 (RAN < 500/mm3) que persista durante más de 7 días o neutropenia febril, se recomienda ajustar la dosis (ver la tabla anterior). Si en el día de la perfusión se aprecia una toxicidad en órganos de Grado 2, el tratamiento debe retrasarse hasta alcanzar los Grados 0, 1 ó volver al valor basal inicial. Forma de preparación La dosis calculada de vinflunina debe mezclarse en una bolsa de 100 ml de solución para perfusión de suero fisiológico. También puede utilizarse solución para perfusión de glucosa 5%. La solución diluida debe protegerse de la luz hasta su administración. Administración La solución una vez preparada sólo puede ser administrada por vía intravenosa. Debe de administrarse en perfusión intravenosa de 20 minutos. Pueden usarse tanto vías periféricas como un catéter central. Farmacocinética Distribución: se une de forma moderada a proteínas plasmáticas (67,2±1,1%). Se distribuye ampliamente a los tejidos (volumen de distribución aproximadamente 35l/kg). Metabolismo: todos los metabolitos identificados son producidos por el isoenzima CYP3A4 del citocromo, excepto en el caso de 4-O-desacetilvinflunina (DVFL), el único metabolito activo y principal metabolito en la sangre el cual se produce tras la acción de múltiples esterasas. Eliminación: se elimina siguiendo una disminución de la concentración multiexponencial, con una semivida Terminal carcana a 40 horas. DVFL se forma lentamente y se elimina más lentamente que vinflunina (t1/2 aproximada 120 h). 5.- Eficacia Ensayos clínicos disponibles para la indicación clínica evaluada Tabla 1. Ref:Bellmunt J et al J Clin Oncol Nº de pacientes:370 -Diseño: Fase III, aleatorizado 2:1, multinacional -Tratamiento grupo activo: vinflunina 320 mg/m 2 cada 21 días + MTS. Tras los primeros 10 pacientes y debido a la toxicidad hematológica se modificó: si ECOG PS = 0 y no irradiación pélvica previa recibieron la dosis establecida. Si ECOG PS =1 o ECOG PS =0 pero con irradiación pélvica previa vinflunina 280 mg/m 2 + MTS el primer ciclo y después escalar dosis hasta 320 mg/m 2 si no toxicidad. (n=253). Los pacientes con toxicidad hematológica que produjera retraso del tratamiento recibieron dosis de 280 mg/m 2 sin escalada de dosis + MTS. Duración: hasta progresión, toxicidad inaceptable, enfermedad intercurrente. Las lesiones se evaluaron cada 42 días. El periodo de seguimiento fueron 30 días después de la última dosis de tratamiento. -Tratamiento grupo control: MTS (radioterapia paliativa, antibióticos, analgésicos, corticoides y transfusión) (n=117). El tratamiento se discontinuó después de completar las 18 semanas contando desde la aleatorización, por recibir un antineoplásico debido a progresión de la enfermedad, por requerimiento del paciente o por imposibilidad del paciente de acudir a la visita cada 3 semanas. -Criterios de inclusión: pacientes 18 años con CUCT localmente avanzado o metastático confirmado histológicamente, con progresión después de tratamiento de 1ª línea con QT conteniendo cisplatino; ECOG PS 0 ó 1. Se permitió radiación previa si afectaba menos del 30% de la médula ósea y había finalizado 30 días antes de la aleatorización con recuperación completa de la toxicidad. Función hepática, hematológica y renal (aclaración creatinina 40 ml/min con la fórmula de Cockcroft-Gault) adecuadas. - Criterios de exclusión: carcinoma del tracto urotelial de células no transicionales, metástasis cerebrales, arritmias cardíacas no controladas, diabetes mellitus, hipercalcemia >2,9 mmol/l, IC clase III-IV NYHA, IM. angina inestable 6 meses antes, QT adyuvante o neoadyuvante, haber recibido más de un régimen de QT sistémica previa para enfermedad metastásica, otras neoplasias. -Tipo de análisis: ITT (pacientes aleatorizados que recibieron tratamiento o no); PP: pacientes elegibles y tratados en el brazo asignado por aleatorización. La población elegible se definió como aquellos sin violaciones importantes
4 de los criterios de inclusión y exclusión. Se excluyeron 13 pacientes (4 en el grupo con VFL +MTS y 9 en el de MTS). Evaluables para respuesta: pacientes elegibles, evaluables y tratados en la rama asignada en la aleatorización. Para ser evaluables tenían que haber recibido un mínimo de 2 ciclos /42 días. Evaluables para seguridad: todos los pacientes tratados en la rama de tratamiento que recibieron. Evaluación calidad de vida: pacientes que completaron (más de 2/3 de las preguntas) el cuestionario en los 14 días antes de la aleatorización y al menos un cuestionario durante el período de estudio al menos 21 después del inicio del tratamiento en estudio o de la primera visita para pacientes en el grupo con MTS. Resultados Variable evaluada en el estudio Resultado principal -SG (pacientes aleatorizados) (mediana; meses) - supervivencia global (población elegible) - supervivencia global (población PP) Resultados secundarios de interés - PLE (pacientes aleatorizados) Resultados por subgrupos -SG en pacientes con cisplatino previo (población elegible) - SG en pacientes sin cisplatino previo (población elegible) - SLE en pacientes con cisplatino previo (población elegible) - SLE en pacientes sin cisplatino previo (población elegible) VFL + MTS N =253 6,9 6,9 6,9 3,0 6,9 6,0 2,9 3,3 MTS N = 117 4,6 4,3 4,3 1,5 4,6 3,4 1,5 1,8 Reducc. riesgo de muerte 12% 22% 25% HR (IC 95%) 0,88 (0,69 a 1,12) 0,78 (0,61 a 0,99) 0,75 (0,59 a 0,96) 0,68 (0,54 a 0,86) 0,80 (0,60 a 1,06) 0,64 (0,40 a 1,03) 0,64 (0,48 a 0,85) 0,55 (0,34 a 0,89) P 0,287 0,040 0,019 0,0012 0,126 0,082 0,004 0,0129 Se observa que no existe diferencia estadísticamente significativa en cuanto a la supervivencia global en la población por ITT, que es análisis que debe realizarse al tratarse de un estudio de superioridad. Esto motivó que la EMA considerase que no se había demostrado efecto sobre la supervivencia. Como consecuencia, el promotor aporta los resultados de un análisis multivariante con los principales factores pronósticos encontrados (ECOG principalmente, pero también valores de Hb y presencia de metástasis hepática) ajustándolos a los datos poblacionales de cada brazo. Con este análisis se encontró un efecto estadísticamente significativo (p<0.05) en términos de supervivencia global en los tres análisis de población: ITT HR 0,77 (IC 95% 0,61 a 0,98), población elegible HR 0,78 (IC 95% 0,61 a 0,99) y PP. Esto motivó que la agencia considerase que cumplían con el requisito mínimo para su aprobación. No obstante, el grupo científico asesor en oncología de la EMA considera que los resultados son sólo modestos, indicando que habría que intentar encontrar subgrupos de población donde se encuentre el mayor efecto. Hasta la fecha esto no ha sido posible. En nuestra opinión, también se ha de tener en cuenta que el grupo comparador de este ensayo no es el adecuado puesto que a pesar de que no existan segundas líneas de tratamiento aprobadas para esta indicación, en estos pacientes se emplean otros esquemas que pueden ser monoterapia o terapia combinada.
5 Existen diferentes estudios (no ensayos clínicos controlados) publicados con los siguientes resultados:
6 Evaluación de las fuentes secundarias: NICE: no recomienda vinflunina para el tratamiento del carcinoma de células transicionales del tracto urotelial metastásico o avanzado que haya progresado tras tratamiento con quimioterapia basada en platino. Por un lado considera que las características de los pacientes incluidos diferían de los de la práctica habitual al ser más jóvenes, con mejor estado funcional y mejor función renal que se encuentran en la práctica clínica diaria. Considera también que el comparador debía haber sido uno de los fármacos utilizados actualmente en segunda línea de los que se benefician los pacientes. No considera el resultado obtenido una vez que se excluyen a los 13 pacientes, ni encuentra favorable la relevancia clínica de los resultados al no demostrar mejora en la calidad de vida de los pacientes. En cuanto a la seguridad del fármaco, el Comité comentó que había preocupación entre los clínicos consultados por la tolerabilidad del mismo. La conclusión final fue que vinflunina no presenta un balance costo efectivo favorable. Señalan un posible papel como tratamiento de tercera línea. Ni las guías canadienses ni las americanas hacen mención a vinflunina, de desarrollo europeo. El NCCN, plantea como alternativas en segunda línea tras progresión a platino, la inclusión en ensayos clínicos o el empleo de agentes únicos cono bleomicina, docetaxel, doxorubicina, 5-fluorouracilo, gemcitabina, ifosfamida, paclitaxel, metotrexato o vinblastina. La ESMO ha aprobado vinflunina como 2ª línea de tratamiento, aunque reconoce que no está claro si otros agentes utilizados podrían conseguir el mismo beneficio. Propuesta de posicionamiento Como consecuencia de la evidencia de uso de las alternativas disponibles se propone emplear vinflunina según el siguiente protocolo: - Como primera línea se emplearía el esquema basado en gemcitabina + CDDP. - En caso de que el paciente progrese en un período superior a 6 meses se retomaría el mismo esquema de tratamiento empleado en primera línea. - Si el paciente progresa a la primera línea en un período inferior a 6 meses, como alternativas en la segunda línea de tratamiento tendríamos: 1. La inclusión del paciente en un ensayo clínico. 2. Utilización de un taxano (docetaxel, paclitaxel,cabazitaxel). 3. Utilización de gemcitabina en monoterapia, en pacientes con una buena respuesta al esquema de primera línea, pero por toxicidad al CDDP, no es posible la administración de este fármaco. 4. Utilización de vinflunina: (con un PS= 0-1) -en caso de imposibilidad de uso de la primera línea por comorbilidades que la contraindiquen -en caso de neuropatía previa a platino (impide taxano) e imposibilidad de uso de gemcitabina en monoterapia por mostrar poca sensibilidad a la primera línea - Como tratamiento de tercera línea se propone la utilización de vinflunina en pacientes con ECOG Seguridad En los estudios realizados hasta la comercialización, un total de pacientes se han expuesto en un total de ciclos a VFL como agente único tanto en pacientes con CUCT (n=450) como en pacientes con tumores no CUCT. Los análisis de seguridad incluyen todos los pacientes que recibieron al menos una dosis del fármaco. Se administraron ciclos en el grupo con 320 mg/m 2 con una mediana de ciclos de 4 (1-21). La mediana de ciclos con la dosis de 280 mg/m 2 fue de 2 (1-20). Las principales toxicidades de VFL son neutropenia, anemia, constipación y astenia/fatiga. Todos estos efectos adversos se consideran efectos de clase de los alcaloides de la vinca. El perfil de seguridad de VFL es similar tanto en población con CCUT como en población con otros tumores, excepto para constipación, infección con neutropenia grave, estomatitis/mucositis y neutropenia febril. El efecto adverso con resultado de muerte más frecuente fue el embolismo pulmonar. Las muertes no se consideraron relacionadas con el fármaco en estudio.
7 Referencia: Ref:Bellmunt J et al J Clin Oncol Resultados de seguridad Variable de VFL + MTS* seguridad evaluada (N=253) en el estudio Incidencia global N (%) -Fatiga/astenia -Náuseas - Vómitos - stomatitis/mucositis -Dolor abdominal -Constipación - Mialgia - Neuropatía - Alopecia - Reacción local - Anemia - Neutropenia - Trombocitopenia - Neutropenia febril 124 (50%) 97 (39,1%) 72 (29,0%) 71 (28,6%) 39 (15,7%) 118 (47,6%) 40 (16,1%) 30 (12,1%) 72 (29,0%) 68 (27,4%) 229 (93,1%) 190 (77,2%) 126 (51,2%) 15 (6,0%) Grado 3 o 4 N (%) 48 (19,3%) 6 (2,4%) 7 (2,8%) 4 (1,6%) 10 (4,0%) 40 (16,1%) 8 (3,2%) 3 (1,2%) 1 (0,4%) 47 (19,1%) 123 (50,0%) 14 (5,7%) 15 (6,0%) MTS (N=117) Incidencia global N (%) 71 (60,7%) 25 (21,4%) 17 (14,5%) 2 (1,7%) 21 (17,9%) 29 (24,8%) 8 6,8%) 13 11,1%) 2 (1,7%) 68 (61,3%) 3 (2,7%) 18 (16,2%) Grado 3 o 4 N (%) 21(17,9%) 1 (0,9%) 7 (6,0%) 1 (0,9%) 9 (8,1%) 1 (0,9%) 1 (0,9%) * un fallecimiento por pancitopenia relacionada con el fármaco Culine S et al La toxicidad hematológica más importante fue la neutropenia grado 3-4, observada en el 67 % de los pacientes; cinco pacientes (10 %) presentaron neutropenia febril, dos de los cuales fueron exitus. El estreñimiento fue frecuente pero fácilmente manejable y sólo en el 8% de los pacientes fue de grado 3-4. La incidencia de nauseas y vómitos (4% y 6% respectivamente) fue baja. No se observó neuropatía sensorial ni irritación venosa seria ni daño de la función renal grado 3-4. Vaughn DJ et al La mielosupresión fue el efecto adverso más frecuente; un 58 % de los pacientes experimentaron neutropenia grado 3-4; la neutropenia febril ocurrió en 10 (7%) pacientes; Otros efectos fueron, estreñimiento (17%), astenia/fatiga (13%), ileo (5%) y dolor abdominal (5%). Un 15% de los pacientes tuvieron que dejar el tratamiento por toxicidad. 7.- Coste Coste tratamiento / día y coste del tratamiento completo. Comparación de costes del tratamiento evaluado frente a otra/s alternativa/s Indicación: MEDICAMENTO Segunda línea de tratamiento en carcinoma de células transicionales del tracto urotelial. Gemcitabina 1000mg/m2 (D1,D8,D15 c/28d) Paclitaxel 200mg/m2 (C/21D) Vinflunina 320mg/m2 c/21d Precio unitario (PVL+ IVA) vial de 1G vial 300mg vial 250mg. Posología (S.C=1.8m2). 1000mg/m2 200mg/m2 (c/21d) 280mg/m2 c/21d (D1,D8,D15 c/28d) Coste ciclo Coste tratamiento completo (o tratamiento/año) Coste incremental respecto a la terapia de referencia (aprox) No se han localizado estudios de coste-efectividad. En la evaluación del NICE se incluye el estudio económico presentado por el laboratorio fabricante. Los resultados se presentan como ratios coste-efectividad incremental (coste por año de vida ganado ajustado por calidad AVAC-). En esta evaluación se cuestionó el estudio realizado por el fabricante, según éste, la
8 ratio CEI para vinflunina+mts vs MTS fue de por AVAC (coste incremental de y beneficio incremental de 0,131 AVAC). El comité tras realizar una serie de análisis de sensibilidad y considerar la falta de robustez del estudio presentado llega a la conclusión de que la ratio CEI puede ser > por AVAC, y puede incrementarse más por el coste de efectos adversos y la modelización de los datos de supervivencia. 8.- Conclusiones Vinflunina ha sido aprobado por la EMA como 2ª línea de tratamiento en el cáncer de vejiga avanzado, tras los resultados estadísticos obtenidos en el análisis multivariante del ensayo clínico en fase 3, donde inicialmente no se conseguían diferencias estadísticamente significativas en eficacia. Este análisis señala que el estado del paciente es el principal factor pronóstico en la respuesta. En cualquier caso no se mejora la calidad de vida de los pacientes con vinflunina. A pesar de no existir tratamientos aprobados en segunda línea, existen numerosos estudios con distintos tratamientos ya conocidos en monoterapia o terapia combinada con buenos resultados, aunque no son ensayos clínicos ni estudios comparativos. La evaluación es del NICE es desfavorable por estos aspectos, además de incorporar una evaluación coste eficacia negativa. La Guía de la ESMO admiten que aunque está indicado en segunda línea no está claro que sea superior a las alternativas empleadas actualmente En consecuencia Vinflunina podría emplearse en segunda línea en pacientes con ECOG 0-1 en caso de imposibilidad de uso de la primera línea por comorbilidades que la contraindiquen, o en caso de neuropatía previa a platino (impide taxano) e imposibilidad de uso de gemcitabina en monoterapia por mostrar poca sensibilidad a la primera línea. Como tratamiento de tercera línea se propone la utilización de vinflunina (siempre con PS=0-1) 9.- Bibliografía 1. Ficha técnica Javlor. Product information 2. Informe EPAR. Public Assessment Report 3. Vinflunina en monoterapia en carcinoma de células transicionales del tracto urotelial tras fracaso a tratamiento previo que incluya derivados de platino. Informe para la Comisión de Farmacia y Terapéutica del Hospital Sant Pau. 28/04/ Bellmunt J, Théodore C, Demkov T, Komyakov B, Sengelov L, Daugaard G et al. Phase III Trial of Vinflunine Plus Best Supportive Care Compared UIT Best Supportive Care Alone Alter a Platinum-Containing Regimen in Patients With Advanced Transitional Cell Carcinoma of the Urothelial Tract. Journal of Clinical Oncology 2009; 5. Culine S, Théodore, De Santis M, Bui B, Demkov T, Lorenz J et al. A phase II study of vinflunine in bladder cancer patients progressing after first-line platinum-containing regimen. British Jourbnal of Cancer 2006; 94: Vaughn D, Srinivas S, Stadler WM, Pili R, Petrylak D, Sternberg CN et al. Vinflunine in Platinum-Pretreated Patients With Locally Advanced or Metastatic Urothelial Carcinoma. Cancer 2009; 115: Yafi FA, North S, Kassouf W. First-and second-line therapy for metastatic urothelial carcinoma of the bladder. Current Oncology 2011; 18: e25-e National Institute for Health and Clinical Excellence (NICE). Vinflunine for the secondline chemotherapy of advanced or metastatic transitional cell carcinoma of the urothelial tract. 19 de noviembre de Disponible en: 9. NCCN Guidelines: bladder cancer. Versión Citado el 2 de diciembre de Disponible en: Bellmunt J, Albiol S, Kataja V. Invasive bladder cancer: ESMO Clinical recommendations for diagnosis, treatment and follow-up. Ann Oncol. 2009; 20 (supp 4): v79 v Bellmunt J, Orsola A, Maldonado X & Kataja V, On behalf of the ESMO Guidelines Working Group. Bladder cancer: ESMO Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2010; 21 (suppl 5): v134-v136.
VINFLUNINA DITARTRATO (JAVLOR / PIERRE FABRE IBERICA, S.A.)
 Presentación CN 663707: vial 25 mg/ml 10mL E/1 CN 663705: vial 25 mg/ml 2 ml E/1 Excipientes Solicitado por VINFLUNINA DITARTRATO (JAVLOR / PIERRE FABRE IBERICA, S.A.) Agua para inyectables Período de
Presentación CN 663707: vial 25 mg/ml 10mL E/1 CN 663705: vial 25 mg/ml 2 ml E/1 Excipientes Solicitado por VINFLUNINA DITARTRATO (JAVLOR / PIERRE FABRE IBERICA, S.A.) Agua para inyectables Período de
Experiencia con vinflunina en pacientes con cáncer urotelial e ILP prolongado
 Experiencia con vinflunina en pacientes con cáncer urotelial e ILP prolongado Cáncer urotelial estadio IV Estrategia de tratamiento en 2ª línea El tratamiento del carcinoma urotelial avanzado tras fracaso
Experiencia con vinflunina en pacientes con cáncer urotelial e ILP prolongado Cáncer urotelial estadio IV Estrategia de tratamiento en 2ª línea El tratamiento del carcinoma urotelial avanzado tras fracaso
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox
 TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
El Inmunomomento en Melanoma: Nivolumab más respuestas y larga supervivencia? Alfonso Berrocal
 El Inmunomomento en Melanoma: Nivolumab más respuestas y larga supervivencia? Alfonso Berrocal Proporción vivos Supervivencia con Ipilumumab en acceso expandido 1.0 0.9 0.8 Mediana de supervivencia meses
El Inmunomomento en Melanoma: Nivolumab más respuestas y larga supervivencia? Alfonso Berrocal Proporción vivos Supervivencia con Ipilumumab en acceso expandido 1.0 0.9 0.8 Mediana de supervivencia meses
Impacto de los nuevos tratamientos. Nuria Muñoz Muñoz Hospital Universitario Virgen Macarena
 Impacto de los nuevos tratamientos Nuria Muñoz Muñoz Hospital Universitario Virgen Macarena Indicaciones. Ipilimumab (Yervoy): EMA: tratamiento del melanoma avanzado (irresecable o metastásico) en adultos
Impacto de los nuevos tratamientos Nuria Muñoz Muñoz Hospital Universitario Virgen Macarena Indicaciones. Ipilimumab (Yervoy): EMA: tratamiento del melanoma avanzado (irresecable o metastásico) en adultos
CONTROVERSIAS HIPERTENSION PULMONAR
 CONTROVERSIAS HIPERTENSION PULMONAR Mª Carmen Torreiro Penas Hospital Xeral-Calde Lugo Eficacia/precio de los fármacos f aprobados? Es necesario evaluar los fármacos f aprobados? TRATAMIENTO Importantes
CONTROVERSIAS HIPERTENSION PULMONAR Mª Carmen Torreiro Penas Hospital Xeral-Calde Lugo Eficacia/precio de los fármacos f aprobados? Es necesario evaluar los fármacos f aprobados? TRATAMIENTO Importantes
Francisco de Asís Aparisi Aparisi. Hospital Virgen de los Lirios, Alcoy
 Estudio fase II de cisplatino (CDDP) y vinorelbina oral (VRLO) concomitante con radioterapia (RT) como tratamiento del cáncer de pulmón no microcítico localmente avanzado(cpnm-la): Resultados del objetivo
Estudio fase II de cisplatino (CDDP) y vinorelbina oral (VRLO) concomitante con radioterapia (RT) como tratamiento del cáncer de pulmón no microcítico localmente avanzado(cpnm-la): Resultados del objetivo
Tratamiento de la recai da del ca ncer de ovario en pacientes no candidatas a platino
 Tratamiento de la recai da del ca ncer de ovario en pacientes no candidatas a platino Ana Santaballa Bertrán, MD, PhD Servicio Oncologi a Me dica, Hospital Universitario y Polite cnico la Fe, Valencia
Tratamiento de la recai da del ca ncer de ovario en pacientes no candidatas a platino Ana Santaballa Bertrán, MD, PhD Servicio Oncologi a Me dica, Hospital Universitario y Polite cnico la Fe, Valencia
SARCOMA DE EWING Y TUMOR NEUROECTODERMICO PRIMITIVO.
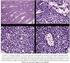 SARCOMA DE EWING Y TUMOR NEUROECTODERMICO PRIMITIVO. Una vez que el paciente ha sido diagnosticado por biopsia como Tumor Neuroectodermico Primitivo o Sarcoma de Ewing, se realizarán los siguientes estudios:
SARCOMA DE EWING Y TUMOR NEUROECTODERMICO PRIMITIVO. Una vez que el paciente ha sido diagnosticado por biopsia como Tumor Neuroectodermico Primitivo o Sarcoma de Ewing, se realizarán los siguientes estudios:
INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) INSULINAS
 Centro de Información de Medicamentos. Servicio de Farmacia. INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) Datos del solicitante INSULINAS Dr. Pedro José Pines Corrales, FEA del servicio
Centro de Información de Medicamentos. Servicio de Farmacia. INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) Datos del solicitante INSULINAS Dr. Pedro José Pines Corrales, FEA del servicio
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
Tratamiento del cáncer de Pulmón
 Tratamiento del cáncer de Pulmón Autor Isla Casado TRATAMIENTO DEL CARCINOMA NO MICROClTlCO DE PULMON El tratamiento del carcinoma no microcítico de pulmón considerado por estadios es el siguiente: 1)
Tratamiento del cáncer de Pulmón Autor Isla Casado TRATAMIENTO DEL CARCINOMA NO MICROClTlCO DE PULMON El tratamiento del carcinoma no microcítico de pulmón considerado por estadios es el siguiente: 1)
MIELOMA MÚLTIPLE: MP 1/5. 1. DENOMINACIÓN DEL ESQUEMA: MP (Melfalán-Prednisona).
 MIELOMA MÚLTIPLE: MP 1/5 1. DENOMINACIÓN DEL ESQUEMA: MP (Melfalán-Prednisona). 2. USO TERAPÉUTICO (1). Mieloma múltiple. Tratamiento de primera línea cuando no está indicado el trasplante de células progenitoras
MIELOMA MÚLTIPLE: MP 1/5 1. DENOMINACIÓN DEL ESQUEMA: MP (Melfalán-Prednisona). 2. USO TERAPÉUTICO (1). Mieloma múltiple. Tratamiento de primera línea cuando no está indicado el trasplante de células progenitoras
Modificaciones respecto a la anterior edición. Elaborado: Revisado Aprobado: Dirección Médica Dirección Enfermería
 Protocolo de nueva elaboración Modificaciones respecto a la anterior edición Elaborado: Revisado Aprobado: Comisión Infección, profilaxis y política antibiótica Dirección Médica Dirección Enfermería Dirección
Protocolo de nueva elaboración Modificaciones respecto a la anterior edición Elaborado: Revisado Aprobado: Comisión Infección, profilaxis y política antibiótica Dirección Médica Dirección Enfermería Dirección
1. DENOMINACIÓN DEL ESQUEMA: CARBOPLATINO- PACLITAXEL. Cáncer de pulmón no microcítico metastásico o localmente avanzado en 1ª línea.
 1. DENOMINACIÓN DEL ESQUEMA: CARBOPLATINO- PACLITAXEL 2. USO TERAPÉUTICO Cáncer de pulmón no microcítico metastásico o localmente avanzado en 1ª línea. 3. ESQUEMA (1,2,3) Medicamento Dosis Días Administración
1. DENOMINACIÓN DEL ESQUEMA: CARBOPLATINO- PACLITAXEL 2. USO TERAPÉUTICO Cáncer de pulmón no microcítico metastásico o localmente avanzado en 1ª línea. 3. ESQUEMA (1,2,3) Medicamento Dosis Días Administración
Tomoterapia: precisión y máximo ajuste en el tratamiento del cáncer
 Tomoterapia: precisión y máximo ajuste en el tratamiento del cáncer Radioterapia guiada por la imagen La Tomoterapia es un sistema de alta tecnología con el que se administra Radioterapia guiada por la
Tomoterapia: precisión y máximo ajuste en el tratamiento del cáncer Radioterapia guiada por la imagen La Tomoterapia es un sistema de alta tecnología con el que se administra Radioterapia guiada por la
COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS
 COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS 1. SOLICITUD DEL FÁRMACO Principio activo solicitado: (erbitux
COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS 1. SOLICITUD DEL FÁRMACO Principio activo solicitado: (erbitux
Estudio BASAL LIXI Presentación de Resultados
 Estudio observacional para evaluar el impacto de la intensificación de la terapia con insulina propuesta por la ADA/EASD 2012 (estrategia insulina basal + GLP-1 RA) sobre el control glucémico en pacientes
Estudio observacional para evaluar el impacto de la intensificación de la terapia con insulina propuesta por la ADA/EASD 2012 (estrategia insulina basal + GLP-1 RA) sobre el control glucémico en pacientes
Estudio SHARP (Study of Heart and Renal Protection )
 El estudio SHARP fue esponsorizado, diseñado, dirigido y analizado por la Universidad de Oxford. Financiado por Merck, la UK MRC, la British Heart Foundation, y la Australiana NHMRC. Estudio SHARP (Study
El estudio SHARP fue esponsorizado, diseñado, dirigido y analizado por la Universidad de Oxford. Financiado por Merck, la UK MRC, la British Heart Foundation, y la Australiana NHMRC. Estudio SHARP (Study
TRATAMIENTO NEO-ADYUVANTE CON GEMCITABINA Y CIS-PLATINO EN CÁNCER DE PULMÓN (NO CÉLULAS PEQUEÑAS)
 TRATAMIENTO NEO-ADYUVANTE CON GEMCITABINA Y CIS-PLATINO EN CÁNCER DE PULMÓN (NO CÉLULAS PEQUEÑAS) DR. CARLOS W. MONTESINO A.*, DRA. SARA J. CORONEL V.* RESUMEN: 25 pacientes con diagnóstico de cáncer de
TRATAMIENTO NEO-ADYUVANTE CON GEMCITABINA Y CIS-PLATINO EN CÁNCER DE PULMÓN (NO CÉLULAS PEQUEÑAS) DR. CARLOS W. MONTESINO A.*, DRA. SARA J. CORONEL V.* RESUMEN: 25 pacientes con diagnóstico de cáncer de
Vacuna frente al papilomavirus humano. (Comentarios a las fichas técnicas)
 Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
MIELOMA MÚLTIPLE: VAD 1/6. 1. DENOMINACIÓN DEL ESQUEMA: VAD (Vincristina, Doxorubucina, Dexametasona).
 MIELOMA MÚLTIPLE: VAD 1/6 1. DENOMINACIÓN DEL ESQUEMA: VAD (Vincristina, Doxorubucina, Dexametasona). 2. USO TERAPÉUTICO (1,2,3,4). Mieloma múltiple avanzado en primera línea de tratamiento previo a trasplante
MIELOMA MÚLTIPLE: VAD 1/6 1. DENOMINACIÓN DEL ESQUEMA: VAD (Vincristina, Doxorubucina, Dexametasona). 2. USO TERAPÉUTICO (1,2,3,4). Mieloma múltiple avanzado en primera línea de tratamiento previo a trasplante
TECNOLOGÍA EN SALUD DE INTERÉS. Oxcarbazepina, lacosamida, vigabatrina, topiramato o levetiracetam. 1. RESUMEN
 TECNOLOGÍA EN SALUD DE INTERÉS Oxcarbazepina, lacosamida, vigabatrina, topiramato y levetiracetam 1. RESUMEN Título del reporte: Efectividad y seguridad de oxcarbazepina, lacosamida, vigabatrina, topiramato
TECNOLOGÍA EN SALUD DE INTERÉS Oxcarbazepina, lacosamida, vigabatrina, topiramato y levetiracetam 1. RESUMEN Título del reporte: Efectividad y seguridad de oxcarbazepina, lacosamida, vigabatrina, topiramato
ENOXPRIM. Solución inyectable. Solución inyectable estéril, libre de pirógenos, contenida en jeringas pre-llenadas listas para usarse.
 ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
: Cáncer renal avanzado o metastásico
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
INSTRUCTIVO REGISTRO PARA LAS ATENCIONES DE QUIMIOTERAPIA
 1. OBJETIVO: Establecer una orientación clara y precisa que permita oficializar el sistema de registro de los tratamientos de quimioterapia en adultos del Hospital Regional de Arica Dr. Juan Noé Crevani,
1. OBJETIVO: Establecer una orientación clara y precisa que permita oficializar el sistema de registro de los tratamientos de quimioterapia en adultos del Hospital Regional de Arica Dr. Juan Noé Crevani,
Hospital Universitario Dr. Peset Valencia, 20 de octubre de 2011.
 EFICIENCIA DE BEVACIZUMAB IRINOTECÁN FLUOROURACILO VERSUS IRINOTECÁN FLUOROURACILO EN PRIMERA LÍNEA DE CARCINOMA COLORRECTAL METASTÁSICO Ruiz Millo O. 1, Sendra García A. 1, Albert Marí A. 1, González
EFICIENCIA DE BEVACIZUMAB IRINOTECÁN FLUOROURACILO VERSUS IRINOTECÁN FLUOROURACILO EN PRIMERA LÍNEA DE CARCINOMA COLORRECTAL METASTÁSICO Ruiz Millo O. 1, Sendra García A. 1, Albert Marí A. 1, González
2. USO TERAPÉUTICO (4) Tratamiento paliativo del cáncer colorrectal metastásico en primera o segunda línea. Medicamento Dosis Días Administración
 1. DENOMINACIÓN DEL ESQUEMA (1,3,4) : IRINOTECAN-LEUCOVORIN- FLUOROURACILO (FOLFIRI) 2. USO TERAPÉUTICO (4) Tratamiento paliativo del cáncer colorrectal metastásico en primera o segunda línea. 3. ESQUEMA
1. DENOMINACIÓN DEL ESQUEMA (1,3,4) : IRINOTECAN-LEUCOVORIN- FLUOROURACILO (FOLFIRI) 2. USO TERAPÉUTICO (4) Tratamiento paliativo del cáncer colorrectal metastásico en primera o segunda línea. 3. ESQUEMA
Tratamiento de la enfermedad tromboembólica venosa y cáncer.
 Tratamiento de la enfermedad tromboembólica venosa y cáncer. 1er Curso Trombosis y Hemostasia Martes, 13 de Octubre de 2015 Sala 10, Acadèmia Can Caralleu Actividad Avalada por: Elisa Orna Montero Laboratorio
Tratamiento de la enfermedad tromboembólica venosa y cáncer. 1er Curso Trombosis y Hemostasia Martes, 13 de Octubre de 2015 Sala 10, Acadèmia Can Caralleu Actividad Avalada por: Elisa Orna Montero Laboratorio
Quimioterapia en el cáncer de próstata. Dr. Álvaro Montesa Pino
 Quimioterapia en el cáncer de próstata Dr. Álvaro Montesa Pino Cáncer de Próstata Resistente a la Castración (CPRC) La mayoría de los pacientes con CP metastásico responden a la supresión androgénica gonadal
Quimioterapia en el cáncer de próstata Dr. Álvaro Montesa Pino Cáncer de Próstata Resistente a la Castración (CPRC) La mayoría de los pacientes con CP metastásico responden a la supresión androgénica gonadal
LLD Abreviado de Zoloft. Todo medicamento debe conservarse fuera del alcance de los niños.
 LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
Fitoestrógenos, nuevos datos, ofreciendo soluciones. Dra. Marisa Andrea David, Febrero 2013
 Fitoestrógenos, nuevos datos, ofreciendo soluciones Dra. Marisa Andrea David, Febrero 2013 Índice Síntomas de la menopausia y su tratamiento Evidencias científicas de las isoflavonas de soja Eficacia Seguridad
Fitoestrógenos, nuevos datos, ofreciendo soluciones Dra. Marisa Andrea David, Febrero 2013 Índice Síntomas de la menopausia y su tratamiento Evidencias científicas de las isoflavonas de soja Eficacia Seguridad
REUNION BIBLIOGRAFICA CLINICA UNIVERSITARIA REINA FABIOLA
 REUNION BIBLIOGRAFICA CLINICA UNIVERSITARIA REINA FABIOLA INTRODUCCION La respuesta al tratamiento sistémico en el cáncer de mama temprano puede ser controlada si el tratamiento se administra previo a
REUNION BIBLIOGRAFICA CLINICA UNIVERSITARIA REINA FABIOLA INTRODUCCION La respuesta al tratamiento sistémico en el cáncer de mama temprano puede ser controlada si el tratamiento se administra previo a
Grupo de estudio internacional del cáncer de mama (IBCSG) 23-01
 Grupo de estudio internacional del cáncer de mama (IBCSG) 23-01 Disección axilar vs. no disección axilar en cáncer de mama con axila clínicamente negativa y micrometástasis en ganglio centinela Viviana
Grupo de estudio internacional del cáncer de mama (IBCSG) 23-01 Disección axilar vs. no disección axilar en cáncer de mama con axila clínicamente negativa y micrometástasis en ganglio centinela Viviana
Costo efectividad de la ingesta de sangre de pollo en el tratamiento de la anemia ferropénica en estudiantes de la EAP de Obstetricia de la UNMSM
 REV ACAD PERU SALUD 14(1), 2007 97 TESIS DE MAESTRÍA Costo efectividad de la ingesta de sangre de pollo en el tratamiento de la anemia ferropénica en estudiantes de la EAP de Obstetricia de la UNMSM Zaida
REV ACAD PERU SALUD 14(1), 2007 97 TESIS DE MAESTRÍA Costo efectividad de la ingesta de sangre de pollo en el tratamiento de la anemia ferropénica en estudiantes de la EAP de Obstetricia de la UNMSM Zaida
LEVETIRACETAM SOLUCION INTRAVENOSA EN EPILEPSIA (Informe para la Comisión de Farmacia y Terapéutica del Hospital Son LLátzer) Fecha Abril 2008
 LEVETIRACETAM SOLUCION INTRAVENOSA EN EPILEPSIA (Informe para la Comisión de Farmacia y Terapéutica del Hospital Son LLátzer) Fecha Abril 2008 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco:
LEVETIRACETAM SOLUCION INTRAVENOSA EN EPILEPSIA (Informe para la Comisión de Farmacia y Terapéutica del Hospital Son LLátzer) Fecha Abril 2008 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco:
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
Equivalentes terapéuticos
 Versión 1 10 Oct 2006 Equivalentes terapéuticos Por qué surge el concepto de equivalentes terapéuticos? El sistema de autorización de medicamentos por parte de las Agencias Reguladoras provoca que en el
Versión 1 10 Oct 2006 Equivalentes terapéuticos Por qué surge el concepto de equivalentes terapéuticos? El sistema de autorización de medicamentos por parte de las Agencias Reguladoras provoca que en el
ABIRATERONA (ZYTIGA / JANSSEN)
 ABIRATERONA (ZYTIGA / JANSSEN) Presentación 683759 Comp 250mg E/120 PVL=3.400 DIAGNÓSTICO HOSPITALARIO. DISPENSACIÓN HOSPITALARIA SIN CUPÓN PRECINTO. Excipientes Lactosa monohidrato, Celulosa microcristalina
ABIRATERONA (ZYTIGA / JANSSEN) Presentación 683759 Comp 250mg E/120 PVL=3.400 DIAGNÓSTICO HOSPITALARIO. DISPENSACIÓN HOSPITALARIA SIN CUPÓN PRECINTO. Excipientes Lactosa monohidrato, Celulosa microcristalina
De qué sistemas se dispone para evaluar el riesgo vascular? A qué población y con qué frecuencia se le debe evaluar el riesgo vascular?
 4. Riesgo vascular Preguntas para responder: De qué sistemas se dispone para evaluar el riesgo vascular? A qué población y con qué frecuencia se le debe evaluar el riesgo vascular? 4.1. Importancia del
4. Riesgo vascular Preguntas para responder: De qué sistemas se dispone para evaluar el riesgo vascular? A qué población y con qué frecuencia se le debe evaluar el riesgo vascular? 4.1. Importancia del
INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA
 BRENTUXIMAB VEDOTIN en el tratamiento del linfoma de Hodgkin CD30+ y del linfoma anaplásico de células grandes. INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Genérico:
BRENTUXIMAB VEDOTIN en el tratamiento del linfoma de Hodgkin CD30+ y del linfoma anaplásico de células grandes. INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Genérico:
Insuficiencia Cardiaca. Betabloqueantes vs. Ivabradina. A favor de Ivabradina. Afonso Barroso de Freitas Ferraz
 Insuficiencia Cardiaca. Betabloqueantes vs. Ivabradina. A favor de Ivabradina Afonso Barroso de Freitas Ferraz Índice La FC en las enfermedades CV Betabloqueantes en IC Mecanismo de acción de la ivabradina
Insuficiencia Cardiaca. Betabloqueantes vs. Ivabradina. A favor de Ivabradina Afonso Barroso de Freitas Ferraz Índice La FC en las enfermedades CV Betabloqueantes en IC Mecanismo de acción de la ivabradina
INFORME SEOM DE EVALUACIÓN DE FÁRMACO
 INFORME SEOM DE EVALUACIÓN DE FÁRMACO Título: Pertuzumab en combinación con trastuzumab y docetaxel como tratamiento de primera línea en el cáncer de mama HER2+ avanzado. 31 de diciembre 2013 1.- RESUMEN
INFORME SEOM DE EVALUACIÓN DE FÁRMACO Título: Pertuzumab en combinación con trastuzumab y docetaxel como tratamiento de primera línea en el cáncer de mama HER2+ avanzado. 31 de diciembre 2013 1.- RESUMEN
Tratamiento inmunoterápico de las metástasis cerebrales. Alfonso Berrocal Hospital General de Valencia
 Tratamiento inmunoterápico de las metástasis cerebrales Alfonso Berrocal Hospital General de Valencia Inmunidad y metástasis cerebrales Cancer 2013;119:2737-46. Ipilimumab y metástasis SNC Ipilimumab bloquea
Tratamiento inmunoterápico de las metástasis cerebrales Alfonso Berrocal Hospital General de Valencia Inmunidad y metástasis cerebrales Cancer 2013;119:2737-46. Ipilimumab y metástasis SNC Ipilimumab bloquea
FICHA TECNICA. Tratamiento de la intoxicación por Amanita phalloides.
 FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
EFECTIVIDAD Y EFICACIA DEL TRASPLANTE DE PROGENITORES HEMATOPOYÉTICOS NO EMPARENTADO PARA EL TRATAMIENTO DE ANEMIA DE FANCONI.
 INSTITUTO NACIONAL DE SALUD EFECTIVIDAD Y EFICACIA DEL TRASPLANTE DE PROGENITORES HEMATOPOYÉTICOS NO EMPARENTADO PARA EL TRATAMIENTO DE ANEMIA DE FANCONI. NOTA TÉCNICA N 16 Unidad de Análisis y Generación
INSTITUTO NACIONAL DE SALUD EFECTIVIDAD Y EFICACIA DEL TRASPLANTE DE PROGENITORES HEMATOPOYÉTICOS NO EMPARENTADO PARA EL TRATAMIENTO DE ANEMIA DE FANCONI. NOTA TÉCNICA N 16 Unidad de Análisis y Generación
Preguntas para responder
 Preguntas para responder TRATAMIENTO DE LA EPOC EN FASE ESTABLE 1. Existe evidencia para aconsejar un tipo concreto de broncodilatador de acción mantenida en monoterapia cuando se inicia el tratamiento
Preguntas para responder TRATAMIENTO DE LA EPOC EN FASE ESTABLE 1. Existe evidencia para aconsejar un tipo concreto de broncodilatador de acción mantenida en monoterapia cuando se inicia el tratamiento
Historia. Fisiopatología. Sistema venoso profundo. JOHN JAIRO BERRêO C. - ADELMA SOFêA HOYOS
 35 JOHN JAIRO BERRêO C. - ADELMA SOFêA HOYOS Historia La terapia anticoagulante ingresó en el arsenal clínico a partir del aislamiento de un glucosaminoglicano del hígado de un canino, que fue denominado
35 JOHN JAIRO BERRêO C. - ADELMA SOFêA HOYOS Historia La terapia anticoagulante ingresó en el arsenal clínico a partir del aislamiento de un glucosaminoglicano del hígado de un canino, que fue denominado
Afatinib En cáncer CPNM avanzado o metastásico Informe de la CFT HOSPITAL REINA SOFÍA CÓRDOBA
 Afatinib En cáncer CPNM avanzado o metastásico Informe de la CFT HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Comercial: GIOTRIF 20 mg, 30 mg, 40 mg y 50 mg Presentaciones: Comprimidos
Afatinib En cáncer CPNM avanzado o metastásico Informe de la CFT HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Comercial: GIOTRIF 20 mg, 30 mg, 40 mg y 50 mg Presentaciones: Comprimidos
PÍLDORA DEL DÍA DESPUÉS
 Programa Nacional de Salud Sexual y Procreación Responsable PÍLDORA DEL DÍA DESPUÉS Anticoncepción Hormonal de Emergencia AHE Guía de Usuarias MÉTODOS ANTICONCEPTIVOS La salud sexual y reproductiva es
Programa Nacional de Salud Sexual y Procreación Responsable PÍLDORA DEL DÍA DESPUÉS Anticoncepción Hormonal de Emergencia AHE Guía de Usuarias MÉTODOS ANTICONCEPTIVOS La salud sexual y reproductiva es
Introducción. Tratamientos específicos
 Introducción Los tumores urológicos representan una importante parcela de trabajo diario para urólogos, oncólogos médicos y radioterapeutas. La diseminación de la enfermedad de los tumores urológicos es
Introducción Los tumores urológicos representan una importante parcela de trabajo diario para urólogos, oncólogos médicos y radioterapeutas. La diseminación de la enfermedad de los tumores urológicos es
PERTUZUMAB AUMENTA LA SUPERVIVENCIA GLOBAL EN CÁNCER DE MAMA METASTÁSICO HER2 POSITIVO
 Los especialistas españoles coinciden en que es el avance más relevante en una década y que permitirá afrontar una necesidad médica urgente PERTUZUMAB AUMENTA LA SUPERVIVENCIA GLOBAL EN CÁNCER DE MAMA
Los especialistas españoles coinciden en que es el avance más relevante en una década y que permitirá afrontar una necesidad médica urgente PERTUZUMAB AUMENTA LA SUPERVIVENCIA GLOBAL EN CÁNCER DE MAMA
EVALUACIÓN DEL TIEMPO DE MUESTREO DE LAS CONCENTRACIONES PLASMÁTICAS DE 2 FARMACOS ANTICONVULSIVANTES EN PACIENTES DE UN HOSPITAL PEDIATRICO.
 EVALUACIÓN DEL TIEMPO DE MUESTREO DE LAS CONCENTRACIONES PLASMÁTICAS DE 2 FARMACOS ANTICONVULSIVANTES EN PACIENTES DE UN HOSPITAL PEDIATRICO. Márquez Cruz Maribel 1, Robles Piedras Ana Luisa 1, Ruiz Anaya
EVALUACIÓN DEL TIEMPO DE MUESTREO DE LAS CONCENTRACIONES PLASMÁTICAS DE 2 FARMACOS ANTICONVULSIVANTES EN PACIENTES DE UN HOSPITAL PEDIATRICO. Márquez Cruz Maribel 1, Robles Piedras Ana Luisa 1, Ruiz Anaya
GENESIS-SEFH. Informe Base Página: 1
 Informe Base Página: 1 INFORME TÉCNICO DE EVALUACIÓN ERIBULINA en cáncer de mama localmente avanzado o metastásico ADAPTACIÓN de informe de Grupo GENESIS de la SEFH y de IPT de la AEMPS Fecha: 07/09/2012
Informe Base Página: 1 INFORME TÉCNICO DE EVALUACIÓN ERIBULINA en cáncer de mama localmente avanzado o metastásico ADAPTACIÓN de informe de Grupo GENESIS de la SEFH y de IPT de la AEMPS Fecha: 07/09/2012
Tratamiento del cáncer de cérvix Amalia Gómez Bernal Complejo Asistencial Universitario de Salamanca
 Tratamiento del cáncer de cérvix 2016 Amalia Gómez Bernal Complejo Asistencial Universitario de Salamanca Datos estadísticos INCIDENCIA Es el 3º tumor más frecuente en las mujeres en el mundo y el 7º del
Tratamiento del cáncer de cérvix 2016 Amalia Gómez Bernal Complejo Asistencial Universitario de Salamanca Datos estadísticos INCIDENCIA Es el 3º tumor más frecuente en las mujeres en el mundo y el 7º del
Control del sangrado. Artículo: Hemorragia por Warfarina (Cortesía de IntraMed.com)
 Control del sangrado En este gran estudio de cohorte de pacientes mayores con fibrilación auricular se halló que las tasas de hemorragia por tratamiento con warfarina son más elevadas durante los primeros
Control del sangrado En este gran estudio de cohorte de pacientes mayores con fibrilación auricular se halló que las tasas de hemorragia por tratamiento con warfarina son más elevadas durante los primeros
Coste por unidad PVL con IVA Vial 100 mg/ 50 ml 1 vial 745026 246,69 204,60
 Servei de Farmàcia Informe CFT: 1/6 Cetuximab Tratamiento de cáncer de células escamosas de cabeza y cuello localmente avanzado, en combinación con radioterapia Informe para la Comisión Farmacoterapéutica
Servei de Farmàcia Informe CFT: 1/6 Cetuximab Tratamiento de cáncer de células escamosas de cabeza y cuello localmente avanzado, en combinación con radioterapia Informe para la Comisión Farmacoterapéutica
PVL con IVA Cápsula dura 1mg 10 660762 406.95 Cápsula dura 0,25mg 10 660763 101.73
 TOPOTECAN VÍA ORAL Cáncer de pulmón de célula pequeña recidivante (Informe para la Comisión de Farmacia y Terapéutica del Hospital Virgen de las Nieves) Fecha 10/03/09 1.- IDENTIFICACIÓN DEL FÁRMACO Y
TOPOTECAN VÍA ORAL Cáncer de pulmón de célula pequeña recidivante (Informe para la Comisión de Farmacia y Terapéutica del Hospital Virgen de las Nieves) Fecha 10/03/09 1.- IDENTIFICACIÓN DEL FÁRMACO Y
DABRAFENIB en el tratamiento dea melanoma INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA
 DABRAFENIB en el tratamiento dea melanoma INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Genérico: Dabrafenib Nombre Comercial: Tafinlar Presentaciones: E/28 comp 50 y
DABRAFENIB en el tratamiento dea melanoma INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Genérico: Dabrafenib Nombre Comercial: Tafinlar Presentaciones: E/28 comp 50 y
Monitorización de niveles de vancomicina en Pediatría
 Monitorización de niveles de vancomicina en Pediatría Chevorn Suzette Adams (R3 Pediatría) María Luz Boquera Ferrer (R4 Farmacia Hospitalaria) Tutor: Dr. Luis Moral 3 febrero, 2016, HGUA. Objetivo Repasar
Monitorización de niveles de vancomicina en Pediatría Chevorn Suzette Adams (R3 Pediatría) María Luz Boquera Ferrer (R4 Farmacia Hospitalaria) Tutor: Dr. Luis Moral 3 febrero, 2016, HGUA. Objetivo Repasar
EPOC : PREVENCIÓN Y ENFERMEDAD CARDIOVASCULAR ADOLFO BALOIRA COMPLEJO HOSPITALARIO UNIVERSITARIO DE PONTEVEDRA
 EPOC : PREVENCIÓN Y ENFERMEDAD CARDIOVASCULAR ADOLFO BALOIRA COMPLEJO HOSPITALARIO UNIVERSITARIO DE PONTEVEDRA QUÉ ES LA EPOC? Enfermedad crónica Afectación bronquial, pulmonar y con el tiempo sistémica
EPOC : PREVENCIÓN Y ENFERMEDAD CARDIOVASCULAR ADOLFO BALOIRA COMPLEJO HOSPITALARIO UNIVERSITARIO DE PONTEVEDRA QUÉ ES LA EPOC? Enfermedad crónica Afectación bronquial, pulmonar y con el tiempo sistémica
VALIDEZ DE LOS CRITERIOS DEFINITORIOS DE PACIENTES CON ENFERMEDADES MÉDICAS EN FASE TERMINAL. PROYECTO PALIAR. IV REUNIÓN PPyEA. Valencia Octubre 2008
 VALIDEZ DE LOS CRITERIOS DEFINITORIOS DE PACIENTES CON ENFERMEDADES MÉDICAS EN FASE TERMINAL. PROYECTO PALIAR IV REUNIÓN PPyEA. Valencia Octubre 2008 VALIDEZ DE LOS CRITERIOS DEFINITORIOS DE PACIENTES
VALIDEZ DE LOS CRITERIOS DEFINITORIOS DE PACIENTES CON ENFERMEDADES MÉDICAS EN FASE TERMINAL. PROYECTO PALIAR IV REUNIÓN PPyEA. Valencia Octubre 2008 VALIDEZ DE LOS CRITERIOS DEFINITORIOS DE PACIENTES
El comité de cáncer de la Federación Internacional de Ginecología y Obstetricia (FIGO) ha establecido la siguiente guía para el diagnóstico de
 El comité de cáncer de la Federación Internacional de Ginecología y Obstetricia (FIGO) ha establecido la siguiente guía para el diagnóstico de Neoplasia Trofoblastica gestacional pos molar. Cuatro valores
El comité de cáncer de la Federación Internacional de Ginecología y Obstetricia (FIGO) ha establecido la siguiente guía para el diagnóstico de Neoplasia Trofoblastica gestacional pos molar. Cuatro valores
Melasma. Andrea Albuja, Nicolás Almeida, Danilo Noboa UIDE
 Melasma Andrea Albuja, Nicolás Almeida, Danilo Noboa UIDE Es la terapia triple la mejor opción de tratamiento en pacientes con melasma? Primer articulo 2003 Criterios Inclusion: muestra de 641 pacientes
Melasma Andrea Albuja, Nicolás Almeida, Danilo Noboa UIDE Es la terapia triple la mejor opción de tratamiento en pacientes con melasma? Primer articulo 2003 Criterios Inclusion: muestra de 641 pacientes
ARTICULOS PUBLICADOS 4. ARTÍCULOS PUBLICADOS
 4. ARTÍCULOS PUBLICADOS 53 4.1. Clinical study and follow-up of 100 patients with the antiphospholipid syndrome. Semin Arthritis Rheum 1999; 29: 182-190. 54 55 56 57 58 59 60 61 62 63 RESUMEN Objetivo:
4. ARTÍCULOS PUBLICADOS 53 4.1. Clinical study and follow-up of 100 patients with the antiphospholipid syndrome. Semin Arthritis Rheum 1999; 29: 182-190. 54 55 56 57 58 59 60 61 62 63 RESUMEN Objetivo:
IPILIMUMAB EN AVANZADO/METASTASICO
 IPILIMUMAB EN MELANOMA AVANZADO/METASTASICO GROWING UP IN ONCOLOGY Sesión 19 de junio de 2012 REBECA ALCALDE PAMPLIEGA R4 ONCOLOGIA MEDICA HOSPITAL UNIVERSITARIO RAMÓN Y CAJAL QUÉ ES IPILIMUMAB? Anticuerpo
IPILIMUMAB EN MELANOMA AVANZADO/METASTASICO GROWING UP IN ONCOLOGY Sesión 19 de junio de 2012 REBECA ALCALDE PAMPLIEGA R4 ONCOLOGIA MEDICA HOSPITAL UNIVERSITARIO RAMÓN Y CAJAL QUÉ ES IPILIMUMAB? Anticuerpo
Nab-paclitaxel, nuevo estándar de tratamiento en el cáncer de páncreas MERCEDES SALGADO FERNÁNDEZ
 Nab-paclitaxel, nuevo estándar de tratamiento en el cáncer de MERCEDES SALGADO FERNÁNDEZ VISIÓN GENERAL: EVOLUCIÓN DEL TRATAMIENTO EN 1ª LÍNEA DEL CÁNCER DE PÁNCREAS CASO CLÍNICO ESTUDIO MPAC: UN NUEVO
Nab-paclitaxel, nuevo estándar de tratamiento en el cáncer de MERCEDES SALGADO FERNÁNDEZ VISIÓN GENERAL: EVOLUCIÓN DEL TRATAMIENTO EN 1ª LÍNEA DEL CÁNCER DE PÁNCREAS CASO CLÍNICO ESTUDIO MPAC: UN NUEVO
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COTRIMOXAZOL 200/40/5 ml SUSPENSIÓN ANTIINFECCIOSO-ANTIBACTERIANO Página 1 COTRIMOXAZOL 200/40/5 ml Suspensión Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COTRIMOXAZOL 200/40/5 ml SUSPENSIÓN ANTIINFECCIOSO-ANTIBACTERIANO Página 1 COTRIMOXAZOL 200/40/5 ml Suspensión Principio
ARIPIPRAZOL En adolescentes contrastorno Bipolar I
 ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
RESULTADOS PRELIMINARES
 ESTUDIO DE LA EFICACIA DE LICOTRIZ COMO CREMA REGENERATIVA Y REGENERADORA EN EL TRATAMIENTO DE CICATRICES POSTQUIRÚRGICAS EN PACIENTES SOMETIDAS A RADIOTERAPIA POR CÁNCERES GINECOLÓGICOS. INTRODUCCIÓN
ESTUDIO DE LA EFICACIA DE LICOTRIZ COMO CREMA REGENERATIVA Y REGENERADORA EN EL TRATAMIENTO DE CICATRICES POSTQUIRÚRGICAS EN PACIENTES SOMETIDAS A RADIOTERAPIA POR CÁNCERES GINECOLÓGICOS. INTRODUCCIÓN
CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG
 CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG COMPOSICIÓN Por ml: Principio activo: Carboplatino (D.C.I.) 10 mg Excipientes: Agua para inyección c.s. FORMA FARMACÉUTICA Y
CARBOPLATINO PHARMACIA 10 mg/ml concentrado para solución para perfusión EFG COMPOSICIÓN Por ml: Principio activo: Carboplatino (D.C.I.) 10 mg Excipientes: Agua para inyección c.s. FORMA FARMACÉUTICA Y
Nab-paclitaxel en 1ªlínea cáncer páncreas metastásico INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA
 Nab-paclitaxel en 1ªlínea cáncer páncreas metastásico INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Genérico: Nab-paclitaxel Nombre Comercial: Abraxane Presentaciones:
Nab-paclitaxel en 1ªlínea cáncer páncreas metastásico INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Genérico: Nab-paclitaxel Nombre Comercial: Abraxane Presentaciones:
Injuria renal aguda en pacientes pos operados de hipertrofia benigna de próstata R2 LOZANO ESPINOZA NORIS
 Injuria renal aguda en pacientes pos operados de hipertrofia benigna de próstata R2 LOZANO ESPINOZA NORIS INTRODUCCION La Injuria Renal Aguda (IRA) es una patología frecuente en la población hospitalizada
Injuria renal aguda en pacientes pos operados de hipertrofia benigna de próstata R2 LOZANO ESPINOZA NORIS INTRODUCCION La Injuria Renal Aguda (IRA) es una patología frecuente en la población hospitalizada
Experiencia con Vinorelbina Oral en el tratamiento del CPNM con histología no escamoso. Dr. Javier de Castro
 Experiencia con Vinorelbina Oral en el tratamiento del CPNM con histología no escamoso Dr. Javier de Castro Caso Clínico: carcinoma de pulmón no escamoso avanzado Mujer de 60 años Fumadora de 30 cig/d
Experiencia con Vinorelbina Oral en el tratamiento del CPNM con histología no escamoso Dr. Javier de Castro Caso Clínico: carcinoma de pulmón no escamoso avanzado Mujer de 60 años Fumadora de 30 cig/d
Programa RIO Rimonabant en Obesidad Estudios clínicos
 Programa RIO Rimonabant en Obesidad Estudios clínicos Evaluación de eficacia y seguridad de Acomplia en más de 6.600 pacientes Buenos Aires, 25 de Agosto de 2005.- El Programa RIO (Rimonabant in Obesity,
Programa RIO Rimonabant en Obesidad Estudios clínicos Evaluación de eficacia y seguridad de Acomplia en más de 6.600 pacientes Buenos Aires, 25 de Agosto de 2005.- El Programa RIO (Rimonabant in Obesity,
ANÁLISIS DE DUPLICIDADES DEL SUBGRUPO TERAPÉUTICO L02 - TERAPIA ENDOCRINA
 ANÁLISIS DE ES DEL SUBGRUPO TERAPÉUTICO L02 - TERAPIA ENDOCRINA Clasificación ATC L02A: HORMONAS Y AGENTES RELACIONADOS L02AB PROGESTÁGENOS L02AE ANÁLOGOS DE LA HORMONA LIBERADORA DE GONADOTROPINAS. Histrelina
ANÁLISIS DE ES DEL SUBGRUPO TERAPÉUTICO L02 - TERAPIA ENDOCRINA Clasificación ATC L02A: HORMONAS Y AGENTES RELACIONADOS L02AB PROGESTÁGENOS L02AE ANÁLOGOS DE LA HORMONA LIBERADORA DE GONADOTROPINAS. Histrelina
TALLER 4: EVALUACIÓN
 TALLER 4: EVALUACIÓN ECONÓMICA Coordina: María Espinosa Bosch FEA. UG de Farmacia. HU Virgen del Rocío. maria.espinosa.sspa@juntadeandalucia.es Colabora: Antonia Perez Moreno Algunas diapositivas son de
TALLER 4: EVALUACIÓN ECONÓMICA Coordina: María Espinosa Bosch FEA. UG de Farmacia. HU Virgen del Rocío. maria.espinosa.sspa@juntadeandalucia.es Colabora: Antonia Perez Moreno Algunas diapositivas son de
Dra. Nayrin A. Súnico B.
 Dra. Nayrin A. Súnico B. Caracas, 14 de marzo de 2012 Introducción Cáncer de cuello uterino: 2da causa de cáncer en la mujer 2da causa de muerte en mujeres entre 14-44 años VPH con carcinoma de cuello
Dra. Nayrin A. Súnico B. Caracas, 14 de marzo de 2012 Introducción Cáncer de cuello uterino: 2da causa de cáncer en la mujer 2da causa de muerte en mujeres entre 14-44 años VPH con carcinoma de cuello
Bevacizumab en Cáncer de Colon
 1 Bevacizumab ONCOLOGÍA en Cáncer de Colon 2013 Bevacizumab en Cáncer de Colon Recomendaciones para su Uso Coordinador: Dr. Esteban Lifschitz Autores: Dr. Patricio Servienti, Dr. Ventura Simonovich Evaluación
1 Bevacizumab ONCOLOGÍA en Cáncer de Colon 2013 Bevacizumab en Cáncer de Colon Recomendaciones para su Uso Coordinador: Dr. Esteban Lifschitz Autores: Dr. Patricio Servienti, Dr. Ventura Simonovich Evaluación
Patricia Novas Vidal R4 oncología médica H.U. Marqués de Valdecilla, Santander
 Neutropenia Febril Patricia Novas Vidal R4 oncología médica H.U. Marqués de Valdecilla, Santander 1. Introducción 2. Definición 3. Epidemiología 4. Evaluación inicial Índice 5. Paciente con bajo riesgo
Neutropenia Febril Patricia Novas Vidal R4 oncología médica H.U. Marqués de Valdecilla, Santander 1. Introducción 2. Definición 3. Epidemiología 4. Evaluación inicial Índice 5. Paciente con bajo riesgo
Pacientes con cáncer. Carlos Lahoz
 Pacientes con cáncer Carlos Lahoz Varón 45 a. con dolor precordial de 45 mn de duración. ECG: Aumento de troponina I Coronariografía: Antecedentes personales No HTA, no DM, no dislipemia. No hábitos tóxicos.
Pacientes con cáncer Carlos Lahoz Varón 45 a. con dolor precordial de 45 mn de duración. ECG: Aumento de troponina I Coronariografía: Antecedentes personales No HTA, no DM, no dislipemia. No hábitos tóxicos.
Cáncer de mama avanzado
 Cáncer de mama avanzado Santander 1 de Julio 2016 Tàrsila Ferro Directora de Cuidados Instituto Catalán de Oncología Profesora Universidad de Barcelona Definiciones Cáncer de mama recurrente o recurrencia:
Cáncer de mama avanzado Santander 1 de Julio 2016 Tàrsila Ferro Directora de Cuidados Instituto Catalán de Oncología Profesora Universidad de Barcelona Definiciones Cáncer de mama recurrente o recurrencia:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO NAVELBINE 20 mg cápsulas blandas
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO NAVELBINE 20 mg cápsulas blandas 1. DENOMINACIÓN DEL MEDICAMENTO NAVELBINE 20 mg cápsulas blandas. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 20 mg de vinorelbina
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO NAVELBINE 20 mg cápsulas blandas 1. DENOMINACIÓN DEL MEDICAMENTO NAVELBINE 20 mg cápsulas blandas. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 20 mg de vinorelbina
NOMBRE DEL MEDICAMENTO COMPOSICIÓN CUALITATIVA Y CUANTITATIVA FORMA FARMACÉUTICA DATOS CLÍNICOS. Edad Peso corporal (aprox.) Posología (cada 6 horas)
 NOMBRE DEL MEDICAMENTO APIRETAL 100 mg/ml solución oral COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Fórmula por ml: Paracetamol... 100 mg Azorrubina (E-122)... 50 μg También contiene AGUA FORMA FARMACÉUTICA
NOMBRE DEL MEDICAMENTO APIRETAL 100 mg/ml solución oral COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Fórmula por ml: Paracetamol... 100 mg Azorrubina (E-122)... 50 μg También contiene AGUA FORMA FARMACÉUTICA
PROYECTOS PRESENTADOS
 Área Calidad, Formación, Investigación y Desarrollo Enfermería PREMIO NACIONAL DE INVESTIGACIÓN EN ENFERMERÍA 15ª EDICIÓN año 2013 PROYECTOS PRESENTADOS TRABAJO Nº 1 Título: EFECTOS Y CONSECUENCIAS DE
Área Calidad, Formación, Investigación y Desarrollo Enfermería PREMIO NACIONAL DE INVESTIGACIÓN EN ENFERMERÍA 15ª EDICIÓN año 2013 PROYECTOS PRESENTADOS TRABAJO Nº 1 Título: EFECTOS Y CONSECUENCIAS DE
Administración de fármacos por vía subcutánea en cuidados paliativos
 Administración de fármacos por vía subcutánea en cuidados paliativos Dña. Mª Trinidad Llopis Llorens D. Francisco Enrique Moltó Abad Enfermer@s UHD. Hospital Virgen de los Lirios. Alcoi 1 Origenes. 1817-1884
Administración de fármacos por vía subcutánea en cuidados paliativos Dña. Mª Trinidad Llopis Llorens D. Francisco Enrique Moltó Abad Enfermer@s UHD. Hospital Virgen de los Lirios. Alcoi 1 Origenes. 1817-1884
Las siguientes son quías de diagnostico y tratamiento de las enfermedades genitourinarias elaboradas por las siguientes asociaciones:
 GUÍA DE DIAGNOSTICO Y TRATAMIENTO DE LAS ENFERMEDADES GENITOURINARIAS DEL SERVICIO DE UROLOGÍA DEL HOSPITAL ESPAÑOL DE MENDOZA (Aprobada por el Comité de docencia e Investigación del Hospital Español)
GUÍA DE DIAGNOSTICO Y TRATAMIENTO DE LAS ENFERMEDADES GENITOURINARIAS DEL SERVICIO DE UROLOGÍA DEL HOSPITAL ESPAÑOL DE MENDOZA (Aprobada por el Comité de docencia e Investigación del Hospital Español)
LA EVALUACIÓN DEL PSA EN EL DIAGNÓSTICO DEL CÁNCER DE PRÓSTATA
 LA EVALUACIÓN DEL PSA EN EL DIAGNÓSTICO DEL CÁNCER DE PRÓSTATA Diana Predescu Isabel Martínez Sáez Centro de Salud de Onda I Unitad Docente MFYC Castellon INTRODUCCIÒN El CaP en España y Europa es el tercer
LA EVALUACIÓN DEL PSA EN EL DIAGNÓSTICO DEL CÁNCER DE PRÓSTATA Diana Predescu Isabel Martínez Sáez Centro de Salud de Onda I Unitad Docente MFYC Castellon INTRODUCCIÒN El CaP en España y Europa es el tercer
CEFUROXIMA STADA EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA
 OBJETIVO CEFUROXIMA STADA EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA El Estudio de Bioequivalencia de Cefuroxima STADA EFG se ha realizado siguiendo las Directrices que la Unión Europea recomienda para
OBJETIVO CEFUROXIMA STADA EFG RESUMEN DEL ESTUDIO DE BIOEQUIVALENCIA El Estudio de Bioequivalencia de Cefuroxima STADA EFG se ha realizado siguiendo las Directrices que la Unión Europea recomienda para
Comissió de Millora de l'adequació de la Pràctica Assistencial i Clínica (MAPAC) Resumen de la evaluación 2011/01
 Comissió de Millora de l'adequació de la Pràctica Assistencial i Clínica (MAPAC) Resumen de la evaluación 2011/01 PREGUNTAS PRESTACIONES EVALUADAS Está recomendado en términos de supervivencia y calidad
Comissió de Millora de l'adequació de la Pràctica Assistencial i Clínica (MAPAC) Resumen de la evaluación 2011/01 PREGUNTAS PRESTACIONES EVALUADAS Está recomendado en términos de supervivencia y calidad
DAÑO RENAL AGUDO. Oscar DuBois Rll Medicinal Interna
 DAÑO RENAL AGUDO Oscar DuBois Rll Medicinal Interna Contenido:! Anatomía! Epidemiología! Definición! Causas! Evaluación clínica! Diagnóstico! Tratamiento Epidemiologia Se estima 13.3 millones de casos
DAÑO RENAL AGUDO Oscar DuBois Rll Medicinal Interna Contenido:! Anatomía! Epidemiología! Definición! Causas! Evaluación clínica! Diagnóstico! Tratamiento Epidemiologia Se estima 13.3 millones de casos
GROWING UP IN ONCOLOGY MEC. María José de Miguel Luken
 GROWING UP IN ONCOLOGY Recomendaciones de guías en MEC Sesión 21 de junio de 2011 María José de Miguel Luken 1. Clasificación 2. ASCO. 3. ESMO/MASCC 4. NCCN 5. SEOM 6. Conclusiones Clasificación MEC Las
GROWING UP IN ONCOLOGY Recomendaciones de guías en MEC Sesión 21 de junio de 2011 María José de Miguel Luken 1. Clasificación 2. ASCO. 3. ESMO/MASCC 4. NCCN 5. SEOM 6. Conclusiones Clasificación MEC Las
TOLERANCIA A LA TRIPLE TERAPIA EN POBLACIONES ESPECIALES
 TOLERANCIA A LA TRIPLE TERAPIA EN POBLACIONES ESPECIALES C a r m e n V i n a i x a, C a r l a S a t o r r e s, B e a t r i z R o d r í g u e z, M a r í a G a r c í a, V i c t o r i a A g u i l e r a, A
TOLERANCIA A LA TRIPLE TERAPIA EN POBLACIONES ESPECIALES C a r m e n V i n a i x a, C a r l a S a t o r r e s, B e a t r i z R o d r í g u e z, M a r í a G a r c í a, V i c t o r i a A g u i l e r a, A
PRESENTACIÓN GANFORT
 PRESENTACIÓN GANFORT PRESENTACIÓN GANFORT John J. Aristizábal Gómez Jefe Oftalmología H.P.T.U Docente Postgrado U.P.B Alcanzando la PIO meta Tratando el glaucoma de manera intensiva Abordaje terapéutico
PRESENTACIÓN GANFORT PRESENTACIÓN GANFORT John J. Aristizábal Gómez Jefe Oftalmología H.P.T.U Docente Postgrado U.P.B Alcanzando la PIO meta Tratando el glaucoma de manera intensiva Abordaje terapéutico
TETRACICLINAS Y FENICOLES CLASIFICACION Y ESPECTRO
 CLASIFICACION Y ESPECTRO TETRACICLINAS: - DE ACCION CORTA: + CLORTETRACICLINA (AUREOMICINA): * FUE LA PRIMERA (1948). + OXITETRACICLINA. + TETRACICLINA. - DE ACCION LARGA: + MINOCICLINA. + DOXICICLINA.
CLASIFICACION Y ESPECTRO TETRACICLINAS: - DE ACCION CORTA: + CLORTETRACICLINA (AUREOMICINA): * FUE LA PRIMERA (1948). + OXITETRACICLINA. + TETRACICLINA. - DE ACCION LARGA: + MINOCICLINA. + DOXICICLINA.
PROFILAXIS ANTIFÚNGICA CON ITRACONAZOL INTRAVENOSO EN TRASPLANTE DE SANGRE DE CORDÓN UMBILICAL (TSCU). ANÁLISIS DE 20 PACIENTES ADULTOS
 PROFILAXIS ANTIFÚNGICA CON ITRACONAZOL INTRAVENOSO EN TRASPLANTE DE SANGRE DE CORDÓN UMBILICAL (TSCU). ANÁLISIS DE 20 PACIENTES ADULTOS. IMPLICACIÓN DE ENFERMERÍA Araceli Aineto García 1 ; Jose Antonio
PROFILAXIS ANTIFÚNGICA CON ITRACONAZOL INTRAVENOSO EN TRASPLANTE DE SANGRE DE CORDÓN UMBILICAL (TSCU). ANÁLISIS DE 20 PACIENTES ADULTOS. IMPLICACIÓN DE ENFERMERÍA Araceli Aineto García 1 ; Jose Antonio
IBANDRONATO INTRAVENOSO
 IBANDRONATO INTRAVENOSO en osteoporosis en mujeres posmenopáusicas con elevado riesgo de fractura. (Informe para la Comisión de Farmacia y Terapéutica del Hospital Universitario Central de Asturias) Fecha
IBANDRONATO INTRAVENOSO en osteoporosis en mujeres posmenopáusicas con elevado riesgo de fractura. (Informe para la Comisión de Farmacia y Terapéutica del Hospital Universitario Central de Asturias) Fecha
NUEVO ENFOQUE DEL CÁNCER DE MAMA EN PAÍSES DE BAJOS INGRESOS. Dra. Levitt Universidad de Oxford Presentado en SABCS 2011
 NUEVO ENFOQUE DEL CÁNCER DE MAMA EN PAÍSES DE BAJOS INGRESOS Dra. Levitt Universidad de Oxford Presentado en SABCS 2011 Copia portada presentacion AFROX Africa Oxford Cancer Foundation «Asociarse con los
NUEVO ENFOQUE DEL CÁNCER DE MAMA EN PAÍSES DE BAJOS INGRESOS Dra. Levitt Universidad de Oxford Presentado en SABCS 2011 Copia portada presentacion AFROX Africa Oxford Cancer Foundation «Asociarse con los
