+ HCO pH. Es el logaritmo negativo de la [H+] ph = - ( log [H+] ) ph = - ( log 40 x 10-9 ) ph = 7.4
|
|
|
- Inmaculada Prado Vera
- hace 8 años
- Vistas:
Transcripción
1 1 1
2 2 (48,/,%5,2È&,'2%$6( 58%e17255(6'Ë$= 3URIHVRU$VLVWHQWH)LVLRSDWRORJtD,QVWLWXWR&LHQFLDV%LRPpGLFDV8QLYHUVLGDGGH&KLOH 1HIUyORJR6HFFLyQ1HIURORJtD6HUYLFLRGH0HGLFLQD +RVSLWDO&OtQLFR8QLYHUVLGDGGH&KLOH,1752'8&&,Ï1 La concentración de protones libres [H + ], determina el estado ácido-base de cada compartimento celular. En condición normal se mantiene una [H + ] estable de 40 nanomoles/l, es decir 1 millón de veces menos que la concentración de la mayoría de los electrolitos como Na +, K +, Cl - etc., que están en rango milimolar. Cuando hay un cambio en la [H + ], las proteínas ganan o pierden H +, resultando en alteraciones en la distribución de sus cargas, su configuración molecular, y de su función. Un ejemplo conocido es la relación entre la [H + ] y la tasa de glicólisis, a menor [H + ] mayor producción de lactato. La concentración de protones también afecta la concentración plasmática de potasio y de calcio iónico; a mayor concentración de protones en el extracelular, mayor es la concentración extracelular de potasio, y mayor es el nivel de calcio iónico. 'HILQLFLRQHV 1.-Ácidos y bases. De acuerdo a la definición propuesta por Bronsted: Ácido: Es una sustancia que puede donar H + Base: Es una sustancia que puede aceptar H + Ej: HCl < --- > H + + Cl - H 2 CO 3 < --- > H HCO 3 Ácidos Bases 2.-pH. Es el logaritmo negativo de la [H+] ph = - ( log [H+] ) ph = - ( log 40 x 10-9 ) ph = Acidosis: Es un proceso que produce un exceso de protones libres. Cuando se demuestra en una medición sanguínea que el ph es menor de lo normal, se habla de DFLGHPLD. Puede ser de origen metabólico (caída en bicarbonato sérico), o respiratorio (aumento en pco 2 ) Tabla 4-1). 4.-Alcalosis. Es un proceso que disminuye la concentración de protones libres. Si se demuestra en la sangre un ph mayor de lo normal se habla de DOFDOHPLD. Puede ser de origen metabólico (aumento en el bicarbonato sérico), o respiratorio (disminución de la pco 2 ). 2
3 3 3DUiPHWURViFLGREDVHHQHOH[DPHQGHJDVHVDUWHULDOHV Cuando analizamos en la práctica clínica diaria un examen de gases arteriales nos encontraremos con los siguientes valores, que es necesario detallar, antes de avanzar en los trastornos ácido base. que es 40 nm, en la práctica se mide como ph = - log [ H + ], con un rango normal de 7,35 7,45 y un rango compatible con la vida de 6,8 7,8. 3UHVLyQ SDUFLDO GH &2 DUWHULDO S&2 Es el componente respiratorio del estado ácidobásico, en condiciones normales alcanza un valor de mmhg. &RQFHQWUDFLyQSODVPiWLFDGHELFDUERQDWR. Bicarbonato real: concentración de bicarbonato plasmática en una muestra de sangre sin que ésta se haya sometido a modificaciones externas (normalmente 24 ± 2 meq/l). Bicarbonato estándar: concentración de bicarbonato a pco 2 de 40 mmhg, una temperatura de 37 C y una presión barométrica de 760 mmhg, es decir el bicarbonato estándar informa sólo del componente metabólico. %DVH EXIIHU. Es la suma de todos los aniones sanguíneos con poder tampón: bicarbonato, proteinatos, oxihemoglobina, etc. (a pco 2 de 40 mmhg, 37 C, 760 mmhg). Es independiente de la pco 2 y tiene un valor normal de meq/l en sangre arterial. ([FHVRGHEDVH. Es la diferencia entre la base buffer real del paciente y la base buffer normal. Su valor normal es ± 2mEq/L. Un valor negativo por ejemplo 10 implica que faltan 10 meq/l de base para alcanzar un ph normal. Un valor positivo por ejemplo + 10 implica que sobran 10 meq/l de base para alcanzar un ph normal. &2 WRWDOHQHOSODVPD. Es la suma de todas las formas de CO 2 disuelto; ácido carbónico, bicarbonato, compuestos carbamino. Equivale en la práctica al valor del bicarbonato real mas 1-2 mmoles/l (VN mmoles/l plasma). $QLyQJDS Aniones no medibles (lactato, sulfatos y proteinatos como albúmina). Se mide a través de la diferencia entre la concentración plasmática de catión principal y los aniones principales del LEC: $* 1D &O +&2 Valor normal 12± 4 meq/l. No se considera al K +, Mg 2+, ni Ca 2+, pues existen aniones que normalmente los balancean como uratos. Es muy útil su determinación especialmente en el diagnóstico diferencial de las acidosis metabólicas. Hay casos en que puede estar falsamente disminuido como son la hipoalbuminemia, y el exceso de proteínas cargadas positivamente como ocurre en el Mieloma. En la alcalosis metabólica puede estar elevado sin que implique aparición de nuevos aniones. 3
4 4 TABLA 1 VALORES ACIDO-BASE NORMALES ph [ H + ] pco 2 [ HCO - 3 ] nanoeq/l mmhg meq/l Arterial 7,37 7, Venoso 7,32 7, ),6,2/2*,$$&,'2%$6( 1. Tampones físico-químicos del LEC y del LIC 2. Control de la pco 2 sanguínea a través de la ventilación alveolar. 3. Control de la concentración de bicarbonato plasmático a través de cambios en la excreción renal. 7DPSRQDPLHQWRItVLFRTXtPLFRGHO/(&\GHO/,&. Es el mecanismo inicial, es rápido, se produce tanto a nivel intracelular como extracelular. Si no existiera este mecanismo los ácidos fijos producidos diariamente (50-80 meq) harían bajar el ph a valores cercanos a 3,0 un valor absolutamente incompatible con la vida. Los buffers del compartimento intracelular son cuantitativamente más importantes, que los del extracelular, pero no son bien conocidos. Además del sistema de la hemoglobina, los más importantes son el del fosfato disódico/fosfato monosódico y el de las proteínas intracelulares (imidazol). Los H + penetran en las células intercambiándose por Na +, K + ó acompañándose de Cl -. Este proceso tarda alrdedor de 2 a 4 horas. En el líquido extracelular (LEC) los tampones que existen son: -Sistema bicarbonato/co 2, en el plasma y líquido intersticial. -Proteínas plasmáticas. -Fosfato disódico/fosfato monosódico, en plasma y líquido intersticial. El principal tampón extracelular es el sistema bicarbonato/co 2. La ecuación general que describe este sistema es: CO 2 + H 2 O < --- > H 2 CO 3 < --- > H + + HCO 3 - El H 2 CO 3 está en una cantidad mínima por lo tanto se puede 4
5 5 sacar de la ecuación: CO 2 + H 2 O < --- > H + + HCO 3 - En condiciones normales, el sistema bicarbonato/co 2 representa el 75% de la capacidad buffer total de la sangre. En este sistema los parámetros ácido básico se relacionan a través de ecuaciones simples. [ H + ] = 24* (pco 2 /[HCO 3 - )] Ecuación de Henderson ph = 6,1 + log [ HCO 3 - )]/(0,03* PCO 2) Ecuación de Henderson-Hasselbach Dado que el bicarbonato normal del plasma arterial es de 24 mmol/l, y la pco 2 arterial normal es de 40 mmhg, el ph de la sangre arterial normal será: ph = log (24/1.2) = = 7.4 El tamponamiento más efectivo de un sistema buffer ocurre cuando el pka del sistema es similar al ph de la solución a tamponar. El pka del sistema tampón bicarbonato/co 2 es 6.1, es decir 1.3 unidades menos que el ph normal que es 7.4, esto se debe a que la relación entre la sal (bicarbonato) y el ácido (pco 2 * 0.03) es 20/1. Pese a que en términos puramente químicos el tampón bicarbonato no sería un buen buffer, al ser su componente ácido (CO 2 ) gaseoso y muy difusible, permite una modificación muy rápida de sus niveles mediante la respiración. Un aumento de la ventilación baja la PCO 2 y una disminución de la ventilación aumenta la PCO 2. Por lo tanto si el bicarbonato tampona un exceso de H +, se produce un aumento de la ventilación minuto alveolar lo que baja la PCO 2 y hace más efectivo al sistema. Además el sistema tampón bicarbonato permite que se regule también la concentración de bicarbonato a través del manejo renal de éste. Si se gasta bicarbonato en tamponar protones, el riñon es capaz de regenerarlo. Todo lo anterior hace que el sistema tampón bicarbonato/co 2 en el organismo completo funcione adecuadamente. $MXVWHVYHQWLODWRULRV&RQWUROGHODS&2 VDQJXtQHDDWUDYpVGHODYHQWLODFLyQDOYHRODU. En condiciones normales todos los ácidos volátiles producidos han de ser eliminados por el pulmón. El principal ácido volátil es el CO 2, produciéndose alrededor de mmoles/minuto, es decir a mmoles/día. 5
6 6 El CO 2 tisular, procedente del metabolismo, se mueve hacia el plasma, donde tiene las siguientes posibilidades: -Disolverse (sólo 5%) -Hidratarse a bicarbonato (sólo 1%) -Ingresar al glóbulo rojo, donde una parte se disuelve (5%), otra se hidrata a bicarbonato (63%), debido a que en el GR hay abundante anhidrasa carbónica. Otra parte se une a la Hb formando compuestos carbamino (21%). La producción contínua de bicarbonato dentro del hematíe hace que su concentración aumente progresivamente. Al alcanzar cierto nivel sale al plasma, intercambiándose por Cl -, por lo tanto parte del CO 2 se transporta en la sangre venosa en forma de bicarbonato plasmático. En el pulmón debido a su gran capacidad de difusión, el CO 2 atraviesa la membrana alvéolocapilar y se elimina con el aire espirado. A mayor pco 2 y/o a menor po 2 arterial, aumenta la ventilación minuto. 0DQHMR UHQDO GH iflgrv ILMRV &RQWURO GH OD FRQFHQWUDFLyQ GH ELFDUERQDWR SODVPiWLFR D WUDYpVGHFDPELRVHQODH[FUHFLyQUHQDO 5HDEVRUFLyQ GHO ELFDUERQDWR ILOWUDGR. Es lo primero que debe ocurrir para evitar la depleción de bicarbonato. Alrededor del 90% del bicarbonato filtrado es reabsorbido en el túbulo proximal, lo que ocurre a través de la combinación del hidrógeno secretado con el bicarbonato filtrado y la formación de ácido carbónico en el lumen tubular. Bajo la influencia de la anhidrasa carbónica del ribete en cepillo celular, el H 2 CO 3, se disocia en CO 2 y H 2 O que serán reabsorbidos. Este proceso remueve bicarbonato de lumen, el cual regresa a la circulación sistémica vía un cotransportador Na + -3HCO 3 - en la membrana basolateral de las células tubulares proximales. La reabsorción de bicarbonato reclama el bicarbonato filtrado, pero no participa en la excreción de la carga ácida diaria (Figura 1). 6
7 7 )LJXUD. 5HDEVRUFLyQGHELFDUERQDWRHQHOW~EXORSUR[LPDO La secreción de hidrogeniones desde la célula al lumen, ocurre fundamentalmente a través de un intercambiador Na + - H + ubicado en la membrana apical. Los protones se combinan con el bicarbonato filtrado formándose H 2 CO 3 el cual pasa a CO 2 y H 2 O vía la anhidrasa carbónica luminal ($&,9). El CO 2 ingresa a la célula tubular proximal especialmente a través de aquaporina-1 (60%), combinándose con agua, lo que a través de la anhidrasa carbónica intracelular ($&,,) formará protones que serán secretados y bicarbonato que se reabsorberá. Cada protón secretado genera un ión bicarbonato dentro de la célula, el cual es regresado hacia el capilar peritubular a través del cotransportador Na + -3HCO - 3. Si el protón secretado hacia el lumen se combinó con bicarbonato filtrado, el proceso final lleva a reabsorción del bicarbonato filtrado. Los niveles de CO 2 y de bicarbonato en la membrana basolateral pueden regular este proceso. Como se aprecia en la figura el túbulo proximal es además el sitio donde se sintetiza amonio a partir de glutamina. Si el amonio es eliminado efectivamente por la orina significará ganancia de bicarbonato. 5HJHQHUDFLyQ GHO ELFDUERQDWR JDVWDGR HQ WDPSRQDU OD FDUJD GLDULD GH iflgrv ILMRV. Diariamente además de reabsorber el bicarbonato filtrado, el riñón debe excretar la carga de ácidos fijos producidos en el organismo (1mEq/kg peso). Si esto no ocurriera, el organismo se depletaría totalmente de bicarbonato. Los ácidos fijos que provienen fundamentalmente de metabolismo proteico constituyen una carga diaria de 50 a 80 meq, son inicialmente tamponados por una cantidad igual de bicarbonato plasmático y a nivel del riñón se excretan en la forma de amonio y acidez titulable, regenerándose el bicarbonato utilizado durante el tamponamiento. No ocurre recuperación del bicarbonato ocupado, hasta que se excreta el H + libre. 7
8 8 /RVPHFDQLVPRVUHQDOHVUHVSRQVDEOHVGHOPDQHMRGHODFDUJDGLDULDGHiFLGRVILMRVLQFOX\HQ 6HFUHFLyQWXEXODUGHSURWRQHV. En túbulo proximal y en asa ascendente de Henle existe un intercambiador Na + -H + apical, cuya energía proviene de la bomba Na + -K + -ATPasa basolateral, que mantiene una concentración baja de sodio intracelular (Figura 1). En el túbulo colector la secreción de hidrogeniones es mediada por una bomba H + - ATPasa que se ubica en la membrana apical de las células intercaladas (Figura 2). $FLGH]WLWXODEOH Los ácidos débiles filtrados en el glomérulo pueden actuar como tampones en la orina. El fosfato monobásico (HPO 4 2 -) es el más efectivo y prevalente en el fluido tubular, funcionando a través de la siguiente reacción (con un pka de 6,8): HPO H + H 2 PO 4 -. A medida que el ph del fluido tubular cae a 5,8 casi todo el HPO 4 2- habrá sido convertido a H 2 PO 4 -. Cada protón secretado que se combina con un ácido titulable, recupera un bicarbonato hacia la circulación, que reemplazará el bicarbonato consumido durante el taponamiento. El poder total de tamponamiento de estos ácidos débiles es igual a la cantidad de base que debe ser agregada para llevar el ph urinario a 7,4 (por esto se llama acidez titulable). La acidez titulable no puede aumentar fácilmente frente a cargas ácidas, pues el proceso está limitado por la cantidad de buffer filtrado. Este mecanismo normalmente da cuenta de la excreción de alrededor de 10mEq de ácidos día. Es importante mencionar que en el caso de una cetoacidosis diabética el β- hidroxibutirato cuyo pk a es 4,8 puede actuar como un efectivo buffer en el nefrón distal pudiendo aumentarse la excreción ácida vía acidez titulable hasta 50 meq/día. ([FUHFLyQ GH DPRQLR Constituye la mayor respuesta adaptativa a una carga ácida. En condiciones normales la excreción de amonio es meq día, pero puede aumentar hasta 300 meq día. La mayoría del amonio se genera dentro de las células tubulares proximales a través del metabolismo de la glutamina proveniente del hígado (figura 2). )LJXUD Formación de glutamina en el hepatocito. 8
9 9 En el riñon la glutamina se metaboliza a α-cetoglutarato generando 2 moléculas de bicarbonato que regresan a la circulación sistémica. En el túbulo proximal el amonio deja la célula directamente a través de un intercambiador Na + + -NH 4 (Figura 1). Este amonio fluye por el lumen del túbulo proximal, asa delgada descendente, hasta llegar al asa gruesa de henle donde se transporta a través del cotransportador Na-K-2Cl - hasta el intersticio medular, donde pasa a NH 3. En el túbulo colector el NH 3 del intersticio tubular difunde hacia el lumen, donde al unirse a un protón secretado por la célula intercalada alfa formará amonio que queda atrapado en el lumen (figura 3). Si el amonio formado en el túbulo proximal no se excretara a la orina y retornara a la circulación sistémica, su metabolismo en el hígado a urea consumiría el bicarbonato que se había regenerado. )LJXUD. Secreción de protones en el nefrón distal. Célula intercalada tipo alfa. La secreción tubular de protones ocurre principalmente en las células intercaladas alfa del túbulo colector cortical, y colector medular externo. La secreción de protones se produce primariamente vía una bomba H + - ATPasa ubicada en la membrana apical. Una bomba H + - K + - ATPasa también está presente pero tendría un rol mayor en la reabsorción de potasio que en la secreción de protones. Los protones secretados al lumen se combinan con el amoníaco (NH 3 ) que viene desde el intersticio peritubular, para formar amonio (NH 4 + ), el cual queda atrapado en el lumen y se eliminara por la orina. Los protones también pueden combinarse con HPO 4 2- para formar acidez titulable. /DH[FUHFLyQQHWDGHiFLGRVHQRULQD(1$ = Acidez Titulable + NH HCO 3-9
10 10 A modo de resumen de la excreción renal de ácidos fijos se puede tomar como ejemplo el ácido sulfúrico proveniente del metabolismo de las proteínas. El ácido sulfúrico destruye bicarbonato de sodio en el LEC, se crea entonces sulfato de sodio, el cual llega al riñón y filtra como sulfato de sodio excretándose finalmente en la orina como sulfato de amonio. Al excretarse sulfato de amonio se eliminan protones libres, permitiendo que el bicarbonato de sodio regrese a la circulación sistémica. Si todo el sistema funciona adecuadamente la concentración plasmática de bicarbonato se mantiene normal. 75$ (1(/0(7$%2/,602$&,'2%$6( $&,'26,60(7$%Ï/,&$ 'HILQLFLyQ. Se refiere a un proceso de exceso de protones libres derivados de un exceso de ácidos fijos. Este proceso lleva a una disminución del bicarbonato plasmático y acidemia. La acidemia resultante estimula la ventilación alveolar y conduce a una hipocapnia secundaria característica de este trastorno. Por cada 1 meq que baja la concentración de bicarbonato la pco 2 baja 1.2 mm Hg. 6tQWRPDV\VLJQRV 6LVWHPDUHVSLUDWRULRHiperventilación, disnea, disminución de la fuerza muscular, fatiga respiratoria. 6LVWHPDFDUGLRYDVFXODU. Deterioro de la contractibilidad miocárdica con caída del gasto cardíaco, disminución de la presión arterial y disminución del flujo hepático y renal, sensibilización por arritmias de reentrada como fibrilación ventricular. 0HWDEyOLFRVAumento de las demandas metabólicas, resistencia a la insulina, inhibición de la glicólisis anaeróbica, disminuye la síntesis de ATP, hiperkalemia, aumento de la degradación proteica. 6LVWHPDQHUYLRVRFHQWUDO Metabolismo alterado, inhibición de la regulación de volumen celular, compromiso de conciencia progresivo hasta el coma. (VTXHOHWR Osteomalacia y fracturas (en especial con acidosis crónica). (WLRORJtDV 10
11 11 TABLA 2 MAYORES CAUSAS DE ACIDOSIS METABOLICA 1.-Aumento en el ingreso de ácidos fijos - Cetoacidosis - Acidosis láctica - Ingestión exógena - aspirina - etilenglicol (solventes y anticongelantes) - metanol (alcohol de madera) - cloruro de amonio 2.-Disminución en la excreción de ácidos - Falla renal - Acidosis tubular renal distal tipo 1 - Acidosis tubular renal tipo 4 (hipoaldosteronismo) 3.-Pérdida de bicarbonato - Diarrea - Acidosis tubular renal proximal (tipo 2) 5HODFLyQ QRUPDO HQWUH +&2 \ S&2 HQ DFLGRVLV PHWDEyOLFD. Cuando se desarrolla una acidosis metabólica, el evento primario es la acumulación de ácidos fijos con la consiguiente caída en la concentración de bicarbonato. Esta acidosis a nivel del tronco encefálico estimula el centro respiratorio, el paciente hiperventila produciéndose una disminución de pco 2. Al producirse una acidosis metabólica siempre debemos preguntarnos si la pco 2 es adecuada para la caída en el bicarbonato. Existen varias fórmulas, siendo las más utilizadas las siguientes : 1.-pCO 2 esperado = 1,5 x [ HCO 3 ] + 8 (rango de ± 2) 2.-Por cada 1 meq/l que baja el bicarbonato la pco 2 debe bajar 1.2 mm Hg 8QHMHPSORSUiFWLFR. Una persona sana que a consecuencia de una diarrea aguda presenta una disminución del bicarbonato a 10mEq/L, debiera presentar una pco 2 de ± 23 mmhg. Si el mismo paciente tuviera una enfermedad pulmonar crónica, sus pulmones no podrían responder apropiadamente y la pco 2 no disminuiría apropiadamente. Si esta diarrea se produjera en una persona sin enfermedad pulmonar, a través de una enterotoxina, el centro respiratorio se estimularía tanto por la acidemia como por la toxina, disminuyendo pco 2 a niveles bajo lo esperable. Tendríamos una acidosis metabólica con una alcalosis respiratoria sobreagregada. Por lo tanto, para cualquier grado de disminución en el bicarbonato plasmático hay un grado predecible de compensación respiratoria, que si no se da implica un trastorno respiratorio sobregregado. $QLyQJDS. La siguiente pregunta a realizar en una acidosis metabólica es cuánto es el valor del anión gap. 11
12 12 AG = Natremia - (bicarbonatemia + cloremia) VN 14 ± 2 Desde un punto de vista diagnóstico, el cálculo de este parámetro es extremadamente útil para acercarse a la etiología generadora de acidosis. $FLGRVLVPHWDEyOLFDFRQDQLyQJDSDXPHQWDGR: La titulación de los H + libres por bicarbonato lleva a que se acumulen los aniones provenientes de los ácidos no medibles (ej. lactato, acetoacetato, etcétera) (Tabla 3). TABLA 3 ACIDOSIS METABOLICA CON AG Etiología Cetoacidosis Acidosis láctica Falla renal Rabdomiolisis Ingesta de metanol Ingesta de etilenglicol Salicilatos Tolueno Paraldehído Aniones circulantes β-hidroxibutirato, acetoacetato lactato, piruvato Sulfato, fosfato, urato, hipurato Fosfato, otros Formato Glicolato, oxalato Salicilato, lactato, cetonas Hipurato Acetato $FLGRVLVPHWDEyOLFDFRQDQLyQJDSQRUPDO: También se le llama acidosis hiperclorémica. El exceso HCl o bien la pérdida de bicarbonato, lleva a nivel renal a retención de CI - debido a su mayor concentración tubular en relación al bicarbonato. En el fondo se reemplaza el HCO - 3 por CI - no habiendo entonces cambios en la suma total de los aniones medidos (ej.diarreas) (Tabla 4). 12
13 13 TABLA 4 ACIDOSIS METABOLICA CON AG NORMAL (ó hiperclorémicas) Con K + elevado Con K + normal o bajo Infusión de HCI Desórdenes gastrointestinales - Hiperalimentación - Diarrea, fístulas pancreáticas, intestinales o biliares - NH 4 CI, colesteramina HCI Post-hipocapnia Hipoaldoteronismo Derivaciones ureterales - Ureterosigmoidostomía - Ileo vesical Acidosis tubular renal - Proximal - Distal -Recuperación de una cetoacidosis -Insuficiencia renal crónica en etapa temprana *DS RVPRODU. Corresponde a la osmolaridad real medida por un osmómetro menos la osmolaridad calculada (2Na + + Glicemia /18 + BUN/2,8). Su valor se encuentra elevado en pacientes con acidosis metabólica por intoxicaciones con metanol o etilenglicol, como también en la falla renal crónica avanzada (no por la azotemia, sino por otros compuestos orgánicos urémicos acumulados). (MHPSORVGHDFLGRVLVPHWDEyOLFDFRQ$*DXPHQWDGR\VXPDQHMR $FLGRVLV XUpPLFD. A medida que la VFG cae, el balance de protones es mantenido por un aumento en la síntesis y excreción de amonio por nefrón remanentes, el problema es que cada vez son menos los nefrones funcionantes, lo que limita la excreción neta de ácidos. Cuando la VFG es menor de 40 ml/min se limita la excreción neta de ácidos por la falta de amonio disponible como buffer. Esto resulta en una progresiva acidosis metabólica con anión gap normal. Parte de la carga ácida que es retenida cada día hace bajar el bicarbonato un poco, sin embargo, la mayor parte de los ácidos retenidos son tamponados por el hueso, lo que contribuye importantemente a la osteodistrofia del enfermo renal. Cuando la VFG cae por debajo de 30mL/min (equivalente a una pérdida de ± 80% de la masa renal), disminuye la excreción de fosfatos y entonces se agrega una acidosis con retención de aniones no medibles (acidosis con anión gap aumentado). El anión gap en la falla renal avanzada 13
14 14 es, sin embargo, raramente mayor de meq/l. Si el valor es mayor de 20 meq/l se debe pensar en otra causa de acidosis metabólica sobreagregada. Debido a la osteodistrofia renal, la destrucción proteica por acidosis, y el daño renal mayor que produce el aumento de la producción de amonio tubular, se recomienda usar bicarbonato para corregir la acidosis metabólica de la falla renal desde etapas tempranas. $FLGRVLVOiFWLFD. El ácido láctico se deriva del metabolismo del ácido pirúvico en una reacción catalizada por la enzima lactato deshidrogenada (LDH). Normalmente es producido en músculo, cerebro, piel y glóbulos rojos a una tasa de mmol/kg peso. La extracción ocurre fundamentalmente en el hígado y en un menor grado en la corteza renal donde pasará a glucosa vía gluconeogénesis. El equilibrio entre producción y utilización de lactato permite mantener una concentración estable de lactato de 1-2 meq/l. La patogénesis de este trastorno incluye entonces sobreproducción de lactato, subutilización de éste o ambos. Durante la hipoxia casi todos los tejidos liberan lactato a la circulación, incluso el hígado puede convertirse en un consumidor primario a un productor neto. &HWRDFLGRVLV GLDEpWLFD. La combinación de deficiencia de insulina más exceso de glucagón conduce a un aumento de la síntesis hepática de cetoácidos, especialmente β-hidroxibutirato y en menor grado acetoacetato. Dos factores se requieren para aumentar la producción de cetoácidos: -Aumento de la llegada de ácidos grasos libres al hígado. Esto se da por aumento de la lipólisis al haber falta de insulina. -El metabolismo hepático está alterado, de forma que estos ácidos grasos libres en lugar de ir a la síntesis de triglicéridos (evento citosólico), se metabolizan a cetoácidos (proceso mitocondrial). La tasa limitante en la síntesis de cetoácidos es la entrada de acetil-coa a la mitocondria, proceso dependiente de la enzima carnitin-palmitoil-transferasa, actividad que es aumentada por el glucagón en exceso. El tratamiento debe estar dirigido a corregir el déficit de volumen extracelular y administrar insulina &HWRDFLGRVLV DOFRKyOLFD. Puede inducir una severa hipobicarbonatemia, que se corrige rápidamente al detener la ingesta de etanol y administrando nutrientes. El tratamiento con suero glucosado estimula la producción de insulina y frena la producción de glucagón, promoviendo el metabolismo de los cetoácidos y regenerándose el bicarbonato.,qwr[lfdflyq VDOLFtOLFD La aspirina (acido acetilsalicílico) es convertida rápidamente en el organismo a ácido salicílico. El rango terapéutico es mg%, produciéndose intoxicación con niveles de mg%. Hay dos mayores trastornos ácido-básicos: alcalosis respiratoria debido a estimulación directa del centro respiratorio y acidosis metabólica debido a interferencia con el metabolismo oxidativo, que conduce a la acumulación de ácidos orgánicos como lactato y cetoácidos. Los signos y síntomas incluyen: Tinitus, vértigo, náuseas. En algunos pacientes puede ocurrir distrés respiratorio presumiblemente del efecto químico de la aspirina en los pulmones. A nivel del sistema nervioso central se observa confusión y en casos de intoxicación severa convulsiones y coma. 14
15 15,QWR[LFDFLyQ SRU PHWDQRO \ HWLOHQJOLFRO. El metanol (alcohol de madera) y el etilenglicol (encontrado en anticongelantes), pueden producir severa acidosis con AG aumentado, por la acumulación de metabolitos tóxicos (Formaldehído, ácido fórmico, lactato y cetoácidos para metanol. Glicolato más lactato para el etilenglicol). Se caracteriza por confusión, convulsiones y coma. A nivel ocular hay diplopia y papilitis causada por el formaldehído y el ácido fórmico. Además hay náuseas, vómitos y dolor abdominal, existiendo el riesgo de pancreatitis aguda severa (especialmente por metanol). $FLGRVLVPHWDEyOLFDFRQDQLRQJDSQRUPDO $SUR[LPDFLyQGLDJQyVWLFD Luego de realizar adecuadamente la anamnesis y el examen físico, el paso siguiente en la acidosis hiperclorémica es ver si la etiología es renal (acidosis tubular renal) o extrarrenal (ej. diarrea). Para esto se utiliza el anion gap urinario. Cuando hay una acidosis metabólica hiperclorémica extrarrenal, el riñon funcionará bien y el amonio urinario aumentará al máximo posible. En una acidosis metabólica hiperclorémica producida por un defecto en la acidificación renal, la producción de amonio urinario estará disminuida. El anion gap urinario es: (Na + + K + ) (Cl - + HCO 3 - ) Cuando existe una acidosis metabólica hiperclorémica con anion gap urinario positivo, la forma más simple de objetivar si la acidosis tubular renal es proximal o distal es en base al ph urinario. En el caso de la distal, no se logra bajar el ph de la orina a menos de 5.5. $OJXQRVHMHPSORVGHDFLGRVLVPHWDEyOLFDFRQ$*QRUPDO $FLGRVLVSRUSpUGLGDVJDVWURLQWHVWLQDOHVGHELFDUERQDWR 'LDUUHD. El agua fecal tiene una alta concentración de bicarbonato, de manera que una diarrea profusa o una diarrea prolongada puede resultar en acidosis metabólica. La acidosis que se produce es hiperclorémica y acompañada de deshidratación. Si hay depleción de volumen e hipopotasemia, debe manejarse con suero salino fisiológico y potasio. Debe administrarse bicarbonato cuando se trate de acidosis aguda y el ph sea menor de 7,2 en caso de acidosis crónica con ph menor de 7,35. 8UHWHURVLJPRLGRVWRPtD. Cuando la orina es desviada hacia el colon, el cloruro de la orina se reabsorbe intercambiándose por bicarbonato el cual se pierde en las deposiciones. $FLGRVLVWXEXODUUHQDO 'LVWDOFOiVLFDRWLSR, Se produce una incapacidad para disminuir el ph bajo 5,5. Los defectos celulares que pueden estar implicados son: falla de la bomba h+-atpasa apical (la gran mayoría de los casos), normalidad en el intercambiador basolateral CL-+HCO3-, falla de la anhidrasa carbónica citosólica, aumento de la permeabilidad de la membrana apical o de las uniones 15
16 16 intercelulares con retrodifusión de los protones secretados al lumen (Figura 4-2). Este tipo de acidosis se sospecha en pacientes con acidosis metabólica y ph urinario inapropiadamente alto (sobre 5,5), incluso luego de una carga ácida. Frecuentemente se asocia a trastornos como estados hiperglobulémicos, nefrocalcinosis, síndrome de Sjögren, drogas o toxinas (tolueno, anfotericina B, litio). El tratamiento consiste en terapia alcalina oral, en alrededor de 1mEq base/kg/día. 'LVWDOWLSRKLSHUNDOLpPLFDRWLSR,9 Representa la forma más común encontrada en adultos. Se produce una disfunción generalizada de túbulo colector que incluyen una disminución de la reabsorción de sodio y excreción de potasio por las células principales del túbulo colector, con la consiguiente menor secreción de protones por las células intercaladas. La hiperkalemia causa además menor excreción de amonio, lo que también colabora en la generación de acidosis metabólica. Se debe a un defecto en la producción o en la acción de la aldosterona (síndrome de hipoaldosteronismo hiporreninémico). Entre las etiologías en que hay deficiencia de aldosterona tenemos: hiporreninemia, falla en la conversión de angiotensina I a II, síntesis anormal de aldosterona. Aquéllas con resistencia a aldosterona pueden incluir bloqueo de receptor mineralocorticoideo, destrucción de las células blanco como ocurre en las nefropatías túbulointersticiales, interferencia con el canal de sodio de la bomba sodio-potasio basolateral, y aumento de la permebalidad al Cl -, la acidosis renal distal tipo IV se asocia con frecuencia a las siguientes situaciones clínicas: nefropatía diabética, SIDA, nefropatías intersticiales, nefritis lúpica, uropatía obstructiva, post-transplante renal, uso de AINEs y de IECA, uso de heparina (disminuye la producción de aldosterona) No se debe restringir el aporte salino de forma de lograr una buena llegada de sodio al túbulo distal. En los casos de déficit de aldosterona se utiliza fluohidrocortisona en dosis de 0,1-0,2 mg/día. 3UR[LPDOWLSR,,. Se caracteriza por una alteración en la reabsorción proximal de bicarbonato, que lleva inicialmente a pérdida de bicarbonato por la orina. El proceso se estabiliza una vez que se alcanza el nuevo umbral renal para el bicarbonato. Dicho de otra forma el paciente que normalmente perdía bicarbonato a una concentración plasmática de 26 meq/l ahora lo pierde a un valor menor por ejemplo 16 meq/l, cuando el nivel plasmático se llegue a 16 meq/l todo el bicarbonato filtrado será reabsorbido, alcanzándose un nuevo equilibrio en el que el paciente es capaz de eliminar la carga diaria de ácidos, pero con un nivel de bicarbonato plasmático menor. Al ser capaces de eliminar la carga diaria de ácidos fijos, no se presentan complicaciones de la acidosis crónica como pérdida ósea y proteólisis muscular. Este desorden habitualmente se observa en niños con síndrome de Fanconi, pero puede ocurrir también en enfermedades como mieloma, amiloidosis, síndrome nefrótico, toxicidad por metales pesados, toxicidad por tetraclinina, bencina, rechazo al trasplante renal, cistinosis y enfermedad de Wilson. El tratamiento es difícil pues se necesitan grandes cantidades de bicarbonato (el déficit puede ser meq/kg/día). Los niños que presentan acidemia siempre deben ser tratados por el riesgo de trastornos en el crecimiento. Muchos adultos, sin embargo, son asintomáticos y no requieren terapia. 16
17 17 $/&$/26,60(7$%Ï/,&$ Es una de las anormalidades ácido-base más frecuentemente encontradas en la práctica clínica. Se define como una elevación primaria de la concentración plasmática de bicarbonato. El aumento del ph sanguíneo disminuye la ventilación alveolar conduciendo a hipercapnea secundaria, característica de este trastorno. Se ha estimado que la pco 2 aumenta alrededor de 0,7 mmhg por cada meq/l que aumenta el bicarbonato. Las etiologías generadoras de este trastorno, pueden dividirse en alcalosis FORUXURVHQVLEOHV y FORUXURUHVLVWHQWHV (Tabla 5). 6LJQRVVtQWRPDV\FRQVHFXHQFLDVDGYHUVDVGHODDOFDORVLV (Tabla 5), La alcalemia cuando es severa (ph>7,6) puede comprometer la perfusión cerebral y miocárdica al causar vasoconstricción arteriolar (un efecto más intenso en la alcalosis respiratoria que en la metabólica). Las anormalidades neurológicas incluyen: cefalea, letargia, delirio, tetania, convulsiones y estupor, explicados en parte también por la hipocalcemia iónica. La alcalemia también predispone al paciente a arritmias supraventriculares, y ventriculares, especialmente en pacientes con enfermedad cardiaca de base. La alcalemia deprime la respiración causando hipercapnea e hipoxemia, especialmente importante en pacientes con compromiso de la ventilación. Respecto de esto último incluso una alcalemia moderada puede frustar el intento de retirar a un paciente del ventilador mecánico. Puede observarse además hipokalemia especialmente prominente en la alcalosis metabólica, apareciendo riesgo de intoxicación digitálica, debilidad, poliuria. La alcalemia también estimula la glicólisis anaeróbica aumentando la producción de cetoácido y ácido láctico. La alcalemia aguda induce menor liberación de oxígeno desde la hemoglobina con la consiguiente hipoxia tisular, efecto que no se ve en la alcalemia crónica debido al aumento del 2,3 DPG en los glóbulos rojos. )LVLRSDWRORJtD Dos preguntas cruciales deben realizarse frente a un paciente con alcalosis metabólica: D FXiO HV OD IXHQWH GHO H[FHVR GH iofdol PHFDQLVPRV GH JHQHUDFLyQ. Al responder esta pregunta se encuentra el evento primario generador del aumento de bicarbonato plasmático. 17
18 18 TABLA 5 CAUSAS DE ALCALOSIS METABÓLICA Cloruro sensibles Cloruro resistentes 3pUGLGDVJDVWURLQWHVWLQDOHVGHiFLGRV&RQKLSHUWHQVLyQDUWHULDO Vómitos, succión gástrica Hiperaldosteronismo primario y secundario Diarrea de Cl - congénita Síndrome de Cushing Adenoma velloso del colon Hipertensión renovascular Exceso de mineralocorticoides exógenos Síndrome de Liddle 3pUGLGDUHQDOGHiFLGRV Ingestión de regaliz Diuréticos de asa y distales Estado post-hipercapnico &RQQRUPRWHQVLyQ Penicilinas Síndrome de Bartter Citrato Depleción severa de potasio Administración de bicarbonato exógeno Hipercalcemia Kayexalate en exceso E 4Xp IDFWRUHV SHUSHW~DQ HO DXPHQWR GHO ELFDUERQDWR SODVPiWLFR PHFDQLVPRV GH PDQWHQFLyQ. Respondiendo a esta pregunta se comprenden los eventos fisiopatológicos que mantiene la alcalosis metabólica. La compensación renal de la alcalosis metabólica debiera ser un aumento de la excreción de bicarbonato. En personas sanas con un funcionamiento renal adecuado es virtualmente imposible aumentar el bicarbonato plasmático en más de 2-3 meq/l, luego de una carga alcalina incluso de meq/día por 2 semanas, debido a la bicarbonaturia que se produce. De esta forma la persistencia de la alcalosis metabólica requiere de alguna anormalidad concomitante. Los principales mecanismos que explican la mantención de la alcalosis metabólica son: 1.-Depleción de Cl - 2.-Contracción de volumen extracelular 3.-Depleción de K + 4.-Hipercapnea compensatoria. 5.-Hiperaldosteronismo La depleción de Cl - (ej.: vómitos ) induce menor secreción de bicarbonato por las células intercaladas tipo β del túbulo colector (son células que poseen el intercambiador Cl - / HCO - 3 en la membrana apical por lo que reabsorben Cl - y secretan bicarbonato). Al llegar menor cantidad de 18
19 19 Cl - a esta zona se secreta menos bicarbonato, explicándose la mantención de la alcalosis frente a depleción severa de Cl -. La hipovolemia además del efecto de inducir hiperaldosteronismo con la consecuente mayor excreción de protones y potasio distal, aumenta la reabsorción del bicarbonato de sodio proximal, produciéndose también una disminución del aporte de Cl - al túbulo colector. La depleción de potasio entre otros efectos lleva a mayor secreción de protones acoplados con reabsorción de potasio en células intercaladas tipo alfa (Figura 2), y aumento de la síntesis de amonio. La hipercapnea al aumentar la pco 2 en células tubulares proximales e intercaladas tipo alfa, favorece la secreción de protones. En el caso de la alcalosis Cl - resistente los mecanismos implicados en la mantención son principalmente: un exceso de mineralocorticoides y la depleción de K+. El exceso de mineralocorticoides lleva a una mayor reabsorción de sodio por las células principales del túbulo colector, en conjunto a una mayor secreción de K + y H +. 'LDJQyVWLFRGLIHUHQFLDO)LJXUD La medición del cloruro urinario ayuda a distinguir entre la alcalosis Cl- sensible y la Cl - resistente. La virtual ausencia de Cl- (concentración menor de 10 meq/l), indica una significativa depleción de Cl -. La medición de la concentración de potasio urinario ayuda aún más en el diagnóstico diferencial. Con la excepción de la fase diurética del uso de diuréticos de asa y distales, al tener Cl - y K + elevado en la orina durante una alcalosis metabólica se asocia a exceso de mineralocorticoides. -Vómitos, succión gástrica Menor de -Fase post diurética 10 meq/l -Fase post-hipercápnica &O XULQDULR -Adenoma velloso colon -Diarrea congénita de Cl- -Post carga alcalina Mayor de 20 meq/l.xulqdulr Menor de -Abuso de laxantes 20 meq/l -Depleción severa de potasio -Fase diurética diuréticos de asa y distales -Sindrome de Bartter y Gitelman -Hiperaldosteronismo primario Mayor de -Hipertensión maligna,y renovascular 30 meq/l -Hiperreninismo primario -Sindrome de Cuhing 19
20 20 -Mineralocorticoides exógenos -Sindrome de Liddle Figura 4.-Electrolitos urinarios en el diagnóstico diferencial de la alcalosis metabólica. 7UDWDPLHQWR GH OD DOFDORVLV PHWDEyOLFD.El manejo efectivo de este trastorno requiere comprender la fisiopatología subyacente. Los esfuerzos terapéuticos se deben enfocar a eliminar o controlar los procesos generadores del exceso de bicarbonato, y en segundo lugar, interrumpir los mecanismos de mantención. Sólo en caso de alcalosis metabólica severa en que se necesita una corrección rápida se usa infusión de HCI. $&,'26,65(63,5$725,$ La acidosis respiratoria o hipercapnea primaria es un disturbio ácido-base iniciado por un aumento en la pco 2 que resulta de una disminución en la ventilación alveolar. La hipercapnea lleva a aumento agudo en el bicarbonato plasmático (5-10 minutos) que se origina por el tamponamiento tisular. Al aumentar la pco 2 difunde CO 2 y H 2 O al interior de las células, donde se genera H 2 CO 3, el cual se disocia a H + que serán tamponados por las proteínas celulares o hemoglobina en glóbulos rojos y HCO - 3 que difunde fuera de la célula elevando el bicarbonato plasmático. Esta compensación aguda es aproximadamente de 1meq/L por cada 10 mmhg que se eleva la pco 2. Cuando la hipercapnea es sostenida se produce un ajuste renal que aumenta la concentración de bicarbonato plasmático. Este ajuste renal toma 3 5 días para completarse y refleja una mayor generación de bicarbonato renal por mayor acidificación renal (especialmente por mayor síntesis de amonio) y pérdida de cloruro, generando la característica hiperbicarbonatemia hipoclorémica de la acidosis respiratoria crónica. Esta compensación crónica es aproximadamente 3,5 meq/l por cada 10 mmhg que sube la pco 2. Por lo anterior, para un mismo grado de elevación en pco 2 el grado de acidemia será mucho menor en acidosis respiratoria crónica que en la aguda. Los signos y síntomas de acidosis respiratoria se enumeran en la Tabla 6 Tabla 6 Síntomas y signos de Acidosis respiratoria Sistema nervioso central Sistema respiratorio Sistema cardiovascular +LSHUFDSQHDVXDYHDPRGHUDGD-Disnea +LSHUFDSQHDVXDYHD PRGHUDGD -Vasodilatación cerebral -Cianosis central -Piel caliente y sudorosa -Aumento de la presión intracraneana y periférica -Pulso fuerte -Cefalea -Hipertensión pulmomar -Presión sanguínea y gasto -Confusión cardíaco mantenidos -Agitación -Diaforesis -Alucinaciones 20
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS
 EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE A continuación se presentan una serie de casos prácticos resueltos,
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE A continuación se presentan una serie de casos prácticos resueltos,
Tema 2. El agua, el ph y los equilibrios iónicos
 Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
Cátedra de Fisiología Humana CAPÍTULO I CAPITULO III. Equilibrio Acido Base PH. Carrera de Enfermería. Universidad Nacional del Nordeste
 CAPÍTULO I Cátedra de Fisiología Humana CAPITULO III Equilibrio Acido Base PH Carrera de Enfermería. Universidad Nacional del Nordeste 37 CAPITULO 3: Cada soluto del organismo, el sodio, el potasio, el
CAPÍTULO I Cátedra de Fisiología Humana CAPITULO III Equilibrio Acido Base PH Carrera de Enfermería. Universidad Nacional del Nordeste 37 CAPITULO 3: Cada soluto del organismo, el sodio, el potasio, el
Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D.
 Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D. Vallejos Javier Serial Marcos Sebastián Rausch Ricardo Simón Laura Solé Juan
Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D. Vallejos Javier Serial Marcos Sebastián Rausch Ricardo Simón Laura Solé Juan
REGULACIÓN DEL EQUILIBRIO ÁCIDO-BASE. Bqca. Sofía Langton Fisiología Humana Junio 2014
 REGULACIÓN DEL EQUILIBRIO ÁCIDOBASE Bqca. Sofía Langton Fisiología Humana Junio 2014 Objetivos 1. Estudiar la importancia del balance ácidobase en el organismo. 2. Comprender los tres sistemas (amortiguadores,
REGULACIÓN DEL EQUILIBRIO ÁCIDOBASE Bqca. Sofía Langton Fisiología Humana Junio 2014 Objetivos 1. Estudiar la importancia del balance ácidobase en el organismo. 2. Comprender los tres sistemas (amortiguadores,
Práctica clínica. Interpretación de los resultados de los gases en sangre
 Práctica clínica Para interpretar los gases en sangre es necesaria la evaluación sistemática de la oxigenación, el ph, el bicarbonato estándar (shco3 ) y el exceso de bases, la presión parcial de anhídrido
Práctica clínica Para interpretar los gases en sangre es necesaria la evaluación sistemática de la oxigenación, el ph, el bicarbonato estándar (shco3 ) y el exceso de bases, la presión parcial de anhídrido
INTOXICACION CON ASPIRINA
 INTOXICACION CON ASPIRINA La intoxicación con aspirina es un hecho sumamente común en la práctica médica. La misma responde entre otras cosas, a que es un medicamento que puede adquirirse sin receta en
INTOXICACION CON ASPIRINA La intoxicación con aspirina es un hecho sumamente común en la práctica médica. La misma responde entre otras cosas, a que es un medicamento que puede adquirirse sin receta en
Sistema renal. Odontología 2008
 Sistema renal Odontología 2008 Sistema renal Los riñones Si están bien perfundidos Mediante los mecanismos básicos: Filtración Reabsorción Secreción Regulan el medio interno Eliminan sustancias de deshecho
Sistema renal Odontología 2008 Sistema renal Los riñones Si están bien perfundidos Mediante los mecanismos básicos: Filtración Reabsorción Secreción Regulan el medio interno Eliminan sustancias de deshecho
TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE
 TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE ALTERACIONES ACIDO-BASE Los ácidos son producidos en forma continua, durante el metabolismo normal La concentración de hidrógeno en el LEC se mantiene en un
TRASTORNOS METABOLICOS DEL ESTADO ACIDO-BASE ALTERACIONES ACIDO-BASE Los ácidos son producidos en forma continua, durante el metabolismo normal La concentración de hidrógeno en el LEC se mantiene en un
FISIOPATOLOGIA. Concentración normal H+: 40 nmoles/l. -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3
 FISIOPATOLOGIA Concentración normal H+: 40 nmoles/l -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3 FISIOPATOLOGIA ACIDO-BASE ACIDO: sustancia capaz de ceder protones BASE: sustancia
FISIOPATOLOGIA Concentración normal H+: 40 nmoles/l -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3 FISIOPATOLOGIA ACIDO-BASE ACIDO: sustancia capaz de ceder protones BASE: sustancia
PARATIROIDES HORMONA PARATIROIDEA, CALCITONINA, METABOLISMO DEL CALCIO Y DEL FOSFATO, VITAMINA D, HUESOS.
 PARATIROIDES HORMONA PARATIROIDEA, CALCITONINA, METABOLISMO DEL CALCIO Y DEL FOSFATO, VITAMINA D, HUESOS. La fisiología del metabolismo del calcio y del fosfato, la función de la vitamina D y la formación
PARATIROIDES HORMONA PARATIROIDEA, CALCITONINA, METABOLISMO DEL CALCIO Y DEL FOSFATO, VITAMINA D, HUESOS. La fisiología del metabolismo del calcio y del fosfato, la función de la vitamina D y la formación
MANEJO DEL ESTADO HIPEROSMOLAR
 MANEJO DEL ESTADO HIPEROSMOLAR DR. RAUL MENDOZA LOPEZ URGENCIAS MEDICO QUIRURGICAS MEDICINA DE REANIMACION ESTADO HIPEROSMOLAR NO CETOSICO: Descompensación aguda severa de diabetes mellitus Estado clínico
MANEJO DEL ESTADO HIPEROSMOLAR DR. RAUL MENDOZA LOPEZ URGENCIAS MEDICO QUIRURGICAS MEDICINA DE REANIMACION ESTADO HIPEROSMOLAR NO CETOSICO: Descompensación aguda severa de diabetes mellitus Estado clínico
Agua corporal: Relación con el peso corporal total y su distribución en los distintos compartimientos. Peso total
 Agua corporal: Relación con el peso corporal total y su distribución en los distintos compartimientos Agua corporal 60-70 % Peso total Agua Extracelular 20-25 % Agua Intracelular 40-45 % Agua transcelular
Agua corporal: Relación con el peso corporal total y su distribución en los distintos compartimientos Agua corporal 60-70 % Peso total Agua Extracelular 20-25 % Agua Intracelular 40-45 % Agua transcelular
ESTADO ACIDO BASE ACIDOSIS METABOLICA. ETIOLOGÍA DE LA ACIDOSIS METABÓLICA Inhabilidad Para Secretar La Carga Acida De La Dieta +
 ESTADO ACIDO BASE Los siguientes pasos son usados para evaluar los desordenes acidobase: 1.Determinar la anormalidad de base acidosis metabólica y/o alcalosis metabólica. 2.Determinar los factores contribuyentes
ESTADO ACIDO BASE Los siguientes pasos son usados para evaluar los desordenes acidobase: 1.Determinar la anormalidad de base acidosis metabólica y/o alcalosis metabólica. 2.Determinar los factores contribuyentes
Equilibrio Ácido - Base
 Equilibrio Ácido - Base OBJETIVOS Comprender la importancia de mantener los valores de ph dentro del rango normal Analizar los diferentes mecanismos de regulación que permiten mantener el equilibrio ácido-base
Equilibrio Ácido - Base OBJETIVOS Comprender la importancia de mantener los valores de ph dentro del rango normal Analizar los diferentes mecanismos de regulación que permiten mantener el equilibrio ácido-base
LA INSULINA DE ACCION EN EL HIPERTIROIDISMO: UN ENFOQUE EN LOS MUSCULOS Y TEJIDO ADIPOSO.
 LA INSULINA DE ACCION EN EL HIPERTIROIDISMO: UN ENFOQUE EN LOS MUSCULOS Y TEJIDO ADIPOSO. INTRODUCCION Las hormonas tiroideas pueden influir en un número de procesos en el cuerpo. Los cambios en sus niveles
LA INSULINA DE ACCION EN EL HIPERTIROIDISMO: UN ENFOQUE EN LOS MUSCULOS Y TEJIDO ADIPOSO. INTRODUCCION Las hormonas tiroideas pueden influir en un número de procesos en el cuerpo. Los cambios en sus niveles
II- Qué es la Diabetes?
 I - Introducción La Diabetes Mellitus es una enfermedad considerada como un problema de salud pública. Su prevalencia ha ido en aumento y las proyecciones en este milenio son de proporciones substanciales,
I - Introducción La Diabetes Mellitus es una enfermedad considerada como un problema de salud pública. Su prevalencia ha ido en aumento y las proyecciones en este milenio son de proporciones substanciales,
Obesidad y sus complicaciones
 Obesidad y sus complicaciones 0123/#$4#(-#%,%#5/&()+)$,/*,/&6#5)%,%7/012)3$#5/8)#$#$/ -,9&(/()#5+&7/0:2;*#5/5&$/*,5/'&$5#'2#$'),57/ INTRODUCCIÓN La obesidad es por sí misma un problema de salud. Antes
Obesidad y sus complicaciones 0123/#$4#(-#%,%#5/&()+)$,/*,/&6#5)%,%7/012)3$#5/8)#$#$/ -,9&(/()#5+&7/0:2;*#5/5&$/*,5/'&$5#'2#$'),57/ INTRODUCCIÓN La obesidad es por sí misma un problema de salud. Antes
APRENDIENDO CON NEFRON SUPERHEROE
 APRENDIENDO CON NEFRON SUPERHEROE DIABETES - UN FACTOR DE RIESGO PARA LA ENFERMEDAD RENAL La Diabetes mellitus, generalmente conocida como diabetes, es una enfermedad en la que su cuerpo no produce suficiente
APRENDIENDO CON NEFRON SUPERHEROE DIABETES - UN FACTOR DE RIESGO PARA LA ENFERMEDAD RENAL La Diabetes mellitus, generalmente conocida como diabetes, es una enfermedad en la que su cuerpo no produce suficiente
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA CICLO ACADÉMICO 2,009
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Equilibrio AcidoAcido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Equilibrio AcidoAcido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
constituye aproximadamente el 60% de la reserva de aminoácidos del músculo esquelético.
 Qué es la glutamina? La glutamina es el más abundante aminoácido libre en el cuerpo humano, y constituye aproximadamente el 60% de la reserva de aminoácidos del músculo esquelético. La glutamina es un
Qué es la glutamina? La glutamina es el más abundante aminoácido libre en el cuerpo humano, y constituye aproximadamente el 60% de la reserva de aminoácidos del músculo esquelético. La glutamina es un
Tratamiento del síndrome hiperglucémico hiperosmolar en adultos diabéticos tipo 2 en el segundo y tercer niveles de atención
 CIE 0: Diabetes mellitus (E 0- E4) Diabetes mellitus no insulino dependiente, con coma E.0 Diabetes mellitus no insulino dependiente, con complicaciones no específicadas Tratamiento del síndrome hiperglucémico
CIE 0: Diabetes mellitus (E 0- E4) Diabetes mellitus no insulino dependiente, con coma E.0 Diabetes mellitus no insulino dependiente, con complicaciones no específicadas Tratamiento del síndrome hiperglucémico
MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ
 MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ 1-Historia clínica G D Varón de 1 año y 5 meses MOTIVO DE CONSULTA retraso del crecimiento ANTECEDENTES RNTPAEG
MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ 1-Historia clínica G D Varón de 1 año y 5 meses MOTIVO DE CONSULTA retraso del crecimiento ANTECEDENTES RNTPAEG
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. 20 g/100 ml
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: CLORURO DE SODIO 20 % Forma farmacéutica: Solución concentrada para infusión IV Fortaleza: Presentación: Titular del Registro Sanitario,
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: CLORURO DE SODIO 20 % Forma farmacéutica: Solución concentrada para infusión IV Fortaleza: Presentación: Titular del Registro Sanitario,
DIABETES: DULCE ENEMIGO
 DIABETES: DULCE ENEMIGO La diabetes está alcanzando proporciones epidémicas. Los expertos atribuyen la causa de la epidemia a nuestro estilo de vida sedentario, la mala alimentación y la obesidad. La diabetes
DIABETES: DULCE ENEMIGO La diabetes está alcanzando proporciones epidémicas. Los expertos atribuyen la causa de la epidemia a nuestro estilo de vida sedentario, la mala alimentación y la obesidad. La diabetes
Fisiopatología del Equilibrio Ácido-Base ACIDOSIS
 Fisiopatología del Equilibrio Ácido-Base ACIDOSIS Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: I. ACIDOSIS:
Fisiopatología del Equilibrio Ácido-Base ACIDOSIS Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: I. ACIDOSIS:
Equilibrio Acido-Base
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Conceptos
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Conceptos
Beneficios de la Ozonoterapia en la Diabetes Mellitus
 Beneficios de la Ozonoterapia en la Diabetes Mellitus Mundialmente afecta a más de 382 millones de personas, la Organización Mundial de la Salud estima que para el año 2030 el número de personas diagnosticadas
Beneficios de la Ozonoterapia en la Diabetes Mellitus Mundialmente afecta a más de 382 millones de personas, la Organización Mundial de la Salud estima que para el año 2030 el número de personas diagnosticadas
Diabetes QUÉ ES LA DIABETES? CUÁNTAS CLASES DE DIABETES EXISTEN? La diabetes está agrupada en tres grandes clases:
 QUÉ ES LA DIABETES? La diabetes es una enfermedad crónica muy frecuente que durante un largo tiempo suele no presentar manifestaciones clínicas. En muchos casos, la enfermedad debuta clínicamente con una
QUÉ ES LA DIABETES? La diabetes es una enfermedad crónica muy frecuente que durante un largo tiempo suele no presentar manifestaciones clínicas. En muchos casos, la enfermedad debuta clínicamente con una
Equilibrio Acido-Base
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,008 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,008 Equilibrio Acido-Base Dr. Mynor A. Leiva Enríquez Las moléculas
FUNCIÓN RENAL. Dr. Adolfo Quesada Chanto, PhD
 FUNCIÓN RENAL Dr. Adolfo Quesada Chanto, PhD Creatinina sérica Normales: Mujeres 0,7-1,2 Hombres 0,8-1,5 mg/dl Es la menos variable de las sustancias nitrogenadas no proteicas (NNP) en el suero, y es un
FUNCIÓN RENAL Dr. Adolfo Quesada Chanto, PhD Creatinina sérica Normales: Mujeres 0,7-1,2 Hombres 0,8-1,5 mg/dl Es la menos variable de las sustancias nitrogenadas no proteicas (NNP) en el suero, y es un
EDUCATIVO. Alteraciones del. - Departamento de Fisiopatología - Facultad de Medicina 2011MATERIAL. Dr MSc José Boggia
 - Departamento de Fisiopatología - Facultad de Medicina Alteraciones del equilibrio i ácido-base 2011 Dr MSc José Boggia PANORAMICA GLOBAL I. Recordatorio de la fisiología ácido-base II. Diagnóstico de
- Departamento de Fisiopatología - Facultad de Medicina Alteraciones del equilibrio i ácido-base 2011 Dr MSc José Boggia PANORAMICA GLOBAL I. Recordatorio de la fisiología ácido-base II. Diagnóstico de
Introducción a la fisiología: la célula y la fisiología general
 I Introducción a la fisiología: la célula y la fisiología general 1 Organización funcional del cuerpo humano y control del «medio interno» 2 La célula y sus funciones 3 Control genético de la síntesis
I Introducción a la fisiología: la célula y la fisiología general 1 Organización funcional del cuerpo humano y control del «medio interno» 2 La célula y sus funciones 3 Control genético de la síntesis
GASES ARTERIALES. Interpretación
 GASES ARTERIALES Interpretación GASES ARTERIALES Técnica básica para valoración del intercambio pulmonar de gases. Técnica de punción Punción de arteria radial no dominante. Utilizar anestesia local (opcional)
GASES ARTERIALES Interpretación GASES ARTERIALES Técnica básica para valoración del intercambio pulmonar de gases. Técnica de punción Punción de arteria radial no dominante. Utilizar anestesia local (opcional)
INTOXICACION DIGITALICA
 INTOXICACION DIGITALICA La digital y los preparados a base de digital (digoxina, digitoxina, lanatósido C y deslanósido) son medicamentos inotrópicos que se usan en el tratamiento de la insuficiencia cardíaca.
INTOXICACION DIGITALICA La digital y los preparados a base de digital (digoxina, digitoxina, lanatósido C y deslanósido) son medicamentos inotrópicos que se usan en el tratamiento de la insuficiencia cardíaca.
Programa de Formación de Entrenadores de la ITF Curso de Nivel 2. Beber para ganar
 Programa de Formación de Entrenadores de la ITF Curso de Nivel 2 Beber para ganar Importancia (I) No se le da importancia a la correcta hidratación en el tenis Jugadores y entrenadores desconocen los aspectos
Programa de Formación de Entrenadores de la ITF Curso de Nivel 2 Beber para ganar Importancia (I) No se le da importancia a la correcta hidratación en el tenis Jugadores y entrenadores desconocen los aspectos
1.- Indica semejanzas y diferencias entre los siguientes conceptos:
 Ejercicios resueltos aparato excretor 1.- Indica semejanzas y diferencias entre los siguientes conceptos: a) Excreción y defecación: La excreción supone la eliminación de los productos de desecho procedentes
Ejercicios resueltos aparato excretor 1.- Indica semejanzas y diferencias entre los siguientes conceptos: a) Excreción y defecación: La excreción supone la eliminación de los productos de desecho procedentes
el agua y la hidratación
 Los fundamentos científicos sobre el agua y la hidratación Grupo de trabajo sobre salud de la EFBW (Federación Europea de Agua Embotellada) 2011 Aviso legal Esta presentación ha sido elaborada por el grupo
Los fundamentos científicos sobre el agua y la hidratación Grupo de trabajo sobre salud de la EFBW (Federación Europea de Agua Embotellada) 2011 Aviso legal Esta presentación ha sido elaborada por el grupo
UNIVERSIDAD CENTROCCIDENTAL LISANDRO ALVARADO DECANATO DE MEDICINA DEPARTAMENTO DE CIENCIAS FUNCIONALES SECCIÓN DE FISIOLOGÍA
 UNIVERSIDAD CENTROCCIDENTAL LISANDRO ALVARADO DECANATO DE MEDICINA DEPARTAMENTO DE CIENCIAS FUNCIONALES SECCIÓN DE FISIOLOGÍA EL FENOMENO DE LA OSMOSIS Selección de Material Audiovisual Preparado por:
UNIVERSIDAD CENTROCCIDENTAL LISANDRO ALVARADO DECANATO DE MEDICINA DEPARTAMENTO DE CIENCIAS FUNCIONALES SECCIÓN DE FISIOLOGÍA EL FENOMENO DE LA OSMOSIS Selección de Material Audiovisual Preparado por:
HEMOGLOBINA GLICOSILADA QUE DEBE SABER EL PACIENTE?
 LA HEMOGLOBINA GLICOSILADA QUE DEBE SABER EL PACIENTE? 1 QUE ES LA HEMOGLOBINA GLICOSILADA? a hemoglobina es una proteína que se encuentra L en los glóbulos rojos de nuestra sangre y es la encargada de
LA HEMOGLOBINA GLICOSILADA QUE DEBE SABER EL PACIENTE? 1 QUE ES LA HEMOGLOBINA GLICOSILADA? a hemoglobina es una proteína que se encuentra L en los glóbulos rojos de nuestra sangre y es la encargada de
EL CUERPO HUMANO (Anatomía, fisiología, higiene y salud para maestros)
 Departamento de Biología Ambiental y Salud Pública EL CUERPO HUMANO (Anatomía, fisiología, higiene y salud para maestros) 7. Los sistemas de nutrición (4): Eliminando residuos... A qué le llamamos residuos
Departamento de Biología Ambiental y Salud Pública EL CUERPO HUMANO (Anatomía, fisiología, higiene y salud para maestros) 7. Los sistemas de nutrición (4): Eliminando residuos... A qué le llamamos residuos
PRIMARIA CO3H - pl BALANCE DE H + ESPACIO DISTRIB. APARENTE CO3H - ( + ) ENTRADA > SALIDA (PRODUCCION) AUMENTADO
 BIOQ. ALEXIS MURYAN PRIMARIA CO3H - pl BALANCE DE H + ESPACIO DISTRIB. APARENTE CO3H - ( + ) ENTRADA > SALIDA (PRODUCCION) AUMENTADO INFUSION RAPIDA DE SALINA HIPEROSMOLAR ( CHICOS ) CARGA DE ACIDOS EXOGENOS
BIOQ. ALEXIS MURYAN PRIMARIA CO3H - pl BALANCE DE H + ESPACIO DISTRIB. APARENTE CO3H - ( + ) ENTRADA > SALIDA (PRODUCCION) AUMENTADO INFUSION RAPIDA DE SALINA HIPEROSMOLAR ( CHICOS ) CARGA DE ACIDOS EXOGENOS
Aspectos destacados del sistema cardiocirculatorio y respiratorio, ligados al entrenamiento deportivo. Dr. Juan Carlos Mazza (Argentina)
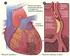 Aspectos destacados del sistema cardiocirculatorio y respiratorio, ligados al entrenamiento deportivo Dr. Juan Carlos Mazza (Argentina) SISTEMA CARDIOVASCULAR Cualquier sistema de circulación requiere
Aspectos destacados del sistema cardiocirculatorio y respiratorio, ligados al entrenamiento deportivo Dr. Juan Carlos Mazza (Argentina) SISTEMA CARDIOVASCULAR Cualquier sistema de circulación requiere
X-Plain Hipertensión esencial Sumario
 X-Plain Hipertensión esencial Sumario Introducción Hipertensión o presión arterial alta es una condición muy común que afecta a 1 de cada 4 adultos. Hipertensión también se llama el Asesino Silencioso
X-Plain Hipertensión esencial Sumario Introducción Hipertensión o presión arterial alta es una condición muy común que afecta a 1 de cada 4 adultos. Hipertensión también se llama el Asesino Silencioso
http://www.biologia54paternal.blogspot.com Unidad 7: Respiración Celular
 1 La energía lumínica es capturada por las plantas verdes y otros organismos fotosintéticos, que la transforman en energía química fijada en moléculas como la glucosa. Estas moléculas son luego degradadas
1 La energía lumínica es capturada por las plantas verdes y otros organismos fotosintéticos, que la transforman en energía química fijada en moléculas como la glucosa. Estas moléculas son luego degradadas
Glucosa sérica. Valores normales en adultos en ayunas. Mujeres 65-100 mg/dl Hombres 70-100 mg/dl.
 Glucosa sérica Valores normales en adultos en ayunas Mujeres 65-100 mg/dl Hombres 70-100 mg/dl. Estados hiperglicémicos Respuesta a la tensión. Enfermedad de Cushing o cualquier trastorno que eleve la
Glucosa sérica Valores normales en adultos en ayunas Mujeres 65-100 mg/dl Hombres 70-100 mg/dl. Estados hiperglicémicos Respuesta a la tensión. Enfermedad de Cushing o cualquier trastorno que eleve la
MODULO EDUCATIVO I CONOCIMIENTO DE HIPERTENSION
 MODULO EDUCATIVO I CONOCIMIENTO DE HIPERTENSION MODULO EDUCATIVO I CONOCIMIENTO DE HIPERTENSION Qué es la presión arterial? Qué es la hipertensión arterial? Por qué sube la tensión? Tipos de hipertensión
MODULO EDUCATIVO I CONOCIMIENTO DE HIPERTENSION MODULO EDUCATIVO I CONOCIMIENTO DE HIPERTENSION Qué es la presión arterial? Qué es la hipertensión arterial? Por qué sube la tensión? Tipos de hipertensión
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
PROSPECTO: INFORMACIÓN PARA EL USUARIO Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
EQUILIBRIO ACIDO - BASE
 EQUILIBRIO ACIDO - BASE Carrera de Médicos Especialistas Universitarios en Medicina Crítica y Terapia Intensiva. Universidad de Buenos Aires CONCEPTOS GENERALES EQUILIBRIO ACIDO-BASE EN FORMA ESTEQUIOMÉTRICA
EQUILIBRIO ACIDO - BASE Carrera de Médicos Especialistas Universitarios en Medicina Crítica y Terapia Intensiva. Universidad de Buenos Aires CONCEPTOS GENERALES EQUILIBRIO ACIDO-BASE EN FORMA ESTEQUIOMÉTRICA
Sistemas de ingreso, intercambio y transporte de sustancias en el organismo. Sistema Circulatorio
 Sistema circulatorio Observe y explore comprensivamente esta presentación Sistemas de ingreso, intercambio y transporte de sustancias en el organismo: Sistema circulatorio. Esta le permitirá avanzar y
Sistema circulatorio Observe y explore comprensivamente esta presentación Sistemas de ingreso, intercambio y transporte de sustancias en el organismo: Sistema circulatorio. Esta le permitirá avanzar y
DIABETES MELLITUS. Dra. Luz Don Centro de Nutrición
 DIABETES MELLITUS Dra. Luz Don Centro de Nutrición DEFINICIÓN ENFERMEDAD CRÓNICA METABÓLICA PRESENCIA DE HIPERGLUCEMIA DEFECTO EN LA SECRECIÓN DE INSULINA O EN LA ACCÍON DE LA INSULINA O DE AMBAS DIAGNÓSTICO
DIABETES MELLITUS Dra. Luz Don Centro de Nutrición DEFINICIÓN ENFERMEDAD CRÓNICA METABÓLICA PRESENCIA DE HIPERGLUCEMIA DEFECTO EN LA SECRECIÓN DE INSULINA O EN LA ACCÍON DE LA INSULINA O DE AMBAS DIAGNÓSTICO
HOSPITAL NACIONAL PROF. A. POSADAS SERVICIO DE PEDIATRÍA
 HOSPITAL NACIONAL PROF. A. POSADAS SERVICIO DE PEDIATRÍA EQUILIBRIO ÁCIDO-BASE DESDE LA FISIOLOGÍA SERVICIO DE PEDIATRÍA HOSP. NAC. PROF. A. POSADAS Dept. Pediatría Fac. Medicina - UBA Horacio A. Repetto
HOSPITAL NACIONAL PROF. A. POSADAS SERVICIO DE PEDIATRÍA EQUILIBRIO ÁCIDO-BASE DESDE LA FISIOLOGÍA SERVICIO DE PEDIATRÍA HOSP. NAC. PROF. A. POSADAS Dept. Pediatría Fac. Medicina - UBA Horacio A. Repetto
ENFERMERÍA CLÍNICA I Felicitas Merino de la Hoz TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS
 TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS ÍNDICE 1. Introducción. 2. Análisis e interpretación de los gases arteriales. 3. Alteraciones del equilibrio ácido- base. 3.1. Acidosis respiratoria. 3.2. Alcalosis
TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS ÍNDICE 1. Introducción. 2. Análisis e interpretación de los gases arteriales. 3. Alteraciones del equilibrio ácido- base. 3.1. Acidosis respiratoria. 3.2. Alcalosis
1 ml/min. Na 18.125 meq 0,13 meq 99,4% K 0,56 meq 0,05 meq 90,5% Glucosa 125 mg 0 meq 100% Urea 0,6 mmol 0,28 meq 53,3% Urico 3,8 mg 0,10 meq 97,4%
 RIÑÓN Y LÍQUIDOS CORPORALES 27. Funciones tubulares Transporte tubular renal: reabsorción y secreción El ultrafiltrado glomerular se transporta a través de la estructura tubular de la nefrona, atravesando:
RIÑÓN Y LÍQUIDOS CORPORALES 27. Funciones tubulares Transporte tubular renal: reabsorción y secreción El ultrafiltrado glomerular se transporta a través de la estructura tubular de la nefrona, atravesando:
Capítulo 6. Valoración respiratoria
 498 Capítulo 6. Valoración respiratoria 6.19. La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 6.19 La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 499
498 Capítulo 6. Valoración respiratoria 6.19. La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 6.19 La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 499
EQUILIBRIO ÁCIDO-BASE
 EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
Tratamiento con Hidroxiurea contra la Enfermedad de Células Falciformes
 Tratamiento con Hidroxiurea contra la Enfermedad de Células Falciformes antes de hidroxiurea después de hidroxiurea Tratamiento con Hidroxiurea contra la Enfermedad de Células Falciformes 1 Este documento
Tratamiento con Hidroxiurea contra la Enfermedad de Células Falciformes antes de hidroxiurea después de hidroxiurea Tratamiento con Hidroxiurea contra la Enfermedad de Células Falciformes 1 Este documento
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 10 ml de solución contiene: Hidrogenocarbonato de sodio
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 10 ml de solución contiene: Hidrogenocarbonato de sodio
El corazón, al tener paredes musculares, puede dilatarse y contraerse, lo que le permite bombear la sangre.
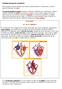 Fisiología del aparato circulatorio El corazón, al tener paredes musculares, puede dilatarse y contraerse, lo que le permite bombear la sangre. El corazón bombea la sangre de forma continua, mediante dos
Fisiología del aparato circulatorio El corazón, al tener paredes musculares, puede dilatarse y contraerse, lo que le permite bombear la sangre. El corazón bombea la sangre de forma continua, mediante dos
QUIMICA ANALÍTICA (63.05) SOLUCIONES REGULADORAS DE ph 63.05.12. Lic. Ana María Martín
 QUIMICA ANALÍTICA (63.05) SOLUCIONES REGULADORAS DE ph 63.05.12 Lic. Ana María Martín Lic. Ana María Martín Introducción SOLUCIONES REGULADORAS DE ph Muchas de las reacciones químicas que se producen en
QUIMICA ANALÍTICA (63.05) SOLUCIONES REGULADORAS DE ph 63.05.12 Lic. Ana María Martín Lic. Ana María Martín Introducción SOLUCIONES REGULADORAS DE ph Muchas de las reacciones químicas que se producen en
PROPÓSITO DE MEDIR LOS GASES ARTERIALES
 FISIOLOGÍA DE GASES ARTERIALES La primera parte de este módulo comprende elementos básicos sobre la fisiología de los gases arteriales. Este módulo ayudará a los profesionales de la enfermería y cardiorrespiratorios
FISIOLOGÍA DE GASES ARTERIALES La primera parte de este módulo comprende elementos básicos sobre la fisiología de los gases arteriales. Este módulo ayudará a los profesionales de la enfermería y cardiorrespiratorios
Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires
 ÁCIDOS Y BASES Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires OBJETIVOS: - Reconocer ácidos, bases y sales, determinar sus disociaciones en agua, según sean electrolitos fuertes
ÁCIDOS Y BASES Lic. Cintia Mendez Vedia Lic. en Nutrición Univesidad de Buenos Aires OBJETIVOS: - Reconocer ácidos, bases y sales, determinar sus disociaciones en agua, según sean electrolitos fuertes
Una píldora diaria. Tres valores de laboratorio importantes
 Tres valores de laboratorio importantes Una píldora diaria Sensipar una vez al día* ayuda a reducir los niveles de HPT, calcio y fósforo en pacientes con hiperparatiroidismo secundario (HPTS) que reciben
Tres valores de laboratorio importantes Una píldora diaria Sensipar una vez al día* ayuda a reducir los niveles de HPT, calcio y fósforo en pacientes con hiperparatiroidismo secundario (HPTS) que reciben
CURRICULAR Versión: 1. DOCUMENTO ACADÉMICO Fecha: 04/03/2010 HIDRATACIÓN GRADO NOVENO PRIMER PERÍODO
 DIRECCIÓN ACADÉMICA Código: DAC C F004 CURRICULAR Versión: 1 DOCUMENTO ACADÉMICO Fecha: 04/03/2010 HIDRATACIÓN GRADO NOVENO PRIMER PERÍODO ÁREA DE EDUCACIÓN FÍSICA RECREACIÓN Y DEPORTES 2015 Introducción.
DIRECCIÓN ACADÉMICA Código: DAC C F004 CURRICULAR Versión: 1 DOCUMENTO ACADÉMICO Fecha: 04/03/2010 HIDRATACIÓN GRADO NOVENO PRIMER PERÍODO ÁREA DE EDUCACIÓN FÍSICA RECREACIÓN Y DEPORTES 2015 Introducción.
Electrólisis. Electrólisis 12/02/2015
 Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Hormonas tiroideas (permisivas ) Contribuye con el desarrollo del sistema nervioso
 CRECIMIENTO Y BALANCE DE CALCIO El crecimiento puede dividirse en crecimiento de tejidos blandos y crecimiento óseo. En los niños el crecimiento óseo puede evaluarse midiendo la estatura y el crecimiento
CRECIMIENTO Y BALANCE DE CALCIO El crecimiento puede dividirse en crecimiento de tejidos blandos y crecimiento óseo. En los niños el crecimiento óseo puede evaluarse midiendo la estatura y el crecimiento
Obesidad e Hipertensión arterial: Qué debe saber el pediatra?
 36 Congreso Argentino de Pediatría Mar del Plata, 24 al 27 de setiembre de 2013. Mesa redonda Consecuencias Graves de la Obesidad temprana Jueves 26 de setiembre /16:15hs Obesidad e Hipertensión arterial:
36 Congreso Argentino de Pediatría Mar del Plata, 24 al 27 de setiembre de 2013. Mesa redonda Consecuencias Graves de la Obesidad temprana Jueves 26 de setiembre /16:15hs Obesidad e Hipertensión arterial:
X-Plain La pancreatitis Sumario
 X-Plain La pancreatitis Sumario La pancreatitis es una enfermedad poco común que provoca la inflamación del páncreas. A pesar de ser una enfermedad poco común, casi 80,000 norteamericanos padecen de pancreatitis
X-Plain La pancreatitis Sumario La pancreatitis es una enfermedad poco común que provoca la inflamación del páncreas. A pesar de ser una enfermedad poco común, casi 80,000 norteamericanos padecen de pancreatitis
SUAVIZACIÓN CONCEPTOS BÁSICOS
 SUAVIZACIÓN CONCEPTOS BÁSICOS Revisemos algunos conceptos que utilizarás para el diseño de los equipos del sistema de suavización, recuerda que muchos ya los has visto en cursos anteriores y que esto es
SUAVIZACIÓN CONCEPTOS BÁSICOS Revisemos algunos conceptos que utilizarás para el diseño de los equipos del sistema de suavización, recuerda que muchos ya los has visto en cursos anteriores y que esto es
INSUFICIENCIA RESPIRATORIA AGUDA GIOVANNY CAMPOMANES ESPINOZA MEDICO INTERNISTA
 INSUFICIENCIA RESPIRATORIA AGUDA GIOVANNY CAMPOMANES ESPINOZA MEDICO INTERNISTA Zona de Conducción TRAQUEA BRONQUIOS BRONQUIOLOS BRONQUIOLOS TERMINALES Z O 1 2 3 4 5 16 Zona de Transición Y Respiratoria
INSUFICIENCIA RESPIRATORIA AGUDA GIOVANNY CAMPOMANES ESPINOZA MEDICO INTERNISTA Zona de Conducción TRAQUEA BRONQUIOS BRONQUIOLOS BRONQUIOLOS TERMINALES Z O 1 2 3 4 5 16 Zona de Transición Y Respiratoria
Equilibrio Acido-Base. Dr Jorge Brenes Dittel. Nefrología.
 Equilibrio Acido-Base Dr Jorge Brenes Dittel. Nefrología. Equilibrio Acido-base. Fisiología ph es el logaritmo de la concentracíon del ión hidrogenion expresada en milimoles por litro. [H+] en sangre es
Equilibrio Acido-Base Dr Jorge Brenes Dittel. Nefrología. Equilibrio Acido-base. Fisiología ph es el logaritmo de la concentracíon del ión hidrogenion expresada en milimoles por litro. [H+] en sangre es
EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller
 2010 Reacciones de intercambio de Protones EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller Recopilación de ejercicios preguntados en exámenes de cursos anteriores Mª Teresa Gómez Ruiz IES Politécnico Cartagena.
2010 Reacciones de intercambio de Protones EJERCICIOS PARA EXAMEN U6 Química 2º Bachiller Recopilación de ejercicios preguntados en exámenes de cursos anteriores Mª Teresa Gómez Ruiz IES Politécnico Cartagena.
MARCO TEORICO. La diabetes es una enfermedad crónica en la cual el cuerpo no puede regular la cantidad de azúcar en la sangre.
 CAPITULO 2 MARCO TEORICO 2.1Que es la Diabetes La diabetes es una enfermedad crónica en la cual el cuerpo no puede regular la cantidad de azúcar en la sangre. Causas La insulina es una hormona producida
CAPITULO 2 MARCO TEORICO 2.1Que es la Diabetes La diabetes es una enfermedad crónica en la cual el cuerpo no puede regular la cantidad de azúcar en la sangre. Causas La insulina es una hormona producida
ALTERACIONES DEL EQUILIBRIO ÁCIDO BASE. Prof. Dra. Liliana G. Bianciotti
 ALTERACIONES DEL EQUILIBRIO ÁCIDO BASE Prof. Dra. Liliana G. Bianciotti lbianc@ffyb.uba.ar 2016 ALTERACIONES DEL EQUILIBIO ACIDO-BASE ph 7.35-7.45 Metabolismo de Ca 2+ y K + Solubilidad de sales óseas
ALTERACIONES DEL EQUILIBRIO ÁCIDO BASE Prof. Dra. Liliana G. Bianciotti lbianc@ffyb.uba.ar 2016 ALTERACIONES DEL EQUILIBIO ACIDO-BASE ph 7.35-7.45 Metabolismo de Ca 2+ y K + Solubilidad de sales óseas
Existen distintos tipos? Efectivamente existen distintos tipos de diabetes, según el mecanismo de producción de la enfermedad.
 Diabetes Qué es la diabetes? La diabetes mellitus comprende un grupo de trastornos metabólicos que comparten la existencia de niveles elevados de glucosa en sangre. Es una enfermedad en la que el organismo
Diabetes Qué es la diabetes? La diabetes mellitus comprende un grupo de trastornos metabólicos que comparten la existencia de niveles elevados de glucosa en sangre. Es una enfermedad en la que el organismo
Terapia Líquida en Pediatría
 PROGRAMA DE EDUCACIÓN MEDICA CONTINUADA TERCER CURSO DE 1974-1975 LÍQUIDOS Y ELECTROLITOS EN LA PRACTICA MEDICA Terapia Líquida en Pediatría Dr. Francisco Cleaves T. La administración de líquidos parenterales
PROGRAMA DE EDUCACIÓN MEDICA CONTINUADA TERCER CURSO DE 1974-1975 LÍQUIDOS Y ELECTROLITOS EN LA PRACTICA MEDICA Terapia Líquida en Pediatría Dr. Francisco Cleaves T. La administración de líquidos parenterales
Dr. José Raúl Recinos Deras
 http://www.medicosdeelsalvador.com Este artículo salió de la página web de Médicos de El Salvador. Fue escrito por: Dr. José Raúl Recinos Deras Clínica Médico Psiquiátrica y de Salud Mental Todos los derechos
http://www.medicosdeelsalvador.com Este artículo salió de la página web de Médicos de El Salvador. Fue escrito por: Dr. José Raúl Recinos Deras Clínica Médico Psiquiátrica y de Salud Mental Todos los derechos
Perfecciona tu protocolo de hidratación
 Perfecciona tu protocolo de hidratación Determina el estado euhidratado (hidratacion normal) simplemente con las mediciones del peso corporal y la gravedad específica de la orina. Si la primera muestra
Perfecciona tu protocolo de hidratación Determina el estado euhidratado (hidratacion normal) simplemente con las mediciones del peso corporal y la gravedad específica de la orina. Si la primera muestra
REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO:
 REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO: - FISIOLOGÍA DE ÁCIDOS Y BASES - EXCRECIÓN RENAL DE H + Miryam Romero R. MSc. PhD. Profesora de Fisiología Departamento de Ciencias Fisiológicas Universidad del Valle
REGULACIÓN DEL BALANCE ÁCIDO-BÁSICO: - FISIOLOGÍA DE ÁCIDOS Y BASES - EXCRECIÓN RENAL DE H + Miryam Romero R. MSc. PhD. Profesora de Fisiología Departamento de Ciencias Fisiológicas Universidad del Valle
Fisiopatología Del Equilibrio Ácido-Base Alcalosis
 Fisiopatología Del Equilibrio Ácido-Base Alcalosis Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: II. ALCALOSIS
Fisiopatología Del Equilibrio Ácido-Base Alcalosis Prof. Marcos Moreira Espinoza Instituto de Farmacología y Morfofisiologia Universidad Austral de Chile ALTERACIONES DEL EQUILIBRIO ACIDO BASE: II. ALCALOSIS
Intoxicación por Paraquat. Dra. Jackeline Berroterán Mejía Marzo 2011.
 Intoxicación por Paraquat Dra. Jackeline Berroterán Mejía Marzo 2011. Epidemiología CNT: 1234 casos de intoxicaciones por sustancias toxicas en el año 2010 50% por plaguicidas Alta mortalidad: 146 fallecidos
Intoxicación por Paraquat Dra. Jackeline Berroterán Mejía Marzo 2011. Epidemiología CNT: 1234 casos de intoxicaciones por sustancias toxicas en el año 2010 50% por plaguicidas Alta mortalidad: 146 fallecidos
WORLD DIABETES FOUNDATION. Universidad de Chile
 LA DIABETES 1 WORLD DIABETES FOUNDATION Universidad de Chile QUÉ ES LA DIABETES? 2 Es una enfermedad crónica, nos acompaña toda la vida. Muchas personas con diabetes no tienen molestias cuando se descubre
LA DIABETES 1 WORLD DIABETES FOUNDATION Universidad de Chile QUÉ ES LA DIABETES? 2 Es una enfermedad crónica, nos acompaña toda la vida. Muchas personas con diabetes no tienen molestias cuando se descubre
La actividad física del hombre es un mecanismo importante degeneración de calor.
 2.EL ORGANISMO HUMANO Y EL AMBIENTE TERMICO El ser humano es un organismo homeotermo, esto implica que las reacciones metabólicas requieren una temperatura constante (37± 1ºC)para desarrollarse, y en consecuencia
2.EL ORGANISMO HUMANO Y EL AMBIENTE TERMICO El ser humano es un organismo homeotermo, esto implica que las reacciones metabólicas requieren una temperatura constante (37± 1ºC)para desarrollarse, y en consecuencia
Ablandamiento de agua mediante el uso de resinas de intercambio iónico.
 Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
Educaguia.com. El agua es el medio en que tienen lugar todas las reacciones bioquímicas y procesos de digestión, absorción, metabolismo y excreción.
 1 EL AGUA El agua es un elemento esencial, sin agua la vida no sería posible. Sin comer podemos sobrevivir aproximadamente dos meses (o más en función de las reservas) pero sin agua moriríamos al cabo
1 EL AGUA El agua es un elemento esencial, sin agua la vida no sería posible. Sin comer podemos sobrevivir aproximadamente dos meses (o más en función de las reservas) pero sin agua moriríamos al cabo
Anemia: concepto 15/11/2013
 FÁRMACOS ANTIANÉMICOS Cruz Miguel Cendán Enfermería.Curso 2013/14 Anemia: concepto Reducción de la hemoglobina (Hb) y presencia de eritrocitos anormales con deficiencia en su función (capacidad de transporte
FÁRMACOS ANTIANÉMICOS Cruz Miguel Cendán Enfermería.Curso 2013/14 Anemia: concepto Reducción de la hemoglobina (Hb) y presencia de eritrocitos anormales con deficiencia en su función (capacidad de transporte
Actualizaciones. Eritropoyetina
 Actualizaciones Eritropoyetina Acciones de la eritropoyetina. La eritropoyetina es una glicoproteína plasmática que estimula la eritropoyesis y actúa además sobre otras células de la sangre como los granulocitos,
Actualizaciones Eritropoyetina Acciones de la eritropoyetina. La eritropoyetina es una glicoproteína plasmática que estimula la eritropoyesis y actúa además sobre otras células de la sangre como los granulocitos,
La importancia de la sangre
 La importancia de la sangre La sangre es un fluido vital, transporta nutrientes esenciales y oxígeno a todos los tejidos y órganos del cuerpo Cerca del 45% del volumen total de la sangre está compuesta
La importancia de la sangre La sangre es un fluido vital, transporta nutrientes esenciales y oxígeno a todos los tejidos y órganos del cuerpo Cerca del 45% del volumen total de la sangre está compuesta
Universidad de Costa Rica Escuela de Medicina SECCIÓN DE MEDICINA HOSPITAL SAN JUAN DE DIOS MEDIO INTERNO
 Universidad de Costa Rica Escuela de Medicina SECCIÓN DE MEDICINA HOSPITAL SAN JUAN DE DIOS MEDIO INTERNO TRASTORNOS HIDROELECTROLÍTICOS Y ÁCIDOBASE Dr. Luis Fdo. Briceño R. Profesor Asociado UCR HIPONATREMIA
Universidad de Costa Rica Escuela de Medicina SECCIÓN DE MEDICINA HOSPITAL SAN JUAN DE DIOS MEDIO INTERNO TRASTORNOS HIDROELECTROLÍTICOS Y ÁCIDOBASE Dr. Luis Fdo. Briceño R. Profesor Asociado UCR HIPONATREMIA
Una hormona, es una sustancia fabricada en el cuerpo, que actúa dentro nuestro, sin salir al exterior.
 QUÉ ÉS LA DIABETES CONCEPTO La diabetes es una enfermedad crónica, en la que hay un defecto en la fabricación de una hormona, que se llama insulina. Las células del cuerpo no pueden utilizar los azúcares
QUÉ ÉS LA DIABETES CONCEPTO La diabetes es una enfermedad crónica, en la que hay un defecto en la fabricación de una hormona, que se llama insulina. Las células del cuerpo no pueden utilizar los azúcares
Generación y Transmisión de señales en las Neuronas
 Generación y Transmisión de señales en las Neuronas Los detalle de la transmisión sináptica (comunicación entre neuronas) se explicará en el siguiente capítulo. En éste trataremos de los cambios intraneuronal:
Generación y Transmisión de señales en las Neuronas Los detalle de la transmisión sináptica (comunicación entre neuronas) se explicará en el siguiente capítulo. En éste trataremos de los cambios intraneuronal:
La presión arterial y su nuevo órgano. Un recurso para la salud cardiovascular después de un trasplante de órgano. Compartir. Informar. Inspirar.
 La presión arterial y su nuevo órgano Un recurso para la salud cardiovascular después de un trasplante de órgano Compartir. Informar. Inspirar. Comprender la presión arterial La presión arterial es la
La presión arterial y su nuevo órgano Un recurso para la salud cardiovascular después de un trasplante de órgano Compartir. Informar. Inspirar. Comprender la presión arterial La presión arterial es la
Cómo es tener diabetes tipo 2?
 Cómo es tener diabetes tipo 2? Según los Centros para el Control y la Prevención de Enfermedades (Centers for Disease Control and Prevention, CDC), hay casi 26 millones de personas con diabetes en los
Cómo es tener diabetes tipo 2? Según los Centros para el Control y la Prevención de Enfermedades (Centers for Disease Control and Prevention, CDC), hay casi 26 millones de personas con diabetes en los
Tipos de células madre
 Biología Bachillerato IES Fuentesnuevas 1 CÉLULAS MADRE O TRONCALES (STEM CELLS) Las células madre son células que tienen capacidad de renovarse continuamente por sucesivas divisiones por mitosis y de
Biología Bachillerato IES Fuentesnuevas 1 CÉLULAS MADRE O TRONCALES (STEM CELLS) Las células madre son células que tienen capacidad de renovarse continuamente por sucesivas divisiones por mitosis y de
Prospecto: información para el usuario. Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio
 Prospecto: información para el usuario Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve
Prospecto: información para el usuario Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve
Glándula Adrenal y Hormonas Adrenales EJE HIIPOTÁLAMO-HIPÓFISIS-GLÁNDULA
 Glándula Adrenal y Hormonas Adrenales EJE HIIPOTÁLAMO-HIPÓFISIS-GLÁNDULA Glándula Adrenal - Las glándulas adrenales están localizadas en la parte superior de los riñones -Cada glándula consiste de una
Glándula Adrenal y Hormonas Adrenales EJE HIIPOTÁLAMO-HIPÓFISIS-GLÁNDULA Glándula Adrenal - Las glándulas adrenales están localizadas en la parte superior de los riñones -Cada glándula consiste de una
HERBICIDAS BIPIRIDILOS. Dr. Diego González Machín Asesor en Toxicología CEPIS/OPS
 HERBICIDAS BIPIRIDILOS Dr. Diego González Machín Asesor en Toxicología CEPIS/OPS HERBICIDAS BIPIRIDILOS NOMBRE QUÍMICO PARAQUAT NOMBRE COMERCIAL GRAMOXONE RADEX PILLAROXONE DIQUAT AQUACIDE REGLONE DEXTRONE
HERBICIDAS BIPIRIDILOS Dr. Diego González Machín Asesor en Toxicología CEPIS/OPS HERBICIDAS BIPIRIDILOS NOMBRE QUÍMICO PARAQUAT NOMBRE COMERCIAL GRAMOXONE RADEX PILLAROXONE DIQUAT AQUACIDE REGLONE DEXTRONE
METABOLISMO CELULAR Y FUENTES BIOQUÍMICAS DE ENERGÍA DURANTE EL EJERCICIO AGUDO. Prof. Edgar Lopategui Corsino M.A., Fisiología del Ejercicio
 METABOLISMO CELULAR Y FUENTES BIOQUÍMICAS DE ENERGÍA DURANTE EL EJERCICIO AGUDO Prof. Edgar Lopategui Corsino M.A., Fisiología del Ejercicio TERMODINÁMICA MICA Primera Ley La Energía ni se Crea ni se
METABOLISMO CELULAR Y FUENTES BIOQUÍMICAS DE ENERGÍA DURANTE EL EJERCICIO AGUDO Prof. Edgar Lopategui Corsino M.A., Fisiología del Ejercicio TERMODINÁMICA MICA Primera Ley La Energía ni se Crea ni se
