Descripción de la enfermedad: Identificación del agente Pruebas serológicas
|
|
|
- Encarnación Rubio Duarte
- hace 6 años
- Vistas:
Transcripción
1 Descripción de la enfermedad: La peste equina (PE) es una enfermedad vírica infecciosa, pero no contagiosa, que afecta a todas las especies de équidos, causada por un orbivirus de la familia Reoviridae y caracterizada por alteraciones de las funciones respiratoria y circulatoria. La PE se transmite por al menos dos especies de Culicoides. Se han descrito nueve serotipos diferentes. En el este y el sur de África se presentan todos los serotipos de la PE. En el norte y el oeste africano, se han detectado los serotipos 9, 4 y 2, desde donde ocasionalmente pasan a países limítrofes del Mediterráneo. Algunos ejemplos de brotes que han tenido lugar fuera de África son: en Oriente Medio ( ), en España (serotipo 9, 1966, serotipo 4, ), y en Portugal (serotipo 4, 1989). El diagnóstico de laboratorio de la PE es esencial. Aunque los signos clínicos y las lesiones son características, se pueden confundir con las de otras enfermedades equinas. Como enfermedad vírica, el diagnóstico de laboratorio de la PE se puede basar en la identificación del virus infeccioso, del ácido nucleico del virus, de los antígenos víricos o de anticuerpos específicos. Se ha adaptado una amplia variedad de pruebas de laboratorio para detectar tanto el virus de la PE (VPE) como los anticuerpos específicos. Identificación del agente: Siempre que se surjan brotes fuera de las regiones enzoóticas es especialmente importante llevar a cabo el aislamiento y la serotipificación del virus, con el fin de escoger un serotipo homólogo para la vacuna. El VPE se puede aislar de sangre tomada durante la fase febril inicial. Otros tejidos adecuados para el diagnóstico y aislamiento del virus son el bazo, los pulmones y los ganglios linfáticos, que se obtienen durante la necropsia. Las muestras se pueden inocular en cultivos celulares, como los de riñón de hámster neonato-21 (BHK-21), células estables de mono (MS) o riñón de mono verde africano (Vero), o bien células de insecto (KC), así como por vía intravenosa en huevos embrionados. Se han desarrollado varios enzimoinmunoanálisis (ELISA) para la detección rápida del antígeno VPE en sangre, en tejidos de bazo y en sobrenadantes de células infectadas. También se ha logrado la identificación del ARN del VPE usando un método de reacción en cadena de la polimerasa con transcripción inversa. Las cepas aisladas se pueden serotipificar por una prueba serológica con especificidad de tipo como la de neutralización vírica (VN) y por una reacción en cadena de la polimerasa con transcripción inversa (PCR) también con especificidad de tipo, y posterior secuenciación. Pruebas serológicas: Los caballos que sobreviven a una infección natural desarrollan anticuerpos contra el serotipo infeccioso del VPE a los 8 12 días de la infección. Esto se puede demostrar por varios métodos serológicos, como la prueba de la fijación de complemento, por el ELISA, por inmunotransferencia y por VN. La última técnica es la usada en la serotipificación.
2 Requisitos para las vacunas: Actualmente se dispone de vacunas vivas atenuadas (mono y polivalentes) en el mercado para uso en caballos, mulas y asnos. Se han evaluado experimentalmente vacunas de subunidades. La peste equina (PE) (African horse sickness, Peste equine) es una enfermedad infecciosa de los équidos, no contagiosa y transmitida por artrópodos, que está causada por un Orbivirus de ARN bicatenario perteneciente a la familia Reoviridae. El género Orbivirus también incluye al virus causante de la lengua azul y al virus de la enfermedad hemorrágica epizoótica, que tienen propiedades morfológicas y bioquímicas similares pero distintas propiedades patológicas y antigénicas, así como un diferente rango de hospedadores. Mediante neutralización vírica se han identificado nueve serotipos del VPE antigénicamente diferenciados; se ha observado cierta reacción cruzada entre 1 y 2, 3 y 7, 5 y 8, y 6 y 9, pero no se producen reacciones cruzadas con otros orbivirus conocidos. El virión es una particular sin envoltura de un tamaño de unos 70 nm. El genoma del virus de la PE (VPE) comprende diez segmentos de ARN bicatenario que codifican siete proteínas estructurales (VP1-7), la mayor parte de las cuales han sido secuenciadas por completo en los serotipos del VPE 4, 6 y 9 (Roy et al., 1991; Venter et al., 2000; Williams et al., 1998), y cuatro proteínas no estructurales (NS1, NS2, NS3, NS3A) (Grubman & Lewis, 1992; Laviada et al., 1993). Las proteínas VP2 y VP5 forman la cápsida externa del virión, y las proteínas VP3 y VP7 son las proteínas principales de la cápsida interna. Las proteínas VP1, VP4 y VP6 constituyen las proteínas minoritarias de la cápsida interna. Las proteínas NS3 son las segundas más variables de entre las proteínas del VPE Van Niekert et al., 2001), siendo la más variable la proteína principal de la cápsida externa, VP2. Esta proteína, VP2, es la principal determinante de los diferentes serotipos del VPE y, junto con VP5, la diana de la neutralización vírica (Martínez-Torrecuadrada et al., 2001). Al menos dos vectores de campo intervienen en la transmisión del virus: Culicoides imicola y C. bolitinos. La PE es una enfermedad enzoótica en el África sub-sahariana, aunque se han dado brotes ocasionales en el norte de África (1965, , ), en el Oriente Medio ( ) y en Europa (España, 1966, , y Portugal, 1989) (Sánchez-Vizcaíno, 2004). Las cuatro formas clínicas clásicas de la PE son: la pulmonar, la cardíaca, la mixta y la febril. La forma pulmonar hiperaguda tiene lugar en animales totalmente susceptibles y es de curso corto, ya que a menudo dura solo unas horas; ocasiona una alta mortalidad. El animal presenta dificultad respiratoria, extiende la cabeza y el cuello y suda profusamente. Por último, excreta espuma por la nariz. La forma cardíaca, edematosa, tiene un curso más subagudo y la mortalidad llega al 50%. La cabeza y el cuello pueden presentar una intensa hinchazón, que puede avanzar hasta el tórax. También es característica una hinchazón de las fosas supraorbitales y puede haber hinchazón conjuntival con petequias. La parálisis del esófago puede dar lugar a neumonía por aspiración, y la presencia de hemorragias sublinguales siempre indican mal pronóstico. La forma mixta, aguda, es más frecuente y tiene rasgos tanto de la cardíaca como de la pulmonar. La mortalidad puede alcanzar el 70%. La febril suele pasar desapercibida, ya que es una forma leve de la enfermedad, y se observa en équidos resistentes, como cebras y asnos (Coetzer & Guthrie, 2005). La enfermedad tiene una incidencia estacional (final de verano/otoño) y cíclica, con las mayores epizootias durante las estaciones calurosas en Sudáfrica (Baylis et al., 1999). La mortalidad por el VPE depende de la especie de équido afectada y de la cepa y el serotipo del virus. Dentro de la familia de los équidos, los caballos son los más susceptibles a la PE, con una mortalidad del 50 95%, seguidos por las mulas, cuya mortalidad es de alrededor del 50%. En las regiones enzoóticas de África, los asnos son muy resistentes al VPE y experimentan solo infecciones subclínicas. Sin embargo, en países europeos y asiáticos, los asnos son moderadamente susceptibles y presentan una mortalidad del 10%. Las cebras son también notablemente resistentes, sin signos clínicos, excepto la fiebre, aunque pueden presentar una larga viremia (de hasta 40 días). Las pruebas de laboratorio son indispensables para establecer y confirmar un diagnóstico correcto. Aunque algunos signos clínicos y lesiones son característicos, la PE se puede confundir con otras enfermedades. Así, por ejemplo, la hinchazón supraorbital, que a menudo está presente en caballos con PE subaguda, es, junto con unos antecedentes determinados, suficiente para establecer un diagnóstico provisional. Otros signos y lesiones son menos específicos de la PE, y deben excluirse otras enfermedades, como la encefalosis equina, la anemia infecciosa equina, el virus Hendra, la arteritis viral equina, la piroplasmosis y la púrpura hemorrágica (OIE, 2010). Actualmente se comercializan vacunas vivas atenuadas (monovalentes y polivalentes) para su uso en caballos, mulos y asnos. No hay indicios de que los humanos se puedan infectar por ninguna cepa natural del VPE, ni por contacto con animales infectados natural o experimentalmente ni por manipulación del virus en los laboratorios. Las
3 manipulaciones de laboratorio deben llevarse a cabo a un nivel de contención adecuado, que vendrá determinado por un análisis del riesgo biológico (véase el Capítulo Bioseguridad y bioprotección: Normas para la gestión del riesgo biológico en el laboratorio veterinario y en las instalaciones de los animales). Propósito Método Demostrar ausencia de infección en la población Demostrar ausencia de infección en animales individuales antes de los desplazamientos Contribuir a las políticas de erradicación Confirmar casos clínicos Determinar la prevalencia de la infección vigilancia Determinar el estado inmunitario en animales o poblaciones tras la vacunación Identificación del agente 1 RT-PCR en tiempo real RT-PCR en gel de agarosa Aislamiento del virus Detección de respuesta inmunitaria ELISA (específico de serogrupo con VP7) CFT VN Clave: +++ = método recomendado, validado para este propósito; ++ = método idóneo pero que puede precisar una posterior validación; + = puede utilizarse en algunas situaciones, pero el coste, la fiabilidad y otros factores limitan mucho su aplicación; = no adecuado para este propósito; n/a = no aplicable. Aunque no todas las pruebas clasificadas como +++ o ++ han sido validadas formalmente, su uso sistemático y hecho de que se hayan utilizado ampliamente sin resultados dudosos las hace aceptables. RT-PCR = reacción en cadena de la polimerasa con transcripción inversa; ELISA = enzimoinmunoanálisis; CF= fijación del complemento; VN = prueba de neutralización vírica Se dispone de varias técnicas para la identificación vírica de la PE que varían desde el enzimoinmunoanálisis (ELISA) de captura (tipo sándwich indirecto), con anticuerpos poli (PAb) o monoclonales (MAb), hasta la prueba de la reacción en cadena de la polimerasa (PCR), incluyendo PCR con transcripción inversa (RT-PCR) para diferenciar entre los nueve serotipos del VPE, o aislamiento vírico en cultivo celular. Si es posible se debe realizar más de una prueba para diagnosticar un brote de PE, especialmente en el caso cero. La primera prueba puede ser una prueba rápida, como el ELISA o la PCR, seguida del aislamiento del virus en cultivo celular. La neutralización del virus (VN) para identificación del serotipo o la RT-PCR específica de tipo con posterior secuenciación deben realizarse cuanto antes en el curso del brote para que pueda identificarse el serotipo y pueda escogerse la vacuna adecuada. Actualmente no hay estándares internacionales para virus ni para reactivos de diagnóstico, ni tampoco una metodología normalizada para la identificación del VPE. Sin embargo, se ha evaluado una serie de virus y de anticuerpos y en varios laboratorios se han realizado estudios comparativos entre diferentes ELISA de detección de antígeno del VPE y de determinación de anticuerpos contra el VPE, como el Laboratorio de Referencia de la 1 Se recomienda aplicar una combinación de métodos de identificación del agente a una misma muestra clínica.
4 UE para la PE. Los resultados han demostrado un alto nivel de correlación tanto en la detección de antígenos como de anticuerpos al emplear una prueba interna y kits comerciales. Se han llevado a cabo estudios similares con distintas RT-PCR en los que también se ha observado un alto nivel de correlación. En los Laboratorios de Referencia de la OIE para la PE se dispone de más información sobre estudios comparativos de los distintos métodos y kits para el análisis. Un aspecto muy importante del diagnóstico es la selección de muestras y que el transporte al laboratorio se realice de forma segura. Las muestras de elección para diagnóstico son: sangre completa no coagulada extraída de animales enfermos durante la fase febril de la enfermedad, así como pequeños trozos (2 4 g) de bazo, pulmón y ganglios linfáticos de los que hayan muerto. Las muestras se deben mantener a 4 C durante el transporte y procesarse en un corto plazo de tiempo. Se ha utilizado con éxito el aislamiento directo del VPE en líneas celulares de mamíferos: riñón de hámster neonato (BHK-21), células estables de mono (MS), células de riñón de mono verde africano (Vero), y en líneas celulares de insectos: Culicoides y mosquitos. Las muestras de sangre recogidas con un anticoagulante adecuado se pueden usar sin diluir como inóculo. Tras minutos de adsorción, y a una temperatura ambiente de 37 C, los cultivos celulares se lavan y se añade medio de mantenimiento. Alternativamente, y de modo más frecuente, la sangre se lava, se lisa y se diluye a 1/10. Este procedimiento elimina anticuerpos indeseables que podrían neutralizar el virus y favorece la liberación de los virus asociados a la membrana celular de los eritrocitos. Cuando se utilizan muestras de tejidos, como el bazo, el pulmón, etc., se prepara una suspensión de tejido al 10% en solución salina tamponada con fosfato (PBS) o en medio de cultivo celular, que contenga antibióticos. Entre los 2 y 10 días después de la infección puede aparecer un efecto citopático (ECP) en las células de mamíferos. Se deben realizar tres pases ciegos antes de considerar una muestra como negativa. No se observa el efecto citopático en las células de insectos, pero sí puede detectarse la presencia del virus en el sobrenadante entre 7 y 10 días después mediante RT- PCR. El sobrenadante de células de insecto infectadas puede pasarse a continuación sobre células de mamífero, lo cual pondrá de manifiesto ECP tras uno o dos pasos. La RT-PCR es una técnica muy sensible que proporciona una identificación rápida del ácido nucleico del virus de la PE en sangre y otros tejidos de los animales infectados. Esta técnica ha mejorado mucho el diagnóstico laboratorial de la PE gracias a un aumento de la sensibilidad de la detección y a un acortamiento del tiempo necesario para el diagnóstico. La RT-PCR detecta ácido nucleico específico del virus incluso después de que el virus ya no sea viable ni capaz de establecer una nueva infección ni en células de insecto ni en células de mamífero. Por lo tanto, un resultado positivo no necesariamente indica la presencia de virus infeccioso. Se han descrito varias RT-PCR basadas en gel de agarosa para la detección específica de ARN del VPE dirigida a los segmentos víricos 3, 7 u 8 (Aradaib, 2009; Bremer et al., 1998; Laviada et al., 1997; Sakamoto et al., 1994; Stone-Marschat et al., 1994; Zientara et al., 1994). El método más utilizado emplea cebadores correspondientes al extremo 5 (nucleótidos 1-21) y 3 (nucleótidos ) del segmento 7 del ARN (que codifica la VP7), que amplifican todo el segmento vírico (Zientara et al., 1994). Se han desarrollado métodos basados en la RT-PCR en tiempo real (rrt-pcr) para una detección muy sensible y específica de ARN del VPE basados en un par de cebadores y una sonda marcada a partir de secuencias conservadas de los segmentos víricos 3, 5 o 7 (Agüero et al ; Bachanek-Bankowska et al., 2014; Fernández-Pinero et al., 2009; Rodríguez- Sánchez et al., 2008). También se ha descrito una rrt-pcr doble que accede a los segmentos 7 y 8 del genoma (que codifican la NS1 y la NS2, respectivamente) (Quan et al., 2010).
5 Aunque tanto los procedimientos basados en gel como la rrt-pcr pueden detectar cepas de referencia de los nueve serotipos víricos, la rrt-pcr aporta ventajas respecto a los métodos de RT-PCR basados en gel de agarosa, por ofrecer un análisis más rápido, una mayor sensibilidad, e idoneidad para una automatización de alto rendimiento. No obstante, los métodos de RT-PCR basados en gel, en concreto los que amplifican largos fragmentos de ARN (Laviada et al., 1997; Zientara et al., 1994), pueden ser muy útiles en la posterior caracterización genética del virus secuenciando los amplicones. Asimismo, en los laboratorios sin capacidad de llevar a cabo una RT-PCR en tiempo real, pueden resultar ventajosos. En 2015, los Laboratorios de Referencia de la OIE para la PE llevaron a cabo un estudio internacional comparativo para recoger información sobre el rendimiento de los distintos métodos empleados en los principales laboratorios de diagnóstico del VPE. Se evaluaron diez protocolos distintos de RT-PCR. Aunque en este estudio comparativo ciertos métodos no pudieron evaluarse en uno o dos laboratorios, produjeron resultados muy buenos y por lo tanto son adecuados para la posterior evaluación y validación. En el estudio se observó que los métodos de RT-PCR en tiempo real de Agüero et al (2008) y Guthrie et al. (2013) detectaban correctamente todas las cepas representativas incluidas en el estudio internacional con una sensibilidad alta en el análisis de las muestras de campo. Estos métodos están validados para la certificación de animales antes de los desplazamientos, y se describen a continuación. A continuación se dan los detalles de los métodos de la RT-PCR basada en gel y de la RT- PCR en tiempo real para el VPE. La desnaturalización del ARN extraído debe llevarse a cabo antes de la RT-PCR, puesto que el genoma del VPE consiste en una doble hebra de ARN. Las secuencias de los cebadores de la PCR empleados son 5 -GTT-AAA-ATT-CGG-TTA-GGA-TG-3, que corresponde a la polaridad del ARN mensajero, y 5 -GTA-AGT-GTA-TTC-GGT-ATT-G-3, que es complementario de la polaridad del ARN mensajero. Todos los componentes necesarios para la transcripción inversa y la PCR se incluyen en el tubo de reacción que contiene el ARN desnaturalizado. Se lleva a cabo una RT-PCR de un solo paso incubando en un termociclador del siguiente modo: 45 minutos a 1 hora a C, 5 10 minutos a 95 C; a continuación, 40 ciclos de: C durante 1 minuto, 55 C durante 1 1,5 minutos, C durante 2 2,5 minutos, seguidos de un paso de extensión final de 7-8 minutos a C. El análisis de los productos de la PCR se realiza mediante electroforesis en gel de agarosa. Las muestras positivas para PE darán una banda de 1179 pares de bases que puede emplearse como molde en la reacción de secuenciación, utilizando independientemente los cebadores de la PCR, para obtener la secuencia de nucleótidos del segmento viral 7. Esta RT-PCR en tiempo real específica de grupo se ha empleado con buenos resultados en los Laboratorios de Referencia nacionales de los estados miembros de la Unión Europea (UE) que han participado en pruebas anuales de eficiencia llevadas a cabo durante el periodo Asimismo, en un estudio internacional comparativo organizado en 2015 y auspiciado por la red de Laboratorios de Referencia de la OIE, se comprobó que se trataba de uno de los protocolos mejor situados en el ranquin: La diana de esta prueba es el segmento 7 (VP7) del VPE y se describe en Agüero et al. (2008). Es capaz de detectar todos los tipos y cepas del VPE actualmente en circulación. i) Extracción de ARN de muestras de sangre y de tejido Existen kits comerciales fáciles de encontrar; el paso de extracción de ARN se puede llevar a cabo según los procedimientos especificados en cada kit. i Existen a la venta varios kits de RT-PCR en tiempo real de un solo paso que pueden emplearse en función de los requisitos locales o específicos de cada caso, del kit que se utilice y del equipo del que se disponga. A continuación se indican algunos pasos básicos descritos por Agüero et al. (2008). (En la Tabla 2 se indican las secuencias de cebadores y sonda). La concentración de la reserva de cebador se diluye a una concentración de trabajo de 8 µm, mientras que la sonda se diluye a una concentración de trabajo de 50 µm.
6 iv) Se añaden 2,5 µl de cada solución de trabajo de cebador a 8 µm (concentración final de 1 µm) a cada pocillo de la placa de PCR (o tubo o tira) que contenga muestras de ARN o controles positivo o negativo. La placa se deja sobre hielo. v) Se añaden a cada pocillo muestras de 2 µl de ARN, tanto de la muestra problema como de los controles positivo y negativo. vi) v Las muestras se someten a desnaturalización por calor a 95 ºC durante 5 minutos, seguida de un enfriamiento rápido sobre hielo durante 5 minutos más. Se prepara un volumen adecuado de mezcla primaria para RT-PCR simple en tiempo real para la cantidad de muestras que deban analizarse siguiendo las instrucciones del fabricante. La sonda debe incluirse a una concentración final de 0,25 µm (0,1 µl de solución de trabajo de sonda, 50 µm por muestra). vi Se distribuyen 13 µl de mezcla primaria a cada pocillo de la placa de PCR que contenga los cebadores desnaturalizados y el ARN. ix) La placa se sitúa en un termociclador en tiempo real programado con los siguientes tiempos: 48 C 25 minutos 95 C 10 minutos 40 ciclos: 95 C 15 segundos, 55 C 35 segundos, 72 C 30 segundos Si se utilizan unos reactivos y un termociclador que permitan reacciones rápidas, puede aplicarse el siguiente programa: 48 C 25 minutos 95 C 10 minutos 40 ciclos: 97 C 2 segundos, 55 C 30 segundos Los datos de fluorescencia se obtienen al final del paso de 55 ºC. Nota: los tiempos y las temperaturas pueden variar y deben optimizarse para cada reactivo o kit empleado. La prueba no se considerará válida si se obtienen curvas de amplificación atípicas. En tal caso, deberá repetirse. La prueba se considerará positiva cuando se obtenga una curva de amplificación típica y el valor de Ct (el número de ciclos de la reacción en cadena de la polimerasa (PCR) necesarios para que la señal de fluorescencia exceda el fondo) sea inferior o igual al umbral de Ct definido (35) en un máximo de 40 ciclos de PCR (Ct 35). La prueba se considerará inconcluyente cuando se obtenga una curva de amplificación típica y el valor de Ct sea superior al umbral de Ct definido (35) en un máximo de 40 ciclos de PCR (Ct 35). La prueba se considerará negativa cuando se obtenga una curva de amplificación horizontal que no cruce la línea umbral en un máximo de 40 ciclos de PCR. i) Determinación del valor umbral El umbral para establecer un resultado positivo en este método analítico es menos de 35 ciclos de PCR (Ct 35). El umbral para establecer un resultado negativo en este método analítico es de 40 ciclos de PCR. Los resultados situados entre 35 y 40 ciclos de PCR se considerarán inconcluyentes (35 Ct 40). Sensibilidad y especificidad para el diagnóstico La especificidad (DSp) y la sensibilidad (DSe) para el diagnóstico se calculan según el procedimiento detallado en el Capítulo Principios y métodos de validación de las pruebas de diagnóstico de las enfermedades infecciosas.
7 Para estimar la DSe y la DSp del método de la RT-PCR en tiempo real de Agüero, se analizó un total de 186 muestras que se sabía que eran negativas y 132 muestras que se sabía que eran positivas, cifras superiores a las necesarias (73) para realizar una estimación de la DSe y de la DSp del 95% con un 5% de error. La DSe y la DSp calculadas fueron del 97% y del 100%, respectivamente. Por lo tanto, se llega a la conclusión de que el número de muestras de resultado previamente conocido utilizadas para calcular estos parámetros del diagnóstico fue suficiente como para cumplir con los requisitos de la OIE. La reproducibilidad del método de la RT-PCR en tiempo real de Agüero según el estudio internacional comparativo citado anteriormente fue de al menos un 93,55%, e identificó correctamente todas las muestras positivas y negativas analizadas. Todos los laboratorios detectaron diluciones de muestras positivas de hasta al menos En otros programas de comprobación de la eficiencia se han obtenido resultados similares. Se pueden solicitar cepas de referencia de virus inactivados de los serotipos 1-9 al Laboratorio de Referencia de la OIE de España con el fin de llevar a cabo el método de detección por RT-PCR. El método analítico aquí descrito es una adaptación de Guthrie et al. (2013) y permite detectar todos los tipos y cepas conocidos del VPE actualmente en circulación. Esta prueba tiene como diana el segmento 7 (VP7) del VPE. El procedimiento indicado puede requerir alguna modificación para ajustarse a los requisitos de cada laboratorio o del kit de RT-PCR empleado. i) Extracción de ARN de muestras de sangre y de tejido i iv) Existen kits comerciales fáciles de encontrar; el paso de extracción de ARN se puede llevar a cabo según los procedimientos especificados en cada kit. Existen a la venta kits de RT-PCR en tiempo real. A continuación se indican algunos pasos básicos descritos por Guthrie et al. (2013), que pueden modificarse en función de los requisitos locales o específicos de cada caso, del kit que se utilice y del equipo del que se disponga. Se preparan soluciones reserva de mezcla de cebador y sonda a una concentración 25x a 5 µm en el caso de los cebadores directo e inverso, y a 3 µm en el caso de la sonda. Se añaden 5 µl de las muestras de ARN, incluida la muestra problema y los controles positivos y negativo, a los pocillos correspondientes de la placa de PCR (o tubo o tira). v) Las muestras se someten a desnaturalización por calor a 95 ºC durante 2 minutos, y se dejan sobre hielo durante al menos 3 minutos. vi) v Se prepara un volumen adecuado de mezcla primaria para RT-PCR simple en tiempo real para la cantidad de muestras que deban analizarse siguiendo las instrucciones del fabricante. Se incluye 1 µl de solución primaria de mezcla de cebador y sonda 25x (del paso iii anterior) en la mezcla primaria para obtener una concentración final en cada pocillo de 200 nm para cada cebador y 120 nm para la sonda. Se distribuyen 20 µl de mezcla primaria a cada pocillo de la placa de PCR que contenga el ARN desnaturalizado. vi La placa se sitúa en un termociclador en tiempo real programado para la transcripción inversa y la amplificación o detección por fluorescencia del ADNc, según indiquen los fabricantes. El siguiente perfil térmico se indica a modo de ejemplo: 48 C 10 minutos 95 C 10 minutos 40 ciclos: 95 C 15 segundos, 60 C 45 segundos
8 Nota: los tiempos y las temperaturas pueden variar y deben optimizarse para cada reactivo o kit empleado. Las muestras se clasificarán como positivas para el VPE si la fluorescencia normalizada para la prueba de la RT-PCR en tiempo real para el VPE supera un umbral de 0,1 en un máximo de 36 ciclos de PCR en todas las réplicas de una muestra. Las muestras se considerarán inconcluyentes para el VPE si la fluorescencia normalizada para la prueba de la RT-PCR en tiempo real para el VPE supera un umbral de 0,1 en 36 a 40 ciclos de PCR en cualquier réplica de una muestra. Las muestras se clasificarán como negativas para el VPE si la fluorescencia normalizada para la prueba de la RT-PCR en tiempo real para el VPE no supera un umbral de 0,1 en un máximo de 40 ciclos de PCR en todas las réplicas de una muestra y si la fluorescencia normalizada obtenida con el control interno positivo supera un umbral de 0,1 en un máximo de 33 ciclos de PCR. Las muestras se clasificarán como muestras en las que no se ha detectado ácido nucleico del VPE si la fluorescencia normalizada para la prueba del VPE no supera un umbral de 0,1 en un máximo de 40 ciclos de PCR en todas las réplicas de una muestra y si la fluorescencia normalizada obtenida con el control interno positivo no supera un umbral de 0,1 en un máximo de 33 ciclos de PCR. i) Determinación del valor umbral El umbral para establecer un resultado positivo en este método analítico es menos de 36 ciclos de PCR (Ct 35). El umbral para establecer un resultado negativo en este método analítico es de 40 ciclos de PCR. Los resultados situados entre 36 y 40 ciclos de PCR se considerarán inconcluyentes. Sensibilidad y especificidad del diagnóstico La DSe y la DSp de la RR-PCR en tiempo real para la detección de ácido nucleico del VPE en muestras de sangre completa se estimaron por comparación con el aislamiento del virus empleando un modelo de clase latente bayesiano de doble prueba y doble población que permite dependencia condicional (correlación) entre los resultados de la prueba. Para representar casos sospechosos de PE se empleó un total de 503 muestras de sangre equina, correspondientes cada una a un solo caballo con pirexia y uno o más signos clínicos característicos de la PE. También se obtuvieron muestras de sangre de dos poblaciones sanas independientes de caballos (de 503 y 98 caballos cada una, respectivamente) no vacunados contra la PE y con muy poca probabilidad de haber estado expuestos a una infección natural por el VPE; estas muestras se utilizaron para representar casos negativos a la PE. La mediana de la especificidad de la prueba para el diagnóstico superó el 99,9%. La mediana de la sensibilidad de la prueba para el diagnóstico superó el 97,8%. En el estudio internacional comparativo citado anteriormente, se observó que el método de la RT-PCR en tiempo real con sonda FRET de Guthrie tenía una sensibilidad superior al 88,1% y una especificidad del 100%, y que identificó correctamente todas las muestras positivas y negativas analizadas. Todos los laboratorios detectaron diluciones de muestras positivas de hasta al menos 10 5.
9 Agüero et al., 2008 Guthrie et al., 2013 Diana Específico de grupo (VP7) Específico de grupo (VP7) Cebadores (5-3 ) CCA-GTA-GGC-CAG-ATC-AAC-AG CTA-ATG-AAA-GCG-GTG-ACC-GT AGA-GCT-CTT-GTG-CTA-GCA-GCC-T GAA-CCG-ACG-CGA-CAC-TAA-TGA Sonda (5-3 ) FAM-GCT-AGC-AGC-CTA-CCA-CTA-MGB FAM-TGC-ACG-GTC-ACC-GCT-MGB Temperatura de hibridación Número de ciclos para la amplificación 55 C 60 C Sensibilidad analítica (LOD) Dilución a 10 5 de una suspensión vírica de la cepa de referencia AHSV-4 con un título de 10 6,3 DICT 50 /ml, que corresponde a un Ct de 34,3±0.5 (10 1,3 DICT 50 /ml ) Dilución a 3, de muestras de sangre positivas para el VPE, con un Ct de 35,71 Especificidad diagnóstica Sensibilidad diagnóstica 100% 99,9%. 97% 97,8%. Hasta hace poco, la prueba de la VN ha sido el método de elección para la tipificación, así como el método de referencia para identificar VPE aislados del campo empleando antisueros específicos de tipo (Verwoerd, 1979). Esta técnica tarda 5 o más días en dar resultados. El desarrollo de RT-PCR basada en gel específica de tipo (Maan et al., 2011; Sailleau et al., 2000), así como de la RT-PCR en tiempo real en la que se emplean sondas (Koekemoer, 2008) que tienen por objetivo el Seg-2 del VPE para la identificación y diferenciación de genotipos del VPE, aporta métodos rápidos de tipificación de los VPE en muestras de tejido y en sangre. Estos métodos se pueden utilizar para aumentar considerablemente la rapidez y la fiabilidad de la detección y la identificación (en comparación con las pruebas de VN) de los nueve serotipos del VPE. Más recientemente, Bachanek-Bankowska et al., 2014, Weyer et al., 2015 han desarrollado RT-PCR en tiempo real específicas de tipo basadas en el uso de sondas Taqman con grupo MGB. No obstante, la variación genética que puede aparecer con el tiempo en el genoma del VPE, en concreto en la región que codifica la proteína VP2, lugar para el cual deben diseñarse cebadores/sondas específicos para las pruebas de tipificación, hace difícil que se puedan detectar todas las variantes genéticas de cada serotipo mediante este tipo de técnica. Por tanto, aunque existen métodos moleculares que pueden tipificar rápidamente el VPE en muchas muestras de campo positivas, la VN debe mantenerse como prueba de referencia para serotipar las cepas del VPE. Se ha demostrado que los ELISA de bloqueo indirectos y de competición en los que se usa o bien antígeno soluble de VPE o proteína recombinante VP7 (Hamblin et al., 1990; Laviada et al., 1992b; Maree & Paweska, 2005; Wade Evans et al., 1993) son buenos métodos para la detección de anticuerpos reactivos frente al grupo de VPE, sobre todo en investigaciones a gran escala (Rubio et al., 1998). Estas dos pruebas han sido reconocidas por la Comisión Europea (2002). El ELISA de bloqueo de competición también se puede utilizar para analizar animales salvajes puesto que no es preciso emplear una anti-globulina específica de especie. Se ha adaptado una prueba de inmunotransferencia para la determinación de anticuerpos anti-pe (Laviada et al., 1992b), que es especialmente adecuado para pequeños números de sueros. Se ha utilizado mucho la prueba de la fijación del complemento (CF), pero algunos sueros son anti-complementarios, especialmente los de burro y cebra.
10 La técnica del ELISA de bloqueo de competición tiene por objetivo detectar anticuerpos específicos contra el VPE, y es aplicable a cualquier especie equina. La VP7 es la principal proteína antigénica de la estructura molecular del VPE y se conserva en los nueve serotipos del VPE. En esta prueba, se utiliza un MAb dirigido contra la VP7, lo cual permite una alta sensibilidad y especificidad. Además, también permite analizar especies distintas del caballo (como asnos, cebras, etc.), evitando así el problema de especificidad que en ocasiones surge cuando se emplean los ELISA indirectos. El antígeno recombinante de la VP7 es no infeccioso, lo cual aporta un alto nivel de seguridad (Comisión Europea, 2002). El principio de esta prueba es bloquear la reacción específica que tiene lugar entre la proteína VP7 recombinante absorbida en una placa de ELISA y un MAb conjugado contra la VP7. Los anticuerpos contra el VPE presentes en una muestra de suero problema bloquearán esta reacción. Así pues, una disminución en la cantidad de color indica la presencia de anticuerpos contra el VPE en la muestra de suero. Está a la venta el ELISA de bloqueo de competición. i) Fase sólida: Recubrir las placas de ELISA de 96 pocillos con ng de VP7 recombinante de VPE-4 diluida en tampón carbonato/bicarbonato, ph 9,6. Incubar toda la noche a 4 C i iv) Lavar las placas tres veces con PBS 0,1x que contenga NaCl 0,135 M y Tween 20 al 0,05% (v/v) (solución de lavado). Tocar suavemente las placas con un material absorbente para eliminar los posibles residuos del lavado Muestras problema: Las muestras de suero a analizar, y sueros control positivos y negativos (si no vienen listos para su uso en el kit), se diluyen a 1/5 en diluyente que contenga NaCl 0,35 M, Tween 20 al 0,05%; y Kathon al 0,1%, a razón de 100 µl por pocillo. Se incuban 1 hora a 37 C. Lavar las placas cinco veces con PBS 0,1x que contenga NaCl 0,135 M y Tween 20 al 0,05% (v/v) (solución de lavado). Tocar suavemente las placas con un material absorbente para eliminar los posibles residuos del lavado v) Conjugado: Se distribuyen 100 µl/pocillo de MAb anti-vp7 conjugado a peroxidasa de rábano. Este MAb se ha diluido previamente a 1/5000 1/15000 en una solución 1/1 de StabiliZyme Select Stabilizer (SurModics. Referencia: SZ03) en agua destilada. Se incuba 30 minutos a 37 C. vi) v Se lavan las placas como se describe en el paso iv. Sustrato/cromógeno: se añaden 100 µl/pocillo de solución de sustrato/cromógeno, es decir, 1 ml de ABTS (ácido 2,2'-azino-di-[3-etil- benzotiazolina]-6-sulfónico), 5 mg/ml + 9 ml de tampón sustrato (tampón fosfato/citrato 0,1 M, ph 4, que contenga H 2 O 2 al 0,03%) y se incuba 10 minutos a temperatura ambiente. La aparición de color se detiene añadiendo 100 µl/pocillo de SDS al 2% (p/v). Pueden utilizarse otros sistemas de cromógeno (como la tetrametil benzidina). vi Se leen las placas a 405 nm. ix) Interpretación de los resultados: se determina el porcentaje de bloqueo (BP) de cada muestra aplicando la siguiente fórmula: BP= Abs (control ) Abs (muestra) Abs (control ) Abs (control + ) 100 Las muestras que presenten un valor de BP inferior al 45% se considerarán negativas a anticuerpos contra el VPE. Las que presenten un valor de BP superior al 50% se considerarán positivas a anticuerpos contra el VPE. Las muestras con valores de BP de entre el 45% y el 50% se considerarán dudosas y deberán volver a analizarse. Si vuelve a obtenerse el mismo resultado, se tomará una nueva muestra y se analizará 2 semanas después.
11 Para la determinación de anticuerpos contra el VPE se ha usado como antígeno 2 la proteína VP7 recombinante con un alto grado de sensibilidad y especificidad (Laviada et al., 1992b; Maree & Paweska, 2005). Otras ventajas de este antígeno son su estabilidad y su falta de infectividad. El conjugado empleado en este método es un anticuerpo anti gamma-globulina de caballo conjugado a peroxidasa de rábano que reacciona con suero de caballos, mulos y asnos. El método descrito por Maree & Paweska (2005) emplea proteína G como conjugado que también reacciona con suero de cebra. i) Fase sólida: Recubrir las placas de ELISA de 96 pocillos con VP7 recombinante de VPE-4 diluida en tampón carbonato/bicarbonato, ph 9,6. Incubar toda la noche a 4 C. i iv) Lavar las placas cinco veces con agua destilada que contenga Tween 20 al 0,01% (v/v) (solución de lavado). Tocar suavemente las placas con un material absorbente para eliminar los posibles residuos del lavado. Bloquear las placas con PBS, ph 7,2 + leche desnatada al 5% (p/v), 200 µl/pocillo, durante 1 hora a 37 C. Retirar la solución de bloqueo y limpiar suavemente las placas con un material absorbente. v) Muestras problema: Las muestras de suero problema, y los controles de suero positivo y negativo, se diluyen 1/25 en PBS + leche desnatada al 5% (p/v) + Tween 20 al 0,05% (v/v), 100 µl por pocillo. Se incuban 1 hora a 37 C. Para la titulación, se añaden diluciones seriadas a la mitad desde 1/25 (100 µl por pocillo), poniendo un suero en cada columna de la placa, dos columnas por suero, y se hace lo mismo con los controles positivos y negativos. Se incuba 1 hora a 37 C. vi) v Se lavan las placas como en el paso (. Conjugado: Se depositan 100µl/pocillo de anticuerpos anti gamma-globulina de caballo conjugados con peroxidasa de rábano y diluidos en PBS + leche al 5% + Tween 20 al 0,05%, ph 7,2. Se incuban 1 hora a 37 C. vi Se lavan las placas como en el paso (. ix) Cromógeno/Sustrato: Se añaden 200 µl/pocillo de solución de cromógeno/substrato (10 ml de DAMB [ácido 3-(dimetilamino) benzoico] 80,6 mm+ 10 ml de TBTH [3-metil-2- benzotiazolinona hidrazona]1,56 mm+ 5 µl de H 2 O 2 ). Después de unos 5 10 minutos, el desarrollo del color se detiene por adición de 50 µl de H 2 SO 4 3N (antes de que el control negativo se empiece a colorear). También se pueden usar otros cromógenos, como ABTS, tetrametil benzidina u ortofenildiamina. x) Se leen las placas a 600 nm (o a 620 nm) xi) Interpretación de los resultados: Se calcula el valor de corte añadiendo 0,06 al valor del control negativo (0,06 es la desviación estándar derivada de un grupo de 30 sueros negativos). Las muestras problema que den valores de absorbancia menores que el corte se consideran negativas. Las muestras problema que den valores de absorbancia mayores que el corte + 0,15 se consideran positivas. Las muestras con valores intermedios de absorbancia se consideran dudosas y se requiere una segunda técnica para confirmar el resultado. La CF se ha empleado mucho en el pasado, pero actualmente se utiliza menos y se ha sustituido en mucho laboratorios por el ELISA como técnica de detección sistemática. Esta sustitución progresiva se debe a la mayor sensibilidad y grado de estandarización del ELISA, así como al hecho de que una cantidad considerable de sueros tienen actividad anti-complementaria. No obstante, la prueba de la CF es una herramienta útil en zonas endémicas para la demostración y titulación de anticuerpos IgM específicos de grupo contra el VPE, sobre todo tras una infección o vacunación reciente. 2 El antígeno puede solicitarse al Centro de Investigación en Sanidad Animal (CISA), España. El tiempo de espera para la entrega es de unos 4-6 meses.
12 i) Solución salina tamponada con Veronal que contiene un 1% de gelatina (VBSG). i iv) Las muestras de suero, libres de eritrocitos, deben ser inactivadas por calor: el suero de caballo a 56 C, el de cebra a 60 C y el de asno a 62 C, durante 30 minutos. El antígeno es un extracto en sacarosa/acetona de encéfalo de ratón infectado por VEP. El antígeno control es encéfalo de ratón no infectado, extraído del mismo modo. En ausencia de un suero estándar internacional, el antígeno debe titularse frente a un suero control positivo preparado localmente. En la prueba, se utilizan de cuatro a ocho unidades. El antígeno también se puede obtener mediante inoculación del virus en un cultivo celular adecuado (véase el apartado B.1. anterior). El complemento es un suero normal de cobaya. v) La hemolisina es un suero de conejo hiperinmune contra eritrocitos de oveja (SRBC). vi) v Los SRBC se obtienen por punción aséptica de la vena yugular y se conservan en solución de Alsever 3 o en citrato sódico. El sistema hemolítico (HS) se prepara diluyendo la hemolisina hasta contener dos dosis hemolíticas y usando esto para sensibilizar a los SRBC lavados. Los SRBC se estandarizan a una concentración del 3%. vi Sueros control: Se obtiene localmente un suero control positivo y se valida. Como suero control negativo se utiliza suero de un caballo sano negativo a anticuerpos. i) La reacción se lleva a cabo en placas de microtitulación de 96 pocillos de fondo redondeado en un volumen final de 100 µl/pocillo, o en tubos si se emplea la macrotécnica, a 4 C durante 18 horas. i iv) Todos los sueros, muestras y controles se diluyen a 1/5 en VBSG y 25 µl de cada suero se añaden por duplicado. SE prepara una serie de diluciones a la mitad de cada suero a partir de 1/5 y hasta 1/180. Se añaden 25 µl del antígeno diluido según la titulación previa. Se añaden 25 µl del complemento diluido según una titulación previa. v) Se incuba a 4 C durante 18 horas. vi) v 25 µl de HS se añaden a todos los pocillos de la placa de microtitulación. La placa se incuba 30 minutos a 37 C. vi A continuación, las placas se centrifugan a 200 g, y a cada pocillo se asigna una puntuación de presencia de hemólisis. Se emplean sueros, complemento, antígeno y HS control. ix) Los resultados se leen empleando hemólisis en el 50% como punto final. La inversa de la dilución más alta de suero que fije específicamente complemento con el antígeno de la CF será considerado el título. x) Un título de 1/10 o superior es positivo, e inferior a 1/10, negativo. El anticuerpo específico para un serotipo se puede detectar mediante la utilización de la VN (House et al., 1990). Esta prueba puede tener un valor adicional en la vigilancia y transmisión epidemiológicas, principalmente en zonas endémicas donde es probable que haya múltiples serotipos. i) A partir de una dilución inicial de 1/5, se preparan diluciones seriadas a la mitad de los sueros problema en una placa de microtitulación de 96 pocillos de fondo plano y grado cultivo celular, empleando medio de cultivo como diluyente. Para cada muestra se emplean dos pocillos a cada dilución. En cada lote de análisis deben incluirse también sueros control, positivo y negativo. A cada pocillo se añade un volumen igual (por 3 20,5 g de dextrosa (114 mm), 7,9 g de citrato sódico 2 H2O (27 mm), 4,2 g NaCl (71 mm), H2O hasta 1 litro. Ajustar el ph con ácido cítrico 1 M.
13 i ejemplo, de 25 µl) de una reserva del VPE que contenga 100 DICT 50 (dosis infectiva en el 50% de los cultivos tisulares expuestos). Las mezclas suero/virus se incuban 60 minutos a 37 C con un 5% de CO 2 y un 95% de humedad antes de añadir a cada pocillo problema 0,1 ml de una suspensión de células Vero ( células/ml). Se prepara una titulación por retroceso de la reserva de virus para cada prueba usando cuatro pocillos por dilución decimal, con 25 µl por pocillo. Las placas problema se incuban a 37 C, con un 5% de CO 2, y con un 95% de humedad, durante 4 5 días, hasta que la titulación por retroceso indique que el virus reserva contiene DICT 50. iv) Tras una incubación de 4-5 días, la prueba se lee mediante microscopio invertido. Se puntúan los pocillos en función de la presencia o ausencia de ECP. La presencia de ECP en los pocillos con muestra de suero indica que el suero problema no contiene anticuerpos neutralizantes específicos contra el virus de la prueba y que el virus no se ha neutralizado, y por lo tanto se ha producido lisis celular con la consiguiente destrucción de la capa celular. Por el contrario, la ausencia de ECP en los pocillos que contienen la muestra de suero indica que el suero problema contiene anticuerpos neutralizantes específicos contra el virus de la prueba que permiten neutralizar el virus, y por lo tanto la capa celular se ha mantenido intacta. v) Como alternativa, las placas se fijan y se tiñen con una solución de cristal violeta al 0,15% (p/v) en glutaraldehído al 2% (v/v) y se lavan. Como alternativa, se pueden fijar con etanol y teñirlas con fucsina básica al 1%. vi) El título del suero a punto final del 50% se calcula por el método de Sperman Kärber y se expresa como log 10 negativo. Las vacunas vivas atenuadas poli o monovalentes contra PE que están basadas en la selección de macrófagos genéticamente estables que producen macroplacas de lisis en cultivos de células Vero se han utilizado para el control del VPE en África y otros (Erasmus, 1976; Sánchez-Vizcaíno, 2004). Se comercializan vacunas polivalentes. A principios de los años 1990 se produjo comercialmente una vacuna monovalente inactivada contra el VPE (de serotipo 4) basada en la purificación e inactivación del virus con formalina, pero ya no está disponible en la actualidad (House et al., 1992). Se han utilizado en distintas combinaciones para inmunizar caballos vacunas de subunidad contra el VPE basadas en las proteínas de la cápsida externa VP2 y VP5, más la proteína de la cápsida interna VP7, derivadas de baculovirus recombinantes que funcionaban como vectores de expresión simples y duales (Martinez et al., 1996). También se evaluó la eficacia protectora de la VP2 en una vacuna de subunidad (Scanlen et al., 2002). No obstante, estas vacunas no se comercializan. Actualmente, solo se comercializan las únicas vacunas que se comercializan contra la PE son las vivas atenuadas (polivalentes o monovalentes). Las directrices para la producción de vacunas veterinarias se indican en el capítulo Principios de producción de vacunas veterinarias. Las normas dadas aquí y en el pretenden ser de carácter general y pueden suplementarse con requisitos nacionales y regionales.
14 El inóculo de virus se prepara a partir de VPE genéticamente estable tomado de grandes placas de lisis seleccionadas en células Vero con bajo nivel de pases. Se liofiliza una gran cantidad de este antígeno y se guarda a 20 C como reserva de antígeno para la siembra. Por técnicas apropiadas debe demostrarse que el virus de inóculo está libre de virus, bacterias y micoplasmas contaminantes. Se debe confirmar la identidad del serotipo del virus de inóculo. Al principio de una fase de producción, se producen antígenos de trabajo en cultivos celulares de células BHK-21 o Vero a partir de la reserva de antígeno de inóculo. Se comprueba la esterilidad, pureza e identidad de los antígenos de trabajo, que deben contener un mínimo de unidades formadoras de placas (UFP)/ml del virus infeccioso. Los cultivos de células Vero se cultivan en frascos rotatorios usando en el medio suero bovino irradiado con rayos gamma. Una vez los cultivos llegan a ser confluentes, el medio se elimina y las células se siembran con los antígenos de trabajo. Tras 1 hora, se añade a los cultivos medio de mantenimiento. La incubación prosigue durante 2 3 días a 37 C. Cuando el ECP está avanzado, se recogen tanto las células como el medio líquido sobrenadante. Los productos del mismo serotipo se agrupan y se guardan a 4 C. Se comprueba la esterilidad del material recogido de los serotipos individuales y se comprueba la infectividad mediante titulación de formación de placas en cultivos de células Vero. El título mínimo aceptable es de UFP/ml. Finalmente, se preparan dos vacunas polivalentes mezclando volúmenes iguales de los serotipos 1, 3, 4 y 2, 6, 7, 8 respectivamente. También se puede preparar un tipo monovalente. Tras la adición de un estabilizador apropiado, la vacuna se distribuye en volúmenes de 1,0 ml en viales de vidrio y se liofiliza. i) Esterilidad Después de la liofilización, se seleccionan al azar cinco frascos de vacuna y se comprueba su esterilidad mediante métodos aceptados internacionalmente. Las pruebas de esterilidad y ausencia de contaminación de los productos biológicos se indican en el capítulo i Inocuidad La inocuidad de una vacuna se comprueba mediante inoculación de la vacuna reconstituida en ratones (0,25 ml, por vía intraperitoneal), cobayas (1,0 ml, por vía intraperitoneal), y un caballo (5,0 ml, por vía subcutánea). Todos los animales se observan a diario durante 14 días. La temperatura rectal del caballo se toma dos veces al día durante 14 días y nunca debe superar los 39 C. Potencia del lote La potencia depende en gran medida de la concentración de virus en la vacuna. La dosis inmunizante mínima para cada serotipo es de alrededor de UFP/dosis. El título de infectividad del producto final se analiza por titulación de placas en cultivo de
15 células Vero y debe contener al menos UFP/dosis. El caballo utilizado en la prueba de inocuidad se utiliza también para determinar la inmunogenicidad de una vacuna. Se toman muestras de suero el día de la vacunación y 21 días después, y se comprueba si contiene anticuerpos neutralizantes contra cada serotipo por la prueba de reducción de placas usando diluciones seriadas a la mitad y unas 100 UFP de virus. El caballo debe desarrollar un título de anticuerpos neutralizantes de al menos 20 contra un mínimo de tres de los cuatro serotipos presentes en la vacuna tetravalente. No existe ninguna directriz descrita para las vacunas contra la PE. No obstante, sí existe una en la UE para el virus de la lengua azul aplicable en circunstancias excepcionales, que probablemente podría aplicarse también al virus de la PE. Esta directriz incluye los requisitos mínimos par la autorización, en circunstancias excepcionales, de la producción de vacuna para uso en emergencias contra el virus de la lengua azul (Reglamento CE Nº726/2004, en concreto, los Artículos 38, 39 y 43 del mismo, y el Artículo 26 de la Directiva 2001/82/EC), incluidas medidas para facilitar la rápida inclusión de serotipos víricos nuevos o distintos. Ninguna comercializada. Se han descrito vacunas experimentales de subunidades, véase el apartado C.1.1, arriba. Ninguno. AGÜERO M., GÓMEZ-TEJEDOR C., ANGELES CUBILLO M., RUBIO C., ROMERO E. & JIMÉNEZ-CLAVERO A. (2008). Realtime fluorogenic reverse transcription polymerase chain reaction assay for detection of African horse sickness virus. J. Vet. Diagn. Invest., 20, ARADAIB I.E. (2009). PCR detection of African horse sickness virus serogroup based on genome segment three sequence analysis. J. Virol. Methods, 159 (1),1 5. BACHANEK-BANKOWSKA K., MAAN S., CASTILLO-OLIVARES J., MANNING N.M., MAAN N.S., POTGIETER A.C., DI NARDO A., SUTTON G., BATTEN C. & MERTENS P.P. (2014). Real-time RT-PCR assays for detection and typing of African horse sickness virus. PLoS One, 9 (4), e BAYLIS M., MELLOR P.S. & MEISWINKEL R. (1999). Horse sickness and ENSO in South Africa. Nature, 397, 574. BREMER C.W., DUNGU-KIMBENGA B. & VILJOEN G.J. (1998). Detection of African horsesickness virus in Zebra by RT- PCR and the development of different methods for confirming AHSV specificity of RT-PCR products. Proceedings of the Eighth International Conference on Equine Infectious Diseases, Dubai, March R & W Publications (Newmarket) Ltd, Newmarket, UK. COETZER J.A.W. & GUTHRIE.A.J. (2005). African horsesickness. In: Infectious Diseases of Livestock, Second Edition. Coetzer J.A.W. & Tustin R.C., eds. Oxford University Press, Cape Town, ERASMUS B.J. (1976). A new approach to polyvalent immunisation against African horse sickness. In: Proceedings of the Fourth International Conference on Equine Infectious Diseases, Lyon, France, September Princeton, N.J. Veterinary Publications, USA, EUROPEAN COMMISSION (2002). Commission decision of 21 February 2002 amending Annex D to Council Directive 90/426/EEC with regard to the diagnostic tests for African horse sickness. Off. J. European Communities, L53,
ANEXO «ANEXO IV PESTE EQUINA DIAGNÓSTICO PARTE A. Pruebas serológicas
 18.10.2016 L 280/35 ANEXO «ANEXO IV PTE EQUINA DIAGNÓSTICO PARTE A Pruebas serológicas El método serológico descrito a continuación consiste en pruebas de inmunoabsorción enzimática (ELISA) basadas en
18.10.2016 L 280/35 ANEXO «ANEXO IV PTE EQUINA DIAGNÓSTICO PARTE A Pruebas serológicas El método serológico descrito a continuación consiste en pruebas de inmunoabsorción enzimática (ELISA) basadas en
(Texto pertinente a efectos del EEE)
 18.10.2016 L 280/33 DECISIÓN DE EJECUCIÓN (UE) 2016/1840 DE LA COMISIÓN de 14 de octubre de 2016 que modifica el anexo IV de la Directiva 2009/156/CE del Consejo en lo que respecta a los métodos de diagnóstico
18.10.2016 L 280/33 DECISIÓN DE EJECUCIÓN (UE) 2016/1840 DE LA COMISIÓN de 14 de octubre de 2016 que modifica el anexo IV de la Directiva 2009/156/CE del Consejo en lo que respecta a los métodos de diagnóstico
PCR gen 16S ARNr bacteriano
 PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
PESTE EQUINA AFRICANA African Horse Sickness
 PESTE EQUINA AFRICANA African Horse Sickness Virus RNA doble cadena Familia Reoviridae Genero Orbivirus Arbovirus (Arthropod-borne) Viscerotrópico Generalidades Enfermedad no contagiosa El pico de la enfermedad
PESTE EQUINA AFRICANA African Horse Sickness Virus RNA doble cadena Familia Reoviridae Genero Orbivirus Arbovirus (Arthropod-borne) Viscerotrópico Generalidades Enfermedad no contagiosa El pico de la enfermedad
TEMA 14. Métodos inmunológicos para la identificación microbiana
 TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
GLOSARIO DE TÉRMINOS
 GLOSARIO DE TÉRMINOS Las definiciones dadas a continuación se han seleccionado con el criterio restrictivo de incluir solamente las que pueden ser de utilidad para los usuarios del Manual de animales terrestres.
GLOSARIO DE TÉRMINOS Las definiciones dadas a continuación se han seleccionado con el criterio restrictivo de incluir solamente las que pueden ser de utilidad para los usuarios del Manual de animales terrestres.
Papel de Laboratorio: Chikungunya Logros y retos para la vigilancia por laboratorio
 Papel de Laboratorio: Chikungunya Logros y retos para la vigilancia por laboratorio Reunión de la Sala Regional de Situación de Salud Tema: Chikungunya 2 de julio del 2015 Naomi Iihoshi SE-COMISCA Chikungunya
Papel de Laboratorio: Chikungunya Logros y retos para la vigilancia por laboratorio Reunión de la Sala Regional de Situación de Salud Tema: Chikungunya 2 de julio del 2015 Naomi Iihoshi SE-COMISCA Chikungunya
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO
 SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
RESOLUCIÓN OIV/OENO 427/2010
 RESOLUCIÓN OIV/OENO 427/2010 CRITERIOS PARA LOS MÉTODOS DE CUANTIFICACIÓN DE LOS RESIDUOS, POTENCIALMENTE ALERGÉNICOS, DE PROTEÍNAS USADAS EN LA CLARIFICACIÓN DE LOS VINOS La ASAMBLEA GENERAL, De conformidad
RESOLUCIÓN OIV/OENO 427/2010 CRITERIOS PARA LOS MÉTODOS DE CUANTIFICACIÓN DE LOS RESIDUOS, POTENCIALMENTE ALERGÉNICOS, DE PROTEÍNAS USADAS EN LA CLARIFICACIÓN DE LOS VINOS La ASAMBLEA GENERAL, De conformidad
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE MEDICINA VETERINARIA Y ZOOTECNIA
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE MEDICINA VETERINARIA Y ZOOTECNIA. Estudio comparativo del diagnóstico del virus del PRRS por RT-PCR, PCR anidada y RT-PCR en tiempo real. Zoalli Angélica
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE MEDICINA VETERINARIA Y ZOOTECNIA. Estudio comparativo del diagnóstico del virus del PRRS por RT-PCR, PCR anidada y RT-PCR en tiempo real. Zoalli Angélica
GLOSARIO DE TÉRMINOS
 GLOSARIO DE TÉRMINOS Las definiciones dadas a continuación se han seleccionado con el criterio restrictivo de incluir solamente las que pueden ser de utilidad para los usuarios del Manual de animales terrestres.
GLOSARIO DE TÉRMINOS Las definiciones dadas a continuación se han seleccionado con el criterio restrictivo de incluir solamente las que pueden ser de utilidad para los usuarios del Manual de animales terrestres.
TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES
 TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES 1. Objetivo del diagnóstico microbiológico 2. Toma de muestra 3. Diagnóstico directo - bacterias - hongos - protozoos -
TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES 1. Objetivo del diagnóstico microbiológico 2. Toma de muestra 3. Diagnóstico directo - bacterias - hongos - protozoos -
2. ESTRATEGIA PARA EFECTUAR LA CLONACION Y EXPRESION DEL GEN
 1. CONTROL FINAL Nombre Internacional y nombre de la vacuna Nombre del propietario Nombre y dirección del fabricante Número de Lote Fecha de fabricación Fecha de caducidad Temperatura de almacenamiento
1. CONTROL FINAL Nombre Internacional y nombre de la vacuna Nombre del propietario Nombre y dirección del fabricante Número de Lote Fecha de fabricación Fecha de caducidad Temperatura de almacenamiento
DIAGNÓSTICO DE LABORATORIO DE LA INFECCIÓN POR EL VIRUS DE LA DIARREA VÍRICA BOVINA (BVDV)
 DIAGNÓSTICO DE LABORATORIO DE LA INFECCIÓN POR EL VIRUS DE LA DIARREA VÍRICA BOVINA (BVDV) Debido a los distintos cuadros que puede originar el BVDV el diagnóstico clínico es complicado. En función de
DIAGNÓSTICO DE LABORATORIO DE LA INFECCIÓN POR EL VIRUS DE LA DIARREA VÍRICA BOVINA (BVDV) Debido a los distintos cuadros que puede originar el BVDV el diagnóstico clínico es complicado. En función de
Parvovirosis canina: Qué ha cambiado realmente con las nuevas variantes virales?
 Parvovirosis canina: Qué ha cambiado realmente con las nuevas variantes virales? Virus de la Parvovirosis canina (CPV): Familia Parvoviridae, pequeño virus de genoma DNA simple hebra de 5.2 Kb. Su genoma
Parvovirosis canina: Qué ha cambiado realmente con las nuevas variantes virales? Virus de la Parvovirosis canina (CPV): Familia Parvoviridae, pequeño virus de genoma DNA simple hebra de 5.2 Kb. Su genoma
HBsAg CONFIRMATORY TEST INTERÉS CLÍNICO
 HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS. INTERÉS CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS. INTERÉS CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
AMPLIFICACIÓN Y DETECCIÓN POR PCR DEL LOCUS HUMANO D1S80
 AMPLIFICACIÓN Y DETECCIÓN POR PCR DEL LOCUS HUMANO D1S80 Ref. PCR1 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción
AMPLIFICACIÓN Y DETECCIÓN POR PCR DEL LOCUS HUMANO D1S80 Ref. PCR1 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción
INFLUENZA AVIAR ALTAMENTE PATÓGENA (PESTE AVIAR)
 INFLUENZA AVIAR ALTAMENTE PATÓGENA (PESTE AVIAR) 1) Señala la respuesta falsa sobre la inactivación del virus de la influenza aviar altamente a. A 53 ºC durante 3 horas o a 60 Cº durante 30 minutos. b.
INFLUENZA AVIAR ALTAMENTE PATÓGENA (PESTE AVIAR) 1) Señala la respuesta falsa sobre la inactivación del virus de la influenza aviar altamente a. A 53 ºC durante 3 horas o a 60 Cº durante 30 minutos. b.
ESTRUCTURA Y PROPIEDADES DE LOS ROTAVIRUS
 ROTAVIRUS EQUINO ESTRUCTURA Y PROPIEDADES DE LOS ROTAVIRUS 123 4 5 6 Segmentos RNA dc Proteínas VP1 VP2 VP3 VP4 NSP1 VP6 VP2 Core - 15% de la masa total del virión VP6 Cápside interna Ag de grupo y subgrupo
ROTAVIRUS EQUINO ESTRUCTURA Y PROPIEDADES DE LOS ROTAVIRUS 123 4 5 6 Segmentos RNA dc Proteínas VP1 VP2 VP3 VP4 NSP1 VP6 VP2 Core - 15% de la masa total del virión VP6 Cápside interna Ag de grupo y subgrupo
1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS
 1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS Existen diferentes métodos para la obtención de ADN bacteriano que varían en duración y complejidad del procedimiento en función de la calidad del ADN que queramos
1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS Existen diferentes métodos para la obtención de ADN bacteriano que varían en duración y complejidad del procedimiento en función de la calidad del ADN que queramos
Identificación del agente: Pruebas serológicas: Requisitos para las vacunas
 La lengua azul (LA) es una enfermedad infecciosa y no contagiosa transmitida por vectores que afecta a rumiantes domésticos y salvajes, como ovejas, cabras, bovinos, búfalos, ciervos, la mayor parte de
La lengua azul (LA) es una enfermedad infecciosa y no contagiosa transmitida por vectores que afecta a rumiantes domésticos y salvajes, como ovejas, cabras, bovinos, búfalos, ciervos, la mayor parte de
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS
 HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
RESULTADOS Y DISCUSIÓN
 RESULTADOS Y DISCUSIÓN Extracción de ADN en sangre periférica La técnica de extracción por GeneClean empleada en este trabajo dio un buen rendimiento, ya que la cantidad de ADN y el nivel de purificación
RESULTADOS Y DISCUSIÓN Extracción de ADN en sangre periférica La técnica de extracción por GeneClean empleada en este trabajo dio un buen rendimiento, ya que la cantidad de ADN y el nivel de purificación
Inmunología. Curso Tema 29
 Inmunología. Curso 2009-10. Tema 29 TEMA 29.- Sistemas de inmunización activa. Vacunas. Vacunas vivas y vacunas inactivadas. Autovacunas. Nuevas estrategias en la elaboración de vacunas. Vacunas de subunidades,
Inmunología. Curso 2009-10. Tema 29 TEMA 29.- Sistemas de inmunización activa. Vacunas. Vacunas vivas y vacunas inactivadas. Autovacunas. Nuevas estrategias en la elaboración de vacunas. Vacunas de subunidades,
ESTUDIO DE POLIMORFISMOS ALU HUMANOS POR PCR
 ESTUDIO DE POLIMORFISMOS ALU HUMANOS POR PCR Ref. PCRALU 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena
ESTUDIO DE POLIMORFISMOS ALU HUMANOS POR PCR Ref. PCRALU 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena
Diagnóstico microbiológico de las hepatitis virales. Juan Carlos Rodríguez S. Microbiología Hospital General Universitario de Alicante
 Diagnóstico microbiológico de las hepatitis virales Juan Carlos Rodríguez S. Microbiología Hospital General Universitario de Alicante Hepatitis A. Características generales Provoca enfermedad aguda en
Diagnóstico microbiológico de las hepatitis virales Juan Carlos Rodríguez S. Microbiología Hospital General Universitario de Alicante Hepatitis A. Características generales Provoca enfermedad aguda en
RESULTADOS Y DISCUSIÓN
 RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
Recomendaciones para definir los casos de enfermedades ocasionadas por el virus del Ébola o de Marburgo 9 de agosto de 2014
 Recomendaciones para definir los casos de enfermedades ocasionadas por el virus del Ébola o de Marburgo 9 de agosto de 2014 Traducción creada el 8 de septiembre de 2014. Realizada y revisada por el equipo
Recomendaciones para definir los casos de enfermedades ocasionadas por el virus del Ébola o de Marburgo 9 de agosto de 2014 Traducción creada el 8 de septiembre de 2014. Realizada y revisada por el equipo
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Kit artus EBV QS-RGQ. Características de rendimiento. Mayo Sample & Assay Technologies. Sensibilidad analítica (plasma)
 Kit artus EBV QS-RGQ Características de rendimiento Kit artus EBV QS-RGQ, versión 1, 4501363 Compruebe la disponibilidad de nuevas revisiones electrónicas de las especificaciones en www.qiagen.com/products/artusebvpcrkitce.aspx
Kit artus EBV QS-RGQ Características de rendimiento Kit artus EBV QS-RGQ, versión 1, 4501363 Compruebe la disponibilidad de nuevas revisiones electrónicas de las especificaciones en www.qiagen.com/products/artusebvpcrkitce.aspx
Clamidia MIF IgG. Características de rendimiento. Código del producto IF1250G Rev. J. No para su distribución en Estados Unidos
 Código del producto IF1250G Rev. J Características de rendimiento No para su distribución en Estados Unidos VALORES ESPERADOS Población con neumonía adquirida en la comunidad Dos investigadores externos
Código del producto IF1250G Rev. J Características de rendimiento No para su distribución en Estados Unidos VALORES ESPERADOS Población con neumonía adquirida en la comunidad Dos investigadores externos
Identificación y medición de la respuesta inmune PRUEBAS SECUNDARIAS
 Identificación y medición de la respuesta inmune PRUEBAS SECUNDARIAS La prueba a realizar depende de las características del Ag SOLUBLE PRECIPITACIÓN PARTICULADO AGLUTINACIÓN SUPERFICIE + COMPLEMENTO FIJACIÓN
Identificación y medición de la respuesta inmune PRUEBAS SECUNDARIAS La prueba a realizar depende de las características del Ag SOLUBLE PRECIPITACIÓN PARTICULADO AGLUTINACIÓN SUPERFICIE + COMPLEMENTO FIJACIÓN
Inmunoanálisis. Análisis Avanzado de Alimentos. Inmunoanálisis. Inmunoanálisis.
 Análisis Avanzado de Alimentos Inmunoanálisis Inmunoanálisis. Son técnicas que permiten cuantificar antígenos o anticuerpos, aprovechando la especificidad y sensibilidad de la unión antígeno/anticuerpo.
Análisis Avanzado de Alimentos Inmunoanálisis Inmunoanálisis. Son técnicas que permiten cuantificar antígenos o anticuerpos, aprovechando la especificidad y sensibilidad de la unión antígeno/anticuerpo.
INSTRUCTIVO PARA LA SOLICITUD DE REGISTRO DE PRODUCTOS VETERINARIOS CONSIDERADOS COMO KITS DE DIAGNÓSTICO
 INSTRUCTIVO PARA LA SOLICITUD DE REGISTRO DE PRODUCTOS VETERINARIOS CONSIDERADOS COMO KITS DE DIAGNÓSTICO Para la evaluación del expediente para el registro nacional de productos veterinarios considerados
INSTRUCTIVO PARA LA SOLICITUD DE REGISTRO DE PRODUCTOS VETERINARIOS CONSIDERADOS COMO KITS DE DIAGNÓSTICO Para la evaluación del expediente para el registro nacional de productos veterinarios considerados
Unidad9. Principios de Ingeniería Genética Aplicaciones de Biología Molecular
 Unidad9. Principios de Ingeniería Genética Aplicaciones de Biología Molecular Aislamiento, análisis y manipulación de ácidos nucleicos Generación de moléculas de DNA recombinante Ingeniería Genética AISLAMIENTO
Unidad9. Principios de Ingeniería Genética Aplicaciones de Biología Molecular Aislamiento, análisis y manipulación de ácidos nucleicos Generación de moléculas de DNA recombinante Ingeniería Genética AISLAMIENTO
Métodos analíticos para el control de alergenos en alimentos. Dr. Luis Mata Responsable de I+D ZEULAB
 Métodos analíticos para el control de alergenos en alimentos Dr. Luis Mata Responsable de I+D ZEULAB Por qué analizar alergenos? Seguridad del consumidor Producto final Control de materias primas Asegurar
Métodos analíticos para el control de alergenos en alimentos Dr. Luis Mata Responsable de I+D ZEULAB Por qué analizar alergenos? Seguridad del consumidor Producto final Control de materias primas Asegurar
MANUAL DE PROTOCOLOS RESUMIDOS DE FABRICACION PROTOCOLO RESUMIDO DE FABRICACIÓN DE VACUNAS DPT
 COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS MANUAL DE PROTOCOLOS RESUMIDOS DE FABRICACION PROTOCOLO RESUMIDO DE FABRICACIÓN DE VACUNAS DPT I. CONTROL FINAL 1. Nombre 2. Nombre del propietario
COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS MANUAL DE PROTOCOLOS RESUMIDOS DE FABRICACION PROTOCOLO RESUMIDO DE FABRICACIÓN DE VACUNAS DPT I. CONTROL FINAL 1. Nombre 2. Nombre del propietario
TRABAJO PRÁCTICO No. 2 EXTRACION DE ACIDO NUCLEICO VIRAL
 Unidad Curricular: Virología y Micología Veterinaria TRABAJO PRÁCTICO No. 2 EXTRACION DE ACIDO NUCLEICO VIRAL Las pruebas para el diagnostico específico de una infección viral se clasifican en dos tipos:
Unidad Curricular: Virología y Micología Veterinaria TRABAJO PRÁCTICO No. 2 EXTRACION DE ACIDO NUCLEICO VIRAL Las pruebas para el diagnostico específico de una infección viral se clasifican en dos tipos:
PLANIFICACIÓN DE ASIGNATURA
 PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUIMICA DEPARTAMENTO BIOLOGIA ASIGNATURA BIOLOGIA MOLECULAR II CÓDIGO 1681 PRERREQUISITOS Biología Molecular I CREDITOS
PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUIMICA DEPARTAMENTO BIOLOGIA ASIGNATURA BIOLOGIA MOLECULAR II CÓDIGO 1681 PRERREQUISITOS Biología Molecular I CREDITOS
INFLUENZA AVIAR SERVICIO DE GANADERIA - NEGOCIADO DE EPIZOOTIOLOGIA
 INFLUENZA AVIAR INFLUENZA AVIAR PESTE AVIAR (Fowl disease) GRIPE AVIAR (Grippe bird) Enfermedad viral altamente contagiosa, de las aves, que produce lesiones necróticas, hemorrágicas o inflamatorias en
INFLUENZA AVIAR INFLUENZA AVIAR PESTE AVIAR (Fowl disease) GRIPE AVIAR (Grippe bird) Enfermedad viral altamente contagiosa, de las aves, que produce lesiones necróticas, hemorrágicas o inflamatorias en
Métodos para Inmunidad Viral
 Métodos para Inmunidad Viral Radioinmunoensayo (RIA) Técnica muy sensible basada en la competencia de unión al anticuerpo específico entre el antígeno a cuantificar y cantidades conocidas del antígeno
Métodos para Inmunidad Viral Radioinmunoensayo (RIA) Técnica muy sensible basada en la competencia de unión al anticuerpo específico entre el antígeno a cuantificar y cantidades conocidas del antígeno
Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia
 Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia LABORATORIO NACIONAL DE BACTERIOLOGIA DIAGNOSTICO DE LABORATORIO EN LA VIGILANCIA DE LEPTOSPIROSIS EN LA RED NACIONAL DE LABORATORIOS
Secretaría de Salud Departamento de Laboratorios Nacional de Vigilancia LABORATORIO NACIONAL DE BACTERIOLOGIA DIAGNOSTICO DE LABORATORIO EN LA VIGILANCIA DE LEPTOSPIROSIS EN LA RED NACIONAL DE LABORATORIOS
1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos
 PRT-712.04-080 Página 1 de 9 1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este
PRT-712.04-080 Página 1 de 9 1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este
LA NUEVA BIOTECNOLOGÍA
 LA NUEVA BIOTECNOLOGÍA Ingeniería genética: técnicas que permiten manipular la información genética de un ser vivo. TECNOLOGÍA TRADICIONAL DEL ADN RECOMBINANTE CLONACIÓN DE GENES: Obtención de muchas copias
LA NUEVA BIOTECNOLOGÍA Ingeniería genética: técnicas que permiten manipular la información genética de un ser vivo. TECNOLOGÍA TRADICIONAL DEL ADN RECOMBINANTE CLONACIÓN DE GENES: Obtención de muchas copias
CYP 2C9 A1075C CYP2C9*3
 CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
Sanidad - Enfermedades Virales Los virus son parásitos intracelulares obligados
 Sanidad - Enfermedades Virales Los virus son parásitos intracelulares obligados Están formados por un núcleo o genoma de ADN o ARN, una cápside proteica que los recubre (nucleocápside) y algunos poseen
Sanidad - Enfermedades Virales Los virus son parásitos intracelulares obligados Están formados por un núcleo o genoma de ADN o ARN, una cápside proteica que los recubre (nucleocápside) y algunos poseen
REACCIONES ANTÍGENO ANTICUERPO
 REACCIONES ANTÍGENO ANTICUERPO CONCEPTO DE ANTÍGENO Características de los determinantes antigénicos Concepto Inmunopotencia Inmunodominancia Determinantes inmunogénicos y hapténicos Inmunogenicidad: Carácter
REACCIONES ANTÍGENO ANTICUERPO CONCEPTO DE ANTÍGENO Características de los determinantes antigénicos Concepto Inmunopotencia Inmunodominancia Determinantes inmunogénicos y hapténicos Inmunogenicidad: Carácter
HPAI - Influenza aviar altamente patógena
 Influenza Aviar (AI) HPAI - Influenza aviar altamente patógena Lista A de la OIE (Enfermedad de declaración obligatoria) Directiva 92/40/CEE del Consejo Real decreto 1025/1993 BOE num.240 LPAI - Influenza
Influenza Aviar (AI) HPAI - Influenza aviar altamente patógena Lista A de la OIE (Enfermedad de declaración obligatoria) Directiva 92/40/CEE del Consejo Real decreto 1025/1993 BOE num.240 LPAI - Influenza
PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS. Es un ácido capaz de formar sales con iones cargados
 Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
DIAGNOSTICO LEPTOSPIROSIS ANIMAL. Dra. Brenda Orellana. IHIMV Simulacro de Leptospirosis
 DIAGNOSTICO LEPTOSPIROSIS DE ANIMAL Dra. Brenda Orellana. IHIMV Simulacro de Leptospirosis Introducción Diagnóstico laboratorial de la Leptospirosis puede ser complejo e implica pruebas que se dividen
DIAGNOSTICO LEPTOSPIROSIS DE ANIMAL Dra. Brenda Orellana. IHIMV Simulacro de Leptospirosis Introducción Diagnóstico laboratorial de la Leptospirosis puede ser complejo e implica pruebas que se dividen
TÉCNICAS GENÓMICAS. 2) Cuantificación del número de virus presentes en muestras de sangre o suero: carga vírica
 TÉCNICAS GENÓMICAS Utilidad/Objetivos: 1) Detección de microorganismos directamente en muestras clínicas identificando un fragmento específico del genoma del microorganismo concreto 2) Cuantificación del
TÉCNICAS GENÓMICAS Utilidad/Objetivos: 1) Detección de microorganismos directamente en muestras clínicas identificando un fragmento específico del genoma del microorganismo concreto 2) Cuantificación del
Universidad de Los Andes Facultad de Medicina Instituto Inmunología Clínica Maestría en Inmunología
 TÉCNICAS EN BIOLOGÍA MOLECULAR RESPONSABLE: Dra. Lisbeth Berrueta. CREDITOS: 2 El curso de Técnicas de Biología Molecular está destinado a profesionales del área biomédica con conocimientos básicos relativos
TÉCNICAS EN BIOLOGÍA MOLECULAR RESPONSABLE: Dra. Lisbeth Berrueta. CREDITOS: 2 El curso de Técnicas de Biología Molecular está destinado a profesionales del área biomédica con conocimientos básicos relativos
Reacción en cadena de la Polimerasa (PCR)
 Explicación de TP Nº 3 Reacción en cadena de la Polimerasa (PCR) Química Biológica Patológica Bioq. Mariana L. Ferramola 2013 Definición de PCR Es la amplificación enzimática de un fragmento de interés
Explicación de TP Nº 3 Reacción en cadena de la Polimerasa (PCR) Química Biológica Patológica Bioq. Mariana L. Ferramola 2013 Definición de PCR Es la amplificación enzimática de un fragmento de interés
DETECCIÓN DE UN FRAGMENTO DEL GEN ENV DEL VIH EN PLASMA Y GLÓBULOS BLANCOS EN PACIENTES CON VIH/sida. Presenta: Fernando I. Puerto
 DETECCIÓN DE UN FRAGMENTO DEL GEN ENV DEL VIH EN PLASMA Y GLÓBULOS BLANCOS EN PACIENTES CON VIH/sida Presenta: Fernando I. Puerto ANTECEDENTES En los 80 s, esta pandemia se identificó como peligro para
DETECCIÓN DE UN FRAGMENTO DEL GEN ENV DEL VIH EN PLASMA Y GLÓBULOS BLANCOS EN PACIENTES CON VIH/sida Presenta: Fernando I. Puerto ANTECEDENTES En los 80 s, esta pandemia se identificó como peligro para
VERSIÓN PARA EQUIPOS COBAS c501/c502 DE ROCHE
 VERSIÓN PARA EQUIPOS COBAS c501/c502 DE ROCHE EQUIPO ADICIONAL NO SUMINISTRADO: La preparación de los reactivos requiere el empleo de micropipetas o sistemas que permitan dispensar los volúmenes especificados.
VERSIÓN PARA EQUIPOS COBAS c501/c502 DE ROCHE EQUIPO ADICIONAL NO SUMINISTRADO: La preparación de los reactivos requiere el empleo de micropipetas o sistemas que permitan dispensar los volúmenes especificados.
2. La figura representa un segmento de la fibra básica de cromatina.
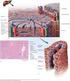 Bloque IV: Base molecular de la herencia 1. a. El esquema representa un cromosoma eucariótico en metafase mitótica. Qué denominación reciben los elementos indicados por los números 1 a 4? b. Dibuje un
Bloque IV: Base molecular de la herencia 1. a. El esquema representa un cromosoma eucariótico en metafase mitótica. Qué denominación reciben los elementos indicados por los números 1 a 4? b. Dibuje un
Reacción en cadena de la Polimerasa (PCR)
 Explicación de TP Nº 2 Reacción en cadena de la Polimerasa (PCR) Química Biológica Patológica Bioq. Mariana L. Ferramola 2014 Definición de PCR Es la amplificación enzimática de un fragmento de interés
Explicación de TP Nº 2 Reacción en cadena de la Polimerasa (PCR) Química Biológica Patológica Bioq. Mariana L. Ferramola 2014 Definición de PCR Es la amplificación enzimática de un fragmento de interés
INFORME SOBRE CASO CONFIRMADO DE ENCEFALITIS EQUINA VENEZOLANA EN LA REGION HUETAR NORTE
 Versión 01 Página 1 de 6 INFORME SOBRE CASO CONFIRMADO DE ENCEFALITIS EQUINA VENEZOLANA EN LA REGION HUETAR NORTE Informe N _01_ Fecha: 05 DE JUNIO DEL 2017 Responsable del informe: Dr. Orlando Jara Barrantes
Versión 01 Página 1 de 6 INFORME SOBRE CASO CONFIRMADO DE ENCEFALITIS EQUINA VENEZOLANA EN LA REGION HUETAR NORTE Informe N _01_ Fecha: 05 DE JUNIO DEL 2017 Responsable del informe: Dr. Orlando Jara Barrantes
DECISIÓN DE LA COMISIÓN
 L 336/36 Diario Oficial de la Unión Europea 18.12.2009 DECISIÓN DE LA COMISIÓN de 15 de diciembre de 2009 por la que se modifica el anexo D de la Directiva 64/432/CEE del Consejo en lo relativo a las pruebas
L 336/36 Diario Oficial de la Unión Europea 18.12.2009 DECISIÓN DE LA COMISIÓN de 15 de diciembre de 2009 por la que se modifica el anexo D de la Directiva 64/432/CEE del Consejo en lo relativo a las pruebas
IDENTIFICACIÓN Y MEDICIÓN DE LA RESPUESTA INMUNE
 IDENTIFICACIÓN Y MEDICIÓN DE LA RESPUESTA INMUNE DESCRIPCIÓN DE UNA ENFERMEDAD INFECCIOSA 1. Nombre y sinonimia 2. Definición 3. Epidemiología 4. Etiología 5. Patogenia 6. Signos y síntomas 7. Lesiones
IDENTIFICACIÓN Y MEDICIÓN DE LA RESPUESTA INMUNE DESCRIPCIÓN DE UNA ENFERMEDAD INFECCIOSA 1. Nombre y sinonimia 2. Definición 3. Epidemiología 4. Etiología 5. Patogenia 6. Signos y síntomas 7. Lesiones
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt
 Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
WITNESS RELAXIN (plasma, serum) RLX RLX u d 9 n n ersio V X RLX L R -W IO B S
 WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
REACCIÓN EN CADENA DE LA POLIMERASA (PCR)
 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología General Microbiología M de los Alimentos Licenciatura en Bioquímica i Ingeniería en alimentos c Microbiología r 2015 Licenciatura en Biotecnología
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología General Microbiología M de los Alimentos Licenciatura en Bioquímica i Ingeniería en alimentos c Microbiología r 2015 Licenciatura en Biotecnología
IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006
 IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006 REACCION EN CADENA DE LA POLIMERASA (PCR) EN EL DIAGNOSTICO DE Campylobacter jejuni/coli Viernes 19 de mayo María Rosa Viñas Servicio
IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006 REACCION EN CADENA DE LA POLIMERASA (PCR) EN EL DIAGNOSTICO DE Campylobacter jejuni/coli Viernes 19 de mayo María Rosa Viñas Servicio
- Clonar un gen (molde ADN o ARN)
 APLICACIONES PCR Aplicaciones de la PCR - Clonar un gen (molde ADN o ARN) - Secuencia conocida - Genes homólogos en especies próximas (primers degenerados) - Información de secuencia proteica (primers
APLICACIONES PCR Aplicaciones de la PCR - Clonar un gen (molde ADN o ARN) - Secuencia conocida - Genes homólogos en especies próximas (primers degenerados) - Información de secuencia proteica (primers
BIOQUIMICA Y GENETICA MOLECULAR APLICADA A LA VETERINARIA
 BIOQUIMICA Y GENETICA MOLECULAR APLICADA A LA VETERINARIA PROFESORADO CURSO 1994-1995: Dr. J. Ariño (Unidad de Bioquímica) Dra. F. Bosch (Unidad de Bioquímica) Dr. A. Sánchez (Unidad de Genética y Mejora)
BIOQUIMICA Y GENETICA MOLECULAR APLICADA A LA VETERINARIA PROFESORADO CURSO 1994-1995: Dr. J. Ariño (Unidad de Bioquímica) Dra. F. Bosch (Unidad de Bioquímica) Dr. A. Sánchez (Unidad de Genética y Mejora)
CLASE DE RESOLUCIÓN DE PROBLEMAS DE PCR LIC. BIOTECNOLOGÍA 2015
 CLASE DE RESOLUCIÓN DE PROBLEMAS DE PCR LIC. BIOTECNOLOGÍA 2015 DEFINICIÓN PCR: Constituye la técnica más importante para amplificar ácidos nucleicos in vitro. Ambas hebras del DNA de interés son replicadas
CLASE DE RESOLUCIÓN DE PROBLEMAS DE PCR LIC. BIOTECNOLOGÍA 2015 DEFINICIÓN PCR: Constituye la técnica más importante para amplificar ácidos nucleicos in vitro. Ambas hebras del DNA de interés son replicadas
Inmunohematología 2017
 Inmunohematología 2017 REACCIONES DE HEMAGLUTINACIÓN 1-Sensibilización 2-Aglutinación Ag + Ac Ag-Ac FACTORES QUE AFECTAN LA HEMAGLUTINACIÓN Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo
Inmunohematología 2017 REACCIONES DE HEMAGLUTINACIÓN 1-Sensibilización 2-Aglutinación Ag + Ac Ag-Ac FACTORES QUE AFECTAN LA HEMAGLUTINACIÓN Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo
1. Contaminación de agua y alimentos por microorganismos patógenos 1
 INTRODUCCIÓN GENERAL 1. Contaminación de agua y alimentos por microorganismos patógenos 1 2. Papel del agua en la transmisión de enfermedades infecciosas 2 2.1. Las aguas residuales 2 2.2. El agua potable
INTRODUCCIÓN GENERAL 1. Contaminación de agua y alimentos por microorganismos patógenos 1 2. Papel del agua en la transmisión de enfermedades infecciosas 2 2.1. Las aguas residuales 2 2.2. El agua potable
LEVADURAS DE INTERÉS MÉDICO PRUEBAS DE IDENTIFICACIÓN
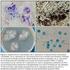 LEVADURAS DE INTERÉS MÉDICO PRUEBAS DE IDENTIFICACIÓN Levaduras de Importancia Médica Levaduras del género Candida Levaduras del género Cryptococcus Levaduras del género Malassezia Levaduras del género
LEVADURAS DE INTERÉS MÉDICO PRUEBAS DE IDENTIFICACIÓN Levaduras de Importancia Médica Levaduras del género Candida Levaduras del género Cryptococcus Levaduras del género Malassezia Levaduras del género
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
Servicio de Bacteriología Clínica INEI-ANLIS Dr. Carlos G Malbrán. Consideraciones Generales en el Cultivo y el Diagnóstico Molecular de Coqueluche.
 Consideraciones Generales en el Cultivo y el Diagnóstico Molecular de Coqueluche. El objetivo de este documento es difundir las herramientas de laboratorio disponibles para realizar un diagnóstico certero
Consideraciones Generales en el Cultivo y el Diagnóstico Molecular de Coqueluche. El objetivo de este documento es difundir las herramientas de laboratorio disponibles para realizar un diagnóstico certero
PLAN DE VIGILANCIA DE LA PESTE EQUINA AFRICANA EN ESPAÑA
 MINISTERIO DE AGRICULTURA, ALIMENTACIÓN Y MEDIO AMBIENTE SECRETARIA GENERAL DE AGRICULTURA Y ALIMENTACIÓN DIRECCION GENERAL DE SANIDAD E HIGIENE ANIMAL Y TRAZABILIDAD PLAN DE VIGILANCIA DE LA PESTE EQUINA
MINISTERIO DE AGRICULTURA, ALIMENTACIÓN Y MEDIO AMBIENTE SECRETARIA GENERAL DE AGRICULTURA Y ALIMENTACIÓN DIRECCION GENERAL DE SANIDAD E HIGIENE ANIMAL Y TRAZABILIDAD PLAN DE VIGILANCIA DE LA PESTE EQUINA
MATERIALES Y MÉTODOS. Cepa de Mycobacterium tuberculosis
 MATERIALES Y MÉTODOS Cepa de Mycobacterium tuberculosis Se utilizó una cepa de referencia de Mycobacterium tuberculosis H37Rv tipificada en el Instituto Nacional de Diagnóstico y Referencia Epidemiológica
MATERIALES Y MÉTODOS Cepa de Mycobacterium tuberculosis Se utilizó una cepa de referencia de Mycobacterium tuberculosis H37Rv tipificada en el Instituto Nacional de Diagnóstico y Referencia Epidemiológica
Inmunohematología. Dra. Ana Cecilia Haro
 Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología de los Alimentos Ingeniería en alimentos
 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología de los Alimentos Ingeniería en alimentos 2015 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente una región
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología de los Alimentos Ingeniería en alimentos 2015 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente una región
Titulaciones en Química Analítica. Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D.
 Titulaciones en Química Analítica Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D. Introducción En el análisis volumétrico, la concentración se determina midiendo su capacidad de reaccionar con un reactivo
Titulaciones en Química Analítica Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D. Introducción En el análisis volumétrico, la concentración se determina midiendo su capacidad de reaccionar con un reactivo
La Patología a Molecular y el Control de Calidad
 UNIDAD DIDÁCTICA 7: LOS PROCESOS EN ANATOMÍA PATOLÓGICA La Patología a Molecular y el Control de Calidad Asunción n Olmo Sevilla Master Diagnóstica S. L. Patología Molecular: Patología del futuro X Personal:
UNIDAD DIDÁCTICA 7: LOS PROCESOS EN ANATOMÍA PATOLÓGICA La Patología a Molecular y el Control de Calidad Asunción n Olmo Sevilla Master Diagnóstica S. L. Patología Molecular: Patología del futuro X Personal:
ESTOMATITIS VESICULAR. 1) La estomatitis vesicular es una enfermedad infecciosa que se caracteriza por:
 ESTOMATITIS VESICULAR 1) La estomatitis vesicular es una enfermedad infecciosa que se caracteriza por: a. Enfermedad de alta mortalidad y morbilidad variable. b. Enfermedad de baja mortalidad y morbilidad
ESTOMATITIS VESICULAR 1) La estomatitis vesicular es una enfermedad infecciosa que se caracteriza por: a. Enfermedad de alta mortalidad y morbilidad variable. b. Enfermedad de baja mortalidad y morbilidad
A qui diagnosticarem la grip? Diagnòstic ràpid de grip.
 A qui diagnosticarem la grip? Diagnòstic ràpid de grip. MªAngeles Marcos Servicio Microbiología. Hospital Clinic de Barcelona Mutaciones puntuales (deriva antigénica)/ Cambios antigénicos mayores Cuándo
A qui diagnosticarem la grip? Diagnòstic ràpid de grip. MªAngeles Marcos Servicio Microbiología. Hospital Clinic de Barcelona Mutaciones puntuales (deriva antigénica)/ Cambios antigénicos mayores Cuándo
Diario Oficial de la Unión Europea
 5.8.2014 L 232/5 REGLAMENTO DE EJECUCIÓN (UE) N o 846/2014 DE LA COMISIÓN de 4 de agosto de 2014 por el que se modifica el anexo D de la Directiva 92/65/CEE del Consejo en lo que se refiere a las condiciones
5.8.2014 L 232/5 REGLAMENTO DE EJECUCIÓN (UE) N o 846/2014 DE LA COMISIÓN de 4 de agosto de 2014 por el que se modifica el anexo D de la Directiva 92/65/CEE del Consejo en lo que se refiere a las condiciones
Técnicas moleculares para
 Técnicas moleculares para detectar enfermedades vasculares en cítricos Isidro Humberto Almeyda-León Mario Alberto Rocha-Peña Fermín n Orona-Castro María a Magdalena Iracheta-Cárdenas rdenas Reyna Xochitl
Técnicas moleculares para detectar enfermedades vasculares en cítricos Isidro Humberto Almeyda-León Mario Alberto Rocha-Peña Fermín n Orona-Castro María a Magdalena Iracheta-Cárdenas rdenas Reyna Xochitl
FICHA DE DATOS DE SEGURIDAD (MSDS) KIT CLART STIs B
 1. Identificación de la sustancia y proveedor Nombre comercial CLART STIs B Referencias: Extracción y purificación 16 determinaciones Ref.: CS-1113-16 48 determinaciones Ref.: CS-1113-48 Amplificación
1. Identificación de la sustancia y proveedor Nombre comercial CLART STIs B Referencias: Extracción y purificación 16 determinaciones Ref.: CS-1113-16 48 determinaciones Ref.: CS-1113-48 Amplificación
Incertidumbre, Validación y Trazabilidad en el Laboratorio de Análisis Clínicos. Cómo cumplir con requisitos de la ISO 15189
 Incertidumbre, Validación y Trazabilidad en el Laboratorio de Análisis Clínicos Cómo cumplir con requisitos de la ISO 15189 Calidad en mediciones químicas Validación de métodos Estoy midiendo lo que intentaba
Incertidumbre, Validación y Trazabilidad en el Laboratorio de Análisis Clínicos Cómo cumplir con requisitos de la ISO 15189 Calidad en mediciones químicas Validación de métodos Estoy midiendo lo que intentaba
A. El punto 3 del método Reactivos queda de la siguiente manera:
 RESOLUCIÓN OIV-OENO 349-2011 COMPLEMENTO DEL MÉTODO DE DETERMINACIÓN DE LA OCRATOXINA A MEDIANTE COLUMNA DE INMUNOAFINIDAD (16/2001) LA ASAMBLEA GENERAL, De conformidad con el Párrafo 2 iv del Artículo
RESOLUCIÓN OIV-OENO 349-2011 COMPLEMENTO DEL MÉTODO DE DETERMINACIÓN DE LA OCRATOXINA A MEDIANTE COLUMNA DE INMUNOAFINIDAD (16/2001) LA ASAMBLEA GENERAL, De conformidad con el Párrafo 2 iv del Artículo
Código: IDK-006 Ver: 1 MTHFR A1298C. Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa
 Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa Reg. MSP 21199 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336
Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa Reg. MSP 21199 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336
Utilidad de las técnicas de biología molecular en el manejo de bacterias fastidiosas.
 Utilidad de las técnicas de biología molecular en el manejo de bacterias fastidiosas. Estudio rutinario de las bacterias en el laboratorio Examen microscópico (en fresco, Gram, Ziehl- Neelsen, otros) Cultivo
Utilidad de las técnicas de biología molecular en el manejo de bacterias fastidiosas. Estudio rutinario de las bacterias en el laboratorio Examen microscópico (en fresco, Gram, Ziehl- Neelsen, otros) Cultivo
El Laboratorio en la Vigilancia de Influenza
 El Laboratorio en la Vigilancia de Influenza QBP MANUEL ARROYO ROJAS Laboratorio de Virus Respiratorios del TIPOS DE MUESTRAS Exudado Faríngeo Exudado Nasofaríngeo Aspirado Bronqueoalveolar Suero (pareados)
El Laboratorio en la Vigilancia de Influenza QBP MANUEL ARROYO ROJAS Laboratorio de Virus Respiratorios del TIPOS DE MUESTRAS Exudado Faríngeo Exudado Nasofaríngeo Aspirado Bronqueoalveolar Suero (pareados)
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar
 4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
REACCIÓN EN CADENA DE LA POLIMERASA (PCR)
 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Lic. en Bioquímica Lic. en Biotecnología Microbiología de los Alimentos 2016 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Lic. en Bioquímica Lic. en Biotecnología Microbiología de los Alimentos 2016 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL
 CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD B. CROMATOGRAFÍA DE FILTRACIÓN EN GEL. 1. Principios. No requiere la unión de la proteína, lo cual
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD B. CROMATOGRAFÍA DE FILTRACIÓN EN GEL. 1. Principios. No requiere la unión de la proteína, lo cual
Kit artus HBV QS-RGQ. Características del rendimiento. Mayo Sample & Assay Technologies. Sensibilidad analítica (plasma)
 Kit artus HBV QS-RGQ Características del rendimiento Kit artus HBV QS-RGQ, versión 1, 4506363, 4506366 Compruebe la disponibilidad de nuevas versiones de la documentación electrónica en www.qiagen.com/products/artushbvpcrkitce.aspx
Kit artus HBV QS-RGQ Características del rendimiento Kit artus HBV QS-RGQ, versión 1, 4506363, 4506366 Compruebe la disponibilidad de nuevas versiones de la documentación electrónica en www.qiagen.com/products/artushbvpcrkitce.aspx
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
 EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
CINÉTICA ENZIMÁTICA: VALORACIÓN DE FOSFATASA ALCALINA
 Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular CINÉTICA ENZIMÁTICA: VALORACIÓN DE FOSFATASA ALCALINA 1.- FUNDAMENTO TEÓRICO Cinética enzimática Las reacciones químicas
Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular CINÉTICA ENZIMÁTICA: VALORACIÓN DE FOSFATASA ALCALINA 1.- FUNDAMENTO TEÓRICO Cinética enzimática Las reacciones químicas
VIGILANCIA DEL VIRUS CHIKUNGUNYA POR LABORATORIO EN ARGENTINA
 VIGILANCIA DEL VIRUS CHIKUNGUNYA POR LABORATORIO EN ARGENTINA Bioq. Victoria Luppo Laboratorio de Arbovirus Instituto Nacional de Enfermedades Virales Humanas (INEVH) Dr. J.I.Maiztegui - ANLIS, Pergamino-Argentina
VIGILANCIA DEL VIRUS CHIKUNGUNYA POR LABORATORIO EN ARGENTINA Bioq. Victoria Luppo Laboratorio de Arbovirus Instituto Nacional de Enfermedades Virales Humanas (INEVH) Dr. J.I.Maiztegui - ANLIS, Pergamino-Argentina
Diagnóstico de tos ferina en consultas de Pediatría de Atención Primaria
 Diagnóstico de tos ferina en consultas de Pediatría de Atención Primaria Cristina Rodríguez Arranz, Miriam Blasco Alberdi Diciembre 2016 AEPap. Copia para uso personal. En caso de reproducción total o
Diagnóstico de tos ferina en consultas de Pediatría de Atención Primaria Cristina Rodríguez Arranz, Miriam Blasco Alberdi Diciembre 2016 AEPap. Copia para uso personal. En caso de reproducción total o
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
PROTOCOLO MANEJO INFECCIONES NOSOCOMIALES
 ÍNDICE 1) Objeto. 2 2) Profesionales implicados. 2 3) Población diana. 2 4) Desarrollo. 2 5) Indicadores de evaluación. 6 6) Control de cambio de protocolo. 6 ELABORADO POR: REVISADO POR: APROBADO POR:
ÍNDICE 1) Objeto. 2 2) Profesionales implicados. 2 3) Población diana. 2 4) Desarrollo. 2 5) Indicadores de evaluación. 6 6) Control de cambio de protocolo. 6 ELABORADO POR: REVISADO POR: APROBADO POR:
TERMINOLOGÍA ANALÍTICA - PROCESO ANALÍTICO - TÉCNICA ANALÍTICA - MÉTODO ANALÍTICO - PROCEDIMIENTO ANALÍTICO - PROTOCOLO ANALÍTICO
 TERMINOLOGÍA ANALÍTICA - PROCESO ANALÍTICO - TÉCNICA ANALÍTICA - MÉTODO ANALÍTICO - PROCEDIMIENTO ANALÍTICO - PROTOCOLO ANALÍTICO PROCESO ANALÍTICO Conjunto de operaciones analíticas intercaladas que se
TERMINOLOGÍA ANALÍTICA - PROCESO ANALÍTICO - TÉCNICA ANALÍTICA - MÉTODO ANALÍTICO - PROCEDIMIENTO ANALÍTICO - PROTOCOLO ANALÍTICO PROCESO ANALÍTICO Conjunto de operaciones analíticas intercaladas que se
Septiembre 2015 artus CMV QS-RGQ Kit: Características de rendimiento
 Septiembre 2015 artus CMV QS-RGQ Kit: Características de rendimiento artus CMV QS-RGQ Kit, versión 1 4503363 Compruebe la disponibilidad de nuevas versiones de la documentación electrónica en www.qiagen.com/products/artuscmvpcrkitce.aspx
Septiembre 2015 artus CMV QS-RGQ Kit: Características de rendimiento artus CMV QS-RGQ Kit, versión 1 4503363 Compruebe la disponibilidad de nuevas versiones de la documentación electrónica en www.qiagen.com/products/artuscmvpcrkitce.aspx
