IgK-IgL Rearrangements Molecular Analysis Kit Nº CAT. MAD M (20 tests)
|
|
|
- David Venegas Carrizo
- hace 8 años
- Vistas:
Transcripción
1 IgK-IgL Rearrangements Molecular Analysis Kit Nº CAT. MAD M (20 tests) El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos, ocasionalmente el diagnóstico diferencial entre un proceso reactivo y un linfoma maligno es difícil de establecer. La detección de clonalidad mediante análisis molecular por PCR de reordenamientos de los genes de las inmunoglobulinas (Ig) y TCR, es un instrumento de gran valor en el diagnóstico de los procesos linfoproliferativos B y T. En el caso del estudio de procesos linfoproliferativos de células B, el análisis de reordenamientos de los genes IgH es ampliamente utilizado como herramienta de análisis de clonalidad B, si bien está descrito que determinadas patologías linfoides de centro germinal y postgerminal, especialmente los linfomas foliculares y linfomas B difusos de células grandes, pueden dar resultados falsos negativos. Esto es debido bien a uniones ineficaces de los cebadores o al efecto de hipermutaciones somáticas en los genes IgH (implica mutaciones de nucleótidos individuales y a veces también inserciones o deleciones de nucleótidos) que pueden originar una unión ineficaz y la ausencia de amplificación. En estos casos, el estudio complementario de reordenamientos de las cadenas ligeras kappa y lambda de las inmunogobulinas (IgK e IgL respectivamente) permitiría mejorar la sensibilidad de detección, debido básicamente a que en ellos son menos frecuentes las hipermutaciones somáticas, resultando esencial su análisis en la rutina diagnóstica de clonalidad de linfomas B. Este kit permite la amplificación de los segmentos reordenados Vκ-Jκ y de los dos tipos de reordenamientos Kde (Vk-Kde e intrón-rss-kde) para la IgK así como segmentos reordenados V λ -J λ de la IgL mediante múltiples cebadores consenso que hibridan con regiones conservadas dentro de dichos genes. Características del kit: - El kit consta de dos mixs de PCR para el estudio de reordenamiento de IgK (Vκ-Jκ y los dos tipos de reordenamientos Kde), una mix para el estudio de reordenamientos IgL (V λ -J λ ) y un control interno (CI) de amplificación. - La enzima Phire Hot Start II ADN Polimerasa está incluida en el kit. - Las mezclas de amplificación se presentan en formato monotest (20 tests) en tubos de PCR de 0.2 ml, identificados con diferentes colores. - Todas las mezclas de PCR incluyen cebadores marcados en su extremo 5 con el fluorocromo 6-FAM, lo que permite hacer un análisis automático de fragmentos por electroforesis capilar (compatible con ABI PRISM 310 Genetic Analyzer, AB 3130, 3130xl, 3500 y 3500xL Genetic Analyzers). - Todas las amplificaciones se pueden realizar con un único programa en el termociclador. Este programa es el mismo que el utilizado en los reordenamientos IgH, TCR gamma y TCR beta (MAD BP, MD TP, MAD TP) permitiendo su análisis simultáneo. Este producto es para diagnóstico in vitro master@vitroweb.com 1/12
2 Componentes incluidos en el kit: Tabla 1. Composición de reactivos: REFERENCIA COMPONENTES CANTIDAD MAD-F122-2 MAD B2 MAD B3 IgK-A (6-FAM) (mezcla de oligonucleótidos de las regiones Vκ y Jκ del gen IgK, dntp y solución tamponada) IgK-B (6-FAM) (mezcla de oligonucleótidos de las regiones Vκ, intrón-rss, y Kde del gen IgK, dntp y solución tamponada) IgL (6-FAM) (mezcla de oligonucleótidos de las regiones Vλ-Jλ del gen IgL, dntp y solución tamponada) Mezcla control interno (6-FAM) (oligonucleótidos específicos del gen p53 exón 5, dntp y solución tamponada) Phire Hot Start II DNA Polymerase* (Phire Hot Start II ADN Polimerasa)* Clonal IgK-IgL Positive Control DNA (ADN Control positivo clonal IgK-IgL ) Polyclonal Positive Control DNA (ADN Control positivo policlonal) 20 tubos PCR color azul (46 µl) 20 tubos PCR color naranja (46 µl) 20 tubos PCR color verde (46 µl) 20 tubos PCR color amarillo (46 µl) 2 x 60 µl 1 x 50 µl 1 x 50µl * Aspectos legales: El precio de venta de este producto incluye una licencia limitada, no transferible, protegida por patentes de EEUU y otras ( y ), propiedad de New England Biolabs, Inc., para el uso de este producto. Ninguna otra licencia bajo estas patentes es otorgada al cliente, expresamente o por implicación, por la compra de este producto. El precio de venta de este producto incluye una licencia limitada, no transferible, protegida por patentes de EEUU y otras, propiedad de BIO-RAD Laboratories, Inc. para el uso de este producto. Ninguna otra licencia bajo estas patentes es otorgada al cliente, expresamente o por implicación, por la compra de este producto. Este producto está protegido por una licencia bajo patente US propiedad de TaKaRa Shuzo Co. Ltd. EL producto se vende bajo licencia de Affibody AB, Suecia. Phire and DyNAzyme son marcas registradas de Finnzymes Oy, una compañía del grupo Thermo Fisher Scientific. Affibody es una marca registrada de of Affibody AB, Suecia. master@vitroweb.com 2/12
3 Material necesario no suministrado en el kit: Instrumentación específica: Termociclador Microcentrífuga Baño termostatizado/estufa Fuente de alimentación Cubeta de electroforesis para ADN Transiluminador para luz ultravioleta Sistema de documentación de geles Equipo de secuenciación con electroforesis capilar Material fungible: Xileno (opcional) Etanol 100% Tampón PBS (para extracción de linfocitos a partir de sangre total) Tampón TE 1x (10 mm Tris, 1 mm EDTA ph 8.0) Tubos eppendorf 1,5/0,6/0,2 ml libres de ADNsa/RNasa Reactivos para llevar a cabo la extracción de ADN genómico a partir de muestras de sangre, botones celulares, tejidos frescos, o tejidos fijados en formalina tamponada e incluidos en parafina. Todos los reactivos están incluidos en el Kit de Master Diagnóstica S.L.: DNA Extraction Kit (from tissue or cell suspensions) Ref: MAD M Reactivos para llevar a cabo la electroforesis del ADN amplificado (geles de agarosa o poliacrilamida y reactivos auxiliares de electroforesis). Todos los reactivos están incluidos en los Kits de Master Diagnóstica S. L.: Agarose Gel DNA Electrophoresis Kit y Polyacrylamide Gel Electrophoresis Kit Ref: MAD M y MAD M respectivamente. Reactivos para análisis de fragmentos por electroforesis capilar (ajustar en función de filtro/equipo que se utilice): polímero POP-7, estándar de peso molecular GeneScan 600 LIZ, Cathode and Anode buffers y formamida desionizada. Precauciones: Durante todo el desarrollo de la técnica es aconsejable el empleo de guantes desechables. Dada la elevada sensibilidad de la técnica de amplificación de ADN se recomienda que la reacción de amplificación se lleve a cabo utilizando puntas de pipeta con filtro para evitar contaminación. La mayor fuente de contaminación suele ser el propio producto amplificado, por lo cual es recomendable llevar a cabo la manipulación de los productos amplificados y la posterior electroforesis en zonas de trabajo separadas de la zona donde se procesen las muestras y emplear pipetas distintas en cada caso. Es conveniente delimitar tres áreas de trabajo: la zona de procesamiento y preparación de las muestras de ADN, la zona de amplificación y la zona de detección (electroforesis). El flujo de trabajo debe ir siempre en una única dirección, desde la zona de preparación de las muestras y amplificación hasta la zona de detección y nunca en dirección opuesta. Se recomienda incluir controles negativos de amplificación que contengan todos los reactivos manejados en el kit, con excepción de la muestra de ADN, con objeto de detectar y controlar cualquier posible contaminación de los reactivos con ADN tanto procedente de muestras problema como de productos amplificados. Almacenamiento y transporte: El Kit se transporta y almacena a -20ºC. Una vez descongelada la solución de lisis se puede guardar a 4ºC sin necesidad de volver congelar. master@vitroweb.com 3/12
4 PROCEDIMIENTO TÉCNICO 1. EXTRACCIÓN DEL ADN GENÓMICO Para la extracción de ADN se recomienda usar los reactivos incluidos en el DNA Extraction Kit (from tissue or cell suspensions) Ref: MAD M. Antes de comenzar con la extracción de ADN, descongelar los reactivos suministrados en el kit: aceite mineral, solución de lisis y un vial de solución de proteasa. Tras su uso, el aceite mineral y la solución de lisis se pueden almacenar a 4º C. La solución de proteasa se debe almacenar congelada a -20 ºC y evitar repetidas congelaciones/descongelaciones SECCIONES DE TEJIDO INCLUIDO EN PARAFINA 1. Tomar 1-4 secciones de tejido (según la cantidad de material presente en cada sección) de 10 µm de grosor y colocar en tubo de microcentrífuga de 1,5 ml valiéndose de una aguja o unas pinzas finas. 2. Añadir 500 µl de aceite mineral (incluido en el kit) y calentar en bloque térmico 2 min a 95º C. Centrifugar 2 min a 8000 rpm en microcentrífuga. 3. Eliminar el aceite mineral sin arrastrar restos de tejido. 4. Repetir los pasos 2 y 3. (Los restos de aceite mineral no interfieren en el proceso de extracción de ADN). 5. Preparar una mezcla de solución de lisis y solución de proteasa en proporción 50:1 (por cada 50 µl de sol. de lisis añadir 1 µl de sol. de proteasa) en volumen suficiente para procesar las muestras de tejido. 6. Al botón de tejido resultante añadir un volumen adecuado de la mezcla anterior ( µl), hasta conseguir que el tejido quede en suspensión en la solución. (Este punto es muy importante para conseguir un buen rendimiento de ADN y degradar los restos celulares contaminantes, que podrían interferir en la posterior amplificación de dicho ADN). 7. Agitar varias veces con la micropipeta para homogenizar, centrifugar 5 segundos para eliminar las burbujas e incubar durante horas a 55ºC en baño termostatizado o bloque térmico. 8. Calentar a 95º C en bloque térmico durante 8-10 min para inactivar la proteasa. 9. Centrifugar 5 min a velocidad máxima. Tras centrifugar deben quedar dos fases, una superior que corresponde a los restos de aceite mineral y una inferior acuosa que contiene el ADN en solución. En el fondo del tubo puede quedar un pequeño botón de restos de tejido no digeridos. RECOGER LA FASE ACUOSA (contiene el ADN) evitando tomar restos de tejido del fondo del tubo. 10. Usar 3 µl de esta solución de ADN para amplificar. La muestra se puede almacenar, siendo estable a 4 ºC durante una semana, o a -20/-80 ºC durante varios meses TEJIDO CONGELADO 1. Cortar 1-2 secciones de tejido en criostato o bien ayudándose con una hoja de bisturí y colocar en tubo de microcentrífuga de 1,5 ml valiéndose de una aguja o unas pinzas finas. 2. Continuar con el paso 5 del protocolo anterior para secciones parafinadas. Nota: Para evitar evaporación de la solución de lisis durante la incubación a 55 ºC se pueden añadir unas gotas de aceite mineral incluido en el kit. master@vitroweb.com 4/12
5 1.3. MUESTRAS DE SANGRE PERIFÉRICA/MÉDULA ÓSEA Nota: No usar sangre total heparinizada. Se recomienda el uso de EDTA o Citrato Sódico como anticoagulantes. 1. Aislar población blanca mediante Buffy Coat: partir de 1,5 ml de sangre/médula con EDTA y fraccionar centrifugando a x g durante min a temperatura ambiente. Este proceso separará una fase superior de plasma, una inferior con la población roja y una delgada interfase entre ambas con las células blancas (buffy coat). (En una centrífuga clínica típica x g equivale a rpm). 2. Recoger la población blanca intermedia y pasar a un tubo limpio. 3. Lavar con 5 ml de tampón TE 1X e incubar 10 min a 37º C para lisar los restos de hematíes. 4. Centrifugar a 3000 rpm 5 min para precipitar las células blancas. 5. Resuspender el botón celular en 1 ml de tampón TE 1X y pasar a un tubo eppendorf de 1,5 ml. 6. Centrifugar a 8000 rpm 5 min en microcentrífuga y eliminar el sobrenadante. 7. Continuar con el paso 5 del protocolo 1.1 para muestras parafinadas. Nota: Para evitar evaporación de la solución de lisis durante la incubación a 55 ºC se pueden añadir unas gotas de aceite mineral incluido en el kit. 2. REACCIÓN DE AMPLIFICACIÓN Por cada muestra de ADN problema a analizar se amplificarán 4 mezclas: dos para IgK, una para IgL y otra para el control interno (CI). Se recomienda preservar las mezclas de la luz, ya que contienen cebadores marcados con fluorescencia PREPARACIÓN DE LAS MUESTRAS 1. Descongelar 1 tubo azul (IgK-A), 1 tubo naranja (IgK-B), un tubo verde (IgL) y un tubo amarillo (CI) por cada muestra, mantener en hielo y añadir a cada uno de ellos: - 1 µl de enzima Phire Hot Start II ADN Polimerasa - 3 µl de la muestra de ADN* 2. Mezclar bien y centrifugar 5 segundos en microcentrífuga para eliminar burbujas *Si se dispone de ADN de concentración conocida, se recomienda poner entre ng de ADN. Nota: Es importante mantener los tubos en hielo hasta el momento de colocar en el termociclador, para evitar uniones inespecíficas de los primers. master@vitroweb.com 5/12
6 2.2. AMPLIFICACIÓN 1. Colocar todos los tubos en el termociclador y amplificar según el siguiente programa: 98ºC 2 min. 35 ciclos: 98ºC 10 s 60ºC 10 s 72ºC 15 s 72ºC 1 min 2. Mantener los tubos a 12-15º C cuando finalice la reacción. Si no se van a procesar las muestras en el momento, se pueden almacenar a 4º C o a -20º C hasta su uso CONTROLES DE AMPLIFICACIÓN RECOMENDADOS En el kit se suministran unos ADNs controles positivo clonal y policlonal. Se recomienda amplificar estos ADNs con cada tanda de muestras analizadas. Para controlar la posible presencia de contaminaciones de unas muestras con otras o de alguno de los reactivos comunes usados durante la manipulación de las muestras, se recomienda procesar una muestra blanco sin ADN. Esta muestra llevaría los mismos reactivos empleados en la extracción del ADN de las muestras y seguiría un procesamiento similar al resto de las muestras pero, al no contener ADN, el resultado tras la amplificación debería ser ausencia de señal para todas las mezclas. Así mismo, aunque no es imprescindible, es aconsejable analizar cada muestra por duplicado; es decir partiendo del mismo ADN genómico realizar por duplicado las amplificaciones para todos los fragmentos. De esta forma se facilita la interpretación de resultados dudosos y se verifica con el duplicado el tamaño de picos monoclonales en el seno de una población policlonal reactiva. 3. ANÁLISIS DE LOS PRODUCTOS AMPLIFICADOS 3.1. ELECTROFORESIS EN GELES Precauciones!: Dada la elevada sensibilidad de la técnica de amplificación que genera cantidades elevadas de un fragmento específico de ADN, dicho producto amplificado representa una potente fuente de contaminación en el laboratorio. Es recomendable llevar a cabo la manipulación y electroforesis de los productos amplificados en una zona de trabajo alejada del lugar donde se realiza el procesamiento de las muestras, para evitar la contaminación de éstas con el ADN amplificado, que podría conducir a resultados falsos positivos. El revelado de los productos amplificados se puede llevar a cabo tanto en geles de agarosa (4%) como en geles de poliacrilamida (6-8%) con tampón TBE 0.5X. La resolución en geles de poliacrilamida es superior a la de los geles de agarosa. master@vitroweb.com 6/12
7 Master Diagnóstica dispone de Kits para electroforesis de ADN tanto en geles de agarosa como de poliacrilamida listos para uso que incluyen además todos los reactivos necesarios para llevar a cabo la electroforesis: marcador peso molecular, tampón de carga, tampón TBE concentrado, EtBr. (Nº de Cat.: MAD M y MAD M para agarosa y poliacrilamida respectivamente). Con objeto de diferenciar productos derivados de poblaciones mono ó policlonales, se recomienda llevar a cabo un análisis de heteroduplex de los productos de PCR, mediante desnaturalización/renaturalización de los productos amplificados. Si ha ocurrido reordenamiento clonal de los genes IgK y/o IgL se obtendrá un homoduplex, mientras que en el caso de población policlonal, tras el proceso de desnaturalización/renaturalización se formarán heteroduplex con uniones heterogéneas PROCEDIMIENTO 1. Desnaturalizar los productos de PCR a 94º C, 5 min. 2. Re-naturalizar transfiriendo rápidamente a hielo (4 ºC) y mantener min. 3. Ensamblar el gel de agarosa o poliacrilamida en su cubeta correspondiente y cubrir con tampón de electroforesis TBE 0,5X. 4. Tomar 20 µl de producto de PCR y mezclar con 4 µl de tampón de carga 6X. 5. Cargar las muestras en los pocillos del gel y colocar en uno de los carriles 10 µl del marcador de peso molecular. 6. Dejar transcurrir la electroforesis 1-2 h. a 100 Voltios. El voltaje y tiempo de corrido se pueden adaptar dependiendo del tipo de gel, cubeta de electroforesis, tamaño del producto amplificado, etc. 7. Teñir con 0.5µg/ml EtBr en agua o TBE 0,5X y visualizar en transiluminador con luz ultravioleta ELECTROFORESIS CAPILAR Las mezclas de PCR IgK-A, IgK-A, IgL y CI, contienen primers marcados con el fluorocromo 6-FAM, lo que permite que estos productos de PCR además de poder visualizarse por electroforesis convencional, se puedan analizar mediante electroforesis capilar. Los secuenciadores automáticos basados en la electroforesis capilar, como los equipos ABI PRISM 3100 o 3500 Genetic Analyzers de Applied Biosystems, constituyen sistemas con una alta tasa de reproducibilidad y sensibilidad en la secuenciación y análisis de fragmentos genómicos. La eficiencia supera a la mayoría de los análisis de secuencias basados en el uso de geles de acrilamida. Además, estos sistemas permiten el análisis de los resultados de un modo rápido y preciso mediante software especificados PREPARACIÓN DEL PRODUCTO DE PCR 1. Mezclar en un tubo eppendorf de 0.2 ml: 15 µl de formamida desionizada µl del marcador 600 LIZ + 1 ó 2 µl de ADN amplificado (este volumen de producto amplificado se puede modificar si la señal fluorescente está fuera del rango óptimo). 2. Homogeneizar en vortex y dar un pulso. 3. Desnaturalizar a 95ºC x 5 min, enfriar a 4º C y cargar en secuenciador master@vitroweb.com 7/12
8 Condiciones de electroforesis (3500 Genetic Analyzer): Polímero: POP-7 POLYMER Buffer: ANODE and CATHODE BUFFER CONTAINER 3500 SERIES Electroforesis: 40 minutos y entre 2-6 segundos de inyección. Intensidad óptima de fluorescencia: hasta un máximo de unidades CONDICIONES ÓPTIMAS PARA CARGAR LAS MUESTRAS Para comprobar que la muestra de ADN ha sido procesada correctamente y que hay ADN en cantidad y calidad suficientes para generar un resultado válido en el electroforograma, se recomienda cargar una alícuota de los productos de PCR (incluido el CI) en una electroforesis convencional teñida con EtBr, antes de analizar por GeneScan. Si se carga una cantidad excesiva de producto de PCR en la electroforesis capilar, se pueden artefactuar los picos tanto en el estándar de peso molecular como en el producto, resultando falsas lecturas. Así, un exceso de una muestra clonal puede resultar en un patrón de picos que simularía lo que podría ser una muestra policlonal. Para evitar este problema hay que asegurarse que la intensidad de la señal fluorescente se mantiene entre unidades de fluorescencia en los modelos 3100 y INTERPRETACIÓN DE LOS RESULTADOS 4.1. CONTROL INTERNO DE AMPLIFICACIÓN (CI) En todas las muestras debe aparecer una banda intensa (un pico, si se carga en 3500 Genetic Analyzer) de 269 pares de bases, lo que indica que el proceso de manipulación de la muestra y la calidad del ADN han sido adecuados. Este control de amplificación es imprescindible, sobre todo en aquellas muestras obtenidas de material incluido en parafina, en donde la calidad y cantidad del ADN obtenido son desconocidas. Si no aparece banda de amplificación con el CI, no se puede valorar un resultado negativo de amplificación de las cadenas IgK e IgL. Puede deberse a que no se haya obtenido ADN suficiente en el proceso de extracción, o a que el ADN esté parcialmente degradado. En estos casos se puede mejorar el rendimiento y la calidad del ADN prolongando la incubación del tejido con el tampón de lisis+proteasa durante horas más. Si tras repetir el proceso no se consigue amplificación, la muestra tendría que informarse como: no valorable para análisis de fragmentos de los genes IgK e IgL por PCR REORDENAMIENTOS DE FRAGMENTOS IgK e IgL En la siguiente tabla se indica el rango de tamaños esperado de los fragmentos amplificados para cada una de las mezclas de amplificación: master@vitroweb.com 8/12
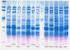
9 Tabla 2. Mezcla de cebadores Rangos de Tamaño (*)Los tamaños de los fragmentos para los controles positivos incluidos en el kit y que se indican en la tabla 2 se han obtenido con un 3500 Genetic Analyzer y analizado con Genemapper. Este tamaño puede variar entre 1-6 pb dependiendo tanto del equipo de electroforesis capilar como del software de análisis empleado. Una vez determinado el tamaño del amplicón en su propia plataforma, podrá considerar este valor como referencia y será reproducible en el resto de sus electroforesis CONTROLES POSITIVOS Y NEGATIVOS DE AMPLIFICACIÓN: ADN control positivo clonal(*) Color (tubo PCR) IgK-A , y pb 267 pb Azul IgK-B , y pb 234 y 280 pb Naranja IgL pb 138 y 142 pb Verde El control negativo de amplificación realizado con una muestra blanco tendría que dar ausencia de amplificación en todas las mezclas ensayadas (incluido CI). Si se detecta producto amplificado en alguna mezcla de PCR, estaría indicando la presencia de contaminación de los reactivos y habría que repetir el ensayo para validarlo. El control positivo policlonal debería dar múltiples bandas (gel) o picos (Genemapper) dentro del rango de tamaño indicado en la tabla 2 para cada mezcla de amplificación. El control positivo clonal dará una banda o pico único para cada una de las mezclas de PCR ensayadas, cuyo tamaño se indica en la tabla 2 Cualquier resultado diferente al esperado, obtenido tras analizar el ADN El control positivo policlonal, estaría indicando que el ensayo no es válido y las muestras problema no podrían ser interpretadas ANÁLISIS DE LA MUESTRA PROBLEMA: Antes de interpretar los resultados obtenidos con la muestra problema es necesario que todos los controles incluidos en el test, tanto positivos como negativos hayan sido correctos. GELES DE AGAROSA- POLIACRILAMIDA El reordenamiento clonal IgK se visualiza mediante electroforesis por la presencia de una única banda intensa y nítida dentro del rango de tamaño esperado (Figura 1). Se considera que una muestra es positiva cuando se detecta una banda con todas o alguna de las dos mezclas de amplificación ensayadas en el caso de IgK (IgK-A y/o IgK-B). Del mismo modo, en el caso de un reordenamiento clonal IgL, observaremos una banda única dentro del rango de tamaño esperado (Figura 1). Si no hay reordenamiento clonal y la muestra problema está compuesta por una población heterogénea policlonal de células B, se formará un heteroduplex y el resultado tras la electroforesis será una multitud de bandas dentro del rango de tamaño, que se visualizan en el gel como una mancha o smear ancha y difusa (Figura 1). ELECTROFORESIS CAPILAR Los productos de amplificación marcados con fluorocromo son separados mediante electroforesis capilar en función de su tamaño y se detectan automáticamente con un láser. master@vitroweb.com 9/12
10 El resultado puede ser una distribución gausiana de múltiples picos, representando múltiples productos amplificados con diferente tamaño (dentro del rango de tamaño esperado), en el caso de un proceso linfoproliferativo policlonal (Figura 2) y se informará como la muestra analizada no presenta reordenamiento clonal para los genes IgK e IgL con las condiciones de este ensayo. Cuando aparecen uno o dos picos únicos o prominentes, dentro del rango de tamaño, con todas o alguna de las mezclas de cebadores ensayadas IgK-A, IgK-B e IgL, se correspondería con un proceso linfoproliferativo clonal (Figura 2). Estos resultados se informarían como: la muestra analizada presenta reordenamiento clonal para el gen IgK con las condiciones de este ensayo (en caso de obtener estos picos para al menos una de las dos mix de PCR de IgK) o la muestra analizada presenta reordenamiento clonal para el gen IgL con las condiciones de este ensayo (si el pico obtenido se observa únicamente con la mix IgL). En caso de obtener un resultado similar a los descritos tanto para IgK como para IgL el caso se informará como: la muestra analizada presenta reordenamiento clonal para los genes IgK e IgL con las condiciones de este ensayo. A veces aparecen en un mismo electroferograma múltiples picos de diferente tamaño, alguno de los cuales resalta en altura frente a los demás. El criterio para considerar uno o dos picos positivos es que tengan una altura como mínimo 2,5 veces superior a la altura del resto de los picos adyacentes que representan el fondo policlonal. Igualmente ayuda a discriminar un pico positivo, el que el tamaño de dicho pico coincida en el duplicado, si se ha realizado un duplicado de amplificación. Si no supera ese valor, todos los picos se considerarían como correspondientes a una población policlonal. Si el pico o picos que resaltan está al límite de altura mínima necesaria para ser considerados clonales y no coinciden en tamaño en el duplicado de la muestra, habría que pensar que son picos pseudoclonales, obtenidos de una amplificación a partir de una muestra de ADN que contiene escaso número de células B en el seno de un proceso linfoproliferativo benigno. Figura 1. Análisis de resultados en gel de poliacrilamida 8%. A. Patrón clonal genes Igk e IgL:1. Estándar de peso molecular (MW), 2. Patrón monoclonal IgK-A, 3. Patrón monoclonal IgK-B, 4. Patrón monoclonal IgL, 5. Control interno de amplificación (CI). B. Patrón policlonal genes Igk e IgL: 1. Estándar MW, 2. Patrón policlonal IgK-A, 3. Patrón policlonal IgK-B, 4. Patrón policlonal IgL, 5. Control interno de amplificación (CI). master@vitroweb.com 10/12
11 Figura 2. Electroferogramas obtenidos tras el análisis por electroforesis capilar y Genemapper. A. Picos monoclonales para los genes IgK-A, IgK-B e IgL B. Típica distribución gaussiana de una población policlonal para los genes IgK-A, IgK-B e IgL. 5. LIMITACIONES DEL ENSAYO En una muestra que contenga una mezcla de células B tumorales (clonales) y una población de células B reactivas acompañante, puede ocurrir que la banda nítida indicativa de clonalidad quede enmascarada por el resto de las múltiples bandas y no sea posible su visualización mediante electroforesis en gel o GeneScan. Este método es capaz de detectar un mínimo de 5-20 células tumorales (IgK-IgL) entre 100 células normales (Tabla 3). Los resultados se han obtenido tras ensayar las tres mezclas de amplificación con diluciones seriadas de una muestra de ADN procedente de la línea celular de linfoma B con un ADN de linfocitos de sangre periférica. Tabla 3. Resultados de límite de detección Mezcla Limite de detección IgK-A 10 ng ADN clonal (5 % en 0.2µg totales) IgK-B 10 ng ADN clonal (5 % en 0.2µg totales) IgK-L 40 ng ADN clonal (20% en 0.2µg totales) Un resultado negativo de clonalidad con este ensayo, no excluye el diagnóstico de linfoma por otro tipo de datos clínicos, morfológicos e inmunofenotípicos. master@vitroweb.com 11/12
12 6. BIBLIOGRAFÍA Langerak AW, Szczepanski T, van der Burg M, Wolvers-Tettero ILM and Dongen JJM. Heteroduplex PCR analysis of rearranged T cell receptor genes for clonality assessment in suspect T-cell proliferations. Leukemia 1997; 11: Pas Evans, et al. Significantly improved PCR-based clonality testing in tissue samples with reactive lymphoproliferations: usefulness and pitfalls. A report of the BIOMED-2 Concerted Action BMH4-CT Leukemia Feb;21(2): Van Krieken JH, et al. Improved reliability of lymphoma diagnostics via PCR-based clonality testing: report of the BIOMED-2 Concerted Action BHM4-CT Leukemia Feb; 21(2): Payne K, Wright P, Grant JW, Huang Y, Hamoudi R, Bacon CM, Du MQ, Liu H. BIOMED-2 PCR assays for IGK gene rearrangements are essential for B-cell clonality analysis in follicular lymphoma. Br J Haematol Oct;155(1):84-92 Langerak AW, et al. EuroClonality/BIOMED-2 guidelines for interpretation and reporting of Ig/TCR clonality testing in suspected lymphoproliferations. Leukemia 2012, 26, Rev.: AO Oct 2013 master@vitroweb.com 12/12
Características del kit:
 ! La detección de clonalidad mediante análisis molecular por PCR de reordenamientos de los genes de las inmunoglobulinas (Ig) y TCR, es un instrumento de gran valor en el diagnóstico de los procesos linfoproliferativos
! La detección de clonalidad mediante análisis molecular por PCR de reordenamientos de los genes de las inmunoglobulinas (Ig) y TCR, es un instrumento de gran valor en el diagnóstico de los procesos linfoproliferativos
- Las mezclas de amplificación se presentan en formato monotest en tubos de PCR de 0.2 ó 0.5 ml, identificadas con diferentes colores.
 ! El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos,
! El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos,
Materiales para la secuenciación de ADN
 Introduccion La Secuenciación Sanger es un método de secuenciación de ADN en el que el ADN diana se desnaturaliza y se hibrida con un cebador de oligonucleótidos, que se extiende entonces gracias a la
Introduccion La Secuenciación Sanger es un método de secuenciación de ADN en el que el ADN diana se desnaturaliza y se hibrida con un cebador de oligonucleótidos, que se extiende entonces gracias a la
- Las mezclas de amplificación se presentan en formato monotest en tubos de PCR de 0.2 0.5 ml, identificados con diferente color.
 ! El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos,
! El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos,
DETERMINACIÓN DEL FACTOR Rh por PCR
 Ref.PCRRh DETERMINACIÓN DEL FACTOR Rh por PCR 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
Ref.PCRRh DETERMINACIÓN DEL FACTOR Rh por PCR 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
3. COMPONENTES. Tampón de electroforesis concentrado 2 x 50 ml 10 X (2 envases 500ml)
 PCR SIMULADA Ref.PCR Simulada (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
PCR SIMULADA Ref.PCR Simulada (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
APLICACIÓN DE LA PCR: DIAGNÓSTICO DE PARÁSITOS
 Prácticas docentes en la COD: 10-71 APLICACIÓN DE LA PCR: DIAGNÓSTICO DE PARÁSITOS FUNDAMENTO TEÓRICO La PCR es una técnica que permite llevar a cabo la síntesis in vitro de fragmentos de ADN. Está basada
Prácticas docentes en la COD: 10-71 APLICACIÓN DE LA PCR: DIAGNÓSTICO DE PARÁSITOS FUNDAMENTO TEÓRICO La PCR es una técnica que permite llevar a cabo la síntesis in vitro de fragmentos de ADN. Está basada
PROBLEMAS MÁS FRECUENTES Y POSIBLES SOLUCIONES
 PROBLEMAS MÁS FRECUENTES Y POSIBLES SOLUCIONES NO SE PRODUCE REACCIÓN O ÉSTA DECAE POCO DESPUÉS DE COMENZAR No hay ADN o hay menos del necesario No hay cebador o la concentración es inferior a la necesaria.
PROBLEMAS MÁS FRECUENTES Y POSIBLES SOLUCIONES NO SE PRODUCE REACCIÓN O ÉSTA DECAE POCO DESPUÉS DE COMENZAR No hay ADN o hay menos del necesario No hay cebador o la concentración es inferior a la necesaria.
Código: IDX-016 Ver: 1 TOXO. Sistema para la detección de la presencia de ADN de Toxoplasma gondii. Reg. MSP 21205
 Sistema para la detección de la presencia de ADN de Toxoplasma gondii Reg. MSP 21205 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. info@atgen.com.uy www.atgen.com.uy
Sistema para la detección de la presencia de ADN de Toxoplasma gondii Reg. MSP 21205 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. info@atgen.com.uy www.atgen.com.uy
Código: IDK-010 Ver: 1. Proteína G C825T. Sistema para la detección de la mutación C825T en el gene de la proteína G.
 C825T Sistema para la detección de la mutación C825T en el gene de la proteína G. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy www.atgen.com.uy
C825T Sistema para la detección de la mutación C825T en el gene de la proteína G. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy www.atgen.com.uy
DANAGENE SALIVA KIT. Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones
 DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION DANAGENE SALIVA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras
DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION DANAGENE SALIVA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras
velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz porosa
 INTRODUCCIÓN En general, la electroforesis es una técnica que separa las moléculas en base a sus diferentes velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz
INTRODUCCIÓN En general, la electroforesis es una técnica que separa las moléculas en base a sus diferentes velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz
ELECTROFORESIS BASICA
 Ref.ELECBASICA (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO ELECTROFORESIS BASICA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref.ELECBASICA (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO ELECTROFORESIS BASICA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Módulo 1 Biología Molecular Genética Molecular II 2009. Módulo 1. Amplificación de un fragmento de ADN genómico por PCR
 Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
PROBLEMAS MAS FRECUENTES DURANTE LA SECUENCIACIÓN NO SE PRODUCE REACCION O ESTA DECAE POCO DESPUÉS DE COMENZAR
 PROBLEMAS MAS FRECUENTES DURANTE LA SECUENCIACIÓN NO SE PRODUCE REACCION O ESTA DECAE POCO DESPUÉS DE COMENZAR Las causas pueden ser las siguientes: No hay ADN o se encuentra en muy baja concentración.
PROBLEMAS MAS FRECUENTES DURANTE LA SECUENCIACIÓN NO SE PRODUCE REACCION O ESTA DECAE POCO DESPUÉS DE COMENZAR Las causas pueden ser las siguientes: No hay ADN o se encuentra en muy baja concentración.
Procesado de muestras en el laboratorio de la clínica (I)
 12.prevención de la salud Procesado de muestras en el laboratorio de la clínica (I) A lo largo de esta primera parte veremos como realizar un manejo correcto de las muestras de sangre, orina y líquidos
12.prevención de la salud Procesado de muestras en el laboratorio de la clínica (I) A lo largo de esta primera parte veremos como realizar un manejo correcto de las muestras de sangre, orina y líquidos
Nuevos paneles de PCR Real Time: El diagnóstico molecular más rápido, fiable y eficaz
 IDEXX VetLab Suite IDEXX SNAP Tests Laboratorio de Referencia IDEXX Nuevos paneles de PCR Real Time: El diagnóstico molecular más rápido, fiable y eficaz Obtenga respuestas definitivas con la IDEXX RealPCR
IDEXX VetLab Suite IDEXX SNAP Tests Laboratorio de Referencia IDEXX Nuevos paneles de PCR Real Time: El diagnóstico molecular más rápido, fiable y eficaz Obtenga respuestas definitivas con la IDEXX RealPCR
ELECTROFORESIS AVANZADA
 Ref.ELECAVANZADA (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref.ELECAVANZADA (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
DETECCIÓN DE C. jejuni EN HAMBURGUESA DE POLLO POR PCR TRADICIONAL PRT-712.04-082
 Página 1 de 5 1. OBJETIVO Detectar la presencia de Campylobacter jejuni en hamburguesa de pollo mediante técnica de PCR. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a muestras de hamburguesa
Página 1 de 5 1. OBJETIVO Detectar la presencia de Campylobacter jejuni en hamburguesa de pollo mediante técnica de PCR. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a muestras de hamburguesa
TaqMan GMO Maize Quantification Kit. Part No: 4481972
 TaqMan GMO Maize Quantification Kit Part No: 4481972 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que ocupan
TaqMan GMO Maize Quantification Kit Part No: 4481972 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que ocupan
PCR gen 18S ARNr humano
 PCR gen 18S ARNr humano Ref.PCR18S 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa (PCR)
PCR gen 18S ARNr humano Ref.PCR18S 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa (PCR)
CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL
 LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
Prueba ABtest. Para la cuantificación del pool beta-amiloide en sangre TOTAL
 Prueba Para la cuantificación del pool beta-amiloide en sangre TOTAL Introducción Es esencial un diagnóstico temprano. En la práctica clínica actual el diagnóstico de la enfermedad de Alzheimer se realiza
Prueba Para la cuantificación del pool beta-amiloide en sangre TOTAL Introducción Es esencial un diagnóstico temprano. En la práctica clínica actual el diagnóstico de la enfermedad de Alzheimer se realiza
Protocolos de secuenciación de ADN
 1 Protocolos de secuenciación de ADN Introducción El método de secuenciación utilizado aquí es el desarrollado por Sanger en 1975. Este consiste en la incorporación de didesixinucleótidos marcados fluorescentemente
1 Protocolos de secuenciación de ADN Introducción El método de secuenciación utilizado aquí es el desarrollado por Sanger en 1975. Este consiste en la incorporación de didesixinucleótidos marcados fluorescentemente
TaqMan GMO Screening Kit. Part No: 4466334
 TaqMan GMO Screening Kit Part No: 4466334 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que ocupan mayor
TaqMan GMO Screening Kit Part No: 4466334 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que ocupan mayor
DANAGENE RNA PURIFICATION KIT
 DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
imegen Alfa-1-AT Manual de Usuario Referencia: IMG-211
 Manual de Usuario imegen Alfa-1-AT Genotipado de las mutaciones Glu342Lys (PI-Z) y Glu264Val (PI-S) del gen SERPINA1 mediante PCR a tiempo real Referencia: Fabricado en España Garantías y responsabilidades
Manual de Usuario imegen Alfa-1-AT Genotipado de las mutaciones Glu342Lys (PI-Z) y Glu264Val (PI-S) del gen SERPINA1 mediante PCR a tiempo real Referencia: Fabricado en España Garantías y responsabilidades
PROCEDIMIENTO PARA LA UTILIZACIÓN DEL POLIMORFISMO DEL GEN COMT (CATECOL-OXI-METILTRANSFERASA) EN EL DIAGNÓSTICO DEL SÍNDROME DE FIBROMIALGIA
 2 PROCEDIMIENTO PARA LA UTILIZACIÓN DEL POLIMORFISMO DEL GEN COMT (CATECOL-OXI-METILTRANSFERASA) EN EL DIAGNÓSTICO DEL SÍNDROME DE FIBROMIALGIA D E S C R I P C I Ó N OBJETO DE LA INVENCIÓN La presente
2 PROCEDIMIENTO PARA LA UTILIZACIÓN DEL POLIMORFISMO DEL GEN COMT (CATECOL-OXI-METILTRANSFERASA) EN EL DIAGNÓSTICO DEL SÍNDROME DE FIBROMIALGIA D E S C R I P C I Ó N OBJETO DE LA INVENCIÓN La presente
CUADERNO DE PRÁCTICAS GENETICA MOLECULAR HUMANA. Grado en Medicina
 DEPARTAMENTO DE BIOQUÍMICA Y BIOLOGÍA MOLECULAR III FACULTAD DE MEDICINA UNIVERSIDAD COMPLUTENSE DE MADRID CUADERNO DE PRÁCTICAS GENETICA MOLECULAR HUMANA Grado en Medicina CURSO ACADÉMICO 2014/2015 INDICE
DEPARTAMENTO DE BIOQUÍMICA Y BIOLOGÍA MOLECULAR III FACULTAD DE MEDICINA UNIVERSIDAD COMPLUTENSE DE MADRID CUADERNO DE PRÁCTICAS GENETICA MOLECULAR HUMANA Grado en Medicina CURSO ACADÉMICO 2014/2015 INDICE
3/22/2010. Iván Ferrer Rodríguez, PhD Catedrático. En el 1983, Kary Mullis dio a conocer la Técnica de reacción en cadena de la Polimerasa o PCR.
 Iván Ferrer Rodríguez, PhD Catedrático En el 1983, Kary Mullis dio a conocer la Técnica de reacción en cadena de la Polimerasa o PCR. Síntesis "in vitro" de secuencias específicas de ADN son amplificadas.
Iván Ferrer Rodríguez, PhD Catedrático En el 1983, Kary Mullis dio a conocer la Técnica de reacción en cadena de la Polimerasa o PCR. Síntesis "in vitro" de secuencias específicas de ADN son amplificadas.
ELABORACIÓN N DE MEZCLA PARA PCR. Raquel Asunción Lima Cordón
 ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN
 5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
SECUENCIACIÓN SANGER DE ADN: GUÍA DE SOLUCIONES TÉCNICAS
 SECUENCIACIÓN SANGER DE ADN: GUÍA DE SOLUCIONES TÉCNICAS Secugen recomienda que para la visualización de las secuencias se usen programas que permitan ver el dato crudo, ya que a partir de ese dato se
SECUENCIACIÓN SANGER DE ADN: GUÍA DE SOLUCIONES TÉCNICAS Secugen recomienda que para la visualización de las secuencias se usen programas que permitan ver el dato crudo, ya que a partir de ese dato se
1. Título. Cuantificacion de ADN por espectrofluorometría mediante el uso de Quant- it PicoGreen dsaadnssay Kit (Invitrogen ).
 1. Título. Cuantificacion de ADN por espectrofluorometría mediante el uso de QuantiT PicoGreen dsaadnssay Kit (Invitrogen ). 2. Finalidad. El presente documento describe el Procedimiento Normalizado de
1. Título. Cuantificacion de ADN por espectrofluorometría mediante el uso de QuantiT PicoGreen dsaadnssay Kit (Invitrogen ). 2. Finalidad. El presente documento describe el Procedimiento Normalizado de
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 Unidad Curricular: Virología y Micología Veterinaria 1 TRABAJO PRÁCTICO No. 3 AMPLIFICACIÓN DE GENES VIRALES Reacción en Cadena de la Polimerasa, conocida como PCR (por sus siglas en inglés: Polimerase
Unidad Curricular: Virología y Micología Veterinaria 1 TRABAJO PRÁCTICO No. 3 AMPLIFICACIÓN DE GENES VIRALES Reacción en Cadena de la Polimerasa, conocida como PCR (por sus siglas en inglés: Polimerase
EFECTO DE LA DIGESTIÓN SOBRE PROTEINAS, GRASAS Y GLÚCIDOS
 EFECTO DE LA DIGESTIÓN SOBRE PROTEINAS, GRASAS Y GLÚCIDOS Objetivos: Mª Jesús González García Mª Amparo Mora Alcácer COLEGIO AVE Mª DE PENYA-ROJA Aprender a trabajar en el laboratorio y apreciar el orden,
EFECTO DE LA DIGESTIÓN SOBRE PROTEINAS, GRASAS Y GLÚCIDOS Objetivos: Mª Jesús González García Mª Amparo Mora Alcácer COLEGIO AVE Mª DE PENYA-ROJA Aprender a trabajar en el laboratorio y apreciar el orden,
AUTOR: JORGE CONTRERAS PINEDA 1. Titulo:
 Página 1 de 1 1. Titulo: Electroforesis de DNA 2. Objetivo Conocer los principios básicos de la electroforesis horizontal en geles de agarosa y aplicarlo para la separación de DNA humano, plasmídico, recombinante
Página 1 de 1 1. Titulo: Electroforesis de DNA 2. Objetivo Conocer los principios básicos de la electroforesis horizontal en geles de agarosa y aplicarlo para la separación de DNA humano, plasmídico, recombinante
PROTOCOLO DE EXTRACCIÓN DE MUESTRAS FRESCAS DE TEJIDO DE AVES PARA ESTUDIOS GENÉTICOS
 PROTOCOLO DE EXTRACCIÓN DE MUESTRAS FRESCAS DE TEJIDO DE AVES PARA ESTUDIOS GENÉTICOS La mejor fuente de tejido fresco para la realización de estudios genéticos son los músculos. En el caso de aves la
PROTOCOLO DE EXTRACCIÓN DE MUESTRAS FRESCAS DE TEJIDO DE AVES PARA ESTUDIOS GENÉTICOS La mejor fuente de tejido fresco para la realización de estudios genéticos son los músculos. En el caso de aves la
1 MATERIALES Y MÉTODOS
 1 MATERIALES Y MÉTODOS El presente protocolo experimental contempla la amplificación del DNA de las bacterias y virus causantes de las ETS Neisseria gonorrhoeae, Chlamydia trachomatis y VPH mediante PCR
1 MATERIALES Y MÉTODOS El presente protocolo experimental contempla la amplificación del DNA de las bacterias y virus causantes de las ETS Neisseria gonorrhoeae, Chlamydia trachomatis y VPH mediante PCR
2. NIVEL MEDIO 1. NIVEL BASICO BIOLOGIA MOLECULAR 2.1 DNA SALIVA
 BIOLOGIA MOLECULAR Hemos elaborado un programa en 3 niveles, en función del tipo de estudiante y las posibilidades del centro educativo: 1. NIVEL BASICO 2. NIVEL MEDIO DANAEXTRACTOR KIT Práctica que constituye
BIOLOGIA MOLECULAR Hemos elaborado un programa en 3 niveles, en función del tipo de estudiante y las posibilidades del centro educativo: 1. NIVEL BASICO 2. NIVEL MEDIO DANAEXTRACTOR KIT Práctica que constituye
17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico
 17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico Carmen Alicia Padilla Peña, Jesús Diez Dapena, Emilia Martínez Galisteo, José
17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico Carmen Alicia Padilla Peña, Jesús Diez Dapena, Emilia Martínez Galisteo, José
PROYECTO MEDICINA PERSONALIZADA PARA EL CÁNCER INFANTIL CÁNCER INFANTIL. Javier Alonso
 Página: 1 de 8 PROYECTO MEDICINA PERSONALIZADA PARA EL Javier Alonso Jefe de Área de Genética Humana. Jefe de la Unidad de Tumores Sólidos Infantiles del Instituto de Investigación de Enfermedades Raras,
Página: 1 de 8 PROYECTO MEDICINA PERSONALIZADA PARA EL Javier Alonso Jefe de Área de Genética Humana. Jefe de la Unidad de Tumores Sólidos Infantiles del Instituto de Investigación de Enfermedades Raras,
Practica la genética Ficha didáctica del profesorado Bachillerato
 Ficha didáctica del profesorado Bachillerato www.eurekamuseoa.es Extracción de ADN Cuál es la función de cada uno de los ingredientes utilizados para realizar la disolución tampón para la visualización
Ficha didáctica del profesorado Bachillerato www.eurekamuseoa.es Extracción de ADN Cuál es la función de cada uno de los ingredientes utilizados para realizar la disolución tampón para la visualización
Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a
 Introducción Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a los investigadores verificar la expresión de una proteína, determinar la cantidad relativa
Introducción Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a los investigadores verificar la expresión de una proteína, determinar la cantidad relativa
RESOLUCIÓN OENO 5/2007
 RESOLUCIÓN OENO 5/2007 CODEX - GLICOSIDASA LA ASAMBLEA GENERAL Visto el Artículo 2, párrafo 2 iv del acuerdo del 3 de abril de 2001 por el cual se creó la Organización Internacional de la Viña y el Vino,
RESOLUCIÓN OENO 5/2007 CODEX - GLICOSIDASA LA ASAMBLEA GENERAL Visto el Artículo 2, párrafo 2 iv del acuerdo del 3 de abril de 2001 por el cual se creó la Organización Internacional de la Viña y el Vino,
P.C.R. "Técnica de amplificación enzimática de secuencias específicas de DNA"
 P.C.R. "Técnica de amplificación enzimática de secuencias específicas de DNA" Paso 1: Desnaturalización del DNA Paso 2: Hibridación de los "Primers" Paso 3: Extensión Paso 1: Desnaturalización del DNA
P.C.R. "Técnica de amplificación enzimática de secuencias específicas de DNA" Paso 1: Desnaturalización del DNA Paso 2: Hibridación de los "Primers" Paso 3: Extensión Paso 1: Desnaturalización del DNA
METODOLOGÍAS UTILIZADAS EN INVESTIGACIÓN BÁSICA Y APLICADA REACCION EN CADENA DE LA POLIMERASA (PCR)
 METODOLOGÍAS UTILIZADAS EN INVESTIGACIÓN BÁSICA Y APLICADA REACCION EN CADENA DE LA POLIMERASA (PCR) Centro de de Microscopía Electrónica Facultad de de Ciencias Médicas Universidad Nacional de de Córdoba
METODOLOGÍAS UTILIZADAS EN INVESTIGACIÓN BÁSICA Y APLICADA REACCION EN CADENA DE LA POLIMERASA (PCR) Centro de de Microscopía Electrónica Facultad de de Ciencias Médicas Universidad Nacional de de Córdoba
INSTRUCCIONES DE INSTALACIÓN Y RECARGA CISS HP CARTUCHO SERIE 1
 Antes de empezar Es muy importante que no realice ninguna acción hasta leer completamente las instrucciones. Léalas de forma detenida y completa!!! Es muy importante que compruebe que su impresora se encuentra
Antes de empezar Es muy importante que no realice ninguna acción hasta leer completamente las instrucciones. Léalas de forma detenida y completa!!! Es muy importante que compruebe que su impresora se encuentra
5. MATERIALES Y MÉTODOS
 5. MATERIALES Y MÉTODOS 5.1 Equipos Los siguientes termocicladores se emplearon para la amplificación por PCR: - Perkin Elmer, GeneAmp PCR System 2400. - Perkin Elmer, GeneAmp PCR System 9600. - Applied
5. MATERIALES Y MÉTODOS 5.1 Equipos Los siguientes termocicladores se emplearon para la amplificación por PCR: - Perkin Elmer, GeneAmp PCR System 2400. - Perkin Elmer, GeneAmp PCR System 9600. - Applied
NMX-F-070-1964. MÉTODO DE PRUEBA PARA LA DETERMINACIÓN DE TIAMINA. THIAMINE DETERMINATION. TEST METHOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS.
 NMX-F-070-1964. MÉTODO DE PRUEBA PARA LA DETERMINACIÓN DE TIAMINA. THIAMINE DETERMINATION. TEST METHOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. ASUNTO Con fundamento en lo dispuesto en los Artículos
NMX-F-070-1964. MÉTODO DE PRUEBA PARA LA DETERMINACIÓN DE TIAMINA. THIAMINE DETERMINATION. TEST METHOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. ASUNTO Con fundamento en lo dispuesto en los Artículos
PROTOCOLOS DE OBTENCIÓN, CONSERVACIÓN Y ENVÍO DE MUESTRAS BIOLÓGICAS
 PROTOCOLOS DE OBTENCIÓN, CONSERVACIÓN Y ENVÍO DE MUESTRAS BIOLÓGICAS ESTUDIO TRASLACIONAL PROSPECTIVO DE DETERMINACIÓN DE FACTORES PREDICTIVOS DE EFICACIA Y TOXICIDAD EN PACIENTES CON CÁNCER ÍNDICE 1 INTRODUCCIÓN....
PROTOCOLOS DE OBTENCIÓN, CONSERVACIÓN Y ENVÍO DE MUESTRAS BIOLÓGICAS ESTUDIO TRASLACIONAL PROSPECTIVO DE DETERMINACIÓN DE FACTORES PREDICTIVOS DE EFICACIA Y TOXICIDAD EN PACIENTES CON CÁNCER ÍNDICE 1 INTRODUCCIÓN....
CUANTIFICACIÓN DE ADENOSIN DESAMINASA (ADA)
 CUANTIFICACIÓN DE ADENOSIN DESAMINASA (ADA) PROTOCOLO ADA FUNDAMENTO DEL METODO: La adenosindesaminasa (ADA) es una enzima del catabolismo de las purinas que cataliza la conversión de la adenosina en inosina
CUANTIFICACIÓN DE ADENOSIN DESAMINASA (ADA) PROTOCOLO ADA FUNDAMENTO DEL METODO: La adenosindesaminasa (ADA) es una enzima del catabolismo de las purinas que cataliza la conversión de la adenosina en inosina
LICITACIÓN PÚBLICA INTERNACIONAL PER/193/1630 ADQUISICIÓN DE ANALIZADORES AUTOMATICOS Y TERMOCICLADOR PARA EL HOSPITAL REGIONAL DE LAMBAYEQUE
 LICITACIÓN PÚBLICA INTERNACIONAL PER/193/1630 ADQUISICIÓN DE ANALIZADORES AUTOMATICOS Y TERMOCICLADOR PARA EL HOSPITAL REGIONAL DE LAMBAYEQUE Consultas y Pedido de Aclaraciones al Contenido de las Bases
LICITACIÓN PÚBLICA INTERNACIONAL PER/193/1630 ADQUISICIÓN DE ANALIZADORES AUTOMATICOS Y TERMOCICLADOR PARA EL HOSPITAL REGIONAL DE LAMBAYEQUE Consultas y Pedido de Aclaraciones al Contenido de las Bases
Operación de Microsoft Excel. Guía del Usuario Página 79. Centro de Capacitación en Informática
 Manejo básico de base de datos Unas de las capacidades de Excel es la de trabajar con listas o tablas de información: nombres, direcciones, teléfonos, etc. Excel puede trabajar con tablas de información
Manejo básico de base de datos Unas de las capacidades de Excel es la de trabajar con listas o tablas de información: nombres, direcciones, teléfonos, etc. Excel puede trabajar con tablas de información
En los programas de estudio para sus estudiantes los Aprendizajes incluidos en la actividad son:
 INTRODUCCIÓN Recordemos que lo que define a un ser vivo entre otras funciones, es su función reproductiva, que permite que una especie se perpetúe en el tiempo, manteniendo las características de sus progenitores,
INTRODUCCIÓN Recordemos que lo que define a un ser vivo entre otras funciones, es su función reproductiva, que permite que una especie se perpetúe en el tiempo, manteniendo las características de sus progenitores,
SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO
 Actividad Experimental SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO Investigación previa 1.- Investigar las medidas de seguridad que hay que mantener al manipular KOH y H SO, incluyendo que acciones
Actividad Experimental SEPARACIÓN DE ALUMINIO A PARTIR DE MATERIAL DE DESECHO Investigación previa 1.- Investigar las medidas de seguridad que hay que mantener al manipular KOH y H SO, incluyendo que acciones
NORMAS DE TRABAJO EN BIOLOGÍA MOLECULAR Y GUÍA DE PROBLEMAS HABITUALES Y SU SOLUCIÓN
 NORMAS DE TRABAJO EN BIOLOGÍA MOLECULAR Y GUÍA DE PROBLEMAS HABITUALES Y SU SOLUCIÓN 1. PROCEDIMIENTOS BÁSICOS: En este apartado pretendemos detallar algunos factores muy importantes a la hora de realizar
NORMAS DE TRABAJO EN BIOLOGÍA MOLECULAR Y GUÍA DE PROBLEMAS HABITUALES Y SU SOLUCIÓN 1. PROCEDIMIENTOS BÁSICOS: En este apartado pretendemos detallar algunos factores muy importantes a la hora de realizar
KIT PARA ANÁLISIS MOLECULAR DEL GEN IgH Nº CAT. MAD BP-2/5 (20 DETERMINACIONES)
 KIT PARA ANÁLISIS MOLECULAR DEL GEN IgH Nº CAT. MAD-003994BP-2/5 (20 DETERMINACIONES) El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología.
KIT PARA ANÁLISIS MOLECULAR DEL GEN IgH Nº CAT. MAD-003994BP-2/5 (20 DETERMINACIONES) El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología.
Reacción en cadena de la polimerasa (PCR)
 Dr. Alejandro Leal Reacción en cadena de la polimerasa (PCR) La reacción en cadena de la polimerasa (PCR, por sus siglas en inglés de "polymerase chain reaction") es un método de amplificación in vitro
Dr. Alejandro Leal Reacción en cadena de la polimerasa (PCR) La reacción en cadena de la polimerasa (PCR, por sus siglas en inglés de "polymerase chain reaction") es un método de amplificación in vitro
Práctico: Genética bacteriana 2007.
 Práctico: Genética bacteriana 2007. Actividad integrada Departamento de Genética Departamento de Bacteriología y Virología. OBJETIVOS Objetivos generales El estudiante al terminar la actividad práctica
Práctico: Genética bacteriana 2007. Actividad integrada Departamento de Genética Departamento de Bacteriología y Virología. OBJETIVOS Objetivos generales El estudiante al terminar la actividad práctica
ASEGURAMIENTO DE LA CALIDAD EN LABORATORIO
 FUNDACION NEXUS ASEGURAMIENTO DE LA CALIDAD EN LABORATORIO Marzo de 2012 CALIDAD, CONTROL DE LA CALIDAD Y ASEGURAMIENTO DE LA CALIDAD El laboratorio de análisis ofrece a sus clientes un servicio que se
FUNDACION NEXUS ASEGURAMIENTO DE LA CALIDAD EN LABORATORIO Marzo de 2012 CALIDAD, CONTROL DE LA CALIDAD Y ASEGURAMIENTO DE LA CALIDAD El laboratorio de análisis ofrece a sus clientes un servicio que se
PROTOCOLO DE ACTUACIÓN PARA EXTRACCIONES PARA ESTUDIOS DE HEMOSTASIA Y TROMBOSIS
 PROTOCOLO DE ACTUACIÓN PARA EXTRACCIONES PARA ESTUDIOS DE HEMOSTASIA Y TROMBOSIS IDENTIFICACIÓN DEL PACIENTE Todas las muestras deben ir acompañadas de una solicitud debidamente formulada. La solicitud
PROTOCOLO DE ACTUACIÓN PARA EXTRACCIONES PARA ESTUDIOS DE HEMOSTASIA Y TROMBOSIS IDENTIFICACIÓN DEL PACIENTE Todas las muestras deben ir acompañadas de una solicitud debidamente formulada. La solicitud
ENFERMEDADES INFECCIOSAS GRADO EN VETERINARIA
 FACULTAD DE VETERINARIA DEPARTAMENTO DE SANIDAD ANIMAL ENFERMEDADES INFECCIOSAS GRADO EN VETERINARIA GUIÓN DE PRÁCTICAS DE LABORATORIO CURSO 2014 2015 MÓDULO: PORCINO Síndrome respiratorio y reproductor
FACULTAD DE VETERINARIA DEPARTAMENTO DE SANIDAD ANIMAL ENFERMEDADES INFECCIOSAS GRADO EN VETERINARIA GUIÓN DE PRÁCTICAS DE LABORATORIO CURSO 2014 2015 MÓDULO: PORCINO Síndrome respiratorio y reproductor
El Banco Nacional de ADN oferta un control de calidad de muestras de ADN y ARN.
 PROGRAMA CONTROL DE CALIDAD DE MUESTRAS El Banco Nacional de ADN oferta un control de calidad de muestras de ADN y ARN. El programa completo de control de calidad de muestras de ADN y ARN engloba diferentes
PROGRAMA CONTROL DE CALIDAD DE MUESTRAS El Banco Nacional de ADN oferta un control de calidad de muestras de ADN y ARN. El programa completo de control de calidad de muestras de ADN y ARN engloba diferentes
PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN DE LAS COMPETENCIAS PROFESIONALES CUESTIONARIO DE AUTOEVALUACIÓN PARA LAS TRABAJADORAS Y TRABAJADORES
 MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
TÉCNICAS GENÓMICAS. 2) Cuantificación del número de virus presentes en muestras de sangre o suero: carga vírica
 TÉCNICAS GENÓMICAS Utilidad/Objetivos: 1) Detección de microorganismos directamente en muestras clínicas identificando un fragmento específico del genoma del microorganismo concreto 2) Cuantificación del
TÉCNICAS GENÓMICAS Utilidad/Objetivos: 1) Detección de microorganismos directamente en muestras clínicas identificando un fragmento específico del genoma del microorganismo concreto 2) Cuantificación del
4. METODOLOGÍA. 4.1 Materiales. 4.1.1 Equipo
 4. METODOLOGÍA 4.1 Materiales 4.1.1 Equipo Equipo de cómputo. Para el empleo del la metodología HAZOP se requiere de un equipo de cómputo con interfase Windows 98 o más reciente con procesador Pentium
4. METODOLOGÍA 4.1 Materiales 4.1.1 Equipo Equipo de cómputo. Para el empleo del la metodología HAZOP se requiere de un equipo de cómputo con interfase Windows 98 o más reciente con procesador Pentium
2.3 SISTEMAS HOMOGÉNEOS.
 2.3 SISTEMAS HOMOGÉNEOS. 2.3.1 DISOLUCIONES. Vemos que muchos cuerpos y sistemas materiales son heterogéneos y podemos observar que están formados por varias sustancias. En otros no podemos ver que haya
2.3 SISTEMAS HOMOGÉNEOS. 2.3.1 DISOLUCIONES. Vemos que muchos cuerpos y sistemas materiales son heterogéneos y podemos observar que están formados por varias sustancias. En otros no podemos ver que haya
TEMA 1 INTRODUCCIÓN AL ANÁLISIS QUÍMICO
 TEMA 1 INTRODUCCIÓN AL ANÁLISIS QUÍMICO Este tema aporta una revisión panorámica del Análisis Químico, sus distintas vertientes y su terminología básica. La importancia de la Química Analítica queda plasmada
TEMA 1 INTRODUCCIÓN AL ANÁLISIS QUÍMICO Este tema aporta una revisión panorámica del Análisis Químico, sus distintas vertientes y su terminología básica. La importancia de la Química Analítica queda plasmada
CUESTIONES. 1. Por qué la PCR convencional no es cuantitativa?
 2º BIOQUÍMICA CUESTIONES 1. Por qué la PCR convencional no es cuantitativa? En la PCR convencional, la cuantificación del ADN de la muestra es complicada debido a que la eficacia de amplificación va disminuyendo
2º BIOQUÍMICA CUESTIONES 1. Por qué la PCR convencional no es cuantitativa? En la PCR convencional, la cuantificación del ADN de la muestra es complicada debido a que la eficacia de amplificación va disminuyendo
ANÁLISIS DE ELEMENTOS TRAZA EN ESPECÍMENES BIOLÓGICOS: Objetivo. Metodología
 FTTM07 Rev-1, 09/06/20119 INSTITUTO DE TOXICOLOGÍA DE LA DEFENSA Hospital Central de la Defensa. Glorieta del Ejército s/n. 28047 MADRID. Tel.: 914222625. Fax: 914222624 E- mails : jlopcol@oc.mde.es //mllobal@oc.mde.es//
FTTM07 Rev-1, 09/06/20119 INSTITUTO DE TOXICOLOGÍA DE LA DEFENSA Hospital Central de la Defensa. Glorieta del Ejército s/n. 28047 MADRID. Tel.: 914222625. Fax: 914222624 E- mails : jlopcol@oc.mde.es //mllobal@oc.mde.es//
CÁMARA THOMA Y NEUBAUER IMPROVED PARA EL RECUENTO DE LEVADURAS (TIRAJE)
 1/5 CÁMARA THOMA Y NEUBAUER IMPROVED PARA EL RECUENTO DE LEVADURAS (TIRAJE) En este documento se pretende explicar de forma clara y sencilla el proceso de recuento y viabilidad de las levaduras para el
1/5 CÁMARA THOMA Y NEUBAUER IMPROVED PARA EL RECUENTO DE LEVADURAS (TIRAJE) En este documento se pretende explicar de forma clara y sencilla el proceso de recuento y viabilidad de las levaduras para el
INTRODUCCION AL CONTROL AUTOMATICO DE PROCESOS
 INTRODUCCION AL CONTROL AUTOMATICO DE PROCESOS El control automático de procesos es parte del progreso industrial desarrollado durante lo que ahora se conoce como la segunda revolución industrial. El uso
INTRODUCCION AL CONTROL AUTOMATICO DE PROCESOS El control automático de procesos es parte del progreso industrial desarrollado durante lo que ahora se conoce como la segunda revolución industrial. El uso
_ Antología de Física I. Unidad II Vectores. Elaboró: Ing. Víctor H. Alcalá-Octaviano
 24 Unidad II Vectores 2.1 Magnitudes escalares y vectoriales Unidad II. VECTORES Para muchas magnitudes físicas basta con indicar su valor para que estén perfectamente definidas y estas son las denominadas
24 Unidad II Vectores 2.1 Magnitudes escalares y vectoriales Unidad II. VECTORES Para muchas magnitudes físicas basta con indicar su valor para que estén perfectamente definidas y estas son las denominadas
C V C. Instrucciones de uso de Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02. Revisión 2. Julio de 2014
 DOT142v1 Instructions for Use Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Página 1 de 7 Instrucciones de uso de Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Revisión 2 Julio de
DOT142v1 Instructions for Use Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Página 1 de 7 Instrucciones de uso de Biofortuna SSPGo TM HLA No Template Control Kit BF-40-02 Revisión 2 Julio de
APÉNDICE. Apéndice 1. Espectrofotómetro. (Users Manual 2100 Series Spectrophotometer) 68
 APÉNDICE Apéndice 1. Espectrofotómetro (Users Manual 2100 Series Spectrophotometer) 68 El espectrofotómetro de la marca UNICO serie 2100 UV posee un rango de longitud de onda de 200-1000 nm. La técnica
APÉNDICE Apéndice 1. Espectrofotómetro (Users Manual 2100 Series Spectrophotometer) 68 El espectrofotómetro de la marca UNICO serie 2100 UV posee un rango de longitud de onda de 200-1000 nm. La técnica
DEPURACIÓN ALMAZARAS TREICO MEDIOAMBIENTE, S.L.
 DEPURACIÓN ALMAZARAS TREICO MEDIOAMBIENTE, S.L. 1 OBJETIVO Nuestro objetivo es la depuración del agua procedente de las almazaras. Somos capaces de obtener un grado de depuración que permita su posterior
DEPURACIÓN ALMAZARAS TREICO MEDIOAMBIENTE, S.L. 1 OBJETIVO Nuestro objetivo es la depuración del agua procedente de las almazaras. Somos capaces de obtener un grado de depuración que permita su posterior
TEMA 3: EN QUÉ CONSISTE?
 Módulo 7 Sesión 3 5/16 TEMA 3: EN QUÉ CONSISTE? La metodología seguida para aplicar correctamente la técnica de RGT se basa en cuatro fases (Figura 1). En la primera de ellas, se seleccionan los elementos
Módulo 7 Sesión 3 5/16 TEMA 3: EN QUÉ CONSISTE? La metodología seguida para aplicar correctamente la técnica de RGT se basa en cuatro fases (Figura 1). En la primera de ellas, se seleccionan los elementos
LA ESTRATEGIA NACIONAL DE BOSQUES Y CAMBIO CLIMÁTICO
 LA ESTRATEGIA NACIONAL DE BOSQUES Y CAMBIO CLIMÁTICO LA ESTRATEGIA NACIONAL DE BOSQUES Y CAMBIO CLIMÁTICO En palabras simples, el Cambio Climático es la modificación del clima que actualmente ocurre en
LA ESTRATEGIA NACIONAL DE BOSQUES Y CAMBIO CLIMÁTICO LA ESTRATEGIA NACIONAL DE BOSQUES Y CAMBIO CLIMÁTICO En palabras simples, el Cambio Climático es la modificación del clima que actualmente ocurre en
ScanGel NEUTRAL 86429 48 Tarjetas 86430 1080 Tarjetas
 ScanGel NEUTRAL 86429 48 Tarjetas 86430 1080 Tarjetas GEL NEUTRO Grupo sérico, screening de Ac irregulares, pruebas cruzadas IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad
ScanGel NEUTRAL 86429 48 Tarjetas 86430 1080 Tarjetas GEL NEUTRO Grupo sérico, screening de Ac irregulares, pruebas cruzadas IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad
Actividad de Biología: Cromatografía de Pigmentos Vegetales Guía del Estudiante
 Actividad de Biología: Cromatografía de Pigmentos Vegetales Guía del Estudiante Objetivos: Los estudiantes serán capaces de Explicar cuáles moléculas hacen que muchas de las plantas tengan hojas verdes
Actividad de Biología: Cromatografía de Pigmentos Vegetales Guía del Estudiante Objetivos: Los estudiantes serán capaces de Explicar cuáles moléculas hacen que muchas de las plantas tengan hojas verdes
Asistente Liberador de Espacio. Manual de Usuario
 1 Manual de Usuario 2 Introducción...3 Qué es el?...3 Propósito de la aplicación...3 Precauciones y recomendaciones al momento de usar el Asistente...3 Cuándo se abre o cierra el Asistente?...4 Conceptos
1 Manual de Usuario 2 Introducción...3 Qué es el?...3 Propósito de la aplicación...3 Precauciones y recomendaciones al momento de usar el Asistente...3 Cuándo se abre o cierra el Asistente?...4 Conceptos
Mezclado y Combinado. Molienda y Pulverizado. Tejido Homogeneización Lisis de la Célula. Agitación Vertical Única
 Mezclado y Combinado Molienda y Pulverizado Tejido Homogeneización Lisis de la Célula Agitación Vertical Única Manipulación de Múltiples muestras desde 96 pocillos hasta tubos para centrífuga de 50 ml
Mezclado y Combinado Molienda y Pulverizado Tejido Homogeneización Lisis de la Célula Agitación Vertical Única Manipulación de Múltiples muestras desde 96 pocillos hasta tubos para centrífuga de 50 ml
ANÁLISIS DE AGUAS: Metodología
 FTTM06 Rev-2,21/11/2013 INSTITUTO DE TOXICOLOGÍA DE LA DEFENSA Hospital Central de la Defensa. Glorieta del Ejército s/n. 28047 MADRID. Tel.: 914222625. Fax: 914222624 E- mail : toxicologia@oc.mde.es Web
FTTM06 Rev-2,21/11/2013 INSTITUTO DE TOXICOLOGÍA DE LA DEFENSA Hospital Central de la Defensa. Glorieta del Ejército s/n. 28047 MADRID. Tel.: 914222625. Fax: 914222624 E- mail : toxicologia@oc.mde.es Web
Conservación de los vinos y control de su evolución. espacio para anotaciones
 4. CLARIFICACIÓN Y FILTRACIÓN DE LOS VINOS La limpidez es una de las características más importantes que el consumidor exige de un vino. No es suficiente que un vino sea bueno, si éste está turbio o contiene
4. CLARIFICACIÓN Y FILTRACIÓN DE LOS VINOS La limpidez es una de las características más importantes que el consumidor exige de un vino. No es suficiente que un vino sea bueno, si éste está turbio o contiene
Identificación varietal en vid por técnicas de Biología Molecular. Lic. Luciana Garcia Lic. Carolina Chiconofri
 Identificación varietal en vid por técnicas de Biología Molecular. Lic. Luciana Garcia Lic. Carolina Chiconofri OBJETIVO Desarrollar un banco de datos a partir de plantas de origen indudable y del uso
Identificación varietal en vid por técnicas de Biología Molecular. Lic. Luciana Garcia Lic. Carolina Chiconofri OBJETIVO Desarrollar un banco de datos a partir de plantas de origen indudable y del uso
FRAGMENTO OLIGO 5-3 Hebra SECUENCIA 5' - - > 3' TAMAÑO (pb) F1. hmtl 569 L AACCAAACCCCAAAGACACC hmth2982 H CTGATCCAACATCGAGGTCG
 ANEXO 1 Protocolo para la PCR para la amplificación del mtdna en 10 fragmentos solapantes: Se prepara la siguiente mezcla: Tampón ( TRIS 100 mm, MgCl 2 12 mm, KCl 500 mm, ph 8,3): 10X dntps : 10 mm (cada
ANEXO 1 Protocolo para la PCR para la amplificación del mtdna en 10 fragmentos solapantes: Se prepara la siguiente mezcla: Tampón ( TRIS 100 mm, MgCl 2 12 mm, KCl 500 mm, ph 8,3): 10X dntps : 10 mm (cada
Diseño y desarrollo de una aplicación informática para la gestión de laboratorios
 Diseño y desarrollo de una aplicación informática para la gestión de laboratorios M. Francisco, P. Vega, F. J. Blanco Departamento de Informática y Automática. Facultad de Ciencias. Universidad de Salamanca
Diseño y desarrollo de una aplicación informática para la gestión de laboratorios M. Francisco, P. Vega, F. J. Blanco Departamento de Informática y Automática. Facultad de Ciencias. Universidad de Salamanca
IMPORTANTE INSTRUCCIONES GENERALES PARA LA PREPARACIÓN DEL PACIENTE
 IMPORTANTE Para cualquier ESTUDIO GENÉTICO (EXCEPTO PRUEBA DEL TALÓN ) es imprescindible: La solicitud debe ir acompañada de la hoja de petición, con datos del paciente y motivos de estudio (resumen de
IMPORTANTE Para cualquier ESTUDIO GENÉTICO (EXCEPTO PRUEBA DEL TALÓN ) es imprescindible: La solicitud debe ir acompañada de la hoja de petición, con datos del paciente y motivos de estudio (resumen de
UNIDAD DE TRABAJO Nº2. INSTALACIONES DE MEGAFONÍA. UNIDAD DE TRABAJO Nº2.1. Descripción de Componentes. Simbología AURICULARES
 UNIDAD DE TRABAJO Nº2. INSTALACIONES DE MEGAFONÍA UNIDAD DE TRABAJO Nº2.1. Descripción de Componentes. Simbología 2. Auriculares. Descripción. AURICULARES Son transductores electroacústicos que, al igual
UNIDAD DE TRABAJO Nº2. INSTALACIONES DE MEGAFONÍA UNIDAD DE TRABAJO Nº2.1. Descripción de Componentes. Simbología 2. Auriculares. Descripción. AURICULARES Son transductores electroacústicos que, al igual
Introducción. Ciclo de vida de los Sistemas de Información. Diseño Conceptual
 Introducción Algunas de las personas que trabajan con SGBD relacionales parecen preguntarse porqué deberían preocuparse del diseño de las bases de datos que utilizan. Después de todo, la mayoría de los
Introducción Algunas de las personas que trabajan con SGBD relacionales parecen preguntarse porqué deberían preocuparse del diseño de las bases de datos que utilizan. Después de todo, la mayoría de los
EL MATERIAL GENÉTICO:
 LA HUELLA GENÉTICA: PRUEBAS DE PATERNIDAD E IDENTIFICACIÓN INTRODUCCIÓN: En éstos últimos años, se ha popularizado a través de los medios de comunicación la expresión: identificación través de pruebas
LA HUELLA GENÉTICA: PRUEBAS DE PATERNIDAD E IDENTIFICACIÓN INTRODUCCIÓN: En éstos últimos años, se ha popularizado a través de los medios de comunicación la expresión: identificación través de pruebas
El valor energético de los alimentos
 El valor energético de los alimentos http://www2.uned.es/pea-nutricion-y-dietetica- I/guia/guia_nutricion/el_valor_energetico.htm?ca=n0 El valor energético o valor calórico de un alimento es proporcional
El valor energético de los alimentos http://www2.uned.es/pea-nutricion-y-dietetica- I/guia/guia_nutricion/el_valor_energetico.htm?ca=n0 El valor energético o valor calórico de un alimento es proporcional
PROCEDIMIENTOS DE ENTREGA
 PROCEDIMIENTOS DE ENTREGA Prefabricados OJEFER dispone de tres modalidades o procedimientos de entrega: 1. Recogida directa por parte de cliente en las instalaciones de Prefabricados OJEFER S.L. En esta
PROCEDIMIENTOS DE ENTREGA Prefabricados OJEFER dispone de tres modalidades o procedimientos de entrega: 1. Recogida directa por parte de cliente en las instalaciones de Prefabricados OJEFER S.L. En esta
Qué requisitos deben cumplir los albaranes o notas de entrega?
 Qué requisitos deben cumplir los albaranes o notas de entrega? Los albaranes o notas de entrega, pese a su frecuente uso práctico, suelen ser documentos bastante desconocidos por parte de la mayoría de
Qué requisitos deben cumplir los albaranes o notas de entrega? Los albaranes o notas de entrega, pese a su frecuente uso práctico, suelen ser documentos bastante desconocidos por parte de la mayoría de
Técnicas moleculares.
 Técnicas moleculares. DMTV Carolina Acevedo Curso de Microbiología 2015 SÍNTESIS IN VITRO DE UNA GRAN CANTIDAD DE COPIAS DE UN SEGMENTO DE ADN EXISTENTE EN UNA MUESTRA. O sea. Amplificamos en forma exponencial
Técnicas moleculares. DMTV Carolina Acevedo Curso de Microbiología 2015 SÍNTESIS IN VITRO DE UNA GRAN CANTIDAD DE COPIAS DE UN SEGMENTO DE ADN EXISTENTE EN UNA MUESTRA. O sea. Amplificamos en forma exponencial
NycoCard CRP Single Test
 NycoCard CRP Single Test ES DESCRIPCION DEL PRODUCTO Aplicaciones NycoCard CRP Single Test es un test de diagnóstico in vitro para medir de una forma rápida la proteína C reactiva (CRP) en la sangre humana.
NycoCard CRP Single Test ES DESCRIPCION DEL PRODUCTO Aplicaciones NycoCard CRP Single Test es un test de diagnóstico in vitro para medir de una forma rápida la proteína C reactiva (CRP) en la sangre humana.
UNIDAD 6.- NEUMÁTICA.
 UNIDAD 6.- NEUMÁTICA. 1.-ELEMENTOS DE UN CIRCUITO NEUMÁTICO. El aire comprimido se puede utilizar de dos maneras distintas: Como elemento de mando y control: permitiendo que se abran o cierren determinadas
UNIDAD 6.- NEUMÁTICA. 1.-ELEMENTOS DE UN CIRCUITO NEUMÁTICO. El aire comprimido se puede utilizar de dos maneras distintas: Como elemento de mando y control: permitiendo que se abran o cierren determinadas
GUIA DE LABORATORIO PRACTICA 8 EXTRACCIÓN ADN PROGRAMA DE ENFERMERIA CURSO INTEGRADO DE PROCESOS BIOLOGICOS
 GUIA DE LABORATORIO PRACTICA 8 EXTRACCIÓN ADN PROGRAMA DE ENFERMERIA CURSO INTEGRADO DE PROCESOS BIOLOGICOS Leidy Diana Ardila Leal Docente. INTRODUCCIÓN En esta práctica se va a realizar la extracción
GUIA DE LABORATORIO PRACTICA 8 EXTRACCIÓN ADN PROGRAMA DE ENFERMERIA CURSO INTEGRADO DE PROCESOS BIOLOGICOS Leidy Diana Ardila Leal Docente. INTRODUCCIÓN En esta práctica se va a realizar la extracción
INTERCAMBIADORES DE CALOR. Mg. Amancio R. Rojas Flores
 INTERCAMBIADORES DE CALOR Mg. Amancio R. Rojas Flores INTRODUCCIÓN Los intercambiadores de calor son aparatos que facilitan el intercambio de calor entre dos fluidos que se encuentran a temperaturas diferentes
INTERCAMBIADORES DE CALOR Mg. Amancio R. Rojas Flores INTRODUCCIÓN Los intercambiadores de calor son aparatos que facilitan el intercambio de calor entre dos fluidos que se encuentran a temperaturas diferentes
