Evaluación de la respuesta inmune humoral por western blot en ratones inmunizados con una biblioteca genómica de expresión de Trypanosoma cruzi
|
|
|
- Paula García Cáceres
- hace 8 años
- Vistas:
Transcripción
1 170 REV CUBANA MED TROP 2001;53(3):170-9 INSTITUTO DE MEDICINA TROPICAL PEDRO KOURI Evaluación de la respuesta inmune humoral por western blot en ratones inmunizados con una biblioteca genómica de expresión de Trypanosoma cruzi Dr. Esteban Alberti Amador, 1 Lic. Ana M. Montalvo Álvarez, 2 Dra. Aniran Ruiz Espinosa, 3 Lic. Rocío García Miniet, 4 Lic. Máximo B. Martínez Benítez, 5 Dra. María E. Sarmiento García 6 y Dr. Armando Acosta Domínguez 7 RESUMEN Se construyó una biblioteca genómica de expresión de Trypanosoma cruzi con la utilización como vector el plásmido pcdna3, con la cual se inmunizaron ratones de la línea isogénica BALB/c por vía intramuscular. Se empleó un grupo control positivo al que se le administraron antígenos solubles de T. cruzi y otro grupo que recibió el plásmido utilizado para la construcción de la biblioteca genómica; un grupo no recibió inmunización. A todos los animales se les extrajo sangre del plexo retrorbital 2 semanas posteriores a la tercera inmunización, para estudiar la respuesta de anticuerpos específicos contra los antígenos solubles del parásito mediante la técnica de western blot. Se obtuvo una respuesta de anticuerpos en los animales inmunizados con la biblioteca genómica de expresión y con antígenos solubles del parásito. DeCS: BIBLIOTECA GENOMICA; RATONES CONSANGUINEOS BALB C/inmunología; ANIMALES DE LABORATORIO; WESTERN BLOTTING/métodos; ANTIGENOS DE PROTOZOARIOS/inmunología; TRYPANOSOMA CRUZI/inmunología; FORMACION DE ANTICUERPOS; VACUNAS DE ADN. La inmunización con ADN es una tecnología surgida a principios de los años 90, que consiste en introducir, mediante inyección, moléculas de ADN, generalmente plasmídico, que contienen genes de algún patógeno específico y que al ser expresados en el tejido donde fue inoculado inducen una respuesta inmune, que en ocasiones puede conducir a la protección contra la enfermedad (Chinchuteck K. Safety and regulatory aspects of nucleic acid vaccination En: Symposium New trends in molecular Biotechnology: basic and applied aspects. Louvain-La-Nueve. September, 1995). 1,2 Esta tecnología promete candidatos vacunales de fácil manipulación y bajo costo de producción, que combinen las ventajas de las vacunas de subunidades y la eficacia de las vacunas de vectores vivos. 3,4 Todo esto permitiría la prevención de enfermedades virales y parasitarias sin correr los riesgos de las vacunas vivas, ya sea la reversión a la virulencia o el posible desencadenamiento de infecciones mortales en huéspedes inmunodeprimidos, por citar algunos. 5,6 El desarrollo de vacunas profilácticas y terapéuticas frente a parásitos, entre ellos 1 Especialista de II Grado en Microbiología. Investigador Auxiliar. Instituto de Medicina Tropical Pedro Kourí (IPK). 2 Licenciada en Biología. Investigadora Agregada. IPK. 3 Máster en Parasitología. Especialista de I Grado en Parasitología. IPK. 4 Licenciada en Bioquímica. Profesora Instructora. Universidad de Granma. 5 Licenciado en Radioquímica. Aspirante a Investigador. IPK. 6 Especialista de II Grado en Fisiología y Patología. Investigador Titular. Instituto Finlay. 7 Especialista de II Grado en Inmunología. Investigador Titular. Instituto Finlay.
2 Tripanosoma cruzi, continúa siendo un reto para los investigadores de todo el mundo. El desarrollo de candidatos vacunales contra este, a través de la caracterización de genes que codifican antígenos que estimulan inmunidad protectora, y su transferencia a vectores establecidos no ha sido posible, pues la caracterización de genes que codifican proteínas con capacidad inmunoprotectora es una tarea aún en desarrollo. 7,8 Con el objetivo de desarrollar esta novedosa estrategia y profundizar en el estudio de los mecanismos inmunológicos estimulados por este tipo de vacunas, los autores de este trabajo se propusieron construir una biblioteca genómica de T. cruzi en un vector de expresión en células eucariotas y evaluar por el método de western blot la respuesta humoral específica inducida en ratones de la línea isogénica BALB/c, inmunizados por vía intramuscular con esta construcción genética. MÉTODOS CEPAS PARASITARIAS Se utilizaron epimastigotes de la cepa Y (CT-10C 106) de T. cruzi donada gentilmente por la doctora María Auxiliadora de Sousa, Instituto Osvaldo Cruz, Río de Janeiro, Brasil. CEPAS BACTERIANAS Escherichia coli (E. coli) XL-1 blue: F : Tn10 proa + B + lacl 8 ^ (lacz) M15/ reca1 end A1 gyra96 (Nal ) thi hsd r17 (r k- m k- ) supe44 rela1 lac (stratagene). PLÁSMIDO Se empleó el vector comercial pcdna3 (vector de expresión en células superiores, suministrado por la firma Invitrogen, EE.UU.). ANIMALES Se emplearon un total de 20 ratones machos, de la línea isogénica BALB/c con un peso entre 16 y 18 g y 6 semanas de edad, suministrados por el Centro Nacional de Producción de Animales de Laboratorio (CENPALAB, Cuba). 171 ENZIMAS DE RESTRICCIÓN Y MODIFICACIÓN Se emplearon las enzimas de restricción Sau3A, Bam HI y Eco RV así como las enzimas T4 ligasa y la fosfatasa alcalina y el patrón de peso molecular (PPM) IV, todos suministrados por la firma Boehringer Mannheim Biochemica (RFA), y utilizados según las instrucciónes del fabricante. PREPARACIÓN DE CÉLULAS COMPETENTES Se inoculó una colonia de E. coli XL-1 blue en un precultivo de 5 ml de medio Luria Bertaini con tetraciclina (Lb T ) (medio Luria-Bertaini: triptona 10 g/l, NaCl 5 g/l, extracto de levadura 5 g/l) ph 7,5 y se incubaron a 37 C con agitación (incubator shaker, Co, EE.UU.) a 200 rpm. A partir del precultivo crecido se sembró 1 µl/ml en un erlenmeyer con 200 ml de medio LB T y se incubó a 37 C con agitación hasta que alcanzó una densidad óptica de 0,6 a 660 nm en un espectrofotómetro (Ultrospec III Pharmacia LKB). El cultivo crecido se dejó reposar en baño de agua helada durante 30 min y se centrifugó a 600 g por 30 min a 4 C en una centrífuga refrigerada (MLW K23D VEB MLW MEDIZINTECHNIK, Alemania). El precipitado celular fue lavado 2 veces con agua destilada estéril fría (4 C) y 2 con glicerol 10 % (Pharmacia). Todas las centrifugaciones se realizaron con iguales condiciones. Finalmente el precipitado celular se resuspendió en la solución de glicerol 10 % y se distribuyó en alícuotas de 80 µl que fueron almacenadas a -70 C hasta el momento de realizar la transformación genética. PURIFICACIÓN DE ADN PLASMÍDICO POR EL MÉTODO DE LISIS ALCALINA La técnica se realizó según Maniatis 9 con algunas modificaciones. Cada clon de E. coli escogido fue inoculado en un precultivo de LB suplementado con los antibióticos de selección escogidos y se dejó crecer a 37 C, con agitación durante 16 h, luego se centrifugó a rpm a 4 C por 10 min. A continuación el botón celular se resuspendió en 1 ml de tris-edta (TE) (tris 10 mmol, EDTA 1 mmol, ph 8) ph 8; frío y se centrifugó a rpm durante 5 min, se eliminó el sobrenadante con micropipetas y se resuspendió
3 172 el pellet en 100 µl de Liso I (tris 25 mmol, EDTA 10 mmol, glucosa 50 mmol, ph 8) frío. Se colocaron los viales 5 min en hielo y se añadieron 200 µl de Liso II (NaOH 0,2 mmol, SDS 1 %) recién preparado, posteriormente se añadieron 150 µl de KAc 5/3 (acetato de potasio 5 mmol, ácido acético 3 mmol) se dejó reposar en hielo durante 5 min y se centrifugó 10 min a rpm. El sobrenadante se depositó en otro tubo y se añadieron 450 µl de fenol-cloroformo (v:v), se agitó y centrifugó 10 min a rpm. La fase acuosa se depositó en viales nuevos y se adicionaron 800 µl de etanol absoluto frío y se dejó precipitar 1 h a -20 C. A continuación se centrifugó 15 min a rpm, se lavó el botón celular con 900 µl de etanol 70 % y se centrifugó. Por último los tubos se secaron al vacío (DNA Mini. Hote. Denmark) durante 3 min. Se resuspendió el precipitado en 20 µl de tampón TE estéril y se guardó a -20 C. Los resultados fueron evaluados mediante electroforesis en gel de agarosa 0,8 %. PURIFICACIÓN DE ADN GENÓMICO DE T. CRUZI El ADN genómico de T. cruzi fue obtenido de las formas epimastigóticas del parásito según el método de Hookey. 10 El cultivo inactivado con formaldehído tamponado 0,5 % se centrifugó a rpm y 4 C durante 20 min. Se resuspendió en 1 ml de TE para luego centrifugarlo 15 min a rpm y 4 C. Se tomaron 10 9 epimastigotes que fueron resuspendidos en tampón lisis e incubados 2 h a 56 C. Seguidamente se procedió a realizar varias extracciones del ADN con fenolcloroformo (v:v) hasta que la interfase se hizo imperceptible. Se precipitó con un décimo del volumen de acetato de sodio y 2 volúmenes de etanol absoluto. El sedimento obtenido fue resuspendido en tampón TE estéril que se dejó toda la noche para que se despegara. La integridad del ADN obtenido fue chequeada por electroforesis en gel de agarosa 0,8 %. ELECTROFORESIS EN GEL DE AGAROSA Se llevó a cabo según el protocolo propuesto por Maniatis. 9 Los geles de agarosa se prepararon a 0,8 % con la utilización de agarosa N.A (Pharmacia) y tampón de corrida tris-borato-edta (TBE) (tris base 0,004 mol, ácido bórico 0,01 mol EDTA 0,5 mol ph8) 0,5 x adicionándole bromuro de etidio a una concentración final de 5 µl/100 ml. DETERMINACIÓN DE LA CONCENTRACIÓN DE ADN La concentración de ADN se determinó espectrofotométricamente según lo recomendado por Maniatis 9 con un cuantificador automático de ADN y ARN, gene quant (Pharmacia Biotech England). DIGESTIONES ANALÍTICAS En todas las digestiones las enzimas de restricción se utilizaron a una concentración de 1 U/µg de ADN, los tampones empleados fueron los recomendados por Boehringer Mannheim Biochemica para la máxima actividad enzimática y la concentración del ADN fue de ng/µl en volúmenes finales de 20 µl. Las mezclas de reacción fueron incubadas en baño térmico durante 1 h a 37 C. DIGESTIONES PREPARATIVAS Las digestiones preparativas se realizaron en las mismas condiciones que las analíticas pero con sus componentes en mayor cantidad. Se digirieron 10 µg de ADN genómico de T. cruzi con la enzima Sau3A, se obtuvieron fragmentos de aproximadamente 5-1, 8 pb, y fue comprobado por electroforesis en gel de agarosa 0,8 % con la utilización del patrón de peso molecular (PPM) IV. Se digirieron 10 µg del vector con la enzima BamH I y fue comprobado de la misma manera. Fueron resuspendidos en un volumen final de 30 y 40 µl el vector y el ADN respectivamente. DESFOSFORILACIÓN DE LOS EXTREMOS 5' DEL VECTOR La reacción de desfosforilación se llevó a cabo en un volumen final de 100 µl. Se empleó 1 U de enzima fosfatasa alcalina, por cada 50 pmol de extremos a desfosforilar del plásmido pcdna3. La mezcla de la reacción se incubó a 37 C durante 1 h.
4 REACCIÓN DE LIGAZÓN Se tomaron 1,5 µg de framentos de ADN genómico de T. cruzi y 800 ng del plásmido pcdna3 que había sido previamente desfosforilado. Los fragmentos a ligar en cada caso fueron colocados en tubos de microcentrífuga con una relación vector-inserto de 1:3. Las reacciones de ligazón fueron realizadas con el empleo de 1 U de T4 DNA ligasa en 10 µl de volumen final a temperatura de 14 C durante 16 h. Por último, la ligasa fue inactivada en un baño a 65 C durante 10 min. ELECTROPORACIÓN A las cubetas de electroporación, enfriadas previamente, se les añadieron 80 µl de células más 20 ng del plásmido o la ligazón. Posterior a este paso se le dio el golpe eléctrico con los parámetros reportados para E. coli (2 500 V; 21 µf y 400 Ω (Recomended Procariotic Protocol. IBI gene Zarpper 450/2500 Electroporation System Cat No. 9100). Se adicionó entonces 1 ml de LB y se dejó crecer durante 1 h a 37 C; a 80 rpm y de esta mezcla se sembró en medio sólido y líquido suplementado con los antibióticos de selección. PORCENTAJE DE RECOMBINANTES Para la determinación del porcentaje de recombinantes presentes en la librería se sembraron en una placa 20 µl de la transformación y se seleccionaron al azar 10 colonias, de las cuales se purificó el ADN plasmídico que fue sometido a análisis de restricción con la enzima EcoRV. El porcentaje de recombinantes se calculó de la forma siguiente: Porcentaje de Número de clones recombinantes x 100 recombinantes = Número de colonias ensayadas PURIFICACIÓN MASIVA DE ADN PLASMÍDICO Para llevar a cabo la purificación de la biblioteca genómica se sembró todo el producto de la transformación genética de E. coli en 500 ml del medio LB con el antibiótico de selección 173 (ampicillina) y se dejó crecer a 37 C, durante 16 h. Posteriormente se centrifugó a rpm durante 10 min, a 4 EC y el sedimento se resuspendió en 10 ml de tampón lisis (tris HCL 100 mmol, ph-8, EDTA 100 mmol, SDS 2 %, NaCL 150 mmol y proteinasa K 200 µg/ml) y se dejó reposar 10 min a temperatura ambiente. Luego se adicionaron 20 ml de Liso II, y se incubó en hielo durante 10 min. A continuación se adicionaron 18,7 µl de solución de KAc, ph 4,8, se mezcló cuidadosamente y se matuvo 20 min en hielo. Se centrifugó durante 15 min a rpm a 4 C. A continuación se añadió 0,6 volúmenes de isopropanol y se dejó reposar 10 min a temperatura ambiente. Se centrifugó 10 min a rpm y las células se resuspendieron en 500 µl de tampón TE, se adicionaron 3 µl de RNAasa (10 µg/µl) y se incubó durante 30 min a 37 C. A continuación se añadió igual volumen de fenolcloroformo (v:v) que se mezlcó con ayuda de vortex, se centrifugó nuevamente a rpm durante 10 min. Este paso se repitió 2 veces, se tomó en cada uno la fase acuosa y se desechó el resto. Después se realizó un lavado con cloroformo isoamílico 24:1 y al botón celular obtenido después de la centrifugación, se le agregó etanol absoluto, se mezcló e incubó a -20 C por 1 h. Por último se centrifugó a rpm durante 15 min y se desechó el sobrenadante. El botón de ADN se lavó con etanol 70 %, se centrifugó en iguales condiciones y el sedimento se secó al vacío durante 5 min y se resuspendió en 1 ml de agua destilada. Se realizó la lectura a 260 y 280 nm de una dilución adecuada del ADN, obtenido en un espectrofotómetro para calcular la concentración y el grado de pureza de este. OBTENCIÓN DEL SONICADO DE TRYPANOSOMA CRUZI Los epimastigotes de la cepa Y (CI-IOC 106) a una concentración de 10 9 fueron mantenidos en medio de cultivo de infusión de hígado-triptosa suplementado con 10 % de suero fetal de ternera (Gibco) y 50 µg/ml de gentamicina, durante 7 d. 11 Seguidamente estas células fueron cosechadas por centrifugación y lavadas 4 veces con solución salina tamponada con fosfato (SSTF) (NaCl 8 g/l, KCl
5 174 0,2 g/l, Na 2 HPO 4 1,15 g/l, KH 2 PO 4 0,24 g/l, ph 7,2) a 400 g durante 10 min a 4 C. Después el botón celular obtenido fue resuspendido en 5 ml de SSTF y sonicado con una intensidad de 18 Hz (Soniprep 120, England) por 3 veces durante 60 s con intervalos de reposo de 60 s en hielo. Por último, el homogenizado fue centrifugado a g durante 1 h a 4 C y el sobrenadante fue distribuido en viales y conservado a - 70 C. Más tarde se determinó la concentración de proteínas por el método de Lowry. 12 ESQUEMA DE INMUNIZACIÓN Los animales se dividieron en 4 grupos distribuidos de la forma siguiente: L: Grupo inmunizado con la biblioteca genómica de T. cruzi (n = 5). T: Grupo inmunizado con antígenos solubles de T. cruzi (n = 5). P: Grupo inmunizado con el plásmido pcdna3 (n = 5). C: Grupo no inmunizado (n = 5). DOSIS Y VÍA DE ADMINISTRACIÓN Se administraron 50 µg de inóculo en cada caso en 0,1 ml de solución salina 0,9 % por vía intramuscular en la región anterior de la pata trasera derecha, con excepción del grupo C que no recibió inmunización. REINMUNIZACIONES Se realizaron 2 reinmunizaciones cada 2 semanas con la misma dosis y vía de administración. WESTERN BLOT El sonicado de T. cruzi fue sometido a electroforesis (SDS-PAGE) 13 en una cámara electroforética Bio Rad, (EE.UU.) acoplada a una fuente Multidrive, Pharmacia, (Suecia). Para esto se prepararon las muestras en condiciones reductoras con 2-mercaptoetanol y se calentaron en baño de agua a 100 C durante 5 min. Las proteínas contenidas en el sonicado de T. cruzi fueron separadas electroforéticamente de acuerdo con sus respectivos pesos moleculares; para esto se empleó un gel 12,5 % de acrilamida, y se realizó la electroforesis a un voltaje constante de 120 V. El patrón de peso molecular empleado en la electroforesis fue el juego de marcadores cuyo rango de peso molecular es de kd, (Sigma, EE.UU.) y que fue sometido a las mismas condiciones de las muestras. Una vez concluida la electroforesis se procedió a hacer la electrotransferencia a una membrana de nitrocelulosa, con la utilización para esto de un equipo de transferencia húmedo (Bio Rad, EE.UU.) y tampón tris (25 mmol)-glicina (125 mmol) ph 8,2, que contenía 20 % de metanol. La electrotransferencia se realizó con la aplicación de una corriente de 300 ma durante 1 h. La membrana de nitrocelulosa fue bloqueada con leche descremada 2 % en PBS durante 1 h a temperatura ambiente con agitación suave en zaranda Janke & Kumkel IKA-Labortechnik, RFA. Se cortaron las tiras correspondientes a cada uno de los puntos de aplicación, con el objetivo de incubar por separado cada una de las muestras de suero de los 4 grupos contemplados en el esquema de inmunización. Las muestras de suero se diluyeron 1/100 en leche descremada 1 %, se incubaron 2 h a temperatura ambiente con agitación suave. Seguidamente se realizaron 3 lavados con PBS y se incubó 1 h con un conjugado de inmunoglobulinas de conejo anti IgG de ratón marcado con peroxidasa (sigma) a una dilución de 1/ 2000, luego se realizaron otros 3 lavados con PBS y se reveló con peróxido de hidrógeno como sustrato y 4-cloro-1-naftol (sigma) como elemento cromógeno. Transcurridos 15 min la reacción se detuvo y se lavaron las tiras de nitrocelulosa con agua destilada. RESULTADOS Como resultado de la purificación del ADN genómico de T. cruzi se obtuvieron 40 µl a una concentración de 1 µg/µl. En la figura 1 (B,C) se muestran los resultados de las digestiones analíticas realizadas con la enzima Sau3A, y los patrones de bandas que se obtuvieron a diferentes tiempos (5, 10, 15, 20, 25 y 30 min, respectivamente). Las
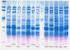
6 tallas de los fragmentos obtenidos se encontraban en un rango de 5-1,8 kb. En corridas electroforéticas anteriores se pudo observar la integridad del genoma sin digerir, lo que indicó la ausencia total de nucleasas inespecíficas en la preparación. Kb 19,3 7,7 5,5 4,2 3,14 2,16 2,3 1,8 1,4 A B C D E F G Línea A: patrón de peso molecular; B, C, D, E, F y G: tiempos de incubación con la enzima a 3, 7, 15 y 21 min respectivamente. Fig. 1. Electroforesis en gel de agarosa 0,8 %. Ensayo de restricción del ADN genómico de Trypanosoma cruzi. Se empleó la enzima Sau3A a diferentes tiempos de incubación y a 37 C. La figura 2 muestra la purificación del plásmido pcdna3 del cual se obtuvieron 200 µl a una concentración final de 14,58 µg/µl, analizado en una electroforesis en gel de agarosa 0,8 %. Se pueden detallar las configuraciones correspondientes al plásmido nativo con predominio de la forma superenrollada y ausencia de ARN (línea C). Una muestra de las digestiones realizadas con la enzima Bam H1 durante la preparación de los vectores para la construcción de la biblioteca puede ser observada también (línea B), el vector linealizado (5,446 kb) que ha migrado 175 muy cerca del patrón de peso molecular empleado. A continuación (línea A) puede observarse el resultado de la desfosforilación con la enzima fosfatasa alcalina, encargada de impedir la recirculación de los plásmidos al eliminar sus grupos fosfatos de los extremos 5'. A pesar de la cantidad de ADN digerido aplicado, no se observan signos de degradación ni bandas por encima del vector, lo que indica una digestión total. En la figura 3 se observa el resultado obtenido del análisis de restricción realizado con la enzima Eco RV, a 10 de los plásmidos purificados de los transformantes obtenidos después de la obtención de la biblioteca. Como resultado de este experimento se observaron 8 clones con insertos de ADN de T. cruzi entre los 10 clones seleccionados (80 %), líneas 4, 8, 10, 12, 14, 16, 18 y 20. Todos los clones recombinantes analizados en este caso muestran bandas con tallas mayores y menores que el vector digerido (línea 2) utilizado como control. El resto de las digestiones se mantienen en el nivel del vector y parecen corresponder con vectores no recombinantes (línea 6). En relación con los resultados obtenidos en la evaluación de la respuesta inmune humoral frente a antígenos solubles de T. cruzi con la utilización del método de western blot, 2 semanas después de la tercera inmunización (fig. 4), se pudo observar el reconocimiento de diferentes bandas, con tallas que oscilaban en un rango aproximado entre 55 hasta 25 kda, por los animales inmunizados con la biblioteca genómica (L1, L2, L3, L4, L5). Todos los animales reconocieron una banda de casi 55 kda, algunos animales (L1 y L3) reconocieron además una banda de aproximadamente 45 kda, mientras que un animal reconoció adicionalmente una banda con talla aproximada de 25 kda (L3). Al analizar la respuesta contra antígenos solubles de T. cruzi en el suero de los animales inmunizados con el vector y en el suero de los animales no inmunizados, considerados ambos grupos como controles negativos, no se observó reactividad. Como era de esperar, los sueros de los animales inmunizados con los antígenos solubles de T. cruzi fueron reactivos y se reconoció una diversidad de bandas correspondientes a un amplio rango de pesos moleculares.
7 176 A B C D Kb 19,3 7,7 5,5 4,2 3,14 2,16 2,3 1,8 1,4 1,5 Línea A: pcdna3 desfosforilados, B: pcdna3 digerido con BamH1, C: pcdna3 nativo, D: patrón de peso molecular. Fig. 2. Electroforesis en gel de agarosa 0,8 %. Preparación del vector. Línea 1: plásmido pcdna3 íntegro; Línea 2: plásmido pcdna3 digerido con EcoRV; Líneas 4, 8, 10, 12, 14, 16, 18 y 20: plásmido con insertos ADN de Trypanosoma cruzi; Línea 6: plásmido sin inserto. Fig 3. Análisis de restricción con la enzima EcoRV de los plásmidos purificados de los transformantes obtenidos. DISCUSIÓN Obtención de la librería genómica de expresión de Trypanosoma cruzi El resultado del análisis de restricción de los recombinantes obtenidos después de la transformación genética de E. coli con la biblioteca genómica de expresión de T. cruzi, permitieron demostrar que en el inóculo que se administró había una elevada cantidad de material genético de T. cruzi. Esto se evidenció por la presencia de bandas con tallas superiores e inferiores a las del plásmido utilizado en la construcción de la biblioteca, al ser digerido con la enzima de restricción Eco RV. En trabajos anteriores, este grupo de trabajo obtuvo resultados similares con la misma metodología. 6,14 Las características del plásmido utilizado no permitieron usar uno de los métodos simples para el análisis de este aspecto. 9 lo que limitó el número de colonias analizadas; no obstante si este resultado fuera un reflejo de la proporción de recombinantes en la biblioteca, indicaría una elevada representatividad del genoma de T. cruzi en el inóculo. Esto elevaría las probabilidades de lograr una respuesta inmune específica detectable y protección, pero haría más compleja la identificación precisa de el o los genes relacionados con la protección; mientras que, una reducida representatividad limitaría las posibilidades de inducir protección aunque facilitaría encontrar los genes responsables, si esta se produjera. Por lo tanto, dentro de ciertos límites, la proporción de recombinantes en la biblioteca no constituiría, y de hecho no constituyó, uno de los elementos limitantes en esta fase del trabajo.
8 177 De izquierda a derecha: Patrón de peso molecular: PM; Línea 2: suero de ratones inmunizados con antígenos solubles de Trypanosoma cruzi (C+); Línea 3: suero de ratones no inmunizados (C-); Línea 4: sueros de ratones inmunizados con el plásmido (CP); Líneas 5-9: suero de ratones inmunizados con la biblioteca genómica de Tripanosoma cruzi (L1- L5). Fig. 4. Western blot. Reactividad de los sueros de ratones BALB/c inmunizados contra antígenos solubles de Trypanosoma cruzi. Evaluación de la respuesta inmune humoral en los ratones inmunizados con la biblioteca genómica mediante la técnica del western blot Al evaluar la respuesta inmune humoral mediante la técnica del western blot en los diferentes grupos de estudio, se pudo confirmar la reactividad de los sueros de los animales inmunizados con la biblioteca genómica. Se demostró que las respuestas encontradas en los animales inmunizados con esta construcción genética estuvieron dirigidas contra los productos de los genes de T. cruzi representados en esta y no contra productos codificados por genes presentes en el vector (fig. 4), pues en ninguna de las determinaciones realizadas se mostró respuesta en los sueros de los animales inmunizados con el vector pcdna3. Las variaciones de la respuesta observada entre distintos animales (fig. 4), e incluso en el mismo animal en diferentes momentos del esquema de inmunización (datos no mostrados), reflejan la composición diferente, en cuanto a genes de T. cruzi se refiere, en los distintos inóculos suministrados a los diferentes animales; porque si bien la dosis de ADN fue la misma, la composición de cada inóculo, en cuanto a fragmentos de ADN de T. cruzi debió ser diferente por tratarse de una biblioteca genómica y no de genes individuales bien definidos como los utilizados en otros trabajos. 15,16 No obstante, se apreció un reconocimiento preferencial de la banda de 55 kda, lo que pudiera estar en relación con una elevada inmunogenicidad de esta proteína, unido a una alta representatividad del gen correspondiente en la biblioteca genómica. Esta proteína reconocida por el suero de todos los animales, pudiera corresponder con una cisteíno proteinasa, a la cual se le ha demostrado una alta inmunogenicidad. 17 En relación con el limitado número de bandas reconocidas por el suero de los animales inmunizados con la biblioteca genómica, entre otros factores, pudiera estar influido por la no expresión de todos los antígenos, porque no todos los plásmidos recombinantes contienen fragmentos de ADN posibles a expresar, ya que para esto sería necesario la presencia de un ATG lo suficientemente cercano al promotor de citomegalovirus (CMV) presente en el vector de expresión, sin que existan secuencias que ocasionen la terminación prematura de la transcripción. Además, también es un hecho fortuito cuáles de las moléculas de ADN de las inyectadas son exitosamente transfectadas en la célula blanco, pues esto condiciona después la expresión de antígenos, los que aunque expresados, no necesariamente son inmunogénicos y en caso
9 178 de serlo, los anticuerpos reaccionantes contra estos pudieran no ser detectados por western blot porque no se evidenciarían los que reaccionan contra epitopes conformacionales. En este análisis también es necesario tener en cuenta la dosis empleada para la inmunización (50 µg), que pudiera considerarse baja si se tiene en cuenta que el inmunógeno no es homogéneo, aunque las dosis comúnmente empleadas para genes individuales oscilan en un amplio rango en dependencia de la vía y el método de inmunización empleado y la especie animal. 18 Otro factor importante a señalar es que en la preparación de antígenos solubles del parásito utilizada en el western blot, no están representados todos los antígenos del microorganismo, mientras que teóricamente en la biblioteca genómica deben estar representados todos los genes del microorganismo, por lo que un grupo de respuestas inducidas en los animales pudo no haber sido detectada. Sería interesante en trabajos futuros inmunizar distintos grupos de animales con fracciones diferentes de la biblioteca genómica, para determinar el patrón de reconocimiento antigénico tanto celular como humoral, así como llevar a cabo estudios de reto que permitan identificar de forma precisa los genes que codifican inmunógenos con una elevada capacidad protectora. La vacuna de ácidos nucleicos representa una efectiva y novedosa forma de expresión de antígenos in vivo que genera respuestas inmune humorales y celulares contra antígenos virales, bacterianos y parasitarios. 18,19 Esta tecnología promete ser una nueva herramienta en la inmunización para el control de las enfermedades. Sin embargo, no se puede afirmar que esta sea la solución para este problema; existen argumentos tanto a favor como en contra de la posible aplicación en seres humanos. 18 Hasta el momento, basta con saber, que la inmunización con ácidos nucleicos permite, de forma práctica, la búsqueda de nuevos antígenos potencialmente útiles para el desarrollo de vacunas de nueva generación. SUMMARY An expression genomic library of Trypanosoma cruzi was built by using plasmid pc DNA3 as a vector. This library served to immunize by intramuscular administration BALB/c inbred mice. A positive control group to which T.cruzi soluble antigens were administered and other group which was given the same plasmid used for the building of the genomic library were included in this study; another group was not immunized. Blood was extracted from the retrorbital plexus of all the mice two weeks after the third vaccination so as to study the specific antibody response to soluble parasite anigens through the Western Blot technique. The antibody response was shown in animals immunized with the expression genomic library and with soluble parasite antigens. Subject headings: GENOMIC LIBRARY; MICE, INBRED BALB C/immunology; ANIMALS, LABORATORY, WESTERN BLOTTING/methods; ANTIGENS, PROTOZOAN; TRYPANOSOMA CRUZI/immunology; ANTIBODY FORMATION; VACCINES, DNA. REFERENCIAS BIBLIOGRÁFICAS 1. Rhodes GH, Dwarki VJ, Abai A, Felgner J, Felgner PL, Gromkowski SH et al. Injection of expression vectors containing viral genes induces cellular, humoral and protective immunity. En: Ginsberg HS, Brown F, Chanock RM, Lerner RA, eds. Vaccines New York: Cold Spring Harbor Laboratory Press, 1993: Danko I, Wolff JA. Direct gene transfer into muscle. Vaccine 1994;12: Spier RE. Meeting on vaccine strategies for tomorrov. Vaccine 1993;11: Waine GJ, Mc Manus DP. Nucleic acids: vaccine of the future. Parasitol Today 1995;11: Manickan E, Karem KL, Rouse BT, DNA vaccines Amodern Gimmick or a boon to vaccinology. Immunology 1997;17: Alberti E, Acosta A, Sarmiento ME, Hidalgo C, Vidal T, Fachado A et al. Specific cellular and humoral inmune response in Balb/c mice inmunized with an expression genomic library of Trypanosomic cruzi. Vaccine. 1998;(16):6: Fouts DL, Ruef BJ, Ridley PT, Wrightsman RA, Peterson DS, Manning JE. Nucleotide sequence and transcription of a trypomastigote surface antigen gene of Trypanosoma cruzi. Mol Biochem Parasitol 1991;46: Parodi AJ, Pollevick GD, Mautner M, Buschiazzo A, Sanchez DO, Frasch ACC. Identification of the gene(s) coding for the trans-sialidase of Trypanosoma cruzi. EMBO J 1992;11: Sambrook J, Frisch EF, Maniatis T. Molecular cloning. A laboratory manual. 2 ed. Cold Spring: Harbor Laboratory Press, 1989: Hookey JV, Palmer MF. A comparative investigation and identification of Leptospira interrogans serogroup icterohaemorrhagiae strains by monoclonal antibody and fingprint analysis. Zbl Bakt 1991;275: Camargo EP. Growth and differentiation in Trypanosoma cruzi. 1 origin of metacyclic tripanosomes in liquid medium. Rev Inst Med Trop Sao Paulo 1964;6: Lowry DH, Rosebrogh NJ, Farr AL, Randal LJ. Protein meassurement with the folin phenol reagent. J Biolg Chem 1951;193:
10 13. Tsang VC, Peralta JM, Simons AR. Enzyme linked immunotransfer blot technique (EITB) for studying the specificities of antigens and antibodies separated by gel electrophoresis. Methodos Enzymol 1983;92: Alberti E, Acosta A, Sarmiento ME, Hidalgo C, Fachado A, Vidal T. et al. Respuesta humoral específica en ratones BALB/c inmunizados con una librería genómica de expresión de Trypanosoma cruzi. Rev Cubana Med Trop 1999;51: Webster RG, Fynan EF, Santoro JC, Robinson H. Protection of ferrets against influenza challenge with a DNA vaccine to the haemaglutinin. Vaccine 1994;12: Montgomery DL, Shiver JW, Leander KR, Perry HC, Friedman A, Martínez D et al. Heterologous and homologous protection against influenza A by DNA vaccination: optimization of vectors. DNA Cell Biol 1993;12: Scharfstein JM, Schechter M, Senna M, Peralta JM, Mendoca- Previato, Miles M. Trypanosoma cruzi characterization and islation of 57/51 M.W suface glycoprotein (GP57/51) expressed by epimastigotes and blood stream trypomastigote. J Immunol 1986;137: Donelly JJ, Ulmer JB, Shever JW, Leu MA. DNA vaccines. Annu Rev Immunol 1997;15: Ulmer JB, Donnelly JJ, Parker SE, Rhodes GH, Felgener PL, Dwarki VJ et al. Heterologous protection against influenza by injection of DNA encoding a viral protein. Science 1993;259: Recibido: 18 de septiembre del Aprobado: 27 de febrero del Dr. Esteban Alberti Amador. Instituto de Medicina Tropical "Pedro Kourí". Apartado 601, Marianao, Ciudad de La Habana, Cuba. Correo electrónico:estebana@ipk.sld.cu
DANAGENE RNA PURIFICATION KIT
 DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
Código: IDX-016 Ver: 1 TOXO. Sistema para la detección de la presencia de ADN de Toxoplasma gondii. Reg. MSP 21205
 Sistema para la detección de la presencia de ADN de Toxoplasma gondii Reg. MSP 21205 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. info@atgen.com.uy www.atgen.com.uy
Sistema para la detección de la presencia de ADN de Toxoplasma gondii Reg. MSP 21205 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. info@atgen.com.uy www.atgen.com.uy
CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL
 LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
39. Aislamiento y purificación del DNA de un plásmido recombinante
 39. Aislamiento y purificación del DNA de un plásmido recombinante Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento de Bioquímica
39. Aislamiento y purificación del DNA de un plásmido recombinante Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento de Bioquímica
RESULTADOS Y DISCUSIÓN. Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv
 RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
C A P Í T U L O 3 M A T E R I A L E S Y M É T O D O. Se ejecutaron varias pruebas para la inactivación de Escherichia Coli ATCC 25922 en agua
 C A P Í T U L O 3 M A T E R I A L E S Y M É T O D O Se ejecutaron varias pruebas para la inactivación de Escherichia Coli ATCC 25922 en agua destilada utilizando Dióxido de Titanio dopado con Nitrógeno,
C A P Í T U L O 3 M A T E R I A L E S Y M É T O D O Se ejecutaron varias pruebas para la inactivación de Escherichia Coli ATCC 25922 en agua destilada utilizando Dióxido de Titanio dopado con Nitrógeno,
AISLAMIENTO DE ÁCIDO DESOXIRRIBONUCLEICO (DNA) GENÓMICO Y PLASMÍDICO
 AISLAMIENTO DE ÁCIDO DESOXIRRIBONUCLEICO (DNA) GENÓMICO Y PLASMÍDICO E l estudio del genoma de los seres vivos a sido uno d los principales objetivos de la Biología. Desde los trabajos de Mendel (1866),
AISLAMIENTO DE ÁCIDO DESOXIRRIBONUCLEICO (DNA) GENÓMICO Y PLASMÍDICO E l estudio del genoma de los seres vivos a sido uno d los principales objetivos de la Biología. Desde los trabajos de Mendel (1866),
5. MATERIALES Y MÉTODOS
 5. MATERIALES Y MÉTODOS 5.1 Equipos Los siguientes termocicladores se emplearon para la amplificación por PCR: - Perkin Elmer, GeneAmp PCR System 2400. - Perkin Elmer, GeneAmp PCR System 9600. - Applied
5. MATERIALES Y MÉTODOS 5.1 Equipos Los siguientes termocicladores se emplearon para la amplificación por PCR: - Perkin Elmer, GeneAmp PCR System 2400. - Perkin Elmer, GeneAmp PCR System 9600. - Applied
Módulo 1 Biología Molecular Genética Molecular II 2009. Módulo 1. Amplificación de un fragmento de ADN genómico por PCR
 Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa
 38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa José Luis Caballero Repullo, Enriqueta Moyano, Juan Muñoz Blanco Departamento de Bioquímica y Biología Molecular, Campus
38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa José Luis Caballero Repullo, Enriqueta Moyano, Juan Muñoz Blanco Departamento de Bioquímica y Biología Molecular, Campus
PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN DE LAS COMPETENCIAS PROFESIONALES CUESTIONARIO DE AUTOEVALUACIÓN PARA LAS TRABAJADORAS Y TRABAJADORES
 MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
23. Hidrólisis ácida y enzimática del glucógeno
 23. Hidrólisis ácida y enzimática del glucógeno Emilia Martínez Galisteo, Carmen Alicia Padilla Peña, Concepción García Alfonso, José Antonio Bárcena Ruiz, Jesús Diez Dapena. Departamento de Bioquímica
23. Hidrólisis ácida y enzimática del glucógeno Emilia Martínez Galisteo, Carmen Alicia Padilla Peña, Concepción García Alfonso, José Antonio Bárcena Ruiz, Jesús Diez Dapena. Departamento de Bioquímica
DETERMINACIÓN DEL FACTOR Rh por PCR
 Ref.PCRRh DETERMINACIÓN DEL FACTOR Rh por PCR 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
Ref.PCRRh DETERMINACIÓN DEL FACTOR Rh por PCR 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
SERVICIO DE ANTICUERPOS POLICLONALES A PEDIDO
 SERVICIO DE ANTICUERPOS POLICLONALES A PEDIDO GrupoBios S.A. Avda.Zañartu 1482 Ñuñoa Santiago-Chile Teléfono: (56-2) 473 6100 Fax: (56-2) 239 4250 e-mail: ventas@grupobios.cl www.grupobios.cl 2011 CONTENIDO
SERVICIO DE ANTICUERPOS POLICLONALES A PEDIDO GrupoBios S.A. Avda.Zañartu 1482 Ñuñoa Santiago-Chile Teléfono: (56-2) 473 6100 Fax: (56-2) 239 4250 e-mail: ventas@grupobios.cl www.grupobios.cl 2011 CONTENIDO
PROTOCOLOS DE OBTENCIÓN, CONSERVACIÓN Y ENVÍO DE MUESTRAS BIOLÓGICAS
 PROTOCOLOS DE OBTENCIÓN, CONSERVACIÓN Y ENVÍO DE MUESTRAS BIOLÓGICAS ESTUDIO TRASLACIONAL PROSPECTIVO DE DETERMINACIÓN DE FACTORES PREDICTIVOS DE EFICACIA Y TOXICIDAD EN PACIENTES CON CÁNCER ÍNDICE 1 INTRODUCCIÓN....
PROTOCOLOS DE OBTENCIÓN, CONSERVACIÓN Y ENVÍO DE MUESTRAS BIOLÓGICAS ESTUDIO TRASLACIONAL PROSPECTIVO DE DETERMINACIÓN DE FACTORES PREDICTIVOS DE EFICACIA Y TOXICIDAD EN PACIENTES CON CÁNCER ÍNDICE 1 INTRODUCCIÓN....
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN
 5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
El Banco Nacional de ADN oferta un control de calidad de muestras de ADN y ARN.
 PROGRAMA CONTROL DE CALIDAD DE MUESTRAS El Banco Nacional de ADN oferta un control de calidad de muestras de ADN y ARN. El programa completo de control de calidad de muestras de ADN y ARN engloba diferentes
PROGRAMA CONTROL DE CALIDAD DE MUESTRAS El Banco Nacional de ADN oferta un control de calidad de muestras de ADN y ARN. El programa completo de control de calidad de muestras de ADN y ARN engloba diferentes
V MATERIALES Y MÉTODOS
 V MATERIALES Y MÉTODOS 5.1 Aislamiento de bacterias e identificación 5.1.1 Cepas tomadas del cepario de la Universidad de las Américas-Puebla En el cepario del Departamento de Química y Biología hay algunas
V MATERIALES Y MÉTODOS 5.1 Aislamiento de bacterias e identificación 5.1.1 Cepas tomadas del cepario de la Universidad de las Américas-Puebla En el cepario del Departamento de Química y Biología hay algunas
Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a
 Introducción Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a los investigadores verificar la expresión de una proteína, determinar la cantidad relativa
Introducción Western Blotting (o inmunotransferencia) es un procedimiento estándar de laboratorio que permite a los investigadores verificar la expresión de una proteína, determinar la cantidad relativa
Práctico: Genética bacteriana 2007.
 Práctico: Genética bacteriana 2007. Actividad integrada Departamento de Genética Departamento de Bacteriología y Virología. OBJETIVOS Objetivos generales El estudiante al terminar la actividad práctica
Práctico: Genética bacteriana 2007. Actividad integrada Departamento de Genética Departamento de Bacteriología y Virología. OBJETIVOS Objetivos generales El estudiante al terminar la actividad práctica
ELECTROFORESIS BASICA
 Ref.ELECBASICA (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO ELECTROFORESIS BASICA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref.ELECBASICA (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO ELECTROFORESIS BASICA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
CLONACIÓN Y EXPRESIÓN DE LA CISTEÍN PROTEINASA RECOMBINANTE TVLEGU-1 DE Trichomonas vaginalis.
 CLONACIÓN Y EXPRESIÓN DE LA CISTEÍN PROTEINASA RECOMBINANTE TVLEGU-1 DE Trichomonas vaginalis. Rodríguez Cabrera N. A. 1, Ortega Arroyo J. 2, Arroyo Verástegui R. A. 3, Brieba de Castro L. 2 y Ortega López
CLONACIÓN Y EXPRESIÓN DE LA CISTEÍN PROTEINASA RECOMBINANTE TVLEGU-1 DE Trichomonas vaginalis. Rodríguez Cabrera N. A. 1, Ortega Arroyo J. 2, Arroyo Verástegui R. A. 3, Brieba de Castro L. 2 y Ortega López
MANUAL DE PRÁCTICAS DE LABORATORIO
 MANUAL DE PRÁCTICAS DE LABORATORIO INGENIERIA ENBIOTECNOLOGÍA INGENIERÍA GENÉTICA FICHA TECNICA FICHA TÉCNICA SEMINARIO DE BIOTECNOLOGÍA MÉDICO-FARMACÉUTICA Fecha: Nombre del catedrático: 10-Julio-2012
MANUAL DE PRÁCTICAS DE LABORATORIO INGENIERIA ENBIOTECNOLOGÍA INGENIERÍA GENÉTICA FICHA TECNICA FICHA TÉCNICA SEMINARIO DE BIOTECNOLOGÍA MÉDICO-FARMACÉUTICA Fecha: Nombre del catedrático: 10-Julio-2012
Bioquímica III- 2009
 Facultad de Ciencias Exactas, Universidad Nacional de La Plata Bioquímica III- 2009 Trabajo Práctico Nro 4 Extracción de RNA y DNA bacteriano INTRODUCCIÓN El RNA es el ácido nucleico más abundante en la
Facultad de Ciencias Exactas, Universidad Nacional de La Plata Bioquímica III- 2009 Trabajo Práctico Nro 4 Extracción de RNA y DNA bacteriano INTRODUCCIÓN El RNA es el ácido nucleico más abundante en la
ELABORACIÓN N DE MEZCLA PARA PCR. Raquel Asunción Lima Cordón
 ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
INTRODUCCIÓN A LA METODOLOGÍA MOLECULAR. 2002 `Derechos Reservados Pontificia Universidad Javeriana Instituto de Genética Humana Bogotá COLOMBIA
 INTRODUCCIÓN A LA METODOLOGÍA MOLECULAR 2002 `Derechos Reservados Pontificia Universidad Javeriana Instituto de Genética Humana Bogotá COLOMBIA Equipos de Laboratorio Un equipo de laboratorio es un conjunto
INTRODUCCIÓN A LA METODOLOGÍA MOLECULAR 2002 `Derechos Reservados Pontificia Universidad Javeriana Instituto de Genética Humana Bogotá COLOMBIA Equipos de Laboratorio Un equipo de laboratorio es un conjunto
turbidez en los medios de cultivo. La duración de la prueba de esterilidad es de 14 días. Las pruebas de toxicidad (específica y general), llamadas
 Para que una prueba se considere validada deberá cumplir los requisitos siguientes: Precisión: es la variación de los resultados de acuerdo a la desviación estándar o al coeficiente de variación. Exactitud:
Para que una prueba se considere validada deberá cumplir los requisitos siguientes: Precisión: es la variación de los resultados de acuerdo a la desviación estándar o al coeficiente de variación. Exactitud:
Normalización de soluciones de NaOH 0,1N y HCl 0,1N.
 Laboratorio N 1: Normalización de soluciones de NaOH 0,1N y HCl 0,1N. Objetivos: - Determinar la normalidad exacta de una solución de hidróxido de sodio aproximadamente 0,1 N, utilizando biftalato de potasio
Laboratorio N 1: Normalización de soluciones de NaOH 0,1N y HCl 0,1N. Objetivos: - Determinar la normalidad exacta de una solución de hidróxido de sodio aproximadamente 0,1 N, utilizando biftalato de potasio
CAPÍTULO III RESULTADOS Y ANÁLISIS DE RESULTADOS
 CAPÍTULO III RESULTADOS Y ANÁLISIS DE RESULTADOS Para el proceso de purificación del aceite, se pudo observar, en el momento del filtrado algunas partículas sólidas retenidas en los diferentes filtros
CAPÍTULO III RESULTADOS Y ANÁLISIS DE RESULTADOS Para el proceso de purificación del aceite, se pudo observar, en el momento del filtrado algunas partículas sólidas retenidas en los diferentes filtros
ELECTROFORESIS AVANZADA
 Ref.ELECAVANZADA (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref.ELECAVANZADA (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
DANAGENE SALIVA KIT. Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones
 DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION DANAGENE SALIVA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras
DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION DANAGENE SALIVA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras
Código: IDK-010 Ver: 1. Proteína G C825T. Sistema para la detección de la mutación C825T en el gene de la proteína G.
 C825T Sistema para la detección de la mutación C825T en el gene de la proteína G. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy www.atgen.com.uy
C825T Sistema para la detección de la mutación C825T en el gene de la proteína G. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy www.atgen.com.uy
FICHA PÚBLICA DEL PROYECTO
 FICHA PÚBLICA DEL PROYECTO PROGRAMA DE ESTÍMULOS A LA INNOVACIÓN NUMERO DE PROYECTO: 214028 EMPRESA BENEFICIADA: PHARMACOS EXAKTA S.A. DE C.V. TÍTULO DEL PROYECTO: DESARROLLO DE UN MINI-ARREGLO DE ANTIGENOS
FICHA PÚBLICA DEL PROYECTO PROGRAMA DE ESTÍMULOS A LA INNOVACIÓN NUMERO DE PROYECTO: 214028 EMPRESA BENEFICIADA: PHARMACOS EXAKTA S.A. DE C.V. TÍTULO DEL PROYECTO: DESARROLLO DE UN MINI-ARREGLO DE ANTIGENOS
TaqMan GMO Maize Quantification Kit. Part No: 4481972
 TaqMan GMO Maize Quantification Kit Part No: 4481972 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que ocupan
TaqMan GMO Maize Quantification Kit Part No: 4481972 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que ocupan
7.012 Serie de ejercicios 5
 Nombre Grupo 7.012 Serie de ejercicios 5 Pregunta 1 Al estudiar los problemas de esterilidad, usted intenta aislar un hipotético gen de conejo que explique la prolífica reproducción de estos animales.
Nombre Grupo 7.012 Serie de ejercicios 5 Pregunta 1 Al estudiar los problemas de esterilidad, usted intenta aislar un hipotético gen de conejo que explique la prolífica reproducción de estos animales.
Tipificación de Grupos Sanguineos e Isohemaglutininas
 Tipificación de Grupos Sanguineos e Isohemaglutininas Introducción Los eritrocitos expresan antígenos de membrana. Dichos antígenos se encuentran determinados genéticamente y pueden ser identificados mediante
Tipificación de Grupos Sanguineos e Isohemaglutininas Introducción Los eritrocitos expresan antígenos de membrana. Dichos antígenos se encuentran determinados genéticamente y pueden ser identificados mediante
Caracterización morfo-agronómica y molecular de frijoles criollos de color rojo claro en Nicaragua y de frijoles negros en Ipala, Guatemala
 Caracterización morfo-agronómica y molecular de frijoles criollos de color rojo claro en Nicaragua y de frijoles negros en Ipala, Guatemala IICA/Red SICTA-CIAT INFORME DE AVANCE Gerardo Gallego - Harold
Caracterización morfo-agronómica y molecular de frijoles criollos de color rojo claro en Nicaragua y de frijoles negros en Ipala, Guatemala IICA/Red SICTA-CIAT INFORME DE AVANCE Gerardo Gallego - Harold
I. DATOS DE IDENTIFICACIÓN
 UNIVERSIDAD AUTÓNOMA DE BAJA CALIFORNIA COORDINACION DE FORMACION BASICA COORDINACION DE FORMACION PROFESIONAL Y VINCULACIÓN PROGRAMA DE UNIDAD DE APRENDIZAJE 1. Unidad Académica: FACULTAD DE CIENCIAS
UNIVERSIDAD AUTÓNOMA DE BAJA CALIFORNIA COORDINACION DE FORMACION BASICA COORDINACION DE FORMACION PROFESIONAL Y VINCULACIÓN PROGRAMA DE UNIDAD DE APRENDIZAJE 1. Unidad Académica: FACULTAD DE CIENCIAS
Guía Práctica 9. Producción de micelio en medio líquido para extracción de ADN. Micelio de hongos. Contenido
 Guía Práctica 9 Micelio de hongos Producción de micelio en medio líquido para extracción de ADN Guillermo Castellanos, Experto en Investigación 2 Carlos Jara, Ing. Agr. M.Sc., Asociado en Investigación
Guía Práctica 9 Micelio de hongos Producción de micelio en medio líquido para extracción de ADN Guillermo Castellanos, Experto en Investigación 2 Carlos Jara, Ing. Agr. M.Sc., Asociado en Investigación
CUANTIFICACIÓN DE ADENOSIN DESAMINASA (ADA)
 CUANTIFICACIÓN DE ADENOSIN DESAMINASA (ADA) PROTOCOLO ADA FUNDAMENTO DEL METODO: La adenosindesaminasa (ADA) es una enzima del catabolismo de las purinas que cataliza la conversión de la adenosina en inosina
CUANTIFICACIÓN DE ADENOSIN DESAMINASA (ADA) PROTOCOLO ADA FUNDAMENTO DEL METODO: La adenosindesaminasa (ADA) es una enzima del catabolismo de las purinas que cataliza la conversión de la adenosina en inosina
1. Título. Cuantificacion de ADN por espectrofluorometría mediante el uso de Quant- it PicoGreen dsaadnssay Kit (Invitrogen ).
 1. Título. Cuantificacion de ADN por espectrofluorometría mediante el uso de QuantiT PicoGreen dsaadnssay Kit (Invitrogen ). 2. Finalidad. El presente documento describe el Procedimiento Normalizado de
1. Título. Cuantificacion de ADN por espectrofluorometría mediante el uso de QuantiT PicoGreen dsaadnssay Kit (Invitrogen ). 2. Finalidad. El presente documento describe el Procedimiento Normalizado de
METODOLOGÍAS UTILIZADAS EN INVESTIGACIÓN BÁSICA Y APLICADA REACCION EN CADENA DE LA POLIMERASA (PCR)
 METODOLOGÍAS UTILIZADAS EN INVESTIGACIÓN BÁSICA Y APLICADA REACCION EN CADENA DE LA POLIMERASA (PCR) Centro de de Microscopía Electrónica Facultad de de Ciencias Médicas Universidad Nacional de de Córdoba
METODOLOGÍAS UTILIZADAS EN INVESTIGACIÓN BÁSICA Y APLICADA REACCION EN CADENA DE LA POLIMERASA (PCR) Centro de de Microscopía Electrónica Facultad de de Ciencias Médicas Universidad Nacional de de Córdoba
ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA
 VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
VIII 1 PRÁCTICA 8 ELECTROLISIS DE UNA DISOLUCIÓN DE YODURO DE POTASIO. PILA ELECTROLÍTICA En esta práctica estudiaremos algunos aspectos prácticos de las reacciones de oxidación reducción que no son espontáneas.
I. 15microlitros de agua esteril, perforar el pozo y diluir. II. Se tomaron 2 microlitros para la primera transformación.
 23 de agosto 2007 Se comenzó la elaboración de la bitácora Medio LB Broth, Billar (Luria-Bertani) 25gr/litro Se preparó 500 mililitros agregando 12.5 gramos Se diluyó y esterilizó por autoclave Medio LB
23 de agosto 2007 Se comenzó la elaboración de la bitácora Medio LB Broth, Billar (Luria-Bertani) 25gr/litro Se preparó 500 mililitros agregando 12.5 gramos Se diluyó y esterilizó por autoclave Medio LB
Informe del trabajo práctico nº7
 Informe del trabajo práctico nº7 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Mostrar las propiedades que presentan
Informe del trabajo práctico nº7 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Mostrar las propiedades que presentan
BLOQUE I. CUÁL ES LA COMPOSICIÓN DE LOS SERES VIVOS? LAS MOLÉCULAS DE LA VIDA
 I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA 6.1. Concepto y estructura. BLOQUE I. CUÁL ES LA COMPOSICIÓN DE
I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA 6.1. Concepto y estructura. BLOQUE I. CUÁL ES LA COMPOSICIÓN DE
Practica la genética Ficha didáctica del profesorado Bachillerato
 Ficha didáctica del profesorado Bachillerato www.eurekamuseoa.es Extracción de ADN Cuál es la función de cada uno de los ingredientes utilizados para realizar la disolución tampón para la visualización
Ficha didáctica del profesorado Bachillerato www.eurekamuseoa.es Extracción de ADN Cuál es la función de cada uno de los ingredientes utilizados para realizar la disolución tampón para la visualización
TRABAJO PRACTICO Nº 3 ENZIMOINMUNOANALISIS ELISA
 TRABAJO PRACTICO Nº 3 ENZIMOINMUNOANALISIS ELISA Docentes encargados: Bioq. Natalia Guiñazú Bioq. Maria Sol Renna Biol. Virginia Andreani Bioq. Mauricio Figueredo Bioq. Vanina Garrido Bioq. Laura Dulgerian
TRABAJO PRACTICO Nº 3 ENZIMOINMUNOANALISIS ELISA Docentes encargados: Bioq. Natalia Guiñazú Bioq. Maria Sol Renna Biol. Virginia Andreani Bioq. Mauricio Figueredo Bioq. Vanina Garrido Bioq. Laura Dulgerian
REACCIONES DE IONES METÁLICOS
 Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
Actividad Experimental 4 REACCIONES DE IONES METÁLICOS Investigación previa -Investigar las medidas de seguridad para trabajar con amoniaco -Investigar las reglas de solubilidad de las sustancias químicas.
4. Materiales y Métodos. Los equipos que a continuación se mencionan se encuentran en el laboratorio de
 39 4. Materiales y Métodos 4.1 Equipos Los equipos que a continuación se mencionan se encuentran en el laboratorio de Ingeniería Ambiental de la Universidad de las Américas Puebla y en el Laboratorio de
39 4. Materiales y Métodos 4.1 Equipos Los equipos que a continuación se mencionan se encuentran en el laboratorio de Ingeniería Ambiental de la Universidad de las Américas Puebla y en el Laboratorio de
EXTRACCIÓN DE ADN DE DISTINTAS MUESTRAS VEGETALES
 EXTRACCIÓN DE ADN DE DISTINTAS MUESTRAS VEGETALES ABSTRACT The objective of the experiment is to extract DNA of different fruits and vegetables. On our case we developed three different experiments, the
EXTRACCIÓN DE ADN DE DISTINTAS MUESTRAS VEGETALES ABSTRACT The objective of the experiment is to extract DNA of different fruits and vegetables. On our case we developed three different experiments, the
Programa donde se inscribe la beca y/o la tesis: Interacciones biológicas: de las
 Titulo: Potencial uso simultáneo de micopatógenos biocontroladores de hormigas cortadoras de hojas. Autores: Natalia G. Armando, Jorge A. Marfetán, Patricia J. Folgarait Correo: ng.armando14@gmail.com
Titulo: Potencial uso simultáneo de micopatógenos biocontroladores de hormigas cortadoras de hojas. Autores: Natalia G. Armando, Jorge A. Marfetán, Patricia J. Folgarait Correo: ng.armando14@gmail.com
PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN DE LAS COMPETENCIAS PROFESIONALES CUESTIONARIO DE AUTOEVALUACIÓN PARA LAS TRABAJADORAS Y TRABAJADORES
 MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
Enfermedad de Newcastle
 Enfermedad de Newcastle Autor: Gerencia División Aves IASA- Sección Técnica. Fecha de Publicación: 12/08/2008 La enfermedad de Newcastle es considerada como uno de los procesos patológicos con mayor impacto
Enfermedad de Newcastle Autor: Gerencia División Aves IASA- Sección Técnica. Fecha de Publicación: 12/08/2008 La enfermedad de Newcastle es considerada como uno de los procesos patológicos con mayor impacto
ENUMERACION BACTERIANA: EL NUMERO MAS PROBABLE
 CUARTA PARTE ENUMERACION BACTERIANA: EL NUMERO MAS PROBABLE EL METODO DE NUMERO MAS PROBABLE (NMP) es una estrategia efeciente de estimación de densidades poblacionales especialmente cuando una evaluación
CUARTA PARTE ENUMERACION BACTERIANA: EL NUMERO MAS PROBABLE EL METODO DE NUMERO MAS PROBABLE (NMP) es una estrategia efeciente de estimación de densidades poblacionales especialmente cuando una evaluación
Identificación varietal en vid por técnicas de Biología Molecular. Lic. Luciana Garcia Lic. Carolina Chiconofri
 Identificación varietal en vid por técnicas de Biología Molecular. Lic. Luciana Garcia Lic. Carolina Chiconofri OBJETIVO Desarrollar un banco de datos a partir de plantas de origen indudable y del uso
Identificación varietal en vid por técnicas de Biología Molecular. Lic. Luciana Garcia Lic. Carolina Chiconofri OBJETIVO Desarrollar un banco de datos a partir de plantas de origen indudable y del uso
3. COMPONENTES. Tampón de electroforesis concentrado 2 x 50 ml 10 X (2 envases 500ml)
 PCR SIMULADA Ref.PCR Simulada (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
PCR SIMULADA Ref.PCR Simulada (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
PCR gen 18S ARNr humano
 PCR gen 18S ARNr humano Ref.PCR18S 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa (PCR)
PCR gen 18S ARNr humano Ref.PCR18S 1.OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa (PCR)
Entender el funcionamiento de los relojes permitiría lidiar con ciertas patologías en humanos. 28 ACTUALIDAD EN I+D RIA / Vol. 41 / N.
 28 ACTUALIDAD EN I+D RIA / Vol. 41 / N.º 1 Entender el funcionamiento de los relojes permitiría lidiar con ciertas patologías en humanos Abril 2015, Argentina 29 Relojes biológicos en plantas Ajustar el
28 ACTUALIDAD EN I+D RIA / Vol. 41 / N.º 1 Entender el funcionamiento de los relojes permitiría lidiar con ciertas patologías en humanos Abril 2015, Argentina 29 Relojes biológicos en plantas Ajustar el
Identificación y caracterización de células madres cancerígenas (CMCs) en Sarcoma de Ewing
 Identificación y caracterización de células madres cancerígenas (CMCs) en Sarcoma de Ewing Introducción Una célula madre o célula troncal es una célula que tiene capacidad de autorrenovarse mediante divisiones
Identificación y caracterización de células madres cancerígenas (CMCs) en Sarcoma de Ewing Introducción Una célula madre o célula troncal es una célula que tiene capacidad de autorrenovarse mediante divisiones
SEMINARIO 2 Parámetros del grado de perecibilidad de un alimento
 UNIVERSIDAD NACIONAL DEL CENTRO DE LA PROVINCIA DE BUENOS AIRES Facultad de Ingeniería Carrera: Licenciatura en Tecnología de los Alimentos Asignatura: Bioquímica de los Alimentos I. HUMEDAD SEMINARIO
UNIVERSIDAD NACIONAL DEL CENTRO DE LA PROVINCIA DE BUENOS AIRES Facultad de Ingeniería Carrera: Licenciatura en Tecnología de los Alimentos Asignatura: Bioquímica de los Alimentos I. HUMEDAD SEMINARIO
Preparación de medios de cultivo
 Objetivos Preparación de medios de cultivo Curso: Métodos en fitopatología 24 de abril de 2009 Dr. Pedro Mondino Conocer a que denominamos medio de cultivo en el laboratorio de Fitopatología. Reconocer
Objetivos Preparación de medios de cultivo Curso: Métodos en fitopatología 24 de abril de 2009 Dr. Pedro Mondino Conocer a que denominamos medio de cultivo en el laboratorio de Fitopatología. Reconocer
QUIMICA ANALÍTICA (63.05) SOLUCIONES REGULADORAS DE ph 63.05.12. Lic. Ana María Martín
 QUIMICA ANALÍTICA (63.05) SOLUCIONES REGULADORAS DE ph 63.05.12 Lic. Ana María Martín Lic. Ana María Martín Introducción SOLUCIONES REGULADORAS DE ph Muchas de las reacciones químicas que se producen en
QUIMICA ANALÍTICA (63.05) SOLUCIONES REGULADORAS DE ph 63.05.12 Lic. Ana María Martín Lic. Ana María Martín Introducción SOLUCIONES REGULADORAS DE ph Muchas de las reacciones químicas que se producen en
Procesado de muestras en el laboratorio de la clínica (I)
 12.prevención de la salud Procesado de muestras en el laboratorio de la clínica (I) A lo largo de esta primera parte veremos como realizar un manejo correcto de las muestras de sangre, orina y líquidos
12.prevención de la salud Procesado de muestras en el laboratorio de la clínica (I) A lo largo de esta primera parte veremos como realizar un manejo correcto de las muestras de sangre, orina y líquidos
Diagnóstico microbiológico de la infección por HIV
 Diagnóstico microbiológico de la infección por HIV Juan Carlos Rodríguez Díaz S. Microbiología Hospital General Universitario de Alicante E-mail: rodriguez_juadia@gva.es http://microbiología-alicante.umh.es
Diagnóstico microbiológico de la infección por HIV Juan Carlos Rodríguez Díaz S. Microbiología Hospital General Universitario de Alicante E-mail: rodriguez_juadia@gva.es http://microbiología-alicante.umh.es
6. Reacciones de precipitación
 6. Reacciones de precipitación Las reacciones de precipitación son aquellas en las que el producto es un sólido; se utilizan en los métodos gravimétricos de análisis y en las titulaciones por precipitación.
6. Reacciones de precipitación Las reacciones de precipitación son aquellas en las que el producto es un sólido; se utilizan en los métodos gravimétricos de análisis y en las titulaciones por precipitación.
NORMAS DE TRABAJO EN BIOLOGÍA MOLECULAR Y GUÍA DE PROBLEMAS HABITUALES Y SU SOLUCIÓN
 NORMAS DE TRABAJO EN BIOLOGÍA MOLECULAR Y GUÍA DE PROBLEMAS HABITUALES Y SU SOLUCIÓN 1. PROCEDIMIENTOS BÁSICOS: En este apartado pretendemos detallar algunos factores muy importantes a la hora de realizar
NORMAS DE TRABAJO EN BIOLOGÍA MOLECULAR Y GUÍA DE PROBLEMAS HABITUALES Y SU SOLUCIÓN 1. PROCEDIMIENTOS BÁSICOS: En este apartado pretendemos detallar algunos factores muy importantes a la hora de realizar
LIMPIEZA Y DESINFECCIÓN EN LA INDUSTRIA LÁCTEA
 LIMPIEZA Y EN LA INDUSTRIA LÁCTEA LD EN LAS INDUSTRIAS DE ALIMENTOS La sanitización/higienización es un concepto general que comprende la creación y mantenimiento de las condiciones óptimas de higiene
LIMPIEZA Y EN LA INDUSTRIA LÁCTEA LD EN LAS INDUSTRIAS DE ALIMENTOS La sanitización/higienización es un concepto general que comprende la creación y mantenimiento de las condiciones óptimas de higiene
ELECTROFORESIS EN GELES DE AGAROSA. Agustín Garrido. agugarrido@hotmail.com
 1 ELECTROFORESIS EN GELES DE AGAROSA Agustín Garrido agugarrido@hotmail.com Introducción En este trabajo práctico se utilizó la técnica de electroforesis. Este proceso se basa en la migración de las moléculas
1 ELECTROFORESIS EN GELES DE AGAROSA Agustín Garrido agugarrido@hotmail.com Introducción En este trabajo práctico se utilizó la técnica de electroforesis. Este proceso se basa en la migración de las moléculas
25. Perfil lipídico. Isaac Túnez Fiñana 1, Aurora Galván Cejudo 2 RESUMEN
 25. Perfil lipídico Isaac Túnez Fiñana 1, Aurora Galván Cejudo 2 1 Departamento de Bioquímica y Biología Molecular, Avda. Menéndez Pidal s/n, 14071- Córdoba, 2 Campus de Rabanales, Edif. Severo Ochoa 14071-Córdoba
25. Perfil lipídico Isaac Túnez Fiñana 1, Aurora Galván Cejudo 2 1 Departamento de Bioquímica y Biología Molecular, Avda. Menéndez Pidal s/n, 14071- Córdoba, 2 Campus de Rabanales, Edif. Severo Ochoa 14071-Córdoba
17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico
 17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico Carmen Alicia Padilla Peña, Jesús Diez Dapena, Emilia Martínez Galisteo, José
17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico Carmen Alicia Padilla Peña, Jesús Diez Dapena, Emilia Martínez Galisteo, José
Prácticas de Análisis Instrumental
 Prácticas de Análisis Instrumental Asignatura: Análisis Instrumental Alumno: Daniel González Mancebo Practica 1. DETERMINACIÓN DE CONSTANTES DE EQUILIBRIO MEDIANTE ESPECTROFOTOMETRÍA UV- VISIBLE. Lo primero
Prácticas de Análisis Instrumental Asignatura: Análisis Instrumental Alumno: Daniel González Mancebo Practica 1. DETERMINACIÓN DE CONSTANTES DE EQUILIBRIO MEDIANTE ESPECTROFOTOMETRÍA UV- VISIBLE. Lo primero
MANUAL DE PRÁCTICAS !!! Heber!Torres! !!!!!!!!!!!!!!!!!!!!!!!!!!!
 MANUAL DE PRÁCTICAS igem-cideb_uanl HeberTorres Índice de Contenidos Presentación... 1 Reglas Generales y Recomendaciones... 3 Prácticas de Laboratorio de Biología Sintética para igem-cideb_uanl... 5
MANUAL DE PRÁCTICAS igem-cideb_uanl HeberTorres Índice de Contenidos Presentación... 1 Reglas Generales y Recomendaciones... 3 Prácticas de Laboratorio de Biología Sintética para igem-cideb_uanl... 5
velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz porosa
 INTRODUCCIÓN En general, la electroforesis es una técnica que separa las moléculas en base a sus diferentes velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz
INTRODUCCIÓN En general, la electroforesis es una técnica que separa las moléculas en base a sus diferentes velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz
Universitat de les Illes Balears
 1, 2S Identificación de la asignatura Créditos 1.6 presenciales (40 Horas) 3.4 no presenciales (85 Horas) 5 totales (125 Horas). 1, 2S(Campus Extens) Semestre Doctorado convocatoria única de impartición
1, 2S Identificación de la asignatura Créditos 1.6 presenciales (40 Horas) 3.4 no presenciales (85 Horas) 5 totales (125 Horas). 1, 2S(Campus Extens) Semestre Doctorado convocatoria única de impartición
FUNDAMENTOS DE ANÁLISIS INSTRUMENTAL. 4ª RELACIÓN DE PROBLEMAS.
 FUNDAMENTOS DE ANÁLISIS INSTRUMENTAL. 4ª RELACIÓN DE PROBLEMAS. 1.- Para determinar el contenido en plomo en una muestra de leche contaminada, se toma 1.0 ml de la leche y se diluye a un volumen final
FUNDAMENTOS DE ANÁLISIS INSTRUMENTAL. 4ª RELACIÓN DE PROBLEMAS. 1.- Para determinar el contenido en plomo en una muestra de leche contaminada, se toma 1.0 ml de la leche y se diluye a un volumen final
Biotecnología. Historia y aplicaciones Su utilización en el INTA Alto Valle. investigación
 Alejandro Giayetto Técnico INTA agiayetto@correo.inta.gov.ar Mirta Rossini Técnico INTA mrossini@correo.inta.gov.ar Diana Vera Biotecnóloga labfitopatologia@correo.inta.gov.ar investigación 10 Biotecnología
Alejandro Giayetto Técnico INTA agiayetto@correo.inta.gov.ar Mirta Rossini Técnico INTA mrossini@correo.inta.gov.ar Diana Vera Biotecnóloga labfitopatologia@correo.inta.gov.ar investigación 10 Biotecnología
PRACTICA Núm. 16 RECUENTO DE BACTERIAS MESOFILAS AEROBIAS EN AGUA PARA CONSUMO HUMANO
 PRACTICA Núm. 16 RECUENTO DE BACTERIAS MESOFILAS AEROBIAS EN AGUA PARA CONSUMO HUMANO I. OBJETIVO Determinar la presencia de bacterias Mesófilas Aerobias en una muestra de agua potable por la técnica de
PRACTICA Núm. 16 RECUENTO DE BACTERIAS MESOFILAS AEROBIAS EN AGUA PARA CONSUMO HUMANO I. OBJETIVO Determinar la presencia de bacterias Mesófilas Aerobias en una muestra de agua potable por la técnica de
RESUMEN La industria alimentaria, en respuesta a la demanda por parte de los consumidores de alimentos naturales, frescos y libres de conservantes
 RESUMEN La industria alimentaria, en respuesta a la demanda por parte de los consumidores de alimentos naturales, frescos y libres de conservantes químicos, ha desarrollado tecnologías de conservación
RESUMEN La industria alimentaria, en respuesta a la demanda por parte de los consumidores de alimentos naturales, frescos y libres de conservantes químicos, ha desarrollado tecnologías de conservación
II. METODOLOGÍA. El proceso de elaboración del biodiesel se constituye de siete pasos fundamentales: 6.1. DETERMINACIÓN DE LOS GRAMOS DE CATALIZADOR
 II. METODOLOGÍA 6. PROCESO DE ELABORACIÓN El proceso de elaboración del biodiesel se constituye de siete pasos fundamentales: 1. Determinación de los gramos de catalizador 2. Preparación del Metóxido de
II. METODOLOGÍA 6. PROCESO DE ELABORACIÓN El proceso de elaboración del biodiesel se constituye de siete pasos fundamentales: 1. Determinación de los gramos de catalizador 2. Preparación del Metóxido de
INACTIVACIÓN DE LOS GENES SUPRESORES PTEN, DMBT1 Y P16 EN GLIOBLASTOMA MULTIFORME, ASTROCITOMAS ANAPLÁSICOS Y ASTROCITOMAS DE BAJO GRADO.
 IV CONGRESO VIRTUAL HISPANO AMERICANO DE ANATOMÍA PATOLÓGICA Abstract PDF CONTENIDO Comentarios Título Resumen Introducción Material Resultados Conclusiones Imágenes INACTIVACIÓN DE LOS GENES SUPRESORES
IV CONGRESO VIRTUAL HISPANO AMERICANO DE ANATOMÍA PATOLÓGICA Abstract PDF CONTENIDO Comentarios Título Resumen Introducción Material Resultados Conclusiones Imágenes INACTIVACIÓN DE LOS GENES SUPRESORES
Detección de patógenos en alimentos, utilizando la técnica de PCR, reacción en cadena de la polimerasa.
 Detección de patógenos en alimentos, utilizando la técnica de PCR, reacción en cadena de la polimerasa. Lic. Esp. Mariano Diego Massari 1er Congreso Bioquímico Córdoba 2011 8ª Jornada de Actualización
Detección de patógenos en alimentos, utilizando la técnica de PCR, reacción en cadena de la polimerasa. Lic. Esp. Mariano Diego Massari 1er Congreso Bioquímico Córdoba 2011 8ª Jornada de Actualización
Rentabilidad, viabilidad y financiamiento de la prevención del cáncer de cuello uterino
 Rentabilidad, viabilidad y financiamiento de la prevención del cáncer de cuello uterino Dra. Carol Levin PATH La transcripción del video está debajo de cada diapositiva. Rentabilidad Compara los costos
Rentabilidad, viabilidad y financiamiento de la prevención del cáncer de cuello uterino Dra. Carol Levin PATH La transcripción del video está debajo de cada diapositiva. Rentabilidad Compara los costos
CARDIOCHEK y CARDIOCHEK P.A
 CARDIOCHEK y CARDIOCHEK P.A NUEVA GENERACIÓN DE ANALIZADORES PORTÁTILES Introducción El Cardiochek y Cardiochek P.A son instrumentos portátiles que proporcionan medidas rápidas y precisas de múltiples
CARDIOCHEK y CARDIOCHEK P.A NUEVA GENERACIÓN DE ANALIZADORES PORTÁTILES Introducción El Cardiochek y Cardiochek P.A son instrumentos portátiles que proporcionan medidas rápidas y precisas de múltiples
1. Cuáles son las diferencias en los componentes químicos del ADN y ARN?
 ACTIVIDADES TEMA 4 - BIOTECNOLOGÍA 1. Cuáles son las diferencias en los componentes químicos del ADN y ARN? Las cadenas de ADN están formadas por fosfato y desoxirribosa y la del ARN por fosfato y ribosa.
ACTIVIDADES TEMA 4 - BIOTECNOLOGÍA 1. Cuáles son las diferencias en los componentes químicos del ADN y ARN? Las cadenas de ADN están formadas por fosfato y desoxirribosa y la del ARN por fosfato y ribosa.
EFECTO DE LA DIGESTIÓN SOBRE PROTEINAS, GRASAS Y GLÚCIDOS
 EFECTO DE LA DIGESTIÓN SOBRE PROTEINAS, GRASAS Y GLÚCIDOS Objetivos: Mª Jesús González García Mª Amparo Mora Alcácer COLEGIO AVE Mª DE PENYA-ROJA Aprender a trabajar en el laboratorio y apreciar el orden,
EFECTO DE LA DIGESTIÓN SOBRE PROTEINAS, GRASAS Y GLÚCIDOS Objetivos: Mª Jesús González García Mª Amparo Mora Alcácer COLEGIO AVE Mª DE PENYA-ROJA Aprender a trabajar en el laboratorio y apreciar el orden,
PRUEBA RAPIDA EN EMBARAZADAS (n=62,214 2009-Junio 2010) NO REACTIVO n=218 REACTIVO INDETERMINADO. Tabla 9: Resultados Prueba rápida
 11-RESULTADOS 11.1-Interpretación y análisis de resultados Un total de de 62,214 mujeres embarazadas se realizaron la prueba rápida de VIH durante años 2009 hasta junio 2010 (Tabla 9). De ellas, 61,808
11-RESULTADOS 11.1-Interpretación y análisis de resultados Un total de de 62,214 mujeres embarazadas se realizaron la prueba rápida de VIH durante años 2009 hasta junio 2010 (Tabla 9). De ellas, 61,808
PRACTICA No. 9 PREPARACION DE DISOLUCIONES
 1 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II PRACTICA No. 9 PREPARACION DE DISOLUCIONES INTRODUCCION:
1 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS QUÍMICAS Y FARMACIA ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II PRACTICA No. 9 PREPARACION DE DISOLUCIONES INTRODUCCION:
Tecnología HaloPlex by Genycell Biotech España
 Paneles de genes custom-made Tecnología HaloPlex by Genycell Biotech España SERVICIO NGS CLÍNICA HALO: OVERVIEW 1. DISEÑO DEL PANEL DE GENES Y DEL KIT DE CAPTURA 2. PREPARACIÓN DE LA MUESTRA EN EL LABORATORIO
Paneles de genes custom-made Tecnología HaloPlex by Genycell Biotech España SERVICIO NGS CLÍNICA HALO: OVERVIEW 1. DISEÑO DEL PANEL DE GENES Y DEL KIT DE CAPTURA 2. PREPARACIÓN DE LA MUESTRA EN EL LABORATORIO
FARMACOPEA MERCOSUR: VACUNAS PARA USO HUMANO
 MERCOSUR/XLII SGT Nº 11/P.RES. Nº 09/14 FARMACOPEA MERCOSUR: VACUNAS PARA USO HUMANO VISTO: El Tratado de Asunción, el Protocolo de Ouro Preto y las Resoluciones N 31/11 y 22/14 del Grupo Mercado Común.
MERCOSUR/XLII SGT Nº 11/P.RES. Nº 09/14 FARMACOPEA MERCOSUR: VACUNAS PARA USO HUMANO VISTO: El Tratado de Asunción, el Protocolo de Ouro Preto y las Resoluciones N 31/11 y 22/14 del Grupo Mercado Común.
Detección de IgE específica.
 Detección de IgE específica. Una forma de identificar los alérgenos responsables de los síntomas alérgicos es la detección de anticuerpos IgE específicos frente a dichos alérgenos. Estos anticuerpos están
Detección de IgE específica. Una forma de identificar los alérgenos responsables de los síntomas alérgicos es la detección de anticuerpos IgE específicos frente a dichos alérgenos. Estos anticuerpos están
EQUIPO PORTÁTIL PARA LA DETERMINACIÓN DE CLORO DISPONIBLE EN SOLUCIONES CONCENTRADAS DE HIPOCLORITO
 UNIDAD DE APOYO TÉCNICO PARA EL SANEAMIENTO BÁSICO DEL ÁREA RURAL EQUIPO PORTÁTIL PARA LA DETERMINACIÓN DE CLORO DISPONIBLE EN SOLUCIONES CONCENTRADAS DE HIPOCLORITO Centro Panamericano de Ingeniería Sanitaria
UNIDAD DE APOYO TÉCNICO PARA EL SANEAMIENTO BÁSICO DEL ÁREA RURAL EQUIPO PORTÁTIL PARA LA DETERMINACIÓN DE CLORO DISPONIBLE EN SOLUCIONES CONCENTRADAS DE HIPOCLORITO Centro Panamericano de Ingeniería Sanitaria
Reyes A.; Martín Luis M.B.; Batista E.; Martínez O.; Darias J.; Díaz Romero C.; Díaz Díaz M.E.; Pérez Trujillo J.P.
 ESTUDIO COMPARATIVO DE DIFERENTES MÉTODOS ANALÍTICOS PARA LA DETERMINACIÓN DE TRES PARÁMETROS DE INTERÉS ENOLÓGICO: GRADO ALCOHÓLICO, ACIDEZ VOLÁTIL Y DIÓXIDO DE AZUFRE LIBRE Y TOTAL Reyes A.; Martín Luis
ESTUDIO COMPARATIVO DE DIFERENTES MÉTODOS ANALÍTICOS PARA LA DETERMINACIÓN DE TRES PARÁMETROS DE INTERÉS ENOLÓGICO: GRADO ALCOHÓLICO, ACIDEZ VOLÁTIL Y DIÓXIDO DE AZUFRE LIBRE Y TOTAL Reyes A.; Martín Luis
PROCEDIMIENTO PARA LA UTILIZACIÓN DEL POLIMORFISMO DEL GEN COMT (CATECOL-OXI-METILTRANSFERASA) EN EL DIAGNÓSTICO DEL SÍNDROME DE FIBROMIALGIA
 2 PROCEDIMIENTO PARA LA UTILIZACIÓN DEL POLIMORFISMO DEL GEN COMT (CATECOL-OXI-METILTRANSFERASA) EN EL DIAGNÓSTICO DEL SÍNDROME DE FIBROMIALGIA D E S C R I P C I Ó N OBJETO DE LA INVENCIÓN La presente
2 PROCEDIMIENTO PARA LA UTILIZACIÓN DEL POLIMORFISMO DEL GEN COMT (CATECOL-OXI-METILTRANSFERASA) EN EL DIAGNÓSTICO DEL SÍNDROME DE FIBROMIALGIA D E S C R I P C I Ó N OBJETO DE LA INVENCIÓN La presente
TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR
 TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DOCENTES: Andrés Ciocchini, Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR Purificación de ácido desoxiribonucleico (ADN) por partición diferencial
TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DOCENTES: Andrés Ciocchini, Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR Purificación de ácido desoxiribonucleico (ADN) por partición diferencial
APLICACIÓN DE LA PCR: DIAGNÓSTICO DE PARÁSITOS
 Prácticas docentes en la COD: 10-71 APLICACIÓN DE LA PCR: DIAGNÓSTICO DE PARÁSITOS FUNDAMENTO TEÓRICO La PCR es una técnica que permite llevar a cabo la síntesis in vitro de fragmentos de ADN. Está basada
Prácticas docentes en la COD: 10-71 APLICACIÓN DE LA PCR: DIAGNÓSTICO DE PARÁSITOS FUNDAMENTO TEÓRICO La PCR es una técnica que permite llevar a cabo la síntesis in vitro de fragmentos de ADN. Está basada
Extracción sólido-líquido
 Extracción sólido-líquido Objetivos de la práctica! Determinar la concentración de saturación del soluto en el disolvente en un sistema ternario arena-azúcar-agua, estableciendo la zona operativa del diagrama
Extracción sólido-líquido Objetivos de la práctica! Determinar la concentración de saturación del soluto en el disolvente en un sistema ternario arena-azúcar-agua, estableciendo la zona operativa del diagrama
NMX-F-070-1964. MÉTODO DE PRUEBA PARA LA DETERMINACIÓN DE TIAMINA. THIAMINE DETERMINATION. TEST METHOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS.
 NMX-F-070-1964. MÉTODO DE PRUEBA PARA LA DETERMINACIÓN DE TIAMINA. THIAMINE DETERMINATION. TEST METHOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. ASUNTO Con fundamento en lo dispuesto en los Artículos
NMX-F-070-1964. MÉTODO DE PRUEBA PARA LA DETERMINACIÓN DE TIAMINA. THIAMINE DETERMINATION. TEST METHOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. ASUNTO Con fundamento en lo dispuesto en los Artículos
BIOLOGÍA GENERAL Y METODOLOGÍA DE LAS CIENCIAS TRABAJO PRÁCTICO Nº 2 GENÉTICA
 BIOLOGÍA GENERAL Y METODOLOGÍA DE LAS CIENCIAS TRABAJO PRÁCTICO Nº 2 GENÉTICA Objetivos: Diferenciar los niveles de organización y compactación del material genético. Comprender los principios básicos
BIOLOGÍA GENERAL Y METODOLOGÍA DE LAS CIENCIAS TRABAJO PRÁCTICO Nº 2 GENÉTICA Objetivos: Diferenciar los niveles de organización y compactación del material genético. Comprender los principios básicos
11.2-DISCUSIÓN Prueba rápida
 11.2-DISCUSIÓN Prueba rápida Como se observa en la tabla 9 del total de las embarazadas (62,214) a las que se les realizo la prueba rápida un 99.3%(61,808) de ellas dio como resultado no reactivo, tan
11.2-DISCUSIÓN Prueba rápida Como se observa en la tabla 9 del total de las embarazadas (62,214) a las que se les realizo la prueba rápida un 99.3%(61,808) de ellas dio como resultado no reactivo, tan
