El melanoma cutáneo es un tumor muy
|
|
|
- María Victoria Blázquez Guzmán
- hace 6 años
- Vistas:
Transcripción
1 1 Facultad de Medicina, Pontificia Universidad Católica de Chile. Santiago, Chile. 2 Departamento de Anatomía Patológica, Facultad de Medicina, Pontificia Universidad Católica de Chile. Santiago, Chile. 3 Departamento de Dermatología, Facultad de Medicina, Pontificia Universidad Católica de Chile. Santiago, Chile. 4 Departamento de Cirugía Oncológica, Facultad de Medicina, Pontificia Universidad Católica de Chile. Santiago, Chile. 5 Departamento de Oncología, Facultad de Medicina, Pontificia Universidad Católica de Chile. Santiago, Chile. 6 Unidad de Melanoma y Cáncer de Piel UC, Facultad de Medicina, Pontificia Universidad Católica de Chile. Santiago, Chile. a Alumno Recibido el 30 de julio de 2015, aceptado el 13 de abril de Correspondencia a: Dr. Pablo Uribe González Depto. de Dermatología Unidad de Melanoma y Cáncer de Piel UC. Facultad de Medicina Pontificia Universidad Católica de Chile. Av. Vicuña Mackenna 4686, primer piso. Macul, Santiago. Tel: Fax: puribeg@med.puc.cl Entendiendo las terapias actuales en melanoma metastásico Rocío Rodríguez 1,a, Angela Parra 1,a, Sergio González 2,5, Montserrat Molgó 3,6, Nicolás Droppelmann 4,6, Francisco Acevedo 5,6, JosÉ Peña 5, Pablo Uribe 3,6 Understanding current therapies in metastatic melanoma Cutaneous melanoma is a highly aggressive tumor developing from melanocytes, its incidence is increasing, and prognosis in advanced stages is daunting. New therapies have been approved during the recent years with unprecedented results, including inhibitors of MAPK/ERK pathway and immune checkpoint blockade (anti-cytotoxic T lymphocyte antigen-4 (CTLA-4) as ipilimumab, anti-programmed cell death protein 1 (PD-L1) as pembrolizumab and anti-programmed cell death protein 1 ligand (PD-L1), among many others). The aim of this paper is to review currently available metastatic melanoma therapies focusing mainly on new therapies that have demonstrated effectiveness, after several decades of little progress in the treatment of this disease. () Key words: CTLA-4 Antigen; Melanoma; Molecular Targeted Therapy; Pembrolizumab; Programmed Cell Death 1 Receptor. CTLA-4: Antígeno 4 del linfocito T citotóxico DTIC: Dimetil Triazeno Imidazol Carboxamida EGFR: Receptor del factor de crecimiento epidérmico ERK: Quinasa regulada por señal extracelular FDA: Administración de drogas y alimentos LT: Linfocito T MAPK: Proteína quinasa activada por mitógenos PD1: Proteína de muerte celular programada PDL-1: Ligando proteína de muerte celular programada RR: Riesgo relativo SLP: Sobrevida libre de progresión SG: Sobrevida global TCR: Receptor de linfocito T El melanoma cutáneo es un tumor muy agresivo desarrollado a partir de melanocitos. Representa aproximadamente el 75% de las muertes relacionadas al cáncer de piel 1 y su incidencia está en aumento, con casos nuevos estimados para 2015 en Estados Unidos 2. En Chile, para los años , se estimó una tasa de incidencia de 2,7 (hombres) y 2,2 (mujeres) por habitantes; la tasa de mortalidad se estimó para el año 2012 en 0,7 por ,4. El pronóstico de melanoma depende de varios factores, entre ellos espesor tumoral de Breslow, ulceración, mitosis, compromiso de linfonodos regionales y metástasis a distancia, variables consideradas en la clasificación TNM 5. En etapas iniciales tiene una sobrevida a 5 años de 98%, en cambio en pacientes con melanoma metastásico la sobrevida a 5 años es solo 16% 6. El pilar del manejo del melanoma cutáneo localizado es la cirugía, que cura a la mayoría de los pacientes, pero un porcen- 1448
2 Terapias actuales en melanoma metastásico - R. Rodríguez et al ARTÍCULO DE REVISIÓN Tabla 1. Terapias actuales en el tratamiento de melanoma metastásico Grupo Farmacológico Comentarios por grupo farmacológico 1. Quimioterapia 2. Inhibidores Farmacológicos de vías moleculares Medicamentos de uso oral Inhibidores de BRAF (BRAFi): Requieren mutaciones BRAF - Vemurafenib (Zelboraf, Roche, FDA 2012) Respuesta rápida antitumoral - Dabrafenib (Tafinlar, GSK, FDA 2013) Resistencia Inhibidores de MEK (MEKi): - Trametinib (Mekinist, GSK, FDA 2013) - Cobimetinib (Cotellic, Roche, FDA 2015) Combinación BRAFi+ MEKi - Dabrafenib + Trametinib (FDA 2014) - Vemurafenib + Cobimetinib (FDA 2015) 3. Inhibidores de puntos de control inmune Anticuerpos Monoclonales Anti CTLA-4: Uso endovenosos c/2-4 sem - Ipilimumab (Yervoy, BMS, FDA 2011) No requieren mutaciones BRAF Anti PD-1: Respuesta más lenta (excepto combinación) - Nivolumab (Opdivo, BMS, FDA 2014) Prolongada - Pembrolizumab (Keytruda, Merck, FDA 2014) Combinación anti CTL4 + anti PD1 - Ipilimumab + Nivolumab (FDA 2015) taje no despreciable desarrollará eventualmente enfermedad irresecable o metástasis 7. Tradicionalmente, en etapas metastásicas, el melanoma es raramente curable. Las nuevas aproximaciones terapéuticas han demostrado beneficios clínicos, principalmente inhibidores de vías moleculares e inhibidores de puntos de control inmune, que hoy están desplazando a la quimioterapia citotóxica como principal herramienta terapéutica para el melanoma metastásico. A continuación revisaremos las terapias de uso actual en melanoma metastásico (Tabla 1), centrándonos en los nuevos tratamientos que han resultado eficaces luego de varias décadas de escaso progreso en el tratamiento de esta enfermedad. Quimioterapia El primer hito en el tratamiento del melanoma avanzado ocurrió en 1975, cuando la dacarbazina (DTIC) fue aprobada por FDA. Agente citostático alquilante que se asocia a tasas de respuesta modestas (12%), y no se ha comparado con placebo, por lo que no hubiese sido aprobada por la FDA bajo los estándares actuales 8. DTIC -y su prodroga temozolomida- han sido los agentes quimioterapéuticos estándares en el tratamiento del melanoma, por lo que son el punto de comparación para muchas de las terapias recién desarrolladas 9. Aunque otros agentes han mostrado actividad en melanoma metastásico (ej. cisplatino, taxanos), ninguno logró reemplazar a DTIC 10,11. Asimismo, el uso de combinaciones de quimioterapia citotóxica, si bien se asocia a mayor respuesta, es más tóxica y no impacta en la sobrevida 12,13. Esto se debe a la alta tasa de quimiorresistencia del melanoma por alteración en transportadores que provocan eflujo de las drogas, desintoxicación aumentada, mutación de topoisomerasa y particularmente por mayor resistencia a la apoptosis Actualmente en el manejo inicial de los pacientes con melanoma metastásico, se prefiere el uso de otros agentes 18 como mencionaremos a continuación. 1449
3 Terapias actuales en melanoma metastásico - R. Rodríguez et al Inhibidores farmacológicos de vías moleculares: inhibidores de vía MAPK ERK Las neoplasias se originan por la acumulación de alteraciones en la función de genes críticos, que alteran la regulación de la proliferación, diferenciación y muerte celular entregando ventaja de crecimiento en comparación con otras poblaciones celulares 19,20. La vía de señalización MAPK RAS/ RAF/MEK/ERK es esencial en procesos celulares fundamentales, como proliferación, diferenciación, migración y apoptosis de los melanocitos 21. Esta vía se encuentra activada por variados mecanismos en melanoma, siendo lo más frecuente la mutación BRAF. El bloqueo de esta vía de señalización mediante la unión selectiva a alguna de las proteínas quinasa de la cascada MAPK/ERK lleva a la inhibición de su fosforilación y de su translocación al núcleo de fosfo-erk, reduciéndose las transcripción de genes importantes en aumento de sobrevida celular, angiogénesis y reducción de la apoptosis, por lo que se ha convertido en un objetivo terapéutico primordial en melanoma metastásico (Figura 1). a) Inhibidores de BRAF (BRAFi) Mutaciones activantes de BRAF están presentes en aproximadamente un 50-60% de los melanomas avanzados, especialmente ubicados en áreas no fotoexpuestas crónicamente 22,23. Más del 70% de las mutaciones en BRAF son V600E (reemplaza valina por ácido glutámico en el aminoácido 600) y entre 10-30% son V600K (valina por lisina) 24. Estas mutaciones determinan una Figura 1. Varios oncogenes y vías moleculares son objetivo de las nuevas terapias en melanoma. La vía con mayor frecuencia alterada es MAPK RAS/RAF/MEK/ERK que controla procesos celulares como crecimiento, diferenciación y apoptosis; 50-60% de los melanomas cutáneos tienen mutaciones activantes de BRAF y % mutaciones en RAS, este último también activa la vía PI3K/PTEN/AKT que controla la proliferación celular. Esta segunda vía en 40-60% de los melanomas interrumpe la expresión anormal de PTEN, cuya expresión aberrante también resulta en aumento de los niveles de AKT activado. La tercera vía de oncogenes clásica en melanoma es c-kit que activa las vías MAPK y PI3K/AKT descritas anteriormente. En la figura se muestran también drogas que bloquean un determinado componente de las vías, por ejemplo BRAF o MAPK. 1450
4 Terapias actuales en melanoma metastásico - R. Rodríguez et al ARTÍCULO DE REVISIÓN activación permanente de la señalización de la vía MAPK, siendo tumorogénicas in vitro e in vivo y un blanco terapéutico en melanoma. Inicialmente se utilizaron BRAFi no selectivos, como sorafenib, demostrándose bajas tasas de respuesta 25,26. Afortunadamente, la capacidad para detectar mutaciones de BRAF en material histopatológico y la disponibilidad de inhibidores específicos de BRAF mutado han cambiado el manejo de pacientes con melanoma 27. Vemurafenib (Zelboraf ) y dabrafenib (Tafinlar ) son inhibidores orales específicos con alta actividad contra BRAF V600E y V600K, y actividad variable ante otras mutaciones de BRAF (Tabla 1). Actúan uniéndose al sitio de unión del ATP de B-Raf mutado, inhibiendo la forma activa de la quinasa. Estos medicamentos mostraron excelentes resultados en estudios fase III en pacientes con melanoma irresecable o metastásico Se estima que la tasa de respuesta completa a ambos agentes es del 50-60%, con una sobrevida libre de progresión (SLP) de 7 meses, llevando la sobrevida global (SG) a meses. Estos resultados favorables también se han visto en pacientes con peor pronóstico (etapa M1c o altos niveles de LDH) 28, incluso en aquellos con metástasis cerebrales 30. Lamentablemente, todos desarrollarán resistencia al tratamiento 32 debido a mecanismos que incluyen alteraciones en proteínas que conforman las vías de las MAPK como mutaciones de NRAS, amplificación de BRAF, expresión de variantes truncas de la proteína, aumento de niveles de CRAS 33, activación de receptores tirosina quinasa y activación o mutación de MEK 34,35, justificándose el uso de inhibidores de MEK (ver más adelante). También está descrita la activación de otras vías de señalización, como PI3K-AKT 36. Los BRAFi se asocian a algunos efectos adversos, lo que se explica en parte por activación paradójica de la vía MAPK en células normales (ej. queratinocito), resultando en queratoderma plantar, queratosis pilaris, queratosis verrucosas y carcinoma escamoso tipo queratoacantoma (19-26%) 28. Estas lesiones aparecen pocas semanas después de iniciado el tratamiento y no determinan su interrupción 37,38. También se observan modificaciones en lesiones pigmentadas; cambios en color, tamaño, erupción de múltiples nevos y aparición de nuevos melanomas primarios 39,40. Otro efecto adverso relevante es fotosensibilidad a UVA, que sólo ocurre con vemurafenib 41,42. b) Inhibidores de MEK (MEKi) MEK es un componente de la vía MAPK que se encuentra río abajo de la vía de BRAF, disponiéndose actualmente de 2 inhibidores selectivos de MEK1/2: trametinib y cobimetinib 28. Trametinib (Mekinist ) fue aprobado por FDA el 2013 como tratamiento de primera línea en pacientes con melanoma metastásico con mutaciones BRAF V600E y V600K. Según el estudio en fase III la SLP es de 4,8 meses para trametinib comparado con 1,5 meses con quimioterapia, mejorando la SG en 14% a 6 meses 43. Cobimetinib (Cotellic ), fue aprobado recientemente para ser utilizado en combinación con vemurafenib (ver más adelante) 44,45. En un 87% de los pacientes que utilizan MEKi se observan efectos adversos cutáneos, similares a los inducidos por inhibidores de EGFR, especialmente erupción acneiforme, xerosis, paroniquia y fisuras acrales La frecuencia de carcinoma escamoso cutáneo no aumenta 43. Otros efectos adversos incluyen diarrea, edema periférico, fatiga, náuseas y más raramente disfunción ventricular, problemas visuales y enfermedad pulmonar intersticial 9. c) Terapia combinada Dabrafenib (BRAFi) + trametinib (MEKi) En un esfuerzo por retrasar el desarrollo de resistencia al tratamiento (que ocurre 6 a 7 meses de iniciada la terapia) 31 y minimizar la toxicidad asociada a la inhibición de BRAF, se estudió el uso combinado de dabrafenib y trametinib, aprobándose por la FDA en 2014 como terapia inicial en pacientes cuyo melanoma contiene la mutación BRAF V600E o V600K. Esta aprobación extendida se basa en estudios fase I/II donde mejoró la SLP, de 5,8 meses para dabrafenib como agente único versus 9,8 meses en terapia combinada. Vemurafenib (BRAFi) + cobimetinib (MEKi) La terapia combinada aumenta la SLP a 11,3 meses comparada con 7,3 meses con vemurafenib, y SG a 12 meses de 72% y 65%, respectivamente 49,50. Esta combinación fue aprobada por FDA el 2015 para pacientes con melanoma irresecable o metastásico con mutación en BRAF V600E o V600K. El uso de terapia combinada disminuye los efectos adversos cutáneos en comparación con la monoterapia, debido a la reducción de la activa- 1451
5 Terapias actuales en melanoma metastásico - R. Rodríguez et al ción paradójica de la vía MAPK. Esta activación ocurre en células que no presentan la mutación de BRAF, por ejemplo, queratinocitos normotípicos, queratinocitos con displasia, nevos melanocíticos, etc. Se produce por la unión de BRAFi a la proteína BRAF nativa, permitiendo la dimerización con otra proteína (CRAF) y siendo este complejo el que activa paradójicamente la vía MAPK. La adición de un MEKi (ej: trametinib) a un BRAFi (ej: dabrafenib), bloquea la activacion paradójica, reduciendo el desarrollo de lesiones cutáneas hiperproliferativas, tales como carcinoma de células escamosas (1% en terapia combinada versus 18% en monoterapia con dabrafenib), queratosis verrucosas (2% versus 23%), queratodermia (4% versus 25%) y teóricamente también disminuye la posibilidad de segundas neoplasias secundarias a la activación paradójica de MAPK. También existe una reducción notable de la frecuencia de erupciones acneiformes 46,47,51, pero un incremento en la frecuencia y severidad de fiebre secundaria al tratamiento. Inhibidores de puntos de control inmune El melanoma posee una alta capacidad inmunogénica y la respuesta inmune del paciente puede influir en su historia natural. Esto se refleja en los fenómenos de regresión de las lesiones primarias, la respuesta a citoquinas como IL2 y la mayor incidencia de melanoma en pacientes inmunosuprimidos. Para estimular ésta respuesta inmune se han desarrollado vacunas, pero sus resultados son variables, no logrando aún demostrar beneficio en sobrevida por lo que son consideradas aún en experimentación. En Chile se desarrolló TAPCells, que logró inducir una respuesta antitumoral efectiva en estudios fase I/II; faltan estudios fase III para definir el impacto y la utilidad clínica de esta terapia 52,53. El problema en melanoma es que a pesar de la generación de una respuesta inmune, no se logra una actividad anti tumoral adecuada, debido a mecanismos que se describen a continuación. La respuesta inmune celular se desarrolla luego que un determinado antígeno, por ejemplo un antígeno asociado al tumor (AAT), es presentado por una célula presentadora de antígenos (CPA) a un linfocito T (LT). Esta sinapsis inmunológica es compleja y en ella existen varias señales activadoras/represoras complementarias (Figura 2A). Inicialmente, la CPA (ej. célula de Langerhans) procesa el antígeno y lo expone en su superficie mediante el complejo mayor de histocompatibilidad II (MHC-II), siendo reconocido por el LT, a través de su receptor TCR (señal 1). La segunda señal puede ser coactivadora o coinhibitoria. La señal coactivadora ocurre cuando B7 (receptor en CPA, también llamado CD80/CD86) se une a CD28 (LT); en esas condiciones el LT se activa, prolifera, madura y circula en la periferia, donde eventualmente se encontrará con el antígeno que le fue presentado, y ejercerá su efecto. Por el contrario, como medida para proteger las células sanas, minimizando la activación no específica de LT y el desarrollo de autoinmunidad, existe coinhibición a través de la unión de B7 a CTLA-4 (antígeno 4 del linfocito T citotóxico, expresado en células T activadas), impidiendo la interacción CD28-B7 e inhibibiendo la activación de LT. Además, CTL-4 produce activación los LT regulatorios, involucrados en la tolerancia inmunológica. En melanoma hay un estado anérgico con una mayor expresión de CTLA-4 (señal co-inhibitoria), como forma de evadir la activación de células T antitumorales (Figura 2A). Por otro lado, se ha descubierto otro mecanismo inhibidor de la respuesta inmune antitumoral, a nivel periférico, en la interacción del LT efector y la célula tumoral: las células cancerosas expresan constitutivamente ligandos, por ejemplo PD-L1, que al unirse a su receptor (PD-1, proteína de muerte celular programada) disminuye la activación del LT efector (Figura 2B) 54. Actualmente, hay estrategias inmunoterapéuticas que bloquean CTLA-4 y PD-1 ( checkpoints del sistema inmune), mediante anticuerpos monoclonales, restableciendo y potenciando mecanismos antitumorales del sistema inmune a expensas de un aumento en la incidencia de fenómenos autoinmunes. a) Anti CTLA-4: ipilimumab y tramelimumab Ipilimumab (Yervoy ) es un anticuerpo monoclonal humanizado con alta afinidad a CTLA-4 (Figura 2A). Aprobado en 2011 por FDA, luego de un estudio fase III que demostró, RR de 10,9%, control de enfermedad (pacientes con respuesta parcial, completa o enfermedad estable) de 28,5% 55 y SG de 23,5% a los 24 meses en pacientes con tratamiento previo. Por primera vez un 1452
6 Terapias actuales en melanoma metastásico - R. Rodríguez et al ARTÍCULO DE REVISIÓN estudio clínico fue capaz de demostrar beneficio en sobrevida global en pacientes con melanoma metástasico. Este beneficio fue independiente de la etapa, LDH basal o uso previo de IL2. Se han buscado marcadores de respuesta que permitan identificar los pacientes que se beneficiarán del tratamiento con ipilimumab; sin embargo, ninguno se encuentra validado y en uso clínico 56,57. Un aspecto importante del tratamiento con Ipilimumab es que puede producir patrones de respuesta que no se observan al usar agentes citotóxicos y que han sido definidos en los Criterios de Respuesta relacionados a la Inmunidad ( Immunerelated response criteria ). Los patrones son: a) respuesta en lesiones medibles a la semana 12 de tratamiento, sin aparición de nuevas lesiones; b) enfermedad estable (en algunos pacientes seguida de lenta disminución del tamaño tumoral); c) aumento inicial de tamaño tumoral, seguido de respuesta; d) Reducción en carga tumoral total, ya sea durante o después de la aparición de nuevas lesiones, después de la semana Un 10-15% de los pacientes en tratamiento con Ipilimumab sufren efectos adversos grado 3 o 4. En su mayoría autoinmunes y se manifiestan como colitis, hepatitis, hipofisitis y manifestaciones dermatológicas como prurito y rash (maculopapulares y liquenoides) 59,60. b) Anticuerpos monoclonales Anti PD-1: Nivolumab, Pembrolizumab Nivolumab (Opdivo ). Aprobado el 2014 por FDA para pacientes previamente tratados con Ipilimumab o BRAFi (Figura 2B), y recientemente como primera línea en pacientes con melanoma avanzado o metastásico sin mutación de BRAF. Un estudio de fase III realizado en pacientes con melanoma sin tratamiento previo y sin mutación BRAF evidenció RR de 40% y OS a 1 año de 72,9% con nivolumab, lo cual se comparó contra DTIC, que logró 13,9% y 42,1%, respectivamente 61. La continuación de este estudio mostró SG con nivolumab de 57,7%, SLP media de 5,4 meses versus SG de 26,7% y SLP de 2,2 meses con DTIC. Respuesta completa de 11% de los pacientes con nivolumab y 1% con DTIC 62. Por otro lado, nivolumab fue comparado con quimioterapia en pacientes con melanoma avanzado que progresaron luego de tratamiento con ipilimumab o ipilimumab y un inhibidor de BRAF en casos de mutación de este último; se vio mejor RR (31,7% vs 10,6%) y menos efectos adversos grado 3 o 4 (5 vs 9%) con el uso de nivolumab 63. Pembrolizumab (Keytruda ). Aprobado en 2014 por FDA para pacientes con fracaso al tratamiento con ipilimumab o un BRAFi, en casos de BRAF mutado y recién aprobado como tratamiento de primera línea en pacientes con melanoma avanzado no tratado, independiente de mutación BRAF; logra RR de 38 a 52%, la mayoría de estas respuestas son duraderas y no varían si hay exposición previa a ipilimumab 64. Pembrolizumab fue comparado con Ipilimumab, en primera línea de tratamiento, en un estudio fase III; logró mejor RR (33% vs 11,9%), SLP a 6 meses (47% versus 26,5%) y OS (74%-68% versus 58% en 12 meses). Con ambos tratamientos las respuestas fueron duraderas (alrededor de 90% con una mediana de seguimiento de 7,9 meses), pero pembrolizumab tuvo menos efectos adversos grado 3 a Estos resultados favorables ocurren independiente del estado funcional, nivel de LDH, mutación BRAF, etapa TNM y número o tipos de tratamientos previos 66. En general, el tratamiento con antipd-1 es bien tolerado, con efectos adversos leves como fatiga, náuseas, diarrea y prurito; y algunos de naturaleza autoinmune como vitíligo (10%) y rash no especifico (15%). En menos del 2% de los casos se presentan efectos adversos grado 3 y 4 como trastornos tiroideos, colitis, hipofisitis, hepatitis y neumonitis 61,63. c) Anticuerpos anti PD-L1. Están en investigación, aún no aprobados por FDA al momento de la revisión. Los más importantes, BMS y MPDL3280A, han mostrado RR de 17% y 26% en estudios preliminares d) Combinación de tratamientos. Ipilimumab (Anti CTLA-4) + nivolumab (anti PD-1) Aprobado por FDA el 2015 para pacientes con melanoma no resecable o metastásico y sin mutaciones de BRAF. Estudios de fase II/III muestran que esta combinación tiene mayor actividad antitumoral en comparación a la monoterapia con Ipilimumab, con RR de 61% versus 11% 70 y SLP significativamente mayor, independiente del estado mutacional de BRAF; 11,5 meses con el tratamiento combinado, 2,9 meses con ipilimumab y 6,9 meses con nivolumab 71. Es destacable que hubo 11,5 a 22% de respuesta completa en el grupo con 1453
7 Terapias actuales en melanoma metastásico - R. Rodríguez et al Figura 2. (A) Para la activación del LT la CPA mediante MHC-II, presenta el antígeno al linfocito T que lo reconoce a través de TCR (señal 1), y el receptor de la célula presentadora CD80/86 se une al receptor CD28 del linfocito T (señal 2). Luego de este proceso se expresa CTLA-4 en la superficie del linfocito T que se une con mayor afinidad a CD80/86 y produce una inhibición de la actividad del linfocito T, resultando en menor actividad antitumoral en melanoma. La inmunoterapia actualmente dispone antictla-4 se une al receptor respectivo en el linfocito T e impide su unión a CD80/86 restaurando la activación de esta célula y permitiendo su acción antitumoral con resultados alentadores. (B) Células de melanoma expresan constitutivamente PD-1 que al unirse a su receptor PD-L1 presente en linfocitos T efectores, regulan de forma negativa la acción de esta célula, por lo que anticuerpos desarrollados contra estos blancos, hoy disponibles, permiten mejorar la respuesta autoinmune antitumoral. MHCII: complejo mayor de histocompatibilidad II; LT: linfocito T, CPA: Célula presentadora de antígenos; TCR: Receptor de linfocito T; CTLA-4: antígeno 4 del linfocito T citotóxico; PD1: proteína de muerte celular programada; PDL1: ligando de proteína de muerte celular programada. 1454
8 Terapias actuales en melanoma metastásico - R. Rodríguez et al ARTÍCULO DE REVISIÓN terapia combinada, 8,9% con nivolumab y sólo 2,2% con ipilimumab. En relación a la sobrevida se ha objetivado con la terapia combinada valores de 85% a 1 año y 79% a 2 años 72. La toxicidad es manejable, pero se observaron mayores efectos adversos grado 3 y 4 en el tratamiento combinado (54% vs 24%) destacando colitis y elevación de alanina aminotransferasa, entre otros 70,71,73. Estrategias de tratamiento en pacientes con melanoma metastásico Están evolucionando constantemente y actualmente el esquema de tratamiento apunta a ser personalizado, dependiendo principalmente de 3 características 74 : 1. Paciente, sus comorbilidades y estado funcional. 2. Las metástasis, su cantidad, ubicación, resecabilidad y síntomatología. 3. Mutaciones genéticas conocidas ( estado mutacional ): BRAF mutado u otras mutaciones. En pacientes con un número limitado de metástasis, estables y potencialmente resecables, se debe considerar la metastasectomía, la que ha mostrado tasas de sobrevida a 5 años de hasta 40% 75. En caso de lesiones irresecables o mayor número de metástasis, se recomienda iniciar terapias sistémicas y para decidir cual utilizar se debe determinar el estado funcional del paciente y estudiar presencia de mutaciones BRAF. Si no hay mutaciones conocidas o el paciente tiene mutaciones asociadas a buen estado funcional, se debe considerar utilizar monoterapia con antipd-1 o combinación anti-pd1 e ipilimumab. Si el estudio mutacional es positivo pero hay pobre capacidad funcional y/o alta carga metastásica, o si la enfermedad progresa a pesar de la inmunoterapia, se recomienda iniciar terapia molecular combinada: BRAFi+ MEKi 74. Conclusiones El conocimiento de la biología molecular del melanoma y el desarrollo de inhibidores de vías moleculares e inmunoterapia han revolucionado el tratamiento del melanoma metastásico. En comparación con la terapia citotóxica, estos fármacos logran mejorar las tasas de respuesta, sobrevida libre de progresión y sobrevida global, con perfiles de toxicidad aceptables, pero aún con un alto costo. En el futuro, algunos biomarcadores predicirán la respuesta a estos tratamientos, mejorando la relación costo-beneficio de estos medicamentos. Actualmente, se están realizando múltiples ensayos clínicos usando combinación de estos tratamientos, siendo algunas altamente efectivas y se estima que en algunos años un subgrupo de pacientes con melanoma metastásico se comportará como portadores de una enfermedad crónica. Referencias 1. Olszanski AJ. Current and future roles of targeted therapy and immunotherapy in advanced melanoma. J Manag Care Pharm 2014; 20 (4): Siegel RL, Miller KD, Jemal A. Cancer statistics, CA Cancer J Clin 2015; 65 (1): Minsal, Unidad de Vigilancia de Enfermedades No transmisibles y Estudios, Departamento de Epidemiología, División de Planificación Sanitaria Subsecretaría de Salud Pública. Primer Informe de Registros Poblacionales de Cáncer de Chile, quinquenio Disponible en: epi.minsal.cl [Consultado el 11 de Mayo de 2015]. 4. GLOBOCAN International Agency for Research on Cancer. World Health Organization. Estimated cancer Incidence, mortality and prevalence Worldwide in 2012, Disponible en: [Consultado 11 de Mayo de 2015]. 5. Balch CM, Gershenwald JE, Soong SJ, Thompson JF, Atkins MB, Byrd DR, et al. Final version of 2009 AJCC melanoma staging and classification. J Clin Oncol 2009; 27 (36): AmericanCancerSociety. Cancer Facts & Figures (Society AC, ed). Atlanta Romano E, Scordo M, Dusza SW, Coit DG, Chapman PB. Site and timing of first relapse in stage III melanoma patients: implications for follow-up guidelines. J Clin Oncol 2010; 28 (18): Middleton MR, Grob JJ, Aaronson N, Fierlbeck G, Tilgen W, Seiter S, et al. Randomized phase III study of temozolomide versus dacarbazine in the treatment of patients with advanced metastatic malignant melanoma. J Clin Oncol 2000; 18 (1): Shah DJ, Dronca RS. Latest advances in chemotherapeutic, targeted, and immune approaches in the treatment 1455
9 Terapias actuales en melanoma metastásico - R. Rodríguez et al of metastatic melanoma. Mayo Clin Proc 2014; 89 (4): Anderson CM, Buzaid AC, Legha SS. Systemic treatments for advanced cutaneous melanoma. Oncology (Williston Park) 1995; 9 (11): ; discussion 63-4, Mays SR, Nelson BR. Current therapy of cutaneous melanoma. Cutis 1999; 63 (5): Chapman PB, Einhorn LH, Meyers ML, Saxman S, Destro AN, Panageas KS, et al. Phase III multicenter randomized trial of the Dartmouth regimen versus dacarbazine in patients with metastatic melanoma. J Clin Oncol 1999; 17 (9): Eigentler TK, Caroli UM, Radny P, Garbe C. Palliative therapy of disseminated malignant melanoma: a systematic review of 41 randomised clinical trials. Lancet Oncol 2003; 4 (12): Rockmann H, Schadendorf D. Drug resistance in human melanoma: mechanisms and therapeutic opportunities. Onkologie 2003; 26 (6): Grossman D, Altieri DC. Drug resistance in melanoma: mechanisms, apoptosis, and new potential therapeutic targets. Cancer Metastasis Rev 2001; 20 (1-2): La Porta CA. Drug resistance in melanoma: new perspectives. Curr Med Chem 2007; 14 (4): Stahl JM, Cheung M, Sharma A, Trivedi NR, Shanmugam S, Robertson GP. Loss of PTEN promotes tumor development in malignant melanoma. Cancer Res 2003; 63 (11): Sosman J. Cytotoxic chemotherapy for metastatic melanoma. En: UpToDate Davies H, Bignell GR, Cox C, Stephens P, Edkins S, Clegg S, et al. Mutations of the BRAF gene in human cancer. Nature 2002; 417 (6892): Millington GW. Mutations of the BRAF gene in human cancer, by Davies, et al. (Nature 2002; 417: ). Clin Exp Dermatol 2013; 38 (2): Dhillon AS, Hagan S, Rath O, Kolch W. MAP kinase signalling pathways in cancer. Oncogene 2007; 26 (22): Long GV, Menzies AM, Nagrial AM, Haydu LE, Hamilton AL, Mann GJ, et al. Prognostic and clinicopathologic associations of oncogenic BRAF in metastatic melanoma. J Clin Oncol 2011; 29 (10): Wellbrock C, Hurlstone A. BRAF as therapeutic target in melanoma. Biochem Pharmacol 2010; 80 (5): Klein O, Clements A, Menzies AM, O Toole S, Kefford RF, Long GV. BRAF inhibitor activity in V600R metastatic melanoma. Eur J Cancer 2013; 49 (5): Eisen T, Ahmad T, Flaherty KT, Gore M, Kaye S, Marais R, et al. Sorafenib in advanced melanoma: a Phase II randomised discontinuation trial analysis. Br J Cancer 2006; 95 (5): Kirkwood JM, Bastholt L, Robert C, Sosman J, Larkin J, Hersey P, et al. Phase II, open-label, randomized trial of the MEK1/2 inhibitor selumetinib as monotherapy versus temozolomide in patients with advanced melanoma. Clin Cancer Res 2012; 18 (2): Kaufman HL. Melanoma as a model for precision medicine in oncology. Lancet Oncol 2014; 15 (3): Chapman PB, Hauschild A, Robert C, Haanen JB, Ascierto P, Larkin J, et al. Improved survival with vemurafenib in melanoma with BRAF V600E mutation. N Engl J Med 2011; 364 (26): Sosman JA, Kim KB, Schuchter L, Gonzalez R, Pavlick AC, Weber JS, et al. Survival in BRAF V600-mutant advanced melanoma treated with vemurafenib. N Engl J Med 2012; 366 (8): Falchook GS, Long GV, Kurzrock R, Kim KB, Arkenau TH, Brown MP, et al. Dabrafenib in patients with melanoma, untreated brain metastases, and other solid tumours: a phase 1 dose-escalation trial. Lancet 2012; 379 (9829): Hauschild A, Grob JJ, Demidov LV, Jouary T, Gutzmer R, Millward M, et al. Dabrafenib in BRAF-mutated metastatic melanoma: a multicentre, open-label, phase 3 randomised controlled trial. Lancet 2012; 380 (9839): Ma XH, Piao SF, Dey S, McAfee Q, Karakousis G, Villanueva J, et al. Targeting ER stress-induced autophagy overcomes BRAF inhibitor resistance in melanoma. J Clin Invest 2014; 124 (3): Montagut C, Sharma SV, Shioda T, McDermott U, Ulman M, Ulkus LE, et al. Elevated CRAF as a potential mechanism of acquired resistance to BRAF inhibition in melanoma. Cancer Res 2008; 68 (12): Van Allen EM, Wagle N, Sucker A, Treacy DJ, Johannessen CM, Goetz EM, et al. The genetic landscape of clinical resistance to RAF inhibition in metastatic melanoma. Cancer Discov 2014; 4 (1): Rizos H, Menzies AM, Pupo GM, Carlino MS, Fung C, Hyman J, et al. BRAF inhibitor resistance mechanisms in metastatic melanoma: spectrum and clinical impact. Clin Cancer Res 2014; 20 (7): McArthur GA, Ribas A. Targeting oncogenic drivers and the immune system in melanoma. J Clin Oncol 2013; 31 (4): Anforth R, Fernandez-Penas P, Long GV. Cutaneous toxicities of RAF inhibitors. Lancet Oncol 2013; 14 (1): e Boyd KP, Vincent B, Andea A, Conry RM, Hughey LC. Nonmalignant cutaneous findings associated with 1456
10 Terapias actuales en melanoma metastásico - R. Rodríguez et al ARTÍCULO DE REVISIÓN vemurafenib use in patients with metastatic melanoma. J Am Acad Dermatol 2012; 67 (6): Dalle S, Poulalhon N, Thomas L. Vemurafenib in melanoma with BRAF V600E mutation. N Engl J Med 2011; 365 (15): ; author reply Zimmer L, Hillen U, Livingstone E, Lacouture ME, Busam K, Carvajal RD, et al. Atypical melanocytic proliferations and new primary melanomas in patients with advanced melanoma undergoing selective BRAF inhibition. J Clin Oncol 2012; 30 (19): Larkin J, Del Vecchio M, Ascierto PA, Krajsova I, Schachter J, Neyns B, et al. Vemurafenib in patients with BRAF(V600) mutated metastatic melanoma: an open-label, multicentre, safety study. Lancet Oncol 2014; 15 (4): Sosman J. Molecularly targeted therapy for metastatic melanoma. En: UpToDate Flaherty KT, Robert C, Hersey P, Nathan P, Garbe C, Milhem M, et al. Improved survival with MEK inhibition in BRAF-mutated melanoma. N Engl J Med 2012; 367 (2): Larkin J, Ascierto PA, Dreno B, Atkinson V, Liszkay G, Maio M, et al. Combined vemurafenib and cobimetinib in BRAF-mutated melanoma. N Engl J Med 2014; 371 (20): Ribas A, Gonzalez R, Pavlick A, Hamid O, Gajewski TF, Daud A, et al. Combination of vemurafenib and cobimetinib in patients with advanced BRAF(V600)-mutated melanoma: a phase 1b study. Lancet Oncol 2014; 15 (9): Anforth R, Liu M, Nguyen B, Uribe P, Kefford R, Clements A, et al. Acneiform eruptions: a common cutaneous toxicity of the MEK inhibitor trametinib. Australas J Dermatol 2014; 55 (4): Uribe P, Anforth RM, Kefford RF, Fernandez-Penas P. Acneiform eruption in a patient with metastatic melanoma after ceasing combination dabrafenib/trametinib therapy. Melanoma Res 2014; 24 (5): Infante JR, Fecher LA, Falchook GS, Nallapareddy S, Gordon MS, Becerra C, et al. Safety, pharmacokinetic, pharmacodynamic, and efficacy data for the oral MEK inhibitor trametinib: a phase 1 dose-escalation trial. Lancet Oncol 2012; 13 (8): Long GV, Stroyakovskiy D, Gogas H, Levchenko E, de Braud F, Larkin J, et al. Combined BRAF and MEK inhibition versus BRAF inhibition alone in melanoma. N Engl J Med 2014; 371 (20): Robert C, Karaszewska B, Schachter J, Rutkowski P, Mackiewicz A, Stroiakovski D, et al. Improved overall survival in melanoma with combined dabrafenib and trametinib. N Engl J Med 2015; 372 (1): Flaherty KT, Infante JR, Daud A, Gonzalez R, Kefford RF, Sosman J, et al. Combined BRAF and MEK inhibition in melanoma with BRAF V600 mutations. N Engl J Med 2012; 367 (18): Lopez MN, Pereda C, Segal G, Muñoz L, Aguilera R, Gonzalez FE, et al. Prolonged survival of dendritic cell-vaccinated melanoma patients correlates with tumor-specific delayed type IV hypersensitivity response and reduction of tumor growth factor beta-expressing T cells. J Clin Oncol 2009; 27(6): Blanchard T, Srivastava PK, Duan F. Vaccines against advanced melanoma. Clin Dermatol 2013; 31(2): Topalian SL, Hodi FS, Brahmer JR, Gettinger SN, Smith DC, McDermott DF, et al. Safety, activity, and immune correlates of anti-pd-1 antibody in cancer. N Engl J Med 2012; 366 (26): Hodi FS, O Day SJ, McDermott DF, Weber RW, Sosman JA, Haanen JB, et al. Improved survival with ipilimumab in patients with metastatic melanoma. N Engl J Med 2010; 363 (8): Hamid O, Schmidt H, Nissan A, Ridolfi L, Aamdal S, Hansson J, et al. A prospective phase II trial exploring the association between tumor microenvironment biomarkers and clinical activity of ipilimumab in advanced melanoma. J Transl Med 2011; 9: Ascierto PA, Kalos M, Schaer DA, Callahan MK, Wolchok JD. Biomarkers for immunostimulatory monoclonal antibodies in combination strategies for melanoma and other tumor types. Clin Cancer Res 2013; 19 (5): Wolchok JD, Hoos A, O Day S, Weber JS, Hamid O, Lebbe C, et al. Guidelines for the evaluation of immune therapy activity in solid tumors: immune-related response criteria. Clin Cancer Res 2009; 15 (23): Di Giacomo AM, Biagioli M, Maio M. The emerging toxicity profiles of anti-ctla-4 antibodies across clinical indications. Semin Oncol 2010; 37 (5): Weber JS, Kahler KC, Hauschild A. Management of immune-related adverse events and kinetics of response with ipilimumab. J Clin Oncol 2012; 30 (21): Robert C, Long GV, Brady B, Dutriaux C, Maio M, Mortier L, et al. Nivolumab in previously untreated melanoma without BRAF mutation. N Engl J Med 2015; 372 (4): Two-Year Survival and Safety Update in Patients (pts) with Treatment-Naïve Advanced Melanoma (MEL) Receiving Nivolumab (NIVO) or Dacarbazine (DTIC) in CheckMate-066. Presented at the Society for Melanoma Research 2015 International Congress; November 18-21, 2015; San Francisco, CA. 1457
11 Terapias actuales en melanoma metastásico - R. Rodríguez et al 63. Weber JS, D Angelo SP, Minor D, Hodi FS, Gutzmer R, Neyns B, et al. Nivolumab versus chemotherapy in patients with advanced melanoma who progressed after anti-ctla-4 treatment (CheckMate 037): a randomised, controlled, open-label, phase 3 trial. Lancet Oncol 2015; 16 (4): Hamid O, Robert C, Daud A, Hodi FS, Hwu WJ, Kefford R, et al. Safety and tumor responses with lambrolizumab (anti-pd-1) in melanoma. N Engl J Med 2013; 369 (2): Robert C, Schachter J, Long GV, Arance A, Grob JJ, Mortier L, et al. Pembrolizumab versus Ipilimumab in Advanced Melanoma. N Engl J Med Ribas AF, Hodi FS, Kefford R, Hamid O, Daud A, Wolchok JD, et al. Efficacy and safety of the anti-pd-1 monoclonal antibody MK-3475 in 411 patients (pts) with melanoma (MEL). ASCO Meeting J Clin Oncol 32: 5s, 2014 (suppl; abstr LBA9000^). 67. Brahmer JR, Tykodi SS, Chow LQ, Hwu WJ, Topalian SL, Hwu P, et al. Safety and activity of anti-pd-l1 antibody in patients with advanced cancer. N Engl J Med 2012; 366 (26): Freeman-Keller M, Weber JS. Anti-programmed death receptor 1 immunotherapy in melanoma: rationale, evidence and clinical potential. Ther Adv Med Oncol 2015; 7 (1): Mahoney KM, Freeman GJ, McDermott DF. The Next Immune-Checkpoint Inhibitors: PD-1/PD-L1 Blockade in Melanoma. Clin Ther 2015; 37 (4): Postow MA, Chesney J, Pavlick AC, Robert C, Grossmann K, McDermott D, et al. Nivolumab and ipilimumab versus ipilimumab in untreated melanoma. N Engl J Med 2015; 372 (21): Larkin J, Chiarion-Sileni V, Gonzalez R, Grob JJ, Cowey CL, Lao CD, et al. Combined Nivolumab and Ipilimumab or Monotherapy in Untreated Melanoma. N Engl J Med 2015; 373 (1): Sznol M, Kluger HM, Callahan MK, Postow MA, Gordon RA, Segal NH, et al. Survival, response duration, and activity by BRAF mutation (MT) status of nivolumab (NIVO, anti-pd-1, BMS , ONO-4538) and ipilimumab (IPI) concurrent therapy in advanced melanoma (MEL). J Clin Oncol 32: 5s, 2014 (suppl; abstr LBA9003^). 73. Wolchok JD, Kluger H, Callahan MK, Postow MA, Rizvi NA, Lesokhin AM, et al. Nivolumab plus ipilimumab in advanced melanoma. N Engl J Med 2013; 369 (2): Sosman J. Overview of the management of advanced cutaneous melanoma. En: UpToDate, Atkins MB (Ed), UpToDate, Waltham, MA. (Consultado el 20 de diciembre de 2015). Disponible en: Ollila DW, Gleisner AL, Hsueh EC. Rationale for complete metastasectomy in patients with stage IV metastatic melanoma. J Surg Oncol 2011; 104(4):
Qué hacemos con los pacientes B-RAF mutados? Alfonso Berrocal Hospital General Universitario, Valencia
 Qué hacemos con los pacientes B-RAF mutados? Alfonso Berrocal Hospital General Universitario, Valencia Ventajas y desventajas de la inmunoterapia Ventajas Pacientes Largos supervivientes Ipilimumab 20%
Qué hacemos con los pacientes B-RAF mutados? Alfonso Berrocal Hospital General Universitario, Valencia Ventajas y desventajas de la inmunoterapia Ventajas Pacientes Largos supervivientes Ipilimumab 20%
Terapias anti PD1- PDL1. Luis de la Cruz Merino Sº Oncología Médica. HUVMacarena (Sevilla)
 Terapias anti PD1- PDL1 Luis de la Cruz Merino Sº Oncología Médica. HUVMacarena (Sevilla) INDICE EL EJE PD1/PD-L1 Y LA SINAPSIS INMUNE ANTICUERPOS MONOCLONALES EN ESTUDIO DESARROLLO AC MO ANTI PD1 EN MELANOMA
Terapias anti PD1- PDL1 Luis de la Cruz Merino Sº Oncología Médica. HUVMacarena (Sevilla) INDICE EL EJE PD1/PD-L1 Y LA SINAPSIS INMUNE ANTICUERPOS MONOCLONALES EN ESTUDIO DESARROLLO AC MO ANTI PD1 EN MELANOMA
Metástasis SNC papel tratamiento sistémico. Dra Ana Arance Hospital Clínic Barcelona
 Metástasis SNC papel tratamiento sistémico Dra Ana Arance Hospital Clínic Barcelona MELANOMA: METÁSTASIS CEREBRALES Melanoma Metastásico: 20% presentan M1 SNC 50% desarrollarán M1 SNC 55-75% autopsias
Metástasis SNC papel tratamiento sistémico Dra Ana Arance Hospital Clínic Barcelona MELANOMA: METÁSTASIS CEREBRALES Melanoma Metastásico: 20% presentan M1 SNC 50% desarrollarán M1 SNC 55-75% autopsias
DABRAFENIB en el tratamiento dea melanoma INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA
 DABRAFENIB en el tratamiento dea melanoma INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Genérico: Dabrafenib Nombre Comercial: Tafinlar Presentaciones: E/28 comp 50 y
DABRAFENIB en el tratamiento dea melanoma INFORME CFT- HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Genérico: Dabrafenib Nombre Comercial: Tafinlar Presentaciones: E/28 comp 50 y
Evolución de la supervivencia en melanoma metastásico BRAF mutado. Nuevas estrategias de tratamiento.
 Evolución de la supervivencia en melanoma metastásico BRAF mutado. Nuevas estrategias de tratamiento. Dra. Ainara Soria Rivas Servicio de Oncología Médica Hospital Ramón y Cajal Cuál es la supervivencia
Evolución de la supervivencia en melanoma metastásico BRAF mutado. Nuevas estrategias de tratamiento. Dra. Ainara Soria Rivas Servicio de Oncología Médica Hospital Ramón y Cajal Cuál es la supervivencia
Tratamiento inmunoterápico de las metástasis cerebrales. Alfonso Berrocal Hospital General de Valencia
 Tratamiento inmunoterápico de las metástasis cerebrales Alfonso Berrocal Hospital General de Valencia Inmunidad y metástasis cerebrales Cancer 2013;119:2737-46. Ipilimumab y metástasis SNC Ipilimumab bloquea
Tratamiento inmunoterápico de las metástasis cerebrales Alfonso Berrocal Hospital General de Valencia Inmunidad y metástasis cerebrales Cancer 2013;119:2737-46. Ipilimumab y metástasis SNC Ipilimumab bloquea
El Inmunomomento en Melanoma: Nivolumab más respuestas y larga supervivencia? Alfonso Berrocal
 El Inmunomomento en Melanoma: Nivolumab más respuestas y larga supervivencia? Alfonso Berrocal Proporción vivos Supervivencia con Ipilumumab en acceso expandido 1.0 0.9 0.8 Mediana de supervivencia meses
El Inmunomomento en Melanoma: Nivolumab más respuestas y larga supervivencia? Alfonso Berrocal Proporción vivos Supervivencia con Ipilumumab en acceso expandido 1.0 0.9 0.8 Mediana de supervivencia meses
Nuevas terapias sistémicas para el tratamiento del melanoma*
 CIRUGÍA AL DÍA Nuevas terapias sistémicas para el tratamiento del melanoma* Drs. Nicolás Droppelmann M. 1,2, Augusto León R. 1,2, Ignacio Goñi E. 1,2, Hernán González D. 1,2, Francisco Domínguez C. 1,2,
CIRUGÍA AL DÍA Nuevas terapias sistémicas para el tratamiento del melanoma* Drs. Nicolás Droppelmann M. 1,2, Augusto León R. 1,2, Ignacio Goñi E. 1,2, Hernán González D. 1,2, Francisco Domínguez C. 1,2,
Multidisciplinary Approach to Brain Metastasis from Melanoma
 Multidisciplinary Approach to Brain Metastasis from Melanoma -Local Therapies for Central Nervous System Metastases. -The Emerging Role of Systemic Therapies. Servicio de Hematología y Oncología Hospital
Multidisciplinary Approach to Brain Metastasis from Melanoma -Local Therapies for Central Nervous System Metastases. -The Emerging Role of Systemic Therapies. Servicio de Hematología y Oncología Hospital
MELANOMA MESA REDONDA 4 DEFINIENDO LA SECUENCIA ÓPTIMA DE TRATAMIENTO EN CÁNCER AVANZADO
 MESA REDONDA 4 DEFINIENDO LA SECUENCIA ÓPTIMA DE TRATAMIENTO EN CÁNCER AVANZADO MELANOMA Salvador Martín Algarra Clínica Universidad de Navarra Pamplona En los últimos años ha habido considerables avances
MESA REDONDA 4 DEFINIENDO LA SECUENCIA ÓPTIMA DE TRATAMIENTO EN CÁNCER AVANZADO MELANOMA Salvador Martín Algarra Clínica Universidad de Navarra Pamplona En los últimos años ha habido considerables avances
Avances en Inmunoterapia del Melanoma Estrategias de Combinación. Luis de la Cruz Merino Sº Oncología Médica HUVMacarena
 Avances en Inmunoterapia del Melanoma Estrategias de Combinación Luis de la Cruz Merino Sº Oncología Médica HUVMacarena Índice 1) Inmunoedición del cáncer 2) Inmunogenicidad del melanoma 3) Inmunoterapia
Avances en Inmunoterapia del Melanoma Estrategias de Combinación Luis de la Cruz Merino Sº Oncología Médica HUVMacarena Índice 1) Inmunoedición del cáncer 2) Inmunogenicidad del melanoma 3) Inmunoterapia
Terapias anti CTLA-4. Curso Básico de Inmunología e Inmunoterapia y cáncer. Alfonso Berrocal Hospital General Valencia
 Terapias anti CTLA-4 Curso Básico de Inmunología e Inmunoterapia y cáncer Alfonso Berrocal Hospital General Valencia Mecanismo de acción Teoría Tres señales: Co-estimulación Interacción B7/CD28 CD28 se
Terapias anti CTLA-4 Curso Básico de Inmunología e Inmunoterapia y cáncer Alfonso Berrocal Hospital General Valencia Mecanismo de acción Teoría Tres señales: Co-estimulación Interacción B7/CD28 CD28 se
Nuevas Estrategias con Inhibidores de Puntos de Control Celular en Linfomas de Hodgkin
 Nuevas Estrategias con Inhibidores de Puntos de Control Celular en Linfomas de Hodgkin Dra. María Alejandra Torres Viera Hematología Oncología 360, Caracas Caracas, Marzo 2016!" LH: Sobrevida De Acuerdo
Nuevas Estrategias con Inhibidores de Puntos de Control Celular en Linfomas de Hodgkin Dra. María Alejandra Torres Viera Hematología Oncología 360, Caracas Caracas, Marzo 2016!" LH: Sobrevida De Acuerdo
Introducción al test molecular DecisionDx-MELANOMA
 i Introducción al test molecular DecisionDx-MELANOMA El primer test genético de pronóstico validado para pacientes con melanoma cutáneo en estadios iniciales I y II 1. Datos clínicos 2. Nuestra solución:
i Introducción al test molecular DecisionDx-MELANOMA El primer test genético de pronóstico validado para pacientes con melanoma cutáneo en estadios iniciales I y II 1. Datos clínicos 2. Nuestra solución:
XX JORNADA DE LA SOCIEDAD DE MEDICINA NUCLEAR E IMAGEN MOLECULAR DE VALENCIA Y MURCIA
 XX JORNADA DE LA SOCIEDAD DE MEDICINA NUCLEAR E IMAGEN MOLECULAR DE VALENCIA Y MURCIA Dra Virtudes Soriano Fundación Instituto Valenciano de Oncologia Valencia 29 de Abril 2016 HISTORIA INMUNOTERAPIA EN
XX JORNADA DE LA SOCIEDAD DE MEDICINA NUCLEAR E IMAGEN MOLECULAR DE VALENCIA Y MURCIA Dra Virtudes Soriano Fundación Instituto Valenciano de Oncologia Valencia 29 de Abril 2016 HISTORIA INMUNOTERAPIA EN
IPILIMUMAB EN AVANZADO/METASTASICO
 IPILIMUMAB EN MELANOMA AVANZADO/METASTASICO GROWING UP IN ONCOLOGY Sesión 19 de junio de 2012 REBECA ALCALDE PAMPLIEGA R4 ONCOLOGIA MEDICA HOSPITAL UNIVERSITARIO RAMÓN Y CAJAL QUÉ ES IPILIMUMAB? Anticuerpo
IPILIMUMAB EN MELANOMA AVANZADO/METASTASICO GROWING UP IN ONCOLOGY Sesión 19 de junio de 2012 REBECA ALCALDE PAMPLIEGA R4 ONCOLOGIA MEDICA HOSPITAL UNIVERSITARIO RAMÓN Y CAJAL QUÉ ES IPILIMUMAB? Anticuerpo
Cómo modificará la Inmunoterapia el panorama de tratamiento del cáncer? Dra Ana Arance Oncología Médica Hospital Clínic Barcelona
 Cómo modificará la Inmunoterapia el panorama de tratamiento del cáncer? Dra Ana Arance Oncología Médica Hospital Clínic Barcelona The Cancer-Immunity Cycle Chen et al. Immunity 39, July 25, 2013 Factores
Cómo modificará la Inmunoterapia el panorama de tratamiento del cáncer? Dra Ana Arance Oncología Médica Hospital Clínic Barcelona The Cancer-Immunity Cycle Chen et al. Immunity 39, July 25, 2013 Factores
TAPCells BIOTECNOLOGÍA GLOBAL La Vacuna Chilena Contra el Melanoma. Prof. Dr. Flavio Salazar Onfray
 TAPCells BIOTECNOLOGÍA GLOBAL La Vacuna Chilena Contra el Melanoma Prof. Dr. Flavio Salazar Onfray MITO CHILE NO PRODUCE CIENCIA A NIVEL GLOBAL no SI! MELANOMA "THE MARKET" Melanoma is growing worldwide
TAPCells BIOTECNOLOGÍA GLOBAL La Vacuna Chilena Contra el Melanoma Prof. Dr. Flavio Salazar Onfray MITO CHILE NO PRODUCE CIENCIA A NIVEL GLOBAL no SI! MELANOMA "THE MARKET" Melanoma is growing worldwide
Impacto de los nuevos tratamientos. Nuria Muñoz Muñoz Hospital Universitario Virgen Macarena
 Impacto de los nuevos tratamientos Nuria Muñoz Muñoz Hospital Universitario Virgen Macarena Indicaciones. Ipilimumab (Yervoy): EMA: tratamiento del melanoma avanzado (irresecable o metastásico) en adultos
Impacto de los nuevos tratamientos Nuria Muñoz Muñoz Hospital Universitario Virgen Macarena Indicaciones. Ipilimumab (Yervoy): EMA: tratamiento del melanoma avanzado (irresecable o metastásico) en adultos
Avances en el tratamiento del melanoma metastásico. José Antonio López Martín HU 12 de Octubre- Madrid
 Avances en el tratamiento del melanoma metastásico. José Antonio López Martín HU 12 de Octubre- Madrid Melanoma metastásico - 2010 Incidencia global en ascenso Edad de inicio menor que otros tumores Mal
Avances en el tratamiento del melanoma metastásico. José Antonio López Martín HU 12 de Octubre- Madrid Melanoma metastásico - 2010 Incidencia global en ascenso Edad de inicio menor que otros tumores Mal
Dr Alejandro Acevedo Gaete Oncólogo Médico Hospital Carlos Van Buren
 Dr Alejandro Acevedo Gaete Oncólogo Médico Hospital Carlos Van Buren Introduccion Perspectiva histórica Principios de Biologia molecular del cáncer colorectal Conceptos de biomarcadores Evidencia clínica
Dr Alejandro Acevedo Gaete Oncólogo Médico Hospital Carlos Van Buren Introduccion Perspectiva histórica Principios de Biologia molecular del cáncer colorectal Conceptos de biomarcadores Evidencia clínica
Cáncer de Mama: Inhibidores de vía PI3K/Akt/mTOR, ciclinas, anti-ctla4 y anti PD1. Dr. Claudio Painemal D. Director Médico
 Cáncer de Mama: Inhibidores de vía PI3K/Akt/mTOR, ciclinas, anti-ctla4 y anti PD1 Dr. Claudio Painemal D. Director Médico PI3K/Akt/mTOR Frecuentemente activada en cáncer de mama PIK3CA es el gen más frecuentemente
Cáncer de Mama: Inhibidores de vía PI3K/Akt/mTOR, ciclinas, anti-ctla4 y anti PD1 Dr. Claudio Painemal D. Director Médico PI3K/Akt/mTOR Frecuentemente activada en cáncer de mama PIK3CA es el gen más frecuentemente
Trametinib ( Mekinist, Novartis) en melanoma no resecable o metastásico
 Trametinib ( Mekinist, Novartis) en melanoma no resecable o metastásico RESUMEN El trametinib es un agente antineoplásico que actúa inhibiendo potente y selectivamente determinadas proteína cinasas implicadas
Trametinib ( Mekinist, Novartis) en melanoma no resecable o metastásico RESUMEN El trametinib es un agente antineoplásico que actúa inhibiendo potente y selectivamente determinadas proteína cinasas implicadas
MELANOMA CUTÁNEO Factores pronósticos y predictivos anatomopatológicos. JJ Ríos Martín Hospital Univ. Virgen Macarena Sevilla
 MELANOMA CUTÁNEO Factores pronósticos y predictivos anatomopatológicos JJ Ríos Martín Hospital Univ. Virgen Macarena Sevilla The poverty of prognosis studies June 2, 2013 by P. Hall Editor in Chief Journal
MELANOMA CUTÁNEO Factores pronósticos y predictivos anatomopatológicos JJ Ríos Martín Hospital Univ. Virgen Macarena Sevilla The poverty of prognosis studies June 2, 2013 by P. Hall Editor in Chief Journal
OPTIMIZACIÓN TRATAMIENTO ANTI-EGFR. Ruth Vera Oncología Médica
 OPTIMIZACIÓN TRATAMIENTO ANTI-EGFR Ruth Vera Oncología Médica OPTIMIZACIÓN TRATAMIENTO anti-egfr OPTIMIZAR quiere decir: Buscar los mejores resultados Planificar una actividad para obtener los mejores
OPTIMIZACIÓN TRATAMIENTO ANTI-EGFR Ruth Vera Oncología Médica OPTIMIZACIÓN TRATAMIENTO anti-egfr OPTIMIZAR quiere decir: Buscar los mejores resultados Planificar una actividad para obtener los mejores
Comunicado de prensa. Roche obtiene la autorización en la UE de Cotellic para su uso en combinación con Zelboraf contra el melanoma avanzado
 Comunicado de prensa Basilea, 25 de noviembre de 2015 Roche obtiene la autorización en la UE de Cotellic para su uso en combinación con Zelboraf contra el melanoma avanzado Roche (SIX: RO, ROG; OTCQX:
Comunicado de prensa Basilea, 25 de noviembre de 2015 Roche obtiene la autorización en la UE de Cotellic para su uso en combinación con Zelboraf contra el melanoma avanzado Roche (SIX: RO, ROG; OTCQX:
Estrategias de inmunoterapia en cáncer genitourinario
 Estrategias de inmunoterapia en cáncer genitourinario Iván Martínez Forero MD, PhD Hospital Pablo Tobón Uribe imforero@hptu.org.co imforero@alumni.unav.es Disclosure BMS-Speaker Contenido Respuesta inmune
Estrategias de inmunoterapia en cáncer genitourinario Iván Martínez Forero MD, PhD Hospital Pablo Tobón Uribe imforero@hptu.org.co imforero@alumni.unav.es Disclosure BMS-Speaker Contenido Respuesta inmune
MESA DIRECTIVA SOCIEDAD MEXICANA DE ONCOLOGIA A.C. 2012-2013
 MESA DIRECTIVA SOCIEDAD MEXICANA DE ONCOLOGIA A.C. 2012-2013 Presidente DR. JORGE MARTÍNEZ CEDILLO Vicepresidenta DRA. LAURA TORRECILLAS TORRES Secretario DR. GREGORIO QUINTERO BEULÓ Tesorera DRA. ARACELI
MESA DIRECTIVA SOCIEDAD MEXICANA DE ONCOLOGIA A.C. 2012-2013 Presidente DR. JORGE MARTÍNEZ CEDILLO Vicepresidenta DRA. LAURA TORRECILLAS TORRES Secretario DR. GREGORIO QUINTERO BEULÓ Tesorera DRA. ARACELI
INFORME SEOM DE EVALUACIÓN DE NIVOLUMAB (OPDIVO )
 INFORME SEOM DE EVALUACIÓN DE NIVOLUMAB (OPDIVO ) 1. RESUMEN Melanoma es la novena causa de cancer en Europa, con más de 100 000 nuevos casos diagnosticados en el 2012. La incidencia del melanoma en España
INFORME SEOM DE EVALUACIÓN DE NIVOLUMAB (OPDIVO ) 1. RESUMEN Melanoma es la novena causa de cancer en Europa, con más de 100 000 nuevos casos diagnosticados en el 2012. La incidencia del melanoma en España
Comunicado de Prensa. La inmunoterapia se consolida como el campo más promisorio para tratar al cáncer
 Comunicado de Prensa Conclusiones del 51 Encuentro Anual de la Sociedad Americana de Oncología Clínica (ASCO) La inmunoterapia se consolida como el campo más promisorio para tratar al cáncer El nuevo enfoque
Comunicado de Prensa Conclusiones del 51 Encuentro Anual de la Sociedad Americana de Oncología Clínica (ASCO) La inmunoterapia se consolida como el campo más promisorio para tratar al cáncer El nuevo enfoque
Biología Molecular del Melanoma (Diapositiva 1)
 Biología Molecular del Melanoma (Diapositiva 1) Muchas gracias a los organizadores de este 2ndo preceptorship de Melanoma, especialmente al Dr. Eduardo Fierro quien me contactó. He dividido mi conferencia
Biología Molecular del Melanoma (Diapositiva 1) Muchas gracias a los organizadores de este 2ndo preceptorship de Melanoma, especialmente al Dr. Eduardo Fierro quien me contactó. He dividido mi conferencia
Transformando la historia natural del cáncer de mama HER2+ con anticuerpos anti-her2. Joan Albanell Hospital del Mar, UPF Barcelona
 Transformando la historia natural del cáncer de mama HER2+ con anticuerpos anti-her2 Joan Albanell Hospital del Mar, UPF Barcelona HER2: a target for breast cancer therapy Rationale (late 80 s early 90
Transformando la historia natural del cáncer de mama HER2+ con anticuerpos anti-her2 Joan Albanell Hospital del Mar, UPF Barcelona HER2: a target for breast cancer therapy Rationale (late 80 s early 90
José Luis Pérez Gracia Departamento de Oncología Clínica Universidad de Navarra Madrid, 20 de noviembre de 2014
 Inmunoterapia en cáncer renal y futuro de las combinaciones con TKI José Luis Pérez Gracia Departamento de Oncología Clínica Universidad de Navarra Madrid, 20 de noviembre de 2014 Steps leading to an anti
Inmunoterapia en cáncer renal y futuro de las combinaciones con TKI José Luis Pérez Gracia Departamento de Oncología Clínica Universidad de Navarra Madrid, 20 de noviembre de 2014 Steps leading to an anti
La Inmunoterapia como tratamiento oncológico: Melanoma. Dr. Joaquín Fra Rodríguez Hospital Universitario Río Hortega Valladolid
 La Inmunoterapia como tratamiento oncológico: Melanoma Dr. Joaquín Fra Rodríguez Hospital Universitario Río Hortega Valladolid LA INMUNIDAD Y LA DISEMINACIÓN DE LOS TUMORES MALIGNOS Desarrollo de las metástasis
La Inmunoterapia como tratamiento oncológico: Melanoma Dr. Joaquín Fra Rodríguez Hospital Universitario Río Hortega Valladolid LA INMUNIDAD Y LA DISEMINACIÓN DE LOS TUMORES MALIGNOS Desarrollo de las metástasis
PERTUZUMAB AUMENTA LA SUPERVIVENCIA GLOBAL EN CÁNCER DE MAMA METASTÁSICO HER2 POSITIVO
 Los especialistas españoles coinciden en que es el avance más relevante en una década y que permitirá afrontar una necesidad médica urgente PERTUZUMAB AUMENTA LA SUPERVIVENCIA GLOBAL EN CÁNCER DE MAMA
Los especialistas españoles coinciden en que es el avance más relevante en una década y que permitirá afrontar una necesidad médica urgente PERTUZUMAB AUMENTA LA SUPERVIVENCIA GLOBAL EN CÁNCER DE MAMA
Melanoma metastásico
 Selección del tratamiento en el melanoma maligno metastásico. Controversias y recomendaciones José Antonio López Martín HU 12 de Octubre- Madrid Melanoma: Melanoma metastásico Incidencia global en ascenso
Selección del tratamiento en el melanoma maligno metastásico. Controversias y recomendaciones José Antonio López Martín HU 12 de Octubre- Madrid Melanoma: Melanoma metastásico Incidencia global en ascenso
Retos presentes y futuros de la aplicación clínica de la inmunoterapia en cáncer
 Retos presentes y futuros de la aplicación clínica de la inmunoterapia en cáncer Juan José Lasarte, Centro de Investigación Médica Aplicada Universidad de Navara, CIMA, Pamplona Concepto de Inmunoedición
Retos presentes y futuros de la aplicación clínica de la inmunoterapia en cáncer Juan José Lasarte, Centro de Investigación Médica Aplicada Universidad de Navara, CIMA, Pamplona Concepto de Inmunoedición
Prometedora terapia para uno de los tumores malignos más agresivos en la mujer
 Prometedora terapia para uno de los tumores malignos más agresivos en la mujer LA ANMAT APROBÓ UNA NUEVA OPCIÓN TERAPÉUTICA PARA EL CÁNCER DE MAMA HER2-POSITIVO METASTÁSICO Se trata del uso de pertuzumab,
Prometedora terapia para uno de los tumores malignos más agresivos en la mujer LA ANMAT APROBÓ UNA NUEVA OPCIÓN TERAPÉUTICA PARA EL CÁNCER DE MAMA HER2-POSITIVO METASTÁSICO Se trata del uso de pertuzumab,
EL EQUIPO MULTIDISCIPLINAR XXVI CONGRESO DE LA SEAP/IAP PAPEL DEL PATOLOGO EN LOS TUMORES DEL APARATO DIGESTIVO BIOMARCADORES PREDICTIVOS
 XXVI CONGRESO DE LA SEAP/IAP PAPEL DEL PATOLOGO EN LOS TUMORES DEL APARATO DIGESTIVO ACTUALIZACION EN BIOMARCADORES Y GUIA DE RECOMENDACIONES EN TUMORES DEL APARATO DIGESTIVO # DIAGNOSTICO # APORTACION
XXVI CONGRESO DE LA SEAP/IAP PAPEL DEL PATOLOGO EN LOS TUMORES DEL APARATO DIGESTIVO ACTUALIZACION EN BIOMARCADORES Y GUIA DE RECOMENDACIONES EN TUMORES DEL APARATO DIGESTIVO # DIAGNOSTICO # APORTACION
Estrategias de Inmunoterapia en Cáncer
 Estrategias de Inmunoterapia en Cáncer Carlos Parra-López. MD., PH.D Universidad Nacional de Colombia, Facultad de Medicina. Departamento de Microbiología Bogotá, Marzo 2014 El Sistema Inmune: Un sistema
Estrategias de Inmunoterapia en Cáncer Carlos Parra-López. MD., PH.D Universidad Nacional de Colombia, Facultad de Medicina. Departamento de Microbiología Bogotá, Marzo 2014 El Sistema Inmune: Un sistema
Recomendaciones para su uso
 1 Ipilimumab DERMATOLOGÍA en Melanoma 2013 Recomendaciones para su uso Coordinador: Dr. Esteban Lifschitz Autores: Dr. Mariano Marini, Dr. Ventura Simonovich 1 LOS AUTORES RECOMIENDAN QUE EN CASO DE ESTAR
1 Ipilimumab DERMATOLOGÍA en Melanoma 2013 Recomendaciones para su uso Coordinador: Dr. Esteban Lifschitz Autores: Dr. Mariano Marini, Dr. Ventura Simonovich 1 LOS AUTORES RECOMIENDAN QUE EN CASO DE ESTAR
Bevacizumab en Cáncer de Colon
 1 Bevacizumab ONCOLOGÍA en Cáncer de Colon 2013 Bevacizumab en Cáncer de Colon Recomendaciones para su Uso Coordinador: Dr. Esteban Lifschitz Autores: Dr. Patricio Servienti, Dr. Ventura Simonovich Evaluación
1 Bevacizumab ONCOLOGÍA en Cáncer de Colon 2013 Bevacizumab en Cáncer de Colon Recomendaciones para su Uso Coordinador: Dr. Esteban Lifschitz Autores: Dr. Patricio Servienti, Dr. Ventura Simonovich Evaluación
Cáncer de Riñón Avanzado (CRm) A quien y con que tratar en 3ª Línea
 Cáncer de Riñón Avanzado (CRm) A quien y con que tratar en 3ª Línea Hospital Universitario Central de Asturias Servicio de Oncología Médica Emilio Esteban González Cual de estas afirmaciones es más correcta
Cáncer de Riñón Avanzado (CRm) A quien y con que tratar en 3ª Línea Hospital Universitario Central de Asturias Servicio de Oncología Médica Emilio Esteban González Cual de estas afirmaciones es más correcta
Ipilimumab en Melanoma Recomendaciones para su uso
 SEMINARIO TALLER PROPUESTA DE GUÍA DE PRACTICAS CLÍNICAS DE PATOLOGÍAS TUTELADAS Patologías/Tecnologías Tuteladas Guía de Práctica Ipilimumab en Melanoma Recomendaciones para su uso Recomendaciones para
SEMINARIO TALLER PROPUESTA DE GUÍA DE PRACTICAS CLÍNICAS DE PATOLOGÍAS TUTELADAS Patologías/Tecnologías Tuteladas Guía de Práctica Ipilimumab en Melanoma Recomendaciones para su uso Recomendaciones para
4. Supervivencia a largo plazo. El futuro de la Inmuno-Oncología y su potencial impacto en el tratamiento del cáncer
 Dossier de prensa Índice 1. Qué es la inmunoterapia 2. Las cifras del cáncer 3. Necesidades no cubiertas 4. Supervivencia a largo plazo. El futuro de la Inmuno-Oncología y su potencial impacto en el tratamiento
Dossier de prensa Índice 1. Qué es la inmunoterapia 2. Las cifras del cáncer 3. Necesidades no cubiertas 4. Supervivencia a largo plazo. El futuro de la Inmuno-Oncología y su potencial impacto en el tratamiento
Cetuximab: mucho más que un estándar en cáncer de cabeza y cuello. Alfonso Berrocal Hospital General Valencia
 Cetuximab: mucho más que un estándar en cáncer de cabeza y cuello Alfonso Berrocal Hospital General Valencia Indicaciones terapéuticas Cetuximab está indicado para el tratamiento de pacientes con cáncer
Cetuximab: mucho más que un estándar en cáncer de cabeza y cuello Alfonso Berrocal Hospital General Valencia Indicaciones terapéuticas Cetuximab está indicado para el tratamiento de pacientes con cáncer
: Cáncer renal avanzado o metastásico
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
Tratamiento adyuvante del melanoma de alto riesgo. Alfonso Berrocal Hospital General Universitario
 Tratamiento adyuvante del melanoma de alto riesgo Alfonso Berrocal Hospital General Universitario Necesidad de tratamiento Balch CM et al. JCO 2009: 6199-6206 Necesidad de nuevos tratamientos DFS SG Mejorado
Tratamiento adyuvante del melanoma de alto riesgo Alfonso Berrocal Hospital General Universitario Necesidad de tratamiento Balch CM et al. JCO 2009: 6199-6206 Necesidad de nuevos tratamientos DFS SG Mejorado
COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS
 COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS 1. SOLICITUD DEL FÁRMACO Principio activo solicitado: (erbitux
COMISIÓN DE FARMACIA Y TERAPÉUTICA INFORME DE INCLUSIÓN DE MEDICAMENTOS EN LA GUÍA FARMACOTERAPÉUTICA CENTRO DE INFORMACIÓN DE MEDICAMENTOS 1. SOLICITUD DEL FÁRMACO Principio activo solicitado: (erbitux
Inmunoterapia en cáncer renal
 Inmunoterapia en cáncer renal José Luis Pérez Gracia Departamento de Oncología Clínica Universidad de Navarra Pamplona, 1 de marzo de 2014 Inmunoterapia en cáncer renal Introducción Inmunoterapia activa
Inmunoterapia en cáncer renal José Luis Pérez Gracia Departamento de Oncología Clínica Universidad de Navarra Pamplona, 1 de marzo de 2014 Inmunoterapia en cáncer renal Introducción Inmunoterapia activa
PANITUMUMAB EN CANCER DE COLON METASTÁSICO:
 PANITUMUMAB EN CANCER DE COLON METASTÁSICO: Romero Soria L 1, Jaraquemada Peláez T 2, Martin Clavo S 1, Rivero Cava MS 1, Braga Fuentes JL, Rangel Mayoral JF 1. 1 Servicio de Farmacia Hospitalaria 2 Servicio
PANITUMUMAB EN CANCER DE COLON METASTÁSICO: Romero Soria L 1, Jaraquemada Peláez T 2, Martin Clavo S 1, Rivero Cava MS 1, Braga Fuentes JL, Rangel Mayoral JF 1. 1 Servicio de Farmacia Hospitalaria 2 Servicio
Descripción CLASES MAGISTRALES, TALLERES PRÁCTICOS DE CITOLOGÍA Y PRESENTACIÓN DE CASOS CLÍNICOS
 CURSO DE POSGRADO EN ONCOLOGÍA VETERINARIA De lo molecular a lo clínico Facultad de Ciencias Agropecuarias Universidad Católica de Córdoba Cupo MÍNIMO 10, MÁXIMO 30 ALUMNOS Descripción CLASES MAGISTRALES,
CURSO DE POSGRADO EN ONCOLOGÍA VETERINARIA De lo molecular a lo clínico Facultad de Ciencias Agropecuarias Universidad Católica de Córdoba Cupo MÍNIMO 10, MÁXIMO 30 ALUMNOS Descripción CLASES MAGISTRALES,
Roche comunica que el vemurafenib mejoró la supervivencia de personas que padecían melanoma metastásico con una mutación BRAFV600
 Comunicado de prensa Basilea, 5 de junio de 2011 Roche comunica que el vemurafenib mejoró la supervivencia de personas que padecían melanoma metastásico con una mutación BRAFV600 El vemurafenib y su prueba
Comunicado de prensa Basilea, 5 de junio de 2011 Roche comunica que el vemurafenib mejoró la supervivencia de personas que padecían melanoma metastásico con una mutación BRAFV600 El vemurafenib y su prueba
New Anticancer Therapies I Nuevas Terapias Antineoplásicas I
 VI InterAmerican Oncology Conference 'Current Status and Future of Anti-Cancer Targeted Therapies' Estado Actual y Futuro de las Terapias Antineoplásicas October 8-9, 2015 Universidad Católica Argentina
VI InterAmerican Oncology Conference 'Current Status and Future of Anti-Cancer Targeted Therapies' Estado Actual y Futuro de las Terapias Antineoplásicas October 8-9, 2015 Universidad Católica Argentina
Farmacogenética y Farmacogenómica. Su aplicación en la gestión clínica diaria.
 Farmacogenética y Farmacogenómica. Su aplicación en la gestión clínica diaria. Montserrat Baiget Servicio de Genética Hospital de la Santa Creu i Sant Pau Barcelona EMA (European Medicines Agency) Genomic
Farmacogenética y Farmacogenómica. Su aplicación en la gestión clínica diaria. Montserrat Baiget Servicio de Genética Hospital de la Santa Creu i Sant Pau Barcelona EMA (European Medicines Agency) Genomic
La Comisión Europea aprueba Cyramza (ramucirumab) para cáncer de pulmón avanzado de células no pequeñas y cáncer colorrectal metastásico
 www.lilly.com Fecha: 1 de febrero de 2016 Eli Lilly and Company Lilly Corporate Center Indianapolis, Indiana 46285 U.S.A. La Comisión Europea aprueba Cyramza (ramucirumab) para cáncer de pulmón avanzado
www.lilly.com Fecha: 1 de febrero de 2016 Eli Lilly and Company Lilly Corporate Center Indianapolis, Indiana 46285 U.S.A. La Comisión Europea aprueba Cyramza (ramucirumab) para cáncer de pulmón avanzado
Comunicado de prensa. Basilea, 17 de agosto de 2011
 Comunicado de prensa Basilea, 17 de agosto de 2011 La FDA aprueba Zelboraf (vemurafenib) y un test diagnóstico de acompañamiento para los pacientes con melanoma metastásico positivo para la mutación BRAF,
Comunicado de prensa Basilea, 17 de agosto de 2011 La FDA aprueba Zelboraf (vemurafenib) y un test diagnóstico de acompañamiento para los pacientes con melanoma metastásico positivo para la mutación BRAF,
Dra. Dulce María Arreguín Porras Servicio de Infectología Hospital General de México Dr. Eduardo Liceaga
 Dra. Dulce María Arreguín Porras Servicio de Infectología Hospital General de México Dr. Eduardo Liceaga Neoplasias definitorias de SIDA Neoplasias no definitorias de SIDA El grado de inmunosupresión manifestado
Dra. Dulce María Arreguín Porras Servicio de Infectología Hospital General de México Dr. Eduardo Liceaga Neoplasias definitorias de SIDA Neoplasias no definitorias de SIDA El grado de inmunosupresión manifestado
Prof. Javier García-Conde
 01.12.2000 Prof. Javier García-Conde Clinico Universitario, Spanien Rituximab más CHOP es superior a CHOP en pacientes ancianos con linfoma difuso de células B grandes (LDCG): Resultados preliminares de
01.12.2000 Prof. Javier García-Conde Clinico Universitario, Spanien Rituximab más CHOP es superior a CHOP en pacientes ancianos con linfoma difuso de células B grandes (LDCG): Resultados preliminares de
2.1 EFICACIA. Cetuximab en combinación con quimioterapia
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
Melanoma. Una guía para periodistas sobre el melanoma y su tratamiento. Contenidos. Parte 1: Melanoma
 Melanoma Una guía para periodistas sobre el melanoma y su tratamiento Contenidos Parte 1: Melanoma i. Qué es el melanoma? 2 ii. Causas y factores de riesgo 3 iii. Diagnóstico 4 Parte 2: Opciones de tratamiento
Melanoma Una guía para periodistas sobre el melanoma y su tratamiento Contenidos Parte 1: Melanoma i. Qué es el melanoma? 2 ii. Causas y factores de riesgo 3 iii. Diagnóstico 4 Parte 2: Opciones de tratamiento
Reunión Clínica: Melanoma Maligno Avanzado: Alternativas Terapéuticas
 Reunión Clínica: Melanoma Maligno Avanzado: Alternativas Terapéuticas Gabriela Bascur Alarcón Residente Primer Año Cirugía General Universidad Austral Dr. Juan Antonio Pérez P. Cirugía Oncológica Hospital
Reunión Clínica: Melanoma Maligno Avanzado: Alternativas Terapéuticas Gabriela Bascur Alarcón Residente Primer Año Cirugía General Universidad Austral Dr. Juan Antonio Pérez P. Cirugía Oncológica Hospital
Cetuximab en Cáncer de Colon
 1 Cetuximab ONCOLOGÍA en Cáncer de Colon 2013 Cetuximab en Cáncer de Colon Recomendaciones para su Uso Coordinador: Dr. Esteban Lifschitz Autores: Dr. Patricio Servienti, Dr. Ventura Simonovich Evaluación
1 Cetuximab ONCOLOGÍA en Cáncer de Colon 2013 Cetuximab en Cáncer de Colon Recomendaciones para su Uso Coordinador: Dr. Esteban Lifschitz Autores: Dr. Patricio Servienti, Dr. Ventura Simonovich Evaluación
COMUNICADO DE PRENSA. Grupo Novartis en España Comunicación Corporativa Gran Via Corts Catalanes, 764 08013 Barcelona
 Grupo Novartis en España Comunicación Corporativa Gran Via Corts Catalanes, 764 08013 Barcelona Tel 93 306 42 00 Fax 93 265 73 89 e-mail: novartis.comunicacion@novartis.com Internet:www.novartis.es COMUNICADO
Grupo Novartis en España Comunicación Corporativa Gran Via Corts Catalanes, 764 08013 Barcelona Tel 93 306 42 00 Fax 93 265 73 89 e-mail: novartis.comunicacion@novartis.com Internet:www.novartis.es COMUNICADO
A mi madre Marcela y mi hermana Sandra, a su memoria dedico con mucho amor mi tesis de Especialista
 A mi madre Marcela y mi hermana Sandra, a su memoria dedico con mucho amor mi tesis de Especialista El objetivo del presente estudio fue comparar el régimen de quimioterapia estándar BEP vs el régimen
A mi madre Marcela y mi hermana Sandra, a su memoria dedico con mucho amor mi tesis de Especialista El objetivo del presente estudio fue comparar el régimen de quimioterapia estándar BEP vs el régimen
INMUNOLOGÍA DEL CÁNCER. Débora E. Aldana Salguero MD, PhD Inmunología y Microbiología
 INMUNOLOGÍA DEL CÁNCER Débora E. Aldana Salguero MD, PhD Inmunología y Microbiología PARA EL SISTEMA INMUNE ES MÁS DIFÍCIL REACCIONAR FRENTE A UNA CÉLULA TUMORAL QUE FRENTE A UNA CÉLULA XENOGÉNICA O A
INMUNOLOGÍA DEL CÁNCER Débora E. Aldana Salguero MD, PhD Inmunología y Microbiología PARA EL SISTEMA INMUNE ES MÁS DIFÍCIL REACCIONAR FRENTE A UNA CÉLULA TUMORAL QUE FRENTE A UNA CÉLULA XENOGÉNICA O A
Virus C y Hepatocarcinoma. Perspectivas en 2013
 Pamplona, junio de 2008 Virus C y Hepatocarcinoma. Perspectivas en 2013 Bruno Sangro Clínica Universidad de Navarra. CIBERehd. Pamplona, Spain Epidemiología del HCC en Europa Globalmente 50.000 casos nuevos
Pamplona, junio de 2008 Virus C y Hepatocarcinoma. Perspectivas en 2013 Bruno Sangro Clínica Universidad de Navarra. CIBERehd. Pamplona, Spain Epidemiología del HCC en Europa Globalmente 50.000 casos nuevos
Grupo de estudio internacional del cáncer de mama (IBCSG) 23-01
 Grupo de estudio internacional del cáncer de mama (IBCSG) 23-01 Disección axilar vs. no disección axilar en cáncer de mama con axila clínicamente negativa y micrometástasis en ganglio centinela Viviana
Grupo de estudio internacional del cáncer de mama (IBCSG) 23-01 Disección axilar vs. no disección axilar en cáncer de mama con axila clínicamente negativa y micrometástasis en ganglio centinela Viviana
Coste por unidad PVL con IVA Vial 100 mg/ 50 ml 1 vial 745026 246,69 204,60
 Servei de Farmàcia Informe CFT: 1/6 Cetuximab Tratamiento de cáncer de células escamosas de cabeza y cuello localmente avanzado, en combinación con radioterapia Informe para la Comisión Farmacoterapéutica
Servei de Farmàcia Informe CFT: 1/6 Cetuximab Tratamiento de cáncer de células escamosas de cabeza y cuello localmente avanzado, en combinación con radioterapia Informe para la Comisión Farmacoterapéutica
Nivolumab (Opdivo, Bristol Myers Squibb) en melanoma avanzado y cáncer de pulmón no microcítico
 (Opdivo, Bristol Myers Squibb) en melanoma avanzado y cáncer de pulmón no microcítico RESUMEN El nivolumab es un anticuerpo monoclonal que se une al receptor de muerte programada PD1 presentes en la superficie
(Opdivo, Bristol Myers Squibb) en melanoma avanzado y cáncer de pulmón no microcítico RESUMEN El nivolumab es un anticuerpo monoclonal que se une al receptor de muerte programada PD1 presentes en la superficie
Poblaciones bacilares y su impacto en el esquema TB
 Poblaciones bacilares y su impacto en el esquema TB MARIA ANGELICA PAREDES MORENO NEUMOLOGA HOSPITAL MARIA AUXILIADORA CLINICA ANGLO AMERICANA Marzo 2016 La tuberculosis (TB) sigue siendo un problema importante
Poblaciones bacilares y su impacto en el esquema TB MARIA ANGELICA PAREDES MORENO NEUMOLOGA HOSPITAL MARIA AUXILIADORA CLINICA ANGLO AMERICANA Marzo 2016 La tuberculosis (TB) sigue siendo un problema importante
ESMO 2012: Roche subraya su liderazgo en oncología con nuevos en el cáncer de mama HER2-positivo y el cáncer de piel
 Comunicado de prensa Basilea, 24 de septiembre de 2012 ESMO 2012: Roche subraya su liderazgo en oncología con nuevos en el cáncer de mama HER2-positivo y el cáncer de piel Roche (SIX: RO, ROG; OTCQX: RHHBY)
Comunicado de prensa Basilea, 24 de septiembre de 2012 ESMO 2012: Roche subraya su liderazgo en oncología con nuevos en el cáncer de mama HER2-positivo y el cáncer de piel Roche (SIX: RO, ROG; OTCQX: RHHBY)
Comunicado de prensa. Basilea, 19 de septiembre de 2011
 Comunicado de prensa Basilea, 19 de septiembre de 2011 Roche presenta datos de nuevas aproximaciones terapéuticas a los carcinomas de mama, piel y pulmón en el Congreso Europeo Multidisciplinario sobre
Comunicado de prensa Basilea, 19 de septiembre de 2011 Roche presenta datos de nuevas aproximaciones terapéuticas a los carcinomas de mama, piel y pulmón en el Congreso Europeo Multidisciplinario sobre
Doble Bloqueo Horizontal. Juan R de la Haba-Rodríguez Hospital Universitario Reina Sofía. Córdoba
 Juan R de la Haba-Rodríguez Hospital Universitario Reina Sofía. Córdoba Pertuzumab Cixitumumab Trastuzumab/DM1 Pertuzumab MM-111 ADAM 17 inhibitors HSP90 Inhibitors HDAC inhibitors Everolimus Temsirolimus
Juan R de la Haba-Rodríguez Hospital Universitario Reina Sofía. Córdoba Pertuzumab Cixitumumab Trastuzumab/DM1 Pertuzumab MM-111 ADAM 17 inhibitors HSP90 Inhibitors HDAC inhibitors Everolimus Temsirolimus
Tratamiento del cáncer de cérvix Amalia Gómez Bernal Complejo Asistencial Universitario de Salamanca
 Tratamiento del cáncer de cérvix 2016 Amalia Gómez Bernal Complejo Asistencial Universitario de Salamanca Datos estadísticos INCIDENCIA Es el 3º tumor más frecuente en las mujeres en el mundo y el 7º del
Tratamiento del cáncer de cérvix 2016 Amalia Gómez Bernal Complejo Asistencial Universitario de Salamanca Datos estadísticos INCIDENCIA Es el 3º tumor más frecuente en las mujeres en el mundo y el 7º del
IDENTIFICACIÓN Y CARACTERIZACIÓN DE LOS MECANISMOS DE TUMORIGÉNESIS MEDIADOS POR FRAGMENTOS CARBOXITERMINALES DE HER2
 IDENTIFICACIÓN Y CARACTERIZACIÓN DE LOS MECANISMOS DE TUMORIGÉNESIS MEDIADOS POR FRAGMENTOS CARBOXITERMINALES DE HER2 Investigador principal: Dr. Joaquín V. Arribas López Hospital Universitari Vall d Hebron
IDENTIFICACIÓN Y CARACTERIZACIÓN DE LOS MECANISMOS DE TUMORIGÉNESIS MEDIADOS POR FRAGMENTOS CARBOXITERMINALES DE HER2 Investigador principal: Dr. Joaquín V. Arribas López Hospital Universitari Vall d Hebron
Comunicado de prensa. Basilea, 29 de septiembre de 2014
 Comunicado de prensa Basilea, 29 de septiembre de 2014 El tratamiento combinado experimental de Roche con cobimetinib y Zelboraf (vemurafenib) tuvo ventajas significativas frente a la monoterapia con Zelboraf
Comunicado de prensa Basilea, 29 de septiembre de 2014 El tratamiento combinado experimental de Roche con cobimetinib y Zelboraf (vemurafenib) tuvo ventajas significativas frente a la monoterapia con Zelboraf
Novartis presenta nuevos datos en ASCO sobre Zykadia y la combinación de Tafinlar y Mekinist en pacientes con NSCLC con necesidades desatendidas
 Grupo Novartis en España Comunicación Corporativa Gran Via Corts Catalanes, 764 08013 Barcelona Tel 93 306 42 00 Fax 93 265 73 89 e-mail: novartis.comunicacion@novartis.com Internet:www.novartis.es COMUNICADO
Grupo Novartis en España Comunicación Corporativa Gran Via Corts Catalanes, 764 08013 Barcelona Tel 93 306 42 00 Fax 93 265 73 89 e-mail: novartis.comunicacion@novartis.com Internet:www.novartis.es COMUNICADO
Equidad sanitaria. Tratamientos oncológicos en el Cáncer de Pulmón No Microcítico. en el País Vasco. 3 de julio de 2015
 Equidad sanitaria Tratamientos oncológicos en el Cáncer de Pulmón No Microcítico en el País Vasco 3 de julio de 2015 Ref. CE/07/2015 Oficina del Comisionado para la equidad 2015 Fundamed y Alianza General
Equidad sanitaria Tratamientos oncológicos en el Cáncer de Pulmón No Microcítico en el País Vasco 3 de julio de 2015 Ref. CE/07/2015 Oficina del Comisionado para la equidad 2015 Fundamed y Alianza General
Medida de resultado primaria
 Agonistas beta2 de acción n prolongada versus antileucotrienos como tratamiento adicional a los corticosteroides inhalados para el asma crónica Dr José Damian López Sánchez Servicio de Alergología H.U.
Agonistas beta2 de acción n prolongada versus antileucotrienos como tratamiento adicional a los corticosteroides inhalados para el asma crónica Dr José Damian López Sánchez Servicio de Alergología H.U.
Universidad de Concepción Facultad de Medicina Carrera de Tecnología Médica
 Universidad de Concepción Facultad de Medicina Carrera de Tecnología Médica Paloma Campos Leyton Cuarto Año Tecnología Médica Mención Bioanálisis Clínico, Hematología y Banco de Sangre 29 de mayo de 2006
Universidad de Concepción Facultad de Medicina Carrera de Tecnología Médica Paloma Campos Leyton Cuarto Año Tecnología Médica Mención Bioanálisis Clínico, Hematología y Banco de Sangre 29 de mayo de 2006
Evaluación de los diferentes criterios de respuesta en imagen oncológica: análisis, evolución, claves y limitaciones.
 Evaluación de los diferentes criterios de respuesta en imagen oncológica: análisis, evolución, claves y limitaciones. Poster no.: S-1359 Congreso: SERAM 2014 Tipo del póster: Autores: Palabras clave: DOI:
Evaluación de los diferentes criterios de respuesta en imagen oncológica: análisis, evolución, claves y limitaciones. Poster no.: S-1359 Congreso: SERAM 2014 Tipo del póster: Autores: Palabras clave: DOI:
Es considerada como una de las características funcionales principales de las células.
 DIVISIÓN CELULAR Es considerada como una de las características funcionales principales de las células. El crecimiento y desarrollo adecuados de los organismos vivos depende del crecimiento y multiplicación
DIVISIÓN CELULAR Es considerada como una de las características funcionales principales de las células. El crecimiento y desarrollo adecuados de los organismos vivos depende del crecimiento y multiplicación
TERAPIA ONCOLÓGICA " UNA VISIÓN DIFERENTE "
 TERAPIA ONCOLÓGICA " UNA VISIÓN DIFERENTE " M. C. Victor Alex Palacios Cabrejos Oncólogo Clínico Servicio de Hematología - Oncología Clínica Hospital Nacional Cayetano Heredia SUMARIO 1. Epidemiología
TERAPIA ONCOLÓGICA " UNA VISIÓN DIFERENTE " M. C. Victor Alex Palacios Cabrejos Oncólogo Clínico Servicio de Hematología - Oncología Clínica Hospital Nacional Cayetano Heredia SUMARIO 1. Epidemiología
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR
 INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - BIOLOGIA CELULAR - Histología Tejidos 1 Tejidos Tejidos 2 Epitelio Clasificación Cilíndrica Cúbica Plana 3 Epitelios simples Plano simple Cúbico simple
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - BIOLOGIA CELULAR - Histología Tejidos 1 Tejidos Tejidos 2 Epitelio Clasificación Cilíndrica Cúbica Plana 3 Epitelios simples Plano simple Cúbico simple
Cáncer de mama avanzado
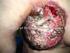 Cáncer de mama avanzado Santander 1 de Julio 2016 Tàrsila Ferro Directora de Cuidados Instituto Catalán de Oncología Profesora Universidad de Barcelona Definiciones Cáncer de mama recurrente o recurrencia:
Cáncer de mama avanzado Santander 1 de Julio 2016 Tàrsila Ferro Directora de Cuidados Instituto Catalán de Oncología Profesora Universidad de Barcelona Definiciones Cáncer de mama recurrente o recurrencia:
CICLO CELULAR Y SU REGULACIÓN G1
 G2 M S CICLO CELULAR Y SU REGULACIÓN G1 EXPRESIÓN de GENES Para dividirse, la célula recibe señales, las transmite y las interpreta como EXPRESIÓN de GENES ESPECÍFICOS para poder pasar por cada una de
G2 M S CICLO CELULAR Y SU REGULACIÓN G1 EXPRESIÓN de GENES Para dividirse, la célula recibe señales, las transmite y las interpreta como EXPRESIÓN de GENES ESPECÍFICOS para poder pasar por cada una de
Experiencia con vinflunina en pacientes con cáncer urotelial e ILP prolongado
 Experiencia con vinflunina en pacientes con cáncer urotelial e ILP prolongado Cáncer urotelial estadio IV Estrategia de tratamiento en 2ª línea El tratamiento del carcinoma urotelial avanzado tras fracaso
Experiencia con vinflunina en pacientes con cáncer urotelial e ILP prolongado Cáncer urotelial estadio IV Estrategia de tratamiento en 2ª línea El tratamiento del carcinoma urotelial avanzado tras fracaso
Todo lo que un residente debe saber
 Todo lo que un residente debe saber Enfermedad curable: cisplatino Clasificación: diagnóstico, recidiva Valor marcadores tumorales Fármacos más activos: cisplatino, etopósido Papel de la cirugía: inicial,
Todo lo que un residente debe saber Enfermedad curable: cisplatino Clasificación: diagnóstico, recidiva Valor marcadores tumorales Fármacos más activos: cisplatino, etopósido Papel de la cirugía: inicial,
LA CIENCIA Y SU IMPORTANCIA SOCIAL
 http://ciencias.unizar.es/web/concienciasnumero13.do Nº 13 MAYO 2014 LA CIENCIA Y SU IMPORTANCIA SOCIAL LOS ASESINOS DEL SISTEMA INMUNITARIO El conocimiento de los mecanismos inmunitarios se puede explotar
http://ciencias.unizar.es/web/concienciasnumero13.do Nº 13 MAYO 2014 LA CIENCIA Y SU IMPORTANCIA SOCIAL LOS ASESINOS DEL SISTEMA INMUNITARIO El conocimiento de los mecanismos inmunitarios se puede explotar
La Biología Molecular del Cáncer: El problema del cáncer de cabeza y cuello.
 1. Título del TÓPICO La Biología Molecular del Cáncer: El problema del cáncer de cabeza y cuello. 2. Tutor responsable Nombre completo: Dr. Alejandro García Carrancá Adscripción: Departamento de Biología
1. Título del TÓPICO La Biología Molecular del Cáncer: El problema del cáncer de cabeza y cuello. 2. Tutor responsable Nombre completo: Dr. Alejandro García Carrancá Adscripción: Departamento de Biología
PATOLOGIA MOLECULAR DEL CARCINOMA DE COLON. Eva Musulén
 PATOLOGIA MOLECULAR DEL CARCINOMA DE COLON Eva Musulén Patología molecular del CCR 1. Identificar pacientes de riesgo (Síndrome de Lynch) Inestabilidad de microsatélites 2. Guiar estrategia terapéutica
PATOLOGIA MOLECULAR DEL CARCINOMA DE COLON Eva Musulén Patología molecular del CCR 1. Identificar pacientes de riesgo (Síndrome de Lynch) Inestabilidad de microsatélites 2. Guiar estrategia terapéutica
La familia del EGFR como diana molecular en cáncer
 en cáncer Muchas gracias por la oportunidad de dirigirme a ustedes en este prestigioso evento, aquí en Lima. En los siguientes 20 minutos voy a cubrir algunos aspectos sobre la terapia dirigida contra
en cáncer Muchas gracias por la oportunidad de dirigirme a ustedes en este prestigioso evento, aquí en Lima. En los siguientes 20 minutos voy a cubrir algunos aspectos sobre la terapia dirigida contra
IDENTIFICACIÓN DE NUEVAS DIANAS TERAPÉUTICAS EN TUMORES GERMINALES REFRACTARIOS
 IDENTIFICACIÓN DE NUEVAS DIANAS TERAPÉUTICAS EN TUMORES GERMINALES REFRACTARIOS Investigadores principales: Dr. Francesc Viñals Canals Facultat de Medicina CSUB Dr. Fco. Javier García del Muro Solans Institut
IDENTIFICACIÓN DE NUEVAS DIANAS TERAPÉUTICAS EN TUMORES GERMINALES REFRACTARIOS Investigadores principales: Dr. Francesc Viñals Canals Facultat de Medicina CSUB Dr. Fco. Javier García del Muro Solans Institut
RETOS CIENTÍFICOS Y ECONÓMICOS PUNTO DE VISTA DEL ONCÓLOGO
 RETOS CIENTÍFICOS Y ECONÓMICOS PUNTO DE VISTA DEL ONCÓLOGO Dr. Fernando Rivera Herrero Vocal de SEOM Servicio de Oncología Médica Hospital Universitario M de Valdecilla. Santander Retos Científicos y económicos
RETOS CIENTÍFICOS Y ECONÓMICOS PUNTO DE VISTA DEL ONCÓLOGO Dr. Fernando Rivera Herrero Vocal de SEOM Servicio de Oncología Médica Hospital Universitario M de Valdecilla. Santander Retos Científicos y económicos
MIELOMA MÚLTIPLE: MP 1/5. 1. DENOMINACIÓN DEL ESQUEMA: MP (Melfalán-Prednisona).
 MIELOMA MÚLTIPLE: MP 1/5 1. DENOMINACIÓN DEL ESQUEMA: MP (Melfalán-Prednisona). 2. USO TERAPÉUTICO (1). Mieloma múltiple. Tratamiento de primera línea cuando no está indicado el trasplante de células progenitoras
MIELOMA MÚLTIPLE: MP 1/5 1. DENOMINACIÓN DEL ESQUEMA: MP (Melfalán-Prednisona). 2. USO TERAPÉUTICO (1). Mieloma múltiple. Tratamiento de primera línea cuando no está indicado el trasplante de células progenitoras
Comunicado de prensa. Perjeta, de Roche, prolongó significativamente la supervivencia en el cáncer de mama HER2-positivo metastásico
 Comunicado de prensa Basilea, 8 de diciembre de 2012 Perjeta, de Roche, prolongó significativamente la supervivencia en el cáncer de mama HER2-positivo metastásico Roche (SIX: RO, ROG; OTCQX: RHHBY) ha
Comunicado de prensa Basilea, 8 de diciembre de 2012 Perjeta, de Roche, prolongó significativamente la supervivencia en el cáncer de mama HER2-positivo metastásico Roche (SIX: RO, ROG; OTCQX: RHHBY) ha
Respiratory Tract Tumors Program Red Temática de Investigación Cooperativa en Cáncer (RTICC)
 Respiratory Tract Tumors Program Red Temática de Investigación Cooperativa en Cáncer (RTICC) J.L. González Larriba Servicio de Oncologia Médica Hospital Clínico San Carlos Reunión 7 de Marzo 2013. Madrid.
Respiratory Tract Tumors Program Red Temática de Investigación Cooperativa en Cáncer (RTICC) J.L. González Larriba Servicio de Oncologia Médica Hospital Clínico San Carlos Reunión 7 de Marzo 2013. Madrid.
Curso de actualización en biología celular y molecular Drogas con múltiples sitios de acción molecular Dr Carlos Garcia Gerardi
 Curso de actualización en biología celular y molecular Drogas con múltiples sitios de acción molecular Dr Carlos Garcia Gerardi Drogas con múltiples sitios de acción molecular Esta presentación no presenta
Curso de actualización en biología celular y molecular Drogas con múltiples sitios de acción molecular Dr Carlos Garcia Gerardi Drogas con múltiples sitios de acción molecular Esta presentación no presenta
TRATAMIENTO PALIATIVO ESPECÍFICO EN PACIENTES CON CÁNCER. Purificación Martínez del Prado
 TRATAMIENTO PALIATIVO ESPECÍFICO EN PACIENTES CON CÁNCER Purificación Martínez del Prado Tratamiento paliativo específico en pacientes con cáncer La demanda social en los aspectos paliativos de la medicina
TRATAMIENTO PALIATIVO ESPECÍFICO EN PACIENTES CON CÁNCER Purificación Martínez del Prado Tratamiento paliativo específico en pacientes con cáncer La demanda social en los aspectos paliativos de la medicina
